KERUSAKAN SEGMENTAL PADA TULANG DOMBA
YANG DIIMPLAN DENGAN KOMPOSIT
HIDROKSIAPATIT-TRIKALSIUM FOSFAT (HA-TKF)
ASMAWATI
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa skripsi Kajian Morfologi Proses Persembuhan Kerusakan Segmental pada Tulang Domba yang Diimplan dengan Komposit Hidroksiapatit-Trikalsium Fosfat (HA-TKF) adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, Februari 2011
Asmawati
ASMAWATI. Kajian Morfologi Proses Persembuhan Kerusakan Segmental pada Tulang Domba yang Diimplan dengan Komposit Hidroksiapatit-Trikalsium Fosfat (HA-TKF). Dibimbing oleh SRIHADI AGUNGPRIYONO dan GUNANTI.
Penelitian ini bertujuan mengkaji secara in vivo proses regenerasi tulang tibia domba yang diimplan dengan bahan pengganti tulang berupa komposit hidroksiapatit-trikalsium fosfat (HA-TKF) dan potensi osteogenesis (persembuhan dan pertumbuhan tulang) dari bahan tersebut. Penanaman implan dilakukan dengan melakukan operasi secara aseptis di bagian proksimal medial tulang tibia domba sebelah kiri sebagai kelompok perlakuan sedangkan pada tulang tibia sebelah kanan dilakukan operasi yang sama tanpa dilakukan penanaman implan dan dibiarkan kosong sebagai kelompok kontrol. Kemudian tulang dipanen setelah 30, 60 dan 90 hari pascaoperasi. Tulang diproses dan diamati secara makroskopis dan mikroskopis dengan mengamati bentuk, tingkat degradasi, ikatan antara implan dan tulang, pertumbuhan pertulangan baru ke dalam implan, dan adanya reaksi inflamasi. Hasil penelitian ini menunjukkan proses regenerasi tulang dan persembuhan tulang pada kelompok kontrol terjadi lebih cepat dibandingkan dengan persembuhan tulang pada kelompok perlakuan. Proses degradasi pada implan tulang sudah terjadi pada kelompok perlakuan hari ke-30 pascaoperasi. Implan HA-TKF yang ditanam menunjukkan sifat biokompatibilitas, bioresorbabilitas, biodegradabilitas, osteokonduktivitas, dan tidak menimbulkan reaksi inflamasi sehingga dianggap memiliki potensi untuk digunakan sebagai bahan implan pengganti tulang pada kerusakan tulang yang memerlukan waktu persembuhan sekitar 30 hari.
ASMAWATI. Morphological Study of Segmental Defect Healing Process on Sheep’s Bone Implanted with Hydroxyapatite-Tricalcium Phosphate (HA-TCP) Composite. Under direction of SRIHADI AGUNGPRIYONO and GUNANTI.
This study was aimed to evaluate in vivo osteogenesis potency of bones implanted with graft of hydroxyapatite-tricalcium phosphate (HA-TCP) composite. This study also observed the potential use of HA-TCP as bone substitution material. Three local sheeps were used in this study. The implant was inserted under aseptic surgery on the proximal medial of the left tibia bone and as control the proximal medial of the right tibia bone was drilled without implant. Bones were harvested after 30, 60, and 90 days post-surgery and observed macroscopic and microscopically. The parameters of observation were the condition, shape and degradation degree of the implant, bonding between implant and host bone, new bone growth into the implant and signs of inflammation reaction around the implant. The result showed that the healing process on control bone was faster than those of the implanted bone. The bone implant had been already degradated in treated group of day 30 post-surgery. HA-TCP bone implant shown some signs for its biocompatibility, biodegradability, bioresorbability and osteoconductivity properties. Therefore, it is suggested that HA-TCP implant might be used as bone substitution in the bone lesions with approximately 30 days of recovery.
© Hak cipta milik IPB, tahun 2011
Hak cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
YANG DIIMPLAN DENGAN KOMPOSIT
HIDROKSIAPATIT-TRIKALSIUM FOSFAT (HA-TKF)
ASMAWATI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Hewan pada
Fakultas Kedokteran Hewan
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
Nama : Asmawati
NIM : B04061859
Disetujui
drh. Srihadi Agungpriyono, Ph. D, PAVet(K) Dr. drh. Hj. Gunanti, MS Pembimbing I Pembimbing II
Diketahui
Dr. Nastiti Kusumorini
Wakil Dekan Fakultas Kedokteran Hewan
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala berkah dan karunia-Nya sehingga skripsi ini dapat diselesaikan. Penelitian ini dilaksanakan sejak tahun 2009 sampai 2010 dengan judul “Kajian Morfologi Proses Persembuhan Kerusakan Segmental pada Tulang Domba yang Diimplan dengan Komposit Hidroksiapatit-Trikalsium Fosfat (HA-TKF)”. Skripsi ini disusun untuk memenuhi salah satu syarat guna menyelesaikan studi di Program Sarjana Fakultas Kedokteran Hewan Institut Pertanian Bogor untuk mencapai gelar Sarjana Kedokteran Hewan.
Dengan tersusunnya skripsi ini, penulis menyampaikan ucapan terima kasih kepada semua pihak yang telah membantu dan membimbing hingga skripsi ini selesai disusun. Ucapan terima kasih ini disampaikan kepada:
1. Ibunda Sutimi AMa.Pd dan adinda Asriyadi atas segala kasih sayang, perhatian, dukungan dan doa yang selalu diberikan kepada penulis.
2. Bapak drh. Srihadi Agungpriyono, Ph.D, PAVet(K) dan Ibu Dr. drh. Gunanti, MS selaku pembimbing skripsi yang telah banyak meluangkan waktu dalam memberikan bimbingan dan arahan kepada penulis dalam menyelesaikan skripsi ini.
3. Ibu drh. Titiek Sunartatie, M.Si. selaku pembimbing akademik dan penguji ujian akhir S.KH atas saran dan arahan yang diberikan dalam penulisan skripsi.
4. Bapak drh. Adi Winarto, Ph.D selaku dosen penilai seminar yang telah memberikan kritik dan saran untuk skripsi ini.
5. Bapak drh. Riki Siswandi, Bapak drh. Fahrul Ulum, Bapak Kosasih, Bapak Dahlan, Bapak Katim dan staf penunjang di Laboratorium Bagian Bedah dan Radiologi FKH IPB atas bantuan yang telah diberikan untuk penulis.
6. Ibu Dr. drh. Savitri Novelina, M.Si, Bapak Dr. drh. Nurhidayat, Ibu Dr. drh. Sri Wahyuni, Bapak drh. Supratikno, M.Si, Bapak Budi, Bapak Bayu, dan staf penunjang di Laboratorium Bagian Anatomi, Histologi dan Embriologi yang telah membantu penulis selama penelitian.
7. Bapak Kasnadi dan staf di Laboratorium Histopatologi atas bantuan yang diberikan untuk penulis.
8. Tim penelitian “Shaker” (Ayu Berlianty, Rachmat Ayu DH, Santi Purwanti, Dwi Kolina P, Gendis Aurum P dan Raditya P) atas perjuangan, kerja sama dan motivasi yang telah diberikan selama penelitian.
9. Novi Tandria, Nina Maria BL, Krisna NF, Gita Nelfa, Hadi P, Binol, Soni, Sifa, Edo, Fiona, Ipin, Ardinta, Galuh, Indra dan keluarga besar Aesculapius 43 atas dukungan dan bantuan yang diberikan kepada penulis. 10.Sahabat-sahabatku (Yona Shylena, Gina Ramadyana, Endah Febrianty,
Citra Resmi) yang selalu memberikan motivasi, semangat dan doa untuk penulis.
13.Keluarga besar HIMAKOMET (Yuni, Catur, Arum, Azis, Yunus, Damas) atas dukungan, motivasi dan doa yang diberikan kepada penulis.
Akhir kata, penulis menyadari bahwa skripsi ini jauh dari kata sempurna sehingga penulis terbuka terhadap saran dan kritik yang diberikan. Semoga skripsi ini bermanfaat.
Bogor, Februari 2011
Penulis dilahirkan di Metro-Lampung pada tanggal 22 Juli 1988. Penulis adalah anak pertama dari dua bersaudara pasangan bapak Ahmad (alm) dan ibu Sutimi, AMa, Pd.
Penulis menyelesaikan jenjang pendidikan sekolah dasar pada tahun 2000 di SD N 2 Tempuran dan pada tahun yang sama penulis melanjutkan pendidikan ke SMP N 1 Metro hingga lulus pada tahun 2003. Pendidikan sekolah menengah umum diselesaikan tahun 2006 di SMU N 1 Metro. Pada tahun yang sama penulis berkesempatan untuk melanjutkan pendidikan di Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI). Setelah masa Tingkat Persiapan Bersama (TPB) IPB, penulis memilih mayor Fakultas Kedokteran Hewan (FKH) IPB.
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
PENDAHULUAN Latar Belakang ... 1
Tujuan Penelitian ... 3
Manfaat Penelitian ... 3
TINJAUAN PUSTAKA Tulang ... 4
Komponen Seluler Tulang ... 4
Komponen Matriks Ekstraseluler Tulang ... 7
Klasifikasi Tulang ... 8
Osteogenesis (Proses Pembentukan Tulang) ... 11
Remodelling Tulang ... 13
Proses Persembuhan Fraktur Tulang ... 14
Biomaterial (Bone Graft) ... 17
Klasifikasi Bone Graft... 18
Mineral Apatit ... 19
Hidroksiapatit ... 20
Trikalsium Fosfat ... 20
Karakteristik Implan Hidroksiapatit-Trialsium fosfat ... 21
Fisiologi Perbaikan Tulang dengan Bone Graft ... 22
Domba sebagai Hewan Coba ... 23
BAHAN DAN METODE Waktu dan Tempat ... 25
Alat dan Bahan ... 25
Metode Penelitian ... 25
Pemeliharaan Hewan Coba ... 25
Operasi Penanaman Implan HA-TKF ... 26
Perawatan Hewan Coba Pascaoperasi ... 27
Pemeriksaan Makroskopis dan Mikroskopis ... 27
Metode Pengamatan ... 29
HASIL DAN PEMBAHASAN Pengamatan Makroskopis ... 30
Pengamatan Mikroskopis ... 33
Gambaran Mikroskopis Preparat Tulang Gosok ... 33
Gambaran Mikroskopis Preparat Tulang Dekalsifikasi ... 37
Kajian Morfologi Persembuhan Tulang ... 45
1. Persembuhan luka pada fraktur tulang tipe uncomplicated ... 17
2. Perubahan makroskopis jaringan tulang tibia dan implan
HA-TKF pada berbagai periode pemanenan ... 30
3. Perubahan mikroskopis jaringan tulang tibia dan implan
Halaman
1. Gambar permukaan luar tulang (periosteum) dan permukaan dalam
tulang (endosteum) ... 5
2. Gambar osteoblas, osteosit, matriks tulang ... 6
3. Gambar osteoklas, Howslip’ lacuna atau resorption bay ... 7
4. Gambar struktur tulang ... 12
5. Gambar proses remodelling tulang ... 13
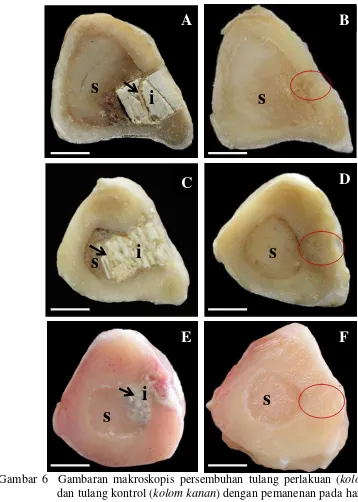
6. Gambaran makroskopis persembuhan dan regenerasi tulang pada kerusakan segmental tulang tibia domba yang diimplan dengan HA-TKF dan tanpa implan ... 32
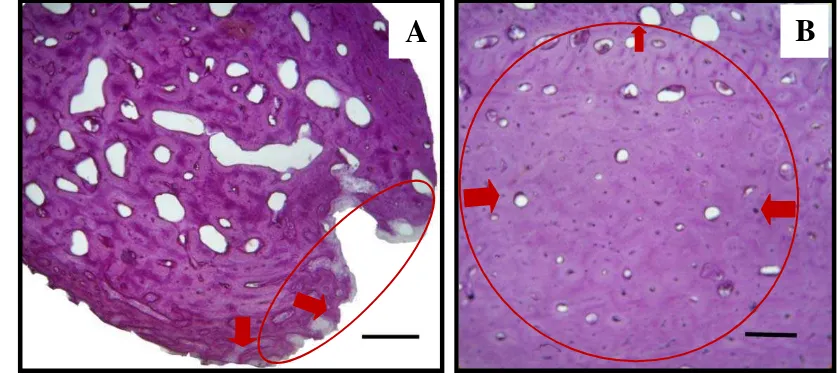
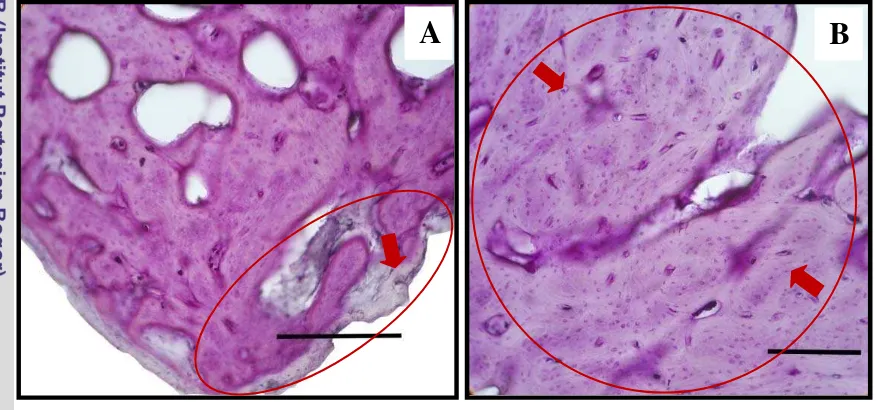
7. Gambaran mikroskopis persembuhan tulang perlakuan (A) dan tulang kontrol (B) pada hari ke-30 pascaoperasi. ... 34
8. Gambaran mikroskopis persembuhan tulang perlakuan (A) dan tulang kontrol (B) pada hari ke-60 pascaoperasi ... 35
9. Gambaran mikroskopis persembuhan tulang kontrol pada hari ke-60 pascaoperasi ... 35
10. Gambaran mikroskopis persembuhan tulang perlakuan (A) dan tulang kontrol (B) pada hari ke-90 pascaoperasi. ... 36
11. Gambaran mikroskopis persembuhan tulang perlakuan pada hari ke-30 pascaoperasi. ... 38
12. Gambaran mikroskopis persembuhan tulang perlakuan pada hari ke-30 pascaoperasi. ... 39
13. Gambaran mikroskopis persembuhan tulang kontrol pada hari ke-30 pascaoperasi ... 40
14. Gambaran mikroskopis persembuhan tulang perlakuan pada hari ke-60 pascaoperasi ... 42
15. Gambaran mikroskopis persembuhan tulang kontrol pada hari ke-60 pascaoperasi ... 43
16. Gambaran mikroskopis persembuhan tulang perlakuan pada hari ke-90 pascaoperasi. ... 44
PENDAHULUAN
Latar Belakang
Peningkatan berbagai kasus penyakit tulang pada manusia seperti kanker tulang, periodontitis, patah tulang dan lain-lain semakin meningkatkan kebutuhan
graft tulang atau biomaterial yang sesuai (Darwis 2008). Setiap tahun, jutaan orang di seluruh dunia menderita kerusakan tulang yang diakibatkan oleh trauma, tumor atau penyakit tulang. Persembuhan spontan pada beberapa kerusakan tulang tersebut tidak mampu mengembalikan stabilitas fisiologis yang diperlukan. Dalam kasus-kasus tersebut bahan pengganti tulang sering diperlukan untuk merekonstruksi morfologi anatomi dan memulihkan stabilitas tulang (Huber et al.
2009). Bahan pengganti tulang yang kurang ideal akan memperburuk keadaan (Murugan & Ramakrishna 2004).
Biomaterial dapat didefinisikan sebagai inert yang diimplantasikan ke dalam sistem hidup sebagai pengganti fungsi jaringan atau organ (Baht 2002). Biomaterial juga dapat didefinisikan sebagai suatu material baik alami maupun buatan manusia (sintetis) yang digunakan dalam berkontak dengan sistem biologi. Tujuan penggunaan biomaterial adalah memperbaiki (repair), memulihkan (restore), mengganti (replace) jaringan yang rusak/sakit atau sebagai interface
dengan lingkungan fisiologis (Darwis 2008). Biomaterial sintetik yang digunakan sebagai bahan pengganti tulang yang ideal memiliki sifat bioaktif, biodegradabel, bioresorbabel, dan biokompatibel dengan tubuh dalam waktu yang lama (Lane et al. 1992). Selain itu, bahan pengganti tulang tidak bersifat toksik sehingga aman dalam tubuh. Bahan pengganti tulang yang ideal juga memiliki sifat osteokonduktif, osteoinduktif, dan dapat berintegrasi pada struktur tulang (Laurencin & Yusuf 2009).
Substansi mineral penyusun tulang yang paling banyak terdiri dari apatit
(95%) serta sejumlah mineral lainnya (5%) (Broto 2004). Apatit dalam tulang disebut apatit biologis. Komponen utama senyawa apatit adalah kalsium fosfat yang terdiri dari berbagai fase, salah satunya adalah fase hidroksiapatit (HA) yang merupakan bentuk paling stabil dibandingkan yang lainnya (Saraswathy et al.
merupakan komponen yang lazim digunakan dalam mengisi kekosongan tulang. Keterbatasan jumlah apatit biologis memicu perkembangan riset di bidang biomaterial. Untuk mengatasinya dilakukan pembuatan HA secara kimia atau apatit sintetik (Purnama 2006).
Percobaan pemasangan implan dengan HA pertama kali diteliti pada hewan anjing dengan kerusakan tulang di bagian proksimal tulang tibia. Pada studi ini persembuhan tulang terjadi dengan baik, cepat dan tanpa efek samping (Karabatsos et al. 2001). HA memiliki sifat stabil, namun bahan ini memerlukan waktu yang lama untuk dapat diserap tubuh. Maka untuk mengimbanginya
ditambahkan trikalsium fosfat (TKF) yang dapat diserap lebih cepat oleh tubuh. Penggabungan HA-TKF diharapkan dapat digunakan dalam implantasi tulang dan ideal untuk manusia.
Domba merupakan salah satu hewan yang dapat digunakan dalam penelitian ortopedik seperti patah tulang, osteoporosis dan osteoarthritis (Martini
et al. 2001). Selain itu, domba cocok digunakan dalam pengujian bahan implantasi tulang karena memiliki dimensi tulang panjang yang sesuai untuk implantasi (Newman et al. 1995). Penggunaan domba dalam eksperimental juga sering diterapkan untuk pengujian biokompatibilitas berbagai biomaterial (Hunziker 2003). Hal tersebut dilakukan untuk mengetahui bioaktivitas yang berkaitan dengan resorpsi, integrasi dari bahan yang ditanam ke dalam tulang (Hing et al. 1998). Struktur morfologi tulang panjang pada domba sesuai dengan fungsi dan beban mekanik serta memiliki kesamaan metabolisme tulang yang sesuai dengan manusia (Nuss et al. 2006). Berbagai riset menunjukkan bahwa domba dan manusia memiliki pola yang sama pada pertumbuhan tulang ke implan berpori dalam hal remodelling tulang (Pearce et al. 2007).
Tujuan Penelitian
Penelitian ini bertujuan mengkaji morfologi proses persembuhan implan tulang dengan bahan pengganti tulang sintetik HA-TKF dan mengevaluasi aspek-aspek yang mungkin terkait dengan biokompatibilitas, osteokonduktivitas, biodegradabilitas dan bioresorbabilitas implan HA-TKF.
Manfaat Penelitian
TINJAUAN PUSTAKA
Tulang
Kerangka tubuh terbentuk dari tulang rawan, tulang dan persendian.
Tulang merupakan jaringan ikat khusus, karena mempunyai fungsi khusus serta
komponennya terdiri dari sel-sel khusus yang berbeda dengan jaringan ikat
lainnya (Astawan 2002). Tulang memiliki fungsi penting bagi tubuh yaitu
melindungi dan menyokong organ-organ internal dan sebagai tempat melekatnya
otot dan tendon (Price & Wilson 2006). Tulang juga berperan dalam fungsi
metabolik dengan menyediakan sumber kalsium untuk memelihara keseimbangan
kadar kalsium dalam darah serta menyediakan beberapa faktor pertumbuhan
(growth factor) seperti transforming growth factor (TGF-ß) yang berperan dalam
remodelling (Dellmann & Eurell 1998).
Tulang dapat dibentuk dari differensiasi jaringan ikat secara langsung atau
bagian dari perubahan dan pertumbuhan tulang rawan sebelumnya. Jaringan ini
memiliki kemampuan sebagai tempat penyimpanan mineral, khususnya kalsium
dan hampir sebagian besar berupa kristal hidroksiapatit. Bahan tersebut yang
membedakan tulang dengan jaringan ikat lainnya, termasuk tulang rawan
(Samuelson 2007).
Tulang memiliki komponen seluler yang terdiri dari berbagai macam sel
tulang. Sel tersebut antara lain prekursor osteogenik atau osteoprogenitor,
osteoblas, osteosit dan osteoklas serta elemen hematopoetik dari sumsum tulang
(Kalfas 2001). Sedangkan komponen ekstraseluler terdiri dari bahan organik dan
anorganik pembentuk matriks (Samuelson 2007).
Komponen Seluler Tulang
Bagian luar permukaan tulang dikelilingi oleh lapisan jaringan yang
disebut periosteum, kecuali pada bagian ujung persendian sinovial (Samuelson
2007). Periosteum terdiri dari pembuluh darah, lapisan tebal jaringan ikat fibrosa
(kapsul) dan stem sel atau sel osteogenik (Gambar 1A) yang akan berkembang
menjadi sel osteoblas. Tulang memiliki ruang internal yaitu ruang sentral atau
ruang sumsum tulang. Ruang tersebut dilapisi oleh selapis jaringan tipis yang
osteogenik dan memiliki jaringan ikat yang sangat sedikit dibandingkan dengan
lapisan periosteum (Samuelson 2007).
Gambar 1 A. Gambaran permukaan luar tulang, lapisan fibrosa (3), lapisan osteogenik (9), sumsum tulang (5), periosteum (10), B. Permukaan dalam tulang, endosteum (2), osteosit (8) dengan pewarnaan Hematoksilin Eosin (HE) (Bacha & Bacha 2000)
Komponen seluler tulang terdiri dari sel osteogenik atau osteoprogenitor,
osteoblas, osteosit, osteoklas, (Samuelson 2007; Dellman & Eurell 1998) dan
unsur-unsur hematopoetik dari sumsum tulang (Kalfas 2001).
Sel osteogenik atau sel osteoprogenitor memiliki peranan penting dalam
perkembangan dan remodelling tulang (Samuelson 2007). Sel tersebut terdapat pada lapisan periosteum, saluran Haver’s, Volkmann, dan kanalis medullaris. Sel
osteoprogenitor merupakan sel primitif turunan sel mesenkimal yang dapat
membentuk sel osteoblas (Mills 2007).
Osteoblas adalah sel yang bertanggung jawab untuk mensintesis,
mentransfer dan mengatur komponen bahan organik matriks tulang yang disebut
osteoid atau prebone (Mills 2007). Bahan organik tersebut berupa kolagen,
proteoglycans dan glycoprotein. Osteoblas berasal dari sel osteogenik yang ada pada permukaan tulang. Bentuk osteoblas dalam keadaan metabolisme aktif
cenderung lebih kuboid dan basophilic. Saat osteoblas dalam keadaan tidak aktif mensintesis osteoid, sel ini berbentuk gepeng dan bersifat kurang basophilic
(Samuelson 2007).
Osteoblas yang masuk ke dalam matrik tulang maka dinamakan osteosit.
Osteosit muda sebenarnya tidak benar-benar bermigrasi ke dalam matriks tulang,
tetapi terisolasi di sekitar matriks, dengan demikian osteosit merupakan osteoblas
dewasa yang terkapsulasi dan termineralisasi oleh matriks tulang. Sel tersebut
berada pada ruang berbentuk oval atau disebut lakuna. Penjuluran dari sel-sel
osteosit akan membentuk kanalikuli. Penjuluran kanalikuli terbentuk secara radial.
Antara kanalikuli tersebut saling dihubungkan dengan formasi gab junction.
Koneksi filopodial gap junctions ini berfungsi sebagai ”life support line” yaitu menyediakan jalur lintasan nutrisi dan jalur lintasan sisa-sisa metabolisme dari sel
ke sel lainnya (Samuelson 2007).
Osteosit memiliki ukuran yang lebih kecil dibandingkan dengan osteoblas,
memiliki sedikit organel dan sitoplasma. Peranan osteosit adalah memelihara
lingkungan ekstraseluler yang termineralisasi. Ketika distimulasi oleh hormon
paratiroid (PTH), osteosit mampu mengeluarkan mineral berupa kalsium secara
cepat dengan mensekresikan enzim hidrolase. Proses ini dikenal dengan osteolisis
osteosit (Samuelson 2007).
Gambar 2 Osteoblas, osteosit, matriks tulang (Caceci 2007)
Osteoklas adalah multinukleat giant sel yang memiliki 6-50 atau lebih inti sel yang berperan dalam penyerapan dan remodelling jaringan tulang (Samuelson 2007). Ukuran diameternya sekitar 40 sampai 100µm (Dellman & Eurell 1998).
Sitoplasma bersifat acidophilic, kaya akan lisosom, memiliki banyak mitokondria dan apparatus Golgi. Osteoklas berasal dari organ sumsum tulang dan merupakan derivat dari gabungan monosit. Pada proses pertumbuhan dan dalam remodelling
tulang, osteoklas akan secara kontinyu melakukan penyerapan (osteoclasia). Proses ini merupakan hasil sekresi dari beragam material yaitu asam laktat dan
enzim hidrolitik kuat (acid hydrolase, collagenase, dll) yang mampu mencerna matriks ekstraseluler (ECM).
Gambar 3 Osteoklas, Howslip’ lacuna atau resorption bay (Caceci 2007)
Setiap osteoklas melalui proses enzimatik kemudian mendepres bagian
matriks yang disebut Howslip’s lacuna atau resorption bay (Gambar 3). Selama tulang aktif melakukan penyerapan, sel tersebut akan berkontak langsung dengan
bony matrik (Samuelson 2007; Mills 2007)
Komponen Matriks Ekstraseluler Tulang
Sebagian besar komposisi tulang berupa matriks ekstraseluler, dua
pertiganya adalah bahan anorganik dan sisanya merupakan bahan organik
(Samuelson 2007). Sebagian besar bahan organik tersebut berupa serabut kolagen
tipe I dan sejumlah kecil bahan dasar (dalam bentuk amorphous). Bahan anorganiknya berupa bahan mineral kalsium yang ditemukan dalam beberapa
varian hidroksiapatit [Ca10(PO4)6(OH)2]. Bahan mineral lainnya seperti
bikarbonat, magnesium, natrium, kalium, tembaga, seng, mangan dan lainnya.
Secara umum tulang tersusun oleh 30% substansi organik, 55% substansi
anorganik dan 10% air (Aoki 1994)
Kristal hidroksiapatit disusun dalam tata cara yang terorganisasi dalam
mengatur pembuatan serabut kolagen dan dengan gap regionya. Molekul-molekul
proteoglycan yang berjumlah sedikit memiliki komponen utama yang terdiri dari
Proteoglycans dalam komposisi tersebut adalah instrumen dalam inisiasi dan inhibisi (penghambat) mineralisasi tulang. Selama terjadi proses mineralisasi
secara normal berlangsung, jumlah proteoglycans di dalam matriks ekstraseluler (ECM) relatif menurun. Jadi terdapat hubungan timbal balik antara jumlah
proteoglycans dan derajat mineralisasi pada pertumbuhan tulang (Samuelson 2007). Bahan dasar yang terutama terdiri dari komponen agregat tersebut,
memungkinkan air untuk berkontak dengan kristal dan terjadi pertukaran ion.
Glycoprotein terdiri dari osteocalcin dan osteopontin, keduanya dapat mengikat kristal kemudian pada bahan lain integrin termasuk protein transmembran yang
berasosiasi dengan osteoblas dan osteoklas dan banyak tipe sel yang lain termasuk
fibroblast. Sialoprotein adalah matrik yang mempunyai fungsi adhesif, dapat mengikat integrin dari sel pembentuk tulang dan komponen matriks tulang.
Proses mineralisasi di dalam ECM tulang tidak sepenuhnya diketahui.
Secara tidak pasti mempengaruhi kehadiran vesikel matriks, dikeluarkan ke
osteoid oleh osteoblas. Vesikel dipenuhi oleh kalsium dan ion fosfat dengan cyclic adenosine monophosphate (AMP), adenosine triphosphate (ATP) dan adenosine triphosphatase (ATPase) kemudian dua enzim lainnya yaitu alkaline phosphatase
dan pyrophosphatase, serta protein yang mengikat kalsium. Selain itu, vesikel memiliki pompa kalsium yang memungkinkan pergerakan lebih jauh dari elemen
ini ke dalam ECM. Setiap vesikel berada pada beberapa level struktur autonom
yang dapat membentuk kristal hidroksiapatit di luar sitoplasma dari osteoblas dan
osteosit dan di daerah ECM prebone. Sebagai kristal yang dikeluarkan dari vesikel dan ditimbun di sepanjang permukaan dekat dengan molekul kolagen,
kemudian daerah tersebut menjadi mikrosenter dari lanjutan kalsifikasi dan
mineralisasi setelah periode terakhir dengan berangsur-angsur kehilangan air.
Klasifikasi Tulang
Klasifikasi tulang dapat dilihat dari segi perkembangannya, konfigurasi
dan pengaturannya. Berdasarkan perkembangannya, tulang dibedakan menjadi
dari pada tulang yang belum dewasa, tersusun dari matriks yang tertimbun oleh
serabut kolagen.
Berdasarkan konfigurasinya, tulang dibagi ke dalam dua tipe yaitu
spongiosa (trabekular) dan tipe kompakta (kortikal). Tulang spongiosa terdiri dari
tulang cancellous merupakan jaringan yang umumnya memiliki bentuk berlubang-lubang seperti spon. Jarak antara lubangnya (interoseus) lebih besar dari pada tulang kompakta. Tipe tulang ini sering dideskripsikan sebagai tulang
yang belum dewasa (immature bone), terutama pada pertumbuhan bagian dari epifisis dan diafisis dari tulang panjang (Samuelson 2007). Tulang trabekular
(cancellous atau medullary) memiliki berat 20% dari keseluruhan massa tulang. Didapatkan pada bagian dalam tulang dan terutama pada tulang vertebra. Terdiri
dari spikula tipis tulang yang meluas dari korteks menuju ruang medula.
Jaring-jaring spikula tulang terlihat sebagai garis yang muncul pada beberapa daerah
yang terdapat osteoblas dan osteoklas serta sel-sel yang terlibat pada remodelling
tulang. Tulang trabekula secara konstan akan disintesa dan diserap oleh elemen
seluler. Tulang kompak (kortikal) menempati 80% dari keseluruhan massa tulang
dan merupakan lapisan terluar (korteks) tulang. Sel tulang kortikal terdiri dari
jaringan padat yang sebagian besar tersusun dari mineral tulang dan elemen
matriks ekstraseluler, terpisahkan oleh penetrasi pembuluh darah dan sekumpulan
osteosit yang ada di dalam tulang. Osteosit ini saling berhubungan satu sama lain
dengan osteoblas pada permukaan tulang yang disebut kanalikuli dimana terjadi
proses penyebarluasan osteosit seluler. Hubungan ini memungkinkan perpindahan
Ca2+dari dalam tulang ke permukaan, proses ini biasa disebut osteolisis osteosit.
Kepadatan tulang kortikal menghasilkan suatu kekuatan terhadap beban yang
berat yang mengenai tulang-tulang panjang (Baron & Emile 2003).
Berdasarkan pengaturannya tulang padat dibedakan antara tulang lamellar
dan tipe tulang osteon. Tulang lamellar terdiri dari lapisan-lapisan atau
lamel-lamel tulang yang berada pada daerah periosteum dan endosteum. Sedangkan tipe
tulang osteonal terdiri dari lamel-lamel yang tersusun secara silinder atau disebut
osteon (Haversian sistem).
Tulang dewasa sebagian besar komponennya terdiri dari satu unit struktur
terdiri atas: a) matriks tulang yang berupa lamel-lamel konsentris (lamel-lamel
khusus) yang mengelilingi saluran Haver’s (canalis centralis). Pada saluran ini terdapat pembuluh darah dan syaraf yang menyuplai nutrisi ke osteon; b) lakuna
yang berisi osteosit, terletak pada lamel-lamel tulang; c) kanalikuli, merupakan
penjuluran-penjuluran osteosit yang tersusun secara radial terhadap saluran
Haver’s. Kanalikuli ini berhubungan dengan saluran Haver’s dan membantu difusi
nutrisi maupun sisa metabolisme baik dari pembuluh darah ke osteosit maupun
sebaliknya (Samuelson 2007; Dellmann & Eurell 1998)
Diantara osteon-osteon terdapat sisa-sisa lamel osteon sebelumnya dan
dinamakan lamel-lamel interstitial. Panjang sumbu osteon sejajar atau paralel
dengan sumbu tulang. Serabut kolagen tulang tersusun paralel satu dengan lainnya
pada lamel-lamel khusus, sehingga potongan memanjangnya menyerupai kayu.
Pada sisi luar osteon, terdapat lamel-lamel umum luar (outer circumferential lamellae), sedangkan lamel-lamel umum dalam (inner circumferential lamellae) terdapat disebelah dalam osteon berbatasan dengan sumsum tulang (Samuelson
2007; Dellmann & Eurell 1998).
Saluran Volkmann (perporating canal) merupakan saluran yang menghubungkan dua saluran Haver’s dan juga merupakan saluran tempat
pembuluh darah dan syaraf berjalan mulai dari permukaan periosteum dan
endosteum sampai mencapai saluran Haver’s (Gambar 4). Saluran ini tidak
dikelilingi oleh lamel dan merupakan ciri khusus dalam identifikasi secara
histologi (Samuelson 2007; Dellmann & Eurell 1998). Berikut gambaran sistem
Gambar 4 Struktur tulang (Lerro 2007).
Osteogenesis (Proses Pembentukan Tulang)
Osteogenesis atau proses pembentukan tulang dapat diklasifikasikan
menjadi dua cara, yaitu osifikasi intramembranous dan osifikasi endokhondral.
Pembentukan tulang langsung dari jaringan ikat, proses ini dinamakan osifikasi
intramembranous sedangkan proses pembentukan tulang dimulai dari tulang
rawan disebut osifikasi endokhondral atau osifikasi intrakartilagous (Samuelson
2007).
Osifikasi Intramembranous
Proses terjadinya osifikasi intramembranous dimulai dari vaskularisasi di
jaringan ikat. Kemudian terjadi kondensasi sel-sel mesenkim ke tempat tulang
yang akan dibentuk. Sel osteoprogenitor berdeferensiasi menjadi osteoblas. Sel
tersebut mulai mensintesis dan mensekresikan osteoid. Komponen utama yang
disekresikan oleh osteoid adalah kolagen. Selama awal osifikasi
intramembrenous, osteoblas dikelilingi oleh sebagian matriks yang dimineralisasi
lengkap. Sebagian osteoblas menjadi terisolasi di lakuna dan menjadi osteosit.
Sebagian kecil menjadi pusat osifikasi. Dari pusat osifikasi kemudian menyebar
ke beberapa arah membentuk trabekular (Dellman & Eurell 1998).
Saat osteoblas mensintesis dan mensekresikan bahan organik matriks,
plasmalemmma buds, disebut vesikel matriks, bentuk selnya panjang dan saling berdekatan di pinggir dengan osteoid dan dalam posisi menjepit. Vesikel matriks
berisi lipid, akumulasi ion kalsium, dan memiliki ativitas alkaline phosphatase, semua ini dibutuhkan untuk menginisiasi dan memelihara mineralisasi
(Samuelson 2007).
Osifikasi Endokhondral
Osifikasi endokhondral merupakan proses pertumbuhan atau pembentukan
tulang yang berasal dari tulang rawan hialin atau kartilago (Mills 2007). Hampir
semua tubuh awalnya tumbuh sebagai tulang rawan pada tingkat embrio, namun
pertumbuhannya dilanjutkan dengan proses osifikasi endokhondral. Pada tingkat
seluler, sel-sel kartilago akan berubah menjadi osteoblas kemudian osteosit. Pada
osifikasi ini dikenal pusat osifikasi primer (primary center of ossification) di diafisis serta pusat osifikasi sekunder (secondary ossification center) di epifisis (Samuelson 2007; Mills 2007).
Pada diafisis, sel-sel kartilago mengalami tiga hal, yaitu hipertropi,
kalsifikasi matriks serta kematian sel-selnya. Selain itu, perikhondrium akan
mengalami vaskularisasi sehingga sel-sel kartilago akan berubah menjadi
osteoblas. Perikhondrium yang merupakan bagian permukaan dari kartilago
berubah menjadi periosteum. Pemanjangan tulang berlangsung hanya pada
perbatasan antara diafisis dan epifisis (lempeng epifisis). Hal ini dikarenakan
hanya sel-sel kartilago di bagian inilah yang mampu berproliferasi. Mendekati
diafisis, sel-sel ini mengalami hipertropi dan matriksnya akan mengalami
kalsifikasi. Osifikasi pertama kali terjadi di diafisis, yaitu pusat osifikasi primer,
pada akhir masa embrionik.
Pada waktu lahir, sebagian besar diafisis telah mengalami osifikasi,
sedangkan epifisis masih berupa kartilago. Osifikasi sekunder baru berlangsung
dan diafisis, hanya daerah di tengah-tengah kedua daerah itulah (lempeng epifisis)
yang masih berupa kartilago. Kartilago ini akan terus berproliferasi yang diikuti
dengan osifikasi. Saat seluruh lempeng epifisis telah mengalami osifikasi, berarti
masa pertumbuhan tulang telah berhenti.
Remodelling Tulang
Remodelling merupakan reorganisasi atau renovasi struktur tulang lama. Terjadi resorpsi jaringan tulang dan deposisi simultan tulang baru pada tulang
normal, kedua proses ini berada dalam keseimbangan yang dinamis (Dorland
2002). Menurut Mills (2007) remodelling adalah proses yang dinamis, pada proses ini terjadi pengurangan dan penggantian tulang baik kortikal atau tulang
trabekular. Proses ini akan berlanjut sepanjang hidup untuk mempertahankan
massa tulang, integritas kerangka dan fungsi kerangka. Kejadiannya sangat
komplek dan sebagian dikontrol oleh sistem syaraf pusat melewati hormon
(contohnya leptin) dan induksi mekanik dari kerusakan kecil. Prosesnya juga sangat bergantung pada integrasi gerakan dari osteoblas, osteosit dan osteoklas.
Sel-sel tersebut secara bersamaan membentuk basic sellular unit dari tulang, pada saat dewasa resorpsi dalam remodelling tulang kira-kira terjadi sebanyak 10% dari jumlah kerangka pertahunnya (Mills 2007). Proses remodelling diawali pada permukaan bony dan tergabung dalam beberapa tahapan aktivitas sel yaitu aktivasi, resorpsi, reversal (pengembalian), dan formasi atau pembentukan tulang.
Rangkaian aktivitas remodelling tersebut dapat dilihat pada Gambar 5.
Tahap aktivasi bergantung pada sel yang berdeferensiasi menjadi
osteoblas, yang ada di permukaan tulang atau sumsum tulang, bertindak pada
prekursor sel darah (hemapoetic cells) untuk membentuk osteoklas yang akan menyerap tulang. Proses resorpsi terjadi di bawah lapisan sel (lining sel) (Gambar 5). Setelah fase reversal, osteoblas memulai untuk pembentukan tulang baru. Sisa
osteoblas di dalam tulang akan berubah menjadi osteosit. Masing-masing osteosit
akan berhubungkan satu sama lain dan dihubungkan juga ke permukaan osteoblas.
Fase resorpsi berakhir hanya pada beberapa minggu tetapi fase formasi terjadi
sebagai lapisan yang banyak pada tulang baru dibentuk oleh berturut-turut
gelombang dari osteoblas.
Gambar 5 Proses remodelling tulang ( Lerro 2007).
Proses Persembuhan Fraktur Tulang
Kerusakan pada fraktur dapat terjadi karena trauma atau tenaga fisik.
Fraktur segmental adalah dua fraktur berdekatan pada satu tulang yang
menyebabkan terpisahnya segmen sentral dari suplai darahnya (Price & Wilson
2006). Dalam kasus ini penggunaan bone graft mungkin diperlukan untuk memperbaiki kerusakan tersebut.
Salah satu aplikasi bone graft yaitu dengan menanamkannya pada kerusakan spinal fusion. Menurut Boden et al. (1995), proses penyatuan bone graft di dalam spinal fusion model hampir sama dengan proses persembuhan tulang yang terjadi dalam keadaan persembuhan fraktur.
Persembuhan fraktur akan mengembalikan jaringan yang rusak menjadi
jaringan tulang yang sesuai. Hal ini dipengaruhi oleh berbagai faktor lokal
maupun sistemik. Persembuhannya terjadi dalam empat tahap berbeda tetapi
tahap perbaikan (pembentukan kalus) dan 3. tahap pembentukan tulang rawan dan
terakhir 4. tahap remodelling (Kalfas 2001).
1. Tahap Hemoragi dan Tahap Awal Inflamasi
Saat terjadi fraktur maka pembuluh darah akan mengalami kerusakan atau
ruptur dan terjadi hemoragi di dalam daerah fraktur, jika darah merembes
melewati periosteum di dalam otot. Kemudian darah mengalami koagulasi dan
mengisi ruang terjadinya fraktur (Cheville 2006), atau terjadi hematoma dalam
ruang fraktur (Kalfas 2001). Adanya trauma pada kejadian fraktur akan
menginduksi tahap inflamasi (Cheville 2006). Pada tahap ini, sel-sel peradangan
seperti monosit, limfosit, sel-sel polimorfonuklear dan fibroblast menginfiltrasi
tulang yang diperantarai oleh prostaglandin (Kalfas 2001). Monosit yang masuk
ke dalam daerah fraktur akan bertransformasi menjadi makrofag yang memainkan
peranan penting dalam persembuhan tulang (Tabel 1) (Cheville 2006). Hal ini
akan menyebabkan pembentukan jaringan granulasi, pertumbuhan jaringan
pembuluh darah (neovaskularisasi), dan migrasi dari sel-sel mesenkimal (Kalfas
2001). Tahap ini terjadi pada awal kerusakan yaitu satu sampai lima hari pertama
setelah terjadi kerusakan.
2. Tahap Perbaikan (Pembentukan Kalus)
Tahap perbaikan fraktur diawali dengan pembentukan kalus kemudian
sampai 48 jam setelah fraktur, darah yang mengendap akan diinfiltrasi oleh sel
osteogenik yang ada pada lapisan periosteum, endosteum dan sumsum tulang. Sel
tersebut berproliferasi di pinggir fraktur dan dengan cepat menghampiri endapan
dan perbatasan area nekrotik. Kalus merupakan jaringan baru antara dua ujung
fraktur yang kemudian akan berubah menjadi jaringan tulang (Dorland 2002).
Awalnya, terjadi jaringan granulasi (kalus lunak) dan kemudian berubah menjadi
kartilago atau tulang (kalus keras). Fase jaringan granulasi diperpanjang dan
formasi jaringan tulang rawan hialin akan menyokong sampai terjadi
pembentukan tulang di kalus.
3. Tahap Pembentukan Tulang Rawan
Dalam waktu satu minggu, proliferasi sel akan mulai berdeferensiasi
menjadi khondroblas. Material matriks yang dilepaskan dari permukaan
kalsifikasi tulang rawan, vesikel matriks kecil keluar dengan proses enzimatik
(alkaline fosfatase dan enzim untuk ATP-dependent calcium transport) yang meningkatkan konsentrasi lokal dari orthofosfat yang akan berfungsi untuk
membentuk hidroksiapatit. Pada hari ke 7-10, pH di dalam kalus meningkat dan
akan menyokong endapan garam kalsium.
Tulang rawan yang terbentuk keberadaannya hanya sementara dan pada
akhirnya akan digantikan dengan tulang sebenarnya (woven bone) melalui tahap
remodelling, dan membutuhkan waktu untuk menjadi tulang lamellar (lamellar bone). Matriks ekstraseluler tulang rawan mengalami kalsifikasi, kemudian menyebabkan khondrosit mati. Tulang baru terbentuk sebagai tulang rawan yang
disintegrasi. Osteosit berkembang dari pluripoten mesenkim sel, fibroblast, dan
deposit osteoid. Selama tahap perbaikan, fibroblast menuju stroma yang akan
membantu pertumbuhan pembuluh darah (vaskular). Tahap perubahan tulang
rawan menjadi tulang terjadi melalui mekanisme osifikasi endokhondral.
4. Tahap Remodelling
Persembuhan fraktur akan sempurna selama tahap remodelling. Pada tahap ini kerusakan tulang telah kembali mempunyai bentuk, struktur, dan kekuatan
mekanik seperti semula. Remodelling tulang terjadi secara perlahan selama beberapa bulan bahkan tahun. Kekuatan tulang yang memadai akan dicapai dalam
tiga sampai enam bulan (Kalfas 2001).
Dalam pemasangan bone graft terdapat penggabungan antara tulang dan biomaterialnya. Persembuhan ini tidak sepenuhnya mirip dengan keadaan
persembuhan fraktur. Seperti pemasangan bone graft (autograft) pada prosedur cangkok tulang belakang, selama proses persembuhannya tulang dan graft
digabungkan oleh proses yang terintegrasi. Tulang lama mengalami nekrosis
secara perlahan dan diserap kembali dan sekaligus digantikan dengan tulang baru
yang lebih baik. Proses penggabungannya disebut “creeping subtitution’’(Lane et al. 1992), sel-sel primitif mesenkim berdeferensiasi menjadi osteoblas yang tersimpan di sekitar inti osteoid dari tulang yang nekrosis. Proses dari penggantian
dan remodelling pada akhirnya akan digantikan dari tulang yang nekrosis dalam
Masa yang paling kritis dalam penyembuhan tulang adalah
minggu-minggu pertama sampai minggu-minggu kedua. Pada saat ini peradangan dan
revaskularisasi terjadi. Penggabungan dan remodelling tulang dari sebuah bone graft membutuhkan sel-sel mesenkim yang memiliki akses vaskuler ke graft
untuk berdeferensiasi menjadi osteoblas dan osteoklas. Berbagai faktor sistemik
dapat menghambat penyembuhan tulang, contohnya malnutrisi, diabetes, rematik
arthritis, dan osteoporosis. Bone graft juga sangat dipengaruhi oleh faktor mekanikal lokal selama tahap remodelling tulang, kepadatan, geometri, ketebalan, dan orientasi trabekular tulang dapat berubah tergantung pada persyaratan
[image:31.595.84.515.338.776.2]mekanik dari graft.
Tabel 1 Persembuhan luka pada fraktur tulang tipe sederhana (uncomplicated)
Waktu Proses persembuhan
Immediate
1-5 hari
3-7 hari
1-4 minggu
>4 minggu
Hemoragi dan pembentukan hematoma Pembekuan darah pada perbatasan fraktur
Invasi makrofag untuk menghilangkan debris, RBC, dan fibrin Nekrosis sel osteosit pada daerah fraktur
Edema dan pengendapan fibrin pada jaringan sekitar fraktur Invasi jaringan granulasi
Proliferasi khondrosit dan osteoblas dari pinggir periosteal dan endosteal Pembentukan provisional kalus sebagai tulang yang merupakan penghubung oleh jaringan dan pulau-pulau granulasi dari tulang rawan
Bony kalus terbentuk oleh proses kalsifikasi, penghubung (jembatan) dari
provisional kalus dari hubungan trabekula osteoid yang diproduksi oleh osteoblas
Remodelling tulang: proses osteoclasia terus berlangsung dan pembentukan oleh osteoblas; Penghilangan eksternal kalus; Pelekukan internal kalus untuk membentuk sumsum tulang
(Cheville 2006)
Biomaterial (Bone graft)
Bone graft merupakan bahan pengganti tulang yang digunakan dalam perbaikan fraktur yang kompleks. Bahan ini digunakan juga untuk perbaikan
kerusakan (defek) tulang karena cacat bawaan, traumatik, operasi kanker tulang
digunakan adalah os ilium. Jaringan autograft memang merupakan jaringan yang sangat ideal untuk bone graft karena memiliki karakteristik yang sesuai dalam memicu pertumbuhan tulang seperti osteokonduktif, osteogenik dan osteoinduktif
(Laurencin & Yusuf 2009). Pemanenan tulang pengganti di bagian tulang lain
dapat menimbulkan komplikasi seperti inflamasi, infeksi, kerusakan kronis
apabila operasi tidak dilakukan dengan baik. Selain itu, jumlah jaringan yang
dapat dipanen sangat sedikit, sehingga menjadi kendala dalam ketersediaan.
Bone graft lainnya yang dapat digunakan yaitu allograft. Allograft adalah bahan pengganti tulang yang diperoleh dari individu lain dari spesies yang sama.
Sebagai alternatif dari autograft, allograft dapat diambil dari donor manusia atau kadaver. Namun penggunaannya memiliki resiko seperti adanya bahan pengawet
jaringan dan perlakuan jaringan sebelum dicangkokkan mengandung bahan
berbahaya seperti bahan pengawet ethylene oxide. Resiko lainnya, allograft
berpotensi menjadi transmisi penyakit-penyakit infeksius dari danor ke resipien
seperti hepatitis dan HIV AIDS. Sedangkan bone graft yang berasal dari hewan sering disebut xenograft. Kedua bone graft ini terkadang menimbulkan reaksi penolakan dari tubuh (Ratih et al. 2003). Sebagai alternatif lain pengganti tulang (bone graft) juga dapat disintesis dari berbagai biomaterial, seperti hidroksiapatit, trikalsium fosfat, hidrogel dan lain-lain.
Klasifikasi Bone Graft
Menurut (Laurencin et al. 2001), klasifikasi bone graft berdasarkan bahan dasarnya antara lain:
• Allograft-based bone graft substitutes, menggunakan allograft itu sendiri atau dikombinasi dengan material lainnya.
• Cell-based bone graft substitutes menggunakan sel-sel untuk membangkitkan jaringan baru, digunakan bahan ini sendiri atau ditanam
ke dalam bahan pendukung matrik (contohnya, mesenchymal stem cells).
• Ceramic-based bone graft substitutes seperti kalsium fosfat, kalsium sulfat dan bioglass, dapat digunakan dari bahan itu sendiri atau dikombinasikan.
• Polymer-based bone graft substitutes, degradable dan nondegradable polymer, dapat digunakan dari bahan itu sendiri atau dikombinasikan dengan material lainnya.
Dalam penelitian ini digunakan implan bone graft ceramic-based bone graft substitutes. Bahan yang digunakan adalah hidroksiapatit (HA) dan trikalsium fosfat (TKF). Penggunaan keramik, khususnya kalsium fosfat merupakan bagian
dari komponen anorganik primer tulang yang berupa kalsium hidroksiapatit, yang
termasuk ke dalam keluarga kalsium fosfat. Kalsium fosfat juga memiliki
karakteristik oseokonduktif, osteointegratif (formula jaringan baru yang
termineralisasi membentuk ikatan yang kuat dengan bahan implan) dan beberapa
menyatakan osteoinduktif (Laurencin & Yusuf 2009). Bahan ini membutuhkan
temperatur yang tinggi untuk membentuk scaffold dan mempunyai sifat rapuh.
Mineral Apatit
Komponen utama senyawa apatit adalah kalsium fosfat. Kalsium fosfat
terdiri dari beberapa fase yaitu oktakalsium fosfat, dikalsium fosfat dihidrat
(DKFD), trikalsium fosfat (TKF) dan hidroksiapatit (HA). Komponen mineral
apatit memiliki rumus kimia M10(ZO4)6X2. Unsur pada bagian M, Z dan X dapat
digantikan dengan unsur-unsur lain, yakni sebagi berikut; M= Ca, Se, Ba, Cd, Pb,
dll; Z= P, V, As, S, Si, Ge, dll; X = F, Cl, OH, O, Br, CO3, dll. Kristal apatit
mengandung banyak karbon dalam bentuk karbonat. Karbonat di dalam tubuh
dapat mensubtitusi formula hidroksiapatit dengan menempati dua posisi yakni
menggantikan posisi OH yang disebut sebagai apatit karbonat tipe A yang
terbentuk pada suhu tinggi. Karbonat menggantikan posisi PO43- disebut apatit
karbonat tipe B yang dapat dibentuk pada suhu rendah. Kalsium fosfat (Ca-P)
Hidroksiapatit
Hidroksiapatit (HA) merupakan material keramik bioaktif dengan
bioafinitas tinggi, bersifat biokompatibel dan bioaktif. Bioaktif adalah
kemampuan material bereaksi dengan jaringan dan menghasilkan ikatan kimia
yang sangat baik sedangkan biokompatibel adalah kemampuan material untuk
menyesuaikan dengan kecocokan tubuh penerima (Purnama 2006). Hidroksiapatit
merupakan unsur mineral terbesar yang terdapat pada tulang dan gigi (Aoki
1991). Hidroksiapatit termasuk ke dalam senyawa kalsium fosfat yang merupakan
senyawa mineral dan anggota kelompok mineral apatit dengan rumus kimia
[Ca10(PO4)6(OH)2] yang mempunyai struktur heksagonal serta memiliki rasio
Ca/P sekitar 1,67 (Aoki 1991). Senyawa ini adalah salah satu dari sedikit material
yang diklasifikasikan sebagai bioaktif material. Material tersebut dapat
mendukung pertumbuhan tulang tanpa adanya penghancuran ketika digunakan
untuk implantasi pada manusia. Hidroksiapatit dapat melekat secara biointegrasi.
Implan yang terbuat dari bahan ini dapat berkontak dan menyatu secara kimiawi
dengan tulang. HA dalam bentuk keramik dan kristal lambat dalam penyerapan
dan pembentukan tulang, sebaliknya pada non keramik, bentuk non kristal cepat
dalam penyerapan dan dalam pembentukan tulang (Reddy & Swamy 2010).
Trikalsium Fosfat
TKF merupakan salah satu jenis kalsium fosfat yang memiliki rasio Ca/P
sebesar 1,50 dan memiliki struktur kimia Ca3(PO4)2 (Aoki 1991). TKF memiliki 4
polymorph yaitu α, ß, γ dan super-α. ß polymorph adalah fase bertekanan tinggi dan super-αpolymorph dapat diobservasi pada temperatur kira-kira diatas 1500oC. Oleh karena itu, TKF polymorph yang sering digunakan dalam penelitian biokeramik adalah α dan ß-TKF (Shi 2004).
Beberapa penelitian menyatakan bahwa TKF memiliki sifat biodegradabel,
walaupun sedikit berbeda dengan karakteristik material yang digunakan (Shi
2004). Strukturnya juga berupa kristal, laju biodegradasi TKF lebih baik daripada
HA. Bahkan dalam penelitian yang dilakukan oleh Takatoshi (2007) menyatakan
penting sebagai bioresorbabel keramik. Bahan ini memperlihatkan tingginya daya
larut dan bioaktifitas. Hasilnya menunjukkan mikrostrutur ß-TKF berefek pada
aktifitas dari sel-sel tulang dan kemudian dapat menggantikan tulang. ß-TKF
dapat diterima dan digunakan di dalam tubuh atau dikenal sebagai biokompatibel,
bioresorbabel material untuk perbaikan tulang yang dibentuk menjadi keramik
blok, granul, atau fosfat semen (Shi 2004).
Karakteristik Implan (Bone Graft) Komposit Hidroksiapatit-Trikalsium Fosfat (HA-TKF)
Implan yang ditanamkan dalam penelitian ini merupakan kombinasi
hidroksiapatit dan trikalsium fosfat. Keduanya merupakan grup kalsium fosfat
namun berbeda fase. Hidroksiapatit memiliki sifat stabil namun memiliki
kemampuan penyerapan yang kecil. Untuk mengimbanginya ditambahkanlah
TKF (trikalsium fosfat) yang memiliki daya penyerapan lebih tinggi. Kombinasi
keduanya sering disebut bifase kalsium fosfat (BKF) keramik. Bifase kalsium fosfat keramik memiliki keuggulan potensi sebagai osteokonduktif dan memiliki
tingkat resorpsi optimal untuk pembentukan tulang (Xue et al. 2009)
Implan (bone graft) yang digunakan merupakan hasil pembuatan yang dilakukan oleh Nur Aisyah Nuzulia dari Departemen Fisika, Fakultas Matematika
dan Ilmu Pengetahuan Alam, IPB. Bikalsium fosfat (BKF) ini merupakan hasil
presipitasi material Na2HPO4.2H2O dengan butiran dari CaCl2.2H2O dengan rasio
Ca/P adalah 1,67. Hasil dari metode ini adalah bubuk BKF dan memiliki massa
sebesar 1,3162 gram. Hasil karakterisasi menggunakan scanning electron microscopy (SEM) menujukkan bahwa BKF keramik memiliki morfologi berupa kumpulan seperti bola besar yang tebal menunjukkan terbentuknya BKF dan bola
kecil yang mengelilinginya dan jumlahnya sangat banyak merupakan
hidroksiapatit (Fellah 2007 diacu dalam Nuzulia 2009). Dari hasil tersebut BKF
terlihat jelas dan terlihat juga pembentukan OCP yang terdiri dari piringan kecil
seperti partikel di permukaan sampel (Imaizumi 2006 diacu dalam Nuzulia 2009)
Kalsium fosfat keramik juga merupakan bahan yang memiliki sifat
spinal fusion, operasi scoliosis, dll (Saikia et al. 2008). Pemeriksaan histologi menunjukkan adanya pertumbuhan tulang baru ke dalam struktur pori-pori dari
implan HA. Di dalam hasil pengamatan preparat tersebut tidak ada bukti yang
meyakinkan bahwa implan terbiodegradasi meskipun terdapat histiosit,
multinukleat giant sel, osteoklas (Saikia et al. 2008). Sedangkan Levin et al
(1975) melaporkan bahwa pada percobaan menggunakan hewan model terjadi
resorpsi ß-TKF secara sempurna.
Fisiologi Perbaikan Tulang dan Bone Graft (Implan)
Penggunaan bone graft untuk mencapai tujuan arthodesis (membuat kaku sendi melalui pembedahan, sehingga tidak terjadi gerakan lagi pada sendi yang
bersangkutan) atau dalam pengisian tulang dipengaruhi oleh karakter anatomi,
histologi dan prinsip biokimiawi. Sebagai tambahan, beberapa sifat fisiologis
bone graft (cangkok tulang) akan mempengaruhi secara langsung keberhasilan atau kegagalan penggabungan graft. Sifat tersebut antara lain osteogenesis, osteoinduktif, dan osteokonduktif (Prolo 1990; Kalfas 2001).
Osteogenesis adalah kemampuan suatu graft untuk memproduksi tulang baru. Pada proses ini dipengaruhi oleh kehadiran sel-sel tulang di dalam graft
tulang. Material osteogenik graft terdiri dari sel dengan kemampuan untuk membentuk tulang (sel osteoprogenitor) atau berpotensi untuk berdiferensiasi
menjadi sel pembentuk tulang (diinduksi sel prekursor osteogenik/sel
osteoprogenitor). Sel yang berpartisipasi dalam tahap awal proses persembuhan
untuk menyatukan graft dengan tulang. Osteogenesis hanya ditemukan dalam properti autogenous tulang segar dan dalam sel sumsum tulang, meskipun penelitian mengenai sel dalam graft menunjukkan sangat sedikit yang ditransplantasikan dapat bertahan (Muschler et al. 1990).
Osteokonduktif adalah sifat fisik dari graft dalam menjalankan fungsi sebagai scaffold untuk mendukung dalam persembuhan tulang. Osteokonduktif memungkinkan untuk pertumbuhan neovaskularisasi dan infiltrasi sel-sel
prekursor osteogenik ke dalam ruang graft. Sifat osteokonduktif ditemukan di
Osteoinduktif adalah kemampuan dari material graft untuk menginduksi stem sel agar dapat berdeferensiasi menjadi sel-sel tulang dewasa. Proses ini
biasanya berkaitan dengan adanya faktor pertumbuhan tulang dalam material graft
atau suplemen pendukung dalam graft tulang. Bone morphogenic protein (BMP) dan mineralisasi matriks tulang merupakan bahan pokok osteoinduktif (Muschler
et al. 1990).
Domba sebagai Hewan Coba
Penggunaan domba dalam penelitian di bidang ortopedik semakin
meningkat dalam dekade terakhir ini, meskipun anjing masih menjadi pilihan
yang paling baik. Pada periode 1990-2001, sebanyak 9-12% domba digunakan
dalam penelitian ortopedik yang melibatkan patah tulang, osteoporosis, bone lengthenin, dan osteoarthritis. Pada periode 1980-1989 yang hanya digunakan kurang lebih sebanyak 5% (Martini et al. 2001). Peningkatan penggunaannya terkait dengan isu-isu etis dan persepsi negatif masyarakat dalam penggunaan
hewan kesayangan untuk penelitian medis.
Ditinjau dari segi makroskopisnya, sebagian besar literatur menyatakan
bahwa anjing lebih cocok digunakan sebagai model untuk tulang manusia dilihat
dari sudut pandang biologis, namun domba dewasa menawarkan keuntungan
diantaranya berat tubuh domba mirip dengan manusia. Kemudian keuntungan
lainnya domba memiliki dimensi tulang panjang yang sesuai untuk implantasi dan
percobaan prosthesis manusia (Newman et al. 1995) yang tidak mungkin dilakukan pada spesies yang lebih kecil seperti kelinci atau anjing dengan ras
kecil.
Penggunaan domba dalam eksperimental sering digunakan untuk menguji
biokompatibilitas berbagai biomaterial (Hunziker 2003), hal ini dilakukan untuk
mengetahui bioaktivitas yang berkaitan dengan resorpsi atau integrasi dari bahan
yang ditanamkan ke dalam tulang (Hing et al. 1998). Struktur khusus dan morfologi tulang panjang pada domba sesuai dengan fungsi dan beban mekanik
daerah tulang tertentu. Penggunaan domba memiliki hasil yang lebih baik
daripada hewan laboratorium kecil seperti tikus karena memiliki kesamaan
dilakukan oleh Nuss et al. (2006) juga menunjukkan bahwa pengujian dengan mengimplantasikan dengan cara membuat lubang bor pada domba terbukti dapat
menjadi model hewan yang sangat baik untuk menguji biokompatibilitas
biomaterial yang harus tertanam dalam tulang.
Secara histologi, struktur tulang domba dan manusia memiliki perbedaan.
Struktur tulang domba didominasi oleh struktur tulang primer (osteonnya
berdiameter kurang dari 100 µm) mengandung pembuluh darah sentral dan tidak
memiliki cement line (deKleer 2006). Komponen tulang pada manusia struktur tulang sekunder lebih mendominasi (Pearce et al. 2007). Perbedaan lainnya terlihat dari densitas atau kepadatan dari kedua tulang. Dalam penelitian Nafei et al. (2000) melaporkan kepadatan (massa/volume, mencerminkan tingkat porositas dari tulang) dari trabekular tulang domba yang diambil dari proksimal tibia domba
dewasa sebesar 0,61 g/cm3 dengan kerapatan abu 0,41 g/cm3 (massa/volume,
mencerminkan tingkat mineralisasi tulang). Data tersebut lebih tinggi dibanding
nilai untuk trabekular tulang femur manusia, dengan kerapatan 0,43 g/cm3 didapat
kepadatan abunya sebesar 0,26 g/cm3 sehingga domba memiliki kepadatan tulang
1,5-2 kali lebih besar dari manusia (Liebschner 2004).
Perbedaan kepadatan tersebut dapat pula berbeda pada lokasi tulang yang
berlainan. Sebagai contoh, Liebschner (2004) melaporkan bahwa kepadatan
trabekular tulang belakang domba sebesar 60±0,16 g/cm3 berbeda dengan tulang
belakang manusia yang kepadatan adalah 0,14±0,06 g/cm3. Dari segi komposisi
mineral tulang, menyimpulakan bahwa selain dari tahap awal fisiologis
pertumbuhan terdapat subsitusi parsial Mg2+ untuk Ca2 di trikalsium magnesium
fosfat, komposisi mineral manusia dan hewan tidak menunjukkan perbedaan yang
signifikan (Ravaglioli et al. 1996). Dalam hal remodelling tulang, berbagai riset melaporkan bahwa domba dan manusia memiliki pola yang sama dalam
BAHAN DAN METODE
Waktu dan Tempat
Penelitian dilakukan pada bulan April 2009 sampai bulan Agustus 2010 bertempat di Kandang Hewan Percobaan yang dikelola oleh Unit Pelayanan Teknis Hewan Laboratorium (UPT Helab), Laboratorium Bedah dan Radiologi, Laboratorium Histopatologi (Departemen Klinik Reproduksi dan Patologi), Laboratorium Anatomi, (Departemen Anatomi, Fisiologi dan Farmakologi), Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
Alat dan Bahan
Bahan dan peralatan yang digunakan dalam percobaan in vivo antara lain: tiga ekor domba sebagai hewan coba, satu set peralatan bedah minor, satu set peralatan bedah ortopedik, satu set perlengkapan operator dan asisten bedah, agen preanestesi (atropine sulfas) dan agen anestesi (xylazine HCl, Isofluran), serta obat-obatan seperti: antibiotika (penicillin, Cefotaxime®), analgesik (Toradol®),
iodium tincture 3%, campuran perubalsam, Levertraan Zalf dan Gusanex®. Bahan yang digunakan dalam pembuatan preparat histologi antara lain: formalin 10%, asam nitrat 5%, silol, parafin, Mayer’s Hematoksilin, larutan Eosin, alkohol dengan konsentrasi bertingkat. Peralatan yang digunakan antara lain: tissue cassatte, automatic tissue processor, alat bedah minor, cetakan parafin, penangas air, mikrotom, lemari pendingin, mikroskop cahaya OLYMPUS BX51® dan alat mikrofotografi MD 130® electric eyepiece.
Metode penelitian
Pemeliharaan Hewan Coba
keperluan evaluasi kondisi hewan sebelum percobaaan dan 90 hari setelah pemasangan implan tulang untuk keperluan pengamatan penelitian. Keseluruhan domba disembelih untuk dilakukan pengambilan tulang pada hari ke-30, 60 dan 90 pascaoperasi penanaman implan tulang.
Operasi Penanaman Material Implan HA-TKF
Operasi penanaman implan tulang dilakukan secara aseptik dengan peralatan dan perlengkapan yang telah disterilisasi. Implan yang akan ditanam sebelumnya dilakukan sterilisasi ultraviolet selama dua jam. Sebelum dilakukan anesthesi, semua domba diberikan preanesthesi atropine sulfas konsentrasi 0,25 mg/ml dengan dosis untuk domba sebesar 0,15-0,3 mg/kg (SC) (Plumbs 2005). Pada satu ekor domba pertama, induksi dan maintenance pembiusan dilakukan dengan sedasi xylazine 2% sedangkan dua ekor domba terakhir induksi juga menggunakan xylazine 2% namun pemberian maintenance menggunakan Isoflurane 1,5-3 % dengan suplai oksigen 500 ml. Dosis xylazine 2% yang digunakan adalah 0,10-0,22 mg/kg (IM) dan 0,10 mg/kg (IV) (Plumbs 2005).
untuk perlakuan 60 hari. Operasi ketiga dilakukan penanaman HA-TKF pada seekor domba betina untuk perlakuan 30 hari.
Setelah penanaman implan, tulang tersebut kemudian ditutup dengan penjahitan periosteum, otot, jaringan sub-kutan dan kulit dengan jahitan sederhana terputus. Operasi dilakukan oleh dokter hewan yang sama untuk mencegah variasi operasi. Semua domba diberi antibiotik topikal saat operasi berupa penicillin 50.000 IU.
Perawatan Hewan Coba Pascaoperasi
Kemudian setelah selesai operasi, semua domba diberi antibiotik per-injeksi yaitu Cefotaxime 250 mg (IM) sebanyak dua kali sehari dan juga diberi agen analgesik Toradol® satu kali sehari (PO) selama 5 hari pascaoperasi. Luka operasi secara rutin dibersihkan dengan revanol dan diberi iodine tincture 3% kemudian dioleskan campuran perubalsem dan Levertraan Zalf. Pada bagian luka dan sekitarnya diberikan Gusanex® sebagai antimiasis.
Pemeriksaan Makroskopis dan Mikroskopis
Sampel tulang tibia diambil dengan penyembelihan domba pada hari ke-30, 60 dan 90. Untuk data makroskopis, bagian tulang yang terdapat implan dipotong melintang menjadi dua sisi menggunakan gergaji triplek dengan mata gergaji kikir (ukuran kecil). Penentuan lokasi pemotongan ditentukan dengan melihat hasil foto radiografi tulang. Kemudian potongan melintang tersebut difoto dengan kamera digital. Sedangkan untuk data mikroskopis, tulang yang telah terpotong dua tersebut kemudian difiksasi dalam cairan formalin 10%. Tulang tersebut kemudian dibersihkan dari otot dan jaringan ikat yang membungkusnya. Bagian tulang tibia kiri yang telah diimplantasi selanjutnya dipotong setebal ±1-2 mm.
Pembuatan Preparat Tulang Gosok
perlahan agar tidak merusak struktur tulang. Setiap kali menggosok, dilakukan pencucian terhadap preparat dengan akuades steril untuk menghilangkan kotoran, debu-debu dari sisa penggosokan. Preparat tulang terus digosok hingga mencapai ketipisan yang sesuai (dicek dengan melihatnya di bawah mikroskop). Setelah mencapai ketipisan yang sesuai, preparat gosok tersebut kemudian dicuci dengan
shaker “EYELA Multi Shaker MMS” dengan skala kecepatan 5-6, dalam akuabides steril selama ± 2 hari. Akuabides diganti setiap hari agar kotorannya terbuang. Setelah preparat bersih, kemudian dilakukan pewarnaan Hematoksilin.
Pembuatan Preparat Tulang Dekalsifikasi
Tulang yang telah terpotong setebal ± 1-2 mm tersebut kemudian direndam dalam larutan dekalsifikasi (asam nitrat 5%) sampai lunak (±2 minggu). Selama itu, kelunakan tulang terus dipantau sampai benar-benar terdekalsifikasi. Ciri-ciri tulang terdekalsifikasi ialah strukturnya menjadi fleksibel, transparan, dan mudah ditusuk/digores. Setelah itu, tulang tersebut diproses secara histologi.
Proses histologi dilakukan mulai dari pemotongan tulang berbentuk
lempengan dan dimasukkan ke dalam tissue cassette. Sedian tulang ini lebih lanjut diproses dengan cara dimasukkan ke dalam automatic tissue processor. Di dalam alat tersebut secara otomatis jaringan akan diproses melalui tahap didehidrasi,
memperbaiki jaringan yang keriput. Irisan yang diletakkan di atas permukaan air hangat tersebut diangkat menggunakan gelas objek. Preparat kemudian dikeringkan dan diberi tanda dengan alat grafir dan disimpan dalam inkubator bertemperatur 60oC minimal 2 jam bertujuan agar jaringan benar-benar melekat.
Setelah itu dilanjutkan dengan proses pewarnaan. Proses pewarnaan dimulai dengan melarutkan sisa parafin dengan dimasukkan ke dalam silol. Kemudian sediaan didehidrasi dengan cara dimasukkan ke dalam alkohol bertingkat mulai dari alkohol absolut, alkohol 96% sampai alkohol 80%. Setelah itu preparat dicuci dengan menggunakan air selama 1 menit. Lalu dimasukkan kedalam larutan Hematoksilin selama 8 menit dan dicuci kembali dengan menggunakan air selama 30 detik. Selanjutnya sediaan dimasukkan kedalam larutan lithium carbonat selama 15-30 detik dan dicuci kembali dengan menggunakan air. Setelah sediaan dicuci dengan menggunakan air, selanjutnya sediaan dimasukkan ke dalam larutan Eosin selama 2-3 menit dan dibilas dengan air selama 30-60 detik. Kemudiaan sediaan didehidrasi dengan alkohol bertingkat mulai dari alkohol 96%, sebanyak 10 kali celupan, alkohol absolut I sebanyak 10
kali celupan, dan alkohol absolut II selama 2 menit. Setelah itu sediaan dimasukkan ke dalam larutan silol I selama 1menit dan silol II selama 2 menit. Selanjutnya sediaan dikeringkan dan ditutup dengan cover glass dan dilekatkan menggunakan entelan.
Metode Pengamatan
HASIL DAN PEMBAHASAN
Pengamatan Makroskopis
Keadaan normal struktur tulang panjang seperti os tibia memiliki bentuk yang kompak dan padat. Pembuatan lubang dengan menggunakan bor gigi pada
[image:44.595.112.515.363.465.2]os tibia akan merubah struktur bagian tulang yang dibor tersebut. Penanaman implan pada bagian defek setelah pengeboran akan direspon oleh jaringan tubuh. Begitu juga apabila tidak diberi implan akan mengalami perbaikan secara alami di dalam tubuh. Tubuh akan merespon suatu defek untuk memperbaiki kerusakan tersebut. Berikut hasil pengamatan makroskopis persembuhan kerusakan tulang segmental yang diimplantasi dengan HA-TKF (Tabel 1).
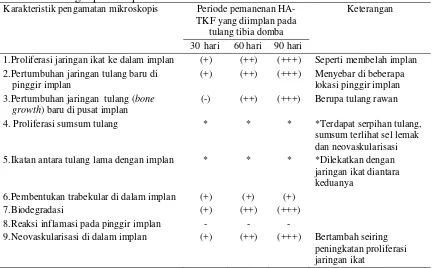
Tabel 1 Perubahan makroskopis jaringan tulang tibia dan implan HA-TKF pada berbagai periode pemanenan
Karakteristik pengamatan makroskopis Periode pemanenan HA-TKF yang diimplantasi pada tulang tibia domba
30 hari 60 hari 90 hari 1.Keadaan implan Terdegradasi Terdegradasi Terdegradasi 2.Warna Putih Putih Putih 3.Bentuk implan Pecah (+) Pecah (++) Pecah (+++) 4.Tingkat degradasi (+) (++) (+++) 5.Pertumbuhan jaringan baru ke dalam implan (+) (++) (+++) Keterangan: (+): sedikit; (++): banyak; (+++): semakin banyak
Berdasarkan pengamatan makroskopis (Tabel 1), pada keseluruhan periode pemanenan bagian implan HA-TKF memperlihatkan keadaan implan terdegradasi. Degradasi terhadap implan HA-TKF semakin meningkat seiring lamanya periode penanaman. Tubuh dapat melakukan respon dengan mendegradasi implan karena implan HA-TKF merupakan bahan material yang bersifat biodegradabel dan dapat digunakan untuk menggantikan jaringan tulang (Sunil et al. 2008).
sedangkan trikalsium fosfat umumnya dapat diresorpsi setelah 6 minggu pascaoperasi. Implan yang diamati berwarna putih, dan memiliki konsistensi yang keras dan rapuh. Beberapa literatur juga menyebutkan komposisi bahan TKF memiliki sifat yang sangat rapuh (Viswanath et al. 2008). Keadaan berbeda terjadi pada tulang kontrol yang dipanen pada hari ke-30 tanpa pemberian implan. Secara makroskopis pada defek tulang kontrol memperlihatkan adanya massa jaringan ikat yang tumbuh menutup lubang defek (Gambar 6B). Massa jaringan tersebut menunjukkan adanya pertumbuhan kalus. Pertumbuhan kalus terjadi pada awal minggu pertama sampai minggu keempat pasca kerusakan (Cheville 2006).
Gambaran pengamatan makroskopis pada hari ke-60 pascaoperasi menunjukkan adanya peningkatan proliferasi jaringan ikat ke dalam bahan implan. Jaringan ikat tumbuh ke dalam implan seperti pada tahap 30 hari dan terjadi peningkatan degradasi (Gambar 6C). Hasil makroskopis memperlihatkan bentuk implan HA-TKF yang terpecah menjadi bagian yang lebih kecil dari pada bentuk implan pada pemanenan 30 hari. Pada daerah pinggir implan terlihat jelas pertumbuhan tulang tetapi bagian pusat implan belum terlihat adanya
pertumbuhan. Sedangkan tulang kontrol memperlihatkan gambaran makroskopis dengan adanya massa jaringan pada lubang defek (Gambar 6D). Tahap persembuhan tersebut telah mencapai fase pertumbuhan kalus keras.
sedangkan pada tulang kontrol lubang defek telah menunjukkan adanya pertumbuhan tulang. Pertumbuhan tersebut sudah mirip dengan tulang disekitarnya (Gambar 6F).
Gambar 6 Gambaran makroskopis persembuhan tulang perlakuan (kolom kiri) dan tulang kontrol (kolom kanan) dengan pemanenan pada hari ke-30 (A, B), ke-60 (C, D), dan hari ke-90 (E, F) pascaoperasi. Peningkatan degradasi ditandai dengan semakin banyaknya pertumbuhan jaringan ikat ke pusat implan (Æ) dan terjadi perubahan struktur implan menjadi terpecah-pecah sehingga berubah menjadi bentuk granul pada hari ke-90. Persembuhan pada kelompok kontrol ditunjukkan pada lingkaran merah. s : sumsum tulang; i: implan. Bar : 5 mm.
A
B
C
D
E
F
s
s
s
s
s
s
i
i
Pengamatan Mikroskopis
Gambaran Mikroskopis Preparat Tulang Gosok
Proses penggosokan pada pembuatan preparat tulang gosok bertujuan untuk mendapatkan ketebalan minimum sehingga preparat mudah diamati dengan mikroskop cahaya. Saat proses penggosokan, bagian implan sulit untuk dipertahankan. Hal ini dikarenakan implan HA-TKF telah mengalami proses degradasi namun belum terbentuk tulang kompakta yang akan menggantikan implan dengan struktur tulang padat. Keadaan di pusat implan menjadi sangat rapuh sehingga dapat hilang karena proses mekanis saat penggosokan. Selain itu proses tersebut juga dapat mengikis jaringan ikat yang melekatkan tulang dengan implan.
Pada preparat tulang gosok yang diimplan dengan HA-TKF, bagian pusat implan tidak dapat diamati. Pertumbuhan jaringan tulang tipe trabekular terlihat pada bagian batas antara implan dan tulang. Adanya sedikit celah antara implan dan tulang tersebut (bagian pinggir implan) diduga memberikan ruang untuk migrasi sel-sel osteogenik dalam melakukan proses perbaikan. Hal sebaliknya
terjadi di pusat implan. Keadaan implan yang padat saat awal implantasi memungkinkan sulitnya vaskularisasi dan migrasi sel-sel osteogenik ke dalam implan, sehingga bagian pinggir antara tulang dan implan terlihat lebih cepat tumbuh dibandingkan dengan bagian pusat implan.
Gambar 7 Gambaran mikroskopis persembuhan tulang perlakuan (A) dan tulang kontrol (B) pada hari ke-30 pascaoperasi. Tanda panah merah menunjukkan daerah pertumbuhan tulang baru berbentuk tulang trabekular dan lingkaran merah menunjukkan daerah defek. Pewarnaan Hematoksilin. Bar: 0,5 mm.
Pada pengamatan preparat gosok yang diberi perlakuan implan selama 60 hari pascaoperasi terlihat pola pertumbuhan tulang di bagian pinggir menuju pusat implan. Pertumbuhan tersebut berasal dari bagian kerusakan di kedua sisinya. Selain itu pertumbuhan tulang trabekular juga aktif terjadi pada bagian pinggir tulang ke arah sumsum tulang (Gambar 8A). Proses ini terjadi karena bagian sumsum tulang mengandung bahan-bahan osteogenik (Kalfas 2001) seperti sel-sel osteoprogenitor yang akan berdeferesiasi menjadi sel osteoblas. Sel osteoblas ini yang nantinya akan berkembang menjadi struktur tulang yang kompak karena proses mineralisasi (Samuelson 2007).
Pada preparat kelompok kontrol pengamatan pascaoperasi selama 60 hari, daerah defek yang tidak diberi implan mengalami pertumbuhan atau proses osteogenesis. Tulang yang terbentuk memperlihatkan keadaan yang lebih baik dibandingkan dengan kelompok perlakuan. Bentukan tulang tidak lagi seperti pengamatan k