ABSTRAK
ADE JAMALUDIN SUNNY. Potensi Antibakteri Propolis
Trigona
spp asal
Bogor. Dibimbing oleh A.E. ZAINAL HASAN dan I MADE ARTIKA.
Propolis merupakan resin yang dikumpulkan lebah madu dari berbagai bagian
tumbuhan. Penelitian terhadap contoh propolis dari berbagai tempat menunjukan
keanekaragaman dalam komposisi kimiawinya. Komposisi kimiawi propolis ini
bergantung kepada jenis flora yang terdapat pada tempat pengambilannya. Hal ini
memberikan kemungkinan adanya perbedaan aktivitas antibakteri dari
masing-masing contoh.
ABSTRACT
ADE JAMALUDIN SUNNY. Potency of Bogor
Trigona spp Propolis as an
Antibacterial Subtance. Under direction A.E. ZAINAL HASAN and I MADE
ARTIKA.
Propolis contains resinous substances collected by honey bees from various
plant sources. Analysis of numerous samples from different geographic regions
led to the disclosure that the chemical composition of propolis is highly variable
depends on the specificity of the local flora at the site of collection and thus on the
geographic and climatic characteristics of this site. This fact results in the striking
diversity of propolis chemical composition, especially of propolis originating
from tropical regions.
PENDAHULUAN
Propolis merupakan produk dari sarang lebah yang sudah sejak lama digunakan sebagai antiseptik dan obat luka. Hasil penelitian modern menunjukkan bahwa propolis dapat berfungsi sebagai anti-imflamasi, pengobatan serangan jantung, diabetes, kanker, antifungal, antibakteri, dan antioksidan (Hegazi & El Hady 2001). Perkembangan penelitian terhadap propolis ini menarik untuk dicermati karena kandungan kimiawi propolis berbeda-beda antara suatu daerah dengan daerah lain.
Perbedaan vegetasi lingkungan tempat hidup lebah madu sangat berpengaruh terhadap kandungan kimiawi propolis. Walaupun demikian ternyata kandungan kimiawi yang berbeda-beda ini tidak serta-merta memberikan perbedaan terhadap aktivitas biologisnya (Bankova 2005). Sebagai contoh, hasil analisis tentang aktivitas antibakteri terhadap propolis yang berasal Eropa, Brazil, dan Amerika tengah yang dilakukan oleh Povova et al. (2004). Hasil analisis tersebut menunjukkan bahwa terdapat kemiripan aktivitas antibakteri dari semua contoh yang diuji kecuali yang berasal dari Amerika Selatan yang aktivitasnya lebih rendah. Kemiripan aktivitas antibakteri cukup mengherankan mengingat kimiawi propolis dari Brazil dan Eropa sangatlah berbeda. Penelitian lain yang dikerjakan oleh Banksota
et al. (2000) terhadap 4 contoh propolis yang berasal dari Brazil, Peru, Belanda, dan China menunjukkan bahwa semua propolis tersebut memiliki aktivitas antiradikal bebas yang relatif sama, kecuali yang berasal dari Peru yang aktivitasnya lebih kecil.
Kemiripan aktivitas biologis dari propolis yang berbeda kandungan kimiawinya ini merupakan hal yang menakjubkan. Penelitian terhadap propolis ini sangat penting untuk terus dilanjutkan untuk memberikan informasi yang detail tentang aktivitas biologis yang dimiliki propolis dalam hubungannya dengan kandungan kimiawinya yang beragam. Salah satu aktivitas biologis yang perlu mendapat perhatian adalah aktivitas antibakterinya. Penentuan senyawa antibakteri dari alam ini setidaknya dapat memberikan sebuah solusi terhadap kekhawatiran terhadap efek samping dari senyawa antibakteri sintetik.
Indonesia sebagai negara yang memiliki keanekaragaman hayati yang sangat kaya. Keanekaragaman ini memberikan tempat hidup yang berbeda-beda bagi lebah Trigona
spp, yang secara tidak langsung membuat
kandungan kimiawi propolis di suatu daerah dengan daerah lain tidak sama. Perbedaan inilah yang kemudian menjadi dasar penelitian untuk mempelajari aktivitas biologis dari propolis yang berasal dari Bogor, terutama aktivitas antibakterinya.
Penelitian bertujuan untuk memberikan informasi tentang aktivitas antibakteri dari propolis yang berasal dari daerah Bogor. Hipotesis penelitian adalah propolis yang berasal dari Bogor mempunyai aktivitas antibakteri dan berpotensi sebagai zat antibakteri alternatif. Manfaat penelitian ini adalah memberikan pengetahuan dan penjelasan propolis yang berasal daerah Bogor dapat dimanfaatkan sebagai zat antibakteri.
TINJAUAN PUSTAKA
Lebah madu Trigona spp
Lebah madu Trigona spp (Gambar 1), yang dalam bahasa daerah sering disebut klanceng, lanceng (Jawa), teweul (sunda) (Perum Perhutani 1986), merupakan salah satu serangga sosial yang hidup berkelompok membentuk koloni. Satu koloni lebah ini berjumlah 300-80.000 lebah. Trigona spp banyak hidup di daerah tropis dan subtropis, antara lain seperti di Amerika Selatan, setengah Afrika bagian selatan, dan Asia Selatan dan Asia Tenggara (Free 1982).
Trigona spp diklasifikasikan dalam divisi
Animalia, filum Arthropoda kelas Insecta,
ordo Hymenoptera, famili Apidae, genus
Trigona, dan spesies Trigona spp (Sihombing 1997).
Lebah Trigona spp merupakan salah satu
stingless bee atau lebah yang tidak memiliki sengat. Trigona spp memiliki sengat sisa, namun tidak digunakan sebagai alat pertahanan. Lebah ini akan menggigit musuhnya atau membakar kulit musuhnya dengan larutan basa. Organ vital (mata, hidung, dan telinga) musuh akan dikelilingi oleh lebah lain dalam satu koloninya. Lebah ini juga dilengkapi sistem kekebalan untuk menyerang serangga pengganggun lain (Free 1982).
Lebah Trigona spp lebih banyak mencari makan di pagi hari dibandingkan dengan di sore hari. Trigona sppdengan ukuran tubuh 5 mm mempunyai jarak terbang sekitar 600 m. Jarak terbang ini dipengaruhi oleh ukuran tubuh lebah, lebah yang lebih besar daripada
PENDAHULUAN
Propolis merupakan produk dari sarang lebah yang sudah sejak lama digunakan sebagai antiseptik dan obat luka. Hasil penelitian modern menunjukkan bahwa propolis dapat berfungsi sebagai anti-imflamasi, pengobatan serangan jantung, diabetes, kanker, antifungal, antibakteri, dan antioksidan (Hegazi & El Hady 2001). Perkembangan penelitian terhadap propolis ini menarik untuk dicermati karena kandungan kimiawi propolis berbeda-beda antara suatu daerah dengan daerah lain.
Perbedaan vegetasi lingkungan tempat hidup lebah madu sangat berpengaruh terhadap kandungan kimiawi propolis. Walaupun demikian ternyata kandungan kimiawi yang berbeda-beda ini tidak serta-merta memberikan perbedaan terhadap aktivitas biologisnya (Bankova 2005). Sebagai contoh, hasil analisis tentang aktivitas antibakteri terhadap propolis yang berasal Eropa, Brazil, dan Amerika tengah yang dilakukan oleh Povova et al. (2004). Hasil analisis tersebut menunjukkan bahwa terdapat kemiripan aktivitas antibakteri dari semua contoh yang diuji kecuali yang berasal dari Amerika Selatan yang aktivitasnya lebih rendah. Kemiripan aktivitas antibakteri cukup mengherankan mengingat kimiawi propolis dari Brazil dan Eropa sangatlah berbeda. Penelitian lain yang dikerjakan oleh Banksota
et al. (2000) terhadap 4 contoh propolis yang berasal dari Brazil, Peru, Belanda, dan China menunjukkan bahwa semua propolis tersebut memiliki aktivitas antiradikal bebas yang relatif sama, kecuali yang berasal dari Peru yang aktivitasnya lebih kecil.
Kemiripan aktivitas biologis dari propolis yang berbeda kandungan kimiawinya ini merupakan hal yang menakjubkan. Penelitian terhadap propolis ini sangat penting untuk terus dilanjutkan untuk memberikan informasi yang detail tentang aktivitas biologis yang dimiliki propolis dalam hubungannya dengan kandungan kimiawinya yang beragam. Salah satu aktivitas biologis yang perlu mendapat perhatian adalah aktivitas antibakterinya. Penentuan senyawa antibakteri dari alam ini setidaknya dapat memberikan sebuah solusi terhadap kekhawatiran terhadap efek samping dari senyawa antibakteri sintetik.
Indonesia sebagai negara yang memiliki keanekaragaman hayati yang sangat kaya. Keanekaragaman ini memberikan tempat hidup yang berbeda-beda bagi lebah Trigona
spp, yang secara tidak langsung membuat
kandungan kimiawi propolis di suatu daerah dengan daerah lain tidak sama. Perbedaan inilah yang kemudian menjadi dasar penelitian untuk mempelajari aktivitas biologis dari propolis yang berasal dari Bogor, terutama aktivitas antibakterinya.
Penelitian bertujuan untuk memberikan informasi tentang aktivitas antibakteri dari propolis yang berasal dari daerah Bogor. Hipotesis penelitian adalah propolis yang berasal dari Bogor mempunyai aktivitas antibakteri dan berpotensi sebagai zat antibakteri alternatif. Manfaat penelitian ini adalah memberikan pengetahuan dan penjelasan propolis yang berasal daerah Bogor dapat dimanfaatkan sebagai zat antibakteri.
TINJAUAN PUSTAKA
Lebah madu Trigona spp
Lebah madu Trigona spp (Gambar 1), yang dalam bahasa daerah sering disebut klanceng, lanceng (Jawa), teweul (sunda) (Perum Perhutani 1986), merupakan salah satu serangga sosial yang hidup berkelompok membentuk koloni. Satu koloni lebah ini berjumlah 300-80.000 lebah. Trigona spp banyak hidup di daerah tropis dan subtropis, antara lain seperti di Amerika Selatan, setengah Afrika bagian selatan, dan Asia Selatan dan Asia Tenggara (Free 1982).
Trigona spp diklasifikasikan dalam divisi
Animalia, filum Arthropoda kelas Insecta,
ordo Hymenoptera, famili Apidae, genus
Trigona, dan spesies Trigona spp (Sihombing 1997).
Lebah Trigona spp merupakan salah satu
stingless bee atau lebah yang tidak memiliki sengat. Trigona spp memiliki sengat sisa, namun tidak digunakan sebagai alat pertahanan. Lebah ini akan menggigit musuhnya atau membakar kulit musuhnya dengan larutan basa. Organ vital (mata, hidung, dan telinga) musuh akan dikelilingi oleh lebah lain dalam satu koloninya. Lebah ini juga dilengkapi sistem kekebalan untuk menyerang serangga pengganggun lain (Free 1982).
Lebah Trigona spp lebih banyak mencari makan di pagi hari dibandingkan dengan di sore hari. Trigona sppdengan ukuran tubuh 5 mm mempunyai jarak terbang sekitar 600 m. Jarak terbang ini dipengaruhi oleh ukuran tubuh lebah, lebah yang lebih besar daripada
yang memiliki nektar dengan kandungan gula yang tinggi. Lebah ini akan memberitahukan keberadaan sumber nektar pada lebah lain dalam koloninya dengan menggunakan suatu tarian. Jenis lebah Trigona yang lain ada yang menandai sumber makanannya dengan menggunakan feromon dari kelenjar mandibular yang dikenali oleh lebah lain dalam satu koloni (Free 1982).
Gambar 1 Lebah madu Trigona spp (Brisbane Insects 2010).
Koloni lebah madu terdiri atas kasta reproduktif (lebah ratu dan lebah jantan) dan kasta nonreproduktif (lebah pekerja). Setiap kasta atau golongan memiliki keunikan anatomis, fisiologis dan dan fungsi biologis yang berbeda-beda (sifat polimorfisme). Di dalam satu koloni lebah hanya terdapat satu ekor ratu yang berukuran paling besar dan bertugas hanya menghasilkan telur, beberapa ratus lebah jantan (drone) yang berfungsi mengawini lebah ratu perawan, dan beberapa puluh ribu lebah pekerja, serta ditambah telur, larva, dan pupa (Sihombing 1997). Semua pekerjaan di dalam koloni dilakukan oleh lebah pekerja. Berdasarkan tempat berlangsungnya tempat pekerjaan, tugas lebah dibagi menjadi 2 golongan, yaitu tugas di dalam sarang dan di luar sarang serta pembagian tugasnya berdasarkan umur.
Propolis
Propolis merupakan resin lengket yang terdapat pada sarang lebah (Hegazi & El Hady 2001). Resin ini dikumpulkan oleh lebah pekerja dari kuncup, kulit tumbuhan atau bagian-bagian lain dari tumbuhan. Resin-resin yang diperoleh dari bermacam-macam tumbuhan ini dicampur dengan saliva dan enzim lebah sehingga berbeda dari resin asalnya lebah menggunakan resin ini untuk berbagai keperluan (Gojmerac 1993).
Propolis ini telah digunakan dalam jangka waktu yang lama dalam pengobatan tradisional di berbagai negara tidak kurang sejak 3000 tahun sebelum Masehi. Beberapa peneliti telah mengonfirmasi tentang kegunaan propolis ini. Propolis dapat berfungsi sebagai
anti-imflamasi, antibakteri, antikanker, antifungi antivirus, dan antioksidan (Hegazi & El Hady 2001).
Gojmerac (1983) menyatakan bahwa propolis mengandung bahan campuran kompleks malam, resin, balsam, minyak, dan sedikit pollen. Komposisinya bervariasi tergantung dari tumbuhan asal. Propolis juga mengandung zat aromatik, zat wangi, dan berbagai mineral. Propolis dan jumlah senyawa-senyawanya menunjukkan berma-cam-macam efek biologis dan aktivitas farmakologis. Lebih dari 200 senyawa yang terkandung di dalam propolis sudah diketahui (Khismatullina 2005).
Banyak peneliti yang percaya bahwa senyawa-senyawa kimia yang bertanggung jawab besar terhadap aktivitas biologis propolis adalah asam kafeat, flavonoid, dan ester fenolat (Katircioglu & Mercan 2006). Flavonoid berperan dalam pewarnaan tumbuhan. Sekurang-kurangnya ada 38 jenis flavonoid yang termasuk flavonol (galanin, kaemferol, quersetin), dan flavonon (pinobanksin), serta flavon (chrysin, acacetin, apigenin, ermanin). beberapa senyawa fenolat yang terkandung di dalam propolis adalah hidroksisinamat, asam sinamat, vanilin, benzin alkohol, asam benzoat, kafeat, kumarat, serta asam ferulat. Nilai nutrisi propolis sangat kecil, yaitu berasal dari protein, asam amino, mineral, dan gula, serta vitamin dalam jumlah kecil seperti vitamin A, B1, B2, B6, C, dan E (Khismatullina 2005).
Kemampuannya sebagai antibakteri tidak terlepas dari senyawa-senyawa aktif yang terdapat di dalamnya. Senyawa aktif yang memberikan efek antibakteri adalah
pinochebrin, pinobanksin, asam kafeat, dan asam ferulat. Senyawa antifunginya adalah
pinochebrin, pinobanksin, asam kafeat, lutseolin, dan quersetin. Zat aktif yang diketahui bersifat antibiotik adalah asam ferulat. Zat ini efektif terhadap bakteri Gram positif dan bakteri Gram negatif. Asam ferulat juga berperan dalam pembekuan darah sehingga dapat dimanfaatkan untuk mengobati luka dan diberikan dalam bentuk salep (Winingsih 2004 diacu dalam Lasmayanty 2008).
agalactiae dengan menghambat pembelahan sel. Mereka juga melihat indikasi bahwa propolis mengganggu organisasi sel dan membran sel.
Kondisi Geografis Asal Propolis
Propolis dikumpulkan lebah dari berbagai macam bagian tanaman. Oleh karena itu komposisi kimiawi resin ini sangat bergantung kepada jenis tanaman yang dijadikan asal resin tersebut. Lingkungan yang berbeda dengan jenis vegetasi yang berbeda akan secara tidak langsung memberikan kandungan kimiawi propolis yang berbeda pula (Bankova & Marcucci, 2000). Pebedaan musim pada suatu tempat umumnya tidak menyebabkan perbedaan kandungan kimiawi propolis. Musim yang berbeda hanya menyebabkan perbedaan kuantitas zat kimia yang ada dalam propolis (Bankova et al. 1998).
Propolis yang dipakai dalam penelitian berasal dari Kota Bogor. Kota Bogor terletak pada ketinggian 190 sampai 330 meter dari permukaan laut. Udaranya relatif sejuk dengan suhu udara rata-rata setiap bulannya adalah 26°C dan kelembaban udaranya kurang lebih 70%. Suhu rata-rata terendah di Bogor adalah 21.8°C, paling sering terjadi pada bulan Desember dan Januari. Arah mata angin dipengaruhi oleh angin muson. Bulan Mei sampai Maret dipengaruhi angin muson barat (Pemerintahan Kota Bogor 2009)
Kemiringan Kota Bogor berkisar antara 0-15% dan sebagian kecil daerahnya mempunyai kemiringan antara 15–30%. Jenis tanah hampir di seluruh wilayah adalah latosol coklat kemerahan dengan kedalaman efektif tanah lebih dari 90 cm dan tekstur tanah yang halus serta bersifat agak peka terhadap erosi. Bogor terletak pada kaki Gunung Salak dan Gunung Gede, sehingga sangat kaya akan hujan orografi. Angin laut dari Laut Jawa yang membawa banyak uap air masuk ke pedalaman dan naik secara mendadak di wilayah Bogor sehingga uap air langsung terkondensasi dan menjadi hujan. Hampir setiap hari turun hujan di kota ini dalam setahun (70%) sehingga dijuluki "Kota Hujan". Keunikan iklim lokal ini dimanfaatkan oleh para perencana kolonial Belanda dengan menjadikan Bogor sebagai pusat penelitian botani dan pertanian, yang diteruskan hingga sekarang (Pemerintahan Kota Bogor 2009).
Iklim basah Bogor ini memungkinkan berbagai macam tumbuhan dapat hidup di dalamnya. Hal ini yang kemudian menjadi awal pembentukan vegetasi yang unik bagi lebah. Vegetasi seperti inilah yang
menyediakan bahan-bahan untuk pembentukan propolis sarang lebah.
Bakteri Uji
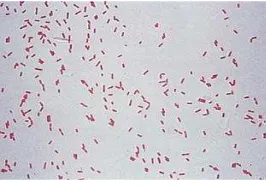
Bakteri merupakan protista prokariot bersel tunggal yang sangat beragam dan terdapat di mana-mana. Dinding sel merupakan salah satu komponen utama sel yang memberikan bentuk serta kekuatan pada sel prokariot. Berdasarkan komposisi dan struktur dinding selnya, bakteri dibagi ke menjadi 2 golongan, yaitu bakteri Gram negatif dan bakteri Gram positif. Perbedaan keduanya dapat dilihat dengan menggunakan pewarnaan Gram. Bakteri Gram positif memberikan warna ungu atau biru, sedangkan bakteri Gram negatif berwarna merah (Pelczar & Chan 1988).
Bacillus subtilis
Bakteri yang Gram positif ini berbentuk batang besar dengan flagel peritrik. Bakteri ini bersifat anaerob dan anaerob fakultatif. Bakteri yang hidup dengan menggunakan sumber C dan N sebagai sumber pertumbuhan ini, berukuran 0.5 -2.5 x 1.2-2.0 μm dengan suhu optimum 25-37°C. bakteri ini sering ditemukan di tanah, air, dan udara (Gambar 2).
Staphylococcus aureus
Staphylococcus aureus merupakan bakteri Gram positif dan termasuk famili
Micrococaceae. Bentuknya kokus dengan diameter 0.5-1.5 µm. bakteri ini ditemukan dalam bentuk tunggal, berpasangan, atau bergerombol seperti anggur. Bakteri ini bersifat patogen, nonmotil, tidak berspora, tidak berkapsul, hidup secara anaerob fakultatif, tetapi tumbuh cepat pada keadaan aerob. Suhu optimum pertumbuhanya adalah 30-37°C. koloni bakteri ini menghasilkan warna putih, kuning, atau kuning orange (Pelczar & Chan 1988; Lay & Hastowo 1992).
Eschericia coli
Eschericia coli merupakan penghuni normal saluran pencernaan manusia dan hewan berdarah panas. Biasanya tidak patogenik, tetapi dapat menimbulkan infeksi. Bila memasuki kandung kemih, dapat menyebabkan sistisis. Bakteri ini sering digunakan sebagai indikator kualitas air. Beberapa galur tertentu dapat menyebabkan gastroentritis, disentri pada manusia, dan diare (Pelczar & Chan 1988).
Bakteri E. coli termasuk ke dalam famili
yang termasuk bakteri Gram negatif yang tidak berspora ini tumbuh baik pada pH 7.0-7.5, dengan suhu optimum 37ºC. Koloni E. coli
menghasilkan warna putih kekuningan, dan permukaan bergelombang di atas agar (Fardiaz 1983). Bakteri ini bersifat nonmotil dan hidup secara anaerob fakultatif (Holt et al. 1994).
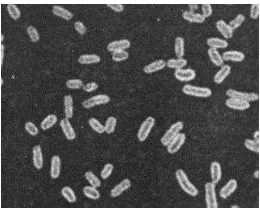
Pseudomonas aeruginosa
Bakteri ini merupakan bakteri Gram negatif. Bakteri ini berbentuk lurus melengkung, berukuran 0.5-1.0 x 1.5-5.0 µm (Gambar 4). Bakteri ini hidup secara aerob, motil dengan flagel polar, tidak berspora, koloninya tidak teratur, serta suhu optimum pertumbuhannya 37ºC.
Bakteri ini dapat tumbuh pada media umum, dapat hidup di dalam air suling dan tumbuh baik pada media Nitrogen dengan bermacam-macam senyawa karbon. Habitatnya di air dan tanah, terdapat pada kulit, membran mukosa, dan tinja. Pada manusia yang sehat, bakteri ini ditemukan dalam usus halus 10-15%. Bakteri ini juga sering kali merupakan pencemar dan penyebab terjadinya infeksi (Felczar & Chan 1988; Fardiaz 1989; Holt et al.. 1994).
Antibakteri
Bahan antimikrob merupakan bahan kimia yang dapat mengganggu pertumbuhan dan metabolisme mikrob. Berdasarkan kelompok metabolismenya, antimikrob meliputi anti-bakteri, antifungi, antivirus, dan antiprotozoa (Koolman 1997). Antibakteri adalah zat yang dapat menghambat pertumbuhan bakteri dan digunakan secara khusus untuk mengobati infeksi (Pelczar & Chan 1988).
Berdasarkan cara kerjanya, antibakteri dibedakan menjadi bakterisidal dan bakteriostatik. Antibakteri yang bersifat bakterisidal adalah zat yang bekerja untuk mematikan bakteri, sedangkan bakteriostatik bekerja untuk menghambat pertumbuhannya. Beberapa zat antibakteri bersifat bakteriostatik pada konsentrasi rendah, dan bersifat bakterisidal pada konsentrasi tinggi (Koolman 1997).
Gambar 2 Hasil pewarnaan Gram terhadap
Bacillus subtilis (Todar 2008).
Gambar 3 Bentuk kapsul E. coli (Stirm & Molbert 1970).
Menurut Koolman (1997), berdasarkan selektifitas dan pengaruh penghambatan terhadap bakteri, antibakteri terbagi menjadi antibakteri berspetrum sempit dan antibakteri berspektrum luas. Antibakteri berspektrum sempit mempunyai kemampuan untuk menghambat pertumbuhan bakteri Gram tertentu, sedangkan yang berspektrum luas dapat menghambat pertumbuhan bakteri baik Gram positif maupun Gram negatif.
Mekanisme kerja antibakteri dapat terjadi melalui beberapa cara, yaitu : 1) kerusakan pada dinding sel, 2) perubahan permeabilitas sel, dan 3 menghambat sintesis protein dan asam nukleat (Koolman 1997).
Banyak faktor dan keadaan yang dapat mempengaruhi kerja antibakteri, antara lain konsentrasi antibakteri, jumlah bakteri, spesies bakteri, adanya bahan organik, suhu, dan pH (Pelczaar & Chan 1988). Antibiotik adalah senyawa khas yang dihasilkan oleh organisme atau merupakan turunannya termasuk analognya yang dibuat secara sintetik, yang dalam kadar rendah mampu menghambat proses penting dalam kehidupan satu spesies atau lebih mikroorganisme (Siswandono & Soekardjo 1995).
Salah satu jenis antibiotik adalah ampisilin. Ampisilin merupakan jenis antibiotik turunan penisilin dan merupakan senyawa antibakteri berspektrum luas dan bersifat bakterisidal. Ampisilin tahan terhadap asam, tetapi tidak tahan terhadap penisilinase (Gambar 5).
Gambar 4 Hasil foto Pseudomonas aeruginosa
Gambar 5 Struktur kimia Ampisilin.
Mekanisme kerja ampisilin di dalam sel bakteri adalah menghambat pembentukan dinding sel dengan cara mencegah bergambungnya asam N-asetilmuramat. Ampisilin digunakan untuk pengobatan infeksi saluran nafas dan saluran seni, gonorhoe,
gastrosentritis, meningitis, dan infeksi tipoid (Siswandono & Soekardjo 1995).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang dibutuhkan adalah 140 gram propolis kasar Trigona spp yang berasal dari Bogor, Jawa Barat, bakteri Bacillus subtilis, Staphylococcus aureus, E. coli, Pseudomonas aeruginosa, NaCl teknis, pepton, ekstrak yeast, glukosa, agar bakto, etanol 70%, propilen glikol teknis, akuades dan pereaksi-pereaksi dalam uji fitokimia.
Alat-alat yang digunakan adalah laminar air flow cabinet, inkubator, autoklaf, autopipet, alumunium foil, kapas, cawan Petri, vortex, alat-alat gelas, dan rotavapor.
METODE PENELITIAN
Ekstraksi Propolis
Propolis diekstraksi dengan metode Matienzo dan Lamorena (2004). Ekstraksi dilakukan dengan maserasi menggunakan etanol 70% sebagai pelarutnya. Sejumlah 140,58 gram propolis kasar Trigona spp direndam dalam 500 mL etanol 70%. Suspensi tersebut ditutup dan dikocok dengan shaker
selama 1 minggu dalam ruang gelap. Setelah 1 minggu filtrat disaring, lalu residunya dimaserasi kembali. Selanjutnya, fitrat diambil setiap hari selama 1 minggu atau sampai filtrat terakhir jernih.
Seluruh filtrat yang diperoleh dipekatkan menggunakan rotavapor pada suhu 45ºC. Setelah itu, ekstrak pekat yang dilarutkan dalam propilen glikol sebanyak 1 kali volumenya, sehingga konsentrasi murni propolis sebesar 50% dari total ekstrak propolis.
Analisis Fitokimia
Analisis fitokimia dilakukan untuk mengetahui golongan senyawa aktif pada ekstrak propolis secara kualitatif. Analisis fitokimia ini dilakukan berdasarkan metode Harborne (1987). Identifikasi yang dilakukan adalah uji flavonoid dan senyawa fenolik, uji tanin, uji minyak atsiri, uji steroid/triterpenoid, uji saponin, uji alkaloid, uji glikosida, uji gula pereduksi. Contoh propolis yang digunakan ialah ekstrak propolis yang telah diencerkan dengan akuades.
Uji flavonoid dan senyawa fenolik. Contoh propolis dengan pengenceran 1:2 dilarutkan dalam metanol lalu dipanaskan pada suhu 50°C. Filtrat ditambah larutan NaOH atau asam sulfat pekat. Warna merah atau jingga yang terbentuk akibat penambahan NaOH menunjukkan adanya senyawafenolik hidrokuinon dan merah akibat penambahan asam sulfat pekat menunjukkan adanya flavonoid. Pembanding yang digunakan ialah buah pinang.
Uji tanin. Contoh propolis dengan pengenceran 1:10 ditambah 1:2 mL FeCl3 10%. Jika terbentuk warna biru atau hijau kehitaman menunjukkan adanya tanin. Pembanding adalah daun teh.
Uji minyak atsiri. Contoh propolis dilarutkan dengan alkohol lalu diuapkan hingga kering. Jika berbau aromatis spesifik, maka contoh mengandung minyak atsri.
Uji triterpenoid dan steroid. Contoh propolis dengan pengenceran 1:10 dipanaskan dengan etanol. Filtratnya diuapkan alu ditambah eter. Lapisan eter ditambah dengan pereaksi Liebermann Burchard (3 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat). Terbentuk warna hijau atau biru menunjukkan adanya steroid warna merah atau ungu menunjukkan adanya senyawa triterpenoid. Pembanding yang digunakan adalah kuning telus.
Uji saponin. Contoh propolis dengan pengeceran 1:10 dikocok selama 5 menit. Busa yang terbentuk setinggi tidak kurang dari 1 cm dan tetap stabil setelah didiamkan selama 15 menit menunjukkan adanya saponin. Pembanding yang digunakan adalah buah klerak.
Gambar 5 Struktur kimia Ampisilin.
Mekanisme kerja ampisilin di dalam sel bakteri adalah menghambat pembentukan dinding sel dengan cara mencegah bergambungnya asam N-asetilmuramat. Ampisilin digunakan untuk pengobatan infeksi saluran nafas dan saluran seni, gonorhoe,
gastrosentritis, meningitis, dan infeksi tipoid (Siswandono & Soekardjo 1995).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang dibutuhkan adalah 140 gram propolis kasar Trigona spp yang berasal dari Bogor, Jawa Barat, bakteri Bacillus subtilis, Staphylococcus aureus, E. coli, Pseudomonas aeruginosa, NaCl teknis, pepton, ekstrak yeast, glukosa, agar bakto, etanol 70%, propilen glikol teknis, akuades dan pereaksi-pereaksi dalam uji fitokimia.
Alat-alat yang digunakan adalah laminar air flow cabinet, inkubator, autoklaf, autopipet, alumunium foil, kapas, cawan Petri, vortex, alat-alat gelas, dan rotavapor.
METODE PENELITIAN
Ekstraksi Propolis
Propolis diekstraksi dengan metode Matienzo dan Lamorena (2004). Ekstraksi dilakukan dengan maserasi menggunakan etanol 70% sebagai pelarutnya. Sejumlah 140,58 gram propolis kasar Trigona spp direndam dalam 500 mL etanol 70%. Suspensi tersebut ditutup dan dikocok dengan shaker
selama 1 minggu dalam ruang gelap. Setelah 1 minggu filtrat disaring, lalu residunya dimaserasi kembali. Selanjutnya, fitrat diambil setiap hari selama 1 minggu atau sampai filtrat terakhir jernih.
Seluruh filtrat yang diperoleh dipekatkan menggunakan rotavapor pada suhu 45ºC. Setelah itu, ekstrak pekat yang dilarutkan dalam propilen glikol sebanyak 1 kali volumenya, sehingga konsentrasi murni propolis sebesar 50% dari total ekstrak propolis.
Analisis Fitokimia
Analisis fitokimia dilakukan untuk mengetahui golongan senyawa aktif pada ekstrak propolis secara kualitatif. Analisis fitokimia ini dilakukan berdasarkan metode Harborne (1987). Identifikasi yang dilakukan adalah uji flavonoid dan senyawa fenolik, uji tanin, uji minyak atsiri, uji steroid/triterpenoid, uji saponin, uji alkaloid, uji glikosida, uji gula pereduksi. Contoh propolis yang digunakan ialah ekstrak propolis yang telah diencerkan dengan akuades.
Uji flavonoid dan senyawa fenolik. Contoh propolis dengan pengenceran 1:2 dilarutkan dalam metanol lalu dipanaskan pada suhu 50°C. Filtrat ditambah larutan NaOH atau asam sulfat pekat. Warna merah atau jingga yang terbentuk akibat penambahan NaOH menunjukkan adanya senyawafenolik hidrokuinon dan merah akibat penambahan asam sulfat pekat menunjukkan adanya flavonoid. Pembanding yang digunakan ialah buah pinang.
Uji tanin. Contoh propolis dengan pengenceran 1:10 ditambah 1:2 mL FeCl3 10%. Jika terbentuk warna biru atau hijau kehitaman menunjukkan adanya tanin. Pembanding adalah daun teh.
Uji minyak atsiri. Contoh propolis dilarutkan dengan alkohol lalu diuapkan hingga kering. Jika berbau aromatis spesifik, maka contoh mengandung minyak atsri.
Uji triterpenoid dan steroid. Contoh propolis dengan pengenceran 1:10 dipanaskan dengan etanol. Filtratnya diuapkan alu ditambah eter. Lapisan eter ditambah dengan pereaksi Liebermann Burchard (3 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat). Terbentuk warna hijau atau biru menunjukkan adanya steroid warna merah atau ungu menunjukkan adanya senyawa triterpenoid. Pembanding yang digunakan adalah kuning telus.
Uji saponin. Contoh propolis dengan pengeceran 1:10 dikocok selama 5 menit. Busa yang terbentuk setinggi tidak kurang dari 1 cm dan tetap stabil setelah didiamkan selama 15 menit menunjukkan adanya saponin. Pembanding yang digunakan adalah buah klerak.
endapan coklat dengan pereaksi Wagner. Pembanding yang digunakan adalah tapak dara berbunga putih.
Uji glikosida. Untuk menunjukkan adanya glikosida digunakan pereaksi Molisch. Sebanyak 2 mL ekstrak propolis dengan pengenceran 1:2 ditambah dengan 2-3 tetes asam sulfat pekat dan dibiarkan selama 3 menit lalu ditambah dengan pereaksi Molisch. Warna ungu kemerahan yang terbentuk menunjukkan adanya glikosida.
Uji gula pereduksi. Contoh propolis dengan pengenceran 1:2 dipanaskan sampai mendidih di dalam larutan 1 mL fehling A dan 1 mL Fehling B lalu didinginkan. Endapan merah bata menunjukkan adanya gula pereduksi.
Uji Aktivitas Antibakteri
Propolis yang diperoleh dari tahap sebelumnya digunakan dalam pengujian antibakteri. Bakteri yang digunakan adalah,
Bacillus subtilis, E. coli, Pseudomonas aeruginosa, Staphylococcus aureus. Sebelum dipakai, bakteri tersebut dikulturkan terlebih dahulu dalam media cair PYG selama sekitar 24 jam jam (media cair PYG mengandung 1% (b/v) pepton, 1% yeast extract, dan 2% glukosa dalam pelarut air).
Pengujian kemampuan antibakteri bakteri ini dimulai dengan uji pendahuluan menggunakan metode difusi sumur. Sebanyak 50µL dimasukkan ke dalam sumur yang telah dibuat sebelumnya pada media agar PYG yang telah diebar dengan bakteri uji. Media agar PYG mengandung 1% (b/v) pepton, 1% yeast extract, 2% glukosa, dan 2% agar bakto dalam pelarut air. Setelah itu, semua contoh diinkubasi di bawah suhu 37ºC selama sekitar 24 jam. Adanya zona bening menunjukan adanya aktivitas antibakteri.
Pengujian kemampuan antibakteri ini dilanjutkan dengan pencarian nilai konsentrasi hambat tumbuh minimum (KHTM). Metode sumur digunakan kembali untuk mencari nilai KHTM ini. Propolis 100% diencerkan menjadi beberapa konsentrasi yang lebih rendah sampai konsentrasi 0,783%. Setelah itu, propolis dalam berbagai konsentrasi ini dimasukan ke dalam sumur-sumur dalam media agar PYG yang telah disebar bakteri uji. Media dan contoh ini lalu diinkubasi dalam suhu 37ºC selama sekitar 24 jam. Konsentrasi terkecil yang menghasilkan zona bening ditetapkan sebagai KHTM.
Kemampuan propolis sebagai antibakteri kemudian dibandingkan dengan beberapa contoh lain. Contoh yang dimaksud adalah ampisilin 10 mg/mL sebagai kontrol positif
yang mempunyai kemampuan antibakteri dan air sebagai kontrol negatif yang tidak mempunyai kemampuan antibakteri. Pengujiannya sendiri dikerjakan menggunakan metode sumur. Pengerjaan metode sumur yang digunakan tidak jauh berbeda dengan pengerjaan sebelumnya untuk pencarian KHTM. Sebanyak 50 µL contoh dimasukan ke dalam sumur-sumur yang telah disediakan dalam media agar yang telah disebar bakteri uji. Perbandingan kemampuan antibakteri antarcontoh ditunjukkan dari zona bening yang dihasilkan masing-masing contoh tersebut.
HASIL DAN PEMBAHASAN
Rendemen Ekstrak Propolis
Ekstraksi propolis asal Bogor ini dilakukan dengan teknik maserasi, yaitu merendam propolis selama 2 minggu dalam pelarut etanol 70%. Teknik ini tepat digunakan untuk mengekstrak propolis karena tidak menggunakan suhu tinggi, mengingat propolis bersifat termostabil dengan titik didih 60-69oC (Woo 2004).
Etanol 70% digunakan sebagai pelarut karena dianggap mampu mengekstrak banyak senyawa aktif yang terdapat dalam propolis. Hal ini karena sifat etanol yang semipolar (nilai kepolaran 0,68), sehingga zat-zat yang terdapat dalam propolis yang memiliki nilai kepolaran yang beragam dapat terekstraksi dengan baik. Beberapa penelitian menunjukkan bahwa etanol 70% memberikan hasil terbaik terhadapi sifat antimikrob propolis (Woo 2004). Flavonoid merupakan senyawa aktif yang terbanyak dalam propolis (Chinthapally 1993 diacu dalam Anggraini 2007) terekstrak dengan baik menggunakan etanol 70% (Harborne 1987). selain itu, penggunaan etanol juga menghindari terlarutnya zat yang tidak diperlukan seperti lilin lebah. Lilin lebah yang terutama terdiri atas ester dari asam lemak dan alkohol dengan rantai karbon yang panjang tidak larut dalam etanol (Fearnley 2005). Titik didih etanol yang rendah, sehingga memudahkan dalam proses menguapkan (evaporasi) menjadi alasan lain penggunaan etanol ini.
endapan coklat dengan pereaksi Wagner. Pembanding yang digunakan adalah tapak dara berbunga putih.
Uji glikosida. Untuk menunjukkan adanya glikosida digunakan pereaksi Molisch. Sebanyak 2 mL ekstrak propolis dengan pengenceran 1:2 ditambah dengan 2-3 tetes asam sulfat pekat dan dibiarkan selama 3 menit lalu ditambah dengan pereaksi Molisch. Warna ungu kemerahan yang terbentuk menunjukkan adanya glikosida.
Uji gula pereduksi. Contoh propolis dengan pengenceran 1:2 dipanaskan sampai mendidih di dalam larutan 1 mL fehling A dan 1 mL Fehling B lalu didinginkan. Endapan merah bata menunjukkan adanya gula pereduksi.
Uji Aktivitas Antibakteri
Propolis yang diperoleh dari tahap sebelumnya digunakan dalam pengujian antibakteri. Bakteri yang digunakan adalah,
Bacillus subtilis, E. coli, Pseudomonas aeruginosa, Staphylococcus aureus. Sebelum dipakai, bakteri tersebut dikulturkan terlebih dahulu dalam media cair PYG selama sekitar 24 jam jam (media cair PYG mengandung 1% (b/v) pepton, 1% yeast extract, dan 2% glukosa dalam pelarut air).
Pengujian kemampuan antibakteri bakteri ini dimulai dengan uji pendahuluan menggunakan metode difusi sumur. Sebanyak 50µL dimasukkan ke dalam sumur yang telah dibuat sebelumnya pada media agar PYG yang telah diebar dengan bakteri uji. Media agar PYG mengandung 1% (b/v) pepton, 1% yeast extract, 2% glukosa, dan 2% agar bakto dalam pelarut air. Setelah itu, semua contoh diinkubasi di bawah suhu 37ºC selama sekitar 24 jam. Adanya zona bening menunjukan adanya aktivitas antibakteri.
Pengujian kemampuan antibakteri ini dilanjutkan dengan pencarian nilai konsentrasi hambat tumbuh minimum (KHTM). Metode sumur digunakan kembali untuk mencari nilai KHTM ini. Propolis 100% diencerkan menjadi beberapa konsentrasi yang lebih rendah sampai konsentrasi 0,783%. Setelah itu, propolis dalam berbagai konsentrasi ini dimasukan ke dalam sumur-sumur dalam media agar PYG yang telah disebar bakteri uji. Media dan contoh ini lalu diinkubasi dalam suhu 37ºC selama sekitar 24 jam. Konsentrasi terkecil yang menghasilkan zona bening ditetapkan sebagai KHTM.
Kemampuan propolis sebagai antibakteri kemudian dibandingkan dengan beberapa contoh lain. Contoh yang dimaksud adalah ampisilin 10 mg/mL sebagai kontrol positif
yang mempunyai kemampuan antibakteri dan air sebagai kontrol negatif yang tidak mempunyai kemampuan antibakteri. Pengujiannya sendiri dikerjakan menggunakan metode sumur. Pengerjaan metode sumur yang digunakan tidak jauh berbeda dengan pengerjaan sebelumnya untuk pencarian KHTM. Sebanyak 50 µL contoh dimasukan ke dalam sumur-sumur yang telah disediakan dalam media agar yang telah disebar bakteri uji. Perbandingan kemampuan antibakteri antarcontoh ditunjukkan dari zona bening yang dihasilkan masing-masing contoh tersebut.
HASIL DAN PEMBAHASAN
Rendemen Ekstrak Propolis
Ekstraksi propolis asal Bogor ini dilakukan dengan teknik maserasi, yaitu merendam propolis selama 2 minggu dalam pelarut etanol 70%. Teknik ini tepat digunakan untuk mengekstrak propolis karena tidak menggunakan suhu tinggi, mengingat propolis bersifat termostabil dengan titik didih 60-69oC (Woo 2004).
Etanol 70% digunakan sebagai pelarut karena dianggap mampu mengekstrak banyak senyawa aktif yang terdapat dalam propolis. Hal ini karena sifat etanol yang semipolar (nilai kepolaran 0,68), sehingga zat-zat yang terdapat dalam propolis yang memiliki nilai kepolaran yang beragam dapat terekstraksi dengan baik. Beberapa penelitian menunjukkan bahwa etanol 70% memberikan hasil terbaik terhadapi sifat antimikrob propolis (Woo 2004). Flavonoid merupakan senyawa aktif yang terbanyak dalam propolis (Chinthapally 1993 diacu dalam Anggraini 2007) terekstrak dengan baik menggunakan etanol 70% (Harborne 1987). selain itu, penggunaan etanol juga menghindari terlarutnya zat yang tidak diperlukan seperti lilin lebah. Lilin lebah yang terutama terdiri atas ester dari asam lemak dan alkohol dengan rantai karbon yang panjang tidak larut dalam etanol (Fearnley 2005). Titik didih etanol yang rendah, sehingga memudahkan dalam proses menguapkan (evaporasi) menjadi alasan lain penggunaan etanol ini.
dihasilkan pada penelitian ini berwarna coklat tua kehitaman.
Analisis Fitokimia
Komposisi kimiawi propolis sangat dipengaruhi oleh berbagai vegetasi pada lingkungan tempat hidup lebah (Bankova 2005). Hal ini dapat menjelaskan tentang beragamnya komposisi kimiawi propolis. Pengujian yang dapat digunakan untuk mengidentifikasi keberagaman senyawa-senyawa aktif dalam propolis secara kualitatif ini adalah analisis fitokimia.
Berdasarkan hasil analisis fitokimia, propolis contoh mengandung golongan senyawa flavonoid, steroid /triterpenoid, tanin, alkaloid, dan saponin (Tabel 1). Komposisi kimiawi seperti ini juga dilaporkan oleh Lasmayanti (2007) untuk propolis yang berasal dari daerah Banten. Anggraini (2006) melaporkan hal yang sama untuk propolis dari Banten kecuali dalam propolis tidak terdapat senyawa alkaloid. Tidak terdeteksinya senyawa alkaloid dapat disebabkan oleh perbedaan musim tempat pengoleksian propolis (Teixeira 2008), sehingga kandungan senyawa ini terlalu kecil untuk terdeteksi oleh uji fitokimia.
Tabel 1 Hasil analisis fitokimia ekstrak propolis
Senyawa Hasil uji fitokimia
Alkaloid +
Flavonoid +
Minyak Atsiri + Steroid/triterpenoid +
Saponin +
Tanin +
Ket: (+) = ada; (-) = tidak ada
Senyawa kimia dalam propolis yang berperan dalam aktivitas antibakteri, menurut Bankova (2005) adalah senyawa fenol flavonoid dan tanin. Selain menunjukkan aktivitas antibakteri, senyawa fenol ini menunjukkan aktivitas antiradang, dan antioksidan. Aktivitas antibakteri flavonoid secara umum disebabkan senyawa ini mempunyai kemampuan mengikat protein ekstraseluler dan protein integral yang bergabung dinding sel bakteri (Murphy 1999). Akibat mekanisme tersebut, per-meabilitas dinding sel terganggu sehingga dinding sel pecah karena tidak mampu menahan tekanan sitoplasma. Adapun senyawa tanin dalam ekstrak propolis, diduga memiliki sifat antimikrob karena kemampuannya dalam menginaktif protein enzim, dan lapisan protein transport (Murphy 1999). Sifat antibakteri dari senyawa tanin didukung dengan hasil
penelitian yang dilakukan oleh Rita (2006) (diacu dalam Lasmayanty 2007).
Uji Pendahuluan
Uji pendahuluan dimaksudkan untuk melihat aktivitas antibakteri propolis contoh secara umum. Hasill uji menunjukkan aktivitas yang hampir serupa antarbakteri Gram positif dan antarbakteri Gram negatif. Pengujian ini juga menunjukkan bahwa zona bening yang dihasilkan pada koloni Gram positif lebih besar dibandingkan pada bakteri Gram negatif (Tabel 2).
Tabel 2 Hasil uji pendahuluan terhadap propolis 50%
Jenis bakteri Zona bening (cm)
B. subtilis 2.37
S. aureus 2.44
E. coli 1.56
P. aeruginosa 1.43
Penentuan KHTM
Konsentrasi hambat tumbuh minimum atau KHTM merupakan konsentrasi terkecil suatu bahan zat yang masih menunjukkan aktivitas antibakteri. Penentuan nilai KHTM untuk setiap bakteri dilakukan menggunakan metode difusi sumur. Hal tersebut dilakukan dengan cara menguji propolis dari konsentrasi terbesar sampai dengan konsentrasi terkecil propolis pada kolini bakteri uji. Konsentrasi terkecil yang masih menunjukkan adanya zona bening ditentukan sebagai KHTM.
Berdasarkan hasil uji, diameter zona bening untuk semua jenis bakteri semakin berkurang dengan berkurangnya konsentrasi propolis yang digunakan. Sebagai pembanding digunakan air atau propolis dengan konsentrasi 0%. Zona bening tidak terlihat sama sekali pada konsentrasi ini. Zona bening yang dihasilkan pada koloni Bacillus subtilis
semakin mengecil dengan berkurangnya konsentrasi propolis yang digunakan, dan tidak menunjukkan zona bening lagi pada konsentrasi yang lebih kecil daripada 3.125% (Gambar 6). Hasil yang sama ditunjukkan pada koloni Staphylococcus aureus, yang memperlihatkan konsentrasi terakhir yang masih menghasilkan zona bening adalah pada 1.563%(Gambar 7). Penurunan diameter zona bening juga terjadi pada koloni E. coli dan
Rendahnya aktivitas antibakteri propolis terhadap bakteri Gram negatif juga dikonfirmasi oleh Muli (2007), El Fadaly, dan El badrawy (2001). Walaupun demikian, hasil yang berbeda diperoleh Fuentes dan Hernandez (1990) seperti yang dilaporkan oleh Marcucci (1995). Fuentes dan Hernandez melaporkan adanya aktivitas antibakteri terhadap sejumlah bakeri, antara lain Bacillus subtilis, E. coli, Staphylococcus aureus, Pseudomonas aeruginosa. Perbedaan aktivitas ini disinyalir oleh Bankova (2005) berhubungan erat dengan fungsi propolis dalam menjaga kondisi steril lingkungan dalam sarang terhadap lingkungan biotik di luar sarang. Perbedaan tempat hidup memberikan tantangan kondisi biotik yang berbeda untuk setiap tempat. Oleh karena itu, maka jenis atau fungsi antibiotik yang terdapat dalam propolis dapat berbeda satu sama lain. Walaupun demikian, ketersediaan bahan-bahan tersebut juga dipengaruhi oleh jenis vegetasi yang terdapat dalam lingkungan tempat hidup lebah.
Gambar 6 Zona bening pada koloni Bacillus subtilis karena pengaruh pemberian propolis pada berbagai konsentrasi (1 = 25%; 2 = 12.5 %; 3 = 6.25 %; 4 = 3.125 %; 5 = 1.563%).
Gambar 7 Zona bening pada koloni
Staphylococcus aureus karena pengaruh pemberian propolis pada berbagai konsentrasi (1 = 25%; 2 = 12.5 %; 3 = 6.25 %; 4 = 3.125 %; 5 = 1.563%).
Gambar 8 Zona bening pada koloni E. coli
karena pengaruh pemberian propolis pada berbagai konsentrasi (1 = 25%; 2 = 12.5 %; 3 = 6.25 %; 4 = 3.125 %).
Gambar 9 Zona bening pada koloni
Pseudomonas aeruginosa karena pengaruh pemberian propolis pada berbagai konsentrasi (1 = 25%; 2 = 12.5 %; 3 = 6.25 %; 4 = 3.125 %).
Tabel 3 Konsentrasi hambat tumbuh minimum (KHTM) untuk keempat bakteri uji
Bakteri KHTM
Bacillus subtilis 1.563%
Staphylococcus aureus 1.563%
Pseudomonas aeruginosa 3.125%
E. coli 3.125%
Efektifitas Propolis Terhadap Ampisilin
Ampisilin telah terbukti memiliki aktivitas antibakteri dalam spektrum yang luas, yaitu dapat menghambat bakteri Gram positif maupun Gram negatif (Siswandono & Soekardjo 1995). Oleh karena itu, ampisilin digunakan sebagai kontrol positif. Walaupun demikian aktivitas antibakteri ampisilin terhadap setiap bakteri tidaklah sama. Aktivitas terhadap E. coli cukup berbeda nyata, yaitu lebih kecil jika dibandingkan terhadap bakteri lainnya (Tabel 4).
0 200 400 600 800 1000 1200
1 2 3 4 5
D ian m e te r zo n a b e n in g (µ m ) 0 500 1000 1500 2000
1 2 3 4 5
D ian m e te r zo n a b e n in g (µ m ) 0 200 400 600 800 1000 1200
1 2 3 4
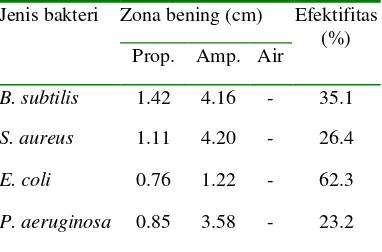
Tabel 4 Efektivitas propolis pada KHTM terhadap ampisilin (Amp) 10 mg/mL Jenis bakteri Zona bening (cm) Efektifitas
(%) Prop. Amp. Air
B. subtilis 1.42 4.16 - 35.1
S. aureus 1.11 4.20 - 26.4
E. coli 0.76 1.22 - 62.3
P. aeruginosa 0.85 3.58 - 23.2
Ket: Propolis yang digunakan diekstrak pada waktu yang berbeda dengan propolis yang digunakan pada uji pendahuluan Prop. = konsentrasi propolis pada KHTM Amp = ampisilin 10 mg/mL
Efektivitas propolis terhadap ampisilin untuk bakteri Bacillus subtilis, Staphylococcus aureus, E .coli, Pseudomonas aeruginosa, masing-masing sebesar 35.11%, 26.43%, 62.30%, 23.22%. Walaupun efek-tivitas propolis terhadap ampisilin paling besar, nilai ini tidak cukup menunjang untuk menyatakan bahwa propolis memiliki potensi paling baik pada E. coli, karena kecilnya aktivitas antibakteri ampisilin dalam terhadap
E. coli. Perbandingan efektivitas propolis terhadap ampisilin untuk bakteri yang lain menunjukkan bahwa efektivitas pada Bacillus subtilis paling baik dibandingkan terhadap
Staphylococcus aureus, Pseudomonas aeruginosa.
SIMPULAN DAN SARAN
Simpulan
Rendemen ekstrak propolis etanol 70% yang dihasilkan sebesar 10.344%. Ekstrak ini, terutama, dapat menghambat pertumbuhan bakteri Gram positif Bacillus subtilis dan
Staphylococcus aureus dengan Konsentrasi Hambat Tumbuh Minimum (KHTM) sebesar 1.563%. Ekstrak ini juga dapat menghambat pertumbuhan Gram negatif E. coli dan
Pseudomonas aeruginosa dalam skala yang lebih kecil, dengan nilai KHTM sebesar 3.125%.
Saran
Perlu dilakukan penelitian yang berkelanjutan untuk mengeksplorasi potensi antibakteri propolis yang berasal dari berbagai tempat, terutama di Indonesia. Lebih dari itu, perlu terus dikaji pemanfaatan propolis menjadi produk-produk yang lebih aplikatif.
DAFTAR PUSTAKA
Angraini AD. 2006. Potensi propolis lebah madu Trigona spp sebagai bahan antibakteri [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Bankova V. 2005. Recent trends and important developments in propolis research. eCAM 2: 29–32.
Banksota AH et al. Cytotoxic, hepato-protective and free radical scavenging effects of propolis from Brazil, Peru, the Netherlands and China. J Ethnopharmacol 72: 239–46.
Brisbane Insects. 2010. http://www.brisbane insects.com/brisbane_wasps/html. [3 Desember 2010]
El Fadaly H & El Badrawi EEY. 2001. Flavonoids of propolis and their antibacterial activities. Pakistan Journal 4: 204-207.
Free J. 2001. Bee and Mindkind. London: George Allen & Unkwin.
Fardiaz S. 1983. Mikrobiologi keamanan Pangan. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Gojmerac WL. 1983. Bee, Beekeeping, Honey ada Polination. Westport: Avi.
Harborne HB. 1987. Metode Fitokimia I. Ed ke-2. Padwadinata K, penerjemah. Bandung. ITB. Terjemahan dari: Phytochemical Method.
Hegazi AG & El Hady FKA. 2001. Antimicrobial Activities and Chemical composition and antimicrobial activity of European propolis. Z. Naturforsch 57c: 395-402.
Holt JG et al. 1994. Begey Manual of Determinative Biology. Ed ke-9. Baltimore: Williams & Wilkins.
Katircioglu H & Mercan N. 2006. Antimicrobial activity and chemical compositions of Turkish propolis from different region. African Journal of Biotechnology 5: 1151-1153.
Khismatullina N. 2005. Apitherapy. Moskwa: Mobile Ltd.
Tabel 4 Efektivitas propolis pada KHTM terhadap ampisilin (Amp) 10 mg/mL Jenis bakteri Zona bening (cm) Efektifitas
(%) Prop. Amp. Air
B. subtilis 1.42 4.16 - 35.1
S. aureus 1.11 4.20 - 26.4
E. coli 0.76 1.22 - 62.3
P. aeruginosa 0.85 3.58 - 23.2
Ket: Propolis yang digunakan diekstrak pada waktu yang berbeda dengan propolis yang digunakan pada uji pendahuluan Prop. = konsentrasi propolis pada KHTM Amp = ampisilin 10 mg/mL
Efektivitas propolis terhadap ampisilin untuk bakteri Bacillus subtilis, Staphylococcus aureus, E .coli, Pseudomonas aeruginosa, masing-masing sebesar 35.11%, 26.43%, 62.30%, 23.22%. Walaupun efek-tivitas propolis terhadap ampisilin paling besar, nilai ini tidak cukup menunjang untuk menyatakan bahwa propolis memiliki potensi paling baik pada E. coli, karena kecilnya aktivitas antibakteri ampisilin dalam terhadap
E. coli. Perbandingan efektivitas propolis terhadap ampisilin untuk bakteri yang lain menunjukkan bahwa efektivitas pada Bacillus subtilis paling baik dibandingkan terhadap
Staphylococcus aureus, Pseudomonas aeruginosa.
SIMPULAN DAN SARAN
Simpulan
Rendemen ekstrak propolis etanol 70% yang dihasilkan sebesar 10.344%. Ekstrak ini, terutama, dapat menghambat pertumbuhan bakteri Gram positif Bacillus subtilis dan
Staphylococcus aureus dengan Konsentrasi Hambat Tumbuh Minimum (KHTM) sebesar 1.563%. Ekstrak ini juga dapat menghambat pertumbuhan Gram negatif E. coli dan
Pseudomonas aeruginosa dalam skala yang lebih kecil, dengan nilai KHTM sebesar 3.125%.
Saran
Perlu dilakukan penelitian yang berkelanjutan untuk mengeksplorasi potensi antibakteri propolis yang berasal dari berbagai tempat, terutama di Indonesia. Lebih dari itu, perlu terus dikaji pemanfaatan propolis menjadi produk-produk yang lebih aplikatif.
DAFTAR PUSTAKA
Angraini AD. 2006. Potensi propolis lebah madu Trigona spp sebagai bahan antibakteri [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Bankova V. 2005. Recent trends and important developments in propolis research. eCAM 2: 29–32.
Banksota AH et al. Cytotoxic, hepato-protective and free radical scavenging effects of propolis from Brazil, Peru, the Netherlands and China. J Ethnopharmacol 72: 239–46.
Brisbane Insects. 2010. http://www.brisbane insects.com/brisbane_wasps/html. [3 Desember 2010]
El Fadaly H & El Badrawi EEY. 2001. Flavonoids of propolis and their antibacterial activities. Pakistan Journal 4: 204-207.
Free J. 2001. Bee and Mindkind. London: George Allen & Unkwin.
Fardiaz S. 1983. Mikrobiologi keamanan Pangan. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Gojmerac WL. 1983. Bee, Beekeeping, Honey ada Polination. Westport: Avi.
Harborne HB. 1987. Metode Fitokimia I. Ed ke-2. Padwadinata K, penerjemah. Bandung. ITB. Terjemahan dari: Phytochemical Method.
Hegazi AG & El Hady FKA. 2001. Antimicrobial Activities and Chemical composition and antimicrobial activity of European propolis. Z. Naturforsch 57c: 395-402.
Holt JG et al. 1994. Begey Manual of Determinative Biology. Ed ke-9. Baltimore: Williams & Wilkins.
Katircioglu H & Mercan N. 2006. Antimicrobial activity and chemical compositions of Turkish propolis from different region. African Journal of Biotechnology 5: 1151-1153.
Khismatullina N. 2005. Apitherapy. Moskwa: Mobile Ltd.
POTENSI ANTIBAKTERI PROPOLIS LEBAH
Trigona
spp
ASAL BOGOR
ADE JAMALUDIN SUNNY
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Tabel 4 Efektivitas propolis pada KHTM terhadap ampisilin (Amp) 10 mg/mL Jenis bakteri Zona bening (cm) Efektifitas
(%) Prop. Amp. Air
B. subtilis 1.42 4.16 - 35.1
S. aureus 1.11 4.20 - 26.4
E. coli 0.76 1.22 - 62.3
P. aeruginosa 0.85 3.58 - 23.2
Ket: Propolis yang digunakan diekstrak pada waktu yang berbeda dengan propolis yang digunakan pada uji pendahuluan Prop. = konsentrasi propolis pada KHTM Amp = ampisilin 10 mg/mL
Efektivitas propolis terhadap ampisilin untuk bakteri Bacillus subtilis, Staphylococcus aureus, E .coli, Pseudomonas aeruginosa, masing-masing sebesar 35.11%, 26.43%, 62.30%, 23.22%. Walaupun efek-tivitas propolis terhadap ampisilin paling besar, nilai ini tidak cukup menunjang untuk menyatakan bahwa propolis memiliki potensi paling baik pada E. coli, karena kecilnya aktivitas antibakteri ampisilin dalam terhadap
E. coli. Perbandingan efektivitas propolis terhadap ampisilin untuk bakteri yang lain menunjukkan bahwa efektivitas pada Bacillus subtilis paling baik dibandingkan terhadap
Staphylococcus aureus, Pseudomonas aeruginosa.
SIMPULAN DAN SARAN
Simpulan
Rendemen ekstrak propolis etanol 70% yang dihasilkan sebesar 10.344%. Ekstrak ini, terutama, dapat menghambat pertumbuhan bakteri Gram positif Bacillus subtilis dan
Staphylococcus aureus dengan Konsentrasi Hambat Tumbuh Minimum (KHTM) sebesar 1.563%. Ekstrak ini juga dapat menghambat pertumbuhan Gram negatif E. coli dan
Pseudomonas aeruginosa dalam skala yang lebih kecil, dengan nilai KHTM sebesar 3.125%.
Saran
Perlu dilakukan penelitian yang berkelanjutan untuk mengeksplorasi potensi antibakteri propolis yang berasal dari berbagai tempat, terutama di Indonesia. Lebih dari itu, perlu terus dikaji pemanfaatan propolis menjadi produk-produk yang lebih aplikatif.
DAFTAR PUSTAKA
Angraini AD. 2006. Potensi propolis lebah madu Trigona spp sebagai bahan antibakteri [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Bankova V. 2005. Recent trends and important developments in propolis research. eCAM 2: 29–32.
Banksota AH et al. Cytotoxic, hepato-protective and free radical scavenging effects of propolis from Brazil, Peru, the Netherlands and China. J Ethnopharmacol 72: 239–46.
Brisbane Insects. 2010. http://www.brisbane insects.com/brisbane_wasps/html. [3 Desember 2010]
El Fadaly H & El Badrawi EEY. 2001. Flavonoids of propolis and their antibacterial activities. Pakistan Journal 4: 204-207.
Free J. 2001. Bee and Mindkind. London: George Allen & Unkwin.
Fardiaz S. 1983. Mikrobiologi keamanan Pangan. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Gojmerac WL. 1983. Bee, Beekeeping, Honey ada Polination. Westport: Avi.
Harborne HB. 1987. Metode Fitokimia I. Ed ke-2. Padwadinata K, penerjemah. Bandung. ITB. Terjemahan dari: Phytochemical Method.
Hegazi AG & El Hady FKA. 2001. Antimicrobial Activities and Chemical composition and antimicrobial activity of European propolis. Z. Naturforsch 57c: 395-402.
Holt JG et al. 1994. Begey Manual of Determinative Biology. Ed ke-9. Baltimore: Williams & Wilkins.
Katircioglu H & Mercan N. 2006. Antimicrobial activity and chemical compositions of Turkish propolis from different region. African Journal of Biotechnology 5: 1151-1153.
Khismatullina N. 2005. Apitherapy. Moskwa: Mobile Ltd.
propolis provenance. Planta Med. 60: 222-227.
Koolman J et al. 1997. Priciples of Microbiology. Ed ke-2. Wanandi SI, penerjemah. Lowa: WNC Brown.
Lay W & Hastowo S. 1992. Mikrobiologi. Jakarta: Rajawali.
Lasmayanty M. 2007. Potensi antibakteri propolis lebah madu Trigona spp terhadap bakteri kariogenik (Streptococcus mutans) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Marcucci MC. 1995. Propolis: chemical composition, biological properties and therapeutic activity. Apidologie 26: 83-99.
Mantienzo AC, Lamorena. 2004. Extraction And initial characterization of Propolis from stingless Bees (Trigona Biro Fries). Di dalam
Proceeding ot7th Asian Apicultural Association Conference and10th BEENET Symposium And Technofora Los Banos, 23-27 Februari 2004. Los Banos: Univ Philippines. Hlm: 321-329.
Muli EM et al. 2007. Antimicrobial Properties of Propolis and Honey from the Kenyan Stingless bee, Dactylurina schimidti. Apiacta 43: 46-61.
Murphy MC. 1999. Plant Products as Antimicrobial Agents. Clin Microbiol Rev. 12: 564–582l.
Nelli. 2004. Waktu pencarian serbuk ari lebah pekerja Trigona (Apidae: Hymenoptera) [skripsi]. Bogor: Program Studi Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam.
Pelczar MJ dan Chan ECS. 1988. Dasar-Dasar Mikrobiologi. Hadioetomo RS et al., penerjemah. Jakarta: UI Pr Terjemahan dari: Element of Microbiology.
Pemerintah Kota Bogor. 2010. http://www. kotabogor.go.id/main. [15 Maret 2010].
Perum Perhutani Unit Jawa Timur. 1986. Peningkatan kesejahteraan masyarakat melalui pelebahan. Di dalam:
Pembudidayaan Lebah Madu untuk Peningkatan Kesejahteraan Masyarakat. Prosiding Lokakarya; Sukabumi 20-22 Mei 1986. Jakarta: Perum Perhutani.hlm 293-302.
Popova M et al. 2000.Comparative study of the biological activity of propolis from different geographic origin: a statistical approach. Macedonian Pharm Bull 50: 9-14.
Suwanda O. 1986. Pengolahan produksi lebah madu dan pemasarannya. Di dalam:
Pembudidayaan Lebah Madu untuk peningkatan Kesejahteraan masyarakat. Prosiding Lokakarya; Sukabumi, 20-22 Mei 1986. Jakarta: Perum perhutani. Hlm 173-180.
Sihombing DTH. 1997. Ilmu Ternak Lebah Madu. Yogyakarta: Gajah Mada Univ Pr.
Siswandono & B. Soekardjo. 1995. Kimia Medisinal. Surabaya: Airlangga University Press.
Teixeira WE et al. 2008. Seasonal Variation, Chemical Composition and Antioxidant activity of Brazilian Propolis Samples. eCAM: 1-9.
Stirm S & Molbert EF. 1970. Escherichia coli
capsule bacteriophages. Journal of Virology: 330-342
Todar K. 2008. http:// www.textbookof bacteriology.net/ staph.html. [11 Juni 2010]
WHO. 2008. Campylobacter. http://www. who.int/en/ campylobacter.html. [21 Juli 2008].
Woo KS. 2004. Use of bee venom and propolis for apitherapy in Korea. Di dalam:
Proceeding of the 7th Asian Agricultural Association Conference and 10th BEENET Symposium technofora: Los Banos, 23-27 Feb 2004. Los banos: Univ Philiphines. Hlm 31-315.
Yang HY et al. 2007. Antibacterial Activity of Propolis Ethanol Extract Against
Lampiran 1 Tahapan penelitian
Lampiran 2 Tahapan ekstraksi propolis
Ekstraksi Propolis
Sterilisasi alat dan
bahan
Peremajaan
biakan
Uji akivitas antibakteri
Maserasi dengan
pelarut etanol 70%
selama 7 hari
Filtrat
Endapan
Sarang
Trigona spp
Propolis
Maserasi kembali
selama 7 hari, filtran
diambil setiap hari
Pemekatan
dengan
rotavapor
Ekstrak pekat
+ PG 1 x volume
ekstrak
Propolis
Lampiran 3 Data zona bening hasil uji aktivitas antibakteri ekstrak propolis pada
berbagai konsentrasi (A= 25%; B = 12.5 %; C = 6.25 %; D = 3.125 %; E = 1.563%)
Jenis bakteri
Ulangan
Zona bening (µm)
A
B
C
D
E
Bacillus subtilis
1
1440
1160
924
863
675
2
830
550
318
253
65
Rata-rata
985
855
621
558
370
Staphylococcus aureus
1
1800
1745
1210
1130
910
2
1190
1135
600
520
300
Rata-rata
1495
1440
905
825
610
E. coli
1
960
742
435
417
-
2
1100
640
652
420
-
Rata-rata
1030
691
543.5
418.5
Pseudomonas aeruginosa
1
872
780
563
494
-
2
986
820
600
458
-
Rata-rata
929
800
581.5
476
Lampiran 4 Efektivitas propolis terhadap ampisilin
Jenis bakteri
Zona bening
Efektivitas
(%)
PropolisKHTM
Amp
Air
Bacillus subtilis
1.45
4.13
-
1.38
4.19
-
Rata-rata
1.42
4.16
35.11
Staphylococcus aureus
1.21
4.19
-
0.99
4.22
-
Rata-rata
1.11
4.20
26.43
E.coli
0.83
1.15
-
0.69
1.28
-
Rata-rata
0.76
1.22
62.30
Pseudomonas
aeruginosa
0.76
3.49
-
0.93
3.66
-
Rata-rata
0.85
3.58
23.22
Perhitungan:
Efektifitas ekstrak propolis terhadap ampisilin untuk Bacillus subtilis
=
100
%
Ampisilin
diameter
propolis
ekstrak
diameter
=
100
%
16
.
4
42
.
1
cm
cm
Efektifitas ekstrak propolis terhadap ampisilin untuk Staphylococcus aureus
=
100
%
Ampisilin
diameter
propolis
ekstrak
diameter
=
100
%
22
..
4
99
.
0
mm
cm
= 26.43%
Efektifitas ekstrak propolis terhadap ampisilin untuk E. coli
=
100
%
Ampisilin
diameter
propolis
ekstrak
diameter
=
100
%
22
.
1
79
.
0
cm
cm
= 62.30%
Efektifitas ekstrak propolis terhadap ampisilin untuk Pseudomonas aeruginosa
=
100
%
Ampisilin
diameter
propolis
ekstrak
diameter
=
100
%
58
.
3
85
.
0
cm
cm
Lampiran 5 Uji Fitokimia
Tanin
Alkaloid
Dragendrof
Meyer wegner
P100%
P100%
Flavonoid
Triterpenoid/steroid
POTENSI ANTIBAKTERI PROPOLIS LEBAH
Trigona
spp
ASAL BOGOR
ADE JAMALUDIN SUNNY
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
POTENSI ANTIBAKTERI PROPOLIS LEBAH
Trigona
spp
ASAL BOGOR
ADE JAMALUDIN SUNNY
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada Departemen Biokimia
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
ADE JAMALUDIN SUNNY. Potensi Antibakteri Propolis
Trigona
spp asal
Bogor. Dibimbing oleh A.E. ZAINAL HASAN dan I MADE ARTIKA.
Propolis merupakan resin yang dikumpulkan lebah madu dari berbagai bagian
tumbuhan. Penelitian terhadap contoh propolis dari berbagai tempat menunjukan
keanekaragaman dalam komposisi kimiawinya. Komposisi kimiawi propolis ini
bergantung kepada jenis flora yang terdapat pada tempat pengambilannya. Hal ini
memberikan kemungkinan adanya perbedaan aktivitas antibakteri dari
masing-masing contoh.
ABSTRACT
ADE JAMALUDIN SUNNY. Potency of Bogor
Trigona spp Propolis as an
Antibacterial Subtance. Under direction A.E. ZAINAL HASAN and I MADE
ARTIKA.
Propolis contains resinous substances collected by honey bees from various
plant sources. Analysis of numerous samples from different geographic regions
led to the disclosure that the chemical composition of propolis is highly variable
depends on the specificity of the local flora at the site of collection and thus on the
geographic and climatic characteristics of this site. This fact results in the striking
diversity of propolis chemical composition, especially of propolis originating
from tropical regions.
Judul Skripsi : Potensi Antibakteri Propolis Lebah Trigona spp Asal Bogor
Nama
: Ade Jamaludin Sunny
NIM
: G44103052
Disetujui
Komisi Pembimbing
Ir. A.E. Zainal Hasan, M.Si
Ketua
Dr. I Made Artika, M. App.Sc
Anggota
Diketahui
Dr. I Made Artika, M. App.Sc
Ketua Departemen Biokimia
RIWAYAT HIDUP
Penulis dilahirkan di Garut pada tanggal 5 Juli 1985 sebagai anak keenam dari
tujuh bersaudara dari Ayah Tiktik Syamsudin dan Ibu Hayati. Tahun 2003 penulis
lulus dari SMU Negeri 1 Tarogong dan pada tahun yang sama lulus seleksi masuk
Institut Pertanian Bogor (IPB) melalui jalur Seleksi Penerimaan Mahasiswa Baru
(SPMB) pada Program Studi Biokimia, Fakultas Matematika dan Ilmu
Pengetahuan Alam.
PRAKATA
Alhamdulillah. Puji syukur penulis panjatkan kehadirat Allah SWT atas
izin-Nya sehingga penulis dapat menyelesaikan karya ilmiah yang berjudul
Potensi Antibakteri Propolis Lebah
Trigona spp Asal Bogor. Karya ilmiah ini
disusun berdasarkan hasil penelitian yang dilaksanakan di Laboratorium biokimia
IPB sebagai salah satu syarat untuk memperoleh gelar sarjana sains pada program
studi Biokimia FMIPA, IPB.
Terima kasih penulis ucapkan kepada Ir. A.E. Zainal Hasan, M.Si, dan Dr.
I Made Artika, M. App.Sc selaku pembimbing, atas semua arahan dan
bimbingannya. Terima kasih juga penulis sampaikan kepada para staf dan laboran
Biokimia atas semua bantuannya. Tak lupa pula terima kasih kepada Ibu, Ayah,
kakak-kakak, adik, dan teman-teman Biokimia atas semua bantuan dan dukungan,
baik berupa materi dan motivasi, dan doanya.
Akhir kata, semoga karya ilmiah ini dapat memberi manfaat kepada yang
membacanya.
Bogor, Januari 2011
DAFTAR ISI
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... ix
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Lebah Madu Trigona spp ... 1
Propolis ... 1
Kondisi Geografis Asal Propolis ... 2
Bakteri Uji ... 3
Antibakteri ... 4
BAHAN DAN METODE
Bahan dan Alat ... 5
Metode Penelitian ... 5
HASIL DAN PEMBAHASAN
Rendemen Ekstrak Propolis ... 6
Analisis Fitokimia ... 6
Uji Pendahuluan ... 7
Penentuan KHTM ... 7
Efektifitas Pr