LAPORAN PENELITIAN
Dana Masyarakat Lembaga Peneliian USU
Bio- nanokomposite Sellulosa Bakteri/Mater-Bi
®Saharman Gea, PhD
Dibiyai oleh:
Dana Masyarakat Peneliian USU T.A. 2011 Sesuai Surat Perjanjian Penugasan Peneliian
No: 36/UN5.2.3.1/SP4/PPM/2011, Tanggal 01 Agustus 2011
S SUMATERA UTARA
MED
PEMBUATAN DAN KARAKTERISASI SELULOSA
MIKROKRISTAL DAN NANOKRISTAL TANDAN AREN
(
Arenga pinnata
(Wurmb) Merr.) DAN PENGGUNAANNYA
SEBAGAI EKSIPIEN DALAM TABLET
NATRIUM DIKLOFENAK
DISERTASI
PEMBUATAN DAN KARAKTERISASI SELULOSA
MIKROKRISTAL DAN NANOKRISTAL TANDAN AREN
(
Arenga pinnata
(Wurmb) Merr.) DAN PENGGUNAANNYA
SEBAGAI EKSIPIEN DALAM TABLET
NATRIUM DIKLOFENAK
DISERTASI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Doktor dalam Ilmu Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
di bawah pimpinan Rektor Universitas Sumatera Utara Prof. Dr. dr. Syahril Pasaribu, DTM&H., M.Sc. (CTM), Sp.A.(K)
untuk dipertahankan di hadapan Sidang Ujian Terbuka
Program Studi Doktor (S-3) Ilmu Farmasi Universitas Sumatera Utara
PROMOTOR
Prof. Dr. Basuki Wirjosentono, M.Sc.
Guru Besar Ilmu Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Medan
KO-PROMOTOR
Prof. Dr. Karsono, Apt.
Guru Besar Ilmu Farmasi
Fakultas Farmasi Universitas Sumatera Utara Medan
KO-PROMOTOR
Dr. M. Pandapotan Nasution, MPS., Apt.
Staf Pengajar Ilmu Farmasi
PERSETUJUAN DISERTASI
Nama Mahasiswa : Sumaiyah
No. Induk Mahasiswa : 098116004
Judul Disertasi : Pembuatan dan Karakterisasi Selulosa Mikrokristal dan Nanokristal Tandan Aren (Arenga pinnata (Wurmb) Merr.) dan Penggunaannya sebagai Eksipien dalam Tablet Natrium Diklofenak
Tempat dan Tanggal Ujian Lisan Disertasi: Medan, 27Februari 2014
Menyetujui:
Komisi Pembimbing,
Prof. Dr. Basuki Wirjosentono, M.Sc. Promotor
Prof. Dr. Karsono, Apt. Dr. M. Pandapotan Nasution, MPS., Apt. Ko Promotor Ko Promotor
Ketua Program Studi, Dekan,
Telah diuji pada Ujian Tertutup
Tanggal 27 Februari 2014
TIM PENGUJI DISERTASI
Ketua : Prof. Dr. Basuki Wirjosentono, M.Sc.
Anggota : Prof. Dr. Karsono, Apt.
Dr. M. Pandapotan Nasution, MPS., Apt.
Prof. Dr. Urip Harahap, Apt.
Prof. Dr. Jansen Silalahi, M.App.Sc., Apt.
Prof. Dr. Elfi Sahlan Ben, Apt.
PENGESAHAN DISERTASI
Nama Mahasiswa : Sumaiyah
No. Induk Mahasiswa : 098116004
Judul Disertasi : Pembuatan dan Karakterisasi Selulosa Mikrokristal dan Nanokristal Tandan Aren (Arenga pinnata (Wurmb) Merr.) dan Penggunaannya sebagai Eksipien dalam Tablet Natrium Diklofenak
Telah diuji dan dinyatakan LULUS di depan Tim Penguji pada hari Kamis tanggal dua puluh tujuh Februari tahun dua ribu empat belas
Tim Penguji Disertasi
Ketua Tim Penguji, Anggota Tim Penguji,
Prof. Dr. Basuki Wirjosentono, M.Sc. Prof. Dr. Karsono, Apt.
Dr. M.Pandapotan Nasution, MPS., Apt.
Prof. Dr. Urip Harahap, Apt.
Prof. Dr. Jansen Silalahi, M.App.Sc., Apt.
Prof. Dr. Elfi Sahlan Ben, Apt.
PERNYATAAN PERSETUJUAN PUBLIKASI ILMIAH UNTUK KEPENTINGAN AKADEMIS
Sebagai sivitas akademik Universitas Sumatera Utara, saya yang bertanda tangan
di bawah ini:
Nama : Sumaiyah
NIM : 098116004
Program Studi : Ilmu Farmasi
Jenis Karya : Disertasi
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada
Universitas Sumatera Utara Hak Bebas Royalti Non Eksklusif (Non-exclusive
Royalty Free Right) atas disertasi saya yang berjudul:
PEMBUATAN DAN KARAKTERISASI SELULOSA MIKROKRISTAL DAN NANOKRISTAL TANDAN AREN (Arenga pinnata (Wurmb) Merr.)
DAN PENGGUNAANNYA SEBAGAI EKSIPIEN DALAM TABLET NATRIUM DIKLOFENAK
Beserta perangkat yang ada (jika diperlukan), dengan Hak Bebas Royalti Non
Eksklusif ini Universitas Sumatera Utara berhak menyimpan dalam bentuk
database, merawat, dan mempublikasikan disertasi saya tanpa meminta izin dari
saya sebagai penulis dan sebagai pemilik hak cipta.
Demikian pernyataan ini saya perbuat dengan sebenarnya.
Dibuat di Medan
Pada tanggal April 2014
Yang menyatakan,
PERNYATAAN ORISINALITAS
Saya yang bertanda tangan di bawah ini:
Nama : Sumaiyah
Nomor Induk Mahasiswa : 098116004
Program Studi : Doktor Ilmu Farmasi
Judul Disertasi : Pembuatan dan Karakterisasi Selulosa Mikrokristal
dan Nanokristal dari Tandan Aren (Arenga
pinnata (Wurmb)Merr.) dan Penggunaannya
sebagai Eksipien dalam Tablet Natrium
Diklofenak
Dengan ini saya menyatakan bahwa disertasi yang saya buat adalah asli karya
saya sendiri, bukan plagiat, dan apabila di kemudian hari diketahui disertasi saya
tersebut plagiat karena kesalahan saya sendiri, maka saya bersedia diberi sanksi
apapun oleh Program Studi Doktor Ilmu Farmasi Fakultas Farmasi USU. Saya
tidak akan menuntut pihak manapun atas perbuatan saya tersebut.
Demikian surat pernyataan ini saya perbuat dengan sebenarnya dan dalam
keadaan sehat.
Medan, April 2014 Yang membuat pernyataan,
ABSTRAK
Selulosa adalah polisakarida yang berperan sebagai jaringan penopang pada tanaman termasuk tandan aren dan dapat diisolasi dan dibuat menjadi kristal. Selulosa mikrokristal merupakan eksipien yang paling sering digunakan dalam pembuatan tablet dengan metode cetak langsung. Selulosa mikrokristal selama ini masih diimpor sehingga harga sediaan farmasi menjadi mahal. Karena itu perlu diupayakan untuk menemukan bahan tambahan alternatif dari sumber yang lebih ekonomis. Untuk meningkatkan luas permukaan dan kristalinitas selulosa mikrokristal, maka dibuat selulosa nanokristal. Tujuan penelitian ini adalah untuk membuat, mengkarakterisasi selulosa mikrokristal dan nanokristal yang diperoleh dari tandan aren (Arenga pinnata (Wurmb) Merr.), dan menggunakannya sebagai eksipien pada tablet natrium diklofenak. Kemudian karakteristik fisik dan pengaruhnya pada sifat tablet dan pelepasan obat dari tablet cetak langsung dibandingkan dengan eksipien komersial (Avicel®).
Pada penelitian ini tandan buah aren digunakan sebagai sumber selulosa. Selulosa mikrokristal dibuat dari α-selulosa tandan aren melalui proses hidrolisis dengan asam klorida 2,5 N. Selulosa mikrokristal tandan aren (SMTA) yang diperoleh ditentukan sifat fisiknya menurut standar United State Pharmacopeia
32-National Formulary 27 (USP 32-NF 27). Selain itu ditentukan juga rendemen dari bahan awal, gugus fungsi, morfologi, struktur kristal, derajat kristalinitas, sifat alir, kapasitas pengembangan, hidrasi, serap lembab, dan toksisitas akut dari SMTA. Selulosa nanokristal dibuat dari α-selulosa tandan aren dengan cara hidrolisis dengan asam sulfat 54% dan dihomogenkan dengan pengaduk magnet selama 45 menit. Untuk menghilangkan sisa asam, suspensi disentrifugasi pada 10.000 rpm selama 15 menit. Endapan didialisis selama 48 jam dengan membran dialisis yang telah diaktivasi. Selulosa nanokristal tandan aren (SNTA) yang diperoleh dikarakterisasi gugus fungsi, morfologi, struktur selulosa,derajat kristalinitas, degradasi termal, sifat alir, dan kompresibilitas. Tablet dibuat dalam 7 formula (F1-F7) dengan menggunakan natrium diklofenak sebagai model obat. Evaluasi tablet, uji pelepasan obat, dan kinetika pelepasan obat dari tablet natrium diklofenak yang diformulasi dengan selulosa nanokristal dibandingkan terhadap tablet yang diformulasi dengan selulosa mikrokristal dan Avicel PH 102®, serta
tablet Voltaren® yang sudah beredar di pasaran dalam medium pH 6,8 dan pH
berganti.
Hasil penelitian menunjukkan bahwa rendemen SMTA dari tandan aren adalah 16-21,33% b/b. SMTA memiliki karakteristik fisik dengan bentuk yang tidak beraturan, permukaan yang tidak rata, dan memenuhi persyaratan USP 32-NF 27. Hasil uji fourier transform infra red (FTIR) menunjukkan spektrum yang sama dengan Avicel PH 102®. Ukuran partikel SMTA lebih besar dibandingkan
dengan Avicel PH 102®. Struktur kristal SMTA adalah selulosa II sedangkan
Avicel PH 102® adalah selulosa I. Sifat alir, kapasitas pengembangan, hidrasi, dan
serap lembab dari SMTA tidak berbeda signifikan dengan Avicel PH 102®. Uji
sferis dengan diameter 15-20 nm dan distribusi ukuran partikel berkisar 257,2-395,8 nm. Struktur kristal SNTA adalah selulosa II dengan derajat kristalinitas 97,57%. Berdasarkan analisis thermogravimetric analysis (TGA), degradasi SNTA terjadi pada suhu 173oC dengan meninggalkan residu massa padat 11,25%
pada 800oC. Sifat alir dan kompresibilitas SNTA adalah cukup baik dan dapat
digunakan sebagai bahan pengisi dan pengikat pada tablet. Konsentrasi SNTA yang dapat digunakan dalam formulasi tablet natrium diklofenak dengan metode cetak langsung adalah 10%. Tablet natrium diklofenak yang diformulasi dengan SNTA (F5) memiliki friabilitas yang lebih rendah, kekerasan yang lebih tinggi, dan waktu hancur yang lebih lambat dari yang diformulasi dengan SMTA (F6) dan Avicel PH 102® (F7) dengan nilai friabilitas untuk F5, F6, dan F7
berturut-turut 0,50%, 0,75%, dan 0,75%, kekerasan 7,98 kg, 7,21 kg, dan 7,15 kg. Waktu hancur dengan cakram, 16,30 menit, 5,48 menit, dan 5,40 menit, dan tanpa cakram 16,78 menit, 5,63 menit, dan 5,55 menit. Laju pelepasan obat dari tablet F5 lebih lambat dari tablet F6, F7, dan Voltaren®. Persentasepelepasan obat dari
tablet F5 adalah 95,22% setelah 240 menit dalam medium pH 6,8, sedangkan dalam medium pH berganti sebesar 93,82% dalam waktu 300 menit. Hasil analisis statistik dengan metode Anova dengan taraf kepercayaan 95% dan menggunakan
Tukey test menunjukkan adanya perbedaan yang signifikan pada persen pelepasan obat dari uji disolusi antara formula F5, F6, F7, dan Voltaren® dalam medium pH
6,8 dan pH berganti (p ≤ 0,05). Kinetika pelepasan obat dari tablet F5 dalam medium pH 6,8 adalah order 1 dan Higuchi, dan dalam medium pH berganti adalah kinetika pelepasan Higuchi.
SMTA memiliki karakteristik dan sifat alir yang baik sehingga dapat digunakan sebagai bahan pengisi, pengikat, dan penghancur dalam pembuatan tablet cetak langsung. SNTA dapat digunakan sebagai bahan pengisi dan pengikat pada tablet dengan memberikan pelepasan obat yang diperlambat.
Kata kunci: tandan buah aren (Arenga pinnata (Wurmb) Merr.), selulosa mikrokristal, selulosa nanokristal, karakterisasi, eksipien tablet,
ABSTRACT
Cellulose is a polysaccharide that occurs as the supporting tissue of the plant including in the fruit bunch and can be isolated and crystallized. Microcrystalline cellulose (MCC) is the most common form of cellulose used in the preparation of tablet by direct compression method. MCC is still imported that makes the production cost of pharmaceutical dosage form is expensive. Therefore it is necessary to find alternative excipients from the more economical sources. To increase the surface area and the crystallinity of the MCC, nanocrystalline cellulose then be made. The objective of this study was to prepare, characterize MCC and nanocrystalline cellulose (NCC) obtained from sugar palm fruit bunches (SPFB) (Arenga pinnata (Wurmb) Merr.), and use it as an excipient in diclofenac sodium tablet. Physical characteristics and influence on tablet properties and drug release from tablets by direct compression were then compared to those of commercial excipient (Avicel®).
In this study, SPFB was used as source of cellulose. MCC was prepared from α-cellulose of SPFB by hydrolysis using 2.5 N hydrochloric acid solution. The physical properties of MCC of SPFB was determined in accordance with the standards of the United State Pharmacopeia National Formulary 27 (USP 32-NF 27). In addition,the yield of the starting material, functional groups, morphology, crystalline structure, degree of crystallinity, flow properties, capacity swelling, hydration, moisture, and acute toxicity of the MCC were also determined. NCC was isolated from α-cellulose of SPFB by hydrolysis method using 54% sulfuric acid solution and homogenized by magnetic stirrer for 45 minutes. To remove residual acid, the milky suspension was centrifuged at 10,000 rpm for 15 minutes. The precipitate was dialyzed for 48 hours with an activated dialysis membrane. Characterization of NCC included functional group, morphology, crystalline structure, degree of crystallinity, thermal degradation, flow property, and compressibility. Tabletswere prepared in 7 formulas (F1-F7) using diclofenac sodium as a model drug. Evaluation, dissolution test, and drug release kinetic of diclofenac sodium tablets that prepared with NCC of SPFB were compared to tablets formulated with the MCC of SPFB and Avicel PH 102®, as
well as the commercially available Voltaren® tablets in the medium of pH 6.8 and
pH changed.
The results showed thatthe yield of MCC from the starting material SPFB were 16 to 21.33% w/w. MCC hasphysical characteristics with irregular in shapes, uneven surfaces, and fulfilled the requirement of USP 32-NF 27. Fourier transform infra red (FTIR) spectra indicated that MCC and Avicel PH 102®
exhibited similar spectra. Particle size of MCC from SPB were larger than Avicel PH 102®. The structure of MCC crystals from SPB was cellulose II whereas
Avicel PH 102® was cellulose I. Flow properties, swelling capacity, hydration, and
moisture absorption of the MCC showed no significant difference from the Avicel PH 102®. The cytotoxicity test of MCC at concentration of 2000 and 5000 mg/kg
distribution ranging from 257.2 to 395.8 nm. The structure of NCC crystals was cellulose II with a degree of crystallinity 97.57%. Based on thermogravimetric analysis (TGA), the degradation of NCCs occured at a temperature of 173oC
leaving a mass of solid residue 11.25% at 800oC. Flow property and
compressibility of NCC were good and therefore can be used as a filler and a binder in the preparation of tablet. Concentration of NCC that can be used in the formulation of diclofenac sodium tablets by direct compression method was 10%. Diclofenac sodium tablets were formulated with NCC (F5) had lower friability, higher hardness, and slower disintegration time than that formulated with MCC (F6) and Avicel PH102 (F7) with the value of friability of F5, F6, and F7 0.50%, 0.75%, and 0.75%, respectively, hardness 7.98 kg, 7.21 kg, and 7.15 kg, respectively, disintegration time with a disc method 16.30 min, 5.48 min, and 5.40 min, and without a disc 16.78 min, 5.63 min, and 5.55 min, respectively. The drug release rate of F5 tablet was slower than F6, F7, and Voltaren® tablets. Percentage
of drug release in diclofenac sodium tablets made using NCC was 95.22% after 240 minutes in pH 6.8 medium, whereas in pH changed medium was 93.82% within 300 minutes. Statistical analysis by ANOVA method with 95% confidence level and using Tukey test showed a significant difference in the percentage drug release from dissolution test between formulas F5, F6, F7, and Voltaren® in pH 6.8
and pH changed medium (p ≤ 0.05). Drug release kinetic of F5 tablet in pH 6.8 medium was first order and Higuchi, and in pH changed medium was Higuchi.
MCC of SPB has characteristics and good flow properties that can be used as filler, binder, and disintegrant in the preparation of tablet by direct compression method. NCC of SPB can be used as filler and binder in slow release tablet.
KATA PENGANTAR
Puji syukur penulis panjatkan kepada Allah SWT atas segala limpahan rahmat dan hidayahNya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan disertasi ini. Shalawat dan salam semoga dilimpahkan Allah SWT ke atas pangkuan Nabi Muhammad SAW sebagai teladan dalam menjalani kehidupan.
Disertasi ini disusun untuk melengkapi salah satu syarat mencapai gelar Doktor Ilmu Farmasi pada Fakultas Farmasi Universitas Sumatera Utara dengan judul Pembuatan dan Karakterisasi Selulosa Mikrokristal dan Nanokristal dari Tandan Aren (Arenga pinnata (Wurmb) Merr.) dan Penggunaannya sebagai Eksipien dalam Tablet Natrium Diklofenak.
Pada kesempatan ini dengan setulus hati penulis mengucapkan terimakasih yang sebesar-besarnya kepada: kesempatan bagi penulis menjadi mahasiswa Program Doktor Ilmu Farmasi Fakultas Farmasi. penulis menjalani pendidikan, penelitian, dan penyelesaian disertasi ini.
5. Bapak Dr. M. Pandapotan Nasution, MPS., Apt. selaku Co-promotor yang telah memberikan waktu, bimbingan, dan arahan selama penelitian hingga selesainya disertasi ini
6. Bapak Prof. Dr. Urip Harahap, Apt., Guru Besar Universitas Sumatera Utara selaku penguji.
7. Bapak Dr. Saharman Gea, M.Si., Dosen Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara selaku penguji
8. Bapak Prof. Dr. Jansen Silalahi, M.AppSc., Apt., Guru Besar Universitas Sumatera Utara selaku penguji
9. Bapak Prof. Dr. Elfi Sahlan Ben, Apt., Guru Besar Universitas Andalas selaku penguji
10. Pimpinan dan staf dosen Laboratorium Penelitian,Laboratorium Fitokimia, dan Laboratorium Teknologi Formulasi II Fakultas Farmasi Universitas Sumatera Utara atas fasilitas yang diberikan
Penulis juga menghaturkan terimakasih tak terhingga kepada Ayahanda Drs. dr. H. Salim Adnan, Sp.M., M.Ag., Ibunda dr. Hj. Murni Mahyudin, Ayahanda mertua Nurhanuddin Nst, Suami tercinta Dr. Wahyudin Nur Nst., M.A. dan anak-anak tercinta Humaira Nst., Balqis Nur Nst., Zahra Afifah Nst., dan Alya Farisah Nst. yang telah sabar dalam memberikan dukungan, semangat, dan do’a hingga penulis dapat menyelesaikan disertasi ini. Terimakasih juga untuk sahabat-sahabat dan semua pihak yang telah membantu penulis namun tidak dapat disebutkan namanya satu per satu. Semoga Allah SWT memberikan balasan yang berlipat ganda atas kebaikan dan bantuan yang diberikan kepada penulis.
Penulis menyadari bahwa disertasi ini masih jauh dari sempurna, sehingga penulis dengan segala kerendahan hati akan menerima kritik dan saran agar disertasi ini menjadi lebih baik dan bermanfaat bagi kita semua.
Medan, April 2014 Penulis,
RIWAYAT HIDUP
A. Identitas Pribadi
1. Nama : Sumaiyah
2. Tempat, tanggal lahir : Medan, 26 Desember 1977
3. Agama : Islam
4. NIP : 197712262008122002
5. Pangkat/Golongan : Penata Muda Tk. I/III c
6. Pekerjaan : Staf Pengajar Departemen Teknologi Farmasi
Fakultas Farmasi USU
7. Jabatan Fungsional : Lektor
8. Alamat Rumah : Jl. Setia Luhur No. 61 Medan
9. Telp. Rumah/HP : (061)8455502/085361323060
10. E-mail : sumaiyah7777@gmail.com
11. Nama Ayah : Drs. dr. H. Salim Adnan, Sp.M., M.Ag.
12. Nama Ibu : dr. Hj. Murni Mahyudin
13. Nama Suami : Dr. Wahyudin Nur Nasution, M.Ag.
14. Nama Anak : Humaira Nasution
3. SMA Taman Siswa LNG Arun, Batuphat, Aceh Utara, tamat 1994
4. Jurusan Farmasi Fakultas Matematika dan Ilmu Pengetahuan Alam USU, tamat 1999
5. Profesi Apoteker Fakultas Matematika dan Ilmu Pengetahuan Alam USU, tamat 2001
6. Program Magister Ilmu Farmasi Fakultas Farmasi USU, tamat 2006 7. Program Doktor Ilmu Farmasi Fakultas Farmasi USU, tamat 2014
C. Riwayat Pekerjaan
D. Publikasi
1. Dissolution Test of Ferrous Sulphate Formulated in Alginate and Gelatin Capsules. (2010). Malaysian Journal of Pharmaceutical Sciences.
2. Ferrous Sulfate Bioavailability Formulated in Alginate Capsule. (2010).
Malaysian Journal Of Pharmaceutical Sciences.
3. Pembuatan dan Karakterisasi Selulosa Mikrokristal Tandan Aren (Arenga pinnata (Wurmb) Merr.). (2011). Prosiding Pharmacy Update 3rd.
4. Nanocrystal Cellulose of Sugar Palm Bunch (Arenga pinnata (Wurmb) Merr.) as Excipients in Diclofenac Sodium Tablet. (2011). Proceeding Innovation in Polymer Science and Technology 2011 (IPST 2011).
5. A Retrospective Study on Drug Interactions of JAMKESMAS Patients in Hasanuddin Damrah Manna Hospital South Bengkulu. (2012). Proceeding 24th Federation of Asian Pharmaceutical Associations (FAPA) Congress 2012.
6. Pemanfaatan Selulosa Mikrokristal dari Tandan Aren (Arenga pinnata
(Wurmb) Merr.) sebagai Eksipien Tablet Cetak Langsung. (2013).
Prosiding Seminar Nasional Herbal.
7. Isolation and Characterization of Nanocrystalline Cellulose from Sugar Palm Bunch (Arenga pinnata (Wurmb) Merr.). (2013). Abstract Book Innovation in Polymer Science and Technology 2013 (IPST 2013).
8. Preparation and Characterization of Nanocrystalline Cellulose from Sugar Palm Bunch (Arenga pinnata (Wurmb) Merr.). (2014). International Journal Pharmaceutical Technology Research.
Halaman
BAB III METODE PENELITIAN ... 45
3.1 Desain Penelitian ... 45
DAFTAR TABEL
Halaman
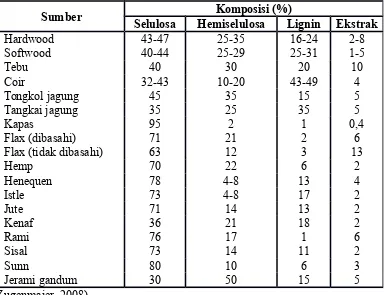
Tabel 2.1 Senyawa kimia yang terdapat dalam beberapa bahan
yang mengandung selulosa ...
15
Tabel 2.2 Spesifikasi selulosa mikrokristal menurut USP 32-NF 27 ... 21
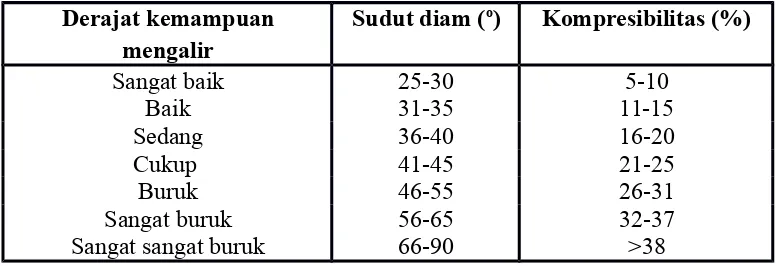
Tabel 2.3 Tabel kemampuan mengalir serbuk menurut Carr ... 22
36 Tabel 3.1 Formula tablet yang dibuat dengan menggunakan Avicel
PH 102, SMTA, dan SNTA ...
61
Tabel 3.2 Persyaratan keseragaman bobot tablet ... 66 Tabel 4.1 Sifat fisikokimia dari α-selulosa tandan aren ... 70 Tabel 4.2 Sifat-sifat fisikokimia dari SMTA ... 71 Tabel 4.3 Bilangan gelombang dari FTIR ... 73 Tabel 4.4 Karakteristik serbuk SMTA dan Avicel PH 102 ... 75 Tabel 4.5 Pengaruh pemberian SMTA terhadap berat badan rata-rata
mencit pada hari ke-14 ... 79
Tabel 4.6 Hasil uji preformulasi tablet SMTA dan Avicel PH 102 ... 82 Tabel 4.7 Hasil uji keseragaman bobot tablet SMTA dan Avicel PH
102 ... 83
Tabel 4.8 Hasil uji friabilitas, kekerasan, dan waktu hancur tablet
SMTA dan Avicel PH 102 ...
84
Tabel 4.9 Bilangan gelombang dari FTIR SMTA, Avicel, dan SNTA 92 Tabel 4.10 Sifat alir serbuk SMTA, SNTA, dan Avicel PH 102 ... 96
Tabel 4.11 Formula tablet yang dibuat dengan menggunakan
Avicel PH 102, SMTA, dan SNTA ... 97
Tabel 4.12 Hasil uji preformulasi tablet natrium diklofenak yang
menggunakan Avicel PH 102, SMTA, dan SNTA ... 98
Tabel 4.13 Hasil uji keseragaman kandungan dari tablet natrium
diklofenak menggunakan Avicel PH 102, SMTA, dan
SNTA ... 100
Tabel 4.14 Hasil uji keseragaman bobot tablet natrium diklofenak
menggunakan Avicel PH 102, SMTA, dan SNTA ... 100
Tabel 4.15 Pengaruh formula terhadap uji friabilitas, kekerasan, dan
waktu hancur dari tablet natrium diklofenak yang
diformulasi dengan SNTA, SMTA, dan Avicel ...
Tabel 4.16 Nilai korelasi dari kinetika pelepasan natrium diklofenak
dari tablet dalam medium pH 6,8 ... 107
Tabel 4.17 Nilai korelasi dari kinetika pelepasan natrium diklofenak
DAFTAR GAMBAR
Halaman
Gambar 1.1 Skema tahapan hidrolisis selulosa ... 4
Gambar 1.2 Kerangka konsep penelitian penmbuatan SMTA dan
SNTA, dan penggunaan selulosa mikrokristal dan
nanokristal dalam tablet natrium diklofenak ... 8
Gambar 2.1 Struktur selulosa ... 12
Gambar 2.2 Kumpulan rantai selulosa dalam mikrofibril yang
Membentuk dinding sel tanaman ... 14
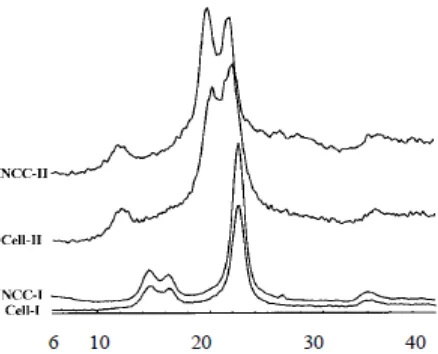
Gambar 2.3 Difraktogram difraksi X-Ray dari selulosa dan selulosa
nanokristal linter …...………... 17
Gambar 2.4 Sintesis selulosa yang dipengaruhi oleh enzim pada
Populus trimula (L) …………..………. 19
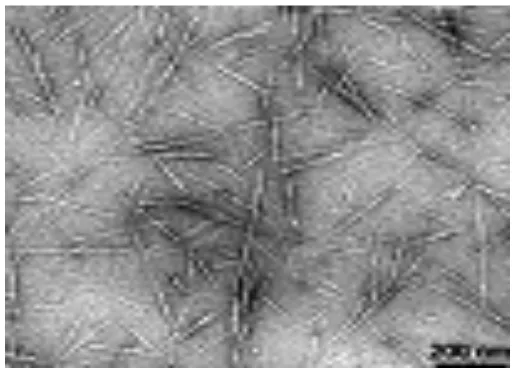
Gambar 2.5 Gambar TEM dari selulosa nanokristal dari sisal ……... 25
Gambar 2.6 Tandan buah aren ... 32
Gambar 2.7 Struktur kimia Natrium Diklofenak …….…………... 38
Gambar 4.1 α-selulosa yang diperoleh dari tandan aren dan selulosa
mikrokristal dari tandan aren (SMTA) ...
69
Gambar 4.2 Spektrum inframerah dari Avicel PH 102 dan SMTA ... 72
Gambar 4.3 SEM dari SMTA dan Avicel PH 102 ... 73
Gambar 4.4 Difraktogram XRD dari SMTA dan Avicel PH 102 ... 74
PH 102 ... 77
Gambar 4.6 Pengaruh pemberian SMTA terhadap indeks massa
organ mencit ... 79
Gambar 4.7 Pengaruh pemberian SMTA terhadap jaringan ginjal
mencit kontrol, dengan dosis 2000 mg/kg bb, dan
dengan dosis 5000 mg/kg bb, dengan pewarnaan HE dan
perbesaran 10 x 40 ... 80 Gambar 4.8 Pengaruh pemberian SMTA terhadap jaringan hati
mencit kontrol, dengan dosis 2000 mg/kg bb, dan
dengan dosis 5000 mg/kg bb, dengan pewarnaan HE dan
perbesaran 10 x 40 ... 81
Gambar 4.9 Tablet SMTA dan Avicel PH 102 ... 83
Gambar 4.10 α-selulosa tandan aren dan SNTA ... 87
Gambar 4.11 Esterifikasi gugus hidroksil oleh ionsulfatdari
perlakuan asam sulfat terhadap selulosa ...
88
Gambar 4.12 Selulosa nanokristal dari tandan aren (perbesaran 20x),
sisal (perbesaran 200x),dan bambu (perbesaran 200x) ...
90
Gambar 4.13 Distribusi ukuran partikel SNTA setelah penggilingan
dengan HEM E3D selama 50 jam ...
91
Gambar 4.14 Spektrum inframerah dari Avicel, SMTA, dan SNTA... 92
Gambar 4.15 Difraktogram XRD dari Avicel PH 102, SMTA, dan
SNTA ... 93
Gambar 4.16 Termogram TGA dari Avicel PH 102, SMTA, dan
SNTA ... 95
SNTA, SMTA, dan Avicel PH 102 ... 99
Gambar 4.18 Profil disolusi tablet natrium diklofenak yang
diformulasi dengan Avicel PH 102 (F7), SMTA (F6),
SNTA (F5), dan Voltaren® dalam medium pH 6,8 ... 103
Gambar 4.19 Profil disolusi tablet natrium diklofenak yang
diformulasi dengan Avicel PH 102 (F7), SMTA
(F6), SNTA (F5), dan Voltaren® dalam medium
pH berganti ... 103
Gambar 4.20 Hubungan pelepasan natrium diklofenak terhadap waktu
dalam medium pH 6,8 ... 106
Gambar 4.21 Hubungan logaritma sisa natrium diklofenak terhadap
waktu dalam medium pH 6,8 ... 106
Gambar 4.22 Hubungan pelepasan natrium diklofenak terhadap akar
waktu dalam medium pH 6,8 ... 107
Gambar 4.23 Hubungan pelepasan natrium diklofenak terhadap waktu
dalam medium pH berganti ... 108
Gambar 4.24 Hubungan logaritma pelepasan natrium diklofenak
terhadap waktu dalam medium pH berganti ... 108
Gambar 4.25 Hubungan pelepasan natrium diklofenak terhadap akar
waktu dalam medium pH berganti ...
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Hasil Identifikasi Tanaman Aren ... 122
Lampiran 2 Sertifikat Analisis Bahan Baku Avicel PH 102 ... 123
Lampiran 3 Sertifikat Analisis Bahan BakuLactose Spray Dried .... 124
Lampiran 5 Rekomendasi Persetujuan Etik Penelitian Kesehatan ... 126
Lampiran 6 Kurva Absorpsi Natrium Diklofenak dalam Medium
pH 1,2 ... 127
Lampiran 7 Kurva Kalibrasi Natrium Diklofenak dalam Medium
pH 1,2 ... 128
Lampiran 8 Kurva Absorpsi Natrium Diklofenak dalam Medium
pH 6,8 ... 129
Lampiran 9 Kurva Kalibrasi Natrium Diklofenak dalam Medium
pH 6,8 ... 130
Lampiran 10 Perhitungan Rendemen SMTA ………...……….. 131
Lampiran 11 Perhitungan Derajat Polimerisasi ... 132
Lampiran 12 Data pH SMTA ... 134
Lampiran 13 Perhitungan Susut Pengeringan SMTA ... 135
Lampiran 14 Perhitungan Kadar Abu Total SMTA ... 136
Lampiran 15 Perhitungan Bobot Jenis Ruahan ... 137
Lampiran 16 Perhitungan Bobot Jenis Mampat ... 138
Lampiran 17 Perhitungan Indeks Hausner ….………. 139
Lampiran 18 Perhitungan Indeks Kompresibilitas ... 140
Lampiran 19 Perhitungan Porositas Serbuk ... 141
Lampiran 20 Perhitungan Kapasitas Hidrasi ... 142 Lampiran 21 Perhitungan Kapasitas Pengembangan ... 143
Lampiran 23 Data Uji Keseragaman Kandungan Tablet Formula F5 .... 145
Lampiran 24 Data Uji Keseragaman Kandungan Tablet Formula F6 .... 150
Lampiran 25 Data Uji Keseragaman Kandungan Tablet Formula F7 .... 155
Lampiran 26 Perhitungan Keseragaman Bobot ... 160
Lampiran 27 Perhitungan Friabilitas ... 163
Lampiran 28 Perhitungan Kekerasan Tablet ... 164
Lampiran 29 Data Waktu Hancur Tablet ... 165
Lampiran 30 Data Uji Pelepasan Obat In VitroMenggunakan
Dissolution Tester dalam Medium pH 6,8 ... 166
Lampiran 31 Data Uji Pelepasan Obat In VitroMenggunakan
Dissolution Tester dalam Medium pH Berganti ... 182
Lampiran 32 Uji ANOVA Profil Disolusi Natrium Diklofenak dari
Tablet F5, F6, F7, dan Voltaren® dalam Medium pH 6,8 198
Lampiran 33 Uji ANOVA Profil Disolusi Natrium Diklofenak dari
Tablet F5, F6, F7, dan Voltaren®dalam Medium pH
Berganti... 199
Lampiran 34 Potensial Zeta Natrium Diklofenak ... 200
Lampiran 35 Potensial Zeta SNTA ... 201
ABSTRAK
Selulosa adalah polisakarida yang berperan sebagai jaringan penopang pada tanaman termasuk tandan aren dan dapat diisolasi dan dibuat menjadi kristal. Selulosa mikrokristal merupakan eksipien yang paling sering digunakan dalam pembuatan tablet dengan metode cetak langsung. Selulosa mikrokristal selama ini masih diimpor sehingga harga sediaan farmasi menjadi mahal. Karena itu perlu diupayakan untuk menemukan bahan tambahan alternatif dari sumber yang lebih ekonomis. Untuk meningkatkan luas permukaan dan kristalinitas selulosa mikrokristal, maka dibuat selulosa nanokristal. Tujuan penelitian ini adalah untuk membuat, mengkarakterisasi selulosa mikrokristal dan nanokristal yang diperoleh dari tandan aren (Arenga pinnata (Wurmb) Merr.), dan menggunakannya sebagai eksipien pada tablet natrium diklofenak. Kemudian karakteristik fisik dan pengaruhnya pada sifat tablet dan pelepasan obat dari tablet cetak langsung dibandingkan dengan eksipien komersial (Avicel®).
Pada penelitian ini tandan buah aren digunakan sebagai sumber selulosa. Selulosa mikrokristal dibuat dari α-selulosa tandan aren melalui proses hidrolisis dengan asam klorida 2,5 N. Selulosa mikrokristal tandan aren (SMTA) yang diperoleh ditentukan sifat fisiknya menurut standar United State Pharmacopeia
32-National Formulary 27 (USP 32-NF 27). Selain itu ditentukan juga rendemen dari bahan awal, gugus fungsi, morfologi, struktur kristal, derajat kristalinitas, sifat alir, kapasitas pengembangan, hidrasi, serap lembab, dan toksisitas akut dari SMTA. Selulosa nanokristal dibuat dari α-selulosa tandan aren dengan cara hidrolisis dengan asam sulfat 54% dan dihomogenkan dengan pengaduk magnet selama 45 menit. Untuk menghilangkan sisa asam, suspensi disentrifugasi pada 10.000 rpm selama 15 menit. Endapan didialisis selama 48 jam dengan membran dialisis yang telah diaktivasi. Selulosa nanokristal tandan aren (SNTA) yang diperoleh dikarakterisasi gugus fungsi, morfologi, struktur selulosa,derajat kristalinitas, degradasi termal, sifat alir, dan kompresibilitas. Tablet dibuat dalam 7 formula (F1-F7) dengan menggunakan natrium diklofenak sebagai model obat. Evaluasi tablet, uji pelepasan obat, dan kinetika pelepasan obat dari tablet natrium diklofenak yang diformulasi dengan selulosa nanokristal dibandingkan terhadap tablet yang diformulasi dengan selulosa mikrokristal dan Avicel PH 102®, serta
tablet Voltaren® yang sudah beredar di pasaran dalam medium pH 6,8 dan pH
berganti.
Hasil penelitian menunjukkan bahwa rendemen SMTA dari tandan aren adalah 16-21,33% b/b. SMTA memiliki karakteristik fisik dengan bentuk yang tidak beraturan, permukaan yang tidak rata, dan memenuhi persyaratan USP 32-NF 27. Hasil uji fourier transform infra red (FTIR) menunjukkan spektrum yang sama dengan Avicel PH 102®. Ukuran partikel SMTA lebih besar dibandingkan
dengan Avicel PH 102®. Struktur kristal SMTA adalah selulosa II sedangkan
Avicel PH 102® adalah selulosa I. Sifat alir, kapasitas pengembangan, hidrasi, dan
serap lembab dari SMTA tidak berbeda signifikan dengan Avicel PH 102®. Uji
sferis dengan diameter 15-20 nm dan distribusi ukuran partikel berkisar 257,2-395,8 nm. Struktur kristal SNTA adalah selulosa II dengan derajat kristalinitas 97,57%. Berdasarkan analisis thermogravimetric analysis (TGA), degradasi SNTA terjadi pada suhu 173oC dengan meninggalkan residu massa padat 11,25%
pada 800oC. Sifat alir dan kompresibilitas SNTA adalah cukup baik dan dapat
digunakan sebagai bahan pengisi dan pengikat pada tablet. Konsentrasi SNTA yang dapat digunakan dalam formulasi tablet natrium diklofenak dengan metode cetak langsung adalah 10%. Tablet natrium diklofenak yang diformulasi dengan SNTA (F5) memiliki friabilitas yang lebih rendah, kekerasan yang lebih tinggi, dan waktu hancur yang lebih lambat dari yang diformulasi dengan SMTA (F6) dan Avicel PH 102® (F7) dengan nilai friabilitas untuk F5, F6, dan F7
berturut-turut 0,50%, 0,75%, dan 0,75%, kekerasan 7,98 kg, 7,21 kg, dan 7,15 kg. Waktu hancur dengan cakram, 16,30 menit, 5,48 menit, dan 5,40 menit, dan tanpa cakram 16,78 menit, 5,63 menit, dan 5,55 menit. Laju pelepasan obat dari tablet F5 lebih lambat dari tablet F6, F7, dan Voltaren®. Persentasepelepasan obat dari
tablet F5 adalah 95,22% setelah 240 menit dalam medium pH 6,8, sedangkan dalam medium pH berganti sebesar 93,82% dalam waktu 300 menit. Hasil analisis statistik dengan metode Anova dengan taraf kepercayaan 95% dan menggunakan
Tukey test menunjukkan adanya perbedaan yang signifikan pada persen pelepasan obat dari uji disolusi antara formula F5, F6, F7, dan Voltaren® dalam medium pH
6,8 dan pH berganti (p ≤ 0,05). Kinetika pelepasan obat dari tablet F5 dalam medium pH 6,8 adalah order 1 dan Higuchi, dan dalam medium pH berganti adalah kinetika pelepasan Higuchi.
SMTA memiliki karakteristik dan sifat alir yang baik sehingga dapat digunakan sebagai bahan pengisi, pengikat, dan penghancur dalam pembuatan tablet cetak langsung. SNTA dapat digunakan sebagai bahan pengisi dan pengikat pada tablet dengan memberikan pelepasan obat yang diperlambat.
Kata kunci: tandan buah aren (Arenga pinnata (Wurmb) Merr.), selulosa mikrokristal, selulosa nanokristal, karakterisasi, eksipien tablet,
ABSTRACT
Cellulose is a polysaccharide that occurs as the supporting tissue of the plant including in the fruit bunch and can be isolated and crystallized. Microcrystalline cellulose (MCC) is the most common form of cellulose used in the preparation of tablet by direct compression method. MCC is still imported that makes the production cost of pharmaceutical dosage form is expensive. Therefore it is necessary to find alternative excipients from the more economical sources. To increase the surface area and the crystallinity of the MCC, nanocrystalline cellulose then be made. The objective of this study was to prepare, characterize MCC and nanocrystalline cellulose (NCC) obtained from sugar palm fruit bunches (SPFB) (Arenga pinnata (Wurmb) Merr.), and use it as an excipient in diclofenac sodium tablet. Physical characteristics and influence on tablet properties and drug release from tablets by direct compression were then compared to those of commercial excipient (Avicel®).
In this study, SPFB was used as source of cellulose. MCC was prepared from α-cellulose of SPFB by hydrolysis using 2.5 N hydrochloric acid solution. The physical properties of MCC of SPFB was determined in accordance with the standards of the United State Pharmacopeia National Formulary 27 (USP 32-NF 27). In addition,the yield of the starting material, functional groups, morphology, crystalline structure, degree of crystallinity, flow properties, capacity swelling, hydration, moisture, and acute toxicity of the MCC were also determined. NCC was isolated from α-cellulose of SPFB by hydrolysis method using 54% sulfuric acid solution and homogenized by magnetic stirrer for 45 minutes. To remove residual acid, the milky suspension was centrifuged at 10,000 rpm for 15 minutes. The precipitate was dialyzed for 48 hours with an activated dialysis membrane. Characterization of NCC included functional group, morphology, crystalline structure, degree of crystallinity, thermal degradation, flow property, and compressibility. Tabletswere prepared in 7 formulas (F1-F7) using diclofenac sodium as a model drug. Evaluation, dissolution test, and drug release kinetic of diclofenac sodium tablets that prepared with NCC of SPFB were compared to tablets formulated with the MCC of SPFB and Avicel PH 102®, as
well as the commercially available Voltaren® tablets in the medium of pH 6.8 and
pH changed.
The results showed thatthe yield of MCC from the starting material SPFB were 16 to 21.33% w/w. MCC hasphysical characteristics with irregular in shapes, uneven surfaces, and fulfilled the requirement of USP 32-NF 27. Fourier transform infra red (FTIR) spectra indicated that MCC and Avicel PH 102®
exhibited similar spectra. Particle size of MCC from SPB were larger than Avicel PH 102®. The structure of MCC crystals from SPB was cellulose II whereas
Avicel PH 102® was cellulose I. Flow properties, swelling capacity, hydration, and
moisture absorption of the MCC showed no significant difference from the Avicel PH 102®. The cytotoxicity test of MCC at concentration of 2000 and 5000 mg/kg
distribution ranging from 257.2 to 395.8 nm. The structure of NCC crystals was cellulose II with a degree of crystallinity 97.57%. Based on thermogravimetric analysis (TGA), the degradation of NCCs occured at a temperature of 173oC
leaving a mass of solid residue 11.25% at 800oC. Flow property and
compressibility of NCC were good and therefore can be used as a filler and a binder in the preparation of tablet. Concentration of NCC that can be used in the formulation of diclofenac sodium tablets by direct compression method was 10%. Diclofenac sodium tablets were formulated with NCC (F5) had lower friability, higher hardness, and slower disintegration time than that formulated with MCC (F6) and Avicel PH102 (F7) with the value of friability of F5, F6, and F7 0.50%, 0.75%, and 0.75%, respectively, hardness 7.98 kg, 7.21 kg, and 7.15 kg, respectively, disintegration time with a disc method 16.30 min, 5.48 min, and 5.40 min, and without a disc 16.78 min, 5.63 min, and 5.55 min, respectively. The drug release rate of F5 tablet was slower than F6, F7, and Voltaren® tablets. Percentage
of drug release in diclofenac sodium tablets made using NCC was 95.22% after 240 minutes in pH 6.8 medium, whereas in pH changed medium was 93.82% within 300 minutes. Statistical analysis by ANOVA method with 95% confidence level and using Tukey test showed a significant difference in the percentage drug release from dissolution test between formulas F5, F6, F7, and Voltaren® in pH 6.8
and pH changed medium (p ≤ 0.05). Drug release kinetic of F5 tablet in pH 6.8 medium was first order and Higuchi, and in pH changed medium was Higuchi.
MCC of SPB has characteristics and good flow properties that can be used as filler, binder, and disintegrant in the preparation of tablet by direct compression method. NCC of SPB can be used as filler and binder in slow release tablet.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Selulosa merupakan salah satu polimer yang dapat diperbaharui. Selulosa
telah digunakan dalam bentuk serat atau turunannya selama sekitar 150 tahun
sebagai bahan baku kimia (Habibi, dkk., 2010). Selulosa merupakan suatu
makromolekul rantai tidak bercabang dari unit-unit anhidroglukopiranosayang
tersambung dengan ikatan β-1,4-glikosida. Setiap unit anhidroglukopiranosa
memiliki tiga gugus hidroksil. Serat selulosa terdapat pada dinding sel semua
tanaman.Senyawa ini juga dijumpai dalam plankton bersel satu atau alga di
lautan, juga pada jamur dan bakteri (Potthast, dkk., 2006; Zugenmaier, 2008).
Turunan selulosa telah digunakan secara luas sebagai bahan tambahan
(eksipien) dalam sediaan farmasetik, seperti etil selulosa, metil selulosa,
karboksimetil selulosa, dan hidroksipropil metil selulosa dalam bentuk sediaan
oral, topikal, dan injeksi. Penggunaan berbagai bentuk selulosa dalam sediaan
farmasi disebabkan sifatnya yang inert dan biokompatibel pada manusia (Bravo,
dkk., 2010; Jackson, dkk., 2011).
Berdasarkan derajat polimerisasi (DP) dan kelarutan dalam larutan NaOH
17,5%, selulosa dapat dibedakan menjadi tiga jenis, yaitu α, β, dan γ-selulosa.
α-selulosa merupakan selulosa berantai panjang, tidak larut dalam larutan NaOH
17,5% dan 9,45% dengan DP 600-1500. α-selulosa adalah penentu sifat
kemurnian selulosa. β-selulosa adalah selulosa berantai pendek, larut dalam
γ-selulosa ialah sama dengan β-γ-selulosa, tetapi DP kurang dari 15 (BSN, 2009;
Sumada, dkk., 2011).
Selulosa mikrokristal merupakan hasil dari hidrolisis α-selulosa dengan
larutan asam encer (Rowe, dkk., 2009). Ini adalah bentuk selulosa yang banyak
digunakan dalam tablet, karena ia dapat digunakan sebagai bahan pengisi,
pengikat, dan penghancur (Soekemi, dkk., 1987; Gohel dan Jogani, 2005; Rowe,
dkk., 2009). Oleh karena itu, selulosa mikrokristal dianggap sebagai bahan
tambahan terbaik dalam pembuatan tablet cetak langsung (Bhimte dan Tayade,
2007; Bushra,dkk., 2008). Beberapa sumber alam telah digunakan untuk
menghasilkan selulosa mikrokristal, seperti serat rami(Bhimte dan Tayade, 2007),
rambut biji Cochlospermum planchonii(Ohwoavworhua dan Adelakun, 2005a),
ampas tebu, jerami (Ilindra dan Dhake, 2008), dan lenan (Leppanen,dkk., 2009).
Selulosa mikrokristal yang telah beredar di pasaran dan banyak digunakan adalah
dengan nama dagang Avicel.
Avicel berfungsi sebagai bahan pengisi, pengikat, dan penghancur, dan
memiliki sifat bebas mengalir, sehingga banyak digunakan dalam pembuatan
tablet cetak langsung. Penggunaan Avicel pada tablet cetak langsung baik sebagai
pengisi maupun penghancur memberikan waktu hancur dan pelepasan obat dalam
waktu yang singkat. Hal ini dikarenakan Avicel mempercepat penetrasi medium
ke dalam tablet (Bhimte dan Tayade, 2007). Avicel merupakan bahan tambahan
yang harganya relatif mahal, padahal penggunaannyamenyusun sebagian besar
dari komponen tablet (50-80%). Ini merupakan salah satu faktor yang
Penggunaan selulosa dalam formulasi tidak terlibat langsung dalam
pengendalian pelepasan obat melalui interaksinya dengan obat. Walaupun selulosa
mikrokristal memiliki muatan sedikit agak negatif pada permukaan akibat adanya
residu hidroksil, namun muatan ini terbatas pada luas permukaan yang kecil pada
massa yang besar sehingga tidak dapat berikatan dengan sejumlah obat (Jackson,
dkk., 2011).
Beberapa tahun belakangan ini selulosa dikembangkan dalam bentuk
nanokristal, yang memiliki ukuran sekitar 0,2-100 nm (Gardner, 2008). Selulosa
nanokristal merupakan bahan penguat nanokomposit selulosa nanokristal-alginat
dengan densitas rendah (1,6 g/ml) dan kekuatan mekanik tinggi (10 GPa). Bahan
ini juga dapat dimanfaatkan dalam pembuatan perangkat biomedis, implan, tekstil
(Benavides, 2011), aditif pada makanan dan kosmetik (Boluk, 2010), dan
penyampaian obat dalam bentuk liposom, misel, mikrogel, dan pembawa dalam
targetted delivery system (Peng, dkk., 2011).
Selulosa nanokristal dibuat dari serat selulosa atau dari selulosa
mikrokristal dengan tahapan hidrolisis asam, sentrifus, dialisis, dan ultrasonikasi
(Oksman dan Mathew, 2007; Jackson, dkk., 2011) atau homogenisasi dengan
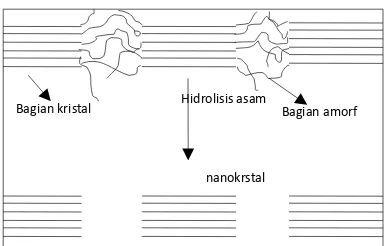
tekanan tinggi (Liu, dkk., 2010). Pada tahap hidrolisis sebagaimana diilustrasikan
pada Gambar 1.1, terjadi perubahan struktur selulosa dengan penghilangan bagian
amorf, sehingga yang tinggal hanya bagian kristal dari selulosa. Proses ini
menghasilkan selulosa dalam bentuk batang, kristal, dan berdimensi nanometer
Bagian kristal Hidrolisis asam Bagian amorf
nanokrstal
Gambar 1.1. Skema tahapan hidrolisis selulosa
Selulosa nanokristal mempunyai rasio luas permukaan dan volume yang
sangat besar (Habibi, dkk., 2010; Liu, dkk., 2010). Luas permukaan yang sangat
besar ini merupakan suatu keuntungan dari selulosa nanokristal yaitu
memungkinkan untuk lebih banyak obat dapat berinteraksi pada permukaannya.
Jackson, dkk. (2011)telah meneliti ikatan dan mekanisme pelepasan beberapa
bahan obat yang menggunakan selulosa nanokristal eksipien. Hasil yang diperoleh
adalah tetrasiklin dan doksorubisin yang sifatnya terionisasi memiliki pelepasan
yang cepat dalam periode 1 hari, sedangkan pelepasan dosetaksel, paklitaksel,
dan etoposida dari selulosa nanokristal yang dimodifikasi permukaannya dengan
setil trimetilamonium bromida (CTAB) pelepasan obatnya terkendali dalam
periode lebih dari 2 hari. Keberadaan gugus-gugus hidroksil pada permukaan
selulosa nanokristal juga memungkinkan derivatisasi selulosa dengan bahan kimia
tertentu. Villanova, dkk. (2011) telah memodifikasi selulosa nanokristal dengan
beberapa akrilat yang kemudian digunakan sebagai eksipien untuk mendapatkan
pelepasan terkendali dari tablet propanolol HCl. Selulosa yang memiliki
kristalinitas yang lebih tinggi akan membuat tablet menjadi lebih kompak dan
keras (Suzuki dan Nakagami, 1999) dan akan mengurangi kemampuan untuk
Tandan buah tanaman Palmae umumnya memiliki kandungan serat yang
tinggi disamping zat-zat lainnya. Seperti pada tandan kosong sawit yang memiliki
kadar serat tinggi pada bagian pangkal dan ujungnya yang keras dan kaku, yaitu
72,67% pada bagian pangkal dan 62,47% pada bagian ujungnya (Darnoko, 1995).
Tidak seperti pada tongkol jagung yang kandungan seratnya hanya 34,02%
(Darliah, 2008). Serat atau selulosa terdiri dari kristal dan amorf. Bagian kristal
dari selulosa menyebabkan serat menjadi keras dan kaku (Darnoko, 1995).
Telah dilaporkan oleh Ohwoavworhua dan Adelakun (2005b) bahwa
α-selulosa diisolasi dari tongkol jagung dan diperoleh rendemen α-α-selulosa
sebanyak 81,23%. Selanjutnya Ohwoavworhua dan Adelakun (2005ba)
menghidrolisis α-selulosa dari rambut biji Cochlospermum planchonii (Bixaceae)
dan dihasilkan selulosa mikrokristal sebanyak 21% dari bahan awal.
Arenga pinnata (Wurmb) Merr., sinonim Arenga saccharifera Labill.,
family Arecaceae (Palmae), disebut juga aren atau enau banyak didapati di
seluruh Nusantara pada ketinggian hingga sekitar 1220 m di atas permukaan laut.
Pohon inibanyak tumbuh di alam liar dan tidak jarang pula dibudidayakan
(Heyne, 1987). Menurut data yang dikeluarkan Direktorat Jenderal Perkebunan
(Ditjenbun) tahun 2003 total luas yang telah ditanami tanaman aren di seluruh
Indonesia mencapai 60.482 ha (Rumokoi, 2004). Sejak tahun 2007, Presiden telah
mencanangkan program nasional penanaman aren di wilayah Indonesia dengan
anggaran biaya Rp 60 miliar. Luas lahan potensial yang dapat digarap untuk lahan
aren diperkirakan sekitar 65.000 ha yang tersebar di wilayah Sulawesi Utara,
Sulawesi Tenggara, Kalimantan Barat, Kalimantan Timur, Jawa Barat, Jawa
Pohon aren memiliki banyak kegunaan untuk kehidupan manusia, seperti
nira yang dihasilkan dalam bentuk cairan manis dan biji buah aren yang dapat
dijadikan makanan yang biasa disebut kolang-kaling (Florido dan De Mesa,
2003). Pada industri kolang-kaling, terdapat limbah padat berupa tandan dan kulit
buah aren. Tandan yang telah diambil buahnya untuk diolah menjadi kolang
kaling hanya dimanfaatkan sebagai kayu bakar. Tandan aren diharapkan juga
memiliki kadar serat tinggi, seperti halnya tandan buah sawit (kandungan serat
62-72%). Komponen senyawa kimia yang terdapat pada limbah tandan aren adalah
27,74% lignin, 68,11% holoselulosa, 33,79% α-selulosa, 11,10% kadar air, dan
1,80% ekstraktif (Sumaiyah, dkk., 2013).
Natrium diklofenak merupakan obat antiinflamasi nonsteroid (AINS) tidak
selektif yang berfungsi sebagai analgetik, antipiretik, dan antiradang. Obat ini
praktis tidak larut dalam larutan asam (pKa = 4,0), tetapi larut dalam cairan usus
dan air (Bravo, dkk., 2002). Natrium diklofenak jika digunakan dalam waktu yang
lama dapat menimbulkan efek samping pada saluran cerna, mulai dari dispepsia
sampai perdarahan (Mycek, dkk., 2001). Kerusakan lambung oleh obat ini yang
digunakan secara oral akibat dari cara kerjanya yang menghambat enzim
cyclo-oxygenase (COX)-1 untuk perlindungan mukosa lambung dan COX-2 untuk
peradangan (Tjay dan Kirana, 2002).
Selulosa mikrokristal yang digunakan selama ini masih diimpor dari luar
negeri sehingga harga selulosa mikrokristal dan produk jadi relatif mahal. Untuk
mengatasi hal ini, maka peneliti berminat untuk mencari alternatif bahan
tambahan untuk formulasi cetak langsung dari sumber yang lebih ekonomis.
permukaannya, maka α-selulosa dipreparasi menjadi selulosa nanokristal.
Selulosa mikrokristal dan nanokristal yang diperoleh akan dikarakterisasi dan
digunakan sebagai eksipien pada tablet natrium diklofenak.
Pada penelitian ini tandan aren yang selama ini menjadi limbah dari
industri kolang-kaling akan dimanfaatkan untuk menghasilkan selulosa yang
berguna dalam bidang farmasi. Selulosa dari tandan aren diolah menjadi selulosa
mikrokristal dan nanokristal. Pembuatan selulosa mikrokristal yaitu dengan cara
menghidrolisis α-selulosa tandan aren dengan asam hidroklorida encer. Selulosa
mikrokristal tandan aren (SMTA) yang diperoleh dikarakterisasi dan diaplikasikan
sebagai eksipien pada tablet natrium diklofenak yang dibuat secara cetak
langsung. Karakteristik SMTA yang ditentukan adalah sesuai dengan United State
Pharmacopeia 32-National Formulary 27 (USP 32-NF 27), yaitu organoleptis,
derajat polimerisasi, pH, morfologi, ukuran partikel, berat jenis, kadar abu, logam
berat, susut pengeringan, mikroba, indeks kompresibilitas, porositas, gugus
fungsi, struktur kristal, sifat alir, kompresibilitas, dan toksisitas akut. Nanokristal
selulosa dibuat dengan cara menghidrolisis α-selulosa tandan aren dengan asam
sulfat, dilanjutkan dengan sentrifugasi, dialisis, ultrasonikasi, dan evaporasi.
Setelah itu akan ditentukan karakteristik selulosa nanokristal tandan aren (SNTA)
yang meliputi morfologi, ukuran partikel, gugus fungsi, struktur kristal,
temperatur degradasi, sifat alir, dan kompresibilitas. Karakteristik selulosa
mikrokristal dan nanokristal dari tandan aren ini akan dibandingkan dengan Avicel
yang merupakan selulosa mikrokristal yang tersedia di pasar. Selanjutnya SMTA
SMTA: Organolepis, derajat polimerisasi, pH, morfologi, ukuran parikel, berat jenis, kadar abu, logam berat, susut pengeringan, mikroba, indeks kompresibilitas,
SNTA: Morfologi, ukuran parikel, gugus fungsi, struktur kristal, temperatur degradasi, sifat alir, dan
α-selulosa
Tandan aren Karakterisik
Keseragaman sediaan, keseragaman bobot, kekerasan, friabilitas, waktu hancur
Disolusi Formulasi tablet natrium diklofenak
% pelepasan obat
Sifat isik tablet
keseragaman bobot, kekerasan, friabilitas, waktu hancur tablet, dan % pelepasan
obat yang terlepas dari tablet.
1.2 Kerangka Konsep Penelitian
a. Pembuatan SMTA dan SNTA
Variabel bebas Variabel terikat Parameter
(a)
b. Penggunaan selulosa mikrokristal dan nanokristal dalam tablet natrium
diklofenak
Variabel bebas Variabel terikat Parameter
(b)
Gambar 1.2. Kerangka konsep penelitian (a) pembuatan SMTA dan SNTA, dan (b) penggunaan selulosa mikrokristal dan nanokristal dalam tablet natrium diklofenak
1.3 Rumusan Masalah
Adapun rumusan masalah penelitian ini adalah:
1. bagaimana metode preparasi yang optimum dapat menghasilkan selulosa mikrokristal dan nanokristal dari tandan aren?
2. bagaimana karakteristik selulosa mikrokristal dan nanokristal dari tandan aren?
3. apakah selulosa mikrokristal dari tandan aren dapat digunakan sebagai eksipien tablet cetak langsung?
4. bagaimana peranan selulosa nanokristal terhadap pelepasan natrium diklofenak dari tablet?
1.4 Hipotesis Penelitian
Hipotesis penelitian ini adalah:
1. metode preparasi yang optimum dapat menghasilkan selulosa mikrokristal dan nanokristal dari tandan aren
2. selulosa mikrokristal dari tandan aren memiliki karakteristik yang menyamai Avicel PH 102 dan karakteristik selulosa nanokristal tandan aren
berbeda dari selulosa mikrokristal tandan aren dan Avicel
3. selulosa mikrokristal dari tandan aren dapat digunakan sebagai eksipien tablet cetak langsung
1.5 Tujuan Penelitian
Tujuan penelitian ini adalah untuk:
1. menghasilkan selulosa mikrokristal dan nanokristal dari tandan arendengan metode preparasi yang optimum
2. mengetahui karakteristik selulosa mikrokristal dan nanokristaldari tandan aren dan membandingkannya dengan Avicel PH 102
3. mengetahui selulosa mikrokristal dari tandan aren dapat digunakan sebagai eksipien tablet cetak langsung
4. mengetahui peranan selulosa nanokristal terhadap pelepasan natrium diklofenak dari tablet
1.6 Manfaat Penelitian
Manfaat penelitian ini adalah untuk menyediakan dan mengkarakterisasi
SMTA dan SNTA, juga untuk memanfaatkan limbah tandan aren menjadi produk
BAB II
TINJAUAN PUSTAKA
2.1 Selulosa
2.1.1 Struktur Selulosa
Selulosa merupakan salah satu polimer yang tersedia melimpah di alam.
Produksi selulosa sekitar 100 milyar ton setiap tahunnya. Sebagian dihasilkan
dalam bentuk selulosa murni seperti yang terdapat dalam rambut biji tanaman
kapas.Namun paling banyak adalah yang berkombinasi dengan lignin dan
polisakarida lain seperti hemiselulosa dalam dinding sel tumbuhan berkayu, baik
pada kayu lunak dan keras, jerami atau bambu. Selain itu selulosa juga dihasilkan
oleh bakteri Acetobacter xylinum secara ekstraseluler (Klemm, dkk., 1998a).
Senyawa ini juga dijumpai dalam plankton bersel satu atau alga di lautan, juga
pada jamur dan bakteri (Potthast, dkk., 2006; Zugenmaier, 2008).Sebagai bahan
baku kimia, selulosa telah digunakan dalam bentuk serat atau turunannya selama
sekitar 150 tahun (Habibi, dkk., 2010).
Selulosa pertama kali dijelaskan oleh Anselme Payen pada 1838 sebagai
serat padat yang tahan dan tersisa setelah pemurnian jaringan tanaman dengan
asam dan amonia (Brown dan Saxena, 2007). Payen mengamati bahwa bahan
yang telah dimurnikan mengandung satu jenis senyawa kimia yang seragam, yaitu
β-1,4-glikosida
juga mengatakan bahwa selulosa adalah isomer dari bahan penyusun pati
(Zugenmaier, 2008).
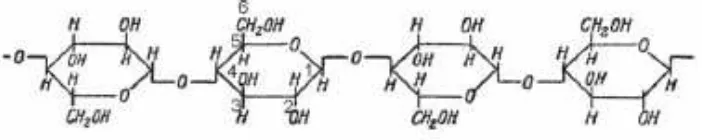
Selulosa tersusun dari unit-unit anhidroglukopiranosa yang tersambung
dengan ikatan β-1,4-glikosidik membentuk suatu rantai makromolekul tidak
bercabang. Setiap unit anhidroglukopiranosa memiliki tiga gugus hidroksil
(Potthast, dkk., 2006; Zugenmaier, 2008), seperti yang terlihat pada Gambar 2.1.
Selulosa mempunyai rumus empirik (C6H10 O5)n dengan n ~ 1500 dan berat
molekul ~ 243.000 (Rowe, dkk., 2009).
Gambar 2.1. Struktur selulosa (Zugenmaier, 2008)
Untuk mendapatkan sifat fisik dan kimia yang lebih baik dan memperluas
aplikasinya, selulosa dibuat dalam berbagai turunannya diantaranya turunan ester
dan eter. Ester selulosa banyak digunakan sebagai serat dan plastik, sedangkan
eter selulosa sebagai pengikat dan bahan tambahan untuk mortir khusus atau
kimia khusus untuk bangunan dan konstruksi juga stabilisator viskositas pada cat,
makanan, produk farmasetik, dan lain-lain. Selulosa juga merupakan bahan dasar
dalam pembuatan kertas. Seratnya mempunyai kekuatan dan durabilitas yang
juga higroskopis. Bahkan dalam keadaan basah, serat selulosa alami tidak
kehilangan kekuatannya (Zugenmaier, 2008).
Turunan selulosa telah digunakan secara luas dalam sediaan farmasi
seperti etil selulosa, metil selulosa, karboksimetil selulosa, dan dalam bentuk
lainnya yang digunakan dalam sediaan oral, topikal, dan injeksi. Sebagai contoh,
karboksimetil selulosa merupakan bahan utama dari SeprafilmTM, yang digunakan
untuk mencegah adesi setelah pembedahan. Baru-baru ini, penggunaan selulosa
mikrokristal dalam emulsi dan formulasi injeksi semipadat telah dijelaskan.
Penggunaan bentuk-bentuk selulosa dalam sediaan disebabkan sifatnya yang inert
dan biokompatibilitas yang sangat baik pada manusia (Jackson, dkk., 2011).
2.1.2 Sifat Fisika Kimia
Bahan berbasis selulosa sering digunakan karena memiliki sifat mekanik
yang baik seperti kekuatan dan modulus regang yang tinggi, kemurnian tinggi,
kapasitas mengikat air tinggi, dan struktur jaringan yang sangat baik (Gea, dkk.,
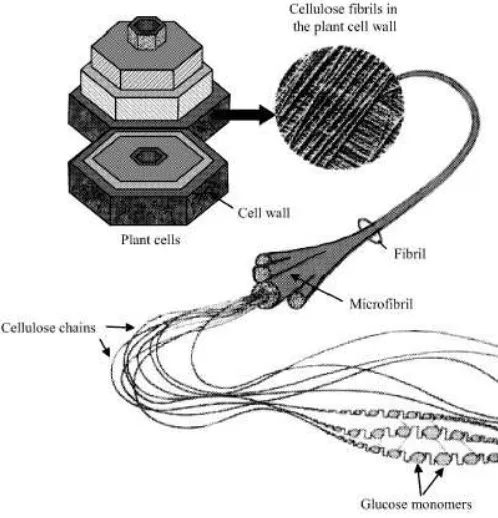
2011). Pada Gambar 2.2 dapat dilihat lapisan-lapisan dinding sel kayu dan
selulosa mikrofibril. Dinding sel kayu dibagi dalam beberapa lapisan yaitu lamela
tengah (LT), dinding sel primer (P), dan dinding sel sekunder (S) (dinding
sekunder terbagi dalam lapisanS1, S2, dan S3). Lapisan-lapisan ini mempunyai
struktur dan komposisi kimia yang berbeda.
Selulosa merupakan polimer yang relatif stabil dikarenakan adanya ikatan
hidrogen. Selulosa tidak larut dalam pelarut air dan tidak memiliki titik leleh.
Serat selulosa juga memiliki fleksibilitas dan elastisitas yang baik sehingga dapat
mempertahankan aspect ratio (perbandingan panjang terhadap diameter (P/d))
Serat selulosa dalam dinding sel tanaman
Sel tanaman
Dinding sel
Serat
Mikroserat
Monomer-monomer glukosa Rantai selulosa
S S1
S2 S3
P LT
keuntungan seperti: densitas rendah, sumber yang dapat diperbaharui,
biodegradable, mengurangi emisi karbondioksida di alam, kekuatan dan modulus
yang tinggi, permukaan yang relatif reaktif sehingga dapat digunakan untuk
grafting beberapa gugus kimia, dan harga yang murah (Frone, dkk., 2011).
Gambar 2.2. Kumpulan rantai selulosa dalam mikrofibril yang membentuk dinding sel tanaman (Modifikasi dari Djerbi, 2005).
2.1.3 Sumber Selulosa
Selulosa diisolasi dari dinding sel tanaman, bahan berkayu, rambut biji,
kulit pohon, dan tanaman laut. Serat kapas mengandung 95% selulosa, sedangkan
kayu 40-50% selulosa (Tabel 2.1). Jumlah selulosa dalam serat bervariasi menurut
sumbernya dan biasanya berkaitan dengan bahan-bahan seperti air, lilin, pektin,
protein, lignin dan substansi-substansi mineral. Selulosa yang diperoleh dari kayu
memerlukan proses yang panjang untuk menghilangkan hemiselulosa dan lignin
seperti tongkol jagung (Ohwoavworhua dan Adelakun, 2005b), rambut biji dari
Cochlospermum planchonii (Ohwoavworhua dan Adelakun, 2005a), ampas tebu
(Sun, dkk., 2004), jerami (Ilindra dan Dhake, 2008), lenan (Leppanen,dkk., 2009).
secara mekanis. Secara kimia proses pulping dapat dilakukan dengan proses sulfit,
basa, dan sulfat untuk melarutkan lignin dan hemiselulosa, dan meninggalkan
senyawa selulosa sebagai bentuk padatan. Proses sulfit menggunakan campuran
asam sulfit (H2SO3) dan ion bisulfit (HSO3-) untuk melarutkan lignin sebagai asam
lignosulfonat yang dapat larut dalam larutan pemasak. Pada proses basa kayu
dimasak dengan larutan NaOH. Proses sulfat (Kraft) menggunakan larutan NaOH
dan Na2S. Penggunaan kedua bahan ini akan meningkatkan delignifikasi dan
kekuatan pulp (Klemm, dkk., 1998a). Metode lain yang dapat digunakan untuk
delignifikasi adalah dengan metode ledakan uap (steam explosion). Pada metode
ini potongan kayu akan diberikan tekanan dan suhu yang tinggi dengan
menggunakan autoklaf (Othmer, 1993).
Sumber lain selulosa adalah hasil biosintesis selulosa oleh
mikroorganismeseperti bakteri, alga, dan jamur. Alga dan jamur menghasilkan
selulosa melalui sintesis in vitro secara enzimatik dari selobiosil fluorida, dan
kemosintesis dari glukosa dengan pembukaan cincin polimerisasi turunan benzil
dan pivaloyl. Dari ketiga mikroorganisme tersebut, hanya spesies Acetobacter
xylinum yang diketahui dapat menghasilkan selulosa dalam jumlah besar. Sumber
selulosa lain adalah dari hewan, yang disebut tunicin atau selulosa hewan karena
diperoleh dari organisme bahari tertentu dari kelas Tunicata (Gea, 2010).
2.1.4 Struktur Kristal dari Selulosa
Selulosa terdiri dari dua bagian yaitu amorf dan kristal. Selulosa dapat
ditemukan dalam bentuk mikrofibril kristalin selulosa I, II, III, dan IV. Fraksi
struktur selulosa bisa dilakukan dengan difraksi X-Ray, NMR, dan FTIR
(Klemm, dkk., 1998a; Gea, 2010).
Selulosa I merupakan bentuk asli selulosa yang terdiri dari dua kristal
allomorf, yaitu Iα dan Iβ. Berdasarkan pengujian difraksi elektron selulosa
Iαmemiliki satu unit sel triklinik, sedangkan selulosa Iβ memiliki dua unit sel
monoklinik, keduanya tersusun dalam satu susunan rantai paralel, dengan rasio
berbeda dalam satu serat, tergantung pada asalnya. Selulosa Iα banyak terdapat
pada selulosa bakteri dan valonia, sedangkan Iβ pada selulosa kapas atau kayu
(Klemm, dkk., 1998a).
Selain selulosa I, terdapat selulosa II yang terbentuk dengan pengendapan
selulosa dari larutan ke dalam medium air pada suhu kamar atau sedikit lebih
tinggi dari suhu kamar pada proses pemintalan serat selulosa buatan manusia
secara teknis. Selulosa II ini juga diperoleh dari proses merserisasi kapas, yang
terjadi melalui pembentukan natrium selulosa melalui interaksi polimer dengan
cairan natrium hidroksida dan peruraian dengan netralisasi atau penghilangan
natrium hidroksida. Proses transformasi dari selulosa I menjadi selulosa II
biasanya irreversible, walaupun ada yang menyatakan bahwa natrium selulosa
dapat diretransformasi sebagian menjadi selulosa I. Sistem ikatan hidrogen
selulosa II lebih rumit daripada selulosa I dan menghasilkan densitas tautan silang
Gambar 2.3. Difraktogram difraksi X-Ray dari selulosa dan selulosa nanokristal linter (Li, dkk., 2003).
Li, dkk. (2003) melakukan kondensasi selulosa alam (linter) yang
memiliki struktur kristal I dengan NaOH 18% dan menghasilkan struktur kristal
baru, yaitu struktur kristal II. Perlakuan terhadap selulosa nanokristal
(nanocrystalline cellulose, NCC) dengan struktur kristal I menggunakan NaOH
4% juga menghasilkan NCC dengan struktur kristal II. Struktur kristal selulosa
dan NCC dari penelitian Li, dkk. (2003) ini dapat dilihat pada Gambar 2.3.
Struktur selulosa III dan IV diturunkan dari selulosa I atau II, disebut
dengan selulosa IIII, IVI, dan IIIII dan IVII. Selulosa III diperoleh dari perlakuan
selulosa I atau II dengan cairan amoniak dibawah -30 oC dan rekristalisasi sampel
dengan evaporasi amoniak (Klemm, dkk., 1998a).
2.1.5 Biosintesis
Selulosa terdapat pada semua dinding sel tumbuhan. Tumbuhan darat
seperti pohon hutan dan kapas menyintesis selulosa dari glukosa, yang dihasilkan
dalam sel tanaman dengan cara fotosintesis. Senyawa ini juga dijumpai dalam
α-glukosa-6-P
Ada 3 (tiga) cara sintesis selulosa adalah sebagai berikut:
1. Biosintesis dalam organisme hidup
2. Sintesis enzimatik in vitro
3. Sintesis kimia dengan polimerisasi dari monomer yang sesuai (Klemm, dkk., 1998b).
Biosintesis selulosa merupakan proses yang sangat kompleks, tidak hanya
pada pembentukan rantai β-1,4-glukan, tetapi juga pada penetapan susunan
supramolekuler dan serat dalam polimer padat yang terbentuk. Mekanisme
pembentukan selulosa dianggap berbeda pada tumbuhan tinggi dan bakteri atau
alga. Biosintesis selulosa pada tumbuhan tinggi dapat dilihat pada Gambar 2.4.
Proses biosintesis diawali dengan konversi β-fruktosa-6-P menjadi
α-glukosa-6-fosfat oleh enzim glukosa-6-α-glukosa-6-fosfat isomerase, kemudian menjadi α-glukosa-1-P
oleh enzim fosfoglukomutase. α-glukosa-1-P diubah menjadi UDP (uridin
difosfatase)-glukosa oleh UTP (uridin trifosfatase)-glukosa-1-fosfat uridil
transferase. Dengan bantuan enzim selulosa sintase UDP-glukosa diubah menjadi
selulosa. Selain dari fruktosa, selulosa juga bisa dihasilkan dari sukrosa. Enzim
sukrosa sintase akan mengubah sukrosa menjadi UDP-glukosa, selanjutnya