LlMBAH CAIR YANG MENGANDUNG MELANOIDIN
Oleh
RIPTO WIDARGO F 28.1340
1996
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Ripto Widargo. F 28.1340. Kajian Kemampuan Bentonit untuk Ockoiorisasl Limbah Cair yang mcngandung Melanoidin. Oibawah bimbingan Muhammad Romli dan Muslich.
RINGKASAN
Melanoidin merupakan penyebab warna coklat kehitaman pada molases yang dihasilkan dari industri pembuatan gula dan ektraksi etanol dengan destilasi. Bila limbah cair molases yang mengandung melanoidin dibuang di perairan bebas. akan menyebabkan BOD dan COO meningkat dan menimbulkan warna coklat. Oalam penelitian ini benton it digunakan sebagai adsorben untuk menghilangkan warn a melanoidin secara adsorpsi.
Penelitian dilakukan terdiri dari dua tahap. yaitu penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan untuk menentukan waktu kontak optimal dan isoterm Freundlich adsorpsi masing-masing adsorben bentonit terhadap melanoidin sintetis. Melanoidin sintetis yang digunakan terbuat dari eampuran antara Glukosa ; Glisin ; Na2CO] (6 : 2.2 : 1.8) dengan perbandingan konsentrasi masing-masing l: l: 0.5 molar. sedangkan penelitian utama dilakukan pada sebuah kolom adsorpsi berukuran diameter 2.5 em dan bed adsorben setinggi 2 em. Ukuran mesh hed adsorben pada kolom adsorpsi untuk Koleang dan Kebon Awi adalah 8 mesh. Tonsil dan arang aktif masing-masing sebesar 200 dan 300 mesh. Debit influen melanoidin sintetis (60 gil) untuk Koleang dan Kebon Awi masing-masing sebesar 1.23 mllmenit. Tonsil dan arang aktif masing-masing sebesar 0.15 dan 0.13 mllmenit.
FAKUL TAS TEKNOLOGI PERTANIAN
KAJIAN KEMAMPUAN
BENTON IT
UNTUK
DEKOLORISASI LlMBAH CAIR YANG MENGANDUNG
MELANOIDIN
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN
pada Jurusan Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
RIPTO WIDARGO F 28.1340
Dilahirkan pada Tanggal19 Desember 1972 diBogor
Disetujui,
Bogor, Oktober 1996
0'
...
o·!
- " \'"" (J) ,
Ir. Muslich .,'.< .. セ@ セ@ '.Ir. Muhammad Romli, MSc
Dosen Pembimbing
1)'''<> , ,
.' ..
Dosen Pembimbing I '. \ «"-t .... セセセL|LGセ|ャNLセ@"'":::----KAT A PENGANT AR
I'uji syukur dipanjatkan kepada Allah S.W.T. atas segal a Rahmat dan Karunia-Nya
sehingga penuIis dapat menyelesaikan penyusunan skripsi. Skripsi ini ditulis berdasarkan
hasil penelitian yang dilakukan di laboratorium Jurusan Teknologi Industri Pertanian.
Institut Pertanian Bogor selama tujuh bulan (Januari sid Juli 1996).
Penyusunan skripsi ini tidak teriepas dari batuan semua pihak. Untuk itu penulis
menyampaikan ucapan terima kasih kepada :
I. Ayah dan Ibu serta saudara-saudaraku yang telah memberikan dukungan baik moril
maupun materil.
2. Dr. Ir. Muhammad Romli, MSc. sebagai dosen pembimbing I yang telah membimbing
penulis menyelesaikan skripsi ini.
3. Ir. Muslich sebagai dosen pembimbing II yang telah membimbing penulis dalam
menyelesaikan skripsi ini.
4. Dr. Ir. Nastiti Siswi Indrasti sebagai dosen penguJI yang telah banyak memberikan
masukan untuk penulisan skripsi ini.
5. Ir. Tika Kartika yang selalu memberikan perhatian. nasehat. semangat dan dorongan.
6. Ir. Arief, Iwan Ramos, Ir. Sujudi, Ir. Eki, Ir. Rio. Ir. Ozi. Ir. Aldo, Sulis, Iskandar dan
rckan-rekan di YYZ.
7. Semua pihak yang tidak bisa disebutkan satu persatu seeara langsung maupun tidak
langsung dalam penyelesaian skripsi ini.
Kritik dan saran yang konstruktif diperlukan untuk penyempurnaan penyusunan
skripsi ini. karella penulis menyadari bahwa skripsi ini jauh dari sempurna. Scmoga
skripsi ini berguna bagi penulis dan bagi semua yang memeriukanllya.
KATA PENGANTAR ..
OAFTAR GAMBAR ..
DAFTAR TABEL.. DAFTAR LAMPIRAN II III IV PENDAHULUAN ..
A LATAR BELAKANG ..
B. TUJUAN ... .
TINJAUAN PUSTAKA
A BENTONIT.
B. MELANOIDIN
c.
KONSEP ADSORPSI ... . D. PENANGANAN LlMBAH CAIR ..BAHAN DAN METODE ..
A BAHAN DAN ALA T ...
1. Bahan ...
2. Alat.. . ... .
B. METODE PENELITIAN ....
1. Penelitian Pendahuluan
a. Penetapan Panjang Gelombang Maksimum Melanoidin ..
b. Penetapan Kurva Standar Konsentrasi Melanoidin ..
c Penentuan waktu kontak ..
d Penentuan nilai K,dan 1/n ...
2. Penelitian Utama ..
HASIL DAN PEMBAHASAN ...
A PENELITIAN PENDAHULUAN ... .
1. Penentuan Waktu Kontak Optimal ..
2. Penentuan Nilai K, dan 1/n ..
B. PENELITIAN UTAMA.
1. Kondisi Operas; ..
2. Waktu Kontak ...
3. Volume dan Konsentrasi pad a saat Breakpoint ..
4. Estlmasl Blaya Operasi dan Kebutuhan Bentonlt Minimum pada
Sistem Kolom Adsorpsi dengan Debit 1 m3/meniL ..
v
KESIMPULAN DAN SARAN ..A KESIMPULAN.
B. SARAN ..
DAFTAR PUSTAKA ....
LAMPIRAN
111
35
37
37
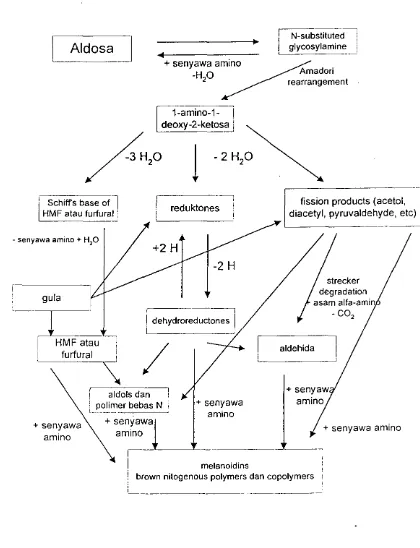
Halaman Gambar 1. Skema reaksi browning non enzimatik dalam pembentukan
melanoid in .. 6
Gambar 2. Kurva hubungan antara waktu kontak dan konsentrasi
akhir yang dicapai . 8
Gambar 3. Kurva kejenuhan kolom adsorpsi Fixed Bed ... 11
Gambar 4. Kurva adsorpsi bentonitjenis Tonsil terhadap melanoidin .. 19
Gambar 5 Kurva adsorpsi bentonit jenis Koleang terhadap melanoidin .... 19
Gambar 6. Kurva adsorpsi bentonit jenis Kebon Awi terhadap melanoidin 20
Gambar 7. Kurva adsorpsi Arang aktif terhadap melanoidin . 20
Gambar 8. Kurva Isoterm Freundlich untuk berbagai adsorben. 23
Gambar 9. Kurva kejenuhan kolom adsorpsi bentonit Koleang
sebagai hubungan antara waktu kontak dan rasio Ce/Ci ... 27
Gambar 10 Kurva kejenuhan kolom adsorpsi bentonit Kebon Awi
sebagai hubungan antara waktu kontak dan rasio Ce/Ci .. 27
Gambar 11 Kurva kejenuhan kolom adsorpsi bentonit Tonsil
sebagai hubungan antara waktu kontak dan rasio Ce/Ci.. 29
Gambar 12. Kurva kejenuhan kolom adsorpsi arang aktif
sebagai hubungan antara waktu kontak dan rasio Ce/Ci 29
Gambar 13. Kurva kejenuhan kolom adsorpsi bentonit Koleang
sebagai hubungan antara volume efluen dan rasio Ce/Ci . 33
Gambar 14. Kurva kejenuhan kolom adsorpsi benton it Kebon Awi
sebagai hubungan antara volume efluen dan rasio Ce/Ci ... 33
Gambar 15. Kurva kejenuhan kolom adsorpsi bentonit Tonsil
sebagai hubungan antara volume efiuen dan rasio Ce/Ci 34
Gambar 16. Kurva kejenuhan kolom adsorpsi arang aktif
sebagai hubungan antara volume efluen dan rasio Ce/Ci. 35
DAFTAR TABEL
Halaman Tabel 1. Komposisi kimiawi dan komponen mineral benton it Koleang dan
セセョセゥ@ ... 3
Tabel 2. Pendekatan formula empirik melanoid in . 7
Tabel 3. Nilai K, dan 1/n berbagai adsorben ... 22
Tabel 4 Kondisi operasi sistem kolom adsorpsi berbagai bed adsorben .... 25
Tabel 5. Kemampuan adsorpsi maksimum dan breakpoint waktu.. 26
Tabel 6. Nilai Vb dan Cb berbagai adsorben pada sistem kolom adsorpsi.. 31
Tabel 7. Estimasi kebutuhan adsorben, biaya dan dimensi kolom adsorpsi pad a konsentrasi awal 60 g/l dan debit 1 m3/menit
(1440 m3/hari) tanpa regenerasi adsorben. 36
Lampiran 1
Lampiran 2
Lampiran 3.
Lampiran 4.
Lampiran 5.
Lampiran 6.
Lampiran 7.
Lampiran 8.
Lampiran 9.
Penentuan panjang gelombang (i.) berdasarkan persen transmiten dan adsorbansi bagi Melanoidin ..
Kurva standar konsentrasi melanoidin.
Evaluasi waktu kontak berdasarkan persen dekolorisasi ... .
Uji statistik terhadap evaluasi waktu kontak .... .
Data penentuan Isoterm Freundlich .. ... .
Data hasil pengukuran kolom adsorpsi berbagai adsorben ..
Halaman
41
42
43
44
46
47
Estimasi dimensi kolom, kebutuhan adsorben dan biaya pad a debit 1
m'/meniL 49
Metoda penelitian pendahuluan untuk penentuan waktu kontak
セゥュオュ@ ... 55
Desain kolom adsorpsi yang dlgunakan untuk memucatkan
melanoidin... 56
I. PENDAHULUAN
A. LATAR BELAKANG
Molases merupakan produk sampingan dari proses pembuatan gula. rum
dan ekstraksi alkohol dengan destilasi. Warna coklat kehitaman pada molases
merupakan komponen melanoidin. Melanoidin merupakan komponen yang
terbentuk dari reaksi non-enzymatic Maillard antara gula dan asam amino.
Apabila molases dibuang ke perairan bebas akan menyebabkan tingginya nilai
COD dan BOD perairan tersebut. Pembuangan molases ke permran Juga
menyebabkan penampakan fisik warna air yang tidak dikehendaki.
Beberapa penelitian telah dilakukan untuk menghilangkan warna
meianoidin melaiui degradasi biologis. Penanganan iimbah cair secara biologis
hanya mampu l11enurunkan warna limbah cair molases hingga 18 persen (Nugraha.
1995). Dalam proses pemucatan terhadap komponen warna tertentu. biasanya
digunakan arang aktiC namun bentonit diketahui memiliki sifat menyerap terutama
jcnis yang tidak l11engembang dalam air (non swelling). Dalam penelitian ini
bentonit jenis Koieang. Kebon Awi dan Tonsil digunakan untuk menghilangkan
kOl11ponen warna melanoidin l11elalui mekanisl11e adsorpsi.
Penelitian dilakukan untuk menilai kcmampuan bcntonit. terutama Jellls
Koleang. Kebon Awi dan Tonsil dalam mengadsorpsi warna pad a melanoidin.
Untuk keperiuan anal isis. digunakan melanoidin sintetis yang terbuat dari
campuran antara I molar glukosa.
perbandingan 6 : 2.2 : 1.8 dalam
molar glisin dan 0.5 molar Na2CO, dengan
liter larutan. Call1puran terse but kel11udian
diotoklaf selama 3 jam dan didialisis selama empat hari dengan air bebas Ion.
LlMBAH CAIR YANG MENGANDUNG MELANOIDIN
Oleh
RIPTO WIDARGO F 28.1340
1996
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Ripto Widargo. F 28.1340. Kajian Kemampuan Bentonit untuk Ockoiorisasl Limbah Cair yang mcngandung Melanoidin. Oibawah bimbingan Muhammad Romli dan Muslich.
RINGKASAN
Melanoidin merupakan penyebab warna coklat kehitaman pada molases yang dihasilkan dari industri pembuatan gula dan ektraksi etanol dengan destilasi. Bila limbah cair molases yang mengandung melanoidin dibuang di perairan bebas. akan menyebabkan BOD dan COO meningkat dan menimbulkan warna coklat. Oalam penelitian ini benton it digunakan sebagai adsorben untuk menghilangkan warn a melanoidin secara adsorpsi.
Penelitian dilakukan terdiri dari dua tahap. yaitu penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan untuk menentukan waktu kontak optimal dan isoterm Freundlich adsorpsi masing-masing adsorben bentonit terhadap melanoidin sintetis. Melanoidin sintetis yang digunakan terbuat dari eampuran antara Glukosa ; Glisin ; Na2CO] (6 : 2.2 : 1.8) dengan perbandingan konsentrasi masing-masing l: l: 0.5 molar. sedangkan penelitian utama dilakukan pada sebuah kolom adsorpsi berukuran diameter 2.5 em dan bed adsorben setinggi 2 em. Ukuran mesh hed adsorben pada kolom adsorpsi untuk Koleang dan Kebon Awi adalah 8 mesh. Tonsil dan arang aktif masing-masing sebesar 200 dan 300 mesh. Debit influen melanoidin sintetis (60 gil) untuk Koleang dan Kebon Awi masing-masing sebesar 1.23 mllmenit. Tonsil dan arang aktif masing-masing sebesar 0.15 dan 0.13 mllmenit.
FAKUL TAS TEKNOLOGI PERTANIAN
KAJIAN KEMAMPUAN
BENTON IT
UNTUK
DEKOLORISASI LlMBAH CAIR YANG MENGANDUNG
MELANOIDIN
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN
pada Jurusan Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
RIPTO WIDARGO F 28.1340
Dilahirkan pada Tanggal19 Desember 1972 diBogor
Disetujui,
Bogor, Oktober 1996
0'
...
o·!
- " \'"" (J) ,
Ir. Muslich .,'.< .. セ@ セ@ '.Ir. Muhammad Romli, MSc
Dosen Pembimbing
1)'''<> , ,
.' ..
Dosen Pembimbing I '. \ «"-t .... セセセL|LGセ|ャNLセ@"'":::----KAT A PENGANT AR
I'uji syukur dipanjatkan kepada Allah S.W.T. atas segal a Rahmat dan Karunia-Nya
sehingga penuIis dapat menyelesaikan penyusunan skripsi. Skripsi ini ditulis berdasarkan
hasil penelitian yang dilakukan di laboratorium Jurusan Teknologi Industri Pertanian.
Institut Pertanian Bogor selama tujuh bulan (Januari sid Juli 1996).
Penyusunan skripsi ini tidak teriepas dari batuan semua pihak. Untuk itu penulis
menyampaikan ucapan terima kasih kepada :
I. Ayah dan Ibu serta saudara-saudaraku yang telah memberikan dukungan baik moril
maupun materil.
2. Dr. Ir. Muhammad Romli, MSc. sebagai dosen pembimbing I yang telah membimbing
penulis menyelesaikan skripsi ini.
3. Ir. Muslich sebagai dosen pembimbing II yang telah membimbing penulis dalam
menyelesaikan skripsi ini.
4. Dr. Ir. Nastiti Siswi Indrasti sebagai dosen penguJI yang telah banyak memberikan
masukan untuk penulisan skripsi ini.
5. Ir. Tika Kartika yang selalu memberikan perhatian. nasehat. semangat dan dorongan.
6. Ir. Arief, Iwan Ramos, Ir. Sujudi, Ir. Eki, Ir. Rio. Ir. Ozi. Ir. Aldo, Sulis, Iskandar dan
rckan-rekan di YYZ.
7. Semua pihak yang tidak bisa disebutkan satu persatu seeara langsung maupun tidak
langsung dalam penyelesaian skripsi ini.
Kritik dan saran yang konstruktif diperlukan untuk penyempurnaan penyusunan
skripsi ini. karella penulis menyadari bahwa skripsi ini jauh dari sempurna. Scmoga
skripsi ini berguna bagi penulis dan bagi semua yang memeriukanllya.
KATA PENGANTAR ..
OAFTAR GAMBAR ..
DAFTAR TABEL.. DAFTAR LAMPIRAN II III IV PENDAHULUAN ..
A LATAR BELAKANG ..
B. TUJUAN ... .
TINJAUAN PUSTAKA
A BENTONIT.
B. MELANOIDIN
c.
KONSEP ADSORPSI ... . D. PENANGANAN LlMBAH CAIR ..BAHAN DAN METODE ..
A BAHAN DAN ALA T ...
1. Bahan ...
2. Alat.. . ... .
B. METODE PENELITIAN ....
1. Penelitian Pendahuluan
a. Penetapan Panjang Gelombang Maksimum Melanoidin ..
b. Penetapan Kurva Standar Konsentrasi Melanoidin ..
c Penentuan waktu kontak ..
d Penentuan nilai K,dan 1/n ...
2. Penelitian Utama ..
HASIL DAN PEMBAHASAN ...
A PENELITIAN PENDAHULUAN ... .
1. Penentuan Waktu Kontak Optimal ..
2. Penentuan Nilai K, dan 1/n ..
B. PENELITIAN UTAMA.
1. Kondisi Operas; ..
2. Waktu Kontak ...
3. Volume dan Konsentrasi pad a saat Breakpoint ..
4. Estlmasl Blaya Operasi dan Kebutuhan Bentonlt Minimum pada
Sistem Kolom Adsorpsi dengan Debit 1 m3/meniL ..
v
KESIMPULAN DAN SARAN ..A KESIMPULAN.
B. SARAN ..
DAFTAR PUSTAKA ....
LAMPIRAN
111
35
37
37
Halaman Gambar 1. Skema reaksi browning non enzimatik dalam pembentukan
melanoid in .. 6
Gambar 2. Kurva hubungan antara waktu kontak dan konsentrasi
akhir yang dicapai . 8
Gambar 3. Kurva kejenuhan kolom adsorpsi Fixed Bed ... 11
[image:17.608.105.504.129.545.2]Gambar 4. Kurva adsorpsi bentonitjenis Tonsil terhadap melanoidin .. 19
Gambar 5 Kurva adsorpsi bentonit jenis Koleang terhadap melanoidin .... 19
Gambar 6. Kurva adsorpsi bentonit jenis Kebon Awi terhadap melanoidin 20
Gambar 7. Kurva adsorpsi Arang aktif terhadap melanoidin . 20
Gambar 8. Kurva Isoterm Freundlich untuk berbagai adsorben. 23
Gambar 9. Kurva kejenuhan kolom adsorpsi bentonit Koleang
sebagai hubungan antara waktu kontak dan rasio Ce/Ci ... 27
Gambar 10 Kurva kejenuhan kolom adsorpsi bentonit Kebon Awi
sebagai hubungan antara waktu kontak dan rasio Ce/Ci .. 27
Gambar 11 Kurva kejenuhan kolom adsorpsi bentonit Tonsil
sebagai hubungan antara waktu kontak dan rasio Ce/Ci.. 29
Gambar 12. Kurva kejenuhan kolom adsorpsi arang aktif
sebagai hubungan antara waktu kontak dan rasio Ce/Ci 29
Gambar 13. Kurva kejenuhan kolom adsorpsi bentonit Koleang
sebagai hubungan antara volume efluen dan rasio Ce/Ci . 33
Gambar 14. Kurva kejenuhan kolom adsorpsi benton it Kebon Awi
sebagai hubungan antara volume efluen dan rasio Ce/Ci ... 33
Gambar 15. Kurva kejenuhan kolom adsorpsi bentonit Tonsil
sebagai hubungan antara volume efiuen dan rasio Ce/Ci 34
Gambar 16. Kurva kejenuhan kolom adsorpsi arang aktif
sebagai hubungan antara volume efluen dan rasio Ce/Ci. 35
DAFTAR TABEL
Halaman Tabel 1. Komposisi kimiawi dan komponen mineral benton it Koleang dan
セセョセゥ@ ... 3
Tabel 2. Pendekatan formula empirik melanoid in . 7
Tabel 3. Nilai K, dan 1/n berbagai adsorben ... 22
Tabel 4 Kondisi operasi sistem kolom adsorpsi berbagai bed adsorben .... 25
Tabel 5. Kemampuan adsorpsi maksimum dan breakpoint waktu.. 26
Tabel 6. Nilai Vb dan Cb berbagai adsorben pada sistem kolom adsorpsi.. 31
Tabel 7. Estimasi kebutuhan adsorben, biaya dan dimensi kolom adsorpsi pad a konsentrasi awal 60 g/l dan debit 1 m3/menit
(1440 m3/hari) tanpa regenerasi adsorben. 36
Lampiran 1
Lampiran 2
Lampiran 3.
Lampiran 4.
Lampiran 5.
Lampiran 6.
Lampiran 7.
Lampiran 8.
Lampiran 9.
Penentuan panjang gelombang (i.) berdasarkan persen transmiten dan adsorbansi bagi Melanoidin ..
Kurva standar konsentrasi melanoidin.
Evaluasi waktu kontak berdasarkan persen dekolorisasi ... .
Uji statistik terhadap evaluasi waktu kontak .... .
Data penentuan Isoterm Freundlich .. ... .
Data hasil pengukuran kolom adsorpsi berbagai adsorben ..
Halaman
41
42
43
44
46
47
Estimasi dimensi kolom, kebutuhan adsorben dan biaya pad a debit 1
m'/meniL 49
Metoda penelitian pendahuluan untuk penentuan waktu kontak
セゥュオュ@ ... 55
Desain kolom adsorpsi yang dlgunakan untuk memucatkan
melanoidin... 56
I. PENDAHULUAN
A. LATAR BELAKANG
Molases merupakan produk sampingan dari proses pembuatan gula. rum
dan ekstraksi alkohol dengan destilasi. Warna coklat kehitaman pada molases
merupakan komponen melanoidin. Melanoidin merupakan komponen yang
terbentuk dari reaksi non-enzymatic Maillard antara gula dan asam amino.
Apabila molases dibuang ke perairan bebas akan menyebabkan tingginya nilai
COD dan BOD perairan tersebut. Pembuangan molases ke permran Juga
menyebabkan penampakan fisik warna air yang tidak dikehendaki.
Beberapa penelitian telah dilakukan untuk menghilangkan warna
meianoidin melaiui degradasi biologis. Penanganan iimbah cair secara biologis
hanya mampu l11enurunkan warna limbah cair molases hingga 18 persen (Nugraha.
1995). Dalam proses pemucatan terhadap komponen warna tertentu. biasanya
digunakan arang aktiC namun bentonit diketahui memiliki sifat menyerap terutama
jcnis yang tidak l11engembang dalam air (non swelling). Dalam penelitian ini
bentonit jenis Koieang. Kebon Awi dan Tonsil digunakan untuk menghilangkan
kOl11ponen warna melanoidin l11elalui mekanisl11e adsorpsi.
Penelitian dilakukan untuk menilai kcmampuan bcntonit. terutama Jellls
Koleang. Kebon Awi dan Tonsil dalam mengadsorpsi warna pad a melanoidin.
Untuk keperiuan anal isis. digunakan melanoidin sintetis yang terbuat dari
campuran antara I molar glukosa.
perbandingan 6 : 2.2 : 1.8 dalam
molar glisin dan 0.5 molar Na2CO, dengan
liter larutan. Call1puran terse but kel11udian
diotoklaf selama 3 jam dan didialisis selama empat hari dengan air bebas Ion.
B. TUJUAN
Tujuan penelitian ini adalah mengkaji kemampuan bentonit jenis Koleang,
Kebon Awi dan Tonsil untuk mengadsorpsi warna pada limbah cair yang
mengandung melanoidin dan melakukan estimasi terhadap biaya preparasi
II. TINJAUAN PUSTAKA
A. BENTON IT
Bentonit adalah nama perdagangan untuk sejenis lempung yang
mengandung lebih dari 85 persen mineral monmorilonit (Grim, 1968). Rumus
kimia penyusun monmorillonite adalah AI203.4Si02.5H20.
Bentonit adalah sejenis tanah pemucat yang mempunyai sifat daya serap
yang aktif baik dalam bentuk alami maupun setelah proses pengaktifan.
Berdasarkan teori Davis dan Messer, keaktifan suatu tanah pemucat tergantung
dari rasio Si02 dengan A1203. Bila rasio itu cukup besar maka daya serapnya
semakin besar. Selain itu tanah pemucat yang baik adalah tanah yang tidak
mengandung garam-garaman yang lamt dalam air serta mempunyai derajat
keasaman sekitar pH 6.5 - 7.5. Komposisi kimia dan komposisi mineral bentonit
Koleang dan Kebon Awi disajikan pada Tabel 1.
Tabel I. Komposisi kimiawi dan komponen mineral bentonit Koleang dan Kebon Awi *.
Jenis Bentonit Komposisi kimiawi -(persen) Komponen mineral
Si02 AI203
Koleang 58.55 20.30 Montmoril1onite, Kuarsa
Kebon Awi 52.7 25.15 Montmoril1onite. Kuarsa. Mika dan Kristoballite
*Wldlastutl, (1995).
Komposisi monmorilonit berbeda dari bentonit yang satu dengan yang
lainnya, kandungan elemennya tergantung pada proses terbentuknya di alam.
I. Berwarna dasar putih dengan sedikit kecoklatan atau kemerahan tergantung
dari j enis dan fragmen mineral yang dikandungnya.
2. Bersifat sangat lunak, ringan, mudah pecah terasa seperti sabun, mudah
menyerap air dan dapat dipakai sebagai penukar ion (ion exchange).
3. Beratjenis bentonit berkisar antara 2.4 - 2.8 g/cm3 (Anonim, 1987).
Menurut Anwar et aI., (1983), bentonit pada umumnya dapat digolongkan
dalam dua jenis :
I. lenis yang volumenya tidak mengembang di dalam air, atau disebut Ca-Mg
bentonit. Bentonit ini digunakan sebagai pengisap dan zat pembawa dan zat
pemisah dalam penghilangan minyak bumi, zat pemutih (penghilang warna).
2. lenis yang volumenya dapat mengembang di dalam air, atau disebut sebagai
Na-bentonit yang digunakan sebagai lumpur pembilas dalam pengeboran.
Jenis kalsium-magnesium bentonit mengandung relatif lebih banyak IOn
Mg dan Ca dibanding ion Na, sifatnya dapat menyerap air (tidak membentuk
suspensi) dan pH-nya adalah sekitar 4 - 7. Natrium bentonit mengandung relatif
lebih banyak ion Na dibandingkan ion Mg dan Ca. Suspensi dari bentonit ini
didalam air mempunyai kisaran pH antara 8.5 - 9.8 (Anonim, 1987).
Aktivasi dilakukan terhadap bentonit untuk mengurangi kadar air, sehingga
diharapkan daya serap bentonit optimal. Kondisi suhu aktivasi dengan
pemanasan yang optimal untuk bentonit dari jenis Koleang adalah 50°C selama 4
jam, sedangkan untuk jenis yang berasal dari Kebon Awi pada suhu 200°C
selama 6 jam. Proses aktivasi meningkatkan kandungan silika bentonit Koleang
dari 58.55 persen menjadi 60.50 persen, dan bentonit Kebon Awi dari 52.70
persen menjadi 55.95 persen (Widiastuti, 1995).
Bahan yang dapat dipakai sebagai adsorben dalam khromatografi
cairan-padatan tidak banyak dan yang paling dikenal adalah silika gel (.')i02) dan
alumina HaャャoセN@ Daya adsorpsi dari bahan tergantung dari sifat kimia
5
Aktivitas alumina dapat diatur dengan mengubah kandungan airnya. Adsorben
ini dapat dikeringkan selama 5 jam pada suhu 3600
C dan membiarkan bahan
kering ini menyerap sejumlah tertentu air (Nur dan Adijuwana, 1989).
B. MELANOIDIN
Melanoidin adalah suatu senyawa organik yang terbentuk dari reaksi non-enzymatic Maillard antara gula dan asam amino. Melanoidin sintetis dibuat dengan melarutkan I molar glukosa, I molar glisin dan 0.5 molar Na2CO]
dengan perbandingan 6: 2.2 : 1.8 dalam I liter air bebas ion dan diotoklaf
selama 3 jam. Melanoidin adalah senyawa turunan dari asam amino yang
memiliki sifat asam yang disebabkan oleh keberadaan gugus hidroksil enolie dan gugus karboksil (Davidek et aI., 1990).
Pembentukan pigmen coklat dan melanoidin pertama kali ditemukan oleh
ahli kimia Prancis Louis Maillard pada tahun 1912 dengan memanaskan larutan
yang mengandung glukosa dan asam amino lisin. Reaksi tersebut melibatkan
gugus amino dan gugus karbonil yang biasa terdapat pada bahan pangan. Secara
umum reaksi pembentukan melanodin dapat dilihat pada Gambar I. (Eskin,
1990).
Struktur kimia dan karakteristik melanoidin secara lengkap dan pasti belum
diketahui, untuk kebutuhan anal isis digunakan melanoidin sintetis yang telah
diketahui bermuatan negatif, memiliki kelarutan yang tinggi di dalam air, non
volatil dan memiliki adsorpsi maksimum pada panjang gelombang 297 nm.
Rumus empirik melanoidin tergantung dari komponen pembentuknya dapat
tampak pada Tabel2. (Migo et aI., 1993b).
Sifat secara kimiawi dan fisiologi, melanoidin merupakan senyawa yang
AldosaJ
N-Substitutedl glycosylamin".J
-H 0 Amadori
+ senyawa 。セゥョッ@
2 rearrangement
1-amino-1-
I
、・ックケMRMォ・エッウセ@
/ H , o
1
-2H,o
I
Schiffs base ofl
HMF atau furfura!J reduktones
fission products (acetol, diacetyl, pyruvaldehyde, etc) .
-senyawa amino + H20
+2 H
-2 H
gula
I
i」Mh」」mM」f]M。Mエ。MオMlセ@
! furfural...J
I ,
I
dehydroreductonesI
I I
/
+ senyawa amino
\
aldols dan polimer bebas N i
+ senyawa amino
+ senyawa amino
L.. _ _ _ _ _ _ _ _ _ _ _
strecker degradation
a5am alfa-amin
- CO,
aldehida
+ senyaw
amino
+ senyawa amino
!
melanoid ins I: brown nitogenous polymers dan copolymers ;
L ______________ . ________ _
[image:25.600.100.520.104.652.2]7
merupakan hasil dari reaksi antara gula dengan gugus karbonil yang mengandung
asam amino melalui ikatan nitrogen (Davidek et aI., 1990).
Tabel 2. Pendekatan formula empiris melanoidin.
Struktur kimia empiris Sumber melanoidin
C6H6402N(CH2)(C02H)05 GIukosa : Glisin
=
I : 10(CnHI3sN057lJO.6 I M Glukosa : I M Glisin : 0.2 M Natrium bikarbonat (6 : 3 : 1)
C I7_IS H26_2701ON Dialisis molases tebu
C. KONSEP ADSORPSI
Adsorpsi secara umum didefinisikan sebagai suatu proses pengumpulan
bahan tedarut dalam suatu sistem larutan pada bagian interface (antar-muka)
yang bersesuaian. Antar muka tersebut dapat berupa antara cairan dan gas,
padatan atau cairan lainnya. Tahapan proses adsorpsi terdiri dari 3 tahapan ; makrotransport, mikrotransport dan sorpsi. Makrotransport melibatkan gerakan
bahan organik ke lapisan antar permukaan padatan-Iarutan melalui difusi.
Mikrotransport melibatkan mekanisme difusi bahan organik melewati sistem
makropori ke bidang adsorpsi pada permukaan granula adsorben. Tahapan
terakhir adalah sorpsi, apabila laju sorpsi sama dengan laju desorpsi maka
kesetimbangan adsorpsi telah dicapai (Metcalf dan Eddy, 1991).
Adsorpsi secara umum dapat digolongkan dalam tiga tipe, yaitu secara
fisik, kimiawi dan adsorpsi pertukaran ion (exchange adsorpsion). Adsorpsi secara fisik disebabkan oleh gaya tarik yang lemah atau gaya Van der Walls
antara kedua molekul. Molekul yang diadsorpsi bebas bergerak di sekitar
permukaan adsorben. Adsorpsi secara fisik umumnya bersifat reversibel,
normal senyawa yang diadsorpsi membentuk lapisan di atas permukaan adsorben
pada ketebalan tertentu. Sifat molekul yang diadsorpsi tidak dapat bergerak
bebas dari sisi yang satu ke sisi yang lain dari permukaan adsorben, bila
permukaan adsorben diselubungi oleh lapisan molekul sejenis (monomoleculer), maka kapasitas adsorben telah mencapai jenuh. Adsorpsi kimiawi seperti ini
jarang bersifat reversibel. Exchange adsorpsion merupakan mekanisme adsorpsi yang disebabkan oleh gaya tarik listrik antara adsorbat dan adsorben. proses
penukaran ion merupakan salah satu bentuk Exchange adsorpsion. Ion dari substansi adsorbat mengumpul pada permukaan melalui gaya elektrostatik
terhadap muatan listrik yang berbeda. Ion dengan muatan yang lebih besar
seperti halnya ion trivalen akan memiliki gaya tarik listrik yang lebih besar bi la
dibanding ion yang muatannya lebih kecil terhadap muatan yang berbeda
(Sawyer and McCarty, 1978).
Waktu kontak untuk mencapai kesetimbangan adsorpsi pertama kali harus
dievaluasi. Evaluasi awal dengan menguji waktu kontak 24 jam. apabila nilai
kesetimbangan setelah 2 jam waktu kontak lebih besar 90 persen dari nilai waktu
kontak 24 jam, maka waktu kontak 2 jam dapat digunakan sebagai acuan
lamanya kontak. Hubungan antara waktu kontak dan konsentrasi akhir adsorbat
yang dicapai dapat dilihat pada Gambar 2. (Eckenfelder, 1989).
Konsentrasi akhir adsorbat (persen)
o
'---t----i'---t-I t-Waktu kontak
9
lumlah adsorbat yang diserap oleh adsorben merupakan fungsi dari
konsentrasi adsorbat dan suhu. Umumnya jumlah bahan yang diserap dihitung
sebagai fungsi dari konsentrasi pada temperatur tetap. Secara matematik oleh
Freundlich telah dikembangkan dan dapat dinyatakan sebagai berikut :
(x/m) = Kf . el/n
dim ana :
x
=
jumlah zat yang diadsorpsi (gram)m
=
jumlah adsorben (gram)e
= konsentrasi zat yang terlarut sisa setelah proses adsorpsipada keadaan setimbang (gram/liter)
Kf (l/gram) dan lin adalah konstanta empiris
(Metcalf dan Eddy, 1991).
N ilai Kr berhubungan dengan kapasi tas adsorpsi, dan lin merupakan indikator dari intensitas adsorpsi. Menurut Eckenfelder (1981) kegunaan isoterm
Freundlich adalah memberikan informasi cukup penting, antara lain:
I. memberikan gambaran mengenai adsorbilitas atau afinitas relatif suatu
komponen adsorben tertentu
2. jumlah adsorben yang dibutuhkan pada pencapaian kesetimbangan adsorpsi
3. untuk mengetahui derajat penyerapan adsorben pada saat pencapaian
kesetimbangan adsorpsi.
Selanjutnya dikatakan bahwa isoterm Langmuir lebih teoritis bila
digunakan dalam adsorpsi pada fasa gas. kadang-kadang dipergunakan dalam
aplikasi terhadap penanganan limbah. Rumusan yang paling umum digunakan
untuk adsorpsi adalah isoterm Freundlich.
Kapasitas adsorpsi pada saat tepat akan jenuh (x/m)b pada skala penuh dari
sistem kolom adsorpsi tunggal dapat diasumsikan mendekati 25 sampai 50 persen
jenuh diketahui, maka waktu breakthrough (tb) dapat dihitung dengan asumsi
konsentrasi influen tetap dan kenaikan konsentrasi efluen linier sampai pada
konsentrasi breakthrough (Cb) sebagai berikut :
(Xlm)bM tb=
-Q[(Ci - Cb I 2)]
dimana:
(Xlm)b isoterm Freundlich bagi adsorben (gIg)
Q
=
laju alir influen yang masuk ke kolom (ml/menit)tb
=
waktu proses yang diperlukan sampai adsorbentepat saat akanjenuh (menit)
Ci
=
konsentrasi influen yang masuk ke kolom (gIl)Cb konsentrasi efluen yang keluar dari kolom pada saat
tepat akan jenuh (gIl)
M
=
massa dari adsorben yang digunakan (gram)(Metcalf dan Eddy, 1991).
Breakpoint didifinisikan sebagai titik volume atau waktu dimana cairan yang dilewatkan pada kolom adsorpsi tepat saat konsentrasi efluen akan
mencapal maksimum. bila zone adsorpsi bergerak ke bagian bawah hed adsorben, konsentrasi efluen meningkat secara linier hingga breakpoint dan akhirnya konsentrasi efluen sarna dengan konsentrasi influen seperti yang
disajikan pada Gambar 3. Titik kejenuhan akan semakin cepat dicapai apabila
ketinggian bed diperkecil, ukuran partikel adsorben. laju alir influen dan
II
Ce/Ci 1.0
0.5
Breakpoint
o
Waktu atau VolumeGambar 3. Kurva kejenuhan kolom adsorpsifixed bed (Eckenfelder, 1981).
D. PENANGANAN LlMBAH CAlR
Penanganan limbah cair secara umum dapat dibagi menjadi tiga bagian
utama yaitu penanganan primer, sekunder dan tersier. Pada penanganan primer
limbah cair dipersiapkan untuk memasuki penanganan biologis, terdiri dari tahap
penyaringan (screening) untuk memisahkan padatan yang berukuran besar dan
pasir, tahap equalisasi untuk menyeragamkan variasi konsentrasi dan laju alir,
tahap netralisasi diperlukan setelah proses equalisasi untuk mencapai pH yang
dikehendaki. tahap flotasi bertujuan untuk memisahkan bahan minyak dan lemak
serta padatan tersuspensi, dan terakhir adalah tahap sedimentasi dan filtrasi.
Penanganan sekunder adalah proses degradasi biologis melalui proses lumpur
aktif. Setelah melalui proses degradasi ini mikroorganisme dan padatan yang
terbawa dalam lumpur diendapkan, sebagian lumpur dikembalikan pada proses
tertentu, tetapi akan dibuang pada akhir proses (Eckenfelder, \989).
Selanjutnya, penanganan secara tersier diperlukan setelah penanganan
biologis agar menghilangkan tipe-tipe residu tertentu, seperti logam-logam be rat
dirasa cukup mahal, diantara rangkaian penanganan tersier adalah adsorpsi dan
oksidasi kimiawi.
Adsorpsi merupakan metode yang paling banyak digunakan untuk
menghilangkan bahan-bahan organik yang masih tertinggal setelah melewati
tahap penanganan sekunder. Adsorpsi adalah proses akumulasi materi terlarut
pada antar permukaan zat dan juga merupakan proses transfer massa dimana
massa yang ditransfer berasal dari fasa cairan ke permukaan fasa padatan melalui
ikatan kimia atau gaya fisik (Davis and Cornwell, 1991).
Limbah cair industri kebanyakan mengandung bahan organik yang sulit
dihilangkan dengan penanganan biologis konvensional. Adsorpsi dengan
menggunakan karbon aktif merupakan adsorben paling umum digunakan
(Eckenfelder, 1989). Dosis karbon aktif yang digunakan umumnya berkisar pada
200 - 50.000 mg/l untuk mengadsorpsi limbah cair yang belum diketahui.
sedangkan volume larutan adsorbat yang digunakan untuk penentuan isoterm
III. BAHAN DAN METODE
A. BAHAN DAN ALA T
1. Bahan
Bahan baku yang dipergunakan adalah tiga jenis produk bentonit yaitu.
Koleang 8 dan 60 mesh, Kebon Awi 8 dan 60 mesh (nama bentonit berdasarkan
daerah asalnya, yaitu dari kawasan Ciampea, Bogor), Tonsil 200 mesh (imporl
dan arang aktif 300 mesh.
2. Alat
Peralatan yang digunakan dalam penelitian lDl antara lain
spektrofotometer Spectronic-20, magnetic stirrer, timbangan, sentrifuse, tanur,
erlenmeyer, pipet, kertas saring dan kolom adsorpsi dengan diameter 2.5 em
dan panjang 35 em.
B. METODE PENELITIAN
Penelitian yang dilakukan terdiri dua tiga tahap, yaitu penelitian
pendahuluan dan penelitian utama.
1. Penelitian Pendahuluan
a. Penetapan Panjang Gelombang Maksimum Melanoidin
Dilakukan pengukuran adsorbansi dengan spektrofotometer terhadap
yang memiliki nilai adsorbansi maksimum dipilih sebagai panJang
gelombang maksimum yang digunakan untuk penelitian selanjutnya.
b. Penetapan Kurva Standar Konsentrasi Melanoidin
Dilakukan pengukuran adsorbansi pada konsentrasi melanoidin 10, 12,
14, 16, 18 dan 20 gil pada spektrofotometer. Kurva standar diperoleh
melalui regresi linier terhadap plot antara konsentrasi dan adsorbansi.
C. Penentuan waktu kontak
Sebanyak 2 gram bentonit ditempatkan pada erlenmeyer yang telah
berisi 100 ml melanoidin dengan konsentrasi 100 gil (telah ditentukan
absorbansinya). Untuk arang aktif (300 mesh) ditimbang sebanyak 0.3 gram,
kemudian dicampurkan dengan melanoidin 100 ml (100 gil). Tahap
selanjutnya adalah pengadukan campuran. kemudian waktu pengadukan
dievaluasi dengan menggunakan 10 taraf selang waktu yang ditetapkan dari
o
sampai 24 jam. Evaluasi waktu kontak dilakukan terhadap ketiga jenisbentonit yang diteliti, begitu pula terhadap arang aktif. Waktu kontak yang
dipilih adalah waktu kontak yang menghasilkan dekolorisasi maksimum.
Secara umum metode penentuan waktu kontak dapat dilihat pada Lampiran
8.
d. Penentuan nilai K,dan 11n
Sebanyak 0.3, 0.7, 1.0, 1.3, 1.7 dan 2 gram bentonit ditempatkan
dalam masing-masing erlenmeyer (dalam 6 erlenmeyer 500 mIl.
Ditambahkan 100 mililiter melanoidin pada setiap erlenmeyer dengan
konsentrasi 60 gil. Campuran tersebut diaduk selama waktu kontak yang
15
bentonit diaduk selama waktu yang telah ditetapkan pada penelitian
pendahuluan. Campuran tersebut disaring setelah pengadukan selesai.
Adsorbansi filtrat tersebut diukur sebagai adsorbansi akhir.
Konsentrasi melanoidin (gil) dapat ditentukan dengan menggunakan
kurva standar konsentrasi melanoidin. Nilai (x/m) dan nilai C dapat ditentukan sebagai berikut :
x = berat melanoidin awal - berat melanoidin akhir (gram) C = konsentrasi akhir pada saat kesetimbangan adsorpsi (gil)
m = massa adsorben yang digunakan (gram)
Langkah selanjutnya adalah membuat plot antara log(xlm) dan log{Cc)
untuk menentukan Kr dan lin (lin sebagai gradien kurva dan log (Kr) dari intersep kurva). Penentuan ini dilakukan terhadap semua jenis bentonit yang
diteliti. Dilakukan pula pengukuran terhadap arang aktif tetapi dengan berat
0.05, 0.1, 0.15, 0.2, 0.25 dan 0.3 gram yang ditempatkan pada 6 erlenmeyer
500 mililiter dan kemudian dilakukan langkah seperti diatas.
2. Penelitian Utama
Penelitian utama bertujuan untuk mengukur breakthrough time (tb )
dengan mengasumsikan bahwa konsentrasi influen tetap dan konsentrasi etluen
naik seeara linier sampai pada breakpoint. Sistem kolom adsorpsi yang digunakan dengan tinggi bed adsorben 2 em, panjang kolom adsorpsi 35 em, dengan diameter sebesar 2.5 em. Laju alir influen melanoidin (Q) ditetapkan berdasarkan kemampuan filtrasi bed adsorben.
Kinerja kolom adsorpsi dapat diketahui dengan melewatkan sejumlah 2
liter melanoidin sintetis dengan konsentrasi awal 60 gil (sebagai Ci ) seeara
kontinyu pada kolom adsorpsi. Sampling dilakukan setiap kenaikan volume 50
mililiter sekaligus dihitung waktu kontak untuk setiap kenaikan 50 mililiter.
adsorbansi dengan spektrofotometer. Nilai adsorbansi dikonversi ke dalam
satuan konsentrasi (sebagai konsentrasi efluen, Ce) melalui kurva standar
konsentrasi melanoidin. Kurva kejenuhan didapatkan dengan memplotkan titik
CelCi terhadap kenaikan volume sample efluen.
Breakthrough time dicapai pada saat konsentrasi efluen melanoidin (Ce) !epat saat akan jenuh. Skema peralatan kolom adsorpsi dapat dilihat pada
Lampiran 9.
Prosedur pengamatan :
Sebanyak 5 ml sampel efluen ditempatkan pada kuvet yang diambil pada
setiap kenaikan volume efluen 50 mililiter sekali. Adsorbansi sampel tersebut
diukur dengan menggunakan alat Spectronic-20, pengukuran sampel dengan
menggunakan panjang gelombang yang telah ditentukan sebelumnya. Langkah
berikutnya nilai adsorbansi dikonversi ke dalam satuan konsentrasi (gil)
melanoidin dengan kurva standar konsentrasi yang telah ditentukan
sebelumnya. Dekolorisasi pada breakthrough time dihitung dengan rum us sebagai berikut :
Dekolorisasi (%) = [(Ci - Cb)/Cil x 100
Rasio antara konsentrasi efluen dan influen (Ce/Ci) digunakan untuk plotting pada kurva kejenuhan. Konsentrasi, waktu dan volume pada
IV. HASIL DAN PEMBAHASAN
A. PENELITIAN PENDAHULUAN
1. Penentuan Waktu Kontak Optimal
Pencapaian kesetimbangan dalam sistem adsorpsi (steady state) melanoidin tergantung dari lamanya kontak (contact-time) antara adsorbat dan
adsorben bentonit, ukuran partikel adsorben bentonit dan banyaknya adsorben
yang digunakan. Bentonit yang digunakan terdiri dari tiga jenis, yaitu dari
daerah Koleang, Kebon Awi berukuran 60 mesh dan Tonsil (impor) yang
berukuran 200 mesh serta arang aktif berukuran 300 mesh. Bentonit jenis
Koleang dan jenis Kebon awi terlebih dahulu diaktivasi dengan pemanasan
masing-masing pada suhu 50 DC selama 4 jam dan pada suhu 200 DC selama 6
jam. Waktu kontak untuk pencapaian kesetimbangan perlu dievaluasi dalam
interval waktu antara 0 sampai 24 jam dengan sistem pengadukan. Untuk
pengujian awal dilakukan pengadukan selama 24 jam waktu kontak, dan
dibandingkan dengan pengadukan dengan waktu kontak 2 jam.
Evaluasi dilakukan untuk mendapatkan waktu kontak yang optimal dari
masing-masing bentonit yang diteliti. Kesetimbangan dicapai pada saat
kapasitas adsorpsi bentonit menurun, semakin lama kontak antara adsorbat
dengan adsorben maka semakin sempurna untuk mencapai keadaan setimbang.
Melanoidin sintetis digunakan sebagai bahan (adsorbat) yang diadsorbsi
oleh bentonit. Hasil pengukuran menunjukkan bahwa panjang gelombang bagi
melanoidin yang memberikan adsorbansi maksimum adalah pada Ie = 335 nm
(Lampiran I), sedangkan kurva standar bagi konsentrasi melanoidin dapat
dilihat pada Lampiran 2, sebanyak 100 ml limbah cair yang melanoidin dengan
cair keseluruhan, kemudian dilakukan pengadukan pada taraf waktu dari 0
sampai 24 jam. Taraf waktu kontak 2 jam (120 menit) digunakan sebagai
pembanding terhadap tarafwaktu kontak 24 jam.
Waktu kontak yang optimal digunakan sebagai acuan lamanya
pengadukan untuk penentuan lsoterm Freundlich dari masing-masing benton it.
Penentuan waktu kontak yang optimal didasarkan pada pengukuran efesiensi
dekolorisasi (penghilangan warna) yang tertinggi diantara perlakuan taraf-taraf
waktu kontak, seperti yang disajikan pada Lampiran 3. Pengujian statistika
pada hasil evaluasi waktu pengadukan menunjukkan pengaruh yang sangat
berbeda nyata terhadap konsentrasi akhir maksimum yang dicapai.
Kurva adsorpsi bentonit Tonsil terhadap melanoidin dapat dilihat pada
Gambar 4. Waktu kontak yang optimum bagi pengadukan bentonit Tonsil dan
melanoidin adalah 2 jam. Konsentrasi akhir maksimum yang dapat dicapai
pada waktu kontak 6 jam adalah sebesar 55.23 persen. Konsentrasi akhir yang
dicapai berfluktuasi untuk setiap selang waktu karena daya adsorpsi oleh
permukaan partikel bentonit telah berkurang pada saat melewati titik jenuh,
sehingga terjadi desorpsi.
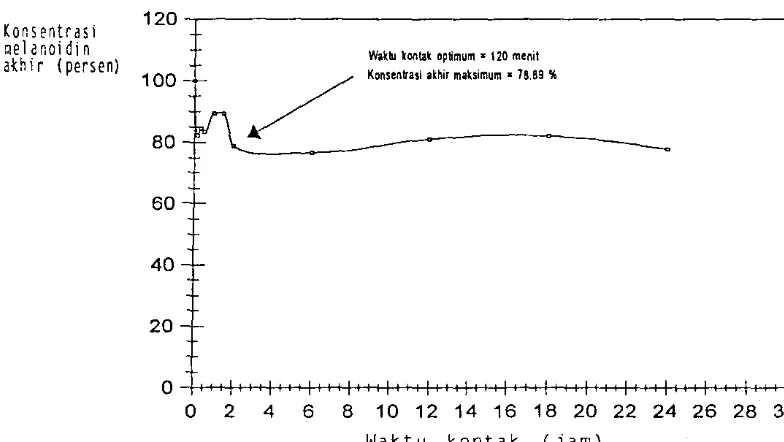
Kurva adsorpsi benton it jenis Koleang pada Gambar 5. menunjukkan
gejala fluktuasi yang serupa, sehingga dipilih waktu kontak 2 jam untuk
pengadukan melanoidin dengan bentonit jenis Koleang. Persentase dekolorisasi
maksimum dicapai pada waktu kontak 6 jam yaitu sebesar 23.23 persen atau
Konsentrasl
meianoidin athlr ipersen)
19
120,---100
80
60
40
20
Gw。セャオ@ kcntak cpijmum '" 120 menit Kcnsentriui 。セャiゥヲ@ maksimum '" 5922 %
o
2 4 6 8 10 12 14 16 18 20 22 24 26 28 30Waktu kontak (jam)
Gambar 4. Kurva adsorpsi bentonit jenis Tonsil terhadap melanoidin
Konsentrasi
,e) anoi di n ath i r i perm)
1 2 0 , - - - ,
Waktu ォcャ|エ。セ@ optimum'" 120 menit Kcnsenhsi akllir maksimum • 78.89 'it
100-'-- /
XPMセセセ@
__-
60+-40
I-
20-1-oセイhNKKLセセKKイLhTKKセTKKKhTKKセhkBtKKセセKエセᄋセLKKKイhTKKセ@
o
2 4 6 8 10 12 14 16 18 20 22 24 26 28 30Waktu kontak (jam)
[image:38.612.124.512.132.355.2] [image:38.612.122.514.437.658.2]Konlentrali me! anoi di n athir (persen)
120.---.
100
80
60
40
20
Waklu konlak optimum' 10 menil
kッョウ・ョセ。ウゥ@ athir maksimum ' 86.85 ,
o
2 4 6 8 10 12 14 16 18 20 22 24 26 28 30Waktu kentak (jam)
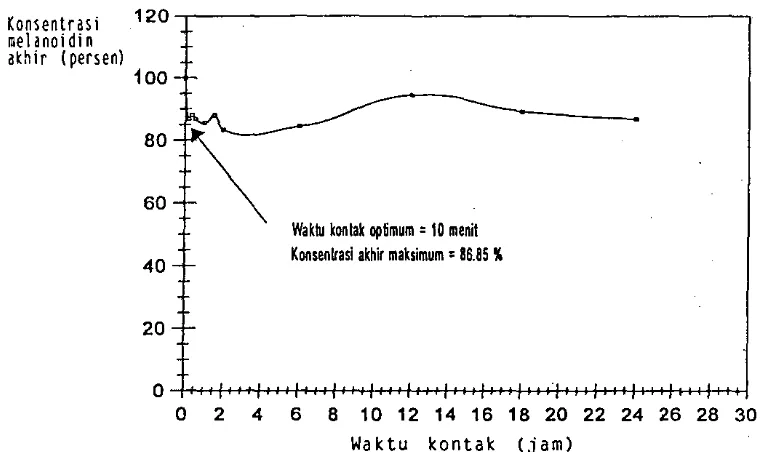
Gambar 6. Kurva adsorpsi bentonit jenis Kebon Awi terhadap melanoidin
Konsentrasi me! ano; di n akhir (persen!
120,---,
100+
80
-60
40+
20+
\
Waktu kontak optimum. 120 menit konsenlnsi akhir maksimum ,. 51."'6 %o
oセセセセ、セBセセNKイGセhKセセKイセセGNjKhGセGセNKイGセhKNセGKNセGセ@
2 4 6 8 1 0 12 14 16 18 20 22 24 26 28 30
Waktu Kentak (jam)
[image:39.607.135.523.124.350.2] [image:39.607.132.514.430.653.2]21
Perilaku kurva adsorpsi bentonit jenis Kebon awi secara umum memiliki
kapasitas adsorpsi yang kecil bila dibandingkan dengan bentonit jenis Tonsil
danjenis Koleang. Pada Gambar 6. terlihat bahwa konsentrasi akhir maksimum
yang bisa dicapai adalah 83.34 persen pada waktu kontak 2 jam, namun uji
statistika menunjukkan bahwa waktu kontak 10 menit sangat tidak berbeda
nyata dengan waktu kontak 30 dan 60 menit dan demikian pula dengan waktu
kontak 2, 6 dan 24 jam. Waktu kontak yang optimal untuk pengadukan
melanoidin dengan bentonit jenis Kebon Awi adalah 10 menit.
Kurva adsorpsi arang aktif menunj ukkan nilai penurunan warna yang
lebih baik. Berdasarkan uji statistika, waktu kontak yang optimum adalah pada
2 jam. Kurva adsorpsi karbon aktif terhadap melanoidin dapat dilihat pada
Dambar 7. Konsentrasi akhir maksimum sebesar 51.46 persen dicapai pada
waktu kontak 2 jam dengan dekolorisasi sebesar 48.54 persen. Waktu kontak
untuk pengadukan melanoidin dengan arang aktif adalah 2 jam.
Efesiensi dekolorisasi tertinggi dicapai oleh arang aktif, walaupun jumlah
adsorben arang aktif yang ditambahkan lebih keciL Disusul kemudian oleh
bentonitjenis Tonsil, Koleang dan Kebon Awi. Efesiensi dekolorisasi terhadap
melanoidin pada waktu kontak optimum untuk bentonit Tonsil adalah 40.78
persen, Koleang 2UI persen dan Kebon Awi 13.15 persen. Arang aktif
mampu menurunkan warna hingga 48.54 persen pada pengadukan 0.3 gram
arang aktif dengan 100 mililiter melanoidin (lOOg/I).
2. Penentuan nilai K, dan 1/n
Harga Kr dan lin betonit berbeda-beda tergantung dari jenis bentonit
yang digunakan dan sifat dari adsorbat melanoidin yang diadsorpsi. Perbedaan
ini disebabkan oleh keaktifan masing-masing bentonit berbeda-beda. Hasil
penelitian pendahuluan untuk menentukan waktu kontak diperoleh efesiensi
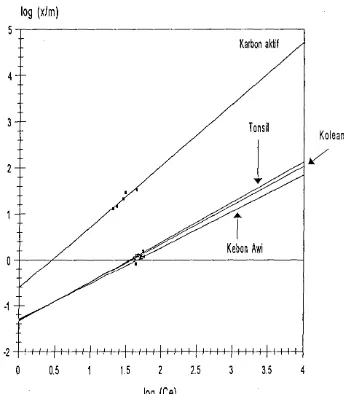
TonsiL Kecendrungan sifat adsorpsi arang aktif dan bentonit Tonsil dapat
dilihat dari kurva isolerm Freundlich pada Gambar 8. Kedudukan kurva isoterm arang aktif berada diatas semua kurva isoterm bentonit. F enomena
tersebut menunjukkan bahwa kapasitas dan intensitas adsorpsi berbeda-beda
menurut jenis adsorben. Kapasitas adsorpsi adalah jumlah gram bahan yang
diadsorpsi per gram adsorben pada keadaan setimbang dengan konsentrasi awal
larutan.
Persamaan isolerm Freundlich yang didapat dari percobaan digunakan
sebagai acuan untuk menentukan berat minimum adsorben pada kolom adsorpsi
pada saat adsorben mencapai titik tepat saat akan jenuh (breakthrough lime). Konstanta Kr dan lin yang diperoleh dari regresi kurva merupakan nilai
empiris, sedangkan yang dipakai sebagai acuan untuk penentuan berat adsorben
minimum pada kolom adsorpsi adalah antara 25 sampai 50 persen dari hasil
pengukuran empiris. Gradien kurva yang didapat merupakan nilai konstanta
lin, sedangkan instersep merupakan Log Kr. Nilai Kr bersifat unik, tergantung dari jenis adsorben bentonit dan adsorbat yang diserap. Nilai Kr dan lin dari
masing-masing bentonit disajikan pada Tabel 3.
Tabel 3. Nilai Kr dan lin untuk berbagai adsorben
Jenis adsorben Kr (I1g) lin
Koleang 0.048 0.838
Kebon awi 0.050 0.785
Tonsil 0.046 0.866
Arang aktif 0.251 1.329
Gradien kurva isoterm yang curam menunjukkan besarnya fraksi
melanoidin yang diserap per gram adsorben yang diberikan. Fenomena terse but
juga dapat menjelaskan bahwa bila ditarik garis vertikal yang tegak lurus
[image:41.608.121.510.493.600.2]23
disusul oleh Tonsil kemudian oleh jenis bentonit Koleang dan Kebon awi. Pola
kedudukan kurva yang lebih tinggi menunjukkan bahwa Log (x/mlcarbon
aktirLog (xlmhonsil>Log (x/m)Koleang>Log (xlm)Kebon Awi, sehingga dapat
dijelaskan pula bahwa untuk mencapai kedudukan konsentrasi akhir Ce yang sarna, dengan berat adsorben yang digunakan sarna jumlahnya, maka urutan
besarnya gram melanoidin yang diserap per gram bentonit adalab Xkarbon akti!" >
Xtonsil> Xkoleang> XKebon Awi"
log
(x/m)
UセMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMセ@
Karbon aktif
4
3
Tonsil
2
1
Koleang
/
Kebon Awi
PTMMMセMMMMMMMMセセMMMMMMMMMMMMMMMMセ@
-1
-2 -H-H--H-++++++H--I-H-H-+-+++++J-+..f+-I++++++++++1
o
0.5 1.5 2 2.5 3 3.5 4log (Ge)
[image:42.610.153.497.249.643.2]Nilai Kr bersifat unik, tergantung dari Jems adsorben bentonit dan
adsorbat yang diserap. Pengukuran adsorpsi melanoidin dalam penentuan
persamaan isoterm Freundlich masing-masing adsorben pada suhu kamar (2Soq.
Kapasitas adsorpsi masing-masing adsorben dapat ditentukan dengan
menarik garis vertikal pada sumbu Log Ce dari titik konsentrasi awal 60 gil,
kemudian ditarik garis horisontal ke arah sumbu Log (x/m) hingga didapatkan jumlah melanoidin yang diserap per satuan berat berat adsorben pada keadaan
setimbang dengan konsentrasi awal. Pada kurva isoterm Freundlich didapatkan
kapasitas adsorpsi dari yang tertinggi ke yang terendah untuk arang aktif adalah
57.92, Tonsil 1.59, Koleang 1.48 dan Kebon Awi 1.24 (dalam unit gram
adsorbat per gram adsorben).
B. PENELITIAN UTAMA
1. Kondisi Operasi
Penelitian utama dilakukan dengan menempatkan adsorben bentonit pada
kolom adsorpsi. Bentonit dalam hal ini bertindak sebagai adsorben. Kondisi
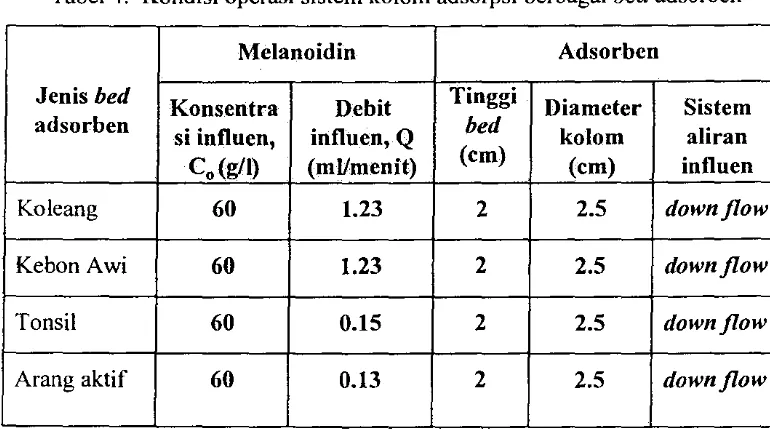
Operasi kolom dari berbagai adsorben yang diteliti dapat dilihat pada Tabel 4.
Sifat aliran limbah cair melanoid in kedalam kolom adalah down flow, yaitu aliran kebawah dengan sistem gravitasi. Debit influen disesuaikan dengan
kemampuan filtrasi limbah cair melanoidin ke dalam butiran bed yang digunakan pada kolom. sehingga diharapkan tidak terjadi akumulasi cairan pada
25
Tabel 4. Kondisi operasi sistem kolom adsorpsi berbagai bed adsorben
Melanoidin Adsorben
.
Jenis bed
Konsentra Debit Tinggi Diameter Sistem adsorben
si influen, influen,
Q
bed kolom aliran C.(gll) (mllmenit) (cm) (cm) influenKoleang 60 1.23 2 2.5 downJlow
Kebon Awi 60 1.23 2 2.5 downJlow
Tonsil 60 0.15 2 2.5 downJlow
Arang aktif 60 0.13 2 2.5 downJlow
2. Waktu Kontak
Penetapan waktu kontak didasarkan pada Empty Bed Contact Time (EBCT), yaitu berdasarkan debit influen dibagi dengan volume bed adsorben pada kolom dalam keadaan kosong. Waktu kontak untuk sistem kolom bentonit
Koleang dan Kebon Awi adalah 7.98 menit. Sedangkan untuk Tonsil dan arang
aktifmasing-masing adalah 65.47 menit dan 75.54 menit.
Pengamatan terhadap waktu kontak yang dihitung dari setiap kenaikan
volume efluen 50 mililiter menunjukkan kecendrungan semakin melebarnya
waktu kontak. Hal ini merupakan pengaruh dari mengecilnya ruang filtrasi bagi
cairan melanoidin sebagai akibat hancurnya butiran bentonit yang kemudian
menutupijalan bagi filtrasi melanoidin, disamping itu kemampuan adsorpsi dari
bentonit dan arang aktif semakin menurun dengan meningkatnya waktu
pengoperasian kolom adsorpsi.
Kurva hubungan antara raslo konsentrasi efluen dan influen (Ce/Ci)
versus waktu kontak dapat digunakan untuk pendugaan breakthrough time
[image:44.608.125.510.102.317.2]preferensi meningkatnya konsentrasi efluen pada setiap waktu. Hal 1111
menunjukkan pola menuju pada keadaan jenuh sempurna, titik breakthrough
diperoleh dari titik dimana konsentrasi efluen atau Ce/Ci mulai meningkat
tajam. Dalam jangka waktu yang lama akan mencapai kejenuhan sempurna
dimana Ce/Ci akan mendekati nilai 1.0.
Tabel5. Kemampuan adsorpsi maksimum dan breakthrough time
JeDis bed Dekolorisasi (perseD) Breakthrough time, tb (jam) adsorbeD
Koleang 84 2.08
KeboD Awi 85 0.66
Tonsil 91 32.83
Arang aktif 86 69.25
Karakteristik kurva kejenuhan sebagai hubungan antara rasio Ce/Ci dan
waktu kontak sistem kolom dengan adsorben jenis Koleang dapat dilihat pada
Gambar 9. Kekeruhan efluen mulai terjadi pada volume 10 mililiter. sedangkan
sebelumnya penampakan efluen adalah jernih, sehiDgga pengukuran adsorbansi
dimulai pada volume tersebut saat 0.14 jam operasi. Titik waktu tepat saat akan
jenuh (tb) untuk sistem kolom adsorpsi bentonit Koleang adalah pada 2.08 jam
operasi. Pada kedudukan titik ini rasio Ce/Ci adalah sebesar 0.16, dan tingkat
dekolorisasi pada saat itu sebesar 84 persen, tetapi dapat mencapai efesiensi
dekolorisasi 88 persen pada jam ke 0.68 operasi. Informasi yang didapat dari
kurva Gambar 9 terse but adalah bahwa pada jam ke 2.08 waktu operasi, adalah
merupakan titik penggantian adsorben yang baru, mengingat kemampuan
adsorpsi yang semakin menurun. Kemampuan adsorpsi maksimum yang
didasarkan pada persentase melanoidin yang diserap hingga tepat saat akan
Ce/Ci
0.5,---,
0.4
0.3
0.2
Breakpoint
Waktu breakthrough = 2.08 jam
0.1
o 1 2 3 4 5 6 7 8 9 10
Waktu kontak Gam)
Gambar 9. Kurva kejenuhan kolom adsorpsi bentonit Koleang sebagai hubungan an tara waktu kontak dan rasio Ce/Ci
Ce/Ci
0.6,---,
0.5
0.4
0.3
0.2
0.1
o
2 4Breakpoint
Waktu breakthrough =- 0.66 jam
6 8 1 0 1 2 14 1 6 1 8 20 22 24
Waktu kontak (jam)
27
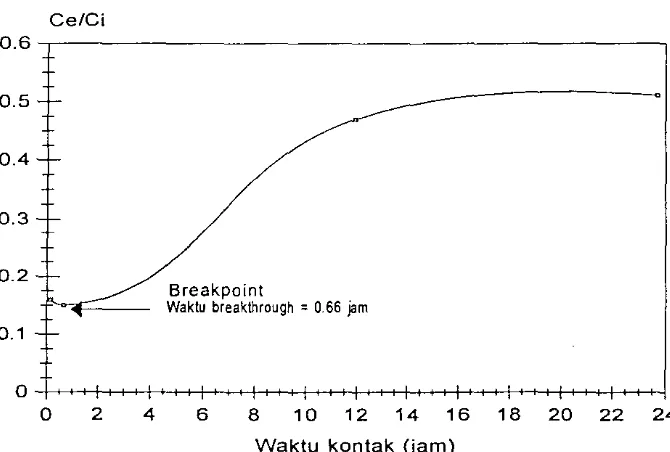
[image:46.605.133.477.101.322.2] [image:46.605.130.465.406.632.2]Karakteristik kurva kejenuhan sistem kolom bentonit Kebon Awi dapat
dilihat pada Gambar 10. Kecendrungan melebarnya waktu kontak per kenaikan
volume efluen 50 militerdialami juga oleh sistem kolom tersebut. Titik waktu
tepat saat akan jenuh adalah pad a 0.66 jam. Rasio Ce/Ci pada saat itu adalah
sebesar 0.15, ini berarti pada saat tersebut kemampuan adsorpsi terhadap
mdanoidin mencapai 85 persen, tetapi bisa mencapai 86 persen pada saat 0.26
jam operasi. Rasio Ce/Ci meningkat dari 0.15 menjadi 0.39 dan seterusnya
hingga mendekati kejenuhan. Pengukuran adsorbansi dilakukan pada saat
mulai terjadi kekeruhan yaitu pada volume efluen 10 mililiter pada 0.13 jam
operasi. Kondisi operasi sistem kolom adsorpsi Koleang dan Kebon Awi
seperti ukuran butiran dan debit influen adalah sarna, tetapi lama pencapaian
breakthrough lebih panjang pada sistem kolom adsorpsi bentonit Koleang. Karakteristik kurva kejenuhan sistem kolom bentonit Tonsil menunjukkan
breakthrough time yang cukup panjang. bila dibandingkan dengan sistem
kolom adsorpsi bentonit Koleang dan Kebon Awi, hal ini berkaitan dengan
kapasitas adsorpsi dari bentonit Tonsil yang lebih besar dibandingkan bentonit
Koleang dan Kebon Awi, selain itu ukuran butiran bentonit Tonsil lebih kecil
yang menyebabkan pencapaian breakthrough semakin panjang.
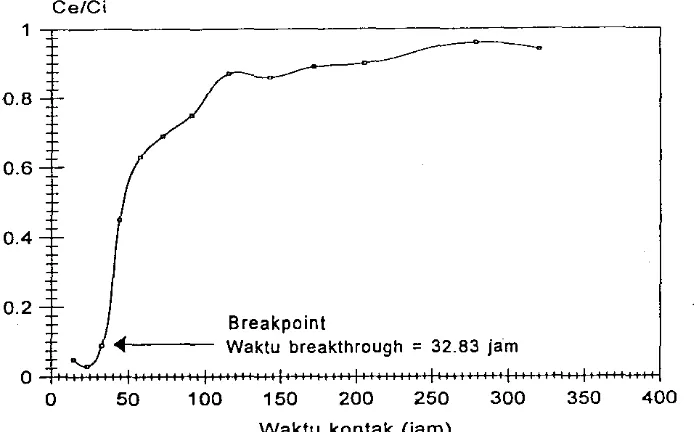
Kurva pada Gambar II. menunjukkan titik waktu tepat saat akan jenuh
bentonit Tonsil adalah pada 32.83 jam. Setelah pada jam tersebut terjadi
kenaikan konsentrasi efluen dimana Ce/Ci meningkat tajan1 dari 0.09 menjadi
0.45 dan seterusnya. Waktu breakthrough pada sistem kolom adsorpsi bentonit Tonsil lebih panjang bila dibandingkan dengan Koleang dan Kebon Awi, hal ini
ini sangat berhubungan sekali dengan besarnya debit influen yang diberlakukan.
semakin kecil debit influen maka akan semakin lebar pula waktu mencapai
breakthrough, semakin kecil ukuran but iran adsorben maka semakin lama
Ce/Ci
QセMMMMMMMMMMMMMMMMセ]]]]]MMMセ@
O.B
-f-0.6
,0.4
0.2
-Breakpoint
J .... '---
Waktu breakthrough = 32.83 jamPThセセセセセセセセセセセセJJセセセセセセ@
o
50 100 150 200 250 300 350 400Waktu kontak Gam)
Gambar II. Kurva kejenuhan kolom adsorpsi bentonit Tonsil sebagai hubungan antara waktu kontak dan rasio Ce/Ci
Ce/Ci
QNRセMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMML@
O.B
0.6
0.4
0.2 Breakpoint
Waktu breakthrough = 69.25 jam
o
100 200 300 400 500 600 700Waktu kontak (jam)
Gambar 12. Kurva kejenuhan kolom adsorpsi arang aktif sebagai hubungan antara waktu kontak dan rasio Ce/Ci
[image:48.605.147.494.108.324.2] [image:48.605.147.474.411.632.2]Awi. Pada keadaan tertentu yaitu pada jam operasi ke 23.33, efesiensi
dekolorisasi dapat mencapai 97 persen.
Sistem kolom adsorpsi arang aktif memiliki waktu kontak yang lebih
lama sebanding dengan besarnya debit influen yang diterapkan. Breakthrough time yang dicapai adalah pada 69.25 jam dengan rasio Ce/Ci sebesar 0.14. Pada
keadaan breakpoint efesiensi dekolorisasi mencapai 86 persen. Posisi breakpoint dapat dilihat pada Gambar 12, yaitu pada Ce/Ci dari 0.14 menjadi 0.24 dan seterusnya. Penampakan efluen dari jam ke nol sanlpai pada jam
operasi ke 55.77 secara fisik jernih, dan mulai terjadi kekeruhan pada volume
efluen 350 mililiter padajam operasi ke 69.25.
Zona adsorpsi pada sistem kolom yang dioperasikan selama dalam
penelitian tidak teramati, batas antara zona adsorpsi dengan bagian bed adsorben yang belum jenuh tidak terlihat nyata. Dalam percobaan ini
pengoperasian sistem kolom hanya terdiri satu tahap, yaitu tahap adsorpsi,
sedangkan tahap pencucian dan regenerasi tidak dilakukan. Keadaan ukuran
fisik dari butiran bentonit dalam kolom menjadi kecil setelah kontak dengan
limbah cair melanoidin.
3. Volume dan Konsentrasi pada sa at Breakpoint
Volume dan konsentrasi pada saat breakpoint ditentukan pada saat tepat akan terjadi kenaikan konsentrasi efluen yang tajam, yang merupakan indikasi
mulai menurunnya kapasitas adsorpsi dari adsorben. Volume breakthrough (V b) adalah jumlah influen yang dapat ditangani hingga pada saat tepat akan
jenuh, dan konsentrasi pada saat Vb yang dicapai merupakan konsentrasi
31
Tabel6. Nilai Vb dan Cb berbagai adsorben pada sistem kolom adsorpsi
Jenis bed Konsentrasi Volume Rasio Ce/Ci
adsorben breakpoint, Cb breakpoint, Vb
(gil) (ml)
Koleang 9.60 150 0.16
Kebon Awi 9.00 50 0.15
Tonsil 5.40 200 0.09
Arang aktif 8.4 350 0.14
Nilai Vb dan Cb setelah pengoperasian kolom adsorpsi berbagai adsorben
dapat dilihat pada Tabel 6. Nilai Vb dan Cb yang bervariasi disebabkan oleh kondisi operasi kolom adsorpsi masing-masing kolom tidak sama (kecuali
Koleang dan Kebon Awi). Ukuran Mesh adsorben Tonsil dan arang aktif yang
digunakan disesuaikan dengan ketersediaan adsorben tersebut di pasaran.
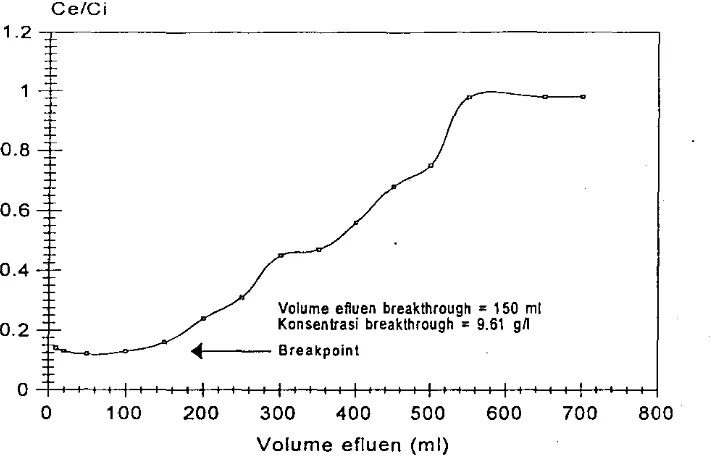
Kurva hubungan volume efluen dan rasio Ce/Ci untuk sistem kolom
adsorpsi bentonit Koleang menunjukkan kecenderungan kenaikan rasio Ce/Ci dengan meningkatnya volume efluen. Konsentrasi efluen pada keadaan tepat
saat akan jenuh adalah sebesar 9.6 gil pada nilai Ce/Ci sebesar 0.16, sedangkan kedudukan volume breakthrough adalah sebesar 150 mil iter. Pada saat titik volume dan konsentrasi terse but merupakan titik penggantian adsorben benton it
koleang. Kurva hubungan volume dan rasio Ce/Ci dapat dilihat pada Gambar
13.
Karakteristik kurva kejenuhan sistem kolom adsorpsi Kebon Awi.
memiliki kecenderungan yang sama dengan Koleang. Kedudukan volume dan
konsentrasi pada saat tepat akan jenuh masing-masing adalah 50 ml dan 9.00 gil dengan nilai rasio Ce/Ci sebesar 0.15. Rasio Ce/Ci meningkat dari 0.15
menjadi 0.39, volume limbah cair yang mampu ditangani oleh sistem kolom
dibandingkan denganjumlah volume yang mampu ditangani oleh sistem kolom
adsorpsi bentonit Koleang. Hal ini disebabkan kapasitas adsorpsi bentonit
Kebon Awi (dari penelitian pendahuluan) lebih kecil daripada bentonit
Koleang, sehingga kemampuan untuk mcnangani sejumlah volume tertentu
melanoidin sangat tergantung dari besarnya kapasitas adsorpsi.
Volume influen yang mampu diadsorpsi oleh sistem kolom adsorpsi
bentonit Tonsil lebih banyak bila dibandingkan volume yang ditangani oleh
sistem kolom adsorpsi bentonit Koleang dan Kebon Awi. Pada rasio Ce/Ci sarna dengan 0.09 sistem kolom adsorpsi bentonit Tonsil mampu menangani
lim bah cair melanoidin sampai pada volume 200 mililiter, setelah melewati
nilai 0.09 terjadi kenaikan konsentrasi efluen yang tajam, dengan demikian
konsentrasi pada saat tepat akan jenuh sarna dengan 5.4 gil. Kurva kejenuhan sistem kolom adsorpsi bentonit Tonsil dapat dilihat pada Gambar 15. Efluen
dari sistem kolom tersebut mulai terlihat keruh pada 14.46 jam operasi,
sehingga pengukuran adsorbansi dilakukan pada saat sampel efluen mencapai
100 mililiter.
Kemampuan sistem kolom adsorpsi arang aktif dalam menangani volume
influen melanoidin hingga 350 mililiter pada rasio Ce/Ci sebesar 0.14 dengan konsentrasi breakthrough 8.4 gil. Penampakan fisik efluen hingga pada volume efluen 300 mililiter masih jernih, sehingga pengukuran terhadap adsorbansi
dilakukan pada volume efluen 350 mililiter yang penampakannya secara fisik
telah keruh. Kurva karakteristik kejenuhan sistem kolom adsorpsi arang aktif
dapa! dilihat pada Gambar 16. Debit influen yang diterapkan lebih kecil yaitu
0.13 mililiter/menit yang disesuaikan dengan kemampuan filtrasi lim bah cair
melanoidin dengan ukuran mesh arang aktif sebesar 300.
Titik konsentrasi dan volume pada keadaan breakpoint dapa! digunakan
sebagai acuan untuk pengoperasian sistem adsorpsi kolol11 pada skala yang
CerCi
NRセMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMMセ@
1
0.8
0.6
0.4
0.2
o
100Volume efluen breakthrough = 150 ml Konsentrasi breakthrough = 9.61 gn セBiMMMMM Breakpoint
200 300 400 500 600
Volume efluen (ml)
700 800
Gamba!" 13. Kurva kejenuhan sistem kolom adsorpsi bentonit Koleang hubungan antara volume efluen dan rasio Ce/Ci
Ce/Ci
0.6,---0.5
0.4
0.3
0.2
0.1
o
20 40 60Volume efluen breakthrough = 50 ml Konsentrasi breakthrough = 9.00 gil
Breakpoint
80 100 120 140 160 180 200
[image:52.603.136.498.91.319.2]Volume efluen (ml)
Gambar 14. Kurva kejenuhan sistem kolom adsorpsi bentonit Kebon Awi hubungan antara volume efluen dan rasio Ce/Ci
Parameter debit influen, ketinggian bed adsorben, konsentrasi influen, waktu dan volume pada keadaan breakpoint hasil percobaan dapat menunjang kearah tersebut. Dalam hal ini parameter-parameter operasi yang didapatkan dari hasil
percobaan seperti konsentrasi inf