Lampiran I. Kitosan Bead/Manik
Lampiran 3. Hasil Adsorbsi Logam Cd dengan Alat Kolom
Lampiran 4. Spektrofotometer Serapan Atom Merk Shimadzu
DAFTAR PUSTAKA
AksuZ. 2005. Application of Biosorption for The Removal of Organic Pollutants: A review. Process Biochemistry 40: 997-1026.
Altschul, A.M. 1976. New Protein Food. Academic Press Ltd. London
Austin PR. 1988. Chitin Solution and Purification of Chitin. Di dalam Wood WA dan Kellog ST. New York: Biomass Academic Pr.
Bassler. 1986. Penyidikan Spektrometrik Senyawa Organik. Jakarta : Erlangga.
Berger, J., M. Reist, J. M. Mayer, O. Felt, N. A. Peppas, and Gurny, R. 2004. Structure and Interactions in Covalently and Ionically Crosslinked Chitosan Hydrogels for Biomedical Applications. European Journal of Pharmaceutics and Biopharmaceutics, 57, 19-34.
Connel, D.W. 1995. Kimia Dan Ekotoksilogi Pencemaran . Jakarta: UI-Press.
Clark, D.V. 1979. Approach to Atomic Absorption Spectroscopy. Analytic Chemistry Consultans Pty Ltd. Sidney-Australia
Haswell,S.J. 1991. Atomic Absorption Spectrometry Theory. Design and Application. Amsterdam: Elsevier
Hirano, S. 1986. Chitin and Chitosan. Weinheim. New York.
Indah, L. 2012. Penyediaaan dan Karakterisasi Kitosan Glutaraldehida Sebagai Adsorben Untuk Menentukan Kadar Ion Logam Cu Dengan SSA.
Karthikeyan G, Anbalagan K, Muthulakshmi AN. 2004. Adsorption dynamis and equilibrium studies Antibiotic Delivery. J wiley DOI 10.1002.1260 Khopkar, S.M.2003. Kosep Dasar Kimia Analitik. Jakarta: UI Press.
Kroschwitz, J. 1990. Polymer Characterization and Analysis. Canada : John Wiley & Sons.
Mulja, M, 1995, Water Treatment Principles and Design, New York : John Willey and Sons, Inc.
Martinou, A., Kafetzopoulos, D., Bouriotis, V. 1995. Chitin Deacetylation by Enzymatic Means : Monitoring of Deacetylation Processes. Carbohydrate Research 273 : 235-242
Monteiro, O. A. C., Airoldi, C. 1999. Some Studies of Crosslinking ChitosanGlutaraldehyde Interaction in a Homogeneous System. InternationalJournal of Biological Macromolecules, 26, 119-128.
No HK., and S.P. Meyers. 1989. Isolation and Characterization of Chitin From Crawfish Shell Waste. J Agri Food Chem 37:575-579
Nugroho, A.2006. Bioindikator Kualitas Air. Universitas Trisakti. Jakarta.
Osifo PO ., 2008. The Influence of The Degree of Cross-Linking on The Adsorption Properties of Chitosan Beads. Bioresource Technol 99: 7377-7382
Rao, A. M., van Buren, J. P., Cooley, H. J. 1993. Rheological Changes During Gelation of High-Methoxyl Pectin/Fructosee Disperaions, Effect of Temperature and Ageing. J Food Sci 58(1) : 173-176.
Rohman, A., 2007. Kimia Farmasi Analisis. Jakarta : Pustaka Pelajar
Silverstein, R. M. 1967. Spectrometric Identification of Organic Compounds. New York : John Wiley and Sons.
Shadidi F, Synowiecki J. 1991. Isolation and Characterization of Nutrients and Value Added Products from Snow Crab (Chinoeages opilio) and Shrimp(Pandalus borealis) Processing Discards. J Agric Food Chem 39:1527-1532.
Singh V, Sharma A.K, Tripathi D.N, Sanghi R. 2008. Poly(Methylmetacrylate) Grafted Chitosan : An Efficient Adsorbent For Anionic Azo Dyes. J Hazard Mater doi: 10. 1016/j. Jhatmat. 2008.04.096
Sugita, P. 2009. Kitosan: Sumber Biomaterial Masa Depan. Bogor : IPB Press.
Tsigos, I., Martinou, A., Kafetzopoulos, D., Bouriotis, V. 2000. Chitin Deacetylases : New, Versatile Tools in Biotechnology. TIBTECH 18 : 305-312.
Walsh, A. 2005. Potensi Kitosan dan Sisa Udang Sebagai Koagulan Logam Berat Limbah Cair Industri Tekstil. Jurnal. Surabaya: ITS
Widowati, W, Sastiono, A, Jusuf, R. 2008. Efek Toksik Logam . Yogyakarta Andy Yogyakarta.
BAB 3
METODE PENELITIAN
3.1. Bahan
- Kitosan
- NaOH p.a (E.Merck)
- Glutaraldehida p.a (E.Merck)
- Asam Asetat p.a (E.Merck)
- CdCl2.H2O p.a (E.Merck)
- Akua steril
- Aquadest
3.2. Alat
- Atomic Absorbtion Spectrophotometer AA 7000-F
- Seperangkat alat spektrofotometer FTIR Shimadzu
- Beaker Glass Pyrex
- Erlenmeyer Pyrex
- Gelas Ukur Pyrex
- Spatula
- Corong
- Kertas Saring Whatman no.1/41
- Labu Takar Pyrex
- Neraca Analitik (presisi±0,0001g) Mettler
3.3. Prosedur Penelitian
3.3.1. Pembuatan Pereaksi
3.3.1.1.Pembuatan Larutan Asetat 5% (v/v)
Sebanyak 5 mL asam asetat glasial dimasukkan ke dalam labu ukur 100 mL,
kemudian diencerkan dengan akua steril sampai garis tanda, dan dihomogenkan.
3.3.1.2.Pembuatan Larutan NaOH 2 M (b/v)
Sebanyak 40 g NaOH pelet dimasukkan kedalam beaker glass. Ditambahkan
500mL aquadest. Lalu diaduk sampai homogen sehingga diperoleh larutan NaOH
2 M.
3.3.1.3. Pembuatan Larutan Glutaraldehida 2.5% dari Glutaraldehida 25%
Sebanyak 2,5 ml glutaraldehida dimasukkan kedalam labu takar 100 ml,
kemudian diencerkan dengan akua steril sampai garis tanda, dan dihomogenkan.
3.3.2. Pembuatan Kitosan Bead/manik
Sebanyak 2 g dilarutkan kedalam larutan asetat 5% (b/v) dengan ratio 1:40 di
dalam beaker glass, lalu diaduk sampai homogen sehingga diperoleh larutan
kitosan, kemudian diteteskan kedalam larutan NaOH 2 M, hingga terbentuk gel.
Gel dicuci dengan aquades hingga netral dan dikeringkan.
3.3.3. Pembuatan Ikat Silang Kitosan DenganGlutaraldehid
Kitosan bead dimasukkan dalam larutan glutaraldehid 2,5% dengan rasio 1,5 ml
tiap gram kitosan bead, dibiarkan pada suhu kamar selama 24 jam. Kitosan yang
telah terikat silang kemudian dicuci dengan aquades. Kitosan yang telah dicuci
3.3.4 Pembuatan Larutan Standar Kadmium ( Cd2+)
3.3.5. Pembuatan Larutan Standar Kadmium ( Cd2+) 1000 mg/L
Sebanyak 0,1475 g kitosan CdCl2.H2O dimasukkan kedalam beaker glass 250 mL lalu dilarutkan dengan HCl(p) sambil diaduk hingga larut kemudian dimasukkan kedalam labu takar 1000 mL. Setelah itu ditambahkan akuades hingga garis tanda
dan dihomogenkan.
3.3.6. Pembuatan Larutan Standar Kadmium ( Cd2+) 100 mg/L
Sebanyak 5 mL larutan induk Kadmium ( Cd2+) 1000 mg/L dimasukkan kedalam labu takar 50 mL lalu diencerkan dengan akuades sampai batas garis tanda.
3.3.5.1. Pembuatan Larutan Standar logam Kadmium ( Cd2+ ) 10 mg/L
Sebanyak 5 mL larutan standar 100 mg/L dimasukkan kedalam labu takar 50 mL
lalu diencerkan dengan akuades sampai batas garis tanda dan dihomogenkan.
3.3.5.2. Pembuatan larutan Standart logam Kadmium ( Cd2+ ) 5 mg/L
Sebanyak 25 mL larutan standar 10 mg/L dimasukkan kedalam labu takar 50 mL
lalu diencerkan dengan aquades sampai batas garis tanda dan dihomogenkan.
3.3.5.3. Pembuatan Larutan Seri Standar Kadmium ( Cd2+ ); 0,2; 0,4; 0,6;
0,8 dan 1,0 mg/L
Sebanyak 2; 4; 6; 8; dan 10 mL Larutan Cd2+ dimasukkan kedalam 5 buah labu takar 50 mL kemudian diencerkan dengan aquades hingga garis batas tanda dan
dihomogenkan sehingga diperoleh larutan seri standar (0,2; 0,4; 0,6; 0,8; dan 1,0
3.3.5.4. Pembuatan Kurva standar
Larutan seri standar 0,2 mg/L dibuat dengan pH tidak lebih dari 3 kemudian
diukur absorbansinya dengan menggunakan Spektrofotometer Serpan Atom pada
panjang gelombang spesifik 228,80 nm. Perlakuan dilakukan sebanyak 3 kali dan
dilakukan hal yang sama dengan larutan standar yang lain (0,4; 0,6; 0,8; dan 1,0
mg/L).
3.3.5.5 Penentuan Waktu Kontak Optimum pada Kitosan Glutaraldehida
Larutan Standar logam Cadmium 5 mg/L dimasukkan kedalam kolom yang telah
berisi kitosan glutaraldehida, didiamkan berdasarkan variasi 15, 30, 45, 60 menit,
kemudian dibuka tutup kolom dan ditampung dengan botol vial, kemudian diuji
3.4. Bagan Penelitian
3.4.1. Pembuatan Pereaksi
3.4.1.1. Larutan asam asetat 5%
3.4.1.2.Larutan NaOH 2 M
3.4.2 Pembuatan Kitosan Bead/Manik (Agusnar, 2006)
3.4.4.Pembuatan Kurva Kalibrasi
Catatan : Dilakukan prosedur yang sama untuk larutan seri standar 0,2; 0,4; 0,6;
0,8; dan 1,0 mg/L
3.4.5 Penentuan Waktu Kontak Optimum pada Kitosan Glutaraldehida
BAB IV
HASIL DAN PEMBAHASAN
4.1Hasil Penelitian
4.1.1. Data Absorbansi Larutan Standar Cadmium(Cd)
Data absorbansi untuk larutan standar Cadmium (Cd) dapat dilihat pada tabel 4.1
dibawah ini
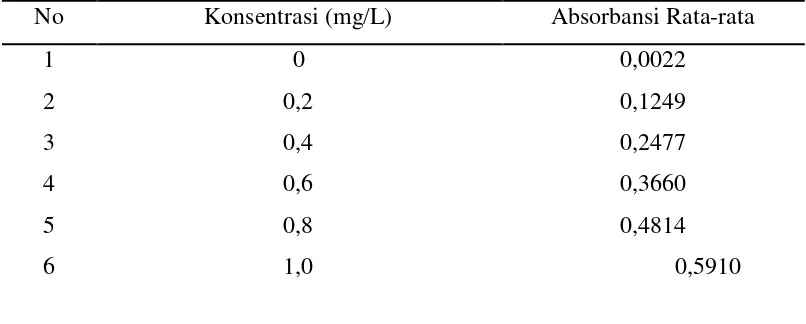
Tabel 4.1 Data Absorbansi Larutan Standar Cadmium(Cd)
No Konsentrasi (mg/L) Absorbansi Rata-rata
1
Kondisi alat spektrofotometer AA-7000 untuk absorbansi logam Cd dapat dilihat
pada tabel 4.2 dibawah ini:
Tabel 4.2 Kondisi Alat Spektrofotometer AA-7000 pada Absorbansi Cd
4.1.1.1. Penurunan Persamaan Garis Regresi dengan Metode Kurva
Kalibrasi untuk Larutan Standar Cd2+
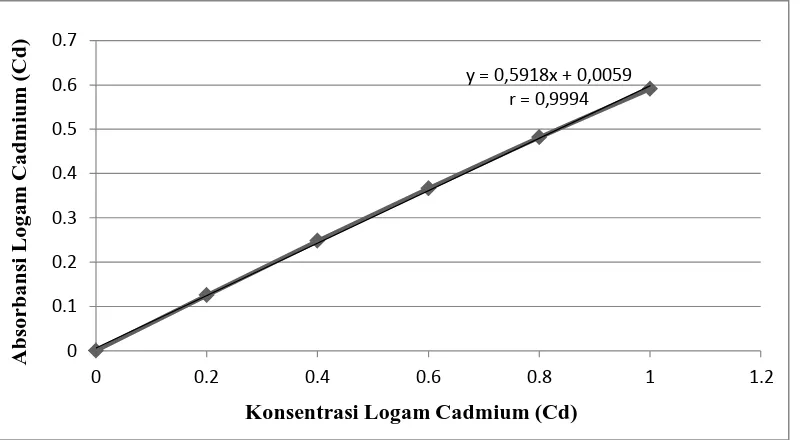
Data absorbansi yang diperoleh untuk suatu seri larutan standar Cd diplotkan
terhadap konsenterasi larutan standar sehingga diperoleh kurva kalibrasi berupa
garis linear seperti pada gambar 4.1 berikut ini:
Gambar 4.1 Kurva Kalibrasi Larutan Seri Standar Cd
Persamaan garis regresi ini diturunkan dengan metode Least Square,
dimana konsenterasi dari larutan standar dinyatakan sebagai Xi dan absorbansi
dinyatakan sebagai Yi seperti pada tabel 4.2 berikut :
Tabel 4.2. Penurunan Persamaan Garis Regresi Untuk Penentuan Konsentrasi
Logam Cd Berdasarkan Pengukuran Absorbansi Larutan Standar
Dari persamaan garis regresi dengan metode Least Square tersebut dapat
diperoleh nilai konsentrasi rata-rata ( ̅ dan nilai absorbansi rata-rata ( ̅ dengan
persamaan berikut :
Harga Slope dan intercept dapat ditentukan dengan menggunakan metode least
square sebagai berikut :
∑ ̅ ̅∑ ̅
∑ ∑
Maka Persamaan Garis Regresi adalah :
Y = 0,5981X + 0,0059
4.1.1.2 Penentuan Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut :
∑ ̅ ̅ √∑ ̅ ̅
4.1.1.3. Persentasi Penurunan Kadar Ion Cadmium (Cd2+) dalam larutan
(Penentuan Persen (%) Adsorpsi)
Persentasi penurunan kadar ion Cd2+ dalam larutan sebelum dan setelah di adsorpsi dapat ditentukan dengan menggunakan persamaan berikut:
%
Adsorpsi =
Dari data hasil pengukuran yang terdapat pada table 4.3 dan 4.4 maka penentuan
4.2. Reaksi-reaksi
4.2.1. Reaksi Ikat Silang Kitosan dengan Glutaraldehida
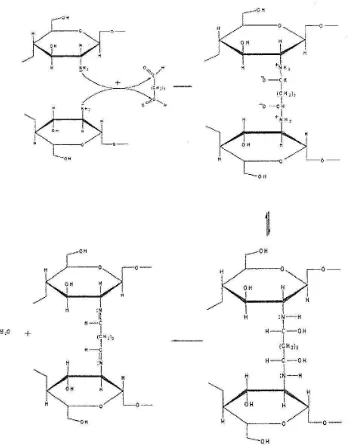
Mekanisme reaksi ikat silang kitosan bead dengan glutaraldehida dapat dilihat
pada gambar 4.2 dibawah ini:
Gambar 4.2. Reaksi Ikat Silang Kitosan dengan Glutaraldehid
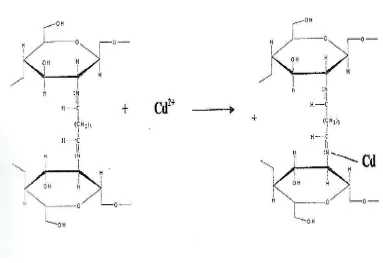
4.2.2. Reaksi Ikat Silang Kitosan Glutaraldehida dengan Ion Logam Cd2+
Mekanisme reaksi ikat silang kitosan glutaraldehida dengan ion logam Cd2+ dapat dilihat pada gambar 4.3. dibawah ini:
4.3. Pembahasan
4.3.1. Analisa Spektrum FT-IR
Analisa dengan spektroskopi FT-IR ini dapat digunakan sebagai informasi
mengenai perubahan gugus yang mengindentifikasi adanya interaksi secara kimia
Spektrum FTIR pada kitosan komersial menunjukkan adanya serapan pada daerah
bilangan gelombang (cm-1) : 3425,58 yang merupakan daerah (N-H bending dan O-H stretching), pita serapan pada bilangan gelombang 2877,79 untuk daerah
puncak gugus (C-H stretching), pita serapan pada bilangan gelombang 1658,78
yang merupakan daerah (C=O).
Spektrum FTIR dari kitosan bead menunjukkan adanya serapan pada daerah
bilangan gelombang (cm-1) : 3448,72 yang merupakan daerah (N-H bending dan O-H stertching), pita serapan pada bilangan gelombang 2924,09 merupakan
daerah (C-H stretching), pita serapan pada bilangan gelombang 1635.64 yang
merupakan daerah (C=O).
Spektrum FTIR ikat silang kitosan dengan glutaraldehida menunjukkan serapan
pada daerah bilang gelombang (cm-1) : 2939,52 yang merupakan daerah (C-H yang berikatan dengan C=O), pita serapan bilangan gelombang 1566,20
merupakan (N-H stretching dan N-H .bending).
4.3.2 Adsorpsi Ion Kadmium(Cd2+)
4.4.2.1. Penentuan Waktu Kontak Optimum Dengan Menggunakan Kitosan
Bead Glutaraldehida
Penentuan kadar logam berat cadmium(Cd2+) dalam larutan standar sebelum dan setelah penambahan kitosan bead glutaraldehida dengan menentukan waktu
kontak optimum dilakukan dengan mengukur nilai absorbansi dan konsentrasi
menggunakan alat Spektrofotometer Serapan Atom.
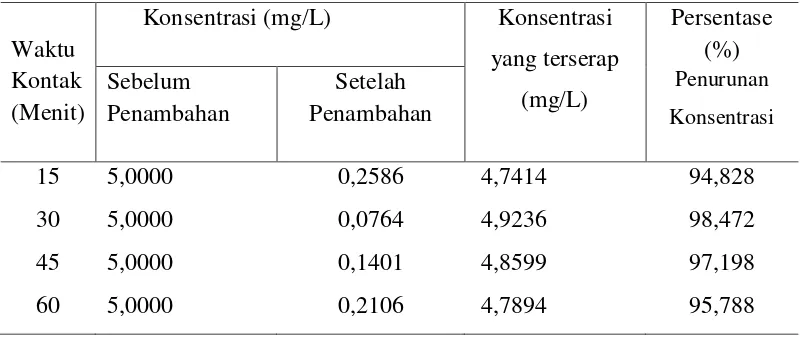
Dari hasil penelitian bahwa persentase (%) penurunan konsentrasi ion
(Cd2+) pada larutan standar sebelum penambahan kitosan memiliki konsentrasi 5,0000 mg/L dan setelah penambahan kitosan bead glutaraldehida konsentrasi
berkurang menjadi, 0,2586; 0,0764; 0,1401; dan 0,2106 dengan variasi waktu
kontak 15; 30; 45; dan 60 menit. Dengan kata lain, persentase penurunan
konsentrasi ion (Cd2+) masing- masing 94,828%; 98,472%; 97,198% dan 95,788%.
Dari data tampak bahwa daya serap kitosan yang telah dimodifikasi
dengan ikat silang glutaraldehida dapat meningkatkan daya serap terhadap logam
berat, Hai ini disebabkan oleh karena adanya asam lemah encer pada matriks
kitosan bead yang menyebabkan gugus -NH2 kitosan bead memiliki afinitas lebih tinggi dibandingkan kitosan tanpa modifikasi. Afinitas yang dimiliki kitosan bead
menyebabkan kemampuan kitosan bead dalam menyerap logam-logam berat.
Agen penautsilang yang digunakan seperti glutaraldehida dapat meningkatkan
proses penjerapan berdasarkan mekanisme reaksi basa schif dimana pasangan
elektron bebas pada gugus N akan berikatan kuat dengan logam yang bermuatan
positif(menyumbang 2 elektron dari Cd) serta kitosan glutaraldehid dapat
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian yang dilakukan, dapat diambil kesimpulan :
1. Kitosan limbah kulit udang dapat dimodifikasi menjadi kitosan bead yang
diikatsilang dengan glutaraldehida.
2. Pengaruh waktu optimum terhadap penyerapan dengan metode
perendaman berdasarkan variasi waktu kontak 15; 30; 45; dan 60 menit
dengan penurunan konsentrasi 0,2586; 0,0764; 0,1401; dan 0,2106
Dengan persentase penurunan konsentrasi ion (Cd2+) masing- masing 94,828%; 98,472%; 97,198% dan 95,788%. dimana pada proses
perendaman akan terjadi interaksi kimia antar permukaan adsorben
(kitosan glutaraldehida) akan membentur adsorbat (ion logam Cd2+), namun waktu yang terlalu lama dapat membuat kinerja penyerapan
semakin berkurang.
3. Waktu kontak optimum pada kitosan bead glutaraldehid adalah 30 menit
dengan persentase penurunan 98,472%
5.2. Saran
1. Disarankan penelitian selanjutnya dapat melakukan penelitian modifikasi
kitosan dengan membuat kitosan nanopartikel yang diikatsilang dengan
agen penautsilang untuk penyerapan pestisida terhadap tanaman pangan.
2. Disarankan penelitian selanjutnya dapat mengembangkan modifikasi
kitosan yang kegunaannya untuk bidang farmasi(obat-obatan) seperti
BAB 2
TINJAUAN PUSTAKA
2.1. Kitin
Kitin merupakan poli (2-asetamido-2-deoksi-β-(1 4)-D-glukopiranosa) dengan
rumus molekul (C8H13NO5)n yang tersusun atas 47% C, 6% H, 7% N, dan 40% O. Struktur kitin menyerupai struktur selulosa dan hanya berbeda pada gugus yang
terikat diposisi atom C-2. Gugus pada selulosa adalah gugus hidroksil, sedangkan
pada C-2 kitin adalah gugus N-asetil(-NHCOCH3asetamida). Seperti yang tampak pada (gambar 2.1) dibawah ini:
O
Gambar 2.1. Struktur polimer selulosa (R= -OH) dan kitin (R= -NHCOCH3) (Sugita, 2009)
Di alam, kitin dikenal sebagai polisakarida yang paling melimpah setelah selulosa,
kitin umumnya banyak dijumpai pada hewan avertebrata laut, darat, dan jamur
dari genus mucor, phycomyces, dan saccharomyces (Hirano,1986; Knorr,1991). Keberadaan kitin di alam umumnya terikat dengan protein, mineral, dan berbagai
pigmen. sebagai contoh, kulit udang mengandung 25-40% CaCO3, dan 15-20% kitin, tetapi besarnya komponen tersebut masih bergantung pada jenis
udangnya(Altschul,1976). Sebagian besar kelompok Crustacea, seperti kepiting, udang, dan lobster merupakan sumber utama kitin komersial. Di dunia, kitin yang
diproduksi secara komersial 120 ribu ton pertahun. Kitin yang berasal dari
kepiting dan udang sebesar 39 ribu ton (32,5%)dan dari jamur 32 ribu ton(26,7%)
Spesifikasi Kitin dapat dilihat pada tabel 2.1 berikut:
Tabel 2.1. Spesifikasi kitin
Parameter Ciri – ciri
Ukuran partikel Serpihan dalam bentuk serbuk
Kadar air (%) ≤ 10,0
- Pelarut organik Tidak larut
- LiCl2/ dimetilasetamida Sebagian larut
Enzim pemecah Lisozim dan kitinase
(Sugita, 2009)
2.2. Kitosan
Kitosan adalah poli-(2-amino-2-deoksi-β-(1 4)-D-glukopiranosa) dengan
rumus molekul (C6H11NO4)n yang dapat diperoleh dari deasetilasi kitin. Kitosan juga dijumpai secara alamiah di beberapa organisme. Struktur polimer kitosan
dapat dilihat pada gambar (Gambar 2.2.) di bawah ini :
O
Gambar 2.2. Struktur polimer kitosan (Sugita, 2009)
Proses deasetilasi kitosan dapat dilakukan dengan cara kimiawi maupun
enzimatik. Proses kimiawi menggunakan basa, misalnya NaOH, dan dapat
menghasilkan kitosan dengan derajat deasetilasi yang tinggi, yaitu mencapai
85-93 % (Tsigos et al., 2000). Namun proses kimiawi menghasilkan kitosan dengan
2.3. Transformasi kitin menjadi kitosan secara kimia
2.3.1. penghilangan protein
Deproteinasi kitin merupakan reaksi hidrolisis dalam suasana asam atau basa.
Lazimnya, hidrolisis dilakukan dalam suasana basa dengan menggunakan larutan
NaOH 2-3% pada suhu 63-65oC selama 1-2 jam (Johnson et al,1982). Efisiensi deproteinasi tidak hanya bergantung pada konsentrasi basa dan suhu, tetapi juga
spesies sumber kitin pada tahap deproteinasi, protein diubah menjadi garam
natrium proteinat yang larut air
Kerangka luar Crustacea mengandung kitin yang berikatan dengan kalsium karbonat (CaCO3) dan protein (Austin, 1988), terkadang juga dengan lapisan lilin, kadar protein yang terikat dalam matriks kulit sekitar 30-40% dari
komponen organik totalnya (Johnson et al, 1982). protein terikat secara fisik dan sebagian lainnya terikat secara kovalen yang kadarnya beragam untuk setiap jenis
crustacea. Austin (1988) menyatakan, bahwa dari jumlah protein total dalam
udang (34%) dengan kontribusi protein yang terikat secara kovalen dan fisik
berturut-turut adalah sekitar 16 dan 18%.
2.3.2. Penghilangan Mineral
Hal yang terpenting dalam tahap penghilangan mineral adalah jumlah asam yang
digunakan (Shadidi et al, 1991). Ion mineral ditentukan melalui destruksi dengan asam kuat HCl terhadap abu dari endapan yang diperoleh pada tahap pemisahan
mineral, selanjutnya penetapan ion mineral dilakukan menggunakan metode
Spektroskopi Serapan Atom (AAS).
2.3.4. Penghilangan gugus asetil (Deasetilasi)
Kandungan gugus asetil pada kitin secara teoretis ialah sebesar 21,2% (No et
al.,1989). Deasetilasi secara kimiawi dapat dilakukan dengan menggunakan basa
kuat NaOH atau KOH. Penggunaan KOH ini dapat memutuskan ikatan hidrogen
2.4. Sifat Fisika-Kimia pada Kitosan
Kitosan merupakan padatan amorf yang berwarna putih kekuningan dengan rotasi
spesifik [ ] -3 ingga -10 pada kon ent a i a am a etat 2 ito an la ut
pada kebanyakan larutan asam organik (Tabel 2.2.) pada pH sekitar 4,0, tetapi
tidak larut pada pH lebih besar dari 6,5, juga tidak larut dalam pelarut air, alkohol,
dan aseton. Dalam asam mineral pekat seperti HCl dan HNO3, kitosan larut pada konsentrasi 0,15-1,1 %, tetapi tidak larut pada konsentrasi 10%. Kitosan tidak
larut dalam H2SO4 pada berbagai konsentrasi, sedangkan didalam H3PO4 tidak larut pada konsentrasi 1% sementara pada konsentrasi 0,1% sedikit larut. Perlu
untuk kita ketahui,bahwa kelarutan kitosan dipengaruhi oleh bobot molekul,
derajat deasetilasi, dan rotasi spesifiknya yang beragam bergantung pada sumber
dan metode isolasi serta transformasinya.
Tabel 2.2. Kelarutan kitosan pada berbagai pelarut asam organik
Konsentrasi asam organik Konsentrasi asam organik (%)
2.5. Keterkaitan Sifat Fisik –Kimia pada Kitosan
Kitosan dalam bentuk terprotonasi menunjukkan kerapatan muatan yang
tinggi dan bersifat sebagai polielektrolit kationik, seperti yang dapat dilihat pada
Gambar 2.3 dan sangat efektif berinteraksi dengan biomolekul bermuatan negatif
dan biomolekul permukaan. Sedangkan dalam bentuk netralnya, kitosan mampu
mengompleks ion logam berat berbahaya seperti Cu, Cr, Cd, Mn, Co, Ph, Hg, Zn,
dan Pd.
Gambar 2.3. Kitosan sebagai polielektrolit kationik (Sugita, 2009)
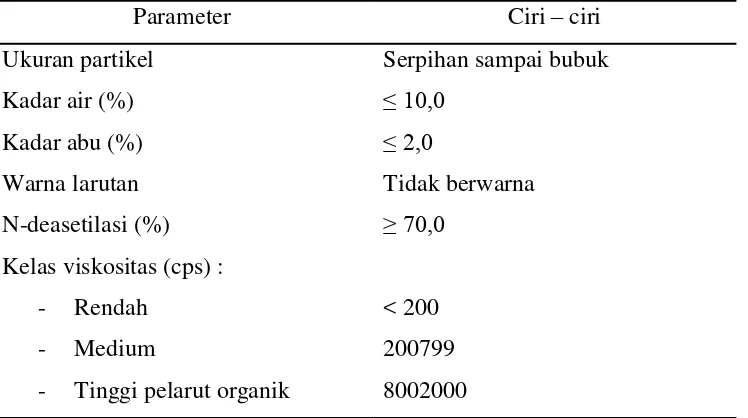
Spesifikasi Kitin dapat dilihat pada tabel 2.3 dibawah ini:
Tabel 2.3. Spesifikasi kitosan
Parameter Ciri – ciri
Ukuran partikel Serpihan sampai bubuk
Kadar air (%) ≤ 10,0
- Tinggi pelarut organik 8002000
2.6. Modifikasi Kitosan
Kitosan dapat dimodifikasi, kitosan sebagai adsorben dapat berada dalam berbagai
bentuk, antara lain bentuk butir, serpih, hidrogel, dan membran (film). Kitosan
sebagai adsorben sering dimanfaatkan untuk proses adsorpsi ion logam berat.
Besarnya afinitas kitosan dalam mengikat ion logam sangat bergantung pada
karakteristik makrostruktur kitosan yang dipengaruhi oleh sumber dan kondisi
pada luas permukaannya. Semakin kecil ukuran kitosan akan semakin besar dan
proses adsorpsi pun dapat berlangsung dengan baik. Modifikasi kimia kitosan
menjadi gel kitosan dapat meningkat kapasitas jerapnya, keunggulan ini
disebabkan oleh bentuk butiran gel mempunyai volume pori yang lebih besar
dibandingkan dengan bentuk serpihan. Kitosan dengan bobot molekul tinggi akan
menghasilkan larutan dengan viskositas yang tinggi pula (Rao, 1993)
2.6.1. Glutaraldehida
Glutaraldehida merupakan agen penaut silang kitosan yang paling banyak
digunakan. Glutaraldehida dapat menautsilangkan rantai kitosan melalui reaksi
pembentukan basa Schiff (imina tersubstitusi ,-CH=NR) antara gugus aldehida
glutaraldehida dan guggus –NH2 kitosan. Jumlah tautan silang tersebut meningkat seiring dengan bertambahnya jumlah glutaraldehida yang ditambahkan. Tautan
silang tersebut telah terbukti dapat menghilangkan stabilitas adsorben kitosan
dalam asam. Namun derajat tautan silang yang terlalu tinggi juga akan
menurunkan jumlah –NH2, sehingga kapasitas adsorpsi maksimumnya juga menurun. Selain itu reaksi glutaraldehida dan kitosan juga dapat melemahkan
ikatan antara atom nitrogen dan ion logam yang akan dijerap (Osifo et al, 2008).
Struktur kimia glutaraldehida dapat dilihat pada gambar 2.4 berikut;
O O
H H
2.7. Aplikasi Kitosan dalam Bidang Lingkungan
Lingkungan sangat berpotensi tercemar zat organik, anorganik, maupun logam
berat. Keberadaan zat-zat pencemar tersebut akan mengganggu ekosistem yang
ada, termasuk juga manusia. Oleh sebab itu, kelestarian lingkungan dari zat
pencemar harus dijaga dan terus mendapatkan perhatian dari masyarakat sekitar,
yang merupakan elemen dari lingkungan hidup itu sendiri. Salah satu cara yang
dapat digunakan untuk mengurangi zat pencemar pada lingkungan adalah dengan
menggunakan kitosan sebagai adsorben.
Kitosan lazimnya disintesis dari deasetilasi kitin yang berasal dari limbah
kulit udang atau kepiting. Oleh karena itu, penggunaan kitosan sejak awal telah
berperan dalam mengurangi pencemaran lingkungan. Manfaat kitosan dalam
bidang lingkungan adalah untuk menjerap logam berat maupun zat warna yang
banyak dihasilkan dari industri tekstil atau kertas. Logam berat merupakan limbah
yang sangat berbahaya. Hal tersebut dikarenakan logam berat dapat menimbulkan
toksisitas akut pada manusia maupun habitat yang ada di lingkungan perairan.
2.7.1. Logam Berat
Logam berat didefinisikan sebagai logam yang memiliki densitas atau kerapatan
tinggi dan merupakan pencemar yang banyak dijumpai baik di lingkungan darat
maupun di perairan. Keberadaan logam berat akan membawa pengaruh pada
kehidupan organisme di lingkungan (termasuk manusia), karena sifatnya yang
meracun dan dapat menyebabkan kematian apabila jumlahnya melewati ambang
batas yang ditetapkan. Kandungan logam berat di lingkungan dapat dikurangi
dengan cara menjerapnya, salah satunya dengan menggunakan kitosan. Beberapa
contoh logam berat adalah Hg,Zn,Cd,Cu,Co,Pb dan Cr. Proses penjerapan logam
2.7.2. Zat Warna
Pada umumnya zat warna yang masuk ke dalam lingkungan berasal dari limbah
tekstil dan kertas. Zat warna kedua industri tersebut menimbulkan warna yang
sangat pekat walaupun dalam konsentrasi yang rendah,sehingga dampaknya dapat
mengurangi estetika lingkungan, selain itu limbah zat warna bersifat karsinogenik
jika dikonsumsi dan sulit terdegradasi.
Berdasarkan muatannya, zat warna dapat dibedakan menjadi 2, yaitu zat warna
anionik dan kationik. Kedua zat warna tersebut dapat dijerap dengan kitosan dan
modifikasinya (Singh et al.,2008). Zat warna anionik dan asam,zat warna anionik
sebagian besar merupakan senyawaan azo yang mengandung gugus
sulfonat,sebagaimana diketahui,bahwa zat warna tersebut lebih banyak digunakan
dalam industri tekstil. zat warna kationik. Berbeda dengan zat warna anionik,
muatan positif pada zat warna kationik disebabkan oleh keberadaan garam
kuartener sekunder. Karena muatannya yang positif, zat warna kationik akan
terjerap dengan baik pada kitosan dengan kitosan dengan kondisi netral atau basa
untuk mencegah protonasi pada gugus amino kitosan.
2.7.3. Pestisida
Dua jenis pestisida yang paling penting ialah organoklorin dan organofosforus.
Organoklorin stabil secara kimia dan resisten terhadap penguraian mikrob.
Beberapa contoh organoklorin yang lazim menjadi polutan ialah
diklorofeniltrikloroetana (DDT) dan turunannya, poliklorinasi bifenil (PCB).
Mikrokapsul kitosan yang terkompleks perak dan tertaut glutaraldehida dan
2.7.4. Senyawaan Fenolik
Fenol merupakan polutan organik yang berbahaya bagi organisme perairan dan
manusia walaupun dalam konsentrasi yang rendah, bahkan hanya dalam
konsentrasi 0,005 mg/L saja sudah dapat merubah rasa dan bau pada air
minum,sehingga tidak baik untuk dikonsumsi, manusia yang mengkonsumsi air
yang terkontaminasi fenol akan mengalami beberapa nyeri yang memicu
kerusakan pembuluh kapiler dan berakibat pada kematian, selain itu proses
klorinasi pada air yang tercemar akan berakibatkan pembentukan klorofenol
(Aksu,2005).
2.8. Kandungan logam berat
I tila “logam” eca a k a membe ikan un u yang me upakan kondukto li t ik
yang baik dan mempunyai konduktivitas panas, rapatan, kemudahan ditempa,
kekerasan dan keelektropositifan yang tinggi. (Connel, 1995) Logam berat (heavy
metal) atau logam (toxic metals) adalah bentuk umum yang digunakan untuk
menjelaskan sekelompok elemen-elemen logam yang kebanyakan tergolong
berbahaya bila masuk ke dalam tubuh mahkluk hidup. Logam berat yang terdapat
baik di lingkungan maupun di dalam tubuh manusia dalam konsentrasi yang
sangat rendah disebut sebagai trace metals. Trace metals seperti Cadmium(Cd),
Timbal (Pb), dan Merkuri (Hg) (Nugroho, 2006).
2.8.1 Efek Toksik Kadmium
Kadmium (Cd) belum diketahui fungsinya secara biologis dan dipandang sebagai
xenobiotik dengan toksisitas yang tinggi dan merupakan unsur lingkungan yang
persisten.Keracunan yang disebabkan oleh Cd bisa bersifat akut dan kronis,
keracunan akut Cd sering terjadi pada pekerja di industri yang berkaitan dengan
Cd. Gejala keracunan akut Cd adalah timbulnya rasa sakit dan panas di dada.
Paparan Cd secara akut bisa menyebabkan nekrosis pada ginjal dan iritasi alat
2.9. Spektrofotometri Serapan Atom
Spektrofotometri serapan atom adalah metoda pengukuran kuantitatif
suatu unsur yang terdapat dalam suatu cuplikan berdasarkan penerapan cahaya
pada panjang gelombang tertentu oleh atom – atom bentuk gas dalam keadaan
dasar. telah lama ahli kimia menggunakan pancaran radiasi oleh atom yang
dieksitasikan dalam suatu nyala sebagai alat analisi. fraksi atom – atom yang
tereksitasi berubah secara eksponensial dengan temperatur. tekni ini digunakan
untuk penetapan sejumlah unsur, kebanyakan logam dan sampel yang sangat
beraneka ragam (Walsh , 1955).
2.9.1 Prinsip dan Teori
Spektrofotometri serapan atom didasarkan pada bahwa atom – atom pada suatu
unsur dapat mengabsropsi energi sinar pada panjang gelombang tertentu. banyak
energi sinar yang di absropsi berbanding lurus dengan jumlah atom – atom unsur
yang mengabsropsi. Atom terdiri atas inti atom yang mengandung proton
bermuatan positif dan neutron berupa pertikel netral, dimana inti atom
dikelilingi oleh elektron –elektron bermuatan negatif pada tingkat energi yang
berbeda – beda. Jika energi diabsropsi oleh atom, maka elektron yang berada di
kulit terluar ( electron valensi ) akan tereksitasi dan bergerak dari keadaan dasar
atau tingkat energi yang terendah kekeadan tereksitasi dengan tingkat energi yang
terendah. Jumlah energi yang dibutuhkan untuk memindahkan elektron ke tingkat
energi tertentu dikenal sebagai potensial eksitasi untuk tingkat energi tersebut
(Clark, 1979).
2.9.2 Instrumentasi
Untuk keperluan analisis kuantitatif dengan spektrofotometer serapan atom, maka
sampel harus dalam bentuk larutan. Untuk menyiapkan larutan, sampel harus
diperlukan sedemikian rupa yang pelaksanaannya tergantung dari macam dan
jenis sampel. Yang penting untuk diingat adalah bahwa larutan yang akan
Ada beberapa cara untuk melarutkan sampel, yaitu:
Langsung dilarutkan dengan pelarut yang sesuai
Sampel dilarutkan dalam suatu asam
Sampel dilarutkan dalam suatu basa atau dilebur dahulu dengan basa
kemudian hasil leburan dilarutkan dengan pelarut yang sesuai
Metode pelarutan apapun yang akan dipilih untuk dilakukan analisis dengan
spektrofotometer serapan atom, yang terpenting adalah bahwa larutan yang
dihasilkan harus jernih, stabil dan tidak mengganggu zat-zat yang akan dianalisis.
Pelarutan juga dimaksudkan untuk destruksi sampel dimana sampel dimana
biasanya digunakan asam-asam seperti asam nitrat pekat (Rohman, 2007)
Komponen penting yang membentuk spektrofotomter serapan atom diperlihatkan
pada gambar 2.5 dibawah ini.
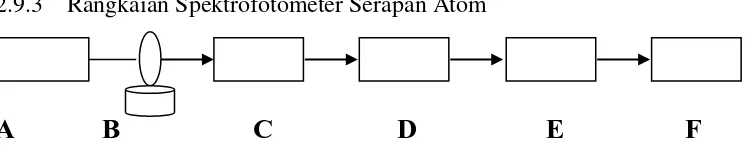
2.9.3 Rangkaian Spektrofotometer Serapan Atom
A
B
C
D E
F
Gambar 2.5. Rangkaian ringkas Spektrofotometer Serapan Atom
Keterangan Gambar :
Sumber sinar yang lazim dipakai adalah lampu katoda berongga. Lampu ini terdiri
b. Tempat sampel
Dalam analisis dengan spektofotometri serapan atom, sampel yang akan dianalisis
harus diuraikan menjadi atom-atom netral yang masih dalam keadaan asas. Ada
berbagai macam yang dapat digunakan untuk mengubah suatu sampel menjadi
uap atom-atom yaitu dengan nyala dan tanpa nyala.
1. Nyala (flameless)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan
menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi.
2. Tanpa nyala(flameless)
Pengatoman dapat dilakukan dalam tungku dari grafit. Sampel diletakkan dalam
tabung grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris dengan
cara melewatkan arus listrik grafit. Akibat pemanasan ini,maka gas yang akan
dianalisis berubah menjadi atom-atom netral (Rohman, 2007).
c. Monokromator
Monokromator memisahkan,mengisolasi dan mengontrol intensitas dari radiasi
energi yang mencapai detektor (Haswell, 1991).
d. Detektor
Detektor dapat diatur sedemikian rupa pada nilai frekuensi tertentu, sehingga tidak
memberikan respon terhadap nilai emisi yang berasal dari eksitasi
termal.(Khopkar, 2007).
e. Read Out
Merupakan suatu alat petunjuk atau dapat juga diartikan sebagai sistem beberapa
2.9.4 Gangguan pada SSA dan cara mengatasinya
Gangguan nyata pada SSA adalah seringkali didapatkan suatu harga yang tidak
sesuai dengan konsentrasi sampel yang ditentukan. Penyebab dari gangguan ini
adalah faktor matriks sampel dan faktor kimia karena adanya gangguan molekuler
yang bersifat radiasi.
Sampel dalam bentuk molekul karena disosiasi yang tidak sempurna akan
cenderung mengabsorpsi radiasi dari sumber radiasi. Demikian juga terjadinya
ionisasi atom akan menjadi kesalahan pada SSA oleh karena spektrum radiasi oleh
ion jauh berbeda denga spektrum absorpsi atom netral yang memang akan
ditentukan. Ada beberapa usaha untuk mengurangi gangguan kimia pada SSA
yaitu dengan cara:
1. Menaikkan temperatur nyala agar mempermudah penguraian untuk itu
dipakai gas pembakar campuran C2H2 + N2O yang memberikan nyala dengan temperatur yang tinggi.
2. Menambahkan elemen pengikat gugus atom penyangga, sehingga terikat
kuat akan tetapi atom yang ditentukan bebas sebagai atom netral. Misalnya
penentuan logam yang terikat sebagai garam, dengan penambahan logam
yang lainnya akan terjadi ikatan lebih kuat dengan anion pengganggu.
3. Pengeluaran unsur pengganggu dari matriks sampel dengan cara eksitasi
(Mulja, 1995).
2.10. FTIR (Fourier Transform Infra Red)
Pancaran infra merah pada umumnya mengacu pada bagian spektrum
elektromagnetik yang terletak di antara daerah tampak dan daerah gelombang
Salah satu hasil kemajuan instrumentasi IR adalah pemrosesan data
seperti Fourier Transform Infra Red (FTIR). Teknik ini memberikan informasi
dalam hal kimia, seperti struktur dan konformasional pada polimer dan
polipaduan, perubahan induksi tekanan dan reaksi kimia. Dalam teknik ini
padatan diuji dengan cara merefleksikan sinar infra merah yang melalui tempat
kristal sehingga terjadi kontak dengan permukaan cuplikan. Sensitivitas FTIR
adalah 80-200 kali lebih tinggi dari instrumentasi dispersi standar karena
resolusinya lebih tinggi (Kroschwitz, 1990).
Teknik pengoperasian FTIR berbeda dengan spektrofotometer infra
merah. Pada FTIR digunakan suatu interferometer Michelson sebagai pengganti
monokromator yang terletak di depan monokromator. Interferometer ini akan
memberikan sinyal ke detektor sesuai dengan intensitas frekuensi vibrasi molekul
yang berupa interferogram (Bassler, 1986).
Interferogram juga memberikan informasi yang berdasarkan pada
intensitas spektrum dari setiap frekuensi. Informasi yang keluar dari detektor
diubah secara digital dalam komputer dan ditransformasikan sebagai domain,
tiap-tiap satuan frekuensi dipilih dari interferogram yang lengkap (fourier transform).
Kemudian sinyal itu diubah menjadi spektrum IR sederhana. Spektrofotometer
FTIR digunakan untuk :
1. Mendeteksi sinyal lemah.
2. Menganalisis sampel dengan konsentrasi rendah.
2.11 Reaksi Ikat Silang
Ikatan silang merupakan ikatan yang menghubungkan rantai polimer yang
satu dengan rantai polimer yang lain di mana ikatan tersebut berupa ikatan
kovalen atau ionik. Reaksi ikat silang memberikan pengaruh yang besar baik
dalam sifat kimia maupun sifat mekanik dari polimer (Nicholson, 2006).
Pembentukan ikat silang dilakukan dengan penambahan suatu agen pengikat
silang ke dalam larutan bahan yang akan dimodifikasi (Berger et al, 2004).
Ikatan silang dapat terjadi dengan dua cara, yaitu dengan membentuk
ikatan kovalen dan dengan membentuk ikatan ionik. Dalam reaksi pembentukan
ikatan silang kovalen, agen pengikat silang yang umum digunakan adalah
dialdehid, contohnya glioksal dan glutaraldehid (Monteiro et al, 1999).
Akan tetapi, kedua agen pengikat silang tersebut bersifat toksik.
Glutaraldehid bersifat neurotoksik, sedangkan glioksal bersifat mutagenik.
Meskipun hasil modifikasi tersebut dimurnikan sebelum pemberian, keberadaan
dialdehid bebas yang tidak ikut bereaksi tidak seluruhnya dapat dihilangkan dan
dapat memberikan efek toksik.
Agen pengikat silang kovalen lainnya yang dapat digunakan untuk
membentuk reaksi ikat silang dengan kitosan telah banyak diteliti sebagai
alternatif pilihan. Di samping dialdehid, asam oksalat dan genipin terbukti dapat
digunakan sebagai agen pengikat silang. Akan tetapi, sampai saat ini belum ada
data yang lengkap mengenai biokompatibilitas dari senyawa-senyawa tersebut.
Kebanyakan agen pengikat silang yang membentuk ikatan kovalen dapat
menginduksi toksisitas jika sebelum pemberian masih terdapat sisa dari pereaksi.
Untuk mengatasi masalah toksisitas yang terjadi tersebut, dapat dilakukan reaksi
ikat silang ionik. Kitosan bersifat polikationik dalam lingkungan asam. Sifat ini
menyebabkan terjadinya interaksi dengan komponen bermuatan negatif (anionik),
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Dewasa ini aplikasi kitin dan kitosan sangat banyak dan meluas. Dibidang industri
kitin dan kitosan berperan antara lain sebagai koagulan polielektrolit pengolahan
limbah cair ,pengikat dan penjerap ion logam, mikroorganisme, mikroalga,
pewarna residu pestisida, lemak, tanin, dan lain sebagainya, sementara dibidang
pertanian dan pangan kitin dan kitosan digunakan antara lain untuk pencampuran
ransum pakan ternak, antimikrob, anti jamur serat bahan pangan, penstabilisasi
pembentuk gel, pembentuk tekstur, pengental, pengemulsi produk olahan pangan,
pembawa zat aditif makanan. Sedangkan dalam bidang farmasi dan kedokteran
kitosan dapat digunakan sebagai bahan pembuat obat-obatan, anti tumor, anti
virus, pembuluh darah kulit dan ginjal sintetik, aditif kosmetik, anti infeksi,
pembalut luka dan benang bedah yang mudah diserap (Sugita, 2009)
Modifikasi kitosan sebagai adsorben dapat berada dalam berbagai bentuk, antara
lain bentuk butir, serpih, hidrogel, membran(film). Kitosan sebagai adsorben
sering dimanfaatkan untuk proses adsorpsi ion logam berat. . Kemampuan kitin
dan kitosan dalam mengadsorpsi logam berat dipengaruhi oleh jumlah gugus –
NH2 yang ditunjukkan oleh derajat deasetilasi. Kitosan dapat disintesis menjadi kitosan bead yang tidak larut dalam asam sehingga dapat dimanfaatkan lebih luas.
Adanya asam lemah encer dalam matriks kitosan bead menyebabkan gugus –NH2 kitosan bead memiliki afinitas lebih tinggi dibanding kitosan. Afinitas yang
dimiliki kitosan bead menyebabkan meningkatnya kemampuan kitosan bead
dalam mengadsorpsi logam berat. Kemampuan penjerapan dapat ditingkatkan
Berbagai modifikasi kitosan telah dimanfaatkan dalam berbagai bidang salah
satunya sebagai adsorben logam-logam berat seperti penelitian oleh Antuni, dkk
melakukan penelitian mengenai “Penggunaan kitosan dari cangkang udang untuk penjerapan berbagai logam berat dan diperoleh hasil efesiensi penjerapan kitosan
yang optimum berturut-turut untuk logam Cr, Fe, Cu, Ni dan Zn adalah 98,44%
untuk berat kitosan 0,375 gram), 99,21% (0,5 gram); 58,62% (0,375 gram);
99,65% (0,375); 56% (0,5 gram) dan pada tahun 2012 Indah, L melakukan
Modifikasi kitosan menjadi kitosan glutaraldehid untuk meningkatkan daya serap
terhadap ion logam (Cu2+) mengalami penurunan konsentrasi sebesar 73%.
Berdasarkan latar belakang ini peneliti tertarik untuk memodifikasi kitosan
dengan mengikatsilangkannya dengan Glutaraldehida untuk penyerapan logam
Cadmium (Cd2+) berdasarkan variasi waktu.
1.2. Permasalahan
1. Bagaimana modifikasi kitosan menjadi kitosan bead yang terikatsilang dengan Glutaraldehida?
2. Bagaimana pengaruh daya serap kitosan terhadap logam berat Cd2+? 3. Berapakah waktu kontak optimum penyerapan ion Cd2+ menggunakan
kitosan bead yang diikatsilang dengan Glutaraldehida
1.3. Pembatasan Masalah
1. Sampel yang digunakan adalah kitosan dari limbah kulit udang 2. Modifikasi kitosan dibuat menjadi kitosan bentuk bead/manik 3. Kitosan bead diikatsilangkan dengan menggunakan Glutaraldehida 4. Konsentrasi ion Cd2+ yang digunakan dalam percobaan adalah
5 mg/L sebanyak 50 mL
1.4. Tujuan Penelitian
1 Untuk mengetahui modifikasi kitosan menjadi kitosan bead yang terikatsilang dengan Glutaraldehida.
2 Untuk mengetahui pengaruh daya serap kitosan bead Glutaraldehid terhadap logam berat Cd2+ .
3 Untuk mengetahui waktu kontak optimum penyerapan ion Cd2+ menggunakan kitosan bead Glutaraldehida.
1.5. Manfaat Penelitian
Hasil yang diperoleh dari penelitian ini diharapkan dapat menjadi salah
satu informasi ilmiah bahwa modifikasi kitosan bead/manik yang diikatsilangkan
hlutaraldehida untuk penanggulangan pencemaran logam berat seperti logam
Cd2+ berdasarkan waktu kontak optimum.
1.6. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik, Fakultas
Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara. Analisis
gugus fungsi menggunakan spektrofotometer Fourier Transform Infra Red (FTIR)
di Laboratorium Kimia Organik, Fakultas Matematika dan Ilmu Pengetahuan
Alam Universitas Gajah Mada. Analisa logam Cadmium dilakukan di Badan Riset
1.7. Metodologi Penelitian
1. Penelitian ini dilakukan secara eksperimen laboratorium.
2. Pembuatan kitosan bead/manik dengan cara menimbang kitosan dan dilarutkan dalam asam asetat 5% dengan ratio perbandingan 1:40 dan selanjutnya diteteskan dalam larutan NaOH 2 M hingga terbentuk bead. kemudian dicuci dengan aquades dan dikeringkan. Kitosan bead diikatsilangkan dengan glutaraldehida dan perendaman selama 24 jam dengan perbandingan 1,5 ml/g kitosan bead. Hasil dikarakterisasi dengan spektrofotometer FTIR.
3. Analisa logam Cd2+ sebelum dan sesudah penyerapan dengan kitosan dianalisa dengan menggunakan Spektrofotometer Serapan Atom
Adapun variabel yang digunakan dalam penelitian ini adalah
1. Variabel terikat meliputi:
a) Konsentrasi ion Cd2+ yang digunakan adalah 5 mg/L
b) Volume ion Cd2+ yang digunakan pada penyerapan adalah 50 mL c) Metode penyerapan dengan menggunakan alat kolom berdasarkan
perendaman variasi waktu kontak 2. Variabel bebas meliputi
ANALISIS DAN KARAKTERISASI, KITOSAN BEAD/MANIK DENGAN IKAT SILANG GLUTARALDEHIDA SEBAGAI
ADSORBEN UNTUK MENURUNKAN KADAR IONLOGAM KADMIUM (Cd2+)
ABSTRAK
Penelitian mengenai analisis dan karakterisasi kitosan bead/manik dengan ikat silang glutaraldehida sebagai adsorben untuk menurunkan kadar ion logam kadmium(Cd2+) telah dilakukan. Pada penelitian ini, didahului dengan pembuatan kitosan bead/manik dengan mencampurkan kitosan dan asam asetat 5% dan diteteskan kedalam larutan NaOH 2M yang kemudian membentuk gel (bead). Kitosan bead yang telah dikeringkan direndam selama 24 jam dalam larutan Glutaraldehida 2,5% dengan perbandingan 1,5 mL tiap gram kitosan, dicuci dan dikeringkan, sebanyak 2 gram kitosan ikat silang glutaraldehida dimasukkan ke dalam kolom, lalu ditambahkan dengan 50 mL larutan standar kadmium 5mg/L.didiamkan berdasarkan variasi waktu. Hasil penelitian menunjukkan bahwa proses adsorpsi diperoleh persentase penyerapan 98,472% pada waktu kontak optimum 30 menit.
ANALYSIS AND CHARACTERIZATION OF BEAD CHITOSAN WITH GLUTARALDEHYDE CROSSLINKING AS REDUCING
ADSORBENT CADMIUM METAL CONTENT
ABSTRACT
Research on the analysis and characterization of chitosan beads with glutaraldehyde crosslink has been done as an adsorbent to reduce concentration of Cd metal. In this research, preceded by making chitosan beads by mixing chitosan and 5% acetic acid and dropped into a solution of NaOH 2M which then forms gel (bead). Chitosan beads were dried soaked for 24 hours in a solution of Glutaraldehyde 2.5% with a ratio of 1.5 mL per gram of chitosan, washed and dried, 2 grams of glutaraldehyde crosslink chitosan included in the column, then was added with 50 ml of standard solution of cadmium 5mg / L was alllowed by variations in time. The results showed that the adsorption process was gained 98.472% in the percentage of absorption optimum contact time of 30 minutes.
ANALISIS DAN KARAKTERISASI,KITOSAN BEAD/MANIK
DENGAN IKAT SILANG GLUTARALDEHIDASEBAGAI
ADSORBEN UNTUK MENURUNKAN KADAR
ION LOGAM KADMIUM (Cd
2+)
SKRIPSI
AYU MANJA
120802022
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
ANALISIS DAN KARAKTERISASI,KITOSAN BEAD/MANIK
DENGAN IKAT SILANG GLUTARALDEHIDA SEBAGAI
ADSORBEN UNTUK MENURUNKAN KADAR ION
LOGAM KADMIUM (Cd
2+)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar sarjana sains
AYU MANJA 120802022
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Analisis Dan Karakterisasi Kitosan Bead/Manik Dengan Ikatan Silang Glutaraldehida Sebagai Adsorben Untuk Menurunkan Kadar Ion Logamcadmium(Cd2+) NIP.195504051983031002 NIP.195308171983031002
Disetujui Oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
ANALISIS DAN KARAKTERISASI, KITOSAN BEAD/MANIK DENGAN IKAT SILANG GLUTARALDEHIDA SEBAGAI
ADSORBEN UNTUK MENURUNKAN KADAR ION LOGAM KADMIUM (Cd2+)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Mei 2016
PENGHARGAAN
Puji dan syukur penulis ucapkan kepada Allah SWT karena dengan limpahan karunia-Nya, penulis dapat menyelesaikan penelitian dan skripsi ini sebagai salah satu persyaratan yang harus dipenuhi untuk mendapat gelar Sarjana Sains di Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Ucapan terima kasih penulis sampaikan kepada Ibu tercinta Fatmawati dan ayah tercinta Alm Zurli,Sk yang telah memberikan doa cinta dan kasih sayang nya serta perjuangan buat kami anak-anaknya, serta kepada keluarga abang dan kakak tersayang,bg Ali, bg Hendrik,bg ijol, kak mery, kk iip, kk maya serta semua keponakan tercinta, dan sanak keluarga yang selama ini memberikan bantuan dan dorongan yang diperlukan.
Ucapan terima kasih juga penulis sampaikan kepada Prof. Dr. Harry Agusnar, M.Sc. selaku pembimbing I yang telah memberikan topik dan tunjuk ajar hingga terselesaikannya penulisan skripsi ini dan Prof. Dr. Zul Alfian, M.Sc. selaku pembimbing II yang pada penyelesaian skripsi ini yang telah memberikan panduan dan penuh kepercayaan kepada penulis untuk menyempurnakannya.
Ucapan terima kasih juga ditujukan kepada ketua dan sekretaris Departemen Kimia, Dr. Rumondang Bulan, MS. dan Drs. Albert Pasaribu, M.Sc., kepala dan laboran Laboratorium Kimia Analitik FMIPA USU, Prof. Dr. Harlem Marpaung dan laboran analitik Sri Pratiwi Aritonang, M,Si serta seluruh staff dosen kimia analitik, abang kakak asisten stambuk 09,010,011.serta terima kasih buat semua asisten analitik teman seperjuangan, Nori, Nany, Ruben, Raniko,Crystina juni,dan Dessy darman yang telah menjadi keluarga kedua dalam hidup saya,terima kasih juga atas bantuan doa dan semangatnya buat adik-adik fitri, Rianda, Jojo, Davi, Dewi dan Ester yang sudah seperti adik kandung bagi saya, serta buat teman-teman stambuk 012, dan kakak abang 09, 010, 011 buat semua pihak yang telah membantu.
ANALISIS DAN KARAKTERISASI, KITOSAN BEAD/MANIK DENGAN IKAT SILANG GLUTARALDEHIDA SEBAGAI
ADSORBEN UNTUK MENURUNKAN KADAR IONLOGAM KADMIUM (Cd2+)
ABSTRAK
Penelitian mengenai analisis dan karakterisasi kitosan bead/manik dengan ikat silang glutaraldehida sebagai adsorben untuk menurunkan kadar ion logam kadmium(Cd2+) telah dilakukan. Pada penelitian ini, didahului dengan pembuatan kitosan bead/manik dengan mencampurkan kitosan dan asam asetat 5% dan diteteskan kedalam larutan NaOH 2M yang kemudian membentuk gel (bead). Kitosan bead yang telah dikeringkan direndam selama 24 jam dalam larutan Glutaraldehida 2,5% dengan perbandingan 1,5 mL tiap gram kitosan, dicuci dan dikeringkan, sebanyak 2 gram kitosan ikat silang glutaraldehida dimasukkan ke dalam kolom, lalu ditambahkan dengan 50 mL larutan standar kadmium 5mg/L.didiamkan berdasarkan variasi waktu. Hasil penelitian menunjukkan bahwa proses adsorpsi diperoleh persentase penyerapan 98,472% pada waktu kontak optimum 30 menit.
ANALYSIS AND CHARACTERIZATION OF BEAD CHITOSAN WITH GLUTARALDEHYDE CROSSLINKING AS REDUCING
ADSORBENT CADMIUM METAL CONTENT
ABSTRACT
Research on the analysis and characterization of chitosan beads with glutaraldehyde crosslink has been done as an adsorbent to reduce concentration of Cd metal. In this research, preceded by making chitosan beads by mixing chitosan and 5% acetic acid and dropped into a solution of NaOH 2M which then forms gel (bead). Chitosan beads were dried soaked for 24 hours in a solution of Glutaraldehyde 2.5% with a ratio of 1.5 mL per gram of chitosan, washed and dried, 2 grams of glutaraldehyde crosslink chitosan included in the column, then was added with 50 ml of standard solution of cadmium 5mg / L was alllowed by variations in time. The results showed that the adsorption process was gained 98.472% in the percentage of absorption optimum contact time of 30 minutes.