59
PENGARUH PERBANDINGAN ETANOL:AIR SEBAGAI PELARUT EKSTRAKSI TERHADAP PEROLEHAN KADAR FENOLAT DAN DAYA
ANTIOKSIDAN HERBA MENIRAN
(
Phyllanthus niruri L.)B.A. Martinus1 , Harrizul Riva’I2
1 STIFI Perintis Padang, 2 Fakultas Farmasi Universitas Andalas Padang
ABSTRAK
Effect of ethanol:water ratio as extraction solvent on obtaining of extractive material, phenolic content and antioxidant activity in Phyllanthus niruri L. herbs have been investigated. The ethanol:water ratio tested were 100:0, 80:20, 70:30, 60:40 and 50:50. Results revealed that ethanol:water ratio gave significant effect on extracted material, phenolic content and antioxidant activity (p<0,05). Among the ethanol:water ratio tested, the best result was obtained by ethanol:water ratio 60:40 as extraction solvent for Pyhllanthus niruri L. herbs to obtain phenolic compound which has antioxidant activity.
Keywords : Phyllanthus niruri L., antioxidant, extraction, phenolic
PENDAHULUAN
Pengembangan bahan obat alam meliputi pengembangan budidayanya sehingga menghasilkan simplisia dengan kualitas yang unggul serta pengembangan cara produksi dan bentuk-bentuk sediaan dari obat-obat tradisional. Obat-obatan yang terbuat dari bahan alam dapat dikelompokkan menjadi tiga yaitu jamu, obat herbal terstandar, dan fitofarmaka. Jamu adalah ramuan tradisional yang belum teruji secara klinis, sedangkan obat herbal yang terstandar adalah yang sudah lulus uji pra klinis. Sementara fitofarmaka adalah suatu sediaan obat bahan alam yang telah dibuktikan keamanan dan khasiatnya secara ilmiah dengan uji praklinik dan uji klinik, bahan baku dan produk jadinya telah distandarisasi. Salah satu bahan baku simplisia yang akan dipakai untuk membuat fitofarmaka ini adalah herba meniran
(Phyllanthus niruri L.) (Nurkhasana, 2006).
Herba meniran mengandung senyawa flavonoid (quarcetin, quercitrin, isoquercitin, astragalin, rutine, physetinglucosid), lignan (phyllanthine, hypophyllanthine, phyltetralin, lintretalin, nirathin, nitretalin, nirphylline, niruri, niruriside), alkaloid (norsecurinine, etnosecurinina, 4-metoxy-norsecurinine, hyllochrysine), terpen (cymene, limonene, lupeol), damar, tanin, dan mineral terutama kalium (Joshi, 1986; Satyanarayana, 1988; Than, 2005). Herba meniran berkhasiat membersihkan hati, anti radang, pereda demam, peluruh kencing, peluruh dahak, peluruh haid, menerangkan penglihatan dan penambah nafsu makan (Heyne, 1987).
60
METODE PENELITIAN Alat – alat
Alat yang digunakan adalah Rotary Evaporator (RVO6-ML kika werke), corong, spatel, cawan penguap, timbangan digital analitik (Denver Instrument Company), aluminium foil, labu ukur, gelas ukur, erlenmeyer, batang pengaduk, pipet gondok, pipet mikro, beaker glass, spektrofotometer UV-Visible mini 1240 (Shimadzu®), Blender, Kertas saring Whatman No.1.
Bahan – bahan
Bahan yang digunakan adalah tanaman herba meniran (Pyllanthus niruri L.), aquadest, metanol p.a (Merck), etanol p.a (Merck), reagen Fenol folin-Ciocalteu (Merck), Natrium Carbonat (Merck), asam galat, DPPH (1,1-diphenyl-2-picrylhydrazyl) p.a (Merck).
Pengambilan sampel
Sampel diambil di sepanjang jalan Bypass Padang, sampel yang akan dianalisa adalah bagian tumbuhan meniran yang berada di atas tanah (Pyhlanthus niruri L.), dibersihkan kemudian dikeringanginkan sampai kering kemudian diserbuk.
Identifikasi Sampel
Identifikasi sampel dilakukan di Herbarium Universitas Andalas (ANDA) dengan nomor koleksi FT-001.
Pembuatan Ekstrak Sampel
herba meniran (5 g) yang telah diserbuk direndam dengan 50 mL etanol-air dengan perbandingan 100:0, 80:20, 70:30, 60:40, 50:50, biarkan selama 24 jam, dalam botol meserasi yang berwarna gelap, sambil
sekali-sekali diaduk, maserat dipisahkan dan sisanya dimaserasi lagi beberapa kali dengan jenis dan jumlah pelarut yang sama, sampai cairan terakhir tidak berwarna. Semua maserat dikumpulkan, diamkan selama dua hari, diendaptuangkan, cairan atas diambil kemudian diuapkan dengan rotary evaporator pada suhu 40 0C dan ditimbang, sebelum dianalisa ekstrak dilarutkan dengan campuran etanol dan air suling sama banyak (1:1) dalam labu ukur 50 mL (Harbone, 1978, Badan Pengawasan Obat, 2004).
Penentuan Kadar Ekstraktif Larutan Sampel
Dari larutan sampel dipipet sebanyak 10 mL, masukkan dalam cawan penguap yang sudah ditara. Uapkan larutan sampel di water bath, kemudian keringkan dalam oven pada suhu 105 0C selama 1 jam kemudian setelah dingin ditimbang. Hitung kadar ekstraktif sampel.
% Ekstraktif = Berat Ekstrak x 100%
Berat Sampel
Pembuatan Reagen
a. Larutan Natrium Karbonat 1 M (Mosquera, 2007)
Ditimbang 5,3 g Na2CO3 dilarutkan dalam aquadest sampai 50 mL, aduk hingga homogen.
b. Larutan DPPH (1,1-diphenyl-2-
picrylhydrazyl) 35 µg/mL
(Keinanen, 1996)
Ditimbang 10 mg DPPH masukkan dalam labu ukur 100 mL, lalu ditambahkan metanol sampai tanda batas kemudian dipipet 17,5 mL larutan DPPH dimasukkan dalam labu ukur 50 mL, lalu tambahkan metanol sampai
61 tanda batas sehingga diperoleh larutan konsentrasi 35 µg/mL.
c. Larutan asam galat 5 mg/mL (Sigma, 2005)
Ditimbang 0,125 g asam galat dimasukkan dalam labu ukur 25 mL, ditambahkan 2,5 mL etanol 96% lalu ditambahkan dengan air suling sampai tanda batas.
Penentuan Kadar Senyawa Fenolat Dengan Metoda Folin-Ciocalteu (Mosquera, 2007, Pourmorad, 2006) a. Penentuan Panjang Gelombang
Serapan Maksimum Asam Galat.
Larutan induk asam galat (5 mg/mL) dipipet sebanyak 1 ml ke dalam labu ukur 50 mL lalu diencerkan dengan campuran metanol dan air suling (1:1) sampai tanda batas. Kemudian dipipet 0,5 mL dan dimasukkan ke dalam vial, tambahkan 5 mL reagen fenol Folin-Ciocalteu yang telah diencerkan dalam air suling 1:10 dan ditambahkan 4 mL natrium karbonat 1 M, kocok homogen. Didiamkan selama 15 menit, kemudian diukur serapannya pada panjang gelombang 400-800 nm dengan spektrofotometer UV-Visebel.
b. Pembuatan Kurva Kalibrasi
Asam Galat
Dari larutan induk asam galat dipipet 0,25; 0,5; 0,75; 1 dan 1,25 mL, diencerkan dengan campuran metanol:aquadest (1:1) dalam labu ukur 50 mL sampai tanda batas sehingga didapatkan konsentrasi 25, 50, 75, 100 dan 125 µg/mL asam galat. Masing-masing konsentrasi larutan dipipet 0,5 mL kemudian dicampur dengan 5 mL pereaksi Folin-Ciocalteu yang sudah diencerkan 1:10 dengan aquadest, ditambahkan 4 mL larutan natrium karbonat 1 M biarkan selama 15 menit,
diukur serapan dengan spektrofotometer UV-Visibel dan dibuat kurva kalibrasi sehingga persamaan regresi liniernya dapat dihitung.
Penentuan Kadar Senyawa Fenolat Total Dengan Metoda Folin-Ciocalteu
Larutan sampel dipipet 0,5 mL dan diencerkan dengan etanol:air suling (1:1) dalam labu ukur 25 mL sampai tanda batas. Dipipet 0,5 mL ekstrak herba meniran kemudian dimasukkan kedalam vial, kemudian ditambahkan 5 mL pereaksi Folin-Ciocalteu yang sudah diencerkan 1:10 dengan aquadest dan 4 ml larutan natrium karbonat 1M, dibiarkan selama 15 menit, diukur serapan maksimum pada panjang gelombang maksimum dengan spektorfotometer UV-Visibel yang akan memberikan komplek warna biru, dilakukan 3x pengulangan sehingga kadar fenolat yang didapat ekivalen dengan mg asam galat /g berat ekstrak kental herba meniran.
Uji Aktivitas Antioksidan Sampel dengan Metoda DPPH (Mosquera, 2007,Pourmorad, 2006)
a. Penentuan Panjang Gelombang
Maksimum DPPH
Sebanyak 4 mL larutan DPPH 35 µg/mL dipipet, masukkan dalam vial dan ditambahkan 2 mL campuran air suling dan metanol (1:1), biarkan selama 30 menit ditempat yang gelap. Serapan larutan diukur dengan spektrofotometer UV-Visible pada panjang gelombang 400-800 nm.
b. Pemeriksaan IC50 Larutan Sampel
Dibuat larutan sampel dengan konsentrasi 40; 50; 60; 70; 80 mg/mL. Masing-masing dipipet sebanyak 2 mL ke dalam vial lalu tambahkan 4 mL larutan DPPH 35 µg/mL. Campuran
62 dihomogenkan dibiarkan selama 30 menit di tempat gelap. Serapan larutan diukur dengan spektrofotometer UV
Visible pada panjang gelombang maksimun.
Hitung % inhibisi dengan menggunakan rumus :
Keterangan :
Abs Kontrol : Serapan larutan radikal DPPH dengan metanol-air (tanpa ekstrak) pada panjang gelombang maksimum.
Abs Sampel : Serapan sampel ditambah DPPH dikurangi dengan serapan sampel blanko (sampel+metanol-air) tanpa DPPH pada panjang gelombang maksimum.
Lalu dibuat kurva antara konsentrasi larutan sampel dan % inhibisi, sehingga diperoleh persamaan regresi liniernya. IC50 larutan sampel adalah konsentrasi larutan sampel yang memberikan inhibisi sebesar 50% yang dapat dihitung menggunakan persamaan regresi linier yang telah diperoleh.
a. Penentuan IC50 Larutan
Pembanding Asam Galat
Dibuat larutan pembanding asam galat dengan konsentrasi 1, 2, 3, 4, dan 5 µg/mL dengan cara memipet 0,01; 0,02; 0,03; 0,04 dan 0,05 mL larutan induk asam galat (5 mg/mL) yang kemudian dilarutkan dengan campuran metanol dan air (1:1) dalam labu ukur 50 mL sampai tanda batas.
Sebanyak 2 mL masing-masing dipipet dan dimasukkan ke dalam vial lalu tambahkan 4 ml larutan DPPH 35 µg/mL. Campuran dihomogenkan dibiarkan selama 30 menit di tempat gelap. Serapan larutan diukur dengan spektrofotometer UV Visible pada panjang gelombang maksimun.
Persentase inhibisi masing-masing dihitiung lalu buat kurva antara konsentrasi larutan pembanding asam galat dan % inhibisi sehingga diperoleh persamaan regresi liniernya. IC50 asam galat adalah kosentrasi larutan pembanding asam galat yang memberikan inhibisi sebesar 50% yang dapat dihitung menggunakan persamaan regresi linier yang telah diperoleh.
Pengolahan Data Secara Anova satu arah
Data hasil penelitian akan diuji secara statistik menggunakan Analisa Variansi (Anova) satu arah. Kadar fenolat total yang diperoleh dari beberapa konsentrasi pelarut ekstraksi etanol diuji dengan Analisa Variasi (Anova) satu arah.
100% x kontrol Abs. sampel Abs. kontrol Abs. inhibisi %
63
HASIL DAN PEMBAHASAN
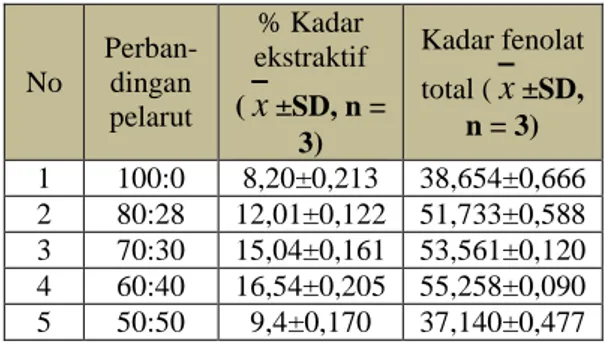
Pada perhitungan kadar ekstraktif dari sampel herba meniran didapatkan ekstrak dengan jumlah terbesar dari perbandingan pelarut etanol:air (60:40) yaitu sebesar 16,54%, seperti terlihat pada tabel I.
Untuk menentukan kadar fenolat total, terlebih dahulu dibuat kurva kalibrasi dari sederet konsentrasi standar asam galat, dimana persamaan regeresi linear yang didapat adalah y = 0,0158 + 0,006384x dengan koefisien korelasi 0,997. Total fenolat dari sampel dinyatakan sebagai kesetaraan dengan mg asam galat per gram sampel kering. Jumlah total fenolat dari tiap sampel bervariasi dengan kadar tertinggi diperolah pada perbandingan pelarut etanol:air (60:40), dapat dilihat pada tabel I. Data ini menunjukkan bahwa pelarut pengekstraksi dengan sistem perbandingan tersebut kemungkinan paling tepat untuk herba meniran.. Tabel I. Persentatse Kadar Ekstraktif
dan Fenolat Total Herba Meniran No Perban-dingan pelarut % Kadar ekstraktif (
x
±SD, n = 3) Kadar fenolat total (x
±SD, n = 3) 1 100:0 8,20±0,213 38,654±0,666 2 80:28 12,01±0,122 51,733±0,588 3 70:30 15,04±0,161 53,561±0,120 4 60:40 16,54±0,205 55,258±0,090 5 50:50 9,4±0,170 37,140±0,477Aktifitas antioksidan yang berasal dari tanaman seringkali dihubungkan dengan kandungan fenolat totalnya. Senyawa-senyawa fenolat telah dilaporkan memiliki aktifitas antioksidan karena sifat redoksnya. Tipe senyawa fenolat yang memiliki aktifitas
antioksidan biasanya adalah seperti asam fenolat dan flavonoid.
Metoda yang digunakan untuk penentuan aktifitas antioksidan adalah dengfan penagkapan radikal DPPH. Daya antioksidan dapat ditentukan dari nilai IC50 yaitu konsentrasi senyawa antioksidan yang memberikan inhibisi terhadap radikal DPPH sebesar 50%. Nilai IC50 yang semakin rendah menunjukkan daya antioksidan yang semakin kuat.
Nilai IC50 terendah didapatkan dari perbandingan pelarut (60:40) sepeti terlihat pada tabel II. Sampel dengan pelarut pengekstraksi ini memperlihatkan suatu korelasi dimana kadar fenolat total tertinggi memberikan daya antioksidan yang paling kuat. Tabel II. Hasil Penentuan IC50 sampel
herba meniran No Perbandingan pelarut IC50 (mg/ml) 1 100:0 50,17 2 80:28 46,44 3 70:30 43,82 4 60:40 42,65 5 50:50 51,21 KESIMPULAN
Dari penelitian ini dapat dilihat bahwa pemakaian pelarut dengan berbagai perbandingan dapat mempengaruhi perolehan kadar ekstraktif, kadar fenolat total dan aktifitas antioksidan dari herba meniran. Perbandingan pelarut etanol:air sebagai pengekstraksi yang paling baik untuk sampel herba meniran adalah 60:40.
DAFTAR PUSTAKA
Departemen Kesehatan, 2004, Monografi Ekstrak Tumbuhan
64 Obat Indonesia. Badan POM Republik Indonesia, Hal 86-89, 2004
Harbone, J. B., 1978, Metoda Fitokimia:
Penuntun Cara Menganalisis
Tumbuhan, Terbitan kedua,
Diterjemahkan oleh K.Padmawinata dan I.Soediro, ITB, Bandung.
Heyne, K., 1987, Tumbuhan Berguna Indonesia, jilid II, cetakan ke-1, Yayasan Sarana Wana Jaya, Jakarta.
Joshi, B., H. Dilip, S. Gawad and W. Pelletier, 1986, Isolation and Structure (x-ray analysis) of Ent-norsecurinine, an alkaloid from Phyllanthus niruri, Journal of Natural Products, Vol. 49, no. 4, pp. 614-620.
Keinanen, M. and R. J. Titto, 1996, Effect of Sampel Preparation Method on Birch (Betula Pendula Roth) Leaft Phenolics, J. Agric.
Food Chem, 44:2724-2727,
Finland.
Kepala Badan Pengawasan Obat dan Makanan Republik Indonesia,
Kriteria dan Tatalaksana
Pendaftaran Obat Tradisional, Obat Herbal Terstandar dan
Fitofarmaka, No:
HK.00.05.41.1384, Jakarta
Mosquera M.O, Yaned M Correa, Diana C Buitrago and Jaime Nino, 2007, Antioxidant Activity of Twenty five Plants from Colombian Biodiversity. Mem Inst Oswaldo Cruz, Rio de Janeiro, vol 102(5) : 631-634.
Nurkhasanah, 2006, Bahan Obat Alam
Sumber Pendapatan
Pembangunan. Prosiding
Persidangan Antarabangsa Pembangunan Aceh, Hal 82. UKM Bangi. 26-27.
Pourmorad, F. S. J., 2006, Hosseinimerh and N.Shahabimajd, Antioxidant Activity, Phenol and Flavonoid contents of some selected Iranian
medical plants. African Journal of Biotechnology, vol. 5 (11), pp, 1142-1145.
Sigma-Aldrich, Folin&Ciocalteu’s Phenol Reagent, Sigma Prod No F-9252, diambil dari http://www.Sigma –aldrich.com, diakses : tgl 5 Februari 2005 Than N. N., S. Fosto, B. Poeggeler, R.
Hardeland, and H. Laatsch, 2005, Niruriflavone, a new antioxidant Flavone Sulfonic Acid from
Phyllanthus niruri, Z.
Naturforsch. 61b, 1-4 (2006); received November 2.