S K R I P S I
NOORM A R OSI TA
PERBANDINGAN DAYA PENURUNAN KADAR GLUKOSA DARAH DARI
TOLBUTAMIDA DAN DISPERSI SOLIDA TOLBUTAMIDA
PVP K -3 0 (2 0 : 80 ) PADA KELINCI
FAKULTAS FARMASI UNIVERSITAS AIRLANQQA 8 U R A B A Y A
PERBANDINGAN DAYA PENURUNAN KADAR GLUKOSA DARAH DARI
TOLBUTAMIDA DAN DISPERSI SOLIDA TOLBUTAMIDA - PVP K-30 ( 20:80 ) PADA KELINCI
SKRIPSI
DIBUAT UNTUK MEMENUHI SYARAT MENCAPAI GELAR SARJANA FARMASI
PADA FAKULTAS FARMASI UNIVERSITAS AIRLANGGA
1989
oleh
NOORMA* ROSITA 058410646
Disetujui oleh pembimbing
S K R I P S I
NOORMA ROSITA
PERBANDINGAN DAYA PENURUNAN KADAR GLUKOSA DARAH DARI
TOLBUTAMIDA DAN DISPERSI SOLIDA TOLBUTAMIDA - PVP K-30 ( 20:80 ) PADA'KELINCI
FAKULTAS FARMASI
UNIVERSITAS AIRLANGGA
P R A K A T A
Segala puji bagi Allah S.W.T. yang telah melimpahkan
rahmat serta hidayah Nya bagi saya, sehingga saya dapat me
nyelesaikan tugas akhir ini sebagai syarat mencapai gelar
sarjana farmasi pada Fakultas Farmasi Universitas Airlang-
ga.
i
Pada kesempatan yang baik ini perkenankanlah saya me
nyampaikan rasa hormat dan terima kasih yang sebesar-besar
nya kepada dosen pembimbimbing saya,Bapak Drs, Moegihardjo,
Bapak Drs. Roesjdi Gawai, SU; serta Bapak DR. H.A. Azis
Hubeis , yang telah banyak meluangkan waktu untuk memberi
petunjuk dan bimbingan kepada saya selama masa penelitian
hingga tersusunnya naskah tugas akhir ini.
Rasa terima kasih juga saya sampaikan kepada P.T. DU
PA Jakarta yang telah merabantu penyediaan bahan obat tol
butamida, P.T. CORONET CROWN Surabaya yang telah membantu
bahan polivinilpirolidon K-30 ( PVP K-30 ), dan kepada
P.T. OTSUKA Lawang yang memberi bantuan berupa hewan per-
cobaan kelinci yang saya gunakan sebagai subyek pada pene
litian ini. Kepada seluruh staf pengajar dan karyawan pada
laboratorium Preskripsi-Formulasi serta laboratorium Bio-
farmasetika Farmakokinetika juga saya ucapkan terima kasih
atas segala bantuannya sehingga saya dapat menggunakan fa-
Tak lupa juga saya ucapkan terima kasih kepada kedua
orang tua saya yang telah membesarkan dan mendidik saya,
saudara-saudara saya yang telah banyak memberikan bantuan
serta dorongan semangat, juga teman dan sahabat yang telah
banyak membantu saya sehingga tugas akhir ini dapat terse-
lesaikan. Akhirnya kepada panitia skripsi yang telah berke
nan memeriksa naskah tugas akhir ini, saya ucapkan terima
kasih. Semoga amal baik yang telah diberikan oleh semua fi
hak yang telah saya sebutkan, maupun yang tidak dapat saya
sebutkan satu persatu mendapat balasan yang sesuai dari
Allah S.W.T.
Saya persembahkan naskah tugas akhir ini kepada alma
mater tercinta Fakultas Farmasi Univorsitas Airlang^a, ha-
rapan saya semoga memberikan manfaat bagi kita semua.
4 11.1.1. Hubungan bioavailabilitas dengan laju disolusj 7 11.2. Ukuran partikel ... 9
11.6.2. Pengaturan kadar glukosa darah ... 19
11.6.3. Cara penentuan kadar glukosa darah ... 19
III. ALAT, BAHAN DAN METODA PENELITIAN ... .21
111.1. Alat ...21
111.2. Bahan ... ... .21
111.3. Metoda penelitian ...22
111.3.3.. Identifikasi tolbutamida ... .22
III.3*1.1* Uji kualitatif ... .22
111.3.1.2. Uji kuantitatif ...' 22
111.3.2..Identifikasi PVP-K-30 ... .22
III.-3.3. Pembuatan dispersi solida tolbutamida - PVP K-30 ( 20:80 ) ... 23
111.3./+. Uji hasil dispersi colida ... 23
111.3.5. Uji kit glukosa ... .... 2^
111.3.6. Pembuatan larutan baku induk glukosa ... .2k 111.3.7. Penentuan panjang gclombang rnaksimum glukosa.. 2k 111.3.8. Pembuatan kurva baku'glukosa ... .26
III.3*9. Penentuan daya penurunan kadar glukosa darah secara in vivo ... ... 26
111.3.9.1. Subyek ...26
111.3.9.2. Protokol ... ... .26
III.3.9.3* Penentuan kadar glukosa darah ... .27
III.3.10. Analisa data ... .28
111.3.10.1. Perhitungan daya penurunan kadar glukosa darah ... 28
111.3.10.2. Analisa data dengan statistik ... 28
IV. HASIL PENELITIAN ... 29
IV.1, Identifikasi tolbutamida ... 29
IV.1.2. UJi kualitatif ...29
IV,2. Identifikasi PVP K - 3 0 ... ... .29
IV.3* Uji dispersi solida ...
29
IV.k* Uji kit glukosa ...30
IV.3- Panjang gelombang maksimum glukosa ... .30
IV. 6. Kurva baku glukosa ... ... .30
IV.7. Penentuan kadar glukosa darah ... .33
IV.8. Analisa data ...34
IV.8.1. Perhitungan daya penurunan kadar glukosa darah 3/+ IV.8.2. Analisa data dengan statxstik ... .35
V..PEMBAHASAN ...4 6 VI. KESIMPULAN ...54
VII. SARAN ...55
VIII. RINGKASAN ... 56
BAB I
PENDAHULUAN
Sehubungan dengan profesinya, seorang farmasis diha-
rapkan dapat membuat sediaan obat yang raempunyai efek tera
pi optimum. Umumnya, obat akan dapat raemberikan efek tera-
pi bila obat dalam darah dengan jumlah yang cukup ( 1 ).
Sifat fisika kimia bahan obat w^rupakan salah satu faktor
yang berpengaruh terhadap kemampuan obat untuk berada da
lam darah ( 1 ). Sehingga untuk dapat membuat sediaan obat
dengan efek terapi optimum, seorang farmasis perlu memper-
timbangkan sifat fisika kimia bahan obat ( 1*2,3 )•
Sebelum sampai ke aliran darah, obat padat yang digu
nakan secara oral dan ditujukan untuk pengobatan eistemik,
akan mengalami proses disintegrasi, deagregasi, disolusi,
dan absorbsi melewati membran ( 1,2,3 )• Khususnya - untuk
obat yang bersifat sukar larut, laju disolusinya lambat se
hingga raerupakan tahap penentu bagi laju absorpsinya ( 1 ).
Keadaan ini akan menyebabkan berkurangnya kadar obat dalam
darah.
Laju disolusi dapat ditingkatkan antara lain dengan
merubah sifat fisika kimia bahan obat, adapun salah satu
contohnya adalah ukuran partikel. Dengan memperkecil uku
ran partikel, maka semakin luas permukaan bahan obat yang
kontak dengan pelarut, hal ini dapat memperbesar kelarut
Pengecilan ukuran partikel tidak selalu disertai de
ngan peningkatan laju disolusi maupun kadar obat dalam da
rah (bioavailabilitas) . Hal tersebut dapat terjadi karena
efek agregasi, aglomerasi dan adsorbsi udara pada permuka
an obat, sehingga obat akan sukar terbasahi dan akan menu-
runkan jumlah luas permukaan efektif partikel yang berpe-
ran dalam proses disolusi ( 6,7,8 )
Pada tahun 1961, Sekiguchi dan Obi ( cit 7,9 ) telah
memperkenalkan suatu cara meningkatkan laju disolusi bahan
obat sukar larut, yaitu dengan sistem dispersi solida, di
mana bahan obat sukar larut didispersikan dalam pembawa
yang bersifat mudah larut. Keuntungan cara ini selain da
pat memperkecil ukuran partikel, juga tidak menyebabkan e-
fek agregasi, aglomerasi, .. maupun adsorbsi udara oleh par
tikel, karena partikel diselubungi oleh pembawa ( 7,9 ).
Salah satu contoh bahan obat yang sukar larut adalah
tolbutamida. Tolbutamida merupakan antidiabetika oral golo
ngan sulfonilurea, yang mekanisme kerjanya dengan merang-
sang sel ^ pankreas untuk mengeluarkan hormon insulin (10,
11 ). Nelson dan kawan^-kawan ( 12 ) melaporkan bahwa, laju
disolusi -tolbutamida merupakan fungsi dari laju . absorbsi
nya, sehingga si fat sukar larut dari tolbutamida menyebab-
kan kadar tolbutamida dalam darah kecil, yang ditunjukkan
dengan kecilnya' d a y a penurunan.kadar glukosa darah.
Laju disolusi tolbutamida dapat ditingkatkan dengan
dibuat dispersi solida. Dari penelitian terdahulu ( 13 ) di
dalam perabawa PVP K-30 lebih tinggi bila dibandingkan laju
disolusi tolbutamida dari campuran fisis tolbutamida - PVP
K-30 maupun tolbutamida murni.Dari berbagai komposisi yang
telah dicoba, dispersi solida tolbutamida - PVP K-30 komx^o
sisi 20:80 menunjukkan peningkatan laju disolusi teroesar,
dimana pada menit ke 2,5 terjadi peningkatan 28,40 kali.
Sampai saat ini masih diasumsikan bahwa makin besar
laju disolusi suatu obat, semakin cepat obat diabsorbsi.
Dengan peningkatan laju disolusi tolbutamida dari dispersi
solida tolbutamida - PVP K-30 ( 20:80 ) maka secara teori-
tis akan menyebabkan peningkatan laju absorbsi tolbutamida
dan kadarnya dalam darah. Semakin besar kadar tolbutami
da dalam daruh, maka daya penurunan kadar glukosa darah yang
merupakan efek farmakologi tolbutamida, juga semakin besar.
Berdasar asumsi tersebut di atas timbul permasalahan
dispersi solida tolbutamida - PVP K-30 ( 20:80 ) yang mem-
punyai laju disolusi lebih tinggi dari tolbutamida murni,
apakah juga menyebabkan penurunan kadar glukosa yang lebih
besar. Oleh karena itu pada tugas akhir ini dilakukan pene
tian tentang pengaruh dispersi solida tolbutamida - PVP K-30
( 20:80 ) terhadap daya penurunan kadar glukosa darah secara
in vivo pada subyek kelinci dengan parameter kadar glukosa
darah.
Tujuan penelitian ini adalah membandingkan daya penu
runan kadar glukosa darah dari tolbutamida dengan dispersi
solida tolbutamida - PVP K-30 ( 20:80 ).
dalam pengembangan dispersi solida sebagai suatu alterna-
BAB II
TINJAUAN PUSTAKA
II.1. Bioavailabilitas
Bioavailabilitas dldefinisikan sebagai kecepatan dan
jumlah obat yang berada di sirkulasi sistemik ( aliran da
rah ), yang sangat berpengaruh terhadap daya terapetik, ak
tivitas klinik dan aktivitas toksik suatu obat ( 1 ). Seca
ra hipotetik, hubungan antara bioavailabilitas obat de
ngan daya terapetik sampai aktivitas .toksik obat dapat di-
garabarkan sebagai berikut :
Obat akan efektif, bila kadar obat dalam darah diatas KEM
( kurva 2 dan 3 )• Pada kurva 1 meskipun kadar obat dalam
darah di atas KEM tetapi obat dengan tipe kurva demikian
tidak dikatakan efektif karena kadar dalam darah melampaui
KBA, sehingga obat bersifat toksik bagi tubuh. Kecilnya ka
dar obat dalam darah sehingga tidak mencapai KEM,menyebab-
kan vpbat tidak memberikan efek terapi ( kurva if ).
Kecepatan absorbsi obat dan kadar obat dalam darah
juga mempengaruhi mula kerja (a), lama kerja (b) dan inten
sitas kerja obat '(c), seperti yang ditunjukkan . kurva. 2
dan 3* Sehingga untuk mencapai efek terapi yang optimum,
diperlukan kontrol pelepasan obat sedemikian rupa sehingga
didapat bioavaibilitas yang cukup ( 1 ).
Bioavaibilitas suatu produk obat dapat diukur dengan
dua cara, yakni : secara langsung dan tidak langsung ( 1,
11+ ). Secara langsung, .dengan menggunakan data plasma atau
urine, sedangkan cara tidak langsung yaitu dengan mengguna
kan parameter respon klinik atau dengan efek farmakologi a
kut ( 1 ). Beberapa contoh efek farmakologi akut yang da
pat digunakan untuk penentuan bioavaibilitas obat. secara
tidak langsung adalah : tekanan darah, penyempitan atau pe
lebaran pupil mata, kadar glukosa darah dan lain sebagai
nya ( 1, 1^, 15 ).
Terdapat dua faktor yang berpengaruh terhadap bioavai
labilitas obat, yaitu faktor fisiologis dan faktor farma
setik ( 1 ). Faktor fisiologis meliputi umur, jenis kela-
motili-tas usus, kemampuan absorbsi membran, adanya penyakit ter-
tentu, jenis makanan, dan pengaruh peraakaian obat lain ( 1,
15 )• Kecepatan pengosongan lambung dan motilitas usus ber
pengaruh terhadap absorbsi obat untuk sampai ke sirkulasi
sistemik ( 1 ). Adanya makanan dalam lambung juga mengaki-
batkan absorbsi obat menjadi lambat, hal .ini disebabkan
terjadinya peningkatan viskositas cairan lambung, sehing
ga kecepatan pengosongan lambung menurun (
15
). Faktorfarmasetik, meliputi : disintegrasi, pelepasan obat, laju
disolusi, sifat fisika kimia dan faktor formulasi ( 1 ).
Laju disolusi suatu obat merupakan hal yang penting karena
berpengaruh terhadap bioavailabilitasnya, makin besar laju
disolusi semakin cepat pula obat tersebut diabsorbsi dalam
darah ( 1, 2 ).
II.1.1. Hubungan bioavailabilitas dengan la.1u disolusi.
Obat bentuk padat yang digunakan secara oral dan ditu
jukan untuk pengobatan sistemik, umumnya melalui suatu
rangkaian proses yaitu : disintegrasi, deagregasi,disolusi
dan absorbsi obat melewati membran raenuju ke aliran darah
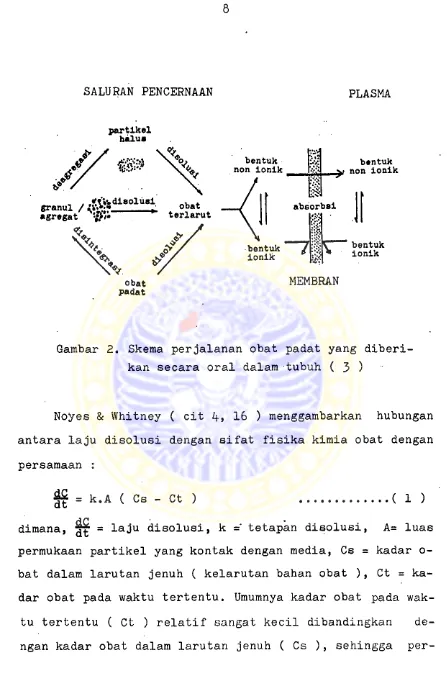
( 1, 2, 3 )• Keadaan tersebut oleh J. Blanchard ( 3 ) di-
gambarkan dengan skema yang ditunjukkan gambar 2. Dari ske
ma dapat dilihat bahwa agar obat dapat diabsorbsi, obat ha
rus dalam keadaan terlarut.
Untuk obat yaftg bersifat sukar larut, tahap disolusi
atau proses dimana suatu senyawa kimia terlarut dalam me
SALURAN PENCERNAAN PLASMA
partikol halus
granul / •gregat
obat terlarut
obat padat
Gambar 2. Skema perjalanan obat padat yang diberi- kan secara oral dalam tubuh ( 3 )
Noyes & Whitney ( cit Zf, 16 ) menggambarkan hubungan
antara laju disolusi d.engan sifat fisika kimia obat dengan
persamaan :
^ = k.A ( Cs - Ct ) ... ( 1 )
dimana, ^ = laju disolusi, k =' tetapan disolusi, A= luas
permukaan partikel yang kontak dengan media, Cs = kadar o-
bat dalam larutan jenuh ( kelarutan bahan obat ), Ct = ka
dar obat pada waktu tertentu. Umumnya kadar obat pada wak-
tu tertentu ( Ct ) relatif sangat kecil dibandingkan de
per-samaan 1 menjadi :
= k.A.Cs ... ( 2 )
dC
Dari persamaan 2 terlihat bahwa laju disolusi ( -jj- ) ber-
banding lurus dengan luas permukaan partikel ( A ) dan ke
larutan bahan ( Cs ). Sehingga untuk meningkatkan laju di
solusi dapat dilakukan dengan cara memperluas permukaan
partikel dan atau meningkatkan kelarutan bahan (3*^ )
II.2, Ukuran partikel
Dengan memperkecil ukuran partikel, luas permukaan
bahan obat yang kontak dengan media disolusi akan mening-
kat ( 2, 1? ). Selain itu dengan mcmperkecil ukuran par
tikel sampai dengan ukuran mikron, dapat inenycbabkan penin^
katan kelarutan suatu bahan ( 6 ).
Berdasar pada rumus Kelvin ( cit 6 ) :
1 n a- S_ _ 2 • Tf , V— ... ••••( 3 )
So “ 2,303 R.T.r c
dimana g0 = perbandingan kelarutan bahan dengan ukuran ke-
cil ( S ) dengan kelarutan bahan dengan ukuran besar (So),
7S = energi bebas permukaan, v = volume molar, R = teta-
pan gas, T = suhu mutlak dan r = jari-jari ; dapat ditun
jukkan pengaruh ukuran partikel terhadap kelarutan bahan.
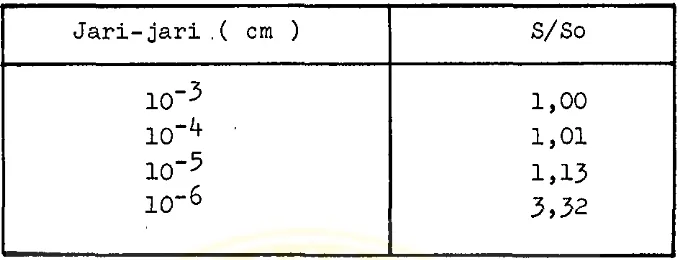
Pada tabel I berikut, dapat dilihat peningkatan kelarutan
suatu bahan obat yang mempunyai berat molekul =
300
,ener-2 3
gi bebas permukaan = 50 erg/cm , berat jenis = 1 g/cm , di
perkecil ukurannya menjadi 10“^, 10_/+, 10-^ dan 10”^ cm ,
TABEL I
PENGARUH UKURAN PARTIKEL TERHADAP KELARUTAN ( 6 )
Dari tabel di atas tampak bahwa peningkatan kelarutan aki-
bat pengecilan ukuran partikel baru berarti, bila ukuran
partikel mencapai daerah mikron.
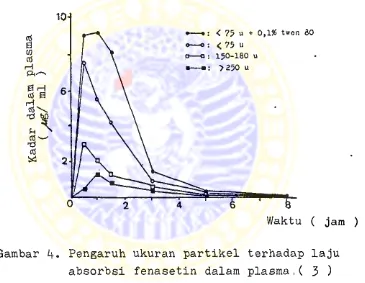
Hubungan ukuran partikel terhadap laju dicolusi da-
pat ditunjukkan pada gambar 3> yang merupakan hasil uji di
solusi fenasetin dari berbagai ukuran partikel dalam cai-
ran lambung,■dimana fenasetin dengan ukuran yang paling ke
oil menunjukkan laju disolusi yang paling besar ( 8 ).
Gambar 3. Pengaruh ukuran partikel terhadap laju
Oleh karena dengan meraporkecil ukuran partikel bahan
obat sukar larut dapat meningkatkan laju disolusinya, maka
laju absorbsi dan kadar obat dalam darah pun meningkat. Pe
ngaruh ukuran partikel terhadap kadar obat dalam darah da
pat dilihat pada gambar k» Pada pemberian fenasetin dengan
berbagai ukuran partikel yang diberikan dalam bentuk sus-
pensi menunjukkan bahwa semakin kecil ukuran partikel fena
setin, kadar fenasetin yang ada dalam plasma semakin besar.
Finholt dan. kawan-kawan ( 8 ) melaporkan bahwa penge
cilan ukuran partikel tidak selalu dapat meningkatkan laju
disolusi obat. Dari penelitian yang telah dilakukan terha
dap fenobarbital, ternyata laju disolusinya menurun dengan
semakin kecilnya ukuran partikel ( Gambar 5 )• Hal ini da
pat disebabkan semakin kecil ukuran partikel,energi bebas 10-1
Waktu ( jam )
permukaan akan meningkat dan adanya gaya van der Wdals an-
tara molekul-molekul sehingga terbentuk agregat dan aglome
rat, sehingga . luas permukaan efektif bahan yang berperan
dalam proses disolusi menjadi berkurang ( 7 ).
. Gambar 5. Pengaruh ukuran partikel terhadap laju disolusi fenobarbital ( 8 )
II.3* Dispersi solida
Dispersi solida adalah dispersi satu atau lebih .ba
han aktif dalam pembawa inert padat yang dibuat dengan ca
ra pelarutan, peleburan atau kombinasi pelarutan dan pele-
buran ( 7 ) •
Dispersi solida merupakan salah satu cara yang dapat
digunakan uituk meningkatkan laju disolusi bahan obat su-
kar larut. Bila bahan obat didispersikan dalam pembawa i-
nert padat yang bersifat mudah larut, bahan obat akan ter-
dispersi dalam pembawa dengan ukuran sangat halus, sehing
ga laju disolusinya akan meningkat. Hal ini juga disebab -
larut sehingga tidak terjadi agregasi, aglomerasi dan ad
sorbs! udara ( 7 ).
Sejak teknik pembuatan dispersi solida diperkenalkan
pertama kali oleh Sekiguchi dan Obi pada tahun 1961 hingga
sekarang, lebih dari 270 publikasi tentang dispersi solida
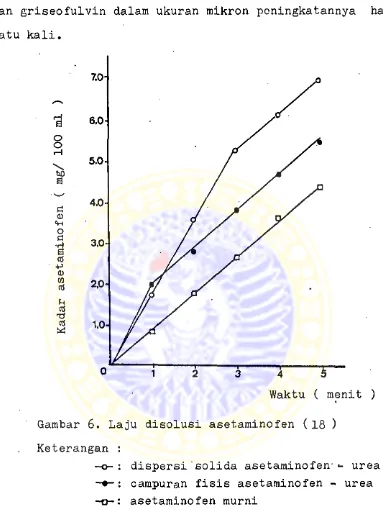
dari bahan-bahan sukar larut ( 7,9 ). Salah satu contoh a-
dalah dispersi solida asetaminofen - urea ( Gambar 6 ), di
mana laju disolusi asetaminofen dari bentuk dispersi soli
da dalam pembawa urea lebih tinggi dibandingkan dengan cam
puran fisis maupun asetaminofen murni ( 18 ).
Dibandingkan laju disolusi griseofulvin yang tidak
diperkecil ukurannya, dispersi solida griseofulvin .dalam
pembawa PVP mempunyai laju disolusi yang lebih besar ( 9 ).
Besar peningkatan laju disolusi dapat dilihat pada t'abel II
TABEL II
LAJU DISOLUSI RELATIF* GRISEOFULVIN ( 9 )
B a h a n 1 menit if menit
Griseofulvin ukuran mikron 1,0 1,0 Griseofulvin - PVP ( 1:5 ) 6,1 5,1 Griseofulvin - PVP ( 1:10 ) 7,2 6,1 Griseofulvin - PVP ( 1:20 ) 11,0 7,3
* = dibandingkan griseofulvin yang tidak diperkecil ukurannya.
Dispersi solida griseofulvin dalam PVP komposisi 1:20 niom-
da menit pertaraa dan 7,3 kali pada menit ke empat. Sedang-
kan griseofulvin dalam ukuran mikron pcningkatannya hanya
satu kali.
C5 0) o
a
•H 6 cC -P <1) CO
b cfl cd
Gambar 6. Laju disolusi asetaminofen (18 )
Keterangan :
: dispersi'solida asetaminofen-*- urea : carapuran fisis asetaminofen - urea : asetaminofen murni
Peneliti terdahulu ( 13 ) juga telah membuktikan bah
wa dengan dibuat dispersi solida dalam pembawa PVP K-30,la
murni. Dengan mencoba pada berbagai komposisi, ternyata
besar peningkatan laju disolusi .tolbutamida pada 2,5 me
nit pertama bervariasi ( Tabel III )
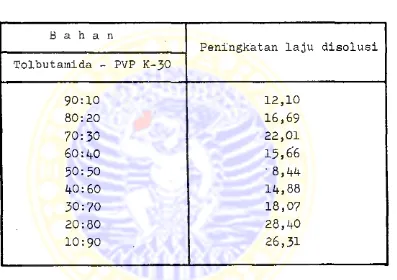
TABEL III
PENINGKATAN LAJU DISOLUSI TOLBUTAMIDA
DARI BENTUK DISPEPSI SOLIDA TOLBUTAMIDA - PVP K-30 BERBAGAI KOMPOSISI PADA MENIT KE-2,5 ( 13 )
B a h a n
Peningkatan laju disolusi Tolbutamida - PVP K-30
90:10
12,1080:20 16,69
70:30 22,01
60:40 15)6*6
50:50 ‘ 8,44
40
: 6014,88
30:70 18,07
20:80 28,40
10:90 26,31
Dari tabel III dapat dilihat bahwa pada semua komposisi
terjadi peningkatan laju disolusi,. dan peningkatan ter-
besar ditunjukkan oleh dispersi solida tolbutamida - PVP K-30
II.J+, Tolbutamida
Il.if.l. Si fat fisika kimia ( 19.20.21 )
Rumus bangun : H^CH^C S02— NHCONH(CH2 )
Nama lain l-butil-3-p-toluilsulfonil-ureum
N-( ^ metil-benzensulfonil )-N'-n-
butil urea
ngan penambahan alkali membentuk
garam yang mudah larut dalam air,
larut dalam etanol ( 95% ) P dan
dalam kloroform P,
sedikit larut dalam eter.
sampai 180 °C membentuk p-tolil-
sulfonamida dan n-butil iso sia-
nat
Tolilsulfonilbutilurea
Nama dagang : Orinase
Rastinon
Pemerian serbuk halus, putih, tidak berbau
dan rasa agak pahit
praktis tidak larut air, tapi ds-Kelarutan
Jarak lebur : antara 126 sampai 132 °C
antara 128,3 sampai
129»5
°CStabilitas : terurai oleh panas pada suhu 160
II.if.2. Khasiat dan pen^gunaan ( 10,11,19)20 )
pankreas untuk mengeluarkan insulin, zat yang di
butuhkan dalam transpor glukosa darah dalam sel. Se
hingga tolbutamida hanya dapat digunakan untuk pe-
ngobatan diabetes tipe II jenis dewasa (“maturity -
onset0 ) dimana pankreasnya masih aktif.
Kadar maksimal dicapai dalam darah setelah 2-4 jam,
dan mempunyai masa kerja 6-12 jam.
Dosis permulaan oral 3 kali sehari 0,5-1 g
selama makan ( guna menghindari iritasi lambung ),
dosis pemeliharaan 2 kali sehari 0,5 g*
11*5. Polivinilpirolidon ( PVP ) ( 9*2.2. )
merupakan polimer dari 1-vinilpiro-
lid-2-on.
( c6h9n o )n
bervariasi mulai dari 10.COO sampai
7 0 0 .0 0 0
polividon, povidon
serbuk putih atau putih kekuningan,
tidak berbau, tidak berasa dan sedi
kit higroskopis.
roform , tetapi tidak larut dalam
eter.
Kelarutan PVP tergantung pada be
rat molekulnya. Semakin besar be
rat molekulnya, semakin berkurang
kelarutannya karena viskositas la
rutannya meningkat.
Berdasar kelarutannya, PVP dibagi dua macam
yaitu larut dalam air dan yang tidak larut 'dalam
air. PVP yang larut air, contohnya PVP K-18, PVP
K-25 dan PVP K-30, yang amumnya digunakan sebagai
zat pendispersi, penyalut tablet, dan sebagai pem
bawa dalam pembuatan dispersi solida suatu 'bahan
obat yang sukar larut. PVP yang tidak larut dalam
air contohnya PVP GL dan PVP KL,jenis ini umumnya
digunakan sebagai disintegrator pada tablet.
II.6. Glukosa darah ( 11.25.2U.25.26 )
III.6.1. Sumber glukosa darah
Selain didapat dari proses glikogenesis da
ri glikogen hati dan glikoneogenesis dari berba-
gai senyawa glukogenik, glukosa darah juga dipe£
oleh dari pemecahan karbohidrat yang terkandung
dalam makanan. Di dalam saluran pencernaan, kar
bohidrat diubah menjadi glukosa, fruktosa dan ga Stabilitas : terurai pada titik leburnya 275°C
laktosa. Glukosa akan langsung diserap melalui vo
na porta, sedangkan fruktosa dan galaktosa sejjera
diubah menjadi glukosa oleh hati
III.6.2. Pengaturan kadar glukosa darah
Kadar glukosa darah manusia pada keadaan se-
telah makan karbohidrat berkisar antara1120-130 mg;6.
Sedangkan pada keadaan "post absorbsi” , kadar glu
kosa darah akan turun menjadi 80-100 mg$. Penuru-
nan semakin besar saat manusia puasa, yaitu anta-
ra 60-70 mg$.
Apabila kadar glukosa dalam cairan ekstra sel
meningkat akibat makan karbohidrat yang berlebihan,
maka peningkatan lersebut akan diikuti dengan pe-
ningkatan pengeluaran insulin dari sel ^ pankreas.
Insulin akan meningkatkan Iranspor glukosa dari on.
iran-ekstra sel menuju intra sel melalui membran,
Pada orang yang terlalu gemuk dan orang yang lan-
jut usia, ser.ingkali mengalami kekurangan hormon
insulin sehingga menggangu metabolisme glukosa da
lam tubuh dan menyebabkan kadar glukosa darah men
jadi tinggi.
III.6.3* Cara nenentuan kadar glukosa’ darah
Kadar glukosa darah dapat ditentukan dengan
beberapa cara, antara lain : metoda Somogyi Nelson,
metoda Hoffman, metoda o-toluidin dan metoda enzi-
di-pakai metoda o-toluidin karena pclaksanaannya ce-
derhana dan mempunyai spesifikasi yang relatif
tinggi. Pada metoda ini reaksinya tidak didc^sar-
kan dari sifat reduksi glukosa sehingga tidak di-
pengaruhi oleh bahan-bahan fisiologis yang ada da
lam serum.
Prinsip reaksi dari metoda ini adalah pem-
bentukan senyawa kompleks yang berwarna biru kehi
jauan, hasil reaksi antara. glukosa dengan o-tolui
din dalam suasana asam asetat panas. . Intensit-as
warna senyawa kompleks yang terbentuk dapat diu-
kur dengan spektrofotometer pada panjang golombang
makuimum larutan glukosa
Metoda o-toluidin dapat digunakan langsung
untuk menentukan kadar glukosa yang terdapat pada
serum, plasma, urine dan cairan serebrospinal. Te,
tapi bila digunakan pada sampel darah, perlu dila
kukan deproteinisasi terlebih dahulu. Sebagai pe-
ngendap protein dapat dipakai asam tungstat atau
ALAT, BAHAN DAN METODA PENELITIAN
III.l. Alat
- "Differential Scanning Calorimeter" ( DSC ) merk
Shimadzu
- "Double Beam Spektrophotometer UV" li|0-02 rnork
Shimadzu
- "Hot: Plate Stirrer" merk Corning tipe PC-3^1
- "Porta Centrifuge" merk Sugico
- "Vortex" merk Genic tipe K-^bO-GE
- Ekaikator hampa
- Penangas air
BAB III
III.2. Bahan
- Tolbutamida p.g. ( PT. DUPA )
- PVP K-30 p.g* ( PT. Coronet Crown )
- Etanol absolut p.a. ( E. Merck )
- Natrium hidroksida p.a. ( E. Merck )
- Heparin
- Clukosa P*a. ( Ferak )
TM
- Seronorm Routine ( E. Merck )
- Kit Glukosa ( E. Merck )
terdiri dari :
reagensia warna ( 800 mmol/ 1 larutan o-toluidin
dalam asam asetat )
larutan standar g l u k o s a ... 5,55 mmol/ 1
III.3* Metoda penelitian
III.3*1* Identifikasi tolbutamida
III.3.1*1- U .11 kualitatif ( 21)
Dilakukan penentuan titik lebur tolbutamida de
ngan menggunakan alat DSC. Dari termogram yang
dihasilkan dapat diketahui titik lebur tolbuta
mida.
111.3.1.2. U.ii kuantitatif ( 19 )
Dilakukan dengan cara asidi-alkalimetri :
Ditimbang teliti 500 mg tolbutamida, dilarutkan
dalam
30
ml etanol 95$ netral, kemudian ditam-bah 20 ml air suling. Dititrasi dengan natrium
hidroksida 0,1 N menggunakan indikator larutan
fenolftalein P.
1 ml natrium hidroksida 0,1 N setara dengan
27,04 mg C12H18N2°3S *
111.3.2. Identifikasi PVP K-^0 ( 19 )
Dilakukan uji kualitatif dengan reaksi warna.
- Pada 10 ml larutan Z% PVP ditumbalikan JO ml 1IC1
. 1 N dan 5 ml larutan I^Cr^O
1 1 1 .3.3 • Pembnatan dispersi solida Loi.bn laniida - PVP K-oO
( 20:80 )
Dilakukan dengan cara pelarutan ( 2? ):
- PVP K-30 yang telah ditimbang dilarutkan dalam
etanol panas di atas "Hot Plate Stirrer".
- Ke dalam larutan tersebut, ditambahkan tolbuta
mida dengan jumlah sesuai komposisi dan diaduk
hingga semua terlarut.
- Etanol diuapkan sampai kering.
- Campuran yang telah kering dimasukkan ke dalam
eksikator hampa selama 2X\ jam,
- Campuran digerus dan diayak dengan B^q.
111.3.4. U.1i hasil dispersi solida ( 9 )
Ditentukan titik lebur dengan menggunakan alat
DSC :
- Dispersi solida sebanyak Z-k mg dimasukkan da lam sampel pan,
- Sampel pan dipanaskan dalam oven DSC bersama -
sama pembanding.
- Perubahan sampel selama pemanasan direkan pada
termogram.
- Titik lebur dihitung dengan cara menentukan ti
tik potong antara garis singgung dengan garis
dasar.
Kemudian profil termogram yang dihasilkan
III.3.
Serbuk serum baku "Seronorm Routine" dilarutkan
dengan 5>0 ml air suling, kemudian dikocok perla-
han hingga terlarut semua. Selanjutnya dilakukan
penetapan kadar glukosa dalam serum baku sebanyak
lima kali pada panjang gelombang 630 nm,
Penentuan kadar glukosa dilakukan dengan caru se-
perti yang tertera pada tabel IV. Bila hasil uji
memenuhi rentang kadar yang dipersyaratkan, maka
kit dapat digunakan untuk penentuan kadar glukosa
dengan metoda o-toluidin.
6. Pembuatan larutan baku induk glukosa
Ditimbang teliti 1,0 g serbuk glukosa dan dilarut
kan dalam air suling sampai volume 100,0 ml.
7. Penentuan pan.iang gelombang maksimum glukosa
Diamati harga resapan dari larutan glukosa kadar
80 dan 120 mg%, hasil pengenceran larutan baku in
duk glukosa dengan air suling, pada panjang gelom
bang antara 620-635 nm dengan cara seperti tabel
IV. Panjang gelombang dengan nilai resapan m^ksi-
mum digunakan sebagai panjang gelombang maksimum
TABEL IV
CARA PENENTUAN KADAR GLUKOSA
' MENGGUNAKAN KIT GLUKOSA METODA O-TOLUIDIN ( 28 )
Dipipet ke dalam tabung sentrifus :
Sampel Standar Blangko
Larutan asam trikloroasetat 1,0 ml 1,0 ml 1,0 ml
Sampel ( tscrum baku/ larutan
glukosa/ darah ) 0,1 ml _
-Larutan standar - 0,1 ml
-Air suling - - 0,1 ml
Campur komudian disen Lrii'us selama
30
menit. Dipipet dalam tabung reaksi :Supernatan bebas protein 0,5 ml -
-Campuran standar - 0,5 ml
-Campuran blangko - - 0,5 ml
Reagensia warna 2,0 ml 2,0 ml 2,0 ml
Campur dan diinkubasikan selama 8 menit dalam penangas
air mendidih, kemudian segera didinginkan.
Diukur resapan sampel ( Rs ) dan resapan standar ( Rst )
terhadap blangko,secara spektrofotometrik pada panjang
gelombang tertentu.
111.3.
111.3.
111.3.
III.3.
8. Pembuatan kurva baku glukosa
Diamati harga resapan dari larutan .glukosa kadar
20,
40
, 60, -80, 100, 120, dan 200 mg%, hasil pe-ngenceran larutan- baku induk glukosa dengan air
suling, pada panjang gelombang maksimum dengan ca
ra seperti tabel IV. Dari pengamatan dibuat kur
va kadar terhadap resapan.
9* Penentuan dava penurunan kadar glukosa darah
secara in vivo
9.1. Subyek
Penelitian dilakukan pada enam ekor kelinci pu
till, jantan, sehat, dengan berat £,5-3j3 kg (27).
Sebelum dilakukan percobaan, subyek diadaptasi
kan dengan lingkungan percobaan selama 1 mingg-
gu. Subyek dipertahankan hidupnya dengan diberi
air dan makanan tertentu, dengan jumlah yang di
sesuaikan berat badannya.
9.2. Protokol
Sebelum dilakukan percobaan, subyek dipuasakan
sepanjang malam, tetapi tetap diberi minum. Se-
telah dilakukan penimbangan, subyek ditempatkan
dalam kandang pengendalian untuk mempermudali pe
ntfambilan sampel darah. Darah diambil dari vena
Setiap subyek mendapat tiga perlakuan dengan
rancangan saling silang ( ’’cross over design” ).
Antara dua perlakuan diberi selang waktu sela-
satu minggu.
Perlakuan I : Sebagai kontrol, tanpa pemberi
an obat.
Perlakuan II : Diberi tolbutamida murni sebanyak
0,25 &/ kg berat badan ( 2y,30 ).
Perlakuan III: Diberi dispersi solida tolbutami
da - PVP K-30 ( 20:80 ) , dengan
jumlah setara tolbutamida 0,25 g/
kg berat badan.
Pada jam ke-1 dari tiap perlakuan*, subyek diberi
glukosa sebanyak 1 g/ kg berat badan secara oral
dalam bentuk larutan glukosa
50
% , sebagai testoleransi glukosa/ GTT ( 29)30 ). Pemberian obat
pada perlakuan II dan III secara oral dalam ben
tuk suspensi dalam air suling 5 ml/ kg berat ba
dan (
31
) segera setelah pengambilan darah pu-asa ( jam ke-0,0 ) ( 29 )
Pengambilan sampel darah dilakukan pada jam ke :
0,0; 0,5; 1|0; 1,5; 2,0; 4,0 dan 6,0 segera iscte
lah pengambilan darah puasa.
III.3.9.3. Penentuan. kadar ftl.ukosa darah
an, ditentukan dengan cara seperti tabol IV yang
pengamatannya dilakukan pada panjang gelombang
maksimum glukosa.
III.3-10* Analisa data
III.3.10.1. Perhitungan dava penurunan kadar glukosa darah
Untuk menghitung daya penurunan kadar glukosa
darah akibat pemberian obat, dilakukan dengan
cara sebagai berikut :
- Ditentukan perubahan kadar glukosa darah pa
da tiap perlakuan, dengan menghitung selisih
kadar glukosa pada setiap w&ktu terhadap ka
dar glukosa darah awal ( C^-Cq )
- Daya penurunan kadar glukosa darah akibat
pemberian obat = selisih antara perubahan ka
dar glukosa kontrol dengan perubahan kadar
glukosa darah akibat pemberian obat ( tolbu
tamida/ dispersi solida tolbutamida - PVP
K-30 ( 20:80 ) ) = {( Ct-CQ )kt - ( Ct-CQ )Qb}
III.3*10.2. Analisa data dengan statistik
Daya penurunan kadar glukosa darah dihitung dg.
ngan metoda statistik secara ANAVA, percobaan
faktorial dari rancangan blok lengkap yang di-
acak ( "Randomized Complete Block Design" /
BAB IV
HASIL PENELITIAN
IV.1. Identifikasi tolbutamida
IV.1.1. U.ii kualitatif
Perneriksaan titik lebur sesuai metoda penelitian
( DSC ), diperoleh titik lebur tolbutamida 131»90°C.
Termogram DSC dapat dilihat pada lampiran 1.
IV.1.2. U.ii kuantitatif
Penotapan kadar tolbutamida yang ditentukan rnenu-
rut metoda ponolitian
111
.3
*1.2
, memberikan ha-sil sebesar
99
,53
%*IV.2. Identifikasi PVP K-50
- dengan pereaksi HC1 1 N dan larutan K^C^O,-, : ter
bentuk endapan warna jingga
- dengan pereaksi larutan iodium 0,1 N : terjadi
warna merah tua
IV.3. U.ii dispersi solida
Sesuai metoda penelitian III.3.4> dispersi solida ha
sil pembuatan diperiksa dengan DSC. Pada termogram
tidak tampak adanya puncak titik lebur ( Lampiran 2,
3
, dan i|. ) dan mempunyai profil yang idontik dengantermogram dispersi solida dari penelitian terdahulu
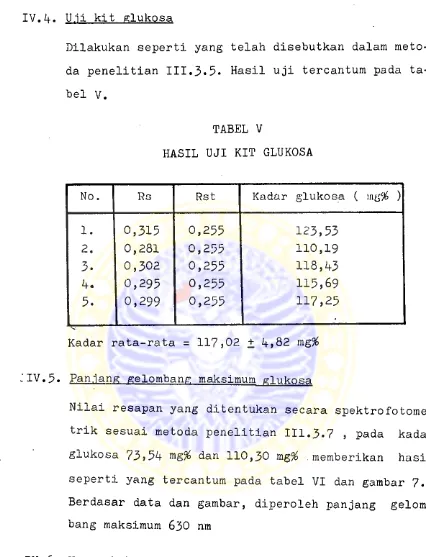
IV.if. U.ii kit glukosa
Dilakukan seperti yang telah disebutkan dalam meto
da penelitian III.3.5. Hasil uji tercantum pada ta-
bel V.
TABEL V
HASIL UJI KIT GLUKOSA
No. Rs Ret Kadar glukosa ( m )
1
. 0,315 0,255 123,532
. 0,281 0,255 110,193.
0,302
0,255 118, if3if. 0,295 0,255 115,69
5. 0,299 0,255 117,25
Kadar rata-rata = 117,02 + if,82 mg%
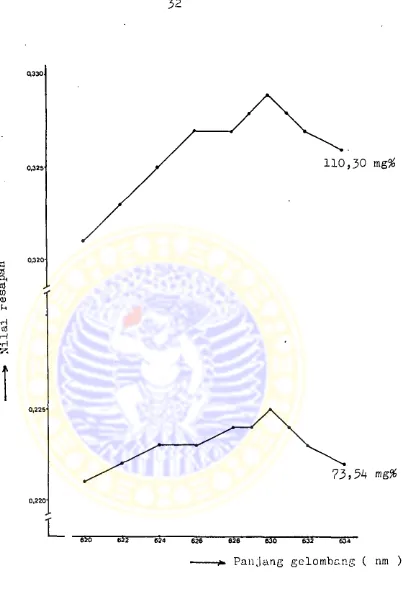
.'IV. 5. Pan.iang gelombang maksimum glukosa
Nilai resapan yang ditentukan secara spektrofotome
trik sesuai metoda penelitian
111
.3* 7
, pada kadarglukosa 73,5if mg% dan
110,30
mg% .memberikan hasilseperti yang tercantum pada tabel VI dan gambar 7,
Berdasar data dan gambar, diperoleh panjang gelom-
bang maksimum
630
nmIV.
6
. Kurva baku glukosaNilai resapan larutan glukosa dengan kadar tertentu
untuk pembuatan kurva baku dapat dilihat pada tabel
TABEL VI
NILAI RESAPAN LARUTAN GLUKOSA PADA BERBAGAI PANJANG GELOMBANG
Panjang gelombang ( nm )
Nilai resapan pada kadar
73>54 mg# 110,30 mg?'?
620 0,221 0,321
622
0,222 0,323624 0,223 0,325 .
626
0,223 0,327628 0,224 0,328
629
0,224 0,328630
0,225
. 0,329631 0,224 0,328
632 0,223 0,327
Ni
la
i
r
e
s
a
p
a
n
0,330
0,325
0,320
0,225
0,220
L
"6 5 5 652 624 6 2 6 6 2 6 6 3 0 632 634
---- Panjang gelombang ( nm )
Gambar 7. Kurva nilai resapan terhadap
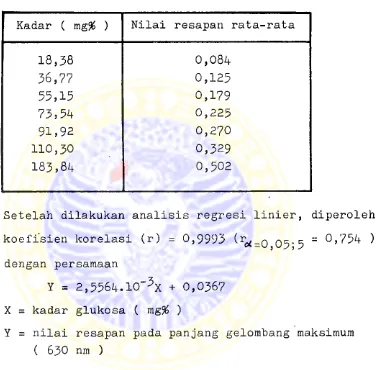
NILAI RESAPAN RATA-RATA LARUTAN GLUKOSA DARI BERBAGAI KADAR PADA 630 nm
TABEL VII
Kadar ( mg% ) Nilai resapan rata-rata
18,38 0,084
36,77 0,125
55,15 0,179
73,54 0,225
91,92 0,270
110,30
0,329183,8if 0,502
Setelah dilakukan analisis regresi linier, diperoleh
koefisien korelasi (r) = 0,9993
05-5
" ^dengan persamaan
Y = 2,556^.10'3X + 0,0367
X = kadar glukosa ( mg% )
Y = nilai resapan pada panjang gelombang maksimum ( 630 nm )
IV.7. Penentuan kadar glukosa darah
Dilakukan sesuai metoda penelitian III.3*9«3» Kadar
glukosa darah pada tiap waktu pengambilan sampel ,
pada perlakuan I, II dan III masing-masin£ subyuk,
Ni
Gambar
8
. Kurva nilai resapan terhadap kadar larutan glukosa pada A =630
nmIV.
8
. Analisa dataIV.8.1. Perhitungan dava penurunan kadar glukosa darah
Dihitung dengan cara seperti yang disebutkan da-
lam metoda penelitian Ili.
3
«10
.1
.Perubahan kadar glukosa dara.li dari keadaan awal
akibat perlakuan dapat dilihat pada tabel IX ,
Dari gambar yang dihasilkan, terlihat adanya pe-
nyimpangan profil kurva pada subyak
6
( gambar14
).Setelah dilakukan "Rejection of a Result", hasil
nya data dari subyek
6
harus di "reject", sehing-ga untuk pengolahan data selanjutnya hanya dipa-
kai data dari 3 subyek kelinci.
Daya penurunan kadar glukosa darah akibat pemberi
an tolbutamida dan dispersi solida tolbutamida
PVP K-30 ( 20:80 ) tiap selang waktu pengamaian
pada masing-masing subyek dapat dilihat pada ta
bel X. Sedangkan daya penurunan maksimum dapat di
lihat pada tabel XI.
IV.8.2. Analisa data dengan statistik
Sesuai metoda penelitian III.3.10.2 , daya penuru
nan kadar glukosa darah diolah dengan statistik
se'cara ANAVA dengan percobaan faktorial RCBD.
Ringkasan hasil statistik dapat dilihat pada ta
HIUftAKAI tAMt 611K0SA IAIAI Mil KAMA* AVAl ACIBA1 PillACUAIt
37
ADLN
-
PERPUSTAKAAN
UNIVERSITAS
AIRLANGGA
PERBANDINGAN
DAYA PENURUNAN
KADAR
GLUKOSA
DARAH
DARI ...
Gambar 9. Kurva perubahan kadar glukosa darah dari
keadaan awal akibat pemberian glukosa se
bagai kontrol (□ — D), tolbutamida (O— O ) , dispersi solida tolbutamida-PVP K30=20:80
Gambar 10. Kurva perubahan kadar glukosa darah dari
keadaan awal akibat pemberian glukosa so
Gambar 11. Kurva perubahan kadar glukosa darah dari
keadaan awal akibat pemberian glukosa so
bagai kontrol (□ — O ) , tolbutamida (O— O),
dispersi solida tolbutamida-PVP K30-20:^0
Gambar 12. Kurva perubahan kadar glukosa darah dari
keadaan awal akibat pemberian glukosa se
Gambar 13. Kurva perubahati kadar glukosa darah dari
keadaan awal akibat pemberian glukosa sc-
Gambar 14« Kurva perubahan kadar glukosa darah dari
keadaan awal akibat pemberjan glukosa se
ba^ai konlrol (□ — Q) , tolbutamida (O— O) ,
DAYA PENURUNAN KADAR GLUKOSA DARAH MAKSIMUM AKIBAT PEMBERIAN BAHAN OBAT
TABEL XI
Subyek
Penurunan kadar glukosa darah maksimum (ro.£%)
Tolbutamida mida - PVP K-30 ( 20:80 )Dispersi solida tolbuta
1 72,37 69,56
2 42,13 43,59
3 35,68 38,40
4 24,87 69,91
5 54,47 67,45
Rata-rata 45,90 ±18,27 57,78 + 15,46
TABEL XII
RINGKASAN HASIL PERHITUNGAN STATISTIK SECARA ANAVA RCBD
Sumber variasi df ss MS Fhitung **=0,05
Bahan obat 1 3570,19 3570,19 7,22 4,06
Waktu 5 4034,30 806,86 1,63 2,43
Interaksi
obat-waktu 5 612,24 122,45 0,25 2,43
Subyek 4 3141,28 785,32 1,59 2,58
Residu 44 21760,42 494 > 56
BAB V
P E M B A H A S A N
Tolbutamida merupakan antidiabetika oral yang kini
jarang dipakai dalam praktek antara lain karena sifatnya
yang sukar larut dalam air, sehingga absorbsi dan daya pe
nurunan kadar glukosa darahnya kecil. Menurut Nelson dkk
(
12
) laju absorbsi tolbutamida yang ditunjukkan oleh daya penurunan kadar glukosa darah, merupaKan fungsi d a n
laju disolusi. Lambatnya laju disolusi tolbutamida menye-
babkaft laju absorbsi yang lambat pula, sehingga bioavaila
bilitas tolbutamida menjadi rendah.
Laju disolusi tolbutamida dapat ditingkatkan dengan
cara dibuat dispersi solida dalam pembawa PVP K-30>dimana
pada komposisi 20:80 menunjukkan peningkatan laju disolu
si terbesar ( 13 ). Untuk mengetahui pengaruh dispersi so
lida tolbutamida - PVP K-30 ( 20:80 ) terhadap bioavaila-
bilitas tolbutamida, dilakukan penelitian terhadap efek far;
makologinya yaitu daya penurunan kadar glukosa darah,yang
dapat digunakan sebagai parameter untuk penentuan bioavai
labilitas secara tidak langsung.
Tahap awal dari penelitian ini dilakukan identifi-
kasi bahan aktif maupun bahan pembawa yang digunakan un
tuk membuat dispersi solida tolbutamida - PVP K-30 (J0:60).
Secara kualitatif hasil yang diperoleh dari titik lebur
u-ji kuantitatif asidi alkalimetri, kadar tolbutamida sebagai
bahan baku = 99,53%.( F.I. Ed.Ill = 98,0-110,0% ). Berda
sarkan reaksi warna sebagai uji kualitatif, PVP K-30 mem
berikan reaksi yang sama dengan yang tertera pada F.I.Ed.
III. Dengan demikian tolbutamida maupun PVP K-30 yang di
guna-kan memenuhi persyaratan Farmakope Indonesi edisi III.
Seperti yang dilakukan Sekikawa ( 27 ) dan Emi ( 13 )
dispersi solida tolbutamida - PVP K-30 dibuat dengan me
toda pelarutan, dimana dari pustaka (
9
) juga diaolmt-kan bahwa muloda pelarutan merupakan metoda terbaik uniuk
pembuatan dispersi solida dalam pembawa PVP. Dispersi so
lida hasil pembuatan diperiksa dengan DSC. Termogram yang
dihasilkan mempmiyai proJ'.U yang ideutik dengan termogram
dispersi solida dari penelitian terdahulu, yaitu tidak ada
puncak titik lebur dari suhu 30-200 °C ( lampiran 2,3 dan
i+ ). Keadaan tersebut menggambarkan bahwa dispersi solida
yang dibuat identik dengan hasil dispersi solida pada pe
nelitian terdahulu. Dispersi solida yang pembuatannya ti
dak sempurna, pada termogram DSC akan terlihat adanya pun
cak titik lebur seperti yang terlihat pada lampiran
6
. A-danya puncak titik lebur tersebut diakibatkan tolbutamida
tidak terdispersi secara sempurna dalam PVP, sehingga pa
da suhu 132 °C yang merupakan suhu lebur tolbutamida tor-
lihat puncak pada termogramnya.
Penentuan kadar'glukosa darah dilakukan secara spek
trofotometri, sehingga perlu dibuat kurva baku glukosa pada
nm ). Dari analisa regresi yang dilakukan, diperoleh per-
samaan Y = 2,556if.lO”'Sc + 0,036? dengan koefisisen korelg,
si (r) = 0,9993 ^=0,005; 5 = ). Metoda yang
dipa-kai untuk menentukan kadar glukosa adalah metoda o-tolui-
din, yang sederhana dalam pelaksanaannya dan spesifikasi-
nya relatif tinggi ( 25)26 )• Oleh karena dalam pelaksan&
an penentuan kadar glukosa darah dengan metoda o-toluidin
digunakan kit, maka perlu dilakukan uji kit sebelum meng
gunakan kit tersebut. Dari hasil uji kit dengan serum ba- TM
ku Seronorm Routine didapat kadar glukosa 117,02 + i+,82
ms% ( rentang kadar yang dipersyaratkan :
108-133
mg# ) ,sehingga kit glukosa dapat digunakan untuk penentuan ka
dar glukosa darah dengan metoda otoluidin.
Penentuan daya penurunan kdar glukosa darah . dari
tolbutamida dan dispersi solida tolbutamida - PVP K-30
( 20:80 ) digunakan subyek kelinci. Kelinci dipilih yang
sehat, berat antara 2,5-3>3 kg dan berkelamin jantan. Ke
linci betina tidak digunakan sebagai subyek dalam peneli
tian ini karena dikhawatirkan adanya pengaruh hormonal p£
da kadar glukosa darahnya. Selain itu, dipilih kelinci d£
ngan warna putih ( albino ) untuk mengurangi pengaruh per
bedaan genetik. Makanan yang diberikan pada kelinci berjj?
nis sama dan jumlahnya disesuaikan dengan berat badannya.
Sebelum dilakukan percobaan, subyek dipuasakan sepanjang
malam agar saat diberi obat lambung dalam keadaan kosong.
Adanya makanan dalam lambung menyebabkan viskositas cair-
si obatnya ( 15 ). Mas'ing-masing subyek mondapat tiga per
lakuan, dimana antara perlakuan subyek diiestirahatkan se-
lama satu minggu. Tujuan diberikannya selang waktu terse-
but adalah untuk menghilangkan pengaruh dari perlakuan se
belumnya, sehingga diharapkan efek farmakologi yang ditim
bulkan benar-benar diakibatkan dari perlakuan pada saat i
tu. Pada saat perlakuan pemberian obat : tolbutamida atau
dispersi solida tolbutamida - PVP K-30 ( 20:80 ), subyek
diberikan glukosa sebagai tes toleransi glukosa ( "Gluco
se Tolerance Test"/ GTT ). GTT merupakan metoda yang umum
digunakan dalam penentuan daya penurunan kadar glukosa da
rah suatu anti antidiabetes, bila tidak digunakan alloxan
untuk membuat subyek menderita diabetes. Oleli karena GTT
juga berfungsi untuk menghindari terjadinya "hypoglicemic
shock" akibat pemberian obat, maka glukosa diberikan pada
jam ke
-1
dengan harapan, agar saat terjadi absorpsi muksimum tolbutamida juga terjadi absorpsi maksimum glukosa.
Dengan adanya perlakuan GTT pada perlakuan II' dan III, ma
ka perlu adanya kontrol akibat pemberian glukosa saja yai
tu pada perlakuan I.
Dari data kadar glukosa yang diperoleh ( tabel VIII )
terlihat bahwa kadar glukosa darah awal ( kadar glukosa -
darah puasa/ saat t=
0
,0
) berbeda untuk tiap perlakuan, meskipun pada subyek yang sama. Keadaan ini dapat disebabkan
oleh pengaruh lingkungan percobaan yang berbeda, misalnya
kebisingan dan lain-lain,sehingga dapat mempengaruhi emo-
da kadar glukosa dairah ( 1,14 ). Untuk mengetahui peruba-
han kadar glukosa darah akibat perlakuan, perlu dikoreksi
terhadap keadaan awalnya.Hasilnya dapat dilihat pada ta -
bel IX dan kurva perubahan kadar glukosa darah tersebut
dapat dilihat pada gambar
9
-14
. .Dari gambar terlihat bahwa umumnya kurva kontrol
berada di atas kurva tolbutamida maupun kurva dispersi so
lida tolbutamida' - PVP K-30 ( 20:80 ), yang berarti bahwa
kadar glukosa darah sebelum diberi obat lebih tinggi di
banding setelah diberi obat. Tetapi pada gambar 14, atau
data dari subyek
6
terlihat hal yang sebaliknya, sehinggadicoba dilakukan ’’Rejection of a Result” secara statistik.
llasilnya, data dari subyek
6
harus di ’’reject” , sehinggauntuk pengolahan data selanjutnya hanya dipakai data dari
lima subyek ( data dari subyek
6
tidak digunakan ).Untuk menentukan daya penurunan kadar glukosa darah
akibat pemberian bahan obat ( perlakuan II dan III ),per
lu dilakukan koreksi terhadap kontrol ( perlakuan I ) de
ngan cara seperti yang disebutkan dalam metoda penelitian
III.3.10.1. Besarnya daya penurunan kadar glukosa darah a
kibat pemberian obat pada masing-masing subyek dapat dili
hat pada tabel XI.
Hasil perhitungan dengan, statistik secara ANAVA
RCBD dari data daya penurunan kadar glukosa darah pada ma
sing-masing subyek dapat dilihat pada tabel XII. Terlihat
bahwa F hitung akibat pemberian obat =7,22 y F tabel
dar glukosa darah dari dispersi solida tolbutamida - PVP
K
-30
( 20:80 ) dan tolbutamida berbeda secara bermaknadimana daya penurunan kadar glukosa darah dari dispersi
solida tolbutamida - PVP K-30 ( 20:80 ) lebih besar dari
tolbutamida murni. Daya penurunan kadar glukosa darah mak
simum dispersi solida tolbutamida - PVP K-30 ( 20:80 ) =
57,78 ± 15,46 mg% dan tolbutamida = 45,90 + 18,27 mg%.Se
dangkan F hitung dari subyek, waktu, dan interaksi obat-
waktu hasilnya lebih kecil dariF tabel, sehingga dapat
dikatakan bahwa daya penurunan kadar glukosa darah yang
disebabkan faktor-faktor tersebut tidak berbeda bermakna.
Bila hasil penelitian ini dikaitkan dengan penoli-
tian terdahulu, yang menyatakan bahwa laju disoliuji dij-
persi solida tolbutamida lebih besar dari tolbutauiida mur
ni, maka dapat dikatakan bahwa peningkatan laju disolusi
tersebut diikuti dengan peningkatan efek farmakologi tol
butamida atau peningkatan bioavailabilitasnya.
Penelitian ini mendukung penelitian yang telah dila
kukan Sekikawa dkk (27). Dilaporkan bahwa ada pengaruh da
ri bentuk dispersi solida tolbutamida dalam pembawa PVP
terhadap laju disolusi in vitro dan bioavailabilitasnya. Dari
gambar
15
taippak bahwa laju disolusi dispersi solida tolbutamida - PVP ( 1:10 ) lebih besar dibandingkan campuran
fisis maupun tolbutamida murni. Peningkatan laju disolusi
tersebut tcrnyata diikuti dengan peningkatan kocepatan dan
jumlah tolbutamida yang mencapai plasma, setelah diberi
Waktu ( menit )
Gambar 15. Profil laju disolusi tolbutamida pada me dia disintegrasi (JP IX) pada suhu 37 °C
keterangan :
— O— : dispersi solida tolbutamida-PVr = 1:10 *— : dispersi solida tolbutamida-PVP = 1:5
— a— : dispersi solida tolbutamida-PVP = 1:3
— *— * : campuran fisis tolbutamida-PVP = 1:3 — •— : tolbutamida murni
Data teryebut sesuai dengan teori yang menyebutkan
bahwa laju disolusi dari bahan obat yang bersifat sukar
larut merupakan tabap penentu bagi proses absorbsinya (
1
).Dengan meningkatnya laju disolusi, akan meningkatkan laju
absorbsi sehingga jumlah obat dalam darah semakin besar.
Jumlah tolbutamida dalam darah dapat ditunjukkan dengan
besarnya efek farmakologi yang ditimbulkan, yaitu daya
penurunan kadar glukosa darah ( 1 4 ) . Sehingga daya penu
runan kadar glukosa darah dari dispersi solida tolbutami
da - PVP K-30 ( 20:80 ) yang lebih besar dari tolbutami
da murninya menunjukkan bahwa terdapat peningkatan bioa-
availabilitas tolbutamida.
Berdasarkan si fat sukar larut dari tolbutamida yan£
mengakibatkan lambatnya efek farmakologi yang ditimbulkan
dan berdasarkan meningkatnya bioavailabilitas tolbutamida
bila dibuat dispersi solida dalam pembawa PVP K-30, khu-
susnya pada komposisi 20:80,maka perlu dilakukan peneli
tian lebih lanjut untuk menentukan formula dan perbandi-
ngan yang tepat antara tolbutamida murni dan dispersi so
lida tolbutamida - PVP K-30 ( 20:80 ) sehingga diperoleh
suatu sediaan obat diabetes dengan efek terapi yang opti
BAB VI
K E S I M P U L A N
Berdasarkan data yang diperoleh dari perlakuan terha
dap lima subyek kelinci, dapat disimpulkan :
1. Ada perbedaan yang bermakna antara daya penurunan kadar
glukosa darah dari dispersi solida tolbutamida - PVP
K-30 ( 20 : 80 ) dan tolbutamida murni, dimana daya pe
nurunan kadar glukosa darah dari dispersi solida tolbu-
mida - PVP K-30 ( 20 : 80 ) lebih besar dibundingkan de
ngan tolbutamida murni,
2. Besar daya penurunan kadar glukosa darah maksimum dari
dispersi solida tolbutamida - PVP K-30 ( 20 : 80 ) ada-
lah 37,78 + 15,46 mg% dan tolbutamida murni adalah
BAB VIII
R I N G K A S A . N
Tolbutamida merupakan anti antidiabetika oral yang
bersifat sukar larut. Oleh karena sifat sukar larut terse
but, laju disolusi menjadi penentu bagi bioavailabilitasnya.
Dari penelitian terdahulu diketahui bahwa dispersi solida
tolbutamida - PVP K-30 ( 20:80 ) mempunyai .laju disolusi
yang lebih tinggi dari tolbutamida murni. Secara teori pe
ningkatan laju disolusi obat sukar larut akan menyebabkan
peningkatan laju absorbsi dan kadar obat dalam darah, se
hingga dapat memperbaiki bioavailabilitasnya.
Bioavailabilitas tolbutamida dapat ditentukan dengan mg,
nentukan daya penurunan kadar glukosa darahnya, yang meru
pakan cara penentuan bioavailabilitas cara tidak langsung.
Sehingga untuk membuktikan kebenaran teori tersebut telah
dilakukan penelitian pengaruh'dispersi solida tolbutamida-
PVP K-30 ( 20:80 ) dengan membandingkan daya penurunan ka
dar glukooa darahnya terhadap tolbutamida murni* dengan tQ,
leransi glukosa pada subyek kelinci. Kadar glukosa darah
ditentukan dengan metoda o-toluidin secara spektrofotometri.
Dari data yang diperoleh, kemudian diolah dengan per
hitungan statistik secara ANAVA dengan percobaan faktorial
dari rancangan blok lengkap yang acak ( "Randomized Com
pada oC =
0,05
menunjukkan bahwa antara daya penurunan ka dar glukosa darah dari dispersi solida tolbutamida - PVPK
-30
( 20:80 ) dengan tolbutamida murni ada perbedaan yangbermakna, dimana daya penurunan kadar glukosa darah dari
dispersi solida tolbutamida - PVP K-30 ( 20:80 ) lebih be
sar dari tolbutamida murni, Besar daya penurunan kadar glu
kosa darah dari dispersi solida tolbutamida - PVP K-30 (2
( 20:80 ) =
57
j78
+, 15,4-6 mg% dan tolbutamida murni = 45,94+ 18,27 mg#.
Dari hasil penelitian ini dapat diketahui bahwa pe
ningkatan laju disolusi dari dispersi solida ' tolbutamida
- PVP K-30 ( 20:80 ) menyebabkan peningkatan bioavailabili
las tolbutamida, yang ditunjukkan dengan poningkatan dava
BAB IX
DAFTAR PUSTAKA
1. Shargel L. and Yu A.B.C. Applied Biopharmaceutics and Pharmacokinetics. 2nd edition. Norwalk, Conecticut : A Apieton-Century-Croft,
1985
:26
-7
,67
-100
,129
-40
.2. Wagner J.G, Biopharmaceutics and Relevant Pharmacokine-s t
tics* 1 edition. Hamilton: Drug Intelegence Publica tion Inc, 1971:91, 98-9.
3* Blanchard J. Formulation Factors Afi'octin^ Dru^ [Uoav^i, bility. Amer. J. Pharm. Sept-Oct, 1978:133-6.
4. Polderman J. Formulation Preparation of Dosage Forms. Oxford: Elsevier, 1977:215-23.
5. Martin A.N. Physical Pharmacy. Philadelphia: Lea and Fe biger, 1969:91-3, 289-324
6
. Shefter Eli. Solubilization by Solid State Manipulation in Techniques of Solubilization of Drug. Marcel Dekker Inc, 1981:170-4.7. Chiou W.L. and Riegelman S. Pharmaceutical Application of Solid Dispersion Systems. J. Pharm. Sci. 1971; 60 : 1281-4.
8
. Lesson L.J. and Cartensen J.T. Dissolution Technology . Washington: The Industrial Pharmaceutical Technology Sec tica of The Academy of Pharmaceutical Science, 1974s8
, 125, 153-5.9. Ford J.L. The Current Status of Solid Dispersions. Pharm. Acta Helv. 1986; 6l:.69-88.
11. Sulistia Gan, Farmakologi dan Terapi. edisi ke-2. Ja -
karta: Bagian Farmakologi Fakultas Kedckteran Universi
tas Indonesia, 1980:353-7.
1'2. Nelson E., Knoechel E.L., Hamlin W.E. , and Wagner J.G. Influence of the Absorption Rate of Tolbutamide on the Rate of Decline of Blood Sugar Levels in Normal Humans. J. Pharm. Sci. 1962; 51 (6):509-14.
13. Yuniastuti E. Studi Penggunaan PVP K-25 dan PVP K-30 Terhadap Kecepatan Melarut Tolbutamida Dalam Sistem Dis persi Solida. Surabaya: Universitas Airlangga, 1988 .
50-106 pp. Skripsi.
14. Metzler C.M. Bioavaibility - A Problem in Equivalence . Biometrics, 1974; 50:309-17.
o t 15. Ritschel W.A. Handbook of Basic Pharmacokinetics. 1 e
edition. Hamilton: Drug Intelligence Publications Inc , 1976:62-75, 281-6.
16. Noyes A.A. and Whitney W.R. The Rate of Solution of So lid Substances in Their Own Solutions. J, Am. Chom,1897
; 19:930-3.
17* Gibaldi M. Biopharmaceutics and Clinical Pharmaceutics. r>ri
3 edition. Philadelphia: Lea and Febiger, 1984-49-70.
18. Goldberg A.H., Gibaldi M., Kanig J.L., Increasing Disso lution Rates and Gastrointestinal Absorption of Drug - .via Solid Solution and Eutectik Mixture II. J. Pharm .
Sci. 1966; 55:482.
19. Departemen Kesehatan Republik Indonesia. Farmakope Indo nesia. edisi III. Jakarta, 1979:610,738.
t h
20. Martindale, The Extra Pharmacopoeia. 28 edition. Lon don: The Pharmaceutical Press, 1982:859-60.
21. Florey K. Analytical Profiles of Drug Substances, volu me 3* New York: Academic Press, 1974:514-43*
23# Hazmam M.W. Endokrinologi dan Metabolisine, Bandung: Uni versitas Padjadjaran, 1968:13-42.
24« Harper H.A. Review of Physiological Chemistry ( Bioki - mia: terjemahan dr, Martin ). California: Lange Medical Publications, 1979:284-315*
25. Henry R.J, Cannon and Winkellman. Clinical Chemistry Principles and Technics. 2nc* edition. New York: Harper and Row, 1974*
26. Gerald R. and Cooper M.D. Workshop Manual of Methods, for the determination of Glucose. Washington D.C.
1966
: 70-5.27* Sekikawa H., Naganuma T., Fujiwara J., Nakano M., and - Arita T. Dissolution Behavior and Gastrointestinal Ab - sorption of Tolbutamide in Tolbutamide-Polyvinylpyroli- done Coprecipitate. Cherm. Pharm, Bull. 1979;27 (1):31-7.
28, Merck E. Diagnosis Merck. Buku Pedoraan Kerja Klinik, E. Merck, D a r m s t a d t 1979*
29, Brahmachari H.D. and Augusti K.T. Oral Hypoglycemic Com pound, Indian J. Physiol. Pharmacol. 1964; 8 (l):60-4.