commit to user
iPERBEDAAN JUMLAH EOSINOFIL, NEUTROFIL SPUTUM,
DAN VOLUME EKSPIRASI PAKSA DETIK PERTAMA
AKIBAT PEMBERIAN VITAMIN C PADA ASMA
TESIS
Untuk Memenuhi Sebagian Persyaratan Mencapai Derajat Magister
Program Studi Magister Kedokteran Keluarga
Minat Utama Biomedik
Oleh
Imron Riyatno
NIM S 500907018
PROGRAM PASCASARJANA
UNIVERSITAS SEBELAS MARET
commit to user
iiPERBEDAAN JUMLAH EOSINOFIL, NEUTROFIL SPUTUM,
DAN VOLUME EKSPIRASI PAKSA DETIK PERTAMA
AKIBAT PEMBERIAN VITAMIN C PADA ASMA
TESIS
Oleh
Imron Riyatno
NIM S 500907018
Komisi
Pembimbing
Nama Tanda Tangan Tanggal
Pembimbing I Dr. Eddy Surjanto, dr., SpP(K)
NIP. 195011041975111001
23-01-2013
Pembimbing II Prof. Dr. Suradi, dr., SpP(K), MARS NIP. 194705211976091001
23-01-2013
Telah dinyatakan memenuhi syarat pada tanggal 23-01-2013
Mengetahui
Ketua Program Studi Magister Kedokteran Keluarga
commit to user
iiiLEMBAR PENGESAHAN
PERBEDAAN JUMLAH EOSINOFIL, NEUTROFIL SPUTUM,
DAN VOLUME EKSPIRASI PAKSA DETIK PERTAMA
AKIBAT PEMBERIAN VITAMIN C PADA ASMA
TESIS
Oleh Imron Riyatno NIM S 500907018
Tim Penguji:
Jabatan Nama Tanda Tangan Tanggal
Ketua Dr. Hari Wujoso, dr., SpF, MM 23-01-2013 NIP. 196210221995031001
Sekretaris Prof. Dr. Muchsin D., dr., MARS, PFarK, AIFO 23-01-2013
NIP. 194805311976031001
Anggota 1. Dr. Eddy Surjanto, dr., SpP(K) 23-01-2013 Penguji NIP. 195011041975111001
2. Prof. Dr. Suradi, dr., SpP(K), MARS 23-01-2013 NIP. 194705211976091001
Telah dipertahankan di depan penguji Dinyatakan telah memenuhi syarat
pada tanggal 23-01-2013
Direktur Program Pascasarjana UNS
Prof. Dr. Ir. Ahmad Yunus, MS NIP. 196107171986011001
Ketua Program Studi Magister Kedokteran Keluarga
commit to user
ivPERNYATAAN ORISINALITAS DAN PUBLIKASI ISI TESIS
Saya menyatakan dengan sebenarnya bahwa :
1. Tesis yang berjudul JUMLAH EOSINOFIL, NEUTROFIL
SPUTUM, DAN VOLUME EKSPIRASI PAKSA DETIK PERTAMA AKIBAT
PEMBERIAN VITAMIN C PADA ASMA
plagiat, serta tidak terdapat karya ilmiah yang pernah diajukan oleh orang lain
untuk memperoleh gelar akademik serta tidak terdapat karya atau pendapat yang
pernah ditulis atau diterbitkan oleh orang lain kecuali secara tertulis digunakan
sebagai acuan dalam naskah ini dan disebutkan dalam sumber acuan serta daftar
pustaka. Apabila di kemudian hari terbukti terdapat plagiat dalam karya ilmiah ini,
maka saya bersedia menerima sanksi sesuai ketentuan peraturan
perundang-undangan (Permendiknas No 17, tahun 2010).
2. Publikasi sebagian atau keseluruhan isi tesis pada jurnal atau forum ilmiah lain
harus seijin dan menyertakan tim pembimbing sebagai author dan PPs UNS
sebagai institusinya. Apabila dalam waktu sekurang-kurangnya satu semester sejak
pengesahan tesis saya tidak melakukan publikasi dari sebagian atau keseluruhan
tesis ini, maka Prodi Magister Kedokteran Keluarga UNS berhak
mempublikasikannya pada jurnal ilmiah yang diterbitkan oleh Prodi Magister
Kedokteran Keluarga PPs-UNS. Apabila saya melakukan pelanggaran dari
ketentuan publikasi ini, maka saya bersedia mendapatkan sanksi akademik yang
berlaku.
Surakarta, -01-2013
Mahasiswa
Imron Riyatno
commit to user
vKATA PENGANTAR
Puji syukur kehadirat Allah SWT penulis ucapkan atas terselesaikannya tesis
ini. Tesis ini merupakan sebagian persyaratan mencapai derajat Magister Kesehatan
dan Pendidikan Dokter Spesialis Pulmonologi dan Ilmu Kedokteran Respirasi
Fakultas Kedokteran Universitas Sebelas Maret Surakarta. Upaya kerjasama berbagai
pihak, bimbingan, pengarahan dan bantuan para guru, keluarga, teman sejawat
residen paru, karyawan rumah sakit, serta para pasien selama penulis menjalani
pendidikan merupakan kunci keberhasilan penyusunan tesis ini.
Ucapan terima kasih dan penghargaan setinggi-tingginya penulis sampaikan
kepada Dr. Hari Wujoso, dr., SpF., MM selaku Ketua Program Studi Magister
Ke-dokteran Keluarga dan Afiono Agung Prasetyo, dr., PhD selaku Ketua Minat Utama
Biomedik, para guru besar dan seluruh staf pengajar serta petugas administrasi Pasca
Sarjana Universitas Sebelas Maret Surakarta atas kesempatan dan bimbingan yang
diberikan kepada penulis untuk memperoleh dan menyelesaikan pendidikan Magister
Kesehatan di Universitas Sebelas Maret Surakarta.
Penulis menyampaikan ucapan terima kasih dan penghargaan
setinggi-tingginya kepada:
1. Prof. Dr. Suradi, dr., SpP(K), MARS
Ketua Program Studi PPDS Pulmonologi dan Ilmu Kedokteran Respirasi Fakultas
Kedokteran Universitas Sebelas Maret Surakarta sekaligus pembimbing II
penelitian ini yang telah memberikan arahan, bimbingan, dorongan, petunjuk, dan
koreksi yang sangat bermanfaat.
2. Dr. Eddy Surjanto, dr., SpP(K)
Kepala Bagian Pulmonologi RSUD Dr. Moewardi Surakarta sekaligus pemxx
bimbing I penelitian ini yang telah memberikan arahan, bimbingan, dorongan,
petunjuk, dan koreksi yang sangat bermanfaat. .
commit to user
viBeliau menanamkan kemandirian, percaya diri, kebersamaan dan dedikasi tinggi
terhadap kemajuan pendidikan kedokteran khususnya di bidang Pulmonologi yang
memberikan makna yang dalam buat penulis. Penulis mengucapkan terima kasih
atas nasehat dan saran beliau terhadap kemajuan ilmu Pulmonologi.
4. Yusup Subagio Sutanto, dr., SpP(K)
Wakil Direktur Pelayanan RSUD Dr. Moewardi Surakarta dan pengajar di bagian
Pulmonologi yang telah memberikan petunjuk, bimbingan, saran dan kritik yang
membangun. Beliau selalu menanamkan nilai-nilai kedisiplinan yang sangat
berarti. Beliau juga mengajarkan ilmu manajemen pelayanan yang sangat
bermanfaat bagi penulis.
5. Dr. Reviono, dr., SpP(K)
Pembantu Dekan II Fakultas Kedokteran Universitas Sebelas Maret Surakarta
sekaligus pengajar di bagian Pulmonologi yang senantiasa membimbing,
mendorong, dan memberi masukan yang bermanfaat selama pendidikan, disela
kesibukannya. Terima kasih penulis ucapkan atas ilmu dan petunjuk yang telah
diberikan selama menjalani pendidikan pulmonologi.
6. Ana Rima Setijadi, dr., SpP(K)
Sekretaris Program Studi PPDS dan pengajar di bagian Pulmonologi dan Ilmu
Kedokteran Respirasi Fakultas Kedokteran Universitas Sebelas Maret Surakarta
yang senantiasa membimbing, mendorong, dan memberi masukan yang
baermanfaat selama pendidikan. Terima kasih penulis ucapkan atas bimbingan,
saran, koreksi dan kritik yang telah diberikan selama penulis menjalani pendidikan
di bagian Pulmonologi.
7. Harsini, dr., SpP
Beliau senantiasa membimbing, mendorong dan memberi masukan yang
bermanfaat selama pendidikan. Terima kasih penulis ucapkan atas bimbingan,
saran, koreksi dan kritik yang telah diberikan selama penulis menjalani pendidikan
commit to user
vii8. Jatu Aphridasari, dr., SpP
Beliau senantiasa membimbing, mendorong dan memberi masukan yang
bermanfaat selama pendidikan. Terima kasih penulis ucapkan atas bimbingan,
saran, koreksi dan kritik yang telah diberikan selama penulis menjalani pendidikan
di bagian Pulmonologi.
Ucapan terima kasih penulis sampaikan kepada staf pengajar lain yaitu:
Fordiastiko, dr., SpP, Hasto Nugroho, dr., SpP, IGN. Widyawati, dr., SpP, Windu
Prasetya, dr., SpP, Dwi Bambang, dr., SpP, Juli Purnomo, dr., SpP atas bimbingan
dan pengarahan yang sangat berguna selama penulis mengikuti pendidikan keahlian.
Penulis menyampaikan ucapan terima kasih juga kepada:
1. Direktur RSUD Dr. Moewardi Surakarta
2. Direktur Pasca Sarjana UNS Surakarta
3. Dekan Fakultas Kedokteran UNS Surakarta
4. Kepala Bagian Imu Bedah RSUD Dr. Moewardi/FK UNS
5. Kepala Bagian Ilmu Penyakit Dalam RSUD Dr. Moewardi/FK UNS
6. Kepala Bagian Radiologi RSUD Dr. Moewardi/FK UNS Surakarta
7. Kepala Bagian Kardiologi RSUD Dr. Moewardi/FK UNS Surakarta
8. Kepala Bagian Kesehatan Anak RSUD Dr. Moewardi/FK UNS Surakarta
9. Kepala Bagian Anestesi RSUD Dr. Moewardi/FK UNS Surakarta
10.Kepala Instalasi Gawat Darurat RSUD Dr. Moewardi Surakarta
11.Direktur Rumah Sakit Paru Dr. Ario Wirawan Salatiga
12.Direktur RSUD Sragen
13.Kepala BKPM Semarang
14.Kepala BKPM Klaten
15.Kepala BKPM Pati
16.Kepala BKPM Magelang
beserta seluruh staf atas bimbingan dan ilmu pengetahuan yang diberikan selama
commit to user
viiiPenghargaan, penghormatan, dan rasa terima kasih yang setinggi-tingginya
penulis sampaikan kepada ayahanda Soekono dan ibunda tercinta Mukajatin atas
asuhan, didikan, pengorbanan, dukungan, ketulusan, dan doa yang senantiasa
dipanjatkan. Kepada istri tercinta Rahayu Susilowati yang senantiasa setia, menerima
apa adanya dan mendukung setiap langkah suami sampai akhirnya dapat
menyelesaikan pendidikan ini. Untuk anak tercinta: Fatin Yurin Azimah, Zarid Yurin
Ganendra, dan Fizara Yurin Mahestri, buah hati tersayang yang mampu mengubah
suasana sedih dan letih menjadi riang. Kepada seluruh keluarga tercinta, kakak, adik
dan keponakan-keponakan yang selalu memberi dukungan dan bantuan penulis
sepenuh hati untuk menyelesaikan pendidikan ini.
Rasa hormat dan terima kasih penulis sampaikan kepada senior yang telah
lebih dulu menyelesaikan pendidikan: Wayan Agus Putra, dr., SpP, Joko Susilo, dr.,
SpP, Eny, dr., SpP, Eva LM, dr., SpP, Rianasari, dr., SpP, Juli P,, dr., SpP, M Irpan,
dr., SpP, M Gani, dr., SpP, Niwan T, dr., SpP, Sofyan B, dr., SpP, Dyah, dr., SpP,
Novita, dr., SpP, Rita, dr., SpP, Fitri, dr., SpP, Aji, dr., SpP, Rudi, dr., SpP, Wawan,
dr., SpP, dan seluruh rekan PPDS Pulmonologi dan Ilmu Kedokteran Respirasi FK
UNS/ RSUD Dr. Moewardi Surakarta.
Ucapan terima kasih khusus penulis ucapkankan kepada rekan seangkatan:
Yudi Prasetyo, dr.,SpP, dan Farih Raharjo, dr., yang telah banyak membantu dan
memberi motivasi sehingga terlaksananya penelitian. Terima kasih pula penulis
ucapkan kepada: Natalie Duyen, dr., Ratna, dr., Miftahuddin, dr., Nugroho, dr.,
Aprilludin, dr., Anita, dr., Yusvi, dr., Lulu, dr., Reni, dr., Dwi Indrayani, dr., Yunita,
dr., Musdalifah, dr., Dina, dr., Magdalena Sutanto, dr., Leonardo, dr., Nisfi, dr.,
Lydia, dr., Prima, dr.,Naifarat, dr., Hayu, dr., serta seluruh rekan peserta PPDS yang
lain atas bantuan selama penelitian berlangsung.
Penghargaan dan terima kasih penulis sampaikan kepada seluruh pasien,
semua rekan perawat poliklinik paru (bu Krisni, bu Lestari, pak Ranto, pak
Kuswanto) dan bangsal rawat/poliklinik paru di RSUD Dr. Moewardi, RSUD Sragen,
commit to user
ixBKPM Semarang serta rekan kerja di SMF paru (mas Waluyo, mbak Yamti, mbak
Anita, mbak Ira dan mas Arif), dan mas Harnoko.
Penulis menyadari bahwa tesis ini masih banyak kekurangan, saran serta
kritik penulis harapkan dalam rangka perbaikan penulisan tesis ini. Semoga dengan
rahmat dan anugerah Allah SWT atas ilmu dan pengalaman yang penulis miliki dapat
bermanfaat bagi sesama.
Surakarta, Desember 2012
commit to user
xImron Riyatno (NIM S 500907018). 2013. Perbedaan Jumlah Eosinofil, Neutrofil
Sputum, dan Volume Ekspirasi Paksa Detik Pertama akibat Pemberian Vitamin C Pada Asma. Tesis. Supervisor I: Dr. Eddy Surjanto, dr., SpP(K). II: Prof. Dr.
Suradi, dr., Sp.P(K),MARS. Program Pendidikan Dokter Spesialis Pulmonologi dan Ilmu Kedokteran Respirasi Fakultas Kedokteran Universtas Sebelas Maret Surakarta.
RINGKASAN
PERBEDAAN JUMLAH EOSINOFIL, NEUTROFIL SPUTUM, DAN VOLUME EKSPIRASI PAKSA DETIK PERTAMA AKIBAT
PEMBERIAN VITAMIN C PADA ASMA
Imron Riyatno
Pendahuluan: Inflamasi kronik saluran napas pasien asma mengakibatkan kondisi
stres oksidatif yang terjadi karena peningkatan produksi oksidan dan atau berkurangnya produksi antioksidan. Vitamin C dapat berperan sebagai antioksidan dan imunoregulator sehingga dapat menurunkan gen proinflamasi. Eosinofil dan neutrofil merupakan indikator derajat inflamasi di saluran napas, nilai VEP1 menunjukkan derajat obstruksi saluran napas.
Tujuan: Mengetahui dan menganalisis perbedaan jumlah eosinofil, neutrofil sputum
dan VEP1 pada asma terkontrol sebagian dan tidak terkontrol terhadap pemberian vitamin C.
Metode: Rancangan penelitian adalah uji klinis quasi-experimental, consecutive
sampling, rancangan pretest-postest.Subyek penelitian adalah pasien asma terkontrol
sebagian dan tidak terkontrol. Variabel bebas adalah vitamin C 2x500 mg selama 14 hari. Variabel tergantung adalah jumlah eosinofil, neutrofil sputum dan %VEP1.
Hasil: Subyek yang dianalisis 30 pasien, terdiri dari 15 pasien (50%) asma terkontrol
sebagian dan 15 pasien (50%) asma tidak terkontrol. Sebelum dan sesudah pemberian vitamin C pada asma terkontrol sebagian didapatkan rerata eosinofil 3,93±2,66% dan 3,07±1,75% (p=0,126), neutrofil 48,80±25,52% dan 33,87±18,56% (p= 0,030),
%VEP1 82,27±14,78% dan 86,98±22,61% (p=0,355). Sebelum dan sesudah
pemberian vitamin C pada asma tidak terkontrol didapatkan rerata eosinofil 5,80±2,40 dan 6,40±5,90% (p=0,587), neutrofil 56,13±22,79% dan 48,87±15,43%
(p=0,349), %VEP1 74,79±28,59% dan 83,91±19,09% (p=0,046).
Kesimpulan: Terdapat penurunan jumlah neutrofil pada asma terkontrol sebagian
dan kenaikan %VEP1 pada asma tidak terkontrol yang bermakna sesudah pemberian
vitamin C. Terdapat perbedaan yang tidak bermakna eosinofil sputum dan % VEP1 penderita asma terkontrol sebagian, serta jumlah eosinofil dan neutrofil sputum pasien asma tidak terkontrol antara sebelum dan sesudah pemberian vitamin C.
commit to user
xiImron Riyatno (NIM S 500907018). 2013. Differences of Eosinophils, Neutrophils
Sputum and FEV1 after Administration of Vitamin C in Asthmatic Patient.
Tesis. Supervisor I: Dr. Eddy Surjanto, dr., SpP(K). II: Prof. Dr. Suradi, dr., Sp.P(K),MARS. Master Program in Family Medicine, Post-Graduate Program, Sebelas Maret University Surakarta.
ABSTRACT
DIFFERENCES OF EOSINOPHILS, NEUTROPHILS SPUTUM AND FEV1
AFTER ADMINISTRATION OF VITAMIN C IN ASTHMATIC PATIENT
Imron Riyatno
Introduction: Chronic inflammation of the asthmatic airways of patients results from
increasing oxidative stress either due to elevation of oxidant production or depression of antioxidants production. Vitamin C acts as antioxidants and imunoregulator thus reducing proinflammatory genes. Eosinophils and neutrophils counts are the indicator of airway inflammation degree. The value of FEV1 indicates airway obstruction degree.
Objective: The studi was conducted to determine and analyze the differences of
sputum eosinophils and neutrophils counts, FEV1 value on partly controlled and uncontrolled asthmatic subject after vitamin C administration.
Methods: The study design was quasi-experimental clinical trial, consecutive
sampling, pretest-posttest design. Subjects were partly-controlled and uncontrolled asthmatic patients. The independent variable was vitamin C 500 mg twice a day for 14 days. Dependent variable were sputum eosinophils and neutrophils counts, and % FEV1 value.
Results: Total sample were 30 patients, consist of 15 patients (50%) partly
controlled asthma and 15 patients (50%) uncontrolled asthma. The sputum eosinophils count before and after vitamin C administration on partly-controlled asthmatic patient were 3.93 ± 2.66% and 3.07 ± 1.75% (p = 0.126), neutrophils count
were 48.80 ± 25.52% and 33.87 ± 18.56% (p = 0.030), %FEV1 were 82.27 ± 14.78%
and 86.98 ± 22.61% (p = 0.355). The sputum eosinophils count before and after vitamin C administration on uncontrolled asthmatic patient were 5.80 ± 2.40% and 6.40 ± 5.90% (p = 0.587), neutrophils count were 56.13 ± 22.79% and 48.87 ± 15.43% (p = 0.349), %FEV1 were 74.79 ± 28.59% and 83.91 ± 19.09% (p = 0.046).
Conclusion: There was a decreasing sputum neutrophils count on partly-controlled of
asthmatic patient and increasing %FEV1 in uncontrolled asthmatic patient after vitamin C administration. There were no significant differences of sputum eosinophils and %FEV1 in partly controlled asthmatic patient, as well as eosinophils and neutrophils count sputum in uncontrolled asthmatic patients before and after vitamin C administration.
commit to user
xiiDAFTAR ISI
HALAMAN JUDUL ... i
LEMBAR PENGESAHAN... ii
PERNYATAAN ORISINALITAS DAN PUBLIKASI ISI TESIS ...iv
KATA PENGANTAR ... v
RINGKASAN ...xi
ABSTRACT ...xii
DAFTAR ISI ... xiii
DAFTAR SINGKATAN KATA ... xvii
DAFTAR GAMBAR DAN TABEL...xix
DAFTAR LAMPIRAN ...xxi
BAB I. PENDAHULUAN A. Latar belakang penelitian... 1
B. Rumusan masalah... 6
C. Tujuan penelitian... 6
D. Manfaat penelitian... 7
BAB II. TINJAUAN PUSTAKA A. . 8
1. 2. Tingkat Kontrol Asma...9
3. Sel Inflamasi Pada Asma...10
a) Sel mast... 10
b) Limfosit T... c) Makrofag... 12
d) Neutrofil ...13
e) Sel dendritik... 14
f) Basofil... 15
commit to user
xiiih)Sel epitel dan fibroblas...16
i) Sitokin... 17
4. Patogenesis Asma... 21
5. Peran Stres Oksidatif Pada Patogenesis 23 6. Patologi Asma... 26
7. Patofisiologi Asma... 28
a) Obstruksi saluran napas b) Hiperesponsivitas saluran napas c) Hipersekresi mukus 8. Peran Stres Oksidatif Pada Patofisiologi Asma .31 9. 10. Pemeriksaan Faal Paru pada B. VITAMIN C... ....35
1. Biokimia vitamin C...36
2. Peran vitamin C pada sistem imunitas...`...37
3. Vitamin C sebagai antioksidan ...37
C. KERANGKA KONSEPTUAL...41
D. HIPOTESIS ...44
BAB III. METODOLOGI PENELITIAN A. RANCANGAN PENELITIAN... 45
B. TEMPAT DAN WAKTU PENELITIAN...45
C. POPULASI PENELITIAN... 45
D. KRITERIA INKLUSI, EKSKLUSI DAN DISKONTINYU... 45
E. JUMLAH SAMPEL.PENELITIAN ...46
F. IDENTIFIKASI VARIABEL... 47
G. DEFINISI OPERASIONAL... 48
H. ANALISIS DATA...51
I. CARA PENELITIAN... 51
commit to user
xivK. ETIKA PENELITIAN... 55
L. ALUR PENELITIAN... 56
BAB IV.HASIL DAN PEMBAHASAN A. HASIL PENELITIAN ... 57
B. PEMBAHASAN ... . 68
BAB V. SIMPULAN DAN SARAN A. ... 82
B. SARAN ... . 82
DAFTAR PUSTAKA...83
commit to user
xvDAFTAR SINGKATAN KATA
AA : asam askorbat
APC : antigen precenting cells
APE : arus puncak ekspirasi
BAL : bronchoalveolar lavage
CD : cluster differentiation
COX-2 : cycloxygenase-2
CTL : cytotoxic T lymphocyte
DALYs : disability-adjusted life years)
DHA : asam dehidroaskorbat
DNA : deoxyribo nucleid acid
ECP : eosinophil cationic protein
EDN : eosinophil derived neurotoxin
EPO : eosinophil peroxidase
FEF : forced expiratory flow
GINA : global initiative for asthma
GM-CSF : granulocyt monocyt-colony stimulating factor
HAA : hydroxyanthranilate
ICAM-1 : intercellular adhesion molecule-1
IFN- : interferon gamma
IgE : imunoglobulin E
IL : interleukin
iNOS : inducible nitric oxide synthase
KV : kapasitas paksa
KVP : kapasitas vital paksa
LPS : lipopoly-saccharide
LTB4 : leucotrien B4
MBP : major basic protein
commit to user
xviMHC : major histocompatibility complex
MIP : macrophage inflammatory protein
NF- : nuclear factor
-NHLBI : National Institute of Health National Heart, Lung, and Blood Institute
Nrf2 : nuclear factor like 2
PAF : plateletactivating factor
PDGF : platelet derived growth factor
PDPI : Perhimpunan Dokter Paru Indonesia
PGF2 : prostaglandin F2
RANTES : regulation on activation normal T cell expressed and secreted
ROS : reactive oxygen species
SOD : superoxide dismutase
STAT : signal transducer and activator of transcription
TGF : transforming growth factor
TGF- : transforming growth factor-
Th2 : T helper2
TLR : toll like receptor
TNF- : tumor necrosis factor-
VCAM-1 : vascular cell adhesion molecule-1
VEP1 : volume ekspirasi paksa detik pertama
WHO : world health organization
commit to user
xviiDAFTAR GAMBAR DAN TABEL Halaman
Gambar 1 : Peran sitokin pada asma... 21
Gambar 2 : Patogenesis asma 23 Gambar 3 : Peran stres oksidatif pada asma 26 Gambar 4 : Patofisiologi asma 32
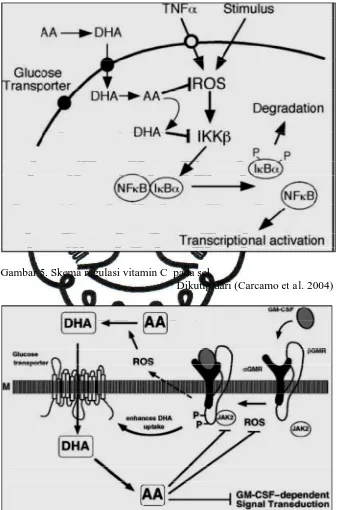
Gambar 5 : Skema 41
Gambar 6 : Skema inhibisi sinyal GM-CSF oleh vitamin C... 42
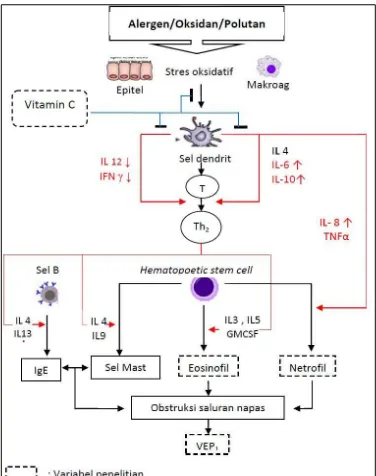
Gambar 7 : Kerangka konseptual... 44
Gambar 8 : Alur penelitian...57
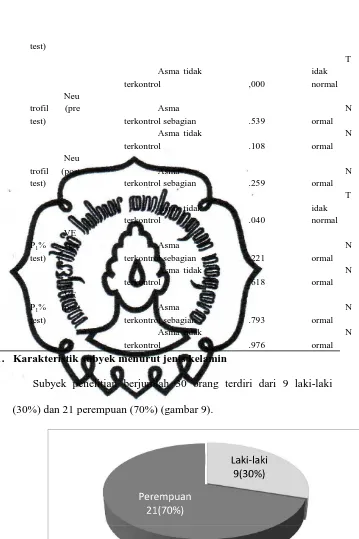
Gambar 9 : Jumlah sampel menurut jenis kelamin... 60
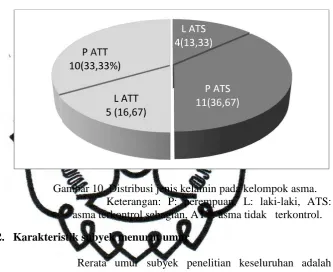
Gambar 10 : Distribusi jenis kelamin pada kelompok asma... 60
commit to user
xviiiDAFTAR TABEL Halaman
Tabel 1 : Karakteristik dasar subyek penelitian... 59
Tabel 2 : Uji normaltas menggunakan parameter Shapiro-Wilk... 59
Tabel 3 : Perbedaan jumlah eosinofil, neutrofil sputum dan volume ekspirasi
paksa detik pertama pada asma terkontrol sebagian terhadap
64
Tabel 4 : Perbedaan jumlah eosinofil, neutrofil sputum dan volume ekspirasi
paksa detik pertama pada asma tidak terkontrol terhadap pemberian
vitamin C...66
Tabel 5 : Perbedaan jumlah eosinofil, neutrofil sputum dan volume ekspirasi
paksa detik pertama antara asma terkontrol sebagian dengan asma
tidak terkontrol sebelu 68
Tabel 6 : Perbedaan jumlah eosinofil, neutrofil sputum dan volume ekspirasi
paksa detik pertama pada asma terkontrol sebagian dan tidak
commit to user
xixDAFTAR LAMPIRAN Halaman
Lampiran 1 : Lembar penjelasan kepada penderita... 90
Lampiran 2 : Lembar persetujuan mengikuti penelitian... 94
Lampiran 3 : Lembar data penderita... 95
Lampiran 4 : Lembar teknik pemeriksaan...97
Lampiran 5 : Lembar isian kelaikan etik...98
Lampiran 6 : Kelaikan etik ...102
Lampiran 7 : Jadwal penelitian...103
Lampiran 8 : Rekapitulasi hasil pemeriksaan laboratorium...104
Lampiran 9 : Rekapitulasi data...111
Lampiran 10: Analisis data SPSS 15...112
commit to user
1
BAB I. PENDAHULUAN
A. LATAR BELAKANG PENELITIAN
Asma tidak hanya menyebabkan masalah kesehatan tetapi juga masalah
ekonomi dan sosial. Data World Health Organization (WHO) menyebutkan
prevalensi total penderita asma di dunia diperkirakan 1-18 %, dan
diperkira-kan meningkat hingga 400 juta pada tahun 2025. Prevalensi asma meningkat
di banyak negara terutama pada anak. Kematian karena asma diperkirakan
250.000 jiwa setiap tahun dan diperkirakan 15 juta disability-adjusted life
years (DALYs) hilang setiap tahun, hal ini mewakili 1% total penyakit global
(NHLBI 2009). Prevalensi asma di Indonesia pada tahun 1995 sekitar
13/1000 (1,3 %) lebih tinggi dibanding bronkitis kronik (1,1 %) (PDPI 2004).
Proses penyakit asma melibatkan inflamasi kronik pada saluran napas.
Reaksi inflamasi tersebut mengakibatkan peningkatan stres oksidatif yang
berperan dalam patogenesis asma (Cho dan Moon 2010). Stres oksidatif
terjadi karena peningkatan produksi oksidan atau berkurangnya produksi
anti-oksidan sehingga mengakibatkan gangguan kesetimbangan antara anti-oksidan
dan antioksidan. Peningkatan produksi oksidan diantaranya disebabkan
inflamasi pada saluran napas pasien asma. Sel makrofag saluran napas pasien
asma menghasilkan kadar superoksida lebih tinggi dibanding subyek normal.
Polusi udara juga merangsang peningkatan oksidan eksogen yang
ber-pengaruh terhadap insidensi asma. Penurunan kapasitas pertahanan
commit to user
2
Beberapa gangguan pertahanan antioksidan pada asma mekanismenya sudah
diketahui, diantaranya: berkurangnya kadar selenium (elemen penting
aktivasi glutathione peroxidase), serta berkurangnya kadar tembaga dan seng
yang mengandung superoxide dismutase (Cu, Zn-SOD). Polimorfisme
genetik pada pengaturan antioksidan enzimatik Mangan yang mengandung
superoxide dismutase (Mn-SOD), glutathione S-transferase, nuclear factor
like 2 (Nrf2) dan peroksiredoksin juga didapatkan pada penderita asma
(Dworski 2000, Cho dan Moon 2010).
Kondisi stres oksidatif dapat meningkatkan sitokin proinflamasi dan
pe-rubahan fungsi enzimatik. Reaksi oksidatif akan merubah struktur protein
penyusun enzim intrasel sehingga aktivitasnya berubah. Perubahan aktivitas
enzim menyebabkan aktivasi faktor transkripsi yang berdampak peningkatan
ekspresi gen penyebab proliferasi sitokin. Kondisi tersebut diatas akan
memperberat reaksi inflamasi dan cedera jaringan (Kregel dan Zhang 2007,
Holguin dan Fitzpatrick 2010). Kehilangan kontrol oksidan di saluran napas
menimbulkan inisiasi sel T helper2 (Th2) yang merupakan fase awal
perkembangan inflamasi alergi dalam saluran napas. Peningkatan kadar
reactive oxygen species (ROS) dalam antigen presenting cel (APC)
mempengaruhi sistem imunitas akibat respon Th2 (Peterson et al. 1998). Stres
oksidatif berperan terhadap perkembangan atau kelangsungan inflamasi
saluran napas dengan cara menginduksi beragam mediator proinflamasi.
Perkembangan dan kelangsungan inflamasi tersebut menimbulkan
commit to user
3
bronkus, dan stimulasi sekresi mukus. Semua hal tersebut diatas terkait
dengan tingkat keparahan asma (Terada 2006, Fitzpatrick et al. 2009, Cho
dan Moon 2010).
Reaksi inflamasi dalam saluran napas penderita asma menyebabkan
aktivasi eosinofil, sehingga jumlahnya meningkat. Terdapat hubungan jumlah
eosinofil, derajat asma, hiperreaktivitas bronkus dan tingkat eksaserbasi pada
pasien asma (Filipofic dan Cekic 2001, Surjanto 2005, Apter dan Weiss
2008). Penelitian membuktikan bahwa jumlah eosinofil di darah perifer dan
bilasan bronkus pasien asma berhubungan dengan berat klinis asma
(Bousquet et al. 2000).
Saluran napas penderita asma akut dan kronik terdapat peningkatan
jumlah dan aktivasi neutrofil (Monteseirin 2009). Peningkatan kadar neutrofil
menyebabkan kerusakan saluran napas akibat pelepaskan sitokin dan
kemokin seperti interleukin (IL)-1, IL-6, IL-8, dan tumor necrosis factor-
(TNF- metabolisme oksigen, protease, dan bahan kationik
(Kips 2001, PDPI 2004).
Tujuan utama pengobatan asma adalah untuk mencapai keadaan asma
terkontrol (NHLBI 2009). Tingkat kontrol asma adalah manifestasi
perubah-an berupa berkurperubah-ang atau hilperubah-angnya gejala dperubah-an tperubah-anda asma setelah mendapat
terapi (Taylor et al. 2008). Kondisi asma terkontrol dapat meningkatkan dan
mempertahankan kualitas hidup agar penderita asma dapat hidup normal
tanpa hambatan dalam melakukan aktivitas sehari-hari (PDPI 2004). Kriteria
commit to user
4
terkontrol, terkontrol sebagian, dan tidak terkontrol. Tingkat kontrol asma
tidak hanya menunjukkan kondisi klinis tingkat keparahan asma tapi juga
dapat dipakai sebagai petunjuk untuk mengetahui derajat inflamasi yang
mendasari patofisiologi asma. Derajat inflamasi yang semakin berat akan
meningkatkan obstruksi saluran napas dan meningkatkan risiko eksaserbasi
(NHLBI 2009).
Gejala asma ditandai dengan adanya keterbatasan aliran udara yang bisa
diukur dengan alat spirometri. Derajat obstruksi dapat dinilai dengan
penurunan volume ekspirasi paksa detik pertama (VEP1). Pemeriksaan
spirometri juga dapat menilai reversibilitas setelah pemberian bronkodilator
(NHLBI 2009).
Mekanisme pertahanan antioksidan meliputi non-enzimatik (vitamin
anti-oksidan dan tiol) serta enzimatik (superoxide dismutases/ SOD, katalase, dan
glutathione peroxidase) (Terada 2006). Vitamin C termasuk salah satu
antioksidan nonenzimatik, bersifat larut air, dan berperan penting pada fungsi
metabolisme tubuh. Vitamin ini terbagi menjadi dua bentuk biologis aktif
yaitu asam askorbat (AA) dan asam dehidroaskorbat (DHA). Vitamin C
bertindak sebagai donor elektron untuk membalikkan reaksi oksidasi
sehingga bisa berfungsi sebagai antioksidan yang bereaksi dengan radikal
bebas dan mendeaktivasi oksidan sebelum terjadi kerusakan pada protein atau
lipid (Padayatty et al. 2003). Sebagai antioksidan kuat dapat membantu
menetralisir polutan dan toksin serta mampu menghambat histamin, suatu
commit to user
5
patogenesis asma (Ottobani F dan Ottobani A 2005). Vitamin C berperan
dalam sistem regulasi intraselular (imunoregulator) yang mengakibatkan
menurunnya ekspresi gen proinflamasi (Carcamo et al. 2002, Carcamo et al.
2004). Vitamin C dapat meregenerasi antioksidan lain (vitamin E), sintesis
kolagen, substansi interselular yang membentuk struktur otot, pembuluh
darah jaringan, tulang, tendon dan ligamen. Vitamin C memainkan peran
dalam sintesis beberapa hormon peptida penting dan neurotransmiter serta
karnitin juga meningkatkan penyerapan zat besi dari makanan yang
diperlukan untuk metabolisme asam empedu (Ottobani F dan Ottobani A
2005).
Terdapat bukti hubungan antara fungsi paru dengan asupan buah,
sayuran, vitamin A, C, dan E pada anak. Asupan vitamin A, C, dan E rendah
dikaitkan dengan penurunan kapasitas vital paksa (KVP), VEP1, dan forced
expiratory flow 25-75 % (FEF 25-75 %) (Gilliland et al. 2003). Tingkat
fungsi paru lebih rendah pada anak juga dihubungkan dengan rendahnya
asupan makanan yang mengandung vitamin antioksidan (Harik et al. 2004).
Pemberian vitamin C dosis 1000 mg per oral pada penderita asma dapat
meningkatkan dosis metakolin yang dibutuhkan untuk menurunkan nilai
VEP1 sebesar 40% (pD40) (Mohsenin et al. 1983). Penelitian tentang
pemberian per oral vitamin C 1000 mg / hari secara bermakna dapat
menurunkan kebutuhan kortikosteroid inhalasi pada penderita asma (Fogarty
commit to user
6
Seberapa besar peran pemberian vitamin C sebagai antioksidan dan
imunoregulator terhadap inflamasi dan derajat obstruksi saluran napas pada
asma belum diketahui. Berdasar hal tersebut dilakukan penelitian untuk
mengetahui peran vitamin C terhadap jumlah eosinofil dan neutrofil sputum
sebagai penanda inflamasi serta nilai VEP1 sebagai penanda obstruksi saluran
napas penderita asma terkontrol sebagian dan tidak terkontrol.
B. RUMUSAN MASALAH
Rumusan masalah pada penelitian ini adalah:
1. Apakah pemberian vitamin C dapat menurunkan jumlah eosinofil dan
neutrofil sputum pada penderita asma terkontrol sebagian.
2. Apakah pemberian vitamin C dapat meningkatkan nilai VEP1 pada
penderita asma terkontrol sebagian.
3. Apakah pemberian vitamin C dapat menurunkan jumlah eosinofil dan
neutrofil sputum pada penderita asma tidak terkontrol.
4. Apakah pemberian vitamin C dapat meningkatkan nilai VEP1 pada
penderita asma tidak terkontrol.
C. TUJUAN PENELITIAN
1. Tujuan umum:
Mengetahui dan menganalisis peran vitamin C terhadap sel inflamasi dan
tingkat obstruksi penderita asma terkontrol sebagian dan tidak terkontrol.
2. Tujuan khusus:
2.1. Mengetahui dan menganalisis perbedaan jumlah eosinofil dan
commit to user
7
2.2. Mengetahui dan menganalisis perbedaan nilai VEP1 pasien asma
terkontrol sebagian akibat pemberian vitamin C.
2.3. Mengetahui dan menganalisis perbedaan jumlah eosinofil,
neutrofil sputum pasien asma tidak terkontrol akibat pemberian
vitamin C.
2.4. Mengetahui dan menganalis perbedaan nilai VEP1 pasien asma
tidak terkontrol akibat pemberian vitamin C.
D. MANFAAT PENELITIAN
1. Manfaat keilmuan
Membuktikan peran vitamin C untuk memperbaiki kondisi stres oksidatif
dalam saluran napas penderita asma terkontrol sebagian dan tidak
ter-kontrol.
2. Manfaat praktis
Perbaikan hasil pemeriksaan eosinofil, neutrofil sputum, dan VEP1 akibat
pemberian vitamin C menjadi dasar pertimbangan terapi tambahan pada
penderita asma terkontrol sebagian dan tidak terkontrol.
3. Manfaat untuk program Magister Kedokteran Keluarga
Perwujudan salah satu Tridharma Perguruan Tinggi yaitu penelitian
khususnya dibidang kedokteran. Hasil penelitian dapat dipakai acuan
jawaban permasalahan ilmiah, pengembangan penelitian lebih lanjut serta
sebagai acuan penanganan klinis pada praktik pelayanan kesehatan dokter
commit to user
8
BAB II. TINJAUAN PUSTAKA
A. ASMA
Asma merupakan penyakit saluran napas kronik yang menjadi masalah
kesehatan masyarakat yang serius di berbagai negara di seluruh dunia. Tingkat
keparahan asma bervariasi mulai ringan dan tidak mengganggu aktivitas
sampai yang berat/ menetap dan mengganggu aktivitas bahkan kegiatan harian.
Asma juga dapat menyebabkan kecacatan serta menurunankan produktivitas
dan kualitas hidup (PDPI 2004).
1. Definisi Asma
Asma adalah gangguan inflamasi kronik saluran napas yang
me-libatkan banyak sel dan elemennya. Inflamasi kronik menyebabkan
peningkatan hiper-responsif saluran napas yang menimbulkan gejala
episodik berulang berupa mengi, sesak napas, dada terasa berat dan
batuk-batuk terutama malam dan atau dini hari. Episodik tersebut berhubungan
dengan obstruksi jalan napas yang luas, bervariasi dan seringkali bersifat
reversibel dengan atau tanpa pengobatan (PDPI 2004).
Inflamasi saluran napas pada asma merupakan proses yang sangat
kompleks, melibatkan faktor genetik, antigen, berbagai sel inflamasi,
interaksi antar sel dan mediator yang membentuk proses inflamasi kronik
dan remodeling (Rahmawati et al. 2003). Faktor lingkungan dan genetik
masing-masing meningkatkan risiko penyakit asma. Pajanan lingkungan
meningkatkan risiko asma pada individu yang mempunyai predisposisi
commit to user
9
ditandai dengan peningkatan eosinofil, sel mast, makrofag serta limfosit-T
di lumen dan mukosa saluran napas. Proses ini dapat terjadi pada asma
yang asimptomatik dan bertambah berat sesuai dengan berat klinis
penyakit (Rahmawati et al. 2003).
2. Tingkat Kontrol Asma
Tingkat kontrol asma adalah manifestasi perubahan berupa berkurang
atau hilangnya gejala dan tanda asma setelah mendapat terapi (Taylor et al.
2008). Penatalaksanaan asma ditujukan untuk mencapai kontrol optimal
yaitu meminimalisasi gejala dan penggunaan agonis 2 kerja singkat,
mencegah bronkokonstriksi sehingga mengurangi risiko eksaserbasi yang
mengancam jiwa dan kematian (Juniper et al. 1999). Pemakaian
anti-inflamasi seperti steroid inhalasi dapat meredakan gejala asma dengan
cepat, walaupun efeknya relatif kecil dalam mengurangi hiperreaktivitas
bronkus (Barnes 1993).
Global Initiative for Asthma (GINA) membagi tingkat kontrol asma
berdasarkan kriteria sebagai berikut (NHLBI 2009):
Asma terkontrol :
Didapatkan seluruh kriteria berikut :
Gejala harian asma tidak ada atau kurang dua kali / minggu.
Keterbatasan aktivitas tidak ada.
Gejala malam tidak ada.
Kebutuhan obat pelega tidak ada atau kurang dua kali / minggu.
commit to user
10
Asma terkontrol sebagian :
Dalam kurun waktu
Gejala harian asma > 2 kali / minggu.
Keterbatasan aktivitas ada.
Gejala malam ada.
Kebutuhan obat pelega > 2 kali / minggu.
Volume ekspirasi paksa detik pertama (VEP1) < 80% prediksi atau
nilai terbaik.
Asma tidak terkontrol :
Dalam beberapa minggu didapatkan 3 atau lebih kriteria asma terkontrol
sebagian.
3. Sel Inflamasi Pada Asma
Elemen selular berperan pada inflamasi kronik saluran napas pasien
asma. Sel mast, eosinofil, limfosit T, makrofag, neutrofil, sel dendritik,
dan sel epitel merupakan sel yang banyak terlibat pada patogenesis asma
(PDPI 2004, NHLBI 2009). Sel-sel penyusun struktur saluran napas yang
lain (sel fibroblas dan sel otot polos juga berperan terhadap kelangsungan
inflamasi dan cedera jaringan (Jarjour dan Kelly 2002). Uraian singkat
peran elemen selular dijelaskan sebagai berikut:
a. Sel mast
Sel mast berperan kunci pada respon awal alergi , biasanya mulai
commit to user
11
Kelly 2002). Sel mast beredar di sirkulasi sebagai sel mononuklear
cluster of differentiation (CD)-34, kemudian bermigrasi ke mukosa dan
sub-mukosa saluran napas serta mengalami maturasi spesifik di
jaringan. Sel mast menghasilkan berbagai sitokin diantaranya adalah
IL-1, IL-2, IL-3, IL-4, IL-5, granulocyte macrophage colony
stimulating factor (GM-CSF), interferon gamma (IFN- tumor
necrosis factor (TNF)- . Sel mast diketahui berperan pada proses
remodeling, diferensiasi, pro-liferasi, adhesi dan motilitas sel-sel
radang, serta morfogenesis jaringan saluran napas. (PDPI 2004,
Boushey et al. 2005, Mangatas et al. 2006). Kemokin yang dihasilkan
sel mast antara lain macrophage inflammatory protein (MIP)-1a,
MIP-1b, monocyte chemoattractant protein (MCP), dan regulated on
activation normal T cell expressed and secreted (RANTES) (Jarjour
dan Kelly 2002).
b. Sel limfosit T
Limfosit T yang berperan pada asma ialah limfosit T-CD4+ subtipe
Th2. Limfosit T ini berfungsi sebagai orkestra inflamasi saluran napas
dengan mengeluarkan berbagai sitokin (PDPI 2004). Sitokin yang
dihasilkan diantaranya adalah IL-4, IL-5, IL-9, dan IL-1. Melalui
sitokin tersebut, sel Th2 berperan dalam rekrutmen dan aktivasi
eosinofil, produksi IgE, sekresi mukus, serta meningkatkan ekspresi
molekul adhesi seperti vascular cell adhesion molecule (VCAM)-1
commit to user
12
Interleukin-4 berperan dalam menginduksi Th0 ke arah Th2 dan
bersama-sama IL-13 menginduksi sel limfosit B mensintesis
imunoglobulin (Ig)E, IL-3, IL-5 serta GM-CSF berperan pada
maturasi, aktivasi serta memperpanjang ketahanan hidup eosinofil
(Jarjour dan Kelly 2002).
Sel T yang belum terpajan dengan antigen disebut sel T naif atau
Th0. Pajanan antigen menyebabkan sel T naif membentuk ikatan
dengan major histo-compatibility complex (MHC) dan dipresentasikan
oleh antigen-precenting cells (APC) atau rangsangan sitokin spesifik
yang berkembang menjadi subset sel T-CD4+ dan CD8+. Sel T CD4+
dipengaruhi sitokin IL-4, IL-5, IL-10, dan IL-13 yang dilepas sel mast
berkembang menjadi sel Th2 yang merangsang sel B untuk
meningkatkan produksi antibodi (Baratawidjaja 2006).
c. Makrofag
Makrofag merupakan anggota famili leukosit mononuklear,
didistribusikan secara luas hampir ke seluruh jaringan. Fenotif
makrofag sangat bervariasi tergantung pada lingkungan mikro lokal.
Makrofag memainkan peran penting untuk memperkuat respons
inflamasi dengan cara stimulasi sitokin pada sel yang tidak merespon
bakteri atau produk bakteri. Sel fagosit mononuklear, neutrofil dan sel
endotel menghasilkan kemokin CXC saat merespons
lipopoly-saccharide (LPS). Makrofag alveolar secara aktif menghambat
commit to user
13
mikro sehingga hambatan makrofag terhadap proliferasi sel T akan
berkurang setelah pajanan alergen (Toews 2009).
Alergen mengaktivasi sel monosit akan berubah menjadi
makro-fag. Makrofag melepaskan berbagai mediator antara lain leukotrien
B4 (LTB4), prostaglandin F2 (PGF2), platelet activating factor
(PAF), IL-1, IL-8, IL-10, GM-CSF, dan TNF- Sel ini juga
melepaskan platelet derived growth factors (PDGF), basic fibroblast
growth factor -FGF), dan transforming growth factor (TGF)- yang
berperan pada proses remodeling saluran napas (Rahmawati et al.
2003, PDPI 2004, Mangatas et al. 2006).
d. Neutrofil
Neutrofil merupakan jenis sel paling banyak dalam sputum
orang sehat dan penderita asma. Jumlah neutrofil tidak meningkat
pada sekresi saluran napas pasien asma ringan dan sedang, tetapi
meningkat lebih tinggi dari normal pada asma berat (Fahyi 2009).
Neutrofil berperan dalam patogenesis asma akut maupun kronik
melalui produksi berbagai sitokin dan kemokin seperti 1, 3,
IL-6, IL-8, IL-12, TNF- , IFN- , GMCSF, MIP, dan TGF- Monteseirin
2009). Mediator yang berhubungan dengan reaksi asma fase cepat
diantaranya: matrix metalloproteinase (MMP)-9, elastase, laktoferin,
myeloperoxidase (MPO), molekul adhesi, thromboxane A2 (TXA2)
sedangkan mediator yang terlibat dalam reaksi asma fase lambat
commit to user
14
neutrofil atas pengaruh IL-8. Terdapat peningkatan kadar MMP-9
teraktivasi pada cairan BAL penderita asma. Penelitian terhadap
pajanan alergen spesifik menunjukkan adanya korelasi antara kadar
MMP-9, perubahan nilai VEP1, dan kadar neutrofil sputum. Produksi
elastase oleh neutrofil pada asma melalui mekanisme IgE dependent.
Elastase terlibat dalam patofisiologi asma diantaranya mengakibatkan
cedera epitel, meningkatkan permeabilitas vaskular, hipersekresi
mukus, metaplasi kelenjar mukus, bronkokonstriksi, dan
hiper-reaktivitas bronkus. Eosinophil cationic protein disekresi oleh
neutrofil akibat stimuli oleh alergen atau antibodi anti-IgE. Eosinophil
cationic protein (ECP) terlibat dalam patofisiologi asma dengan
merangsang pelepasan histamin dan laktoferin oleh basofil yang
mengakibatkan hipersekresi mukus (Monteseirin 2009).
e. Sel dendritik
Fungsi utama sel dendritik adalah sebagai antigen presenting cell
(APC) yang menyajikan antigen ke sel T. Sel ini mempunyai potensi
terbesar menginisisasi dan mempertahanakan inflamasi dalam saluran
napas. Sel dendritik ditemukan di dalam dan dibawah lapisan epitel,
sehingga sangat ideal untuk menangkap, memproses kemudian
mem-presentasikan antigen. Sel ini berasal dari sel sumsum tulang atau dari
prekursor monosit dalam darah dan hanya bertahan hidup selama
commit to user
15
Sel dendritik juga mensekresi beberapa mediator inflamasi
diantaranya IL-12, PGE2, dan IL-10. Mediator ini akan memicu
perkembangan dan diferensiasi sel T (Boushey 2005). Sel dendritik
berasal dari sel progenitor di sumsum tulang dan sel di bawah epitel
saluran napas. Sel dendritik akan bermigrasi ke jaringan limfe lokal di
bawah pengaruh GMCSF (Rahmawati et al. 2003).
f. Basofil
Sel basofil berasal dari sel CD 34+ di sumsum tulang, yang
ber-deferensiasi dan matur di sumsum tulang kemudian masuk sirkulasi
darah serta mempunyai reseptor IgE afinitas tinggi yaitu Fc RI seperti
sel mast. Sel basofil merupakan efektor dari respons imun yang
diperantarai IgE, termasuk asma dan penyakit alergi yang lain
(Arinobu et al. 2009). Sel ini mampu melepaskan histamin dan LTB4,
sehingga diduga berperan dalam patogenesis asma. Didapatkan sedikit
peningkatan basofil pada saluran napas penderita asma setelah pajanan
alergen (PDPI 2004, Rahmawati et al. 2003).
g. Eosinofil
Eosinofil berasal dari progenitor sel pluripoten CD34+ yang
mengalami diferensiasi dan maturasi di sumsum tulang, akibat
pengaruh IL-3, IL-5, dan GM-CSF (Filipofic dan Cekic 2001).
Eosinofil meninggalkan sumsum setelah matur menuju sirkulasi
darah selanjutnya ke jaringan dan bertahan hidup selama 4-10 hari
commit to user
16
Eosinofil mengandung granula yang memproduksi mediator
inflamasi toksik dan disintesis setelah terjadi interaksi aktivasi sel.
Granula tersebut mengandung inti kristaloid yang terdiri dari major
basic protein (MBP), eosinophil cationic protein (ECP), eosinophil
derived neurotoxin (EDN), dan eosinophil peroxidase (EPO). Major
basic protein (MBP) dapat menyebabkan kerusakan saluran napas dan
berperan pada hiperresponsivitas saluran napas. Eosinofil juga
memproduksi leukotrien, sitokin, matriks metaloproteinase, dan
reaktif oksigen spesies yang berperan pada obstruksi dan cedera
saluran napas (Jarjour dan Kelly 2002).
Jumlah eosinofil dalam darah bisa digunakan sebagai marker
inflamasi secara tidak langsung pada saluran napas penderita asma.
Jumlah eosinofil mencerminkan aktivitas asma, dapat digunakan
untuk menentukan dosis steroid dan deteksi dini eksaserbasi (Filipofic
dan Cekic 2001, Surjanto 2005). Peningkatan jumlah eosinofil dalam
darah perifer dan hasil sekresi saluran napas merupakan gambaran
khas pada asma dan berhubungan dengan derajat keparahan asma.
Kelompok asma eosinofilia menunjukkan subepithelial basement
membrane lebih tebal dibanding noneosinofilia (Mitchell 2009).
h. Sel epitel dan fibroblas
Sel epitel dan fibroblas merupakan sel penyusun struktur saluran
napas. Sel tersebut juga berperan pada inflamasi dan cedera saluran
commit to user
17
protein (elastin, fibronektin, laminin, dan kolagen) (Jarjour dan Kelly
2002). Miofibroblas menyebabkan penebalan membran basal retikuler
(PDPI 2004, Barnes dan Rennard 2002).
i. Sitokin
Sitokin yang terlibat dalam proses inflamasi saluran napas pada
asma meliputi:
Interleukin-4
Interleukin-4 terutama dihasilkan oleh Th2, sel mast,
basofil, dan eosinofil. Sintesis IL-4 diinduksi oleh stimulasi
reseptor antigen dalam sel T. Peran IL-4 berhubungan dengan
aktivasi limfosit B dengan jalan meningkatkan ekspresi molekul
MHC kelas II, CD-23, reseptor Fc RI CD-40 dan reseptor IL-2.
Sitokin ini mampu meningkatkan sintesis IgE dan IgG4 oleh sel B
(Chung dan Barnes 1999). Stimuli IL-4 terhadap IgE akan
mengaktivasi sel mast yang berperan penting dalam
per-kembangan reaksi alergi tipe cepat. Interleukin-4 juga dapat
menyebabkan obstruksi saluran napas melalui induksi gen musin
dan hipersekresi mukus. Ekspresi eotaksin dan sitokin inflamasi
dari fibroblas yang lain juga ditingkatkan oleh IL-4 sehingga akan
menyebabkan inflamasi dan remodeling saluran napas (John et al.
1999). Efek IL-4 di sisi lain juga menghambat biosintesis
metalloproteinase oleh makrofag alveolar, menghambat sintesis
commit to user
18
dan IL l-8 pada sel otot polos saluran napas (Chung dan Barnes
1999).
Vascular cell adhesion molecule-1 (VCAM-1) pada endotel
juga distimuli oleh IL-4, sehingga dapat meningkatkan inflamasi
pada pasien asma (John dan Larry 2001). Interaksi VCAM-1
dengan IL-4 secara langsung menyebabkan migrasi limfosit T,
monosit, basofil, dan eosinofil ke daerah inflamasi (Moser et al.
1992). Aktivitas biologis IL-4 dapat mengendalikan diferensiasi
sel limfosit Th0 menjadi Th2, yang bisa mensekresikan IL-4, IL-5,
IL-9, dan IL-13 (Scott et al. 2001). Ekspresi IL-4 pada CD4+,
CD8+, eosinofil, dan sel mast penderita asma atopi maupun
nonatopi meningkat. Terdapat bukti peningkatan jumlah limfosit
yang mengekspresikan IL-4 dan IL-5 secara bersama-sama pada
cairan BAL setelah pajanan alergen (Chung dan Barnes 1999).
Interleukin-5
Interleukin-5 diproduksi oleh limfosit T dan peningkatan
ekspresi IL-5 mRNA ditunjukkan pada sel CD4+ saluran napas
pasien asma. Sel CD8+ dan eosinofil diduga juga dapat
mensekresi IL-5. Sitokin ini berperan pada produksi, maturasi,
aktivasi dan menjaga kelangsungan hidup eosinofil. Interleukin-5
merupakan sitokin utama yang mengaktifkan eosinofil pada
commit to user
19
eksogen terbukti menyebabkan eosinofilia pada model percobaan
invivo (Chung dan Barnes 1999).
Interleukin-5 berperan penting dalam recruitment eosinofil
dari darah ke jaringan, serta memicu aktivasi eosinofil jaringan
yang mengalami inflamasi (Scott et al. 2001). Sitokin ini juga
berfunsi sebagai kemoatraktan dan terlibat dalam peningkatan
hiperresponsivitas saluran napas. Peningkatan ekspresi IL-5
dalam sel dan jaringan penderita asma mendukung keterlibatan
sitokin ini dalam patogenesis asma (Chung dan Barnes 1999).
Interleukin-9
Interleukin-9 dihasilkan oleh Th2 dan sebelumnya
di-identifikasi sebagai faktor pertumbuhan sel T. Interleukin-9
merangsang proliferasi sel T yang telah teraktivasi, meningkatkan
produksi IgE dari sel B, merangsang proliferasi dan diferensiasi
sel mast dari haematopoietic progenitor (Chung dan Barnes
1999). Sitokin ini juga berperan dalam hiperplasia sel goblet dan
perkembangan sel mast (Yuhong et al. 2001). Pada percobaan
hewan peningkatan ekspresi IL-9 berhubungan dengan infiltrasi
eosinofil dan limfosit yang masif serta peningkatan jumlah sel
mast pada saluran napas. Percobaan yang lain menunjukkan
terjadi peningkatan hiperresponsivitas saluran napas tanpa terjadi
commit to user
20 Interleukin-13
Interleukin-13 disintesis oleh sel T CD4+ dan CD8+ yang
teraktivasi, akibat respon terhadap rangsang antigen spesifik.
Aktivitas biologis dan struktur reseptor IL-13 mirip dengan IL-4
(Chung dan Barnes 1999). Peran IL-13 pada asma overlap dengan
IL-14 diantaranya merangsang sel B untuk mensintesis Ig E,
mengatur ekspresi reseptor Ig E, mengatur peningkatan ekspresi
VCAM-1 meningkatkan survival eosinofil, kemotaksis dan
aktivasi fibroblas, serta merangsang produksi mukus (Humbert et
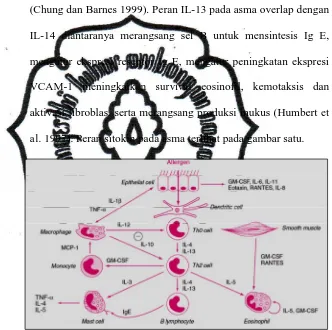
al. 1997). Peran sitokin pada asma terlihat pada gambar satu.
[image:39.595.168.500.233.563.2]
Gambar 1. Sitokin yang terlibat dalam patogenesis asma. Berbagai sitokin dikeluarkan oleh sel inflamasi dan sel pembentuk struktur saluran napas, membentuk suatu orkestra inflamasi.
commit to user
21
4. Patogenesis Asma
Asma merupakan penyakit inflamasi kronik saluran napas yang
melibatkan beberapa sel, menyebabkan pelepasan mediator yang dapat
mengaktivasi sel target saluran napas sehingga terjadi bronkokonstriksi,
kebocoran mikrovaskular, edema, hipersekresi mukus dan stimulasi
refleks saraf (Barnes dan Rennard 2002).
Asma berhubungan dengan peningkatan kepekaan saluran napas
sehingga memicu episode mengi berulang, sesak napas dan batuk
terutama pada malam atau dini hari. Gejala ini berhubungan dengan luas
inflamasi, menyebabkan obstruksi saluran napas yang bervariasi
derajatnya dan bersifat reversible secara spontan maupun dengan
pengobatan (Barnes dan Rennard 2002)
Proses inflamasi pada asma khas ditandai dengan peningkatan
eosinofil, sel mast, makrofag serta limfosit-T di lumen dan mukosa
saluran napas. Proses ini mulai terjadi pada asma yang asimptomatik dan
bertambah berat sesuai dengan berat klinis penyakit (Bousquet et al.
2000). Sel inflamasi yang terlibat dalam asma adalah sel limfosit,
eosinofil, basofil, neutrofil, makrofag, dan sel mast. Limfosit yang
berperan pada asma adalah limfosit T-CD4+ subtipe Th2. Limfosit ini
mengeluarkan sitokin antara lain IL-3, IL-4, IL-5, IL-13 dan GM-CSF.
Interleukin-5 dan GM-CSF memicu pembentukan eosinofil di sumsum
tulang. Neutrofil berperan sebagai efektor reaksi inflamasi melalui fungsi
commit to user
22
Neutrofil juga menghasilkan sitokin dan kemokin seperti IL- -6,
IL-8, dan
TNF-membuat dan mensekresi activator plasminogen dan metalloproteinase
yang dapat merusak komponen matriks ekstraseluler saluran napas
(Mangatas et al. 2006). Inflamasi terdapat pada semua derajat asma
(asma intermiten maupun asma persisten) serta ditemukan pada berbagai
bentuk asma (asma alergi, non alergi, asma kerja, dan asma yang
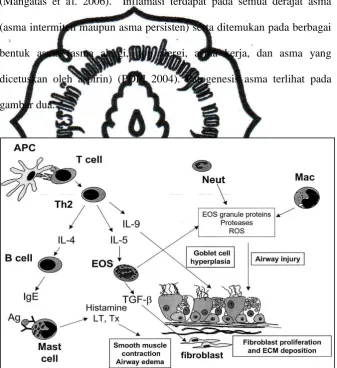
[image:41.595.165.503.241.610.2]dicetuskan oleh aspirin) (PDPI 2004). Patogenesis asma terlihat pada
gambar dua.
Gambar 2. Patogenesis asma.
Dikutip dari (Jarjour dan Kelly 2002)
Ekspresi protein inflamasi (sitokin, enzim, reseptor, molekul
adhesi) secara bersamaan berpengaruh terhadap proses inflamasi pada
commit to user
23
meningkatkan transkripsi gen target. Nuclear factor-
(NF-merupakan salah satu faktor transkripsi yang memainkan peran penting
dalam asma. Faktor transkripsi ini diaktivasi oleh banyak rangsangan
termasuk aktivator protein C kinase, oksidan, dan sitokin proinflamasi
(seperti IL- - dan Rennard 2002).
5. Peran Stres Oksidatif Pada Patogenesis Asma
Stres oksidatif terjadi karena peningkatan produksi oksidan atau
ber-kurangnya produksi antioksidan sehingga mengakibatkan gangguan
kese-timbangan antara oksidan dan antioksidan. Peningkatan produksi oksidan
diantaranya disebabkan inflamasi pada saluran napas pasien asma. Sel
makrofag saluran napas pasien asma menghasilkan kadar superoksida
lebih tinggi dibanding subyek normal. Polusi udara juga merangsang
peningkatan oksidan eksogen yang berpengaruh terhadap insidensi asma.
Pengurangan produksi antioksidan pada asma disebabakan oleh beberapa
gangguan yang mekanismenya sudah diketahui yaitu berkurangnya kadar
selenium (elemen penting aktivitas aktivasi glutathione peroxidase), serta
berkurangnya aktivitas tembaga dan seng yang mengandung superoxide
dismutase (Cu, Zn-SOD) pada sel epitel bronkus dan cairan BAL.
Terdapat bukti adanya polimorfisme genetik pada antioksidan enzimatik
Mn-SOD dan glutathione S-transferase pada penderita asma (Dworski
2000). Penelitian pada model hewan coba asma menunjukkan adanya
penurunan kadar nuclear factor like 2 (Nrf2) dan peroksiredoksin
commit to user
24
aktivitas pertahanan antioksidan intraselular berpengaruh terhadap
perkembangan asma (Cho dan Moon 2010). Kehilangan kontrol oksidan
di saluran napas dapat menimbulkan inisiasi sel Th2 yang merupakan fase
awal perkembangan inflamasi alergi dalam saluran napas. Peningkatan
kadar ROS dalam APC mempengaruhi sistem imunitas akibat respon Th2
(Peterson et al. 1998). Kondisi stres oksidatif menyebabkan gangguan
maturasi sel dendritik ditandai penurunan sekresi IL-12 dan IFN- yang
berdampak down regulation terhadap Th1 (Kim et al. 2007, Kroening et
al. 2010). Pajanan oksidan terhadap sel dendritik terbukti meningkatkan
produksi IL-4, IL-8 dan
TNF-(Verhasselt et al. 1998). Sel makrofag yang mengalami stres oksidatif
akan mengalami peningkatan produksi IL-6 dan IL-10 dan akan
mendeferensiasi Th0 ke arah respons Th2 (Murata et al. 2002).
Peningkatan stres oksidatif juga berkontribusi pada perkembangan atau
kelangsungan inflamasi saluran napas, menimbulkan peningkatan
hiperresponsivitas saluran napas, stimulasi sekresi mukus, dan induksi
berbagai mediator kimia proinflamasi. Semua hal tersebut diatas terkait
dengan tingkat keparahan asma (Fitzpatrick et al. 2009).
Sel makrofag saluran napas pasien asma menghasilkan kadar
superoksida lebih tinggi dibanding subyek normal. Pajanan antigen juga
terbukti meningkatkan kadar ROS saluran napas. Sel inflamasi pada
sirkulasi diduga juga menjadi sumber stres oksidatif. Monosit darah
commit to user
25
mensekresi superoksida. Isolasi eosinofil dari pasien asma setelah
pajanan antigen selama 24 jam menghasilkan kadar hidrogen peroksida
lebih tinggi. Eosinofil dan monosit darah pasien asma terbukti juga
mengandung kadar ROS lebih tinggi dibandingkan dengan subyek
normal. Data tersebut di atas menunjukkan bahwa sel-sel inflamasi
saluran napas maupun intravaskular berkontribusi pada peningkatan
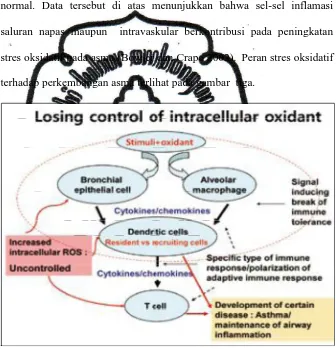
stres oksidatif pada asma (Bowler dan Crapo 2002). Peran stres oksidatif
[image:44.595.164.500.237.587.2]terhadap perkembangan asma terlihat pada gambar tiga.
Gambar 3. Peran stres oksidatif pada asma.
Dikutip dari (Cho dan Moon 2010)
Sebagian besar bukti epidemiologis dan klinis mendukung adanya
hubungan antara peningkatan ROS dan patogenesis asma bronkial.
Molekul yang terlibat dalam stres oksidatif lebih banyak ditemukan dari
commit to user
26
kontrol subyek normal. Insidensi pasien asma juga dilaporkan lebih
tinggi di daerah dengan polusi udara, menunjukkan adanya pengaruh
rangsang oksidan eksogen terhadap asma (Cho dan Moon 2010).
Kenaikan ROS pada asma terkait dengan kerusakan berbagai molekul
biologis di paru. Peningkatan nitrotyrosine dan chlorotyrosine pada
sampel cairan BAL menunjukkan adanya kerusakan protein, yang
berhubungan dengan penurunan aktivitas 1 protease inhibitor (Bowler
dan Crapo 2002).
6. Patologi Asma
Inflamasi saluran napas pada asma melibatkan interaksi berbagai sel
dan mediator berperan sentral pada patologi asma (Barnes dan Rennard
2002). Mediator inflamasi dan protein hasil sekresi sel-sel inflamasi
berperan terhadap perubahan struktur dan fungsi saluran napas. Proses
inflamasi kronik tersebut akan mengakibatkan perubahan struktur berupa
peningkatan epitel, hiperplasia sel goblet, peningkatan jumlah pembuluh
darah, peningkatan dan perubahan matriks ekstraselular (extra-cellular
matrix / ECM) serta pe-ningkatan massa otot polos saluran napas (airway
smooth muscle / ASM) (Postma dan Timens 2006).
Analisis patologi penderita asma berat menunjukkan terjadi
peningkatan sebagian besar unsur dinding saluran napas (otot polos,
jaringan ikat, dan kelenjar mukus). Peningkatan ini terjadi pada saluran
napas semua ukuran kecuali kelenjar mukus. Perubahan patologis saluran
commit to user
27
di saluran napas kecil dengan diameter 2-4 mm. Ketebalan dinding
saluran napas juga berhubungan dengan derajat keparahan dan lama
penyakit (Homer dan Elias 2005).
Penyebab terpenting penebalan saluran napas adalah peningkatan
massa otot polos karena hipertrofi dan hiperplasia (Larsson 2010).
Penebalan lapisan kolagen saluran napas penderita asma juga menonjol.
Tebal lapisan kolagen saluran napas normal sekitar 5 m. Tebal lapisan
kolagen pasien asma meningkat menjadi 20 m (Larsson 2010).
Penebalan ini semula hanya digambarkan sebagai penebalan basement
membrane. Kelainan juga terjadi pada matriks nonkolagen termasuk
elastin, proteoglikan, dan kartilago. Fibrosis subepitel memberikan
kontribusi terjadi perubahan distensibilitas saluran napas dan mungkin
berhubungan dengan hiperesponsif saluran napas pada asma. Fibrosis
subepitel merupakan tanda sangat dini fenotipe asma pada anak-anak dan
tidak berkorelasi dengan lama waktu atau tingkat keparahan inflamasi
(Homer dan Elias 2005).
Peningkatan vaskularisasi juga memberikan kontribusi terhadap
penebalan dinding saluran napas pada asma dan berhubungan dengan
keparahan penyakit. Angiogenesis merupakan gambaran khas asma berat
tetapi juga muncul pada beberapa kasus asma ringan (Larsson 2010).
Penderita asma berat memiliki jumlah pembuluh darah mukosa saluran
napas lebih banyak dibanding penderita asma ringan. Peningkatan
commit to user
28
epitel saluran napas. Dinding pembuluh kapiler dan venula penderita
asma terjadi edema dan penebalan subendothelial basement membrane,
hipotrofi atau atrofi miosit serta fibrosis arteriol. Pembuluh darah
penderita asma menunjukkan recruitment eosinofil, aktivasi, dan lisis
intravaskular (Homer dan Elias 2005).
Dilatasi, kongesti, dan edema dinding pembuluh darah mukosa
bronkus merupakan gambaran yang muncul konsisten pada asma berat
dan dapat menjelaskan penyebab penebalan dan kekakuan dinding
saluran napas (Larsson 2010).
7. Patofisiologi Asma
Respons inflamasi kronik pada asma mendasari kelainan faal paru.
Kelainan faal paru tersebut akibat kerusakan epitel saluran napas, fibrosis
subepitel saluran napas, hiperplasia dan hipertrofi saluran napas,
vasodilatasi pembuluh darah, kebocoran plasma, hipersekresi mukus,
serta aktivasi saraf sensorik (Barnes dan Rennard 2002). Perubahan faal
paru pada asma diantaranya adalah:
a. Obstruksi saluran napas
Obstruksi saluran napas pada asma bersifat difus dan derajatnya
ber-variasi, dapat membaik dengan atau tanpa pengobatan. Penyebab
utama obstruksi adalah kontraksi otot polos bronkus yang diprovokasi
oleh mediator yang dilepaskan sel inflamasi (Rahmawati et al. 2003).
Fibrosis subepitel saluran napas dengan penimbunan kolagen
commit to user
29
yang terdapat pada penderita asma. Peningkatan aliran darah mukosa
saluran napas menyebabkan peningkatan volume pembuluh darah
diduga juga berperan terhadap penyempitan saluran napas yang
mengakibatkan obstuksi. Peningkatan produksi mukus berperan dalam
peningkatan viskositas mucus plugs yang dapat menyebabkan oklusi
saluran napas penderita asma (Barnes dan Rennard 2002).
b. Hiperesponsivitas saluran napas
Mekanisme hiperresponsivitas saluran napas belum diketahui
secara pasti. Salah satu penyebabnya diduga karena perubahan sifat
otot polos saluran napas sekunder terhadap perubahan fenotip
kontraktilitas. Inflamasi dinding saluran napas terutama di daerah
peribronkial dapat menambah penyempitan saluran napas selama
kontraksi otot polos. Hiperesponsivitas saluran napas dapat diukur
dengan uji provokasi bronkus. Pada penderita asma terjadi
peningkatan pemendekan otot polos bronkus saat kontraksi isotonik.
Perubahan fungsi kontraksi mungkin disebabkan oleh perubahan
aparatus kontraksi (Rahmawati et al. 2003). Kerusakan epitel saluran
napas diduga penting dalam kontribusi terjadinya hiperesponsivitas
saluran napas. Kerusakan epitel dapat terjadi melalui beberapa
mekanisme yaitu: kehilangan fungsi pertahanan untuk melawan
masuknya alergen, kehilangan enzim (neural peptidase) yang secara
normal menurunkan mediator inflamasi, kehilangan faktor relaksasi,
commit to user
30
juga berperan dalam hiperresponsivitas saluran napas pada penderita
asma (Barnes dan Rennard 2002).
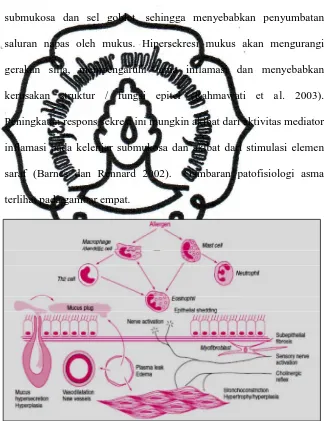
c. Hipersekresi mukus
Saluran napas penderita asma terjadi hiperplasia kelenjar
submukosa dan sel goblet, sehingga menyebabkan penyumbatan
saluran napas oleh mukus. Hipersekresi mukus akan mengurangi
gerakan silia, mempengaruhi lama inflamasi dan menyebabkan
kerusakan struktur / fungsi epitel (Rahmawati et al. 2003).
Peningkatan respons sekresi ini mungkin akibat dari aktivitas mediator
inflamasi pada kelenjar submukosa dan akibat dari stimulasi elemen
saraf (Barnes dan Rennard 2002). Gambaran patofisiologi asma
terlihat pada gambar empat.
[image:49.595.173.499.234.655.2]
Gambar 4. Patofisiologi asma.
commit to user
31
8. Peran Stres Oksidatif Pada Patofisiologi Asma
Stres oksidatif berperan pada peningkatan dan kelangsungan inflamasi
saluran napas berdampak pada peningkatan hiperresponsivitas saluran
napas, merangsang sekresi mukus, dan menginduksi mediator
proinflamasi, yang semua terkait dengan derajat keparahan asma
(Fitzpatrick et al. 2009). Peningkatan produksi ROS berkorelasi
ter-balik dengan FEV1 (Bowler dan Crapo 2002). Kekurangan
asup-an makasup-anasup-an yang mengandung antioksidan juga terkait dengan
peningkatan insiden asma (Grievink et al. 1998). Pajanan polusi udara
juga menyebabkan peningkatan keparahan dan frekuensi serangan.
Peningkatan stres oksidatif pada pasien asma juga ber-hubungan dengan
penurunan fungsi paru (Cho dan Moon 2010).
Kadar antioksidan sirkulasi rendah darah atau asupan antioksidan yang
rendah diduga menjadi faktor risiko asma. Reaktif oksigen spesies secara
langsung dapat menimbulkan eksaserbasi melalui efek pada otot polos
saluran napas dan sekresi mukus. Reaktif oksigen spesies juga
menurunkan -adrenergik pada paru, serta meningkatkan kepekaan
kontraksi otot polos saluran napas terhadap induksi asetilkolin. Hidrogen
peroksida mampu mengaktivasi mitogen-activated kinase dalam sel otot
serta me-rangsang kontraksi otot polos saluran napas (Bowler dan Crapo
commit to user
32
9. Peran Steroid Terhadap Tingkat Stres Oksidatif
Glukokortikoid terbukti tidak bisa menghambat pembentukan
oksidan dalam eosinofil pada percobaan invitro, tetapi inhalasi
glukokortikoid mampu menurunkan kadar H2O2 dalam udara ekshalasi
napas pasien asma. Dosis rendah glukokortikoid inhalasi juga mampu