SKRIPSI
EKO JULIANTO
TOKSISITAS AKUT DAN SUBAKUT GRANUL EKSTRAK ETANOL
80% KULIT BATANG CEMPEDAK DENGAN PARAMETER
HISTOPATOLOGI HATI SERTA ENZIM SGOT DAN SGPT PADA
MENCIT
FAKULTAS FARMASI UNIVERSITAS AIRLANGGA
DEPARTEMEN FARMAKOGNOSI & FITOKIMIA
SURABAYA
Lembar Pengesahan
TOKSISITAS AKUT DAN SUBAKUT GRANUL
EKSTRAK ETANOL 80% KULIT BATANG
CEMPEDAK DENGAN PARAMETER
HISTOPATOLOGI HATI SERTA ENZIM SGOT DAN
SGPT PADA MENCIT
SKRIPSI
Dibuat untuk memenuhi syarat
Mencapai gelar sarjana farmasi pada Fakultas Farmasi
Universitas Airlangga
2011
Oleh :
Eko Julianto
NIM : 050710052
Disetujui Oleh :
Pembimbing Utama Pembimbing Serta
LEMBAR PERSETUJUAN
PUBLIKASI KARYA ILMIAH
Demi perkembangan ilmu pengetahuan, saya menyetujui skripsi/karya ilmiah saya, dengan judul: “Toksisitas Akut Dan Subakut Granul Ekstrak
Etanol 80 % Kulit Batang cempedak Dengan Parameter Histopatologi Hati
Serta Enzim SGOT dan SGPT Pada Mencit“ untuk dipublikasikan atau ditampilkan di internet, digital library Perpustakaan Universitas Airlangga atau media lain untuk kepentingan akademik sebatas sesuai dengan Undang-Undang Hak Cipta.
Demikian pernyataan publikasi skripsi/karya ilmiah ini saya buat dengan sebenarnya.
Surabaya, 14 Agustus 2011
LEMBAR PERNYATAAN
Dengan ini saya menyatakan, bahwa sesungguhnya hasil skripsi/tugas akhir ini adalah benar-benar merupakan hasil karya saya sendiri. Apabila di kemudian hari diketahui bahwa skripsi ini menggunakan data fiktif atau merupakan hasil dari plagiarisme, maka saya bersedia menerima sanksi berupa pembatalan kelulusan dan atau pencabutan gelar yang saya peroleh.
Surabaya, 14 Agustus 2011
KATA PENGANTAR
Assalamu’alaikum Wr.Wb
Segala puji dan syukur saya panjatkan kepada Allah SWT, hanya karena rahmat dan ridha-Nya sehingga saya dapat menyelesaikan skripsi saya dengan judul “Toksisitas Akut Dan Subakut Granul Ekstrak Etanol 80 % Kulit
Batang Cempedak Dengan Parameter Histopatologi Hati Serta Enzim SGOT
dan SGPT Pada Mencit“ ini dapat saya selesaikan dengan sebaik – baiknya. Saya juga ingin menyampaikan rasa terima kasih kepada :
1. Dekan Fakultas Farmasi Universitas Airlangga Surabaya yang telah memberikan fasilitas selama mengikuti kuliah dan melakukan penelitian ini. 2. Drs. Herra Studiawan, MS, Apt selaku dosen pembimbing utama yang telah
berkenan meluangkan waktu dan tenaganya untuk memberi petunjuk, bimbingan serta dorongan sehingga saya dapat menyelesaikan skripsi ini. 3. Ajik Azmijah ,S.U,drh selaku dosen pembimbing serta yang juga telah
memberikan bimbingan dan masukan sehingga skripsi ini terselesaikan. 4. Dr. Agil Mangestuti, Msi dan Dr. Achmad Fuad.,Apt selaku dosen penguji
yang telah meluangkan waktu dan tenaganya untuk menguji skripsi ini.
5. Dr. Aty Widyawaruyanti, Msi selaku dosen proyek penelitian ini yang telah meluangkan waktu dan tenaga untuk memberikan petunjuk, bimbingan serta dorongan sehingga saya dapat menyelesaikan skripsi ini.
6. Dr. Bambang Prayogo.,Apt sebagai dosen wali yang telah sabar membimbing dan memberikan motivasi selama masa pendidikan sarjana ini.
7. Para dosen Fakultas Farmasi Universitas Airlangga yang telah mendidik dan membimbing saya sampai menyelesaikan pendidikan sarjana ini.
8. Laboran Departemen Farmakognosi dan Fitokimia serta lab.Patologi FKH Unair yang telah membantu dalam penyelesaian skripsi ini.
9. Kedua Orang tuaku serta seluruh keluargaku tercinta yang selalu menyayangi dan mendoakan, memberi bantuan baik moril maupun materiil sehingga skripsi ini dapat terselesaikan.
11.Mbak Lidya,Mbak Anggi,Rori,Dina,Ima,Dewi,Suci,Widji,Prita,Nike yang telah memberi banyak masukan dan motivasi dalam menyelesaikan skripsi ini. 12.Riga Ayu Dinar yang telah menemani dalam suka maupun duka serta memberikan masukan dan memotivasi saya dalam menyelesaikan skripsi ini.
Saya menyadari bahwa penyusunan skripsi ini masih sangat banyak kekurangan, untuk itu saya mengharapkan kritik dan saran dari semua pihak. Semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan dan pembaca pada umumnya demi kemajuan Universitas Airlangga.
Wassalamu’alaikum Wr.Wb
Surabaya, Agustus 2011
RINGKASAN
TOKSISITAS AKUT DAN SUBAKUT GRANUL EKSTRAK ETANOL 80% KULIT BATANG CEMPEDAK DENGAN PARAMETER
HISTOPATOLOGI HATI SERTA ENZIM SGOT DAN SGPT PADA MENCIT
Eko Julianto
Penggunaan tanaman obat sebagai obat alternatif dalam pengobatan oleh masyarakat semakin meningkat sehingga diperlukan penelitian untuk membuktikan khasiat dan keamanan tanaman obat tersebut. Pada penelitian ini dilakukan uji toksisitas akut dan subakut dengan parameter histopatologi hati serta enzim SGOT dan SGPT mencit pada granul ekstrak etanol 80% kulit batang
Artocarpus champeden Spreng atau lebih banyak dikenal dengan nama cempedak.
Uji toksisitas akut dan subakut dilakukan dengan hewan coba mencit. Untuk Uji toksisitas Akut menggunakan mencit sebanyak 20 ekor yang dibagi ke dalam 2 kelompok dimana masing-masing kelompok terdiri dari 10 ekor mencit yaitu masing-masing 5 ekor jantan dan 5 ekor betina . Kelompok kontrol diberikan CMC-Na 0,5%. Kelompok I merupakan kelompok uji yang diberikan granul ekstrak etanol 80% kulit batang cempedak (Artocarpus champeden Spreng) yang diberikan dalam bentuk suspensi CMC-Na 0,5%. Dosis yang diberikan pada kelompok I merupakan dosis tertinggi (dosis LD50 yang relatif tidak berbahaya) yaitu 21 g ekstrak/Kg BB mencit atau 0,42 g / 20 g BB mencit. Pemberian sediaan dilakukan satu kali dengan cara per oral. Kemudian diamati jumlah hewan coba yang mati selama 24 jam setelah pemberian dan dilanjutkan pengamatan selama 7 hari. Hasil uji toksisitas akut pada mencit menunjukkan bahwa pada dosis tersebut tidak menimbulkan kematian pada hewan coba sehingga dapat disimpulkan bahwa semua toksisitas akut yang berbahaya dapat disingkirkan dan LD50 tidak perlu ditentukan.
Parameter yang digunakan pada uji toksisitas subakut adalah aktivitas enzim SGOT, SGPT dan gambaran histopatologi organ hati. Dipilihnya aktivitas enzim SGOT dan SGPT sebagai tolak ukur kemungkinan terjadinya kelainan hati oleh karena peningkatan aktivitas enzim-enzim tersebut merupakan indikator yang kuat dan peka terhadap adanya kelainan sel-sel hati. Parameter lain yang digunakan pada penelitian ini adalah melihat gambaran histopatologi organ hati, karena efek toksik terlihat dari adanya kelainan hati berupa deganerasi dan nekrosis.
coba. Pada akhir masa uji dilakukan pembedahan dan diambil organ hati serta darahnya dari jantung (intra cardial). Kemudian diamati perubahan yang terjadi pada preparat histopatologi yaitu berupa degenerasi dan nekrosis. Perubahan diamati pada lima lapang pandang, diberi skor kemudian diolah datanya.
Data dari enzim SGOT dan SGPT setelah didapat dianalisis menggunakan uji ANAVA pada tingkat kepercayaan 95%. Hasil yang didapat untuk SGPT setelah dianalisis didapatkan harga sig= 0,225. Sig tersebut lebih besar dari 0,05. Sehingga dapat disimpulkan bahwa tidak ada perbedaan bermakna diantara kontrol dengan semua kelompok perlakuan . Sedangkan enzim SGOT setelah dianalisis didapatkan harga sig = 0,978. Sig tersebut lebih besar dari 0,05. Sehingga dapat disimpulkan bahwa tidak ada perbedaan bermakna diantara kontrol dengan semua kelompok perlakuan.
Sedangkan hasil analisis Histopatologi dengan menggunakan uji Kruskal Wallis untuk degenerasi pada perubahan degenerasi didapatkan harga signifikansi (Asymp.Sig.) = 0,000 . Harga signifikansi tersebut lebih kecil dari 0,05. Sehingga dapat disimpulkan bahwa ada perbedaan bermakna diantara semua kelompok uji. Selanjutnya dilanjutkan dengan uji statistik Mann-Whitney U antara kelompok kontrol dengan kelompok 1x dosis efektif ; kontrol dengan 5x dosis efektif ; kontrol dengan 10x dosis efektif, didapatkan hasil adanya perbedaan yang nyata antara kelompok kontrol dengan seluruh kelompok uji. Sedangkan hasil analisis Kruskal Wallis untuk histopatologi hati pada perubahan berupa nekrosis didapatkan harga signifikansi (Asymp.Sig.) = 0,548 signifikansi tersebut lebih besar dari 0,05. Sehingga dapat disimpulkan bahwa ada tidak ada perbedaan bermakna diantara semua kelompok uji. Berdasarkan hasil analisis di atas maka dapat disimpulkan bahwa granul ekstrak etanol 80% kulit batang cempedak (Atrocarpus champeden Spreng) dapat menyebabkan perubahan histopatologi hati berupa degenerasi.
ABSTRACT
The test was about acute toxicity and subacute toxicity effects from granul ethanolic 80% extract of cempedak(Artocarpus champeden Spreng) The effect of its use was observed by SGOT and SGPT enzyme activities and the histopathology of the liver organ of male white mice.
Study of acute toxicity used twenty mice for each extract and for subacute toxicity used thirty six mice and divide into four groups, one as control group with CMC-Na 0,5% and three groups were tested (Group I,Group II and Group III). extract of cempedak (Artocarpus champeden Spreng) orally one ml during a two weeks every day. After a two weeks those mice in eutanasi, be cut opened and then take the liver and blood from intra-cardial.
DAFTAR ISI
BAB II TINJAUAN PUSTAKA………. 6
2.1. Tinjauan tentang Artocarpus champeden Spreng………… 6
2.1.1. Klasifikasi Tanaman………... 6
2.1.2. Nama Daerah Tanaman………... 7
2.1.3. Deskripsi Tanaman………. 7
2.1.4. Kandungan Kimia………... 8
2.1.5. Bioaktivitas dan Kegunaan Tanaman………. 8
2.2. Tinjauan Toksisitas……….. 9
2.2.1. Tujuan Studi Toksisitas………... 9
2.2.2. Macam Studi Toksisitas………. 9
2.2.2.1. Toksisitas Akut……… 9
2.2.2.2. Toksisitas Sub Akut……… 10
2.3. Tinjauan Hati………..……… 11
2.3.1. Anatomi dan Fisiologi Hati……….. 11
2.3.2. Fungsi Hati………... 13
2.3.2.1. Fungsi Vaskular untuk Menyimpan Darah…. 13 2.3.2.2. Fungsi Metabolisme………. 13
2.3.2.3. Fungsi Ekskresi……… 14
2.3.2.4. Fungsi Proteksi……… 14
2.3.2.5. Fungsi Detoksifikasi……… 14
2.3.3. Test Gangguan Hati………. 15
2.3.4. Tinjauan Parameter Kerusakan Hati……… 15
2.4. Tinjauan Enzim………. 18
2.4.1. Sifat Umum Enzim………. 18
2.4.2.1. Kadar Enzim dan Substrat………. 18
2.4.2.2. Suhu……… 19
2.4.2.3. pH……….. 19
2.4.2.4. Inhibitor………. 19
2.4.3. Tinjauan Enzim SGOT dan SGPT……… 19
BAB III KERANGKA KONSEPTUAL………. 22
3.1. Skema Kerangka Penelitian………. 24
BAB IV METODE PENELITIAN……… 25
4.1. Bahan ……….……….. 25
4.1.1. Bahan Kimia………….………... 25
4.1.2. Bahan Larutan Uji Toksisitas………... 4.1.3. Bahan Uji………. 25 25 4.2.Hewan Coba……….. 26
4.3. Alat-Alat Penelitian……….. 4.4. Penyiapan Obyek Penelitian………. 26 26 4.5. Cara Kerja……….. 26
4.5.1. Pemilihan Dosis Uji Toksisitas Akut...……… 26
4.5.2. Pemilihan Dosis Uji Toksisitas Subakut…………... 27
4.5.3. Penyiapan Bahan Uji………. 27
4.5.4. Pengumpulan Data Uji Toksisitas Akut……… 27
4.5.5. Pengumpulan Data Uji Toksisitas Subakut………. 28
4.5.6. Analisis Data Uji Toksisitas Akut…………... 28
4.5.7. Analisis Data Uji Toksisitas Subakut……….. 28
4.5.7.1. Pemeriksaan Preparat………. 28
4.5.7.2. Analisis Data Preparat………. 29
4.5.7.3. Pembuatan Preparat Histopatologi…………. 29
4.5.7.4. Analisis Enzim SGOT dan SGPT………. 30
BAB V HASIL PENELITIAN………... 34
5.1. Data Hasil Penelitian….……….……… 34
5.1.1. Uji Toksisitas Akut…….……… 34
5.1.2. Uji Toksisitas Subakut………. 35 5.1.2.1. Nilai Skor Perubahan Gambar Histopatologi
Hati Pada Mencit………..
5.1.2.2. Hasil Pengamatan Histopatologi Hati Pada
Mencit………...
5.2.3. Aktivitas Enzim SGOT & SGPT Mencit……….
DAFTAR PUSTAKA……… 53
DAFTAR GAMBAR
Halaman
Gambar 2.1. Pohon dan buah cempedak………. 6
Gambar 2.2. Kulit batang pohon cempedak……….... 7
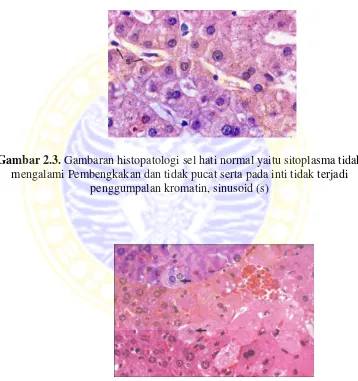
Gambar 2.3. Gambaran histopatologi sel hati normal yaitu sitoplasma tidak mengalami pembengkakan dan tidak pucat serta pada inti tidak terjadi penggumpalan kromatin, sinusoid (s)……….. 17
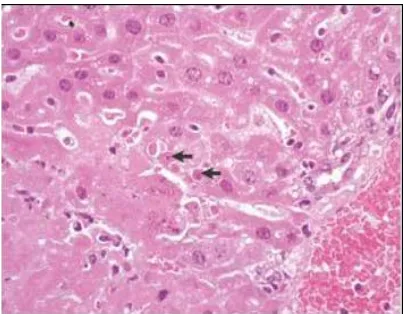
Gambar 2.4. Gambaran histopatologi sel hati yang mengalami degenerasi yaitu terjadinya pembengkakan pada sitoplasma nampak bervakuola dan lebih pucat daripada sel normal ……… 17
Gambar 2.5. Gambaran histopatologi sel hati yang mengalami nekrosis berupa piknotik yaitu terjadinya penggumpalan kromatin, inti tampak lebih padat dan bewarna gelap hitam………... 18
Gambar 2.6. Reaksi penentuan aktivitas enzim SGOT……….. 20
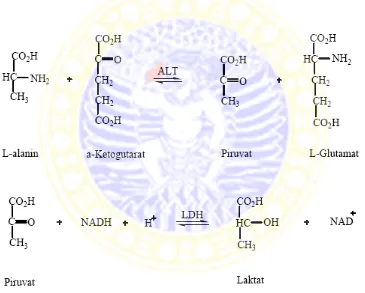
Gambar 2.7. Reaksi penentuan aktivitas enzim SGPT……….. 21
Gambar 3.1. Skema kerangka konseptual……… 24
Gambar 4.1. Skema pemberian bahan uji toksisitas akut………….. 31 Gambar 4.2.
Gambar 5.1. Gambar 5.2.
Gambar 5.3.
Skema pemberian bahan uji toksisitas subakut………
Gambaran histopatologi hati normal pada perbesaran
400x………
Gambaran histopatologi hati pada perbesaran 400x yang terjadi degenerasi yakni terjadi pembengkakan pada sitoplasma, sitoplasma Nampak bervakuola
daripada sel normal……….
Gambaran histopatologi hati pada perbesaran 400x yang terjadi nekrosis berupa piknotik yakni terjadinya penggumpalan kromatin dan tidak dikenali lagi inti (nukleus), inti tampak lebih padat dan berwarna gelap
hitam………...
32 37
37
DAFTAR TABEL
Halaman Tabel II.1.
Tabel IV.1.
Kategori Toksisitas Zat Kimia Pada Tikus………
Formulasi Granul Sediaan Kapsul Ekstrak Kulit Batang
Cempedak………...
Skor Perubahan Gambaran Histopatologi Hati Mencit………….
Hasil Uji Toksisitas Akut pada Mencit………. Nilai Skor Perubahan Histologi Mencit pada Kelompok
Perlakuan yang mengalami perubahan berupa degenerasi………
29
Nilai Skor Perubahan Histologi Mencit pada Kelompok
Perlakuan yang mengalami perubahan berupa nekrosis…………
Aktivitas Enzim SGOT Mencit pada Seluruh Kelompok
Perlakuan………
Aktivitas Enzim SGPT Mencit pada Seluruh Kelompok
Perlakuan………
Harga Rerata Hasil Pengamatan Histopatologi pada Perubahan
berupa Degenerasi………..
Hasil Uji Kruskal-Wallis pada Perubahan berupa Degenerasi….. Harga Rerata Hasil Pengamatan Histopatologi pada Perubahan
berupa Nekrosis………..
Hasil Uji Kruskal-Wallis pada Perubahan berupa Nekrosis…….. Hasil Uji Mann-Whitney U Antara Kontrol dengan Kelompok 1
yang Mengalami Perubahan berupa Degenerasi………
Hasil Uji Mann-Whitney U Antara Kontrol dengan Kelompok 2
yang Mengalami Perubahan berupa Degenerasi………
Hasil Uji Mann-Whitney U Antara Kontrol dengan Kelompok 3
yang Mengalami Perubahan berupa Degenerasi………
Hasil Rerata Aktivitas SGOT Hewan Coba Tiap Kelompok…… Ringkasan ANAVA untuk Aktivitas Enzim SGOT Hewan Coba
Hasil Rerata Aktivitas SGPT Hewan Coba Tiap Kelompok……
DAFTAR LAMPIRAN
Halaman Lampiran 1 Contoh Perhitungan Toksisitas Akut……….. 57 Lampiran 2 Data hasil pemeriksaan SGOT dan SGPT……….
Hasil uji Kruskal-Wallis………. Hasil uji Mann-Whitney U……….
BAB I
PENDAHULUAN
1.1. Latar Belakang
Saat ini, dunia berada dalam iklim back to nature atau dikenal dengan gerakan kembali ke alam yang dalam pelaksanaannya membiasakan hidup dengan menghindari bahan-bahan kimia sintesis dan lebih mengutamakan bahan alami. Semua hal yang serba natural semakin digemari dan dicari orang, salah satunya adalah penggunaan tumbuhan untuk pengobatan (Kardinan & Kusuma, 2003). Para ahli dari berbagai negara seperti Jerman, India, Cina, Australia, Indonesia dan sebagainya, tidak henti-hentinya mengadakan penelitian dan pengujian berbagai tumbuhan yang secara tradisional dipakai untuk penyembuhan penyakit tertentu. Hasil penelitian dan pengujian secara ilmiah tersebut disimpulkan bahwa dapat dipertanggungjawabkan sebab telah diketahui adanya komposisi kandungan kimiawi yang berguna sebagai obat (Thomas,1992). Di Indonesia penggunaan obat tradisional masih banyak dilakukan dan hal ini sudah menjadi tradisi masyarakat di Indonesia sejak lama. Sampai saat ini masyarakat masih menggunakan obat tradisional, bahkan ada kecenderungan hal tersebut meningkat, karena obat tradisional dianggap relatif tidak menimbulkan efek samping yang bermakna (Sutarjadi, 1991).
Berdasarkan penelitian penelitian Boonlaksiri et al, (2000) melaporakan bahwa senyawa stilbene terprenilasi dari Artocarpus intreger (nama lain dari cempedak) mempunyai aktivitas anti malaria in vitro pada Plasmodium falcifarum
. Sedangkan penelitian yang lain menunjukkan kulit batang cempedak dapat menurunkan jumlah parasit Plasmodium berghei darah mencit yang telah terinfeksi malaria (Utomo,2003;Hidayati,2004). Aktivitas malaria juga ditunjukkan dari beberapa isolat yang diperoleh dari tanaman ini dan salah satunya isolat terindentifikasi sebagai heteroflavon C, suatu flavon terprenilasi menunjukan aktivitas yang lebih poten daripada kloroquin (Widyawaruyanti et al, 2007).
Maretnowati (2007) telah melakukan uji toksisitas akut dan subakut ekstrak etanol dan ekstrak air kulit batang Artocarpus champeden Spreng dengan parameter histopatologi hati mencit menunjukkan bahwa harga LD50 ekstrak etanol dan ekstrak air kulit batang cempedak di atas 21 g/kg BB untuk mencit relatif kurang berbahaya. Akan tetapi pada pemberian ekstrak etanol dapat menyebabkan terjadinya perubahan gambaran histopatologi berupa degenerasi dan nekrosis pada dosis 10x dosis lazim sedangkan ekstrak air dapat menyebabkan terjadinya degenerasi dan tidak terjadi nekrosis. Penelitian lainnya uji toksisitas ekstrak etanol 80% kulit batang cempedak juga menunjukkan zat yang relatif kurang berbahaya akan tetapi pula ekstrak ini dapat menyebabkan perubahahan morfologi hati dan meningkatkan kadar enzim SGOT dan SGPT pada mencit (Wardhani, 2008).
Mengingat cempedak mempunyai aktivitas yang poten sebagai obat antimalaria dan prospektif untuk obat fitofarmaka sehingga perlu dikembangkan. Pengembangan produk fitofarmaka ini perlu dilakukan untuk menjamin keefektifan,khasiat,keamanannya.
Pada penelitian ini akan dilakukan uji toksisitas dengan menggunakan hewan uji mencit (Mus musculus). Uji toksisitas yang dilakukan yaitu uji toksisitas akut dan subakut. Uji toksisitas akut dilakukan dengan menggunakan parameter LD50 untuk mendapatkan dosis yang aman. Sedangkan uji toksisitas subakut dilakukan dengan pemeriksaan histopatologi organ hati untuk mengetahui derajat kerusakan yang mungkin di timbulkan akibat pemakaian obat dalam jangka waktu tertentu dan peningkatan enzim SGOT dan SGPT.
Pemilihan hati sebagai organ sasaran yang mungkin dirusak oleh adanya efek toksik dari obat dikarenakan hati merupakan organ tubuh yang rentan terhadap pengaruh bahan toksik. Kerentanan tersebut terkait dengan posisinya dalam sirkulasi cairan tubuh. Hati memiliki dua sumber suplai darah, yaitu dari saluran cerna dan limpa melalui vena porta hepatika, dan dari aorta melalui arteri hepatika. Setelah diabsorbsi, zat-zat toksik maupun bahan obat akan masuk ke peredaran darah dan kemudian didetoksifikasi dalam hati menjadi zat-zat yang tidak berbahaya yang kemudian diekskresi melalui ginjal. Adanya zat-zat toksik dalam jumlah besar dan terus menerus dapat menyebabkan kerusakan pada sel-sel hati (Koeman, 1987 ; Price dan Wilson, 2002). Selain itu, hati merupakan organ parenkim terbesar dan memegang peranan penting pada proses metabolisme tubuh (Hadi, 2002).
Parameter yang digunakan pada penelitian ini adalah aktivitas enzim SGOT dan SGPT karena aktivitas enzim-enzim tersebut merupakan indikator yang kuat dan peka terhadap adanya kerusakan atau kelainan sel-sel hati. Terjadinya kerusakan sel-sel tersebut menyebabkan bebasnya enzim-enzim intraseluler masuk ke dalam sirkulasi sistemik, sehingga kadarnya di dalam darah meningkat (Hadi, 2002). Parameter yang lain adalah gambaran histopatologi organ hati. Ini digunakan untuk mengetahui derajat kerusakan yang mungkin ditimbulkan akibat pemakaian obat dalam jangka waktu tertentu. Sel hati yang mengalami kerusakan ditandai dengan adanya degenerasi dan nekrosis (meliputi piknosis, karioeksis, dan kariolisis).
80 % sedangkan pada penelitian ini menggunakan sediaan granul yang dibuat berasal dari penelitian sebelumnya. Diharapkan pada penelitian ini sediaan granul ini dapat meningkatkan kemananannya dibanding dalam keadaan ekstraknya.
1.2. Rumusan Masalah
1. Apakah granul ekstrak etanol 80% kulit batang cempedak (Artocarpus champeden Spreng) dapat menimbulkan efek toksisitas akut berdasarkan parameter LD50 ?
2. Apakah granul berasal dari ektrak etanol 80% kulit batang cempedak (Artocarpus champeden Spreng) dapat menimbulkan efek toksisitas subakut berdasarkan parameter histopatologi organ hati dan aktivitas enzim SGOT dan SGPT ?
1.3. Tujuan Penelitian
1.3.1. Tujuan Umum
Tujuan umum penelitian ini adalah untuk mengetahui toksisitas akut dan subakut dari granul berasal dari ektrak etanol 80% kulit batang cempedak (Artocarpus champeden Spreng) pada mencit.
1.3.2. Tujuan Khusus
1. Menentukan toksisitas akut dari granul berasal dari ektrak etanol 80% kulit batang cempedak (Artocarpus champeden Spreng) berdasarkan parameter LD50
1.4. Hipotesis
Granul berasal dari ektrak etanol 80% kulit batang cempedak (Artocarpus champeden Spreng) tidak menimbulkan efek toksik dan tidak mempengaruhi aktivitas enzim SGOT dan SGPT pada hati mencit.
1.5. Manfaat Penelitian
1. Untuk memperkirakan spektrum efek toksik berdasarkan toksisitas relatifnya dengan keamanan penggunaan tablet berasal dari granul ektrak etanol 80% kulit batang cempedak (Artocarpus champeden Spreng)
BAB II
TINJAUAN PUSTAKA
2.1. Tinjauan Tentang Artocarpus champeden Spreng
2.1.1. Klasifikasi Tanaman
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Monocotyledoneae Sub kelas : Monochlamydae Bangsa : Morales
Suku : Moraceae Marga : Artocarpus
Jenis : Artocarpus champeden Spreng (Van Steenis, 1975; Backer & Van den Brink,1965)
Gambar 2.2. Kulit batang pohon cempedak
2.1.2. Nama Daerah Tanaman
Di beberapa daerah, Artocarpus champeden Spreng. Dikenal dengan berbagai nama antara lain :
Sunda : Campedak, cempedak, nangka beuri
Jawa : Campedak, cepedak, cempedak, nangka cina
Madura : Nangka, comedak, cempedak (Van Steenis, 1975; Backer & Van Den Brink, 1965)
2.1.3.Deskripsi Tanaman
Habitus : Pohon berumah satu, tinggi 10-20 m, liar atau ditanam, berbuah pada Juli sampai September
Batang : Tumbuhan berbatang sedang, membulat dengan banyak getah yang rekat
Daun : Helaian daun tipis berbentuk bulat 10-25 x 5-10 cm dengan panjang tangkai 1-3 cm, terdapat banyak trikoma pada tulang daun, betajuk pangkal pendek yang menyempit, tepi rata, warna daun mengkilat hijau tua.
hijau pucat atau kekuningan, bunga sangat kecil dengan bertajuk dua pipih pada ujungnya dan satu benang sari
Buah : Buah semu, silindris memanjang, bau menusuk, berbentuk segi 4-7.
Biji : Biji panjangnya 2-3 cm, diliputi oleh semacam lapisan daging biji berwarna kuning tua, lembut, tipis mengandung banyak air terasa manis (Van Steenis, 1975; Morton, 1987).
2.1.4.Kandungan Kimia
Hakim et al (1998) melaporkan adanya senyawa flavonoid yang diberi nama siklocampedol telah ditemukan pada kulit batang tumbuhan ini, bersama-sama dengan empat senyawa triterpen, yakni sikloeukalenol, glutinol, sikloartenon, dan 24-metilsikloartenon, serta suatu sterol, β-sitosterol (Hakim, 1996). Selain itu cempedak mempunyai tujuh kandungan senyawa flavonoid lainnya : artonin A , sikloheteropilin, heteroflavon C, artoindosianin E, artoindosianin R, artoindosianin A-2, heteropilin (Widyawaruyanti et al, 2007) dan empat senyawa flavon : artocarpon A & artocarpon B (Widyawaruyanti et al, 2007), artoindosianin A & artoindosianin B (Hakim et al,1999).
2.1.5. Bioaktivitas dan Kegunaan Tanaman
Artocarpus champeden Spreng adalah tumbuhan pangan yang endemik untuk Indonesia, kayunya keras, awet, dan digunakan sebagai bahan bangunan (Heyne, 1987). Buah dan bijinya digunakan sebagai bahan pangan, sedangkan beberapa bagian tanaman lain digunakan untuk bahan ramuan tradisional, antara lain digunakan sebagai obat demam, malaria, dan penyakit kulit.
Berdasarkan penelitian penelitian Boonlaksiri et al, (2000) melaporkan bahwa senyawa stilbene terprenilasi dari Artocarpus intreger (nama lain dari cempedak) mempunyai aktivitas anti malaria in vitro pada Plasmodium falcifarum
Aktivitas malaria juga ditunjukkan dari beberapa isolat yang diperoleh dari tanaman ini dan salah satunya isolat terindentifikasi sebagai heteroflavon C, suatu flavon terprenilasi menunjukan aktivitas yang lebih poten daripada kloroquin (Widyawaruyanti,2006).
2.2. Tinjauan Toksisitas
2.2.1. Tujuan Studi Toksisitas
Untuk menjamin keamanan dari suatu produk obat perlu dilakukan uji toksisitas. Banyak manfaat yang dapat diperoleh dari studi toksisitas (Ghosh, 1971; Loomis, 1978). Manfaat antara lain adalah :
a) Mendapatkan gejala-gejala yang timbul akibat pemberian obat. b) Mengetahui batas keamanan obat.
c) Mengetahui derajat kematian hewan coba akibat pemberian.
Dari hasil-hasil tersebut di atas, akan dapat dilakukan evaluasi obat dalam bidang medis. Selain itu juga dapat juga menunjukkan organ sasaran (misalnya hati), sistem (misalnya sistem kardiovaskular), atau toksisitas khusus (misalnya karsinogenitas) yang membutuhkan penelitian lebih lanjut (Lu, 1995).
2.2.2. Macam Studi Toksisitas
2.2.2.1 Toksisitas Akut
mati dan pada beberapa hewan hidup terutama hewan yang tampak sakit pada akhir percobaan. Otopsi dapat memberikan informasi yang berharga tentang organ sasaran, terutama bila kematian tidak terjadi dengan segera setelah pemberian obat (Andreas et al., 1992; Lu, 1995).
LD50 merupakan dosis tunggal suatu zat yang secara statistik diharapkan akan membunuh 50% hewan coba. Nilai LD50 berguna untuk hal-hal sebagai berikut :
a) Mengevaluasi efek keracunan yang tidak disengaja b) Klasifikasi zat kimia sesuai dengan toksisitas relatifnya
c) Perencanaan penelitian toksisitas sub akut dan kronik pada hewan d) Memberikan informasi tentang reaktivitas suatu populasi hewan
e) Memberikan sumbangan informasi yang dibutuhkan dalam merencanakan pengujian obat pada manusia dan dalam pengedalian mutu zat kimia f) Deteksi pencemaran toksik serta perubahan fisik yang mempengaruhi
bioavaibilitas (Lu, 1995).
Tabel II.1. Kategori Toksisitas Zat Kimia Pada Tikus
Kategori LD50
Luar biasa toksik ≤ 1 mg/kg BB
Sangat toksik 1-50 mg/kg BB
Cukup toksik 50-500 mg/kg BB Sedikit toksik 0,5-5 g/kg BB Praktis tidak toksik 5-15 g/kg BB Relatif kurang berbahaya > 15 g/kg BB (Loomis, 1978)
2.2.2.2. Toksisitas Sub Akut
waktu yang lebih pendek, misalnya pemberian zat selama 14 dan 28 hari (Lu, 1995).
Pengamatan yang perlu dilakukan pada toksisitas sub akut meliputi : a. Berat badan dan konsumsi makanan
Kedua hal tersebut harus diukur setiap minggu. Berkurangnya pertambahan berat badan merupakan indeks efek toksik yang sederhana namun sensistif. Konsumsi makanan merupakan indikator yang berguna sebab bila konsumsi makanan berkurang dapat menimbulkan efek yang mirip atau memperberat manifestasi toksik zat kimia.
b. Pengamatan umum
Hal yang harus diamati adalah penampilan, perilaku dan semua abnormalitas. Hewan yang mati atau sakit harus dipisah dari kandang untuk diperiksa secara umum dan kalau mungkin secara mikroskopik. c. Uji laboratrium
Pemeriksaan hematologik biasanya mencakup hematokrit, hemoglobin, hitung leukosit total dan hitung jenis leukosit. Uji laboratrium klinik biasanya mencakup glukosa darah puasa, SGOT, SGPT, alkali fosfatase, protein total, albumin, globumin, BUN dan unsur-unsur seperti natrium, kalium, kalsium dan klorit. Sedangkan urinalis mencakup warna, berat jenis, protein, glukosa, keton, unsur berbentuk kristal dan benda amorf (Lu, 1995).
2.3. Tinjauan Hati
2.3.1. Anatomi dan Fisiologi Hati
falsiforme yang dapat dilihat dari luar. Ligamentum falsiforme berjalan dari hati ke diafragma dan dinding depan abdomen. ( Price & Wilson, 1995).
Dasar unit fungsional hati adalah lobulus hati yang merupakan struktural silindris dengan panjang beberapa milimeter dan garis tengah 0,8-2 mm. Hati manusia mengandung 50.000-100.000 lobulus (Guyton & Hall, 1997).
Lobulus hati terbentuk mengelilingi sebuah vena sentralis yang bermuara ke dalam vena hepatika dan kemudian ke dalam vena cava. Lobulus sendiri dibentuk terutama dari banyak lempeng sel hati yang memancar secara sentrifugal dari vena sentralis seperti jeruji roda. Masing- masing lempeng hati tebalnya satu sampai dua sel, dan diantara sel-sel yang berdekatan terdapat kanalikuli biliaris di dalam septum fibrosa yang memisahkan lobulus hati yang berdekatan (Guyton & Hall, 1997).
Dalam septa juga terdapat venula porta kecil yang menerima darah terutama dari vena saluran pencernaan melaui vena porta. Dari venula ini darah mengalir ke sinusoid hati gepeng dan bercabang yang terletak diantara lempeng-lempeng hati dan kemudian masuk vena sentralis. Dengan demikian, sel hati terus menerus terpapar dengan darah vena porta (Guyton & Hall, 1997).
Selain vena porta, juga ditemukan arteriol hati di dalam septum interlobularis. Arterol ini menyuplai darah arteri ke jaringan septum diantara lobulus yang berdekatan,dan banyak arteriol kecil juga mengalir langsung ke sinusoid hati, paling sering pada sepertiga jarak ke septum interlobularis (Guyton & Hall, 1997).
2.3.2. Fungsi Hati
Hati merupakan organ parenkim terbesar dan menduduki urutan pertama dalam hal jumlah, kerumitan, dan ragam fungsi. Hati sangat penting untuk mempertahankan hidup dan berperan dalam hampir setiap fungsi metabolik tubuh, dan terutama bertanggung jawab atas lebih dari 500 aktifitas yang berbeda. Telah dilakukan penenlitian pada hewan coba, bahwa pengambilan 80-90% parenkim hati, hewan masih dapat menunujukkan fungsi hati yang normal. Sehingga untuk menghabiskan daya cadangan ini, diperlukan penyakit yang mengenai seluruh parenkim hati (Robbin & Kumar , 1995 ; Price & Wilson, 1995). Hati merupakan kelenjar tubuh terbesar dan memiliki multifungsi komplek, diantaranya adalah : 1. Fungsi vaskular untuk menyimpan darah, 2. Fungsi metabolisme, 3.Fungsi ekskresi, 4. Fungsi proteksi, 5. Fungsi detoksifikasi
2.3.2.1. Fungsi Vaskular untuk Menyimpan Darah
Kira-kira 1100 ml darah mengalir dari vena porta ke sinusoid hati setiap menit, dan tambahan sekitar 350 ml lagi mengalir ke sinusoid dari arteri hepatika, dengan total rata-rata 1450 ml/menit. Jumlah ini sekitar 29% dari sisa curah jantung, hampir satu pertiga dari aliran total darah tubuh. Karena hati merupakan suatu organ yang dapat diperluas, sejumlah besar darah dapat disimpan di dalam pembuluh darah hati. Volume darah normal hati, meliputi yang di dalam vena hati dan yang di dalam jaringan hati, adalah 450 ml, atau hampir 10 % dari total volume darah tubuh. Bila tekanan tinggi di dalam atrium kanan menyebabkan tekanan balik di dalam hati , hati meluas dan oleh karena itu 0,5 sampai 1 L cadangan darah kadang-kadang disimpan di dalam vena hepatika dan sinus hepatika. Keaadaan ini terjadi terutama pada gagal jantung disertai dengan kongesti perifer (Guyton & Hall, 1997).
2.3.2.2. Fungsi Metabolisme
turun terlalu rendah. Walaupun beberapa metabolisme lemak dapat terjadi di semua sel tubuh, aspek metabolisme lemak tertentu terjadi di hati. Beberapa fungsi spesifik dalam metabolisme lemak adalah pembentukan sebagian besar lipoprotein, kecepatan oksidasi beta asam lemak yang sangat cepat untuk mensuplai energi bagi fungsi tubuh yang lain, pembentukan sejumlah besar kolesterol dan fosfolipid, pengubahan sejumlah besar karbohidrat dan protein menjadi lemak.
Fungsi hati yang paling penting dalam metabolisme protein adalah deaminasi asam amino, pembentukan protein plasma. Selain itu fungsi metabolik hati yang lain adalah penyimpanan vitamin dan besi (Guyton & Hall, 1997).
2.3.2.3. Fungsi Ekskresi
Empedu disekresi secara terus menerus oleh hati. Empedu hati tidak dapat segera masuk ke duodenum, akan tetapi setelah melewati duktus hepatikus, empedu masuk ke dalam duktus sistikus dan ke kandung empedu. Dalam kandung empedu, pembuluh limfe dan pembuluh darah mengabsorbsi air dan garam-garam anorganik, sehingga empedu dalam kandung empedu kira-kira lima kali lebih pekat dibandingkan dengan empedu hati. Secara berkala kandung empedu mengosongkan isinya ke dalam duodenum melalui kontraksi simultan lapisan ototnya dan relaksasi sfingter Oddi (Price & Wilson, 1995).
2.3.2.4. Fungsi Proteksi
Hati berfungsi sebagai alat pertahanan tubuh karena pada hati terdapat sel kupffer yang mempunyai kemampuan memfagositosis sel-sel yang sudah tua, partikel atau benda asing, sel tumor, bakteri, virus dan parasit di dalam hati (Sherlock, 1995).
2.3.2.5 Fungsi Detoksifikasi
2.3.3. Test Gangguan Hati
Untuk mengetahui gangguan fungsi organ tubuh dapat ditentukan melalui test laboratrium atau diagnosa dengan pemeriksaan jaringan. Test laboratrium untuk evaluasi penyakit hati pada umumnya dapat dikelompokkan menjadi :
1. Diagnosis terhadap hasil ekskresi dan sekresi dari hati
Dapat dilakukan dengan pemeriksaan bilirubin dalam serum dan urin. Penimbunan pigmen empedu dalam tubuh menyebabkan warna jaringan menjadi kuning dan disebut sebagai ikterus. Ikterus biasanya dapat dideteksi pada sklera, kulit, atau urine yang menjadi gelap bila serum mencapai 2 sampai mg/dl (bilirubin serum normal adalah 0,3 sampai 1,0 mg/dl). Jaringan permukaan yang kaya elastin, seperti sklera dan permukaan bawah lidah biasanya menjadi kuning pertama kali. Bilirubin terkonjugasi diekskresi dalam urin bila kadarnya meningkat dalam serum, mengesankan adanya obstruksi pada sel hati atau saluran empedu (Prince & Wilson, 1995).
2. Diagnosis terhadap fungsi biokimia yang spesifik
Beberapa enzim yang dapat digunakan untuk membantu diagnosis adanya kerusakan parenkim hati adalah :
a. Glutamat Piruvat Transaminase (GPT), Glutamat Oxaloacetat Transaminase (GOT), Laktat Dehidrogenase (LDH) adalah enzim intrasel terutama berada di jantung, hati, dan jaringan skelet, yang dilepaskan dari jaringan yang rusak (seperti nekrosis), meningkat pada kerusakan sel hati dan pada keadaan lain terutama infark miokard. b. Alkali fosfatase adalah enzim yang dibentuk dalam tulang, hati,
ginjal, usus halus dan diekskresikan ke dalam empedu. Kadarnya meningkat pada obstruksi biliaris, penyakit tulang dan metastasis hati. Dari enzim-enzim tersebut GPT dan GOT lebih sering digunakan untuk menilai adanya kerusakan parenkim hati (Price & Wilson, 1995).
2.3.4. Tinjauan Parameter Kerusakan Hati
radial, inti sel berwarna biru dan sitoplasma berwarna merah. Sitoplasma sel terlihat penuh dan tidak berlubang-lubang.
Tanda-tanda kerusakan hati yang dapat diamati secara mikrokopis adalah degenerasi. Degenerasi merupakan perubahan morfologi sel akibat dari luka yang tidak mematikan (non letal injury) yang bersifat reversibel. Dikatakan reversibel karena apabila rangsangan yang menimbulkan cedera dapat dihentikan, maka sel akan kembali seperti semula. Tetapi apabila berjalan terus menerus dan dosis berlebihan, maka akan mengakibatkan nekrosis atau kematian sel yang tidak dapat pulih kembali (Price & Wilson, 1995 ; Himawan, 1994).
Degenerasi bengkak keruh atau dapat juga disebut cloudy swelling merupakan degenerasi yang paling ringan dan merupakan degenerasi yang terdeteksi paling dini dari suatu keadaan patologik. Apabila diamati dibawah mikroskop, maka akan terlihat perubahan-perubahan berupa pembengkakan mitokondria, sitoplasma tampak keruh karena kadar protein atau asam amino bertambah, inhibisi sel oleh protein serum dan hidrasi ion natrium akibat permeabilitas dinding sel hati yang terganggu. Bengkaknya sel hati dengan sitoplasma berbutir keruh disebabkan oleh pengendapan protein yang disebut juga
albuminous degeneration. Pada kelainan ini, sitoplasma akan tampak sedikit bervakuola dan lebih gelap daripada biasanya akibat dari kadar glikogen yang berkurang (Himawan,1994).
Degenerasi hidropik atau hydropic deneration adalah degenerasi yang ditandai dengan penumpukan air dalam sel. Pada prinsipnya sama dengan bengkak keruh, tetapi tingkat kerusakan jaringan yang ditimbulkan lebih berat dengan jangka waktu yang lebih lama.
Sitoplasma mulai memanjang dan menyerap zat warna lebih banyak sehingga warna menjadi lebih gelap setelah dilakukan pewarnaan. Kariolisis ditandai dengan inti yang mulai hilang hingga sulit dikenali secara mikroskopik, bentuk sel lebih memanjang dan warnanya menjadi tidak jelas setelah dilakukan pewarnaan (Himawan, 1994). Gambaran Hispatolgi hati hewan coba ditujukan pada gambaran 2.3, 2.4, 2.5 (Donald & Zachary, 2007)
Gambar 2.3. Gambaran histopatologi sel hati normal yaitu sitoplasma tidak mengalami Pembengkakan dan tidak pucat serta pada inti tidak terjadi
penggumpalan kromatin, sinusoid (s)
Gambar 2.4. Gambaran hispatologi sel hati yang mengalami degenerasi yaitu terjadinya pembengkakan pada sitoplasma, sitoplasma nampak bervakuola dan
Gambar 2.5. Gambaran hispatologi sel hati yang mengalami nekrosis berupa piknotik yaitu terjadinya penggumpalan kromatin, inti tampak lebih padat dan
berwarna gelap hitam
2.4. Tinjauan Enzim
2.4.1. Sifat Umum Enzim
Enzim befungsi sebagai katalisator dalam sel dan mempunyai sifat yang sangat khas. Sebagian besar reaksi kimia dalam sel hidup akan terjadi sangat lambat jika tidak dikatalisa oleh enzim (Wilson, 1982). Dalam jumlah yang sangat kecil, enzim dapat mengatur reaksi tertentu sehingga dalam keadaan normal tidak terjadi penyimpangan-penyimpangan hasil akhir reaksinya. Enzim akan kehilangan aktivitasnya akibat panas, asam atau basa kuat, dan pelarut organik yang bisa menyebabkan denaturasi protein (Girinda, 1986). Pada keadaan patologis tertentu kadar enzim dalam serum dapat digunakan sebagai parameter diagnostik yang penting (Wilson, 1982).
2.4.2. Faktor-Faktor yang Mempengaruhi Berlangsungnya Reaksi Enzim
2.4.2.1. Kadar Enzim dan Substrat
seluruhnya oleh substrat dan pada saat itu enzim telah bekerja dengan kapasitas penuh (Girinda, 1986).
2.4.2.2. Suhu
Enzim sebagai protein akan mengalami denaturasi jika suhunya dinaikan. Sehingga daya kerja enzim menurun. Pada suhu di atas 45°C timbul efek denaturasi termal dan pada suhu yang mendekati 55°C fungsi katalisis enzim hilang (Girinda, 1986).
2.4.2.3 pH
Aktivitas enzim juga dipengaruhi oleh pH karena sifat gugus karboksil dan gugus amino mudah dipengaruhi oleh pH. Di dalam sel dan lingkungan sel sekelilingnya, pH dalam keadaan normal harus tetap sebab adanya perubahan akan menyebabkan pergeseran aktivitas enzim. Hal ini akan mempengaruhi sistem katabolik dan anabolik dalam sel dan jaringan (Girinda, 1986).
2.4.2.4. Inhibitor
Enzim sangat peka terhadap senyawa atau gugus senyawa yang diikatnya. Senyawa atau gugus senyawa yang menghambat aktivitas enzim disebut inhibitor. Tidak semua inhibitor bersifat merugikan karena dalam sel bisa juga terdapat inhibitor yang berfungsi sebagai regulasi reaksi enzim. Dalam hal ini inhibitor mengontrol produk enzim sehingga hanya cukup untuk kebutuhan sel saja (Girinda, 1986).
2.4.3. Tinjauan Enzim SGOT dan SGPT
Transaminase adalah sekelompok enzim dan bekerja sebagai katalisator dalam proses pemindahan gugusan amino antara suatu asam alfa amino dengan asam alfa keto (Page, 1997).
akut, kadarnya dalam serum meningkat. Kadar yang meningkat terdapat pada hepatoseluler nekrosis atau infark miokard (Hadi, 2002).
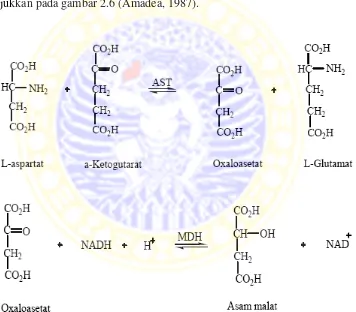
Prinsip reaksi penentuan kadar enzim SGOT adalah Glutamat Oksaloasetat Transaminase mengkatalisis reaksi antara asam α-ketoglutarat dengan asam aspartat menghasilkan suatu asam oksaloasetat dan asam L-glutamat. Asam oksaloasetat yang terbentuk, dengan adanya MDH, akan direduksi menjadi asam malat, bersamaan dengan itu NADH menjadi NAD+. NADH diabsorbsi pada panjang gelombang 340 nm. Kecepatan penurunan absorbsi pada panjang gelombang tersebut sebanding dengan aktivitas SGOT. Persamaan reaksi yang digunakan untuk menentukan aktivitas enzim SGOT ditunjukkan pada gambar 2.6 (Amadea, 1987).
Gambar 2.6. Reaksi penentuan aktivitas enzim SGOT
dalam serum meningkat terutama pada kerusakan dalam hati jika dibandingkan dengan GOT (Hadi, 2002).
Prinsip reaksi penentuan kadar enzim SGPT adalah Glutamat Piruvat Transaminase mengkatalisis reaksi antara α-ketoglutarat dengan L-alanin menghasilkan suatu asam piruvat dan asam L-glutamat. Asam piruvat yang terbentuk, dengan adanya LDH, akan direduksi menjadi asam laktat, bersamaan dengan itu NADH menjadi NAD+. NADH diabsorbsi pada panjang gelombang 340 nm. Kecepatan penurunan absorbsi pada panjang gelombang tersebut sebanding dengan aktivitas SGPT. Persamaan reaksi yang digunakan untuk menentukan aktivitas enzim GPT ditunjukan pada gambar 2.7 (Amadea, 1987).
BAB III
KERANGKA KONSEPTUAL
Saat ini, dunia berada dalam iklim back to nature atau dikenal dengan gerakan kembali ke alam yang dalam pelaksanaanya membiasakan hidup dengan menghindari bahan-bahan kimia sintesis dan lebih mengutamakan bahan alami. Semua hal yang serba natural semakin digemari dan dicari orang, salah satunya adalah penggunaan tumbuhan untuk pengobatan (Kardinan & Kusuma, 2003).
Di Indonesia penggunaan obat tradisional masih banyak dilakukan dan hal ini sudah menjadi tradisi masyarakat di Indonesia sejak lama. Sampai saat ini masyarakat masih menggunakan obat tradisional, bahkan ada kecenderungan hal tersebut meningkat, karena obat tradisional dianggap relatif tidak menimbulkan efek samping yang bermakna (Sutarjadi, 1991).
Tumbuhan Artocarpus champeden (suku Moraceae) atau yang dikenal masyarakat dengan nama daerah cempedak, secara empirik digunakan untuk bahan ramuan tradisional, antara lain sebagai obat demam,disentri, malaria, dan penyakit kulit. Cempedak mempunyai tujuh kandungan senyawa flavonoid : artonin A , sikloheteropilin, heteroflavon C, artoindosianin E, artoindosianin R, artoindosianin A-2, heteropilin (Widyawaruyanti et al, 2007) dan empat senyawa flavon : artocarpon A & artocarpon B (Widyawaruyanti et al, 2007), artoindosianin A & artoindosianin B (Hakim et al,1998). Selain itu terdapat kandungan lain yaitu empat senyawa triterpen : sikloeukalenol, glutinol, sikloartenon, 24-metilsikloartenon serta suatu senyawa sterol yaitu β-sitosterol (Hakim et al, 1996).
Berdasarkan penelitian penelitian Boonlaksiri et al, (2000) melaporakan bahwa senyawa stilbene terprenilasi dari Artocarpus intreger (nama lain dari cempedak) mempunyai aktivitas anti malaria in vitro pada Plasmodium falcifarum
. Sedangkan penelitian yang lain menunjukkan kulit batang cempedak dapat menurunkan jumlah parasit Plasmodium berghei darah mencit yang telah terinfeksi malaria (Utomo,2003;Hidayati,2004).
flavon terprenilasi menunjukan aktivitas yang lebih poten daripada kloroquin(Widyawaruyanti,2007).
Maretnowati(2007) telah melakukan uji toksisitas akut dan subakut ekstrak etanol dan ekstrak air kulit batang Artocarpus champeden Spreng dengan parameter histopatologi hati mencit menunjukkan bahwa harga LD50 ekstrak etanol dan ekstrak air kulit batang cempedak di atas 21 g/kg BB untuk mencit relatif kurang berbahaya. Akan tetapi pada pemberian ekstrak etanol dapat menyebabkan terjadinya perubahan gambaran histopatologi berupa degenerasi dan nekrosis pada dosis 10x dosis lazim sedangkan ekstrak air dapat menyebabkan terjadinya degenerasi dan tidak terjadi nekrosis. Penelitian lainnya uji toksisitas ekstrak etanol 80% kulit batang cempedak juga menunjukkan zat yang relatif kurang berbahaya akan tetapi pula ekstrak ini dapat menyebabkan perubahahan morfologi hati dan meningkatkan kadar enzim SGOT dan SGPT pada mencit (Wardhani, 2008).
Mengingat cempedak mempunyai aktivitas yang poten sebagai obat antimalaria dan prospektif untuk obat fitofarmaka sehingga perlu dikembangkan. Pengembangan produk fitofarmaka ini perlu dilakukan untuk menjamin keefektifan,khasiat,keamanannya.
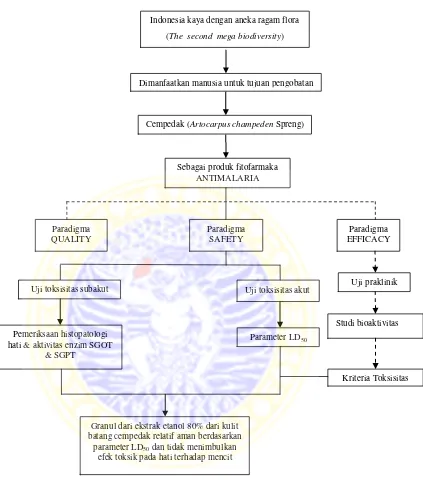
3.1. Skema Kerangka Konseptual
Gambar 3.1. Skema kerangka konseptual Indonesia kaya dengan aneka ragam flora
(The second mega biodiversity)
Sebagai produk fitofarmaka ANTIMALARIA
Paradigma SAFETY
Paradigma EFFICACY Paradigma
QUALITY
Uji toksisitas subakut Uji toksisitas akut
Pemeriksaan histopatologi hati & aktivitas enzim SGOT
& SGPT
Parameter LD50
Granul dari ekstrak etanol 80% dari kulit batang cempedak relatif aman berdasarkan
parameter LD50 dan tidak menimbulkan efek toksik pada hati terhadap mencit
Uji praklinik
Studi bioaktivitas
Kriteria Toksisitas Dimanfaatkan manusia untuk tujuan pengobatan
BAB IV
METODE PENELITIAN
4.1. Bahan
4.1.1. Bahan Kimia
Bahan untuk penentuan toksisitas dan keamanan :
Formalin 10%, hematoxylin eosin, xylol, paraffin cair, dan kanada balsam
4.1.2. Bahan Larutan Uji Toksisitas
CMC Na 0,5% , Granul dari ekstrak 80% etanol dari kulit batang cempedak diperoleh dari desa Mugirejo, Samarinda, Kalimantan Timur. Tgl pemanenan 17 Juni 2009, ketinggian permukaan tanah ± 50 m DPL, ketinggian pohon ± 15 m, diameter pohon ± 80 cm, usia tanaman ± 6 tahun.
4.1.3. Bahan Uji
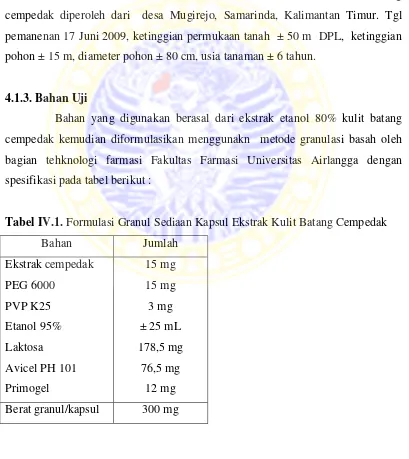
Bahan yang digunakan berasal dari ekstrak etanol 80% kulit batang cempedak kemudian diformulasikan menggunakn metode granulasi basah oleh bagian tehknologi farmasi Fakultas Farmasi Universitas Airlangga dengan spesifikasi pada tabel berikut :
Tabel IV.1. Formulasi Granul Sediaan Kapsul Ekstrak Kulit Batang Cempedak
4.2. Hewan Coba
Hewan coba yang digunakan untuk penentuan uji toksisitas adalah mencit jantan dan betina dewasa (2-3 bulan dengan berat 20-30 g), galur BALB/C yang diperoleh dari Universitas Gajah Mada,Yogyakarta.
4.3. Alat-Alat Penelitian
Alat untuk penentuan toksisitas dan keamanan :
Alat-alat bedah (gunting,pisau,pinset), alat-alat gelas, kaca objek, alat sonde, labu ukur, gelas beker, cawan porselen, batang pengaduk, sudip, mortir, stamper, lemari pendingin, timbangan hewan, mikroskop cahaya, spet injeksi,
venoject, pot plastik, bak hewan, dan kawat penutup.
4.4. Penyiapan Obyek Penelitian
Mencit yang akan digunakan diadaptasikan dengan lingkungan minimal 1 minggu. Semua mencit dipelihara dengan cara yang sama dan diberi diet makanan sama pula. Sebelum perlakuan semua mencit ditimbang untuk mengetahui berat badan sehingga mempermudah pengaturan dosis.
4.5. Cara Kerja
4.5.1. Pemilihan Dosis Uji Toksisitas Akut
Pemilihan dosis awal yang digunakan untuk penelitian ini dipilih dosis dengan harga tertinggi dari suatu bahan yang dikategorikan sebagai “relatively harmless” menurut tabel Toxicity Rating (Dorelanko, 1995). Dinyatakan bahwa suatu bahan dikatakan praktis tidak beracun jika jumlah bahan uji pada tikus 15 g/kg BB. Kemudian dilakukan penyetaraan dosis dari tikus ke mencit, dan diperoleh dosis sebesar 21 g/kg BB mencit.
4.5.2. Pemilihan Dosis Uji Toksisitas Subakut
Dosis yang digunakan pada uji toksisitas ini adalah dosis efektif dari kulit cempedak dari penelitian antimalaria Dr. Aty Widyawaruyanti sebesar 10 mg/kg BB mencit. Dari dosis efektif ini ditingkatkan lagi menjadi 5 kali dan 10 kalinya berdasarkan penelitian uji toksisitas ekstrak etanol 80% kulit batang cempedak oleh Esti Eka Wardhani pada tahun 2008 untuk mengetahui perbedaan kerusakan hati yang ditimbulkan dari ketiga dosis yang berbeda tersebut apabila digunakan secara oral sebanyak 1 kali pada mencit selama 14 hari. Dosis yang digunakan pada uji toksisitas subakut adalah 1x dosis efektif ; 5x dosis efektif ; dan 10x dosis efektif.
4.5.3. Penyiapan Bahan Uji
Pemberian tiap dosis dalam bentuk ekstrak kering yang disuspensikan dalam mucilago CMC Na 0,5%. Kontrol negative diberi mucilage CMC Na 0,5%. Pembuatan mucilago CMC Na 0,5% dengan cara ditimbang 0,5 g CMC Na, ditaburkan di atas air panas secukupnya, dibiarkan mengembang ± 15 menit di dalam mortir. Digerus sampai homogen, setelah homogen beri sedikit air agar sediaan menjadi encer kemudian dipindahkan ke dalam labu ukur dan ditambah dengan aquadest sampai 100 ml. Mucilago CMC Na ini diberikan ke kelompok kontrol sebanyak 1ml secara oral.
4.5.4. Pengumpulan Data Uji Toksisitas Akut
Disiapkan dua kelompok mencit untuk tiap granul dari ekstrak etanol yang masing-masing menerima dosis yang berbeda. Masing-masing kelompok terdiri dari 5 ekor mencit jantan dan 5 ekor betina, tiap hewan coba diberi granul esktrak etanol cempedak sesuai dengan dosis masing-masing, kecuali kelompok kontrol. Pemberian dilakukan secara per oral sebanyak satu kali, kemudian dilakukan pengamatan selama 7 hari.
Kontrol : Sebagai kelompok kontrol, diberi suspensi CMC Na 0,5% Kelompok I : Diberi granul dari ekstrak cempedak dosis tertinggi yang
4.5.5. Pengumpulan Data Uji Toksisitas Subakut
Disiapkan 4 kelompok mencit untuk tiap granul ekstrak yang masing-masing menerima dosis yang berbeda. Masing-masing-masing kelompok terdiri dari 9 ekor mencit jantan. Tiap hewan coba diberi granul ekstrak etanol cempedak sesuai dengan dosis masing-masing, kecuali kelompok kontrol. Pemberian dilakukan secara per oral sebanyak 1 kali selama 14 hari, kemudian hewan coba dikorbankan diambil organ hatinya untuk dibuat preparat dan darahnya secara intra cardial. Kemudian diukur aktivitas enzim SGOT dan SGPT-nya.
Kontrol : Sebagai kelompok kontrol, diberi suspensi CMC Na 0,5%
Kelompok I : diberi granul dari esktrak cempedak setara dengan dosis efektif yaitu 10 mg/kg BB atau 0,2 mg / 20 g BB mencit
Kelompok II : diberi granul dari ekstrak cempedak dengan 5x dosis efektif yaitu 50 mg/kg BB atau 1 mg / 20 g BB mencit
Kelompok III : diberi granul dari ekstrak cempedak dengan 10x dosis efektif yaitu 100 mg/kg BB atau 2 mg / 20 mg BB mencit
4.5.6. Analisis Data Uji Toksisitas Akut
Data yang diperoleh dalam penelitian ini diolah dengan menggunakan probit analisis, suatu program komputer yang dibuat untuk menentukan LD50 dari granul ekstrak etanol 80% kulit batang cempedak yang diuji. Prinsip pengolahan data dari program ini adalah mengintrapolasikan dosis bahan uji dengan persen letalitas (kematian) mencit yang diuji.
4.5.7. Analisis Data Uji Toksisitas Subakut
4.5.7.1. Pemeriksaan Preparat
Pada penelitian ini menggunakan mikroskop cahaya agar dapat mengamati secara mikroskopik preparat hati mencit. Mula-mula digunakan perbesaran 100 kali kemudian digunakan perbesaran 400 kali. Setiap preparat hati mencit diamati perubahannya melalui lima lapang pandang yang berbeda.
dijumlah dan dibagi lima, maka hasil dari lima kali pergeseran itu adalah data dari satu preparat. (Sukardja, 1998).
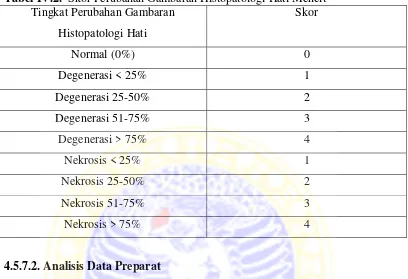
Tabel IV.2. Skor Perubahan Gambaran Histopatologi Hati Mencit Tingkat Perubahan Gambaran
Histopatologi Hati
Skor
Normal (0%) 0
Degenerasi < 25% 1
Degenerasi 25-50% 2
Degenerasi 51-75% 3
Degenerasi > 75% 4
Nekrosis < 25% 1
Nekrosis 25-50% 2
Nekrosis 51-75% 3
Nekrosis > 75% 4
4.5.7.2. Analisis Data Preparat
Data Perubahan gambaran histopatologi hati mencit yang telah diberi skor, diolah dengan penilaian peringkat (rank) lalu dianalisis menggunakan uji Kruskal Wallis. Dipilih uji Kruskal Wallis karena data yang diperoleh berdasarkan nilai skoring ataua penilaian derajat perubahan. Bila terjadi perbedaan yanga nyata diantara kelompok perlakuan, maka dilanjutkan dengan Uji Perbandingan Berganda (uji Z) 5% (Daniel, 1989).
4.5.7.3. Pembuatan Preparat Histopatologi
4.5.7.4.Analisis Enzim SGPT dan SGOT
Data yang diperoleh dari aktivitas enzim SGOT dan SGPT, dianalisis dengan ANAVA (one way) pada derajat kepercayaan 95% untuk mengetahui apakah ada perbedaan yang bermakna antar kelompok perlakuan.
Hipotesa yang diajukan adalah sebagai berikut :
Ho : Tidak ada perbedaan bermakna aktivitas enzim SGOT dan SGPT antar kelompok perlakuan.
Ha : Ada perbedaan bermakna aktivitas enzim SGOT dan SGPT antar kelompok perlakuan
Untuk menilai hipotesis statistik, dilihat harga Sig. harga ini kemudian
dibandingkan dengan α (0,05). Bila Sig. < α (0,05) maka Ho ditolak dan Ha
diterima. Untuk mengetahui kelompok mana yang berbeda secara bermakna, dilanjutkan dengan uji LSD (Least Significant Difference). Dari hasil uji
Skema Pemberian Bahan Uji Toksisitas Akut
Keterangan gambar 4.1. :
Kelompok Kontrol = sebagai kontrol , diberi suspensi CMC-Na 0,5%
Kelompok Dosis I = diberi granul dari ekstrak etanol 80% kulit batang cempedak dengan dosis 21 g/kg BB atau 0,42 g / 20 mg BB mencit
Granul dari ekstrak 80% etanol kulit batang cempedak (Artocarpus
champeden Spreng )
Kontrol
4 jam pertama
Pengamatan
24 jam – 7 hari
Hitung jumlah mencit mati
Analisis data
Skema Pemberian Bahan Uji Toksisitas Subakut
Keterangan gambar 4.2. :
Kelompok Kontrol = sebagai kontrol , diberi suspensi CMC-Na 0,5% Kelompok Dosis I = Diberi granul dari ekstrak etanol 80% kulit batang
cempedak dengan dosis efektif 10 mg/kg BB atau 0,2 mg / 20 g BB mencit
Kelompok Dosis II = Diberi granul dari ekstrak etanol 80% kulit batang cempedak dengan dosis efektif 50 mg/kg BB atau 1 mg / 20 g BB mencit
Granul dari ekstrak 80% etanol kulit batang cempedak (Artocarpus
champeden Spreng )
Dosis I Dosis II Dosis III Dosis IV
Pemberian sediaan sehari satu kali selama 14 hari
Pengambilan organ hati Pengambilan darah
Pembuatan preparat hati
Pengamatan mikroskopik
Analisis data
Analis data
Pengamatan SGOT & SGPT
BAB V
HASIL PENELITIAN
5.1. Data Hasil Penelitian
5.1.1. Uji Toksisitas Akut
Hasil uji toksisitas akut sediaan suspensi dari sediaan granul ekstrak etanol 80% kulit batang cempedak pada mencit ditunjukkan pada tabel sebagai berikut :
Tabel V.1. Hasil Uji Toksisitas Akut pada Mencit
Kelompok Jumlah Mencit Jantan
Mati Hidup
Kontrol 0 5
I 0 5
Kelompok Jumlah Mencit Betina
Mati Hidup
Kontrol 0 5
I 0 5
Keterangan :
KEL Kontrol = Kelompok Kontrol diberi suspensi CMC-Na 0,5%
5.1.2. Uji Toksisitas Subakut
5.1.2.1. Nilai Skor Perubahan Gambar Histopatologi Hati Mencit
Untuk mengetahui efek hepatotoksik granul ekstrak etanol 80 % kulit batang cempedak (Artocarpus champeden Spreng) selain dilakukan pengukuran aktivitas dari enzim SGOT dan SGPT pada hewan coba, dilakukan pula pengamatan histopatologi sel hepar hewan coba. Pengamatan histopatologi ini untuk melihat kerusakan sel hati secara mikroskopis.
Perubahan yangnampak pada gambaran histopatologi hati mencit diperoleh dari pengamatan secara mikroskopik melalui lima lapang pandang yang berbeda terhadap seluruh kelompok perlakuan, dicatat, diskor lalu diolah dengan penilaian peringkat (rank), seperti dapat dilihat pada tabel 5.2 dan 5.3 sebagai berikut :
Tabel V.2. Nilai Skor Perubahan Histologi Mencit pada Seluruh Kelompok Perlakuan yang Mengalami Perubahan Berupa Degenerasi Akibat Pemberian Granul Ekstrak Etanol Cempedak ( Artocarpus
champeden Spreng )
KEL Kontrol = Kelompok Kontrol diberi suspensi CMC-Na 0,5% KEL I = Kelompok Dosis 0,2 mg/ 20 g BB mencit
Tabel V.3. Nilai Skor Perubahan Histologi Mencit pada Seluruh Kelompok Perlakuan yang Mengalami Perubahan Berupa Nekrosis Akibat
Pemberian Granul Ekstrak Etanol Cempedak ( Artocarpus champeden
Spreng )
Replikasi KONTROL KEL I KEL II KEL III
1 0 0,2 0,8 0,6
2 0 2,2 0,6 1
3 0,6 1,4 0,6 0,6
4 0,6 0,6 0,4 0,4
5 0,6 0,4 0 0,4
6 0,4 0 0,8 1
7 0,6 1 0,6 0,8
8 1,0 0 1,2 0,6
9 0,6 0 1 0,8
rerata 0,49 0,64 0,67 0,69
Keterangan :
Replikasi = Ulangan
KEL Kontrol = Kelompok Kontrol diberi suspensi CMC-Na 0,5% KEL I = Kelompok Dosis 0,2 mg/ 20 g BB mencit
KEL II = Kelompok Dosis 1 mg/ 20 g BB mencit KEL III = Kelompok Dosis 2 mg/ 20 g BB mencit
5.1.2.2. Hasil Pengamatan Histopatologi Hati Pada Mencit
Gambar 5.1
Gambaran Histopatologi Hati Normal pada Perbesaran 400x
Gambar 5.2
Gambaran Histopatologi Hati Pada Perbesaran 400x yang Terjadi Degenerasi Yakni Terjadi Pembengkakan pada Sitoplasma, Sitoplasma
Gambar 5.3
Gambaran Histopatologi Hati Pada Perbesaran 400x yang Terjadi Nekrosis Berupa Piknotik Yakni Terjadinya Penggumpalan Kromatin dan Tidak Dikenali Lagi Inti (nukleus), Inti Tampak Lebih Padat dan Berwarna Gelap
Hitam
5.1.2.3. Hasil Pengamatan Enzim SGOT dan SGPT Mencit
Tabel V.4. Aktivitas Enzim SGOT Mencit pada Seluruh Kelompok Perlakuan
Replikasi Aktivitas Enzim SGOT ( U / L )
KONTROL KEL I KEL II KEL III
1 63 72 48 31
2 51 28 66 85
3 39 96 66 78
4 73 54 73 64
5 74 50 46 56
6 74 79 45 56
7 70 59 43 46
8 64 36 78 73
9 31 53 74 70
Keterangan :
Replikasi = Ulangan
KEL Kontrol = Kelompok Kontrol diberi suspensi CMC-Na 0,5% KEL I = Kelompok Dosis 0,2 mg/ 20 g BB mencit
KEL II = Kelompok Dosis 1 mg/ 20 g BB mencit KEL III = Kelompok Dosis 2 mg/ 20 g BB mencit
Tabel V.5. Aktivitas Enzim SGPT Mencit pada Seluruh Kelompok Perlakuan
Replikasi Aktivitas Enzim SGPT ( U / L )
KONTROL KEL I KEL II KEL III
1 18 21 33 60
2 12 25 23 20
3 15 21 16 25
4 48 26 72 13
5 26 15 77 19
6 20 21 17 34
7 25 12 36 18
8 22 22 22 21
9 25 26 19 18
rerata 23,45 21,00 35,00 25,33
Keterangan :
Replikasi = Ulangan
KEL Kontrol = Kelompok Kontrol diberi suspensi CMC-Na 0,5% KEL I = Kelompok Dosis 0,2 mg/ 20 g BB mencit
5.2. Analisis Data
5.2.1. Uji Toksisitas Akut
Pada uji toksisitas akut pada mencit digunakan dosis yang tertinggi yaitu 21 g/kg BB mencit kemudian disetarakan ke mencit dengan berat 20 g sehingga didapatkan dosis 0,42 g / 20 g BB mencit. Hasil uji toksisitas akut dengan dosis tertinggi tersebut tidak menunjukkan kematian pada mencit sehingga disimpulkan bahwa LD50 tidak perlu ditentukan atau dapat pula dianggap dosis yang digunakan yaitu dosis yang tergolong klasifikasi relatif tidak berbahaya tersebut dijadikan sebagai LD50 untuk sediaan suspensi granul ekstrak etanol 80% dari kulit batang cempedak ( Artocarpus champeden Spreng ).
Dengan demikian dapat pula disimpulkan bahwa LD50 untuk ekstrak etanol kulit batang cempedak ( Artocarpus champeden Spreng ) di atas dosis 0,42 g / 20g BB mencit.
5.2.2. Histopatologi Sel Hati
5.2.2.1. Uji Statistik Kruskal-Wallis
Data skoring masing-masing perubahan patologis yang diperoleh kemudian dianalisis menggunakan analisis Kruskal-Wallis. Hipotesis yang diajukan adalah sebagai berikut :
Ho: Tidak ada perbedaan bermakna antar kelompok. Ha : Ada perbedaan bermakna antar kelompok
Untuk menilai hipotesis statistik, terlebih dahulu ditentukan harga signifikasi (Asymp. Sig.) yang akan dibandingkan dengan harga tingkat kepercayaan 95%. Bila signifikansi (Asymp. Sig.) < (0,05) maka Ho ditolak dan Ha diterima. Untuk mengetahui kelompok mana saja yang berbeda makna, maka dilakukan uji U Mann-Whitney.
Tabel V.6. Harga Rerata Hasil Pengamatan Histopatologi Hatipada Perubahan Berupa Degenerasi
Kelompok N Rerata Perubahan
Histopatologi
Simpangan Baku
I 9 1,31 0,98
II 9 1,16 0,89
III 9 2,16 0,65
.
Tabel V.7. Hasil Uji Kruskal-Wallis Pada Perubahan Berupa Degenerasi
Chi-Square 19,873
Derajat Bebas 3
Asymp.Sig 0,000
Dari tabel ringkasan uji Kruskal-Wallis histopatologi hati pada perubahan degenerasi didapatkan harga signifikasi (Asymp. Sig.) = 0,000 signifikansi tersebut lebih kecil dari 0,05. Maka dapat disimpulkan Ha diterima dan Ho ditolak Hal ini menunjukkan bahwa ada perbedaan bermakna diantara kelompok kontrol dengan kelompok perlakuan.
Tabel V.8. Harga Rerata Hasil Pengamatan Histopatologi Hatipada Perubahan Berupa Nekrosis
Kelompok N Rerata Perubahan
Histopatologi
Simpangan Baku
Kontrol 9 0,49 0,32
I 9 0,64 0,76
II 9 0,67 0,35
III 9 0,69 0,23
Tabel V.9. Hasil Uji Kruskal-Wallis Pada Perubahan Berupa Nekrosis
Chi-Square 2.118
Derajat Bebas 3
Asymp.Sig 0.548
menunjukkan bahwa tidak ada perbedaan bermakna diantara kelompok kontrol dengan kelompok perlakuan
5.2.2.2. Uji Mann-Whitney U
Hasil perhitungan uji Kruskal-Wallis menunjukkan bahwa terdapat perbedaan yang nyata diantara kelompok perlakuan, maka dilanjutkan dengan uji U Mann-Whitney.
Hasil analisis data dengan uji Mann-Whitney U akan dapat diketahui urutan tingkat perubahan gambaran histopatologi hati diantara kelompok uji.
Tabel V.10. Hasil Uji Mann-Whitney U Antara Kontrol Dengan Kelompok I yang Mengalami Perubahan Berupa Degenerasi
DEG Mann-Whitney U 8.500 Wilcoxon W 53.500
Z -2.886
Asymp. Sig. (2-tailed) .004 Exact Sig. [2*(1-tailed
Sig.)] .003
a
Dari tabel uji Mann-Whitney U antara kelompok kontrol dengan kelompok I didapatkan harga signifikansi (Asymp. Sig.) = 0,004 signifikansi tersebut lebih kecil dari 0,05, sehingga dapat disimpulkan adanya perbedaan bermakna antara kelompok.
Tabel V.11. Hasil Uji Mann-Whitney U Antara Kontrol Dengan Kelompok II yang Mengalami Perubahan Berupa Degenerasi
DEG Mann-Whitney U 13.000
Wilcoxon W 58.000
Z -2.506
Asymp. Sig. (2-tailed) .012 Exact Sig. [2*(1-tailed
Sig.)] .014
a
kecil dari 0,05, sehingga dapat disimpulkan adanya perbedaan bermakna antara kelompok.
Tabel V.12. Hasil Uji Mann-Whitney U Antara Kontrol Dengan Kelompok III yang Mengalami Perubahan Berupa Degenerasi
DEG Mann-Whitney U .000
Wilcoxon W 45.000
Z -3.625
Asymp. Sig. (2-tailed) .000 Exact Sig. [2*(1-tailed
Sig.)] .000
a
Dari tabel uji Mann-Whitney U antara kelompok kontrol dengan kelompok III didapatkan harga signifikansi (Asymp.Sig.) = 0,000 signifikansi tersebut lebih kecil dari 0,05, sehingga dapat disimpulkan adanya perbedaan bermakna antara kelompok.
5.2.3. Aktivitas Enzim SGOT / SGPT Mencit
5.2.3.1. Uji ANAVA ( One Way )
Dari data di atas dilakukan analisis dengan uji ANAVA ( One Way ) menggunakan pada tingkat kepercayaan 95 % ( α = 0,05 ) untuk membuktikan apakah ada perbedaan bermakna yang ditunjukkan antar kelompok perlakuan dan kelompok kontrol.
Tabel V.13. Hasil Rerata Aktivitas SGOT Hewan Coba Tiap Kelompok
Kelompok N Rerata kadar SGOT
U/L
Simpangan Baku
Kontrol 9 59,9 16,00
I 9 58,6 21,12
II 9 55,2 14,20
Tabel V.14. Ringkasan ANAVA Untuk Aktivitas Enzim SGOT Hewan
Dari Tabel di atas, diperoleh harga signifikansi = 0,978 untuk SGOT, harga sigfikansi tersebut lebih besar dari 0,05. Maka dapat disimpulkan Ha ditolak dan Ho diterima. Hal ini menunjukkan tidak ada perbedaan bermakna diantara kelompok kontrol dan kelompok perlakuan.
Tabel V.15. Hasil Rerata Aktivitas SGPT Hewan Coba Tiap Kelompok
Kelompok N Rerata kadar SGPT
U/L