Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 6
BAB II
TEORI DASAR
2.1 Pendahuluan
Air merupakan kebutuhan primer makluk hidup, karena tanpa energi makluk hidup tidak akan bisa berkembang biak, seperti air, air merupakan yang paling dibutuh oleh manusia karena lebih dari 60% tubuh manusia mengandung air,. Karena air berfungsi untuk membantu metabolisme tubuh., selain itu energi – energi yang ada di alam semesta sangat berfungsi untuk mendorong kemajuan peradaban manusia. Seperti minyak bumi yang digunakan sebagai bahan bakar, aspal yang digunakan untuk membuat jalan yang dilalui kendaraan.
Energi yang saat ini digunakan adalah energi yang tidak dapat diperbaharui
(fosil), oleh sebeb itu sangatlah penting untuk mengembangkan energi
terbarukan/energialternatif, di karenakan semakin menipisnya cadangan energi. Untuk itu sangatlah penting jika mengembangkan atau meng-konversi energi2 yang dapat diperbaharui / energi alternatif lainnya, seperti energi matahari, aingin, air laut, air itu sendiri, air tejun,tumbuhan dll.
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 7
Pada masa kita hidup sekarang ini, sebagai makluk hidup kita begitu tergantu pada mesin. Mesin membuat jarak di muka bumi ini menjadi tidak berarti. Baik hanya bertemu secara virtual maupun fisik.
Sementara itu, mesin sendiri hanyalah alat. Mesin hanya bisa berjalan kalau ada energi, tanpa energi tidak ada mesin, tidak ada mesin tidak ada kehidupan modern, oleh karena itu dalam peradaban modern ini Energi menjadi isu yang paling besar yang penguasanya di perebutkan dengan ketat oleh semua agam, perebutan kuasa atas sumber energi ini tidak jarang sampai menimbulkan perang.
Selama bertahun – tahun belakangan ini, bahan bakar fosil nyaris menjadi satu – satunya sumber energi di planet ini. Belakangan setelah penggunaan energi fosil dengan skala besar terutama dalam seabab terakhir ini, kita pun dihadapkan dengan berbagai masalah, ketika dibakar unutuk menghasilkan energi, bahan bakar fosil ini melepaskan karbon ke udara. Pelepasan karbon ini menyebabkan polusi dan merusak ozo, membuat bumi yang kita diami ini semakin panas, meningkatnya produksi karbon hasil pembakaran bahan bakar fosil ini belakangan disinyalir telah menyebabkan terjadinya pemanasan global (global warming). Meskipun fenomena pemanasan global ini masih di perdebatkan oleh beberapa ilmuwan.
Karena alasan itu, belakangan ini mulai kita lihat banyak penelitian tetntang energi terbarukan dengan lebih maksimal. Sumber energi terbarukan itu bisa berupa tenaga matahari, angin, air,panas bumi, bio massa bahkan gelombang laut.
Masih ada satu sumber energi lain yang sangat potensial menggantikan bahan bakar fosil sebagai sumber energi utama. Sumber energi alternatif pengganti bahan bakar fosil ini bernama hidrogen(h2) dibanding semua energi terbarukan seperti yang telah saa
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 8
sebut diatas, hidrogen memiliki beberapa keunggulan anatara lain ; bahan bakar hidrogen berfungsi sama seperti bahan bakar dari fosil kelebihannya hidrogen tidak akan menimbulkan polusi udara, karena ketika terbakar hidrogen melepas energi berupa panas dan mengahasilkan air sebagai bahan buangnya (2h2 + o2 - 2h20). Sama sekalai tidak mengeluarkan karbon. Jadi penggunaan hidrogen sebagai bahan bakar sangatlah membantu mengurangi polusi udara (meskipun pembakaran hidrogen sjuga menghasilkan polusi berupa nitrogen oksidasi dalam jumlah kecil ).
Sebagai perbandingan :
1 pound bensin yang dibakar pada suhu 25 derajat celcius dan tekanan 1 atm akan menghasilkan panas antara 44,5 kj/g – 47,5 kj/g.
1 pound solar menghasilkan panas antara 42,5 kj/ g – 44,5 kj/g
Hidrogen sendiri dalam kondisi yang sama (25 derajat celcius dan tekanan 1 atm dengan berat yang sama mampu menghasilkan panas 119,93 kj/g – 141, 86 kj/g
Yang berarti hampir 3 x lipat dari panas yang bisa dihasilkan oleh pembakaran bensin dan solar.
Keunggulan lain dari hidrogen adalah jumlahnyad\ dialam ini sangat melimpah, 93% dari seluruh atom yang ada dijagat raya ini adalah hidrogen.
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 9
Niels borh menerapkan teory kuantum terhadap model atom rutherford dengan mengasumsikan bahwa elektron – elektron bergerak pada orbit stasioner tertentu akibat adanya momentum anguler elektron – elektron tersebut. Model atom ini memungkinkan para ilmuwan untuk menghitung tingkat energi yang mungkin untuk orbit – orbit ini dan menghasilkan sebuah postulat bahwa emisi cahaya terjadi ketika sebuah elektron berpindah ke orbit yang energinya lebih rendah.
Meskipun pada tahun 1897 Thomson sudah menemukan elektron ,namun ukuran dan posisi elektron dalam suatu atom belum diketahui. Para ilmuwan berusaha menjelaskan bentuk atom dengan model dari yang paling sederhana sampai yang sangat rumit.
a. Teori atom Dalton.
Jauh sebelum Dalton mengemukakan teori atom, seorang filsuf yang bernama Demokritus (460-370 SM) sudah mengemukakan teori atom. Teori atom yang diajukannya tidak berdasarkan eksperimen namun didasarkan hasil pemikiran saja. Menurut Demokritus,atom adalah bagian terkecil suatu partikel/zat yang tak dapat dibagi-bagi lagi. Istilah atom berasal dari kata a yang berarti tidak dan tomos yang berarti dibagi sehingga atom mempunyai arti harfiah tak dapat dibagi. John Dalton (1766-1844),seorang ilmuwan Inggris, mengemukakan teori atomnya berdasarkan berbagai percobaan yang dilakukan ditambah kesimpulan dari percobaan orang lain. Teori atom Dalton berhasil menjelaskan peristiwa-peristiwa yang terjadi dalam reaksi kimia.
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 10
Rangkian dari teori atom Dalton, Thomson dan bohr adalah : a. Teori atom dalton
1. Atom adalah bagian dari suatu unsur atau zat yang tak dapat di bagi-bagi.
2. Atom dari unsur mempunyai bentuk yang serupa dan tidak mungkin berubah
menjadi unsur yang lain.
3. Dua atom atau lebih dari unsur yang berbeda dapat bergabung dalam reaksi
kimia membentuk suatu molekul. Sebagai contoh ,dua atom hidrogen dapat bergabung dengan atom oksigen menjadi molekul air lewat sebuah reaksi kimia.
4. Dalam reaksi kimia, berbagai atom unsur yang terlibat hanya sekedar memisahkan dan bergabung sedangkan massa keseluruhan tetap. Ide ini sesuai dengan hukum Lavoisier yang menyatakan massa sebelum reaksi sama dengan massa sesudah reaksi.
5. Dalam reaksi kimia, banyaknya atom yang bergabung dengan unsur lain mempunyai perbandingan yang tertentu dan sedsrhana. Gagasan ini sesuai dengan hukum Proust yang menyatakan bahwa perbandingan berat unsur-unsur yang menyusun suatu senyawa selalu tetap.
b. Teori atom Thomson
Model atom lain dikemukakan oleh Thomson. Sedikit berbeda dengan model atom sebelumnya, Thomson mengemukakan bahwa atom bukan merupakan seseuatu yang tidak dapat dibagi-bagi lagi. Pada atom terdapat sejumlah muatan negatif. Karena
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 11
secara keseluruhan atom adalah netral, maka muatan negatif tersebut akan diseimbangkan oleh
Muatan positif yang jumlahnya sama.
Menurut Thomsomn, atom mempunyai massa yang jauh lebih besar dibandingkan dengan massaelektron. Ini berarti muatan positif menjadi pusat massa sebuah atom. Sebagai ilustrasi model atom Thomson, jika diandaikan sebuah atom adalah semangka, sedangkan muatan positif atom adalah ''daging'' semangka.
c. Teori Atom Bohr
Model atom Bohr dikemukakan oleh Niels Bohr yang berusaha menjelaskan kestabilan atom dan spektrum garis atom hidrogen yang tidak dapat dijelaskan oleh model atom Rutherford. Model atom Bohr memuat tiga postulat sebagai berikut.
1. Di dalam atom hidrogen, elektron hanya dapat mengelilingi lintasan tertentu tertentu yang diijinkan tanpa membebaskan (melepaskan) energi. Lintasan ini disebut lintasan stasioner dan memiliki energi tertentu yang sesuai.
2. Elektron dapat berpindah dari satu lintasan ke lintasan yang lain. Energi dalam bentuk foton cahaya akan dilepaskan jika elektron berpindah ke lintasan yang lebih dalam, sedangkan Energi dalam bentuk foton cahaya akan diserapkan supaya elektron berpindah ke lintasan yang lebih luar. Energi dilepas atau diserap dalam paket sebesar hf sesuai dengan persamaan Planck.
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 12
Dimana h adalah konstanta Planck dan f adalah frekuensi cahaya atau foton yang dilepas atau diserap.
3. lintasan-lintasan stasioner yang diijinkan untuk ditempati elektron memiliki momentum sudut yang merupakan kelipatan bulat dari nilai
(nilai ini biasa ditulis juga sebagai ћ)
2.3. Sejarah HHO GENERATOR
Teknologi penghematan bahan bakar dengan menggunakan air in diawali dengan keberadaan dan perkembangan penggunaan alat bahan bakar air berupa kendaraan berbahan bakar air. (water car)yang telah dirilis sejak tahin 1908 oleh beberapa peneliti dan ilmuan – ilmuan berikut percobaan yang dilakukan oleh beberapa ilmuan dalam kaitannya dengan penggunaan air sebagai bahan bakar.
“Watercar” oleh Issac de Rivas‟‟
„‟ada tahun 1805 Isaac de Rivas berkebangsaan Swiss sebagai orang pertama yang menggunakan Hidrogen yang dihasilkan dari elektrolisa sebagai bahan bakar mesin dengan pembakaran internal, namun rancangannya belum memuaskan dan penemuan ini dikenal dengan “watercar”. Kemudian penelitian ini dikembangkan dan dilanjutkan oleh Luther Wattles dan Rudolf A Erren‟‟.
”BBA oleh Nicola Tesla dan Stanley Meyer‟‟
„‟Pada tahun 1943 kedua orang tersebut telah mengembangkan penggunaan bahan bakar air namun karena alasan bisnis hasil temuannya dihilangkan, bahkan bukan hanya
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 13
temuannya tetapi juga hasil penelitiannya, kemudian Nicola Tesla dipenjara dan dihukum mati tahun 1943 dan Stanley Meyer dari Amerika Serikat terbunuh tahun 1998”
“Brown Gas atau Yull Brown‟‟
”yang berasal dari Sydney Australia pada tahun 1974 berhasil mengembangkan BBA untuk menggerakkan mesin, bahan bakar air ini sebenarnya merupakan campuran gas hidrogen-hidrogen-oksigen yang dihasilkan dari elektrolisa air. Dalam tabung elektrolisa dipasang kumparan magnetik untuk memecahkan campuran air destilasi dan soda kue hingga menjadi campuran gas hidrogen-hidrogen-oksigen (HHO). Hidrogen bersifat eksplosif dan oksigen mendukung pembakaran, gas ini ditampung dalam tabung elektrolisa yang dialirkan kedalam ruang pembakaran mesin dan akan bercampur dengan gas hidrokarbon dari bahan bakar minyak, sehingga terjadi penghematan dalam tingkat yang signifikan‟‟
Lewat penemuan dan percobaan yang dilakukan tersebut, menjadi dasar acuan teknologi menghemat bahan bakar menggunakan air. Yaitu dengan proses elektrolisasi air yang menghasilkan hidrogen- hidrogen oksida (HHO) atau gas brown (berasal dari nama penemunya yull brown) yang dapat menghemat konsumsi bahan bakar pada kendaraan bermotor.
Jelang tahun 2006 ke tahun 2007 teknologi ini mulai berkembang pesat pada tahun 2008 teknologi ini makain banyak mendapat perhatian yang cukup besar dan beberapa negara sepeti india, jerman,afrika selatan, kanada, cinadan indonesia,
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 14
khususnya pada negara pecinta hemat bahan bakar di indonesia.cukup banyak juga beberapa peneliti yang melakukan eksperimen dengan teknologi ini. Seperti voll johanes bosco di palu, Ir. FX agus unggul santoso dosen sanata dharma, joko suprapto di jawa timur, dan beberapa penelitian dan kaum awan yang yang sudah mulai menerapkan dan meneliti teknologi penghematan bahan bakar ini.
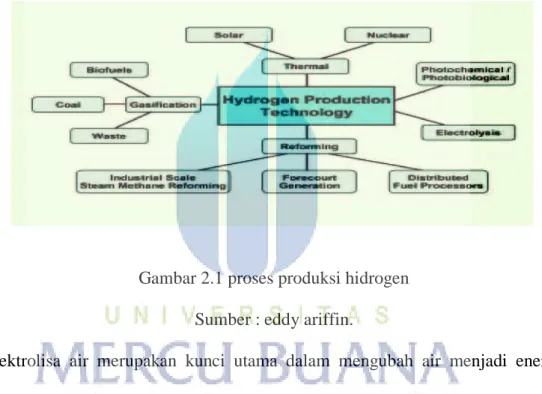
Gambar 2.1 proses produksi hidrogen Sumber : eddy ariffin.
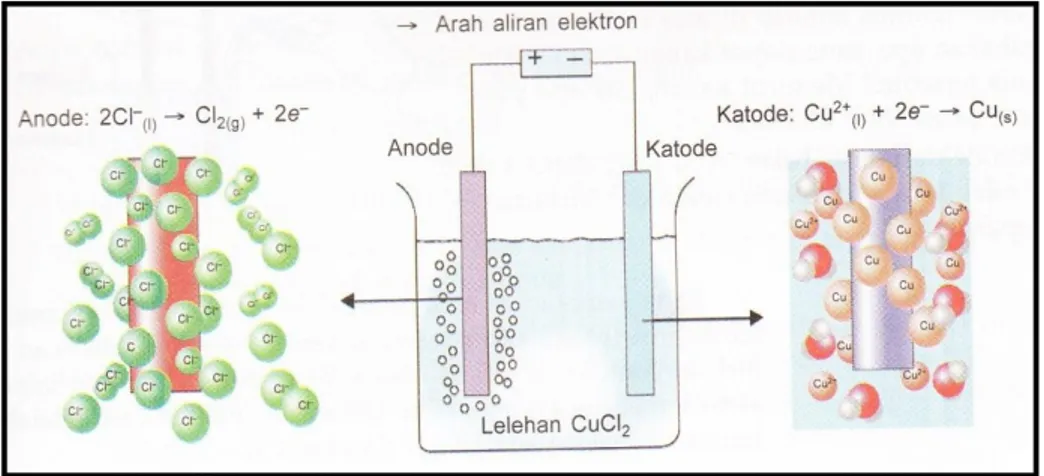
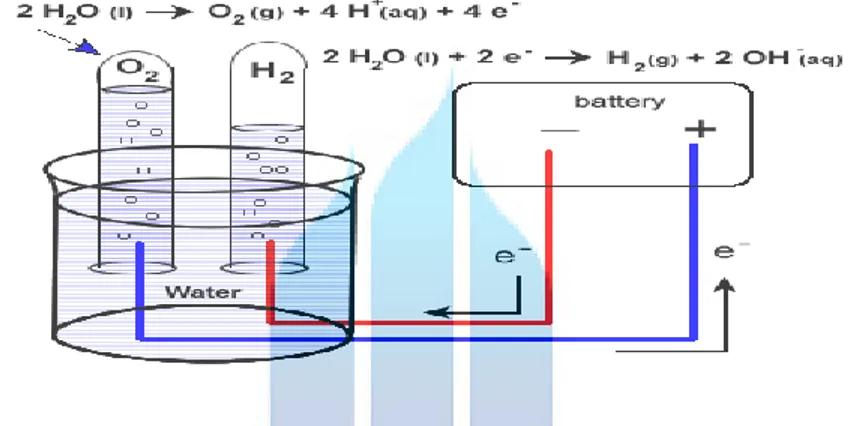
Elektrolisa air merupakan kunci utama dalam mengubah air menjadi energi. Dalam proses elektrolisis digunakan sumber energi yang berfungsi untuk memecah molekul H2O menjadi unsur-unsur asalnya. Pada katoda, dua molekul air bereaksi dengan menangkap dua elektron, dan akan tereduksi menjadi gas H2 dan OH-. Sedangkan pada anoda, dua molekul air terurai menjadi gas O2 dan melepaskan 4H+ serta mengalirkan elektron ke katoda. Ilustrasi tentang reaksi elektrolisis H2O dapat dilihat pada gambar dibawah. Pada proses elektrolisis ini, akan timbul gelembung berupa gas H2 yang dapat dikumpulkan menjadi energi.
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 15
Gambar 2.2. proses elektrolisis air Sumber :
http://kimia.upi.edu/staf/nurul/Web%202011/0800361/Proses%20Elektrolisis.html
2.4. Teknologi Elektrolisa HHO (Hydrogen-Oxygen)
Teknologi pemanfaatan air sebagai energi telah banyak dikembangkan, dari beberapa teknologi yang ada, semuanya menggunakan proses elektrolisis air sebagai prinsip dasarnya.
Hingga saat ini sudah ditemukan teknologi untuk memanfaatkan air sebagai energi yaitu fuel cell sistem HOD (Hydrogen Oxygen Demand) yaitu sistem pembangkit tenaga listrik dari hasil pencampuran H2 dengan O2 lansung pada saat listrik dibutuhkan, dan elektrolisa HHO (Hydrogen-Oxygen).
Teknologi elektrolisa HHO lebih murah dan lebih efisien. Teknologi optimalisasi air dengan fuel cell memiliki kelemahan terhadap biaya yang diperlukan dan efisiensi terhadap penerapannya. Sedangkan untuk sistem HOD memiliki kelemahan terhadap tingginya biaya yang diperlukan dan masih sulit untuk menampung
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 16
gas hidrogen dalam satu tempat. Perbandingan yang lebih lengkap tentang teknologi optimalisasi air sebagai alternatif energi dapat dilihat pada tabel berikut ini.
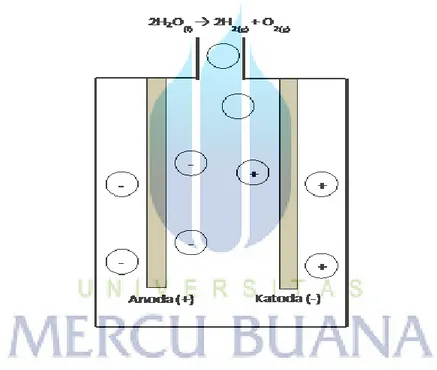
Sudah lebih dari 80 tahun proses elektrolisa ini dipergunakan secara komersial, seperti halnya penyepuhan emas, perak dan lain sebagainya. Prinsip Elektrolisa pada air biasa adalah untuk memecahkan ikatan kimia air (H2O) menjadi H2 dan O2, diperlukan tegangan listrik searah (DC), yg dialirkan melalui lempengan plat stainless.
Gambar 2.3 : prosese lektrolisasi air H2O
sumber : http://insentif.ristek.go.id/PROSIDING/RT-2012-0069.htm
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 17
Proses elektrolisis telah digunakan secara luas, tapi pemanfaatannya masih terbatas untuk kapasitas kecil, mengingat efisiensi termalnya yang sangat rendah. Namun demikian pada saat ini telah banyak peneliti yang berhasil meningkatkan efisiensi termal proses elektrolisis. Sel elektrolisis yang bekerja pada suhu dan tekanan tinggi, mampu memisahkan hidrogen dan oksigen dengan tingkat efisiensi yang signifikan
Pada prinsipnya, hidrogen bisa diperoleh dengan memecah senyawa yang paling banyak mengandung unsur hidrogen. Sampai saat ini, produksi hidrogen skala komersial yang paling maju adalah produksi hidrogen berbasis bahan bakar fosil dan air. Untuk produksi hidrogen dengan bahan baku bahan bakar fosil, steam reforming metana merupakan proses yang paling maju di dunia. Lebih dari 85% kebutuhan hidrogen dunia dipasok dengan sistem produksi steam reforming metana. Produksi hidrogen dengan bahan baku air yang sudah komersial adalah proses elektrolisis. Sayangnya, karena proses elektrolisis membutuhkan listrik dalam jumlah besar sebagai pemicu terjadinya reaksi, sehingga proses ini memberikan efisiensi termal total yang relatif rendah. Proses elektrolisis hanya bisa ekonomis jika tersedia listrik dalam jumlah besar dengan harga murah.
Dengan berjalannya waktu banyak penelitian dilakukan yang mengarah pada penyempurnaan, bahkan melebihi nilai standar dari perhitungan Faraday, sehingga menjadikan gas H2 lebih bermanfaat bagi kebutuhan manusia dalam menggunakan energi, karena H2 dapat diperoleh dari air dan air cukup banyak ada dimana-mana,
sehingga dapat dikatakan bahwa H2 adalah sumber energi masa depan yang
berkelimpahan dan murah. Berdasarkan penelitian akhir-akhir ini dapat disimpulkan bahwa kegunaannya gas hydrogen bagi masyarakat luas dapat diterapkan untuk untuk
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 18
kompor rumah tangga, dan pemanas ruangan serta di industri pada burner, uap air panas (steam), metode pengelasan dan lain sebagainya.
Melalui berbagai penelitian, maka gas hydrogen dapat memenuhi kebutuhan energi nasional yang merupakan energy masa depan yang dapat digunakan oleh sebagian besar untuk moda transportasi yang diprediksi akan menyongsong era energi berbasis hidrogen yang diramalkan akan tercapai pada dasawarsa 2050.
Elektrolisa ada 2 macam:
- Elektrolisa basah (wet cell electrolyse) : yaitu lempengan plat kathoda Dan Anoda dicelupkan kedalam air
- Elektrolisa kering (Dry cell electrolyse = Drycell) : disini lempengan plat Kathoda dan Anoda berada disebelah luar dan airnya disebelah dalam.
Alat yang akan telah kami buat adalah elektrolisa kering (dry cell electroda = dry cell).
2.5.1. Elektrolisa basah (wetcell electrolyse)
Elektrolisa Basah adalah elektrolisa yang biasa digunakan sampai saat ini, yaitu dengan memasukan kedua plat kondensator tersebut kedalam air destilasi atau air RO (Reverse Osmosis = air murni), apabila kedua elektroda tersebut diberi tegangan listrik maka akan terjadi proses pemisahan H2 dan O2, kemudian hasil H2 tersebut perlu dihitung dan di-data dari hasil percobaan, selain itu perlu diteliti variabel yang mempengaruhi produksi H2 tersebut, sehingga dapat diambil kesimpulan penggunaan elektrolisa yang paling efisien & efektif.
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 19
Elektrolisa Basah adalah dengan memasukan kedua plat kondensator tersebut kedalam air destilasi atau air - RO (Reverse Osmosis = air murni), apabila kedua elektroda tersebut diberi tegangan listrik maka akan
terjadi proses pemisahan H2 dan O2, kemudian hasil H2 tersebut perlu dihitung dan di-data dari hasil percobaan, selain itu perlu diteliti variable variabel yang mempengaruhi produksi H2 tersebut, sehingga dapatdi ambil kesimpulan penggunaan elektrolisa yang paling efisien & efektif.
Keuntungan generator gas HHO tipe wet cell adalah :
1. Gas yang dihasilkan umumnya lebih banyak dan stabil. 2. Perawatan generator lebih muda.
3. Rancangan bangun pembuatan generator lebih mudah.
pada tipe wet cell atau tipe basah, area luasan elektroda platnya terendam air untuk proses elektrolisis menghasilkan gas HHO.
2.5.2. Elektrolisa kering (Drycell electrolyse = Drycell)
Elektrolisa Kering (Dry electrolyze) adalah pada proses ini plat kondensotornya tidak direndam kedalam larutan akan tetapi plat nya berada disebelah luar dan larutannya didalam plat tersebut.
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 20
Gambar 2.4. generator hydrogen system drycell Sumber : http://hho4save.blogspot.com/feeds/posts/default
Pada proses Dry cell panas yang ditimbulkan oleh plat kondensator dapat
dibuang langsung keluar, sehingga tidak membuat larutan menjadi lebih panas, dibandingkan dengan elektrolisa biasa atau elektrolisa basah (Wet Electrolyze).
Keuntungan generator HHO tipy dry cell adalah :
1. air yang di elektrolisa hanya seperlunya, yaitu hanya air yang terjebak diantara lempengan cell
2. Panas yang ditimbulkan relative kecil karena selalu terjadi sirkulasi antara air panas dan air dingin di reservoir
3. Arus listrik yang digunakan relatif lebih kecil, karena daya yang terkonversi menjadi semakin panas semakin sedikit.
Besarnya plat elektroda yang terendam air adalah area terjadinya elektrolisis untuk menghasilkan gas HHO.
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 21
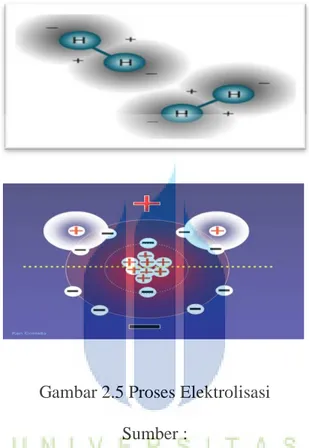
Rumus Kimia pada proses Elektrolisa :
Gambar 2.5 Proses Elektrolisasi Sumber :
http://ecopowerbooster.blogspot.com/2012/04/air-elektrolisis-air-dan-hidrogen.html / eddy ariffin
Pada elektroda Kathoda terjadi penambahan elektron (e−), sehingga reaksi kimia yang terjadi sbb;
Kathode (reduksi): 2H+(cair) + 2e− → H2(gas)
Sedangkan pada elektroda Anoda, terjadi proses oxidasi dimana pelepasan elektron yang bergerak kearah elektroda kathoda, reaksi kimia pada Anoda sbb;
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 22
Anode (oxidasi) : 2H2O(l) → O2(gas) + 4H+(cair) + 4e− ; (l = Larutan) Reaksi kimia penye-imbangan, reaksi air dengan larutan basa sbb :
Kathode (reduksi): 2H2O(l) + 2e− → H2(gas) + 2OH−(cair) Anode (oxidasi) : 4OH−(cair) → O2(gas) + 2H2O(l) + 4e−
Gambar 2.6 rumusan kimia pada elektroklisa air(H2O) Sumber : Eddy Ariffin Dpl. Ing
Bahwa pemisahan air (H2O) akn menjadi:
2H2O(l) 2H2(gas) + O2(gas) →H2O(liquid) disebut HHO HHO adalah bahasa yang telah digunakan kalangan peneliti HIDROGEN. Elektrolisa Air akan menghasilkan Gas HHO:
1 Liter Air = 1,750 Liter Gas
Bentuk Gas HHO yang terjadi ada 14 macam
Flame Speed 1,300 M/S pada kondisi Vakum (Pabs = – 820 mmHg) Self Ignite: t = 550 oC pada P = 15 Psi
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 23
1. Proses elektrolisa air dapat menjadikan ;
1 liter air menghasilkan 1,750 liter gas HHO, sehingga dapat dikatakan bahwa bahan bakar berasal dari air merupakan bahan bakar gas yang diproduksi pada saat diperlukan (HHO gas on demand) tanpa harus menyimpannya pada tabung yang besar dan tidak harus ada kebocoran gas yang dapat memungkinkan terjadinya ledakan pada gas. Dalam penggunaan gas HHO pada kendaraan bermotor, memiliki dua macam bahan bakar (dual fuel) yang masuk keruang bakar secara bersamaan yaitu bensin atau diesel dengan gas HHO, sehingga penggunaan bahan bakar utama berkurang dari seharusnya (hemat bahan bakar) dengan atau tanpa mengurangi tenaga mesin, bahkan menambah tenaga mesin yang disebabkan oleh kecepatan bakar (flame speed) gas H2 yang sangat besar (130 m/s), sehingga seluruh bahan bakar yang berada diruang bakar habis terbakar oleh karena itu emisi gas buang juga menurun dan ramah lingkungan.
2. Standar produksi gas HHO
standar yang dapat dijadikan acuan adalah berdasarkan hasil penelitian Faraday yaitu: 1 liter gas HHO per jam memerlukan catu daya sebesar 2,36watt atau 1/60liter per menit (16,6cc), standar ini dijadikan 100% produktivitas gas HHO.
3. Luas permukaan plat elektrolisa
yang dapat berproduksi dengan sempurna adalah: 1 cm2 memerlukan 0,24 Ampere atau 1 Ampere = 4 cm2 , dari perhitungan ini dapat dirancang besarnya
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 24
plat yang diperlukan sesuai dengan besarnya arus listrik yang akan dibebankan pada plat.
4. sel elektrolisa
yaitu 1 sel positif dan 1 sel negatif memerlukan tegangan 1,23 Volt dan ditambah dengan kehilangan efisiensi sehingga tegangan maximal adalah 2 Volt, diatas 2 Volt terjadi panas.
Satu unit HHO generator terdiri dari :
Generator hydrogen, ( 2N4.15 , 2N4.20, atau 2N5.15, 2N5.20 )
Tanki reservoir untuk larutan katalis ( aquades dan KOH ) kapasitas 1 liter, berfungsi juga sebagai bubler pertama.
Slang plastic transparan 2 meter
Relay switch 30 A, Fuse /sekering 30A, kabel 2 meter, pipa kapiler tembaga 2mm, Kalium hydroxide (KOH) untuk 1 liter aquades.
Tabung Bubbler dan Check valve.
Dry Cell ada 2 type, Di sesuaikan dengan kebutuhan mesin.
1. 2N4.15 –plat Stainless steel 304, 11 plat, 4 netral, luas plat 15X15 cm Hydrogen yang dihasilkan : 0,6 -1,1 LPM pada arus listrik : 5-12,5 ampere dan tegangan : 13,5 volt, mmw : 5,2
Program Studi Teknik Mesin
Universitas Mercubuana Jakarta 25
2. 2N4.20 –plat Stainless steel 304, 11 plat, 4 netral, luas plat 20X20 cm. Hydrogen yang dihasilkan : 0,8 – 2,2 LPM pada arus listrik : 5 – 26 Ampere dan tegangan : 13,5 volt, mmw : 6,2