SITOTOKSISITAS FRAKSI PROTEIN DAUN MIMBA (Azadirachta indica A. Juss) FP30, FP40, FP50, dan FP60 TERHADAP
KULTUR SEL SIHA
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh: Bertha Mellina NIM : 038114116
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2007
Just Be
Be strong enough to face the world each day
Be weak enough to know you cannot do everything alone Be generous to those who need your help
Be frugal with what you need yourself
Be wise enough to know that you do not know everything Be foolish enough to believe in miracles
Be willing to share your joys
Be willing to share the sorrows of others Be a leader when you see a path others have missed
Be a follower when you a shrouded in the midst of uncertainty
Be the first to congratulate an opponent who succeeds Be the last to criticize a colleague who fails Be sure of your final destination, in case you are
going the wrong way
Be loving to those who love you
Be loving to those who do not love you, and they may change
Above all, be yourself
Ku persembahkan karyaku ini kepada: Tuhan dan Bunda Maria yang telah membimbing aku, Bapak dan ibu yang telah sabar mendidikku, mendukungku dan
mengiring setiap langkahku dengan doa tulus ikhlasnya, serta Lisa dan Linda yang terkasih, untuk sesorang yang telah mengisi hatiku dan
untuk almamaterku.
PRAKATA
Puji syukur kepada Tuhan Yang Maha Esa atas berkat rahmat dan
anugerahnya, sehingga penulis bisa menyelesaikan skripsinya yang berjudul “
Sitotoksisitas Fraksi Protein Daun Mimba (Azadirachta indica A. Juss) FP30, FP40,
FP50,dan FP60terhadap Kultur Sel SiHa”. i
Selesainya skripsi ini tidak lepas dari bantuan banyak pihak. Oleh karena
itu itu penulis ingin sekali mengucapkan terima kasih kepada:
1. Drs. A. Yuswanto S.U., Ph.D., Apt., selaku dosen pembimbing yang telah
banyak meluangkan waktu, tenaga dan atas segala masukan serta sarannya
dalam penyusunan skripsi ini.
2. Drs. Mulyono, Apt, selaku dosen penguji atas segala arahan, kritik, saran dan waktunya.
3. dr. Luciana Kuswibawati, M.Kes., selaku dosen penguji atas segala arahan,
kritik, saran dan waktunya.
4. Rita Suhadi, MSi, Apt selaku dekan Fakultas Farmasi Universitas Sanata
Dharma.
5. Mbak Yuli, Pak Rajiman dan segenap teknisi Laboratorium Ilmu Hayati
Universitas Gadjah Mada yang telah membantu jalannya penelitian sehingga
dapat terselesaikan dengan baik.
6. Orang tua dan adik-adikku tercinta atas doa dan dukungannya selama ini.
7. R. Ari Sidharta atas perhatian, bantuan, dukungan dan kebersamaan selama
ini.
8. Sari, Ana, Vita, Lusi, Jeny, Ndari, Lea, atas kebersaman dan kerjasamanya
selama penelitian.
9. Icha, Mila, Vita,Avi, Sinta, dan teman-teman kost buat kebersamaannya
selama ini.
10.Shinta, Ari, Wenny, Melin, Eka, Mellisa, Willy, Rinto, Galaeh, Agnes dan
teman- teman kelas C angkatan 2003 atas persahabatan yang indah.
11.Semua pihak yang telah banyak membantu penyusunan skripsi ini.
Harapan penulis karya ini bermanfaat dan dapat mendorong mahasiswa
angkatan berikutnya untuk berkarya lebih baik bagi kemajuan dunia farmasi di
Indonesia. Oleh karena itu penulis menerima saran dan kritik yang membangun
guna tercapainya kesempurnaan tulisan ini.
INTISARI
Banyak studi dilakukan untuk memperoleh senyawa-senyawa baru yang memiliki aktivitas antikanker, termasuk dari bahan-bahan alam. Satu diantaranya adalah tanaman mimba (Azadirachta indica A. juss). Daun mimba banyak digunakan untuk mengatasi berbagai penyakit dan diperkirakan mempunyai efek sebagai antikanker. Penelitian ini bertujuan untuk mengetahui apakah fraksi protein daun mimba FP30, FP40, FP50, FP60 dapat dikembangkan sebagai antikanker.
Penelitian ini termasuk penelitian eksperimental murni dengan rancangan acak, lengkap, dengan pola satu arah. Metode yang digunakan adalah uji sitotoksisitas fraksi protein daun mimba FP30, FP40, FP50, FP60 terhadap sel SiHa dan sel Vero. Efek sitotoksik fraksi protein daun mimba FP30, FP40, FP50, FP60 terhadap sel SiHa dan sel Vero menggunakan metode MTT (3,(4,5-dimetiltiazoldifeniltetrazolium bromide). Data yang diperoleh berupa persen kematian sel yang kemudian diolah dengan menggunakan analisis probit dan uji T sampel independen.
Hasil penelitian menunjukkan bahwa harga LC50 yang diperoleh dari fraksi protein daun mimba FP30, FP40, FP50, dan FP60 terhadap sel SiHa berturut- turut adalah sebesar 0,38 μg/ml; 0,45 μg/ml, 0,72 μg/ml, 0,79μg/ml. Harga LC50 untuk FP30, FP40, FP50, dan FP60 terhadap sel vero berturut- turut adalah 0,01 μg/ml; > 1 g/ml; 0,03 μg/ml; 0,05 μg/ml. Hasil uji t padaFP30, FP50, dan FP60 menunjukkan bahwa LC50 sel SiHa berbeda tidak bermakna dengan LC50 sel Vero (sig.>0,05). Hal ini berarti fraksi protein daun mimba FP30, FP50, dan FP60 memiliki kemampuan yang sama untuk menginduksi kematian sel SiHa dan sel Vero, sehingga tidak dapat dikembangkan sebagai antikanker. Sedangkan pada FP40 dapat dikembangkan sebagai senyawa antikanker.
Kata kunci: sitotoksisitas, fraksi protein, daun mimba, sel SiHa, sel Vero, LC50
ABSTRACT
Many studies has been done to gain new active compound which have anticancer activity, including from natural resources. One of them is neem plant (Azadirachta indica A. juss). The neem leaves are used to cure a lot of diseases and suspected have anticancer activity. The objective of this research is to know whether neem leaves protein fraction FP30, FP40, FP50 and FP60 can be developed to become anticancer or not.
This research was a pure experiment with one-way completely randomized design. The method which is used is cytotoxicity test od neem leaves protein fration FP30, FP40, FP50 and FP60 against SiHa cells and Vero cells. The cytotoxic effects of neem leaves protein fraction FP30, FP40, FP50 and FP60 against SiHa cells and Vero cells used MTT (3,(4,5-dimetiltiazoldifeniltetrazolium bromide) method. The obtained data (percentage of the death cells) are analyzed with probit test and independent sample T-test.
The result of the research showed that LC50 value, obtained from neem leaves protein fraction FP30, FP40, FP50 and FP60 against the SiHa cells continuously 0,38 μg/ml; 0,45 μg/ml; 0,72μg/ml; 0,79 μg/ml. The LC50 value for FP30, FP40, FP50 dan FP60 against the Vero cells continuously 0,01 μg/ml; > 1 g/ml; 0,03 μg/ml; 0,05 μg/ml. The T-Test result in FP30, FP50 and FP60 showed that LC50 SiHa cells different unsignificant with LC50 Vero cells (sig>0,05). From the LC50 value indicate that protein fraction of mimba’s leaf PF40 have potency to be developed as anticancer.
Key word: cytotoxicity, protein fraction, neem leaves, SiHa cells, Vero cells, LC50
DAFTAR ISI
Halaman
HALAMAN JUDUL... . i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
PRAKATA... vi
INTISARI... viii
ABSTRACT... ix
DAFTAR ISI... x
DAFTAR TABEL... xiv
DAFTAR GAMBAR ... xvi
DAFTARLAMPIRAN... xvii
ARTI SINGKATAN DAN ISTILAH PENTING……….. xviii
BAB I PENDAHULUAN ... 1
A. Latar Belakang ... 1
1. Permasalahan ... 3
2. Keaslian karya... 3
3. Manfaat penelitian... 4
B. Tujuan Penelitian… ... 4
1. Tujuan umum…… ... 4
2. Tujuan khusus………. 4
BAB II PENELAAHAN PUSTAKA... 6
A. Tanaman Mimba (Azadirachta indica A. Juss)... 6
1. Keterangan Botani... 6
2. Kandungan kimia ... 6
3. Khasiat dan penggunaan ... 6
4. Deskripsi ... 6
B. Protein………. ... 7
C. Kanker… ... 10
D. Kultur Sel. ………... 14
E. Sel Vero ... 15
F. Uji Sitotoksisitas ... 15
G. MekanismeSenyawa Antikanker ... 17
H. Landasan Teori ... 17
I. Hipotesis... 18
BAB III METODOLOGI PENELITIAN ... 19
A. Jenis dan Rancangan Penelitian... 19
B. Variabel Penelitian dan Definisi Operasional... 19
1. Variabel bebas... 19
2. Variabel tergantung... 19
3. Variabel pengacau terkendali... 19
4. Variabel pengacau tak terkendali ... 19
5. Definisi operasional ... 20
C. Alat dan Bahan ... 20
1. Alat ... 20
2. Bahan ... 20
D. Tata Cara Penelitian ... 21
1. Determinasi tanaman... 21
2. Pengumpulan daun mimba... 22
3. Sterilisasi alat dan bahan... 22
4. Preparasi fraksi protein daun mimba ... 22
5. Pengukuran kadar protein dengan spektrofotometri UV ... 24
6. Propagasi dan panen sel SiHa ... 24
7. Propagasi dan panen sel Vero………... 25
8. Uji sitotoksisitas fraksi protein daun mimba pada sel SiHa... 26
9. Uji sitotoksisitas fraksi protein daun mimba pada sel Vero... 27
E. Analisis Hasil... 28
BAB IV HASIL DAN PEMBAHASAN ... 29
A. Determinasi Tanaman ... 29
B. Sterilisasi Alat dan Bahan ... 29
C. Preparasi Sampel Fraksi Protein Daun Mimba ... 30
D. Pengukuran Kadar Protein dengan Metode Spektrofotometri UV ... 32
E. Uji SitotoksisitasFraksi Protein Daun Mimba... 33
BAB V. KESIMPULAN DAN SARAN... 42
A. Kesimpulan ... 42
B. Saran... 42
DAFTAR PUSTAKA ... 43
LAMPIRAN... 46
BIOGRAFI PENULIS ... 87
DAFTAR TABEL
Halaman Tabel I. Data absorbansi fraksi protein dengan menggunakan
metode spektrofotometer UV dan rasio serapan pada
panjang gelombang 280 nm dan 260 nm ... 33
Tabel II. Hasil uji sitotoksisitas fraksi protein terhadap
sel SiHa ……….………. 36
Tabel III. Hasil uji sitotoksisitas fraksi protein terhadap
sel Vero……….……….. 37
Tabel IV. Harga LC50 fraksi protein daun mimba terhadap
sel SiHa……….……….. 39
Tabel V. Hasil LC50 fraksi protein daun mimba terhadap
sel Vero……….……… 39
Tabel VI. Data absorbansi fraksi protein dengan menggunakan
metode spektrofotometer UV dan rasio serapan pada
panjang gelombang 280 nm dan 260 nm ...47
Tabel VII. Hasil Uji sitotoksisitas fraksi protein daun mimba FP30
terhadap kultur sel SiHa... 48
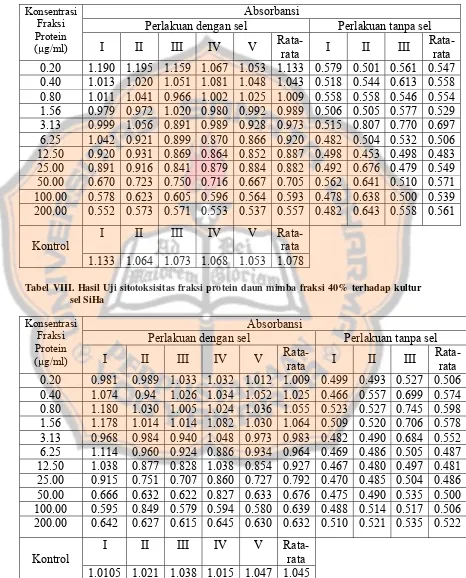
Tabel VIII. Hasil Uji sitotoksisitas fraksi protein daun mimba FP40
terhadap kultur sel SiHa... 48
Tabel IX. Hasil Uji sitotoksisitas fraksi protein daun mimba FP50
terhadap kultur sel SiHa... 49
Tabel X. Hasil Uji sitotoksisitas fraksi protein daun mimba FP60
terhadap kultur sel SiHa... 49
Tabel XI. Hasil Uji sitotoksisitas fraksi protein daun mimba FP30
terhadap kultur sel Vero... 50
Tabel XII. Hasil Uji sitotoksisitas fraksi protein daun mimba FP40
terhadap kultur sel Vero...50
Tabel XIII. Hasil Uji sitotoksisitas fraksi protein daun mimba FP50
terhadap kultur sel Vero...50
Tabel XIV. Hasil Uji sitotoksisitas fraksi protein daun mimba FP60
terhadap kultur sel Vero...51
DAFTAR GAMBAR
Halaman
Gambar 1. Sel SiHa dan Sel Vero tanpa perlakuan …………..…... 33
Gambar 2. Kultur sel SiHa yang diberi perlakuan fraksi protein daun mimba ………...……… 34
Gambar 3. Kultur sel Vero yang diberi perlakuan fraksi protein daun mimba ………...……… 34
Gambar 4. Reaksi Pembentukan Kristal Formazan... 35
Gambar 5. Kristal Formazan di Bawah Mikroskop ... 35
Gambar 6. Grafik Persen kematian sel SiHa vs konsentrasi fraksi protein daun mimba ………...……… 37
Gambar 7. Grafik Persen kematian sel SiHa vs konsentrasi fraksi protein daun mimba ………...……… 38
Gambar 8. Foto tanaman mimba …………... 83
Gambar 9. Foto daun mimba …………... 83
Gambar 10. Foto ELISA reader SLT 340ATC…………... 84
Gambar 11. Foto Spektrofotometer UV …………... 84
Gambar 12. Foto Sentrifuse KPLC Series …………... 85
DAFTAR LAMPIRAN
Halaman Lampiran 1. Jumlah penambahan amonium sulfat... .. 46
Lampiran 2. Cara Perhitungan Kadar Protein ... 47
Lampiran 3. Absorbansi Sel dengan Metode MTT... 48
Lampiran 4. Hasil analisis probit fraksi protein daun mimba
(Azadirachta indica A. Juss) terhadap kultur sel SiHa
dengan metode MTT………....…… 52
Lampiran 5. Hasil analisis probit fraksi protein daun mimba
(Azadirachta indica A. Juss) terhadap kultur sel vero
dengan metode MTT………....…… 63
Lampiran 6. Uji distribusi data dengan Kolmogorov- Smirnov
pada sel SiHa dan sel Vero………….……… 74
Lampiran 7. Hasil Uji Signifikansi LC50 antara Sel SiHa
dan Sel Vero dengan Analisis Statistik ……… 78
Lampiran 8. Perhitungan nilai kolerasiLC50 Sel SiHa dan Sel Vero
pada Taraf Kepercayaan 95%……….……….. 81
Lampiran 10. Foto tanaman dan daun mimba... 82
Lampiran 11. Foto ELISA reader, Spektrofotometer UV, dan Sentrifuge... 83
Lampiran 12. Surat Determinasi Tanaman ………... 86
ARTI SINGKATAN DAN ISTILAH ASING
FBS : Fetal Bovine Serum
FP : Fraksi Protein
LC50 : Lethal Concentration 50%
MTT : 3-(4,5-dimetil-tiazol-2-il)-2,5-dipheniltetrazolium bromid )
reagen Stopper : reagen yang terdiri dari larutan SDS 10% dalam HCl 0,01N
RPMI : Rosswell Park Memorial Institute
SDS : Sodium Dodesil Sulfat
tissue culture flask : tempat untuk menumbuhkan sel, berbentuk botol dengan
leher bengkok
96 well plate : sumuran mikro yang terdiri dari 96 lubang tempat
menanam sel pada uji sitotoksisitas
FP30 : fraksi protein yang diendapkan dengan larutan amonium
sulfat dengan kadar 30% dari kadar ammonium sulfat jenuh
FP40 : fraksi protein yang diendapkan dengan larutan amonium
sulfat dengan kadar 40% dari kadar ammonium sulfat jenuh
FP50 : fraksi protein yang diendapkan dengan larutan amonium
sulfat dengan kadar 50% dari kadar ammonium sulfat jenuh
FP60 : fraksi protein yang diendapkan dengan larutan amonium
sulfat dengan kadar 60% dari kadar ammonium sulfat jenuh
BAB I PENDAHULUAN
A. Latar Belakang
Penyakit kanker menempati urutan kedua di Amerika setelah penyakit
jantung, sedangkan di Indonesia penyakit kanker menempati urutan keenam
setelah penyakit jantung. Menurut Organisasi Kesehatan Dunia, World Health
Organization (WHO) dalam 10 tahun mendatang diperkirakan 9 juta orang akan
meninggal setiap tahun akibat kanker. Di negara-negara industri sekitar satu dari
lima orang meninggal karena tumor ganas. Saat ini kanker dengan demikian
merupakan salah satu penyebab kematian yang paling sering terjadi dan kasus
penderita kanker senantiasa bertambah (Nafrialdi dan Sulistya, 1995). Penyakit
yang diderita oleh sekitar tujuh juta orang lebih ini menjadi penyakit yang paling
ditakuti oleh semua orang.
Pengobatan kanker dilakukan dengan cara operasi, penyinaran, dan
kemoterapi, menggunakan obat-obat sintetik maupun menggunakan obat-obat
tradisional. Obat-obat yang termasuk obat-obat sintetik memiliki toksisitas tinggi,
selain itu obat sintetik juga memiliki efek samping yang tinggi pula. Oleh karena
itu perlu dikembangkan obat antikanker dari bahan alami yang memiliki efek
samping yang relatif kecil daripada obat antikanker sintetik (Mulyadi, 1996).
Salah satu tanaman yang telah terbukti memiliki kegunaan sebagai obat
antikanker adalah tanaman mimba. Tanaman mimba secara tradisional telah
dikenal oleh masyarakat sebagai tanaman obat alami untuk mengobati berbagai
penyakit, diantaranya tukak lambung, cacar air, penyakit kulit, penyakit lepra,
penyakit kuning, bisul, atau borok, dll (Anonim,2006e). Daun mimba diteliti
sebagai antikanker dalam penelitian yang berjudul “Sitotoksisitas Fraksi Protein
Daun Mimba (Azadirachta indica A. Juss) Hasil Pengendapan dengan
Ammonium Sulfat 30%, 60%, dan 100% Jenuh terhadap Kultur Sel SiHa (Candra,
2006)”. Penelitian Candra (2006) menyebutkan bahwa harga LC50 fraksi protein
daun mimba hasil pengendapan dengan amonium sulfat 30%, 60% dan 100%
jenuh berturut-turut adalah sebesar 1,72 μg/ml; 0,04 μg/ml; dan 32,56 μg/ml.
Menurut NCI (National Cancer Institute) suatu senyawa berpotensi sebagai
antikanker bila harga LC50 ≤ 20 µg/ml (Suffnes and Pezzuto, 1991). Dengan
demikian, dapat disimpulkan bahwa fraksi protein 60% berefek paling sitotoksik
terhadap sel SiHa dan fraksi protein 30% dan 60% diperkirakan memiliki aktivitas
sebagai antikanker.
Dari hasil penelitian tersebut diduga bahwa fraksi protein daun mimba
yang lebih spesifik yaitu antara fraksi protein daun mimba 30% dan 60% jenuh
juga mempunyai efek sitotoksik terhadap sel SiHa dan diperkirakan memiliki
aktivitas sebagai antikanker. Hal tersebut yang mendasari dilakukannya penelitian
dengan cara fraksinasi protein daun mimba dengan pengendapan menggunakan
amonium sulfat FP30, FP40, FP50,dan FP60 terhadap kultur sel SiHa untuk
mengetahui fraksi protein mana yang menghasilkan efek sitotoksik paling besar
Hasil yang didapatkan dari penelitian ini diharapkan dapat menambah
pengetahuan tentang khasiat dan kegunaan tanaman mimba, juga untuk
memberikan informasi sitotoksik dari daun mimba terhadap sel kanker.
1. Rumusan masalah
Berdasarkan latar belakang dari penelitian timbul berbagai permasalahan, yaitu :
a. fraksi protein daun mimba (Azadirachta indica A. Juss) FP30, FP40, FP50,dan
FP60, manakah yang mempunyai efek sitotoksisitas paling besar terhadap sel
SiHa?
b. seberapa besar nilai LC50 dari fraksi protein daun mimba (Azadirachta indica
A. Juss) FP30, FP40, FP50,dan FP60 terhadap sel SiHa?
c. apakah fraksi protein daun mimba (Azadirachta indica A. Juss) FP30, FP40,
FP50,dan FP60, juga memiliki efek sitotoksisitas terhadap sel Vero?
d. apakah fraksi protein daun mimba (Azadirachta indica A. Juss) FP30, FP40,
FP50,dan FP60 memiliki efek sitotoksisitas sehingga berpotensi untuk
dikembangkan sebagai antikanker?
2. Keaslian Karya
Sebelumnya telah dilakukan penelitian mengenai “Sitotoksisitas Fraksi
Protein Daun Mimba (Azadirachta indica A. Juss) Hasil Pengendapan dengan
Amonium Sulfat 30%, 60%, dan 100% Jenuh terhadap Kultur Sel SiHa (Candra,
2006)”. Sejauh ini, penulis belum menemukan adanya penelitian mengenai
sitotoksisitas fraksi potein daun Mimba (Azadirachta indica A. Juss) FP30, FP40,
3. Manfaat Penelitian
a. Manfaat teoritis
Penelitian ini diharapkan dapat melengkapi dan memperkaya
informasi yang telah ada mengenai khasiat, penggunaan dan efek
sitotoksisitas fraksi protein daun mimba terhadap kultur sel SiHa dan sel
Vero.
b. Manfaat praktis
Penelitian ini diharapkan dapat memberikan alternatif untuk
pengobatan kanker dengan menggunakan bahan dari alam.
B. Tujuan Penelitian
1. Tujuan Umum
Penelitian ini bertujuan untuk mengetahui apakah fraksi protein daun
Mimba (Azadirachta indica A. Juss) FP30, FP40, FP50,dan FP60 berpotensi
sebagai antikanker.
2. Tujuan khusus dari penelitian ini adalah :
a. untuk mengetahui fraksi protein daun mimba (Azadirachta indica A. Juss)
FP30, FP40, FP50,dan FP60 yang mempunyai efek sitotoksisitas paling besar
terhadap sel SiHa.
b. untuk mengetahui nilai LC50 dari fraksi protein daun mimba (Azadirachta
c. untuk mengetahui apakah fraksi protein daun mimba (Azadirachta indica
A. Juss) FP30, FP40, FP50,dan FP60, juga memiliki efek sitotoksisitas
terhadap sel Vero.
d. untuk mengetahui apakah fraksi protein daun mimba (Azadirachta indica
A. Juss) FP30, FP40, FP50,dan FP60 memiliki efek sitotoksisitas sehingga
BAB II
PENELAAHAN PUSTAKA
A. Azadirachta indica A. Juss
1. Keterangan Botani
Daun mimba (Azadirachta indica A. Juss) merupakan divisi
spermatophyta dan termasuk dalam kelas dikotiledon, famili Meliaceae, Genus
Azadirachta, Spesies Azadirachta indica A. Juss, Sinonim Melia azadirachta Linn
(Backer dan Backuizen van den Brink, 1965; Hutapea, 1993).
2. Kandungan kimia
Daun mimba mempunyai kandungan azadirachtin, nimbin, nimbinene,
nimbandiol, nimbolide, quercetin, dan margosin (Anonim,2006a).
3. Khasiat dan penggunaan
Tanaman mimba secara tradisional digunakan oleh masyarakat untuk
mengobati bisul atau borok, penyakit kuning, penyakit kulit, tukak lambung, dll.
Daun mimba dapat menghilangkan toksin, membersihkan darah, dan mencegah
kerusakan karena senyawa radikal bebas dalam tubuh. (Anonim,2006e).
4. Deskripsi
Tanaman mimba berupa pohon dengan tinggi 10-15 meter. Batang tegak,
berkayu, bulat, permukaan kasar, percabangan simpodial, dan berwarna coklat.
Daun berwarna hijau, majemuk, berhadapan, lonjong, melengkung, tepi bergerigi,
ujung lancip, pangkal meruncing, pertulangan menyirip, panjang 5-7 cm, lebar 3-4
berkelamin dua, terletak di ujung cabang, bertangkai silindris, panjang 8-15 cm,
kelopak hijau, mahkota halus, benang sari silindris berwarna putih kekuningan,
putih lonjong, dan coklat muda. Buah berwarna hijau, berbentuk bulat telur, dan
buni. Biji berbentuk bulat, berwarna putih, dan mempunyai diameter 1 cm.
Tanaman mimba mempunyai akar tunggang yang berwarna coklat (Hutapea,
1993).
B. Protein
Protein adalah suatu polipeptida yang mempunyai bobot molekul yang
sangat bervariasi, dari 5000 hingga lebih dari satu juta. Di samping berat molekul
yang berbeda-beda, protein mempunyai sifat yang berbeda-beda pula. Ada protein
yang mudah larut dalam air, tetapi ada juga yang sukar larut dalam air (Poedjiadi,
1994).
Fraksinasi protein dilakukan dengan memisahkan masing–masing
protein dalam campuran secara fraksi demi fraksi. Ada dua macam cara yang
biasa digunakan dalam proses fraksinasi yakni dengan jalan pengendapan dan
kromatografi. Fraksinasi protein dengan jalan pengendapan dapat dilakukan
dengan menggunakan amonium sulfat dalam konsentrasi tertentu (Poedjiadi,
1994).
Keuntungan fraksinasi menggunakan amonium sulfat adalah lebih efektif
dari garam kation yang lain, selain itu harganya lebih murah dan ada manfaat
yang lebih besar lagi yaitu dapat menstabilkan protein yang dimurnikan. Pada
konsentrasi garam yang tinggi dapat mencegah terjadinya proteolisis dan juga
bereaksi dengan protein yang dipisahkan. Namun kelemahannya, amonium sulfat
biasanya terkontaminasi oleh logam berat seperti besi, sehingga dapat
mengganggu proses pengendapan. Jumlah amonium sulfat yang ditambahkan
untuk mencapai kejenuhan yang diinginkan dapat ditentukan dengan rumus yang
mudah (Scopes, 1994).
Beberapa metode tersedia untuk determinasi protein, antara lain:
1) metode Spektrofotometri
Sebagian besar protein memiliki absorbansi maksimal pada panjang
gelombang 280 nm karena adanya residu asam amino tirosin dan triptofan.
Keuntungan metode ini yaitu sensitifitasnya tinggi dan tidak membutuhkan
reagen. Komponen yang mengandung cincin purin dan pirimidin akan menyerap
UV pada panjang gelombang 260 nm. Dengan demikian keberadaan beberapa
komponen tersebut akan mengganggu pengukuran absorbansi protein pada
panjang gelombang 280 nm. Oleh karena itu untuk pengukuran protein dilakukan
pada panjang gelombang 260 nm dan 280 untuk mengoreksi adanya komponen-
komponen tersebut (Kerese, 1984).
2) metode Biuret
Prinsip dari metode biuret adalah mencampur larutan yang
mengandung protein dengan basa kuat kemudian direaksikan dengan larutan
CuSO4 yang sangat encer, sehingga menghasilkan warna violet kemerahan sampai
biru violet. Warna yang dihasilkan merupakan senyawa kompleks yang dihasilkan
karena reaksi antara Cu2+ dengan 4 atom N. Dua atom N yang berdekatan dari
berikatan dengan Cu2+ sehingga membentuk kompleks warna biru violet, dimana
semakin lama warna yang terbentuk akan semakin pekat (tua). Reaksi ini tidak
dapat terjadi pada dipeptida dan asam amino bebas (kecuali serin dan treonin).
Range protein yang dapat dianalisis menggunakan merode biuret yaitu 0,2 sampai
2 mg.
3) metode Lowry
Prinsip dari metode Lowry adalah mencampur larutan yang
mengandung protein dengan basa kuat kemudian direaksikan dengan larutan
CuSO4 yang sangat encer, sehingga menghasilkan warna violet kemerahan sampai
biru violet. Warna yang dihasilkan merupakan senyawa kompleks yang dihasilkan
karena reaksi antara Cu2+ dengan 4 atom N. Dua atom N yang berdekatan dari
satu rantai peptida dengan 2 atom N yang berdekatan dari rantai peptida yang lain
berikatan dengan Cu2+ sehingga membentuk kompleks warna biru violet.
Kemudian terjadi reduksi reagen fosfomolibdat- fosfotungstat (reagen Folin-
Ciocalteau) oleh tirosin, triptofan, dan sistein.
4) metode “Dye- Binding”
Interaksi antara reagen Coomassie Brilliant Blue G250 dengan protein
memberikan perubahan warna yang teramati, sehingga kadar protein dapat
ditetapkan dengan mengukur absorbansinya pada panjang gelombang 595 nm
C. Kanker
1. Definisi Kanker
Kanker merupakan penyakit berbahaya yang merusak bagian-bagian
tubuh, ditandai pertumbuhan yang cepat dan tidak terkendali dari sel-sel secara
abnormal serta membentuk massa yang sangat banyak yang bersama-sama
membentuk suatu tumor. Apabila proses tersebut tidak ditahan pertumbuhannya
akan menyebabkan kematian sel organisme (Dewick, 1989).
Sifat umum dari kanker adalah : 1) pertumbuhan berlebihan umumnya
berbentuk tumor; 2) gangguan diferensiasi dari sel dan jaringan; 3) bersifat infasif,
mampu tumbuh di jaringan sekitarnya; 4) bersifat metastatik, menyebar ke tempat
lain dan mengakibatkan pertumbuhan baru; 5) memiliki hereditas bawaan; dan 6)
pergeseran metabolisme ke arah pembentukkan makromolekul dari nukleosida
dan asam amino serta peningkatan katabolisme karbohidrat untuk energi sel
(Nafrialdi dan Sulistya, 1995).
Neoplasma merupakan pertumbuhan baru yang lazim dikenal dengan
tumor. Neoplasma cenderung untuk diuraikan sebagai suatu pertumbuhan pada
jaringan yang tidak terkendali. Menurut cara penyebarannya neoplasma ini dapat
dibagi menjadi dua :
a). tumor benigna
Tumor benigna dapat terus membesar namun tidak akan menyerang
jaringan-jaringan di sekitarnya dan juga tidak akan menyebar di luar lokasi yang
semestinya (metastasis). Tumor benigna ini umumnya dianggap lebih tidak
menerus membesar sekalipun tidak menyebar, dapat pula berakibat fatal jika
pertumbuhanya kemudian mengganggu organ-organ vital tubuh dan fungsinya.
b). tumor malignan
Berbeda dengan tumor benigna, tumor malignan dapat menyerang
jaringan-jaringan di sekitarnya dan juga mampu melakukan metastasis sehingga
dianggap lebih berbahaya. Banyak tumor malignan pada manusia berasal dari
jaringan epitel. Hal ini dapat terjadi karena jaringan ini memiliki kontak langsung
dengan lingkungan yang cukup tinggi (Greens & Harris, 2000). Umumnya, yang
dimaksud dengan kanker adalah tumor malignan karena sel-selnya dapat
menyebar ke daerah lain, merusak jaringan tubuh di sekitarnya dan bahkan dapat
merusak bagian organ lain dalam tubuh. Salah satunya, dengan jalan menyebar
atau metastasis lewat aliran darah. Ketika mencapai organ baru, sel-sel tersebut
akan membentuk lagi tumor yang baru (Kardinan & Taryono, 2003).
2. Proses terjadinya kanker
Sel-sel normal dapat berubah menjadi sel-sel kanker karena adanya satu
atau lebih mutasi yang terjadi pada DNA sel. Perkembangan penyakit kanker
merupakan suatu proses rumit yang melibatkan tidak hanya suatu perubahan
genetik namun juga faktor-faktor epigenetik (misalnya, aksi hormonal tubuh,
bahan-bahan karsinogen, dan lain-lain) yang tidak berkembang menjadi tumor itu
sendiri namun dapat meningkatkan kemungkinan terjadinya mutasi pada DNA sel
Ada dua kategori utama perubahan genetik yang mampu mendorong
terjadinya kanker :
a). aktivasi proto-onkogen menjadi onkogen
Proto-onkogen adalah gen yang berfungsi untuk mengontrol proses
pembelahan, apoptosis dan diferensiasi pada sel-sel normal. Pada kejadian kanker
proto-onkogen ini dapat berubah menjadi onkogen oleh adanya virus maupun aksi
dari senyawa-senyawa karsinogen.
b). inaktivasi gen penekan terbentuknya tumor
Sel-sel normal memiliki suatu gen yang mempunyai kemampuan untuk
menekan terbentuknya tumor yang disebut gen penekan terbentuknya tumor atau
anti-onkogen. Saat ini, telah ditemukan bukti bahwa adanya mutasi pada gen
tersebut terlibat dalam banyak kejadian kanker. Hilangnya fungsi dari gen
penekan terbentuknya tumor tersebut dapat menjadi penyebab utama terjadinya
kanker (Rang et al, 2003).
Beberapa karakteristik umum yang dapat membedakan antara sel kanker
dengan sel normal antara lain, sel kanker memiliki pertumbuhan yang tidak
terkontrol, proses pembelahan pada sel kanker tidak lagi dapat dikendalikan oleh
proses regulasi dari pembelahan dan pertumbuhan sel yang normal sehingga
terjadilah gangguan diferensiasi dan fungsi dari sel tersebut. Sel normal umumnya
akan berdiferensiasi menjadi sel yang matang dan bergabung dengan sel-sel
lainnya membentuk jaringan dan baru kemudian dapat melaksanakan fungsi yang
semestinya. Pada sel kanker, proses pembelahan yang terlalu cepat
tidak mature sehingga tidak dapat menjalankan fungsi yang semestinya. Sel
kanker juga memiliki kemampuan berinvasif yakni, kemampuan untuk tumbuh di
jaringan sekitarnya dan mengganggu fungsi jaringan tersebut. Selain itu, sel
kanker juga mampu melakukan metastasis yang merupakan penyebaran dari
tumor induk membentuk tumor sekunder, yang mampu mencapai daerah lain pada
tubuh, lewat pembuluh darah atau pun limpa. Dilaporkan bahwa metastasis
merupakan penyebab utama kematian pada banyak kasus kanker dan hal ini
pulalah yang mendasari permasalahan utama pada terapi kanker (Rang et al,
2003).
Tingkatan perubahan sel pada pertumbuhan kanker adalah sebagai berikut:
1. hiperplasi adalah pembengkakan organ tubuh akibat pertumbuhan sel- sel baru
yang abnormal karena hilangnya kontrol pertumbuhan.
2. metaplasi yaitu pertumbuhan epitel suatu jenis jaringan dewasa menjadi
jaringan lain yang juga dewasa.
3. displasi yaitu perubahan sel dewasa ke arah kemunduran dalam hal bentuk,
besar dan orientasinya yang masih bersifat reversibel.
4. anaplasi yaitu perubahan serupa displasi yang menyimpang lebih jauh dari
normal. Merupakan suatu ciri tumor ganas yang bersifat ireversibel.
5. karsinoma insitu yaitu gambaran sel menjadi sangat atipik namun belum
terdapat pertumbuhan infiltratif.
6. invasi yaitu sel kanker telah menembus lapisan basal jaringan (Kuswibawati,
2. Kanker leher rahim
Penyebab dari terjadinya kanker leher rahim (cervix) disebut–sebut karena
adanya infeksi dari HPV (Human Papiloma Virus). Human Papiloma Virus
(HPV) merupakan virus DNA yang sangat kecil namun infektif serta dapat
menimbulkan lesi pada kulit maupun sel epitel pipih. Ada lebih dari 100 tipe
HPV, tipe yang umum adalah tipe 16 dan 18. Kedua tipe ini dapat menimbulkan
perubahan abnormal sel–sel cervix (CIN) dan selanjutnya menyebabkan terjasinya
kanker cervix atau kanker leher rahim (Widyani, 2005).
Faktor seluler dari HPV yang bertanggung jawab atas munculnya kanker
leher rahim adalah viral E6 dan E7. DNA E6 dan E7 dari virus ini mampu
menyebabkan kekacauan pada siklus dan proliferasi sel akibat tidak aktifnya gen
penekan tumor p53 dan pRb pada sel normal. Viral DNA E6 akan mengikat kuat
p53 sedangkan DNA E7 akan mengikat pRb (King, 2000).
D. Kultur Sel
Penggunaan kultur sel sebagai subyek uji dikarenakan selain banyaknya
tekanan publik untuk mengurangi bahkan tidak menggunakan hewan sebagai
subyek uji dalam percobaan mengingat segi moral. Alasan lain tidak
menggunakan hewan percobaan ialah untuk menghemat biaya yang besar apabila
menggunakan hewan percobaan dan juga rendahnya nilai korelasi antara hasil
yang diperoleh dengan penelitian menggunakan hewan jika dikorelasikan dengan
manusia. Dengan menggunakan kultur sel sebagai alternatif subyek dalam
dengan lebih efektif. Hal ini dikarenakan kondisi dari sel dapat dikontrol dan
dimodifikasi (Wallin, 1998).
Sel SiHa adalah salah satu kanker cervix yang menyebabkan kematian
yang tinggi pada wanita. Sel SiHa diperoleh dari fragmen sampel jaringan primer
dari suatu karsinoma cervix dan merupakan squamosa yang tidak terdiferensiasi.
Sel ini ditemukan pada manusia sekitar tahun 1995. Morfologi sel SiHa mirip
dengan sel epitelial dan tipe inti selnya tidak diketahui. Sel ini mengandung
Human Papilloma Virus 16 (HPV-16) (Anonim, 2006d).
E. Sel Vero
Sel Vero ditemukan pertama pada tahun 1962 oleh Y. Yasumura dan Y.
Kawakita di Universitas Chiba di Chiba, Jepang. Sel Vero diambil dari ginjal kera
dewasa (jenis African Green Monkey) yang sehat. Selain sering digunakan dalam
produksi vaksin, sel Vero juga sering digunakan untuk mendeteksi Verotoksin.
Saat ini, sel Vero telah banyak digunakan untuk mengembangkan pengobatan
berbagai macam penyakit, salah satu diantaranya yaitu diabetes (Anonim, 2006c).
Sel Vero digunakan secara luas pada studi replikasi virus dan uji penyakit
pes. Selain itu juga digunakan untuk uji berbagai penyakit yang diakibatkan oleh
virus (Anonim, 1983).
F. Uji Sitotoksisitas
Uji sitotoksisitas ialah suatu uji yang secara in vitro menggunakan kultur
sel dalam mengevaluasi keamanan obat, makanan, kosmetik maupun bahan-bahan
Uji sitotoksisitas ini merupakan suatu uji yang cepat, terstandarisasi,
sensitif dan tidak terlalu mahal, dengan kepentingan untuk menentukan apakah
suatu material mengandung bahan yang berbahaya (toksis) secara biologik dalam
jumlah yang signifikan. Sensitifitas yang tinggi dari uji ini karena adanya sel uji
yang terisolasi dalam kultur dan tidak adanya mekanisme protektif tubuh yang
mempengaruhi sel uji (Wallin, 1998).
Ada beberapa metode untuk mengetahui hasil uji sitotoksisitas, yaitu
metode Trypan Blue Staining, Tritium-labeled Thymidine dan MTT. Trypan Blue
Staining adalah cara sederhana untuk mengevaluasi integritas dari membran sel,
yang kemudian dari hasilnya dapat menunjukkan kematian atau proliferasi sel.
Namun metode ini kurang sensitif. Metode kedua yaitu Tritium-labeled Thymidine
adalah metode yang menggunakan senyawa radioaktif tritium yang dilabelkan
pada timidin. Pengukuran jumlah bahan radioaktif yang terambil oleh sel ini
sangat akurat namun metode ini memerlukan waktu yang lebih lama. Sedangkan
metode MTT adalah metode kolorimetrik yang mengukur hasil reduksi dengan
garam tetrazolium menjadi kristal formazan yang berwarna ungu oleh
mitokondria sel hidup melalui metabolismenya. Kemudian warna ungu yang
dibentuk diukur dengan pembacaan ELISA plate reader. Jumlah warna yang
dibentuk proporsional dengan jumlah sel yang hidup. Metode MTT bersifat
kuantitatif dan lebih sensitif bila dibandingkan dengan metode Trypan Blue
Staining karena adanya hubungan yang linear antara keaktifan sel dan absorbansi,
Staining bersifat kualitatif dan hanya mengindikasikan sel yang masih hidup
(Anonim, 2006b).
G. Mekanisme Senyawa Antikanker
Senyawa yang digunakan sebagai bahan obat kanker memiliki salah satu
kemampuan untuk menghambat terjadinya kanker dengan mekanisme
menghambat sintesis asam nukleat atau dengan menghambat proses pembelahan
sel pada saat mitosis dengan cara mengikat protein tubulin dalam spindle mitosis
dan menghalangi polymerase ke dalam mikrotubulus. Mekanisme lain yaitu
menghambat sintesis DNA dan replikasinya melalui enzim topoisomerase
(Dewick, 1986).
H. Landasan Teori
Kanker merupakan penyakit berbahaya yang merusak bagian- bagian
tubuh, ditandai pertumbuhan yang cepat dan tidak terkendali. Apabila proses
tersebut tidak ditahan pertumbuhannya akan menyebabkan kematian sel
organisme. Banyak penelitian menggunakan fraksi protein dari berbagai jenis
tanaman. Daun mimba diteliti sebagai antikanker dalam penelitian yang berjudul
“Sitotoksisitas Fraksi Protein Daun Mimba (Azadirachta indica A. Juss) Hasil
Pengendapan dengan Ammonium Sulfat 30%, 60%, dan 100% Jenuh terhadap
Kultur Sel SiHa (Candra, 200)”.
Dari penelitian Candra (2006) diketahui bahwa bahwa harga LC50 yang
diperoleh dari fraksi protein daun mimba hasil pengendapan dengan amonium
sulfat 30%, 60%, dan 100% jenuh berturut-turut adalah sebesar 1,72 μg/ml; 0,04
protein 60% berefek paling sitotoksik terhadap sel SiHa dan fraksi protein 30%
dan 60% diperkirakan memiliki aktivitas sebagai antikanker.
Dari hasil penelitian tersebut maka diduga bahwa fraksi protein yang lebih kecil
dari 60% juga mempunyai daya sitotoksik terhadap sel SiHa dan diperkirakan
memiliki aktivitas sebagai antikanker. Hal tersebut yang mendasari dilakukannya
penelitian tentang Sitotoksisitas Fraksi Protein Daun Mimba (Azadirachta indica
A. Juss) FP30, FP40, FP50,dan FP60 Terhadap Kultur Sel SiHa.
Penelitian ini bertujuan untuk mengetahui fraksi protein mana yang
menghasilkan efek sitotoksik paling besar dan lebih berpotensi untuk
dikembangkan ke depannya sebagai senyawa antikanker.
I. Hipotesis
Sitotoksisitas Fraksi Protein Daun Mimba (Azadirachta indica A. Juss)
FP30, FP40, FP50,dan FP60 Terhadap Kultur Sel SiHa memiliki efek sitotoksisitas
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian sitotoksisitas fraksi protein daun mimba (Azadirachta indica A.
Juss)FP30, FP40, FP50, dan FP60 terhadap kultur sel SiHa ini termasuk penelitian
eksperimental murni dengan rancangan acak lengkap pola satu arah.
B. Variabel Penelitian dan Definisi Operasional
1. Variabel bebas
Kadar fraksi protein daun mimba yaitu 0,20 μg/ml; 0,39 μg/ml; 0,78 μg/ml;
1,56 μg/ml; 3,13 μg/ml; 6,25 μg/ml; 12,5 μg/ml; 25 μg/ml; 50 μg/ml; 100
μg/ml dan 200 μg/ml.
2. Variabel tergantung
Persentase kematian sel SiHa dan sel Vero.
3. Variabel pengacau terkendali
a. pH dan suhu pembuatan fraksi protein, dikendalikan pada pH 7,2 dan
suhu 4oC.
b. medium tumbuh sel dikendalikan dengan menggunakan medium RPMI
1640-serum (untuk sel SiHa) dan M199 (untuk sel Vero).
c. tempat tumbuh dan waktu pemanenan daun mimba dikendalikan dengan
memanen daun pada tempat dan waktu yang sama.
4. Variabel pengacau tak terkendali
5. Definisi operasional
a.sitotoksisitas ialah sifat toksik atau beracun dari fraksi protein daun
mimba terhadap sel SiHa dan sel Vero.
b.fraksi protein ialah fraksi protein daun mimba (Azadirachta indica A.
Juss.)FP30, FP40, FP50, dan FP60, dinyatakan dalam µg/ml.
c.LC50 ialah konsentrasi fraksi protein daun mimba yang mampu membunuh
atau menyebabkan kematian sejumlah 50% sel uji dan dinyatakan dalam
µg/ml.
C. Alat dan Bahan 1. Alat
Peralatan yang digunakan dalam penelitian ini antara lain: alat-alat gelas,
stamper, mortir, timbangan analitik (AND ER-400 H), alumunium foil, magnetic
stirrer, tabung conical, autoklaf, tissue culture flask, swing rotor sentrifuge
(PLC), inkubator (Nuaire), mikropipet, membran dialisis (Sigma), lemari
pendingin, cell counter (Nunc), 96-well plate (Nunc), spektrofotometer UV (Cecil
CE-292), ELISA reader (SLT 340 ATC), laminar air flow (Nuaire), mikroskop
(Olympus IMT-2), haemocytometer (Nebauer), kain monel, tissue, glove, masker.
2. Bahan
Bahan-bahan yang digunakan dalam penelitian ini ialah :
a. daun mimba segar
b. kultur sel SiHa yang diambil dari persediaan di Laboratorium Hayati
c. kultur sel Vero (normal) yang diambil dari stok di Laboratorium Hayati
Universitas Gadjah Mada, Yogyakarta.
d. pereaksi-peraksi yang digunakan untuk preparasi fraksi protein daun
mimba
1) larutan dapar natrium fosfat 5 mM pH 7,2 (Merck)
2) larutan dapar natrium fosfat 5 mM pH 7,2 yang mengandung 0,14
M NaCl (Merck)
3) amonium sulfat p.a. (Merck)
e. Pereaksi-pereaksi untuk uji sitotoksisitas
1) media pencuci: RPMI 1640 (Sigma), natrium bikarbonat, Hepes
2) media penumbuh: RPMI 1640, M199, FBS (Foetal Bovine Serum)
10%, Penisilin-Streptomisin 1% (Gibco), dan Fungison 0,5%
(Gibco).
3) reagen Stopper : SDS (sodium dodeksil sulfat) dalam HCl 0,01 N
(Merck)
4) MTT (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium
bromide) (Sigma)
D. Tata Cara Penelitian 1. Determinasi tanaman
Bahan utama yang akan digunakan dalam penelitian yaitu daun mimba,
telah dideterminasi terlebih dahulu di Laboratorium Farmakognosi Fitokimia,
kebenarannya menggunakan acuan baku (Backer dan Backuizen van den Brink,
1965).
2. Pengumpulan daun mimba
Daun mimba yang digunakan diambil dari pohon mimba yang tumbuh di
pekarangan Laboratorium Hayati, Universitas Gadjah Mada, Yogyakarta, pada
bulan Juni 2006.
3. Sterilisasi alat dan bahan
Sterilisasi alat dilakukan untuk menghilangkan mikroorganisme dari
alat-alat yang akan digunakan agar tidak mengganggu penelitian. Adapun metode
sterilisasi yang digunakan dalam penelitian ini adalah metode uap panas dengan
menggunakan autoklaf. Alat–alat gelas yang akan digunakan dalam keadaan
steril, dicuci sampai bersih kemudian di sterilisasi menggunakan autoklaf pada
suhu 121oC selama 20 menit.
4. Preparasi fraksi protein dari daun mimba
Daun tanaman mimba dikumpulkan segar, diseleksi, dibersihkan tulang
daunnya, dan ditimbang sebanyak 400 gram. Daun kemudian dicuci bersih dengan
air mengalir, dibungkus plastik dan disimpan dalam freezer semalam. Bahan
ditumbuk halus dalam mortir bersih dan steril dengan penambahan sedikit demi
sedikit dapar natrium fosfat 5 mM pH 7,2 yang mengandung 0,14 M NaCl pada
suhu dingin (dengan penambahan es di sekitarnya). Bahan diperas dan disaring
dengan kain monel, ditampung dalam tabung conical yang bersih dan steril.
Cairan yang diperoleh disentrifus dengan 4000 rpm selama 30 menit. Supernatan
diukur volumenya. Supernatan ekstrak gubal yang diperoleh, diendapkan
proteinnya dengan menambahkan amonium sulfat hingga mencapai kejenuhan
30%. Penambahan amonium sulfat dilakukan sedikit demi sedikit, diikuti
pengadukan teratur dengan magnetic stirrer pada suhu dingin, dilanjutkan dengan
sentrifugasi ultra dengan kecepatan 10000 rpm pada suhu 4°C selama 25 menit.
Supernatan (1) ditampung dalam labu ukur sedangkan endapan yang diperoleh
dilarutkan dalam sesedikit mungkin larutan dapar natrium fosfat 5 mM pH 7,2.
Selanjutnya endapan tadi didialisis dengan memasukkan larutan endapan dalam
dapar natrium fosfat ke dalam membran dialisis yang salah satu ujungnya telah
dijepit dengan penjepit khusus membran kemudian ujung membran yang lainnya
ditutup dengan dijepit dengan penjepit khusus membran dengan kuat. Membran
dialisis lalu digantung dalam bekerglass yang berisi dapar natrium fosfat 5 mM
pH 7,2 sebanyak 1000 ml. Proses dialisis dilakukan dalam almari es selama
semalam dengan di-stirrer perlahan dan dilakukan penggantian dapar natrium
fosfat satu kali. Hasil dialisis disentrifus dengan kecepatan 8000 rpm selama 20
menit. Endapan hasil dialisis dibuang dan supernatan diambil. Supernatan ini
merupakan sampel fraksi protein daun mimba dengan konsentrasi amonium sulfat
30% jenuh.
Supernatan (1), (2), dan (3) ditampung secara bertahap, kemudian
ditambah amonium sulfat hingga mencapai kejenuhan 40%, 50%, 60% dengan
5. Pengukuran kadar protein dengan spektrofotometri UV
Sampel fraksi protein daun mimba 30%, 40%, 50% dan 60%,
masing-masing sebanyak 10 µl dimasukkan ke dalam kuvet 1 ml lalu ditambah 990 µl
larutan dapar natrium fosfat 5 mM, diukur serapannya dengan spektrofotometer
UV pada panjang gelombang 280 nm dengan blanko larutan dapar natrium fosfat
5 mM. Untuk mengoreksi adanya serapan oleh asam nukleat pada panjang
gelombang tersebut maka pengukuran juga dilakukan pada panjang gelombang
260 nm. Perbandingan antar serapan pada 280 nm dan 260 nm merupakan rasio
serapan R 280/260, dan digunakan untuk menghitung faktor koreksi dengan cara
ekstrapolasi terhadap tabel kadar protein Layne (1957). Selanjutnya, kadar protein
dihitung dari perkalian antara serapan pada 280 nm, faktor koreksi dan faktor
pengenceran.
6. Propagasi dan panen Sel SiHa
a. Propagasi Sel SiHa
Sel diambil dari tangki nitrogen cair, kemudian segera dicairkan dalam
penangas air 37oC, kemudian ampul disemprotkan dengan etanol 70%. Ampul
dibuka dan sel SiHa dipindahkan dalam tabung conical steril yang berisi medium
RPMI 1640. Suspensi sel disentrifugasi selama 5 menit, supernatan dibuang,
diganti dengan medium RPMI yang baru, kemudian disuspensikan perlahan.
Suspensi sel lalu disentrifugasi kembali selama 5 menit kemudian dicuci ulang
sekali lagi. Supernatan dibuang, pelet ditambahkan 1 ml medium penumbuh yang
mengandung 10% FBS. Resuspensikan secara perlahan sampai homogen,
dalam inkubator dengan suhu 37oC dengan aliran 5% CO2. Setelah 24 jam,
medium penumbuh diganti dan sel ditumbuhkan hingga konfluen dan jumlahnya
cukup untuk penelitian.
b. Panen Sel SiHa
Setelah jumlah sel cukup (kurang lebih setelah berumur 7 hari), media
diganti dengan RPMI 1640 baru sebanyak 5 ml kemudian sel dilepaskan dari
dinding flask dengan cara diresuspensikan menggunakan pipet Pasteur. Sel
dipindahkan dalam tabung conical steril dan ditambahkan medium RPMI sampai
volume 10 ml dan disentrifugasi 3000 rpm selama 5 menit. Supernatan dibuang
dan pelet sel diresuspensikan perlahan dengan 1 ml medium. Sel kemudian
dihitung menggunakan haemocytometer. Suspensi sel ditambah sejumlah medium
sehingga memperoleh konsentrasi sel sebesar 2,5x104/100 μl dan siap dipakai
untuk penelitian.
8. Propagasi dan panen sel Vero
a. Propagasi Sel Vero
Sel diambil dari tangki nitrogen cair, kemudian segera dicairkan dalam
penangas air 37oC, kemudian ampul disemprotkan dengan etanol 70%. Ampul
dibuka dan sel SiHa dipindahkan dalam tabung conical steril yang berisi medium
M199. Suspensi sel disentrifugasi selama 5 menit, supernatan dibuang, diganti
dengan medium M199 yang baru, kemudian disuspensikan perlahan. Suspensi sel
lalu disentrifugasi kembali selama 5 menit kemudian dicuci ulang sekali lagi.
Supernatan dibuang, pelet ditambahkan 1 ml medium penumbuh yang
kemudian sel ditumbuhkan dalam tissue culture flask kecil dan diinkubasikan
dalam inkubator dengan suhu 37oC dengan aliran 5% CO2. Setelah 24 jam,
medium penumbuh diganti dan sel ditumbuhkan hingga konfluen dan jumlahnya
cukup untuk penelitian.
b. Panen sel Vero
Setelah jumlah sel cukup (kurang lebih setelah berumur 7 hari), sel dicuci
dengan FBS 10% sebanyak 3 ml. Untuk melepaskan sel-sel dari dinding flask,
diberi tripsin 2,5% sebanyak 1 ml. Sel dipindahkan dalam tabung conical steril
yang sudah berisi M199 sebanyak 7 ml. Kemudian sel dibilas kembali dengan
FBS 10% sebanyak 3 ml. Hasil bilasan dituang ke dalam tabung conical yang
sama dan disentrifuse selama 5 menit. Untuk menghilangkan sisa tripsin, sel
dicuci sekali lagi dengan menggunakan medium yang sama. Kemudian pelet
ditambah media kultur sebanyak 1 ml. Selanjutnya lakukan perhitungan jumlah
sel dengan menggunakan haemocytometer. Suspensi sel ditambah sejumlah
medium sehingga memperoleh konsentrasi sel sebesar 2,5x104/100 μl dan siap
dipakai untuk penelitian.
9. Uji sitotoksisitas fraksi protein daun mimba pada sel SiHa
Untuk uji sitotoksisitas, sebanyak 100 μl suspensi sel SiHa dengan
kepadatan 2,5x104/100 μl dimasukkan dalam sumuran-sumuran 96-well plate
yang telah berisi 100 μl fraksi protein daun mimba dengan kadar 200 µg/ml pada
sumuran A1, B1 dan C1 pada kolom 1, kemudian pada sumuran A2, B2 dan C2 di
kolom 2 ditambahkan 100 μl suspensi sel SiHa pada sumuran yang telah berisi
hingga diperoleh seri kadar yang terendah yang digunakan dalam penelitian.
Sebagai kontrol, 100 µl suspensi sel ditambahkan ke dalam sumuran yang berisi
medium RPMI 1640 dan dapar natrium fosfat 5 mM pH 7,2 sedangkan untuk
faktor koreksi, 100 µl sampel ditambahkan ke dalam sumuran yang berisi medium
RPMI 1640 dan dapar natrium fosfat 5 mM pH 7,2. Selanjutnya 96-well plate
diinkubasikan selama 24 jam pada suhu 37oC, dalam inkubator dengan aliran 5%
CO2.
Pada akhir inkubasi, ke dalam masing-masing sumuran ditambahkan 10 μl
MTT 2,5 μg/ml dalam media RPMI 1640, lalu diinkubasikan semalam pada suhu
37oC, dalam inkubator dengan aliran CO2 5%. Sel hidup akan bereaksi dengan
MTT dan membentuk warna ungu. Reaksi dihentikan dengan menambahkan 50 μl
reagen stopper pada setiap sumuran dan inkubasi semalam pada suhu kamar.
Serapan setiap sumuran dibaca deangan ELISA reader pada panjang gelombang
550 nm. Besarnya serapan berbanding lurus dengan jumlah sel yang hidup.
10. Uji sitotoksisitas fraksi protein daun mimba pada sel Vero
Untuk uji sitotoksisitas, sebanyak 100 μl suspensi sel Vero dengan
kepadatan 2,5x104/100 μl dimasukkan dalam sumuran-sumuran 96-well plate
yang telah berisi 100 μl fraksi protein daun mimba dengan kadar 200 µg/ml pada
sumuran A1, B1 dan C1 pada kolom 1, kemudian pada sumuran A2, B2 dan C2 di
kolom 2 ditambahkan 100 μl suspensi sel Vero pada sumuran yang telah berisi
100 μl fraksi protein daun mimba dengan kadar 100 µg/ml, demikian seterusnya
hingga diperoleh seri kadar yang terendah yang digunakan dalam penelitian.
medium M199 dan dapar natrium fosfat 5 mM pH 7,2 sedangkan untuk faktor
koreksi, 100 µl sampel ditambahkan ke dalam sumuran yang berisi medium M199
dan dapar natrium fosfat 5 mM pH 7,2. Selanjutnya 96-well plate diinkubasikan
selama 24 jam pada suhu 37oC, dalam inkubator dengan aliran 5% CO2.
Pada akhir inkubasi, ke dalam masing-masing sumuran ditambahkan 10 μl
MTT 2,5 μg/ml dalam media M199, lalu diinkubasikan semalam pada suhu 37oC,
dalam inkubator dengan aliran CO2 5%. Sel hidup akan bereaksi dengan MTT
dan membentuk warna ungu. Reaksi dihentikan dengan menambahkan 50 μl
reagen stopper pada setiap sumuran dan inkubasi semalam pada suhu kamar.
Serapan setiap sumuran dibaca deangan ELISA reader pada panjang gelombang
550 nm. Besarnya serapan berbanding lurus dengan jumlah sel yang hidup.
E. Analisis Hasil
Pada metode MTT ini, serapan terbaca menunjukkan jumlah sel yang
hidup dan hasil akhir uji sitotoksisitas yaitu persentase kematian sel yang dihitung
menggunakan modifikasi rumus Abbot, dengan persamaan berikut:
% Kematian sel = x 100%
A C) (B A− −
Keterangan :
A = Rata-rata absorbansi kontrol B = Rata-rata absorbansi perlakuan
C = Rata-rata absorbansi perlakuan tanpa sel
Untuk menghitung harga LC50 dilakukan perhitungan secara statistik
menggunakan analisis probit sedangkan untuk menganalisis signifikansi
dilakukan pengolahan data dengan statistik uji T sampel independen
BAB IV
HASIL DAN PEMBAHASAN
A. Determinasi Tanaman
Penelitian ini menggunakan bahan utama berupa daun mimba. Untuk
menghindari terjadinya kesalahan pada penggunaan tanaman yang digunakan
maka dilakukan determinasi. Determinasi dilakukan di Laboratorium Kebun
Tanaman Obat, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
B. Sterilisasi Alat dan Bahan
Alat-alat yang akan digunakan dalam penelitian ini harus disterilkan terlebih
dahulu untuk menghilangkan semua pengotor dan kontaminan yang bisa
mengganggu pada saat proses penelitian. Sterilisasi dilakukan dengan
menggunakan metode uap panas bertekanan yang dilakukan pada suhu 121°C
selama kurang lebih 20 menit dan tekanan 1 atm. Metode uap panas ini dapat
membunuh mikroorganisme secara cepat disebabkan uap air panas yang lebih
mudah melakukan penetrasi ke dalam membran sel mikroorganisme. Prinsip
pemusnahan mikroorganisme dengan metode ini adalah uap air panas yang
berpenetrasi ke dalam sel mikroorganisme akan mengakibatkan koagulasi dan
denaturasi protein mikroorganisme. Penetrasi uap air panas yang cepat
mengakibatkan perusakan sel mikroorganisme yang lebih cepat.
C. Preparasi Sampel Fraksi Protein Daun Mimba
Pada penelitian ini menggunakan sampel berupa fraksi protein daun
yang bertujuan untuk menghilangkan pengotor-pengotor yang menempel pada
daun, kemudian sampel disimpan di dalam freezer semalaman agar daun menjadi
lebih kaku sehingga mudah dihaluskan. Daun ditumbuk sampai halus dengan
menggunakan mortir yang dialasi dengan wadah yang berisi es sehingga tercipta
suasana yang dingin di sekitar mortir. Pada saat penumbukan ditambahkan dapar
natrium fosfat 5 mM yang mengandung NaCl. Dapar ini berfungsi untuk
mengeluarkan atau mengekstraksi protein yang terdapat pada daun dan NaCl akan
mempermudah proses ekstraksi tersebut sehingga protein dapat larut dan stabil di
dalam buffer penggerak. Proses tersebut dilakukan pada suhu dingin supaya
protein tidak rusak, karena jika dilakukan pada suhu tinggi protein akan
mengalami denaturasi. Supernatan yang diperoleh merupakan ekstrak gubal daun
mimba yang kemudian ditambahkan amonium sulfat sampai mencapai kejenuhan
30%. Penambahan amonium sulfat ini bertujuan untuk menarik air yang terdapat
di dalam larutan sehingga akan terjadi penurunan kelarutan protein dan agregasi
molekul protein yang menyebabkan protein terendapkan. Proses di atas disebut
mekanisme salting out. Pada mekanisme salting out tersebut, penambahan
amonium sulfat dilakukan secara sedikit demi sedikit agar dapat larut sempurna.
Dari proses sentrifugasi akan diperoleh supernatan dan endapan. Supernatannya
ditampung untuk digunakan pada proses preparasi sampel fraksi berikutnya,
sedangkan endapan yang diperoleh dilarutkan dalam sesedikit mungkin larutan
dapar natrium fosfat 5 mM pH 7,2.
Endapan yang diperoleh didialisis dengan tujuan untuk menghilangkan
berlangsung karena adanya perbedaan gradien konsentrasi yang besar di dalam
dan di luar permukaan tubing dialysis sehingga memungkinkan terjadinya
mekanisme difusi pasif. Konsentrasi amonium sulfat di dalam tubing dialysis
yang lebih tinggi dibanding di luar tubing dialysis mengakibatkan amonium sulfat
akan keluar dari dalam tubing dialysis dengan mekanisme difusi pasif. Selain
karena adanya perbedaan gradien konsentrasi yang besar, tubing dialysis ini
bersifat semipermeabel, yang memiliki pori yang hanya mengeluarkan
partikel-partikel yang berukuran sekitar 15.000–20.000 Dalton sehingga partikel-partikel amonium
sulfat yang berukuran lebih kecil daripada protein dapat keluar dari dalam tubing
dialysis sedang protein yang merupakan makromolekul tetap tertinggal di dalam.
Pengggantian dapar dilakukan dengan tujuan agar amonium sulfat yang keluar
dari tubing dialysis dan berada dalam dapar tidak terlalu jenuh sehingga
perbedaan gradien konsentrasi amonium sulfat yang di dalam dengan yang di luar
permukaan tubing dialysis tetap besar dan dengan demikian mekanisme difusi
pasif dapat terus berjalan.
Endapan hasil dialisis dibuang dan supernatan diambil. Supernatan ini
merupakan sampel fraksi protein daun mimba dengan konsentrasi amonium sulfat
30% jenuh.
Pada preparasi sampel fraksi protein daun mimba konsentrasi amonium
sulfat 40%, 50% dan 60% jenuh langkah pengerjaannya sama seperti di atas, yaitu
dengan menggunakan supernatan hasil pengendapan amonium sulfat. Jumlah
gram amonium sulfat yang ditambahkan berturut- turut untuk sampel fraksi
jenuh dari kadar jenuh adalah sebanyak 28,35 gram; 29,29 gram; 30,29 gram;
31,36 gram.
D. Pengukuran Kadar Protein dengan Spektrofotometri UV
Sampel fraksi-fraksi protein daun mimba yang diperoleh kemudian diukur
kadarnya dengan menggunakan metode spektrofotometer UV dengan kuvet
kuarsaglass. Panjang gelombang yang digunakan ialah 280 nm dan 260 nm.
Digunakan panjang gelombang 280 nm karena protein dapat menyerap secara
aktif dan memberi respon maksimal pada panjang gelombang tersebut. Umumnya
protein mengandung residu asam amino seperti tirosin, triptofan dan fenilalanin di
mana residu-residu asam amino tersebut mempunyai cincin aromatis yang
mengandung kromofor atau juga auksokrom sehingga dapat menyerap sinar UV.
Untuk mengoreksi adanya senyawa-senyawa yang juga dapat mengabsorbsi pada
panjang gelombang tersebut maka pengukuran juga dilakukan pada panjang
gelombang 260 nm. Metode ini kurang tepat karena terganggu oleh adanya asam
nukleat serta senyawa yang mengandung cincin pirimidin dan purin yang
mempunyai serapan maksimum pada panjang gelombang 260 nm. Oleh karena
itu, dalam perhitungan kadar protein dengan metode ini perlu dilakukan koreksi
yakni dengan mengalikan absorbansi pada panjang gelombang 280 nm dengan
faktor koreksi dan faktor pengenceran. Hasil pengukuran konsentrasi protein FP30,
FP40, FP50, FP60 berturut-turut adalah 15,95 mg/ml; 9,25 mg/ml; 15,20 mg/ml;
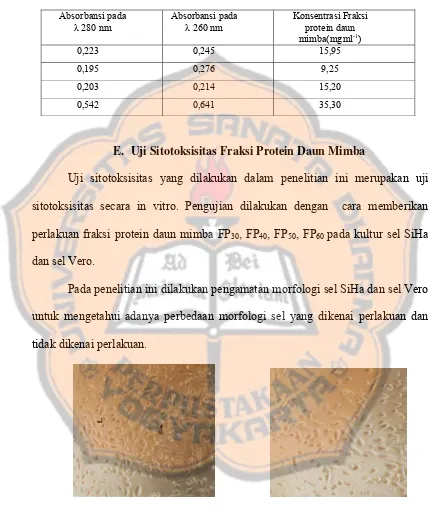
Tabel I. Data absorbansi fraksi protein dengan menggunakan metode spektrofotometer UV dan rasio serapan pada panjang gelombang 280 nm dan 260 nm
Absorbansi pada λ 280 nm
Absorbansi pada λ 260 nm
Konsentrasi Fraksi protein daun mimba(mgml-1)
0,223 0,245 15,95
0,195 0,276 9,25
0,203 0,214 15,20
0,542 0,641 35,30
E. Uji Sitotoksisitas Fraksi Protein Daun Mimba
Uji sitotoksisitas yang dilakukan dalam penelitian ini merupakan uji
sitotoksisitas secara in vitro. Pengujian dilakukan dengan cara memberikan
perlakuan fraksi protein daun mimba FP30, FP40, FP50, FP60 pada kultur sel SiHa
dan sel Vero.
Pada penelitian ini dilakukan pengamatan morfologi sel SiHa dan sel Vero
untuk mengetahui adanya perbedaan morfologi sel yang dikenai perlakuan dan
tidak dikenai perlakuan.
sel SiHa sel Vero
Gambar 2. Kultur sel SiHa yang diberi Gambar 3. Kultur sel Vero yang diberi
perlakuan fraksi protein daun mimba perlakuan fraksi protein daun mimba
keterangan: (i) sel SiHa yang hidup keterangan : (i) sel Vero yang hidup
(ii) sel SiHa yang mati (ii) sel Vero yang mati
Sel SiHa yang hidup tampak berbentuk panjang dan menempel pada flask.
Sel SiHa yang mati tampak berbentuk bulat, berukuran lebih kecil, dan tidak
menempel pada flask. Sel Vero yang hidup tampak berbentuk lonjong dan
menempel pada dasar flask. Sedangkan sel Vero yang mati tampak berbentuk
bulat dan tidak menempel pada dasar flask.
Metode uji sitotoksisitas yang digunakan dalam penelitian ini adalah
metode MTT (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide).
Prinsip dari metode MTT adalah adanya pemecahan garam tetrazolium MTT
(3-(4,5-dimetil-tiazol-2-il)-2,5-dipheniltetrazolium bromid) oleh sistem enzim
reduktase suksinat tetrazolium yang terdapat di dalam mitokondria sel sehingga
N N N N
S N
CH3
CH3
NH N
N N
S N
CH3
CH3
NADH
NAD+
MTT Formazan
Br
Gambar 4. Reaksi Pembentukan Kristal Formazan
Kristal formazan ini bersifat tidak larut air. Penambahan detergen
(natrium dodesil sulfat 10%) yang terdapat dalam stopper reagent, akan
menyebabkan kristal formazan larut. Intensitas warna ungu yang terbentuk dapat
dibaca dengan ELISA reader. Jumlah sel hidup berbanding lurus dengan
intensitas warna dari formazan yang terbentuk.
Gambar 5. Kristal Formazan di Bawah Mikroskop
Metode MTT ini termasuk metode yang cukup akurat karena absorbansi
yang terbaca sebanding dengan jumlah sel hidup yang masih aktif melakukan
metabolisme. Selain itu, uji ini juga dirasa cukup aman, sederhana, dan cepat.
Aman karena tidak memerlukan penggunaan zat-zat yang berbahaya, sederhana
mudah, dan cepat karena waktu yang dibutuhkan cukup singkat sehingga sangat
memungkinkan untuk menguji sampel dalam jumlah yang cukup banyak.
Data yang diperoleh dari uji toksisitas dengan metode MTT adalah nilai
absorbansi yang selanjutnya diolah dengan menggunakan modifikasi rumus Abbot
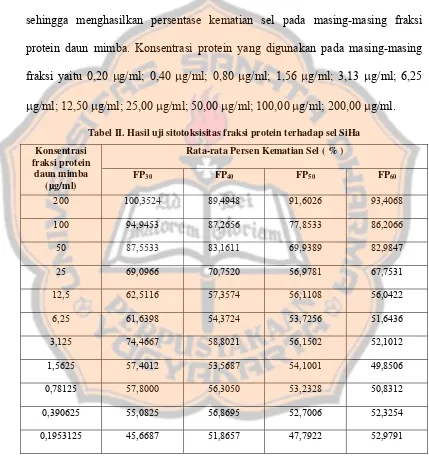
sehingga menghasilkan persentase kematian sel pada masing-masing fraksi
protein daun mimba. Konsentrasi protein yang digunakan pada masing-masing
fraksi yaitu 0,20 μg/ml; 0,40 μg/ml; 0,80 μg/ml; 1,56 μg/ml; 3,13 μg/ml; 6,25
μg/ml; 12,50 μg/ml; 25,00 μg/ml; 50,00 μg/ml; 100,00 μg/ml; 200,00 μg/ml.
Tabel II. Hasil uji sitotoksisitas fraksi protein terhadap sel SiHa
Rata-rata Persen Kematian Sel ( % ) Konsentrasi
fraksi protein daun mimba
(µg/ml)
FP30 FP40 FP50 FP60
200 100,3524 89,4948 91,6026 93,4068
100 94,9453 87,2656 77,8533 86,2066
50 87,5533 83,1611 69,9389 82,9847
25 69,0966 70,7520 56,9781 67,7531
12,5 62,5116 57,3574 56,1108 56,0422
6,25 61,6398 54,3724 53,7256 51,6436
3,125 74,4667 58,8021 56,1502 52,1012
1,5625 57,4012 53,5687 54,1001 49,8506
0,78125 57,8000 56,3050 53,2328 50,8312
0,390625 55,0825 56,8695 52,7006 52,3254
Gambar 6. Grafik persentase kematian sel SiHa perlakuan fraksi protein daun mimba
10%, 20%, 30%, 60% secara metode MTT
Konsentrasi fraksi protein daun mimba vs persen kematian sel SiHa
0 20 40 60 80 100 120
0 50 100 150 200 250
konsentrasi fraksi protein daun m im ba (ug/m l)
p e rs en k em a ti an s el SiH a FP30 FP40 FP50 FP60
Tabel III. Hasil uji sitotoksisitas fraksi protein terhadap sel Vero
Sampel
no.
Kadar fraksi
protein daun
mimba (μg/ml)
Rata-rata persen kematian sel (%)
1 200 89,5067 74,4089 71,8804 83,5849
FP30 FP40 FP50 FP60
2 100 79,8833 75,4239 73,7826 84,8535
3 50 90,5968 85,1326 72,4783 74,0704
4 25 85,4878 79,2214 76,5870 73,7642
5 12,5 78,3858 66,8139 85,4022 71,2380
6 6,25 82,0634 70,0740 75,0761 68,8211
7 3,125 76,8113 77,0361 63,2609 67,1697
8 1,5625 69,3349 75,8419 64,1304 57,3819
9 0,78125 67,7054 85,0609 52,5000 56,3867
10 0,390625 68,9386 79,6394 58,0000 63,6155
Gambar 7. Grafik persentase kematian sel Vero perlakuan fraksi protein daun mimba
30%, 40%, 50%, 60% secara metode MTT
Konsentrasi Fraksi Protein Daun Mimba vs Persen Kematian Sel Vero
0 20 40 60 80 100
0 50 100 150 200 250
Konsentrasi Fraksi Protein Daun Mimba (ug/ml)
P e rs en k e m a ti an s e l Ve ro FP30 FP40 FP50 FP60
Nilai persentase kematian sel SiHa yang didapat cukup tinggi dan relatif
terus meningkat seiring dengan meningkatnya konsentrasi yang diberikan. Pada
grafik FP30, terlihat persen kematian sel yang paling tinggi.
Dari tabel dan grafik sel Vero di atas dapat dilihat bahwa persen kematian
sel naik turun sehingga tidak dapat ditarik suatu korelasi yang dapat menyatakan
aktivitas sitotoksik dari fraksi protein daun mimba yang digunakan. Kematian sel
Vero yang naik turun tersebut kemungkinan disebabkan karena adanya kematian
alami sel.
Selanjutnya ditentukan nilai LC50 yang dilakukan dengan analisa probit
menggunakan SPSS 13. Penentuan nilai LC50 ini bertujuan untuk mengetahui
ketoksikan fraksi protein daun mimba terhadap sel SiHa dan sel Vero. Dari hasil
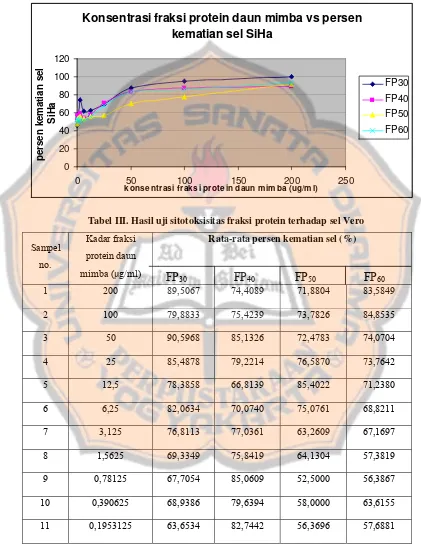
Tabel IV. Harga LC50 fraksi protein daun mimba pada sel SiHa
Fraksi protein Harga LC50 (µg/ml)
FP30 0,38
FP40 0,45
FP50 0,72
FP60 0,79
Tabel V. Harga LC50 fraksi protein daun mimba pada sel Vero
Fraksi protein Harga LC50 (µg/ml)
FP30 0,014
FP40 > 1 g/ml
FP50 0,033
FP60 0,048
Semakin kecil harga LC50 maka senyawa semakin bersifat toksik,
sebaliknya semakin besar harga LC50 maka semakin bersifat tidak toksik (Meyer
et al, 1982). Dari data di atas dapat dilihat bahwa pada sel SiHa, nilai LC50 paling
kecil dimiliki oleh FP30, yang berarti FP30 bersifat sangat toksik. Berdasarkan NCI
(National Cancer Institute) yang menyatakan suatu senyawa berpotensi sebagai
antikanker bila memiliki harga LC50 ≤ 20 μg/ml (Suffness dan Pezzuto, 1991)
Fraksi protein FP30, FP40, FP50 dan FP60 memiliki nilai LC50 lebih kecil dari 20
µg/ml, sehingga bisa dikembangkan sebagai senyawa antikanker.
Hasil yang diperoleh pada penelitian ini berbeda dengan penelitian
sebelumnya (Candra, 2006). Pada penelitian Candra, LC50 yang diperoleh pada
karena protein-protein yang memiliki kemampuan untuk menghambat
pertumbuhan sel SiHa telah banyak mengendap di fraksi protein 30% dan 60%
jenuh sehingga banyak sel kanker yang mati pada fraksi protein daun mimba 30%
dan 60%.
Sedangkan untuk sel Vero, nilai LC50 paling kecil juga dimiliki oleh FP30,
yang berarti fraksi protein tersebut bersifat sangat toksik. Dari data di atas dapat
dilihat bahwa fraksi protein daun mimba juga bersifat toksik pada sel Vero. Hal
ini dapat menjadi penghambat untuk mengembangkan fraksi protein daun mimba
sebagai senyawa antikanker. Dilakukan pula uji Kolmogorov-Smirnov yang
bertujuan untuk membandingkan tingkat kesesuaian sampel dengan suatu
distribusi tertentu. Hasil dari uji Kolmogorov-Smirnov menunjukkan bahwa
semua fraksi protein baik pada sel SiHa maupun sel Vero memiliki distribusi
normal (sig. > 0,05).
Kemudian dilakukan penghitungan nilai kolerasi LC50 sel SiHa dan sel
Vero pada taraf kepercayaan 95%. Untuk sel SiHa diperoleh hasil bahwa pada
semua fraksi (FP30, FP40, FP50 dan FP60) kolerasinya linier ( r hitung > r tabel ).
Untuk melihat perbedaan antara persen kematian sel SiHa dengan sel Vero
karena pemaparan fraksi protein daun mimba digunakan uji t sampel independen
dengan menggunakan program SPSS 13,0. Hasil uji t pada FP40 menunjukkan
bahwa LC50 sel SiHa berbeda bermakna dengan LC50 sel Vero (sig.<0,05). Hal ini
berarti terdapat perbedaan respon antara sel SiHa dengan sel Vero karena adanya
fraksi protein daun mimba FP40. Hasil uji t pada FP30, FP50, dan FP60 menunjukkan
Hal ini berarti fraksi protein daun mimba FP30, FP50, dan FP60 memiliki
kemampuan yang sama untuk menginduksi kematian sel SiHa dan sel Vero
sehingga fraksi protein daun mimba FP30, FP50, dan FP60 diduga tidak dapat
dikembangkan sebagai antikanker. Sedangkan fraksi protein daun mimba FP40
<