INTISARI
Buah Mahkota Dewa banyak digunakan dalam berbagai pengobatan tradisional untuk mengobati berbagai penyakit. Buah ini memiliki banyak khasiat. Selama ini, masyarakat mengkonsumsinya antara lain dalam bentuk perasan dan belum pernah dalam sediaan sirup.
Penelitian ini bertujuan untuk membandingkan stabilitas fisis sirup yang dibuat dengan 650 g sukrosa dan campuran sukrosa 422,5 g – sorbitol 227,5 g sebagai bahan pemanis. Hasil yang diperoleh merupakan data pemeriksaan stabilitas fisis sirup sebelum dan sesudah penyimpanan selama 6 minggu penyimpanan. Stabilitas fisis sirup yang diamati meliputi keadaan organoleptis (warna, bau, rasa, kejernihan), pengkristalan, kerapatan, pH, profil dan tipe alir sirup.
Perubahan nilai kerapatan dan pH sirup pada tiap minggu penyimpanan dianalisis secara statistik dengan uji Independent-Sample T Test. Profil alir sirup diamati dari kurva hubungan antara penambahan beban dan perubahan kecepatan alir sirup, sedangkan tipe alir ditentukan dengan melihat ada tidaknya hubungan yang proporsional antara penambahan beban dan perubahan kecepatan alir sirup.
Hasil penelitian menunjukkan bahwa organoleptis kedua formula sirup perasan daging buah mahkota dewa tidak stabil selama penyimpanan. Sirup dengan 650 g sukrosa memiliki pH yang lebih stabil selama penyimpanan. Tetapi bila ditinjau dari segi kerapatan dan pengkristalan yang terjadi, sirup dengan campuran sukrosa 422,5 g - sorbitol 227,5 g memiliki stabilitas fisis lebih baik dibandingkan sirup dengan 650 g sukrosa. Tipe alir kedua formula sirup tidak mengalami perubahan selama penyimpanan.
ABSTRACT
Crown of God (Phaleria macrocarpa (Scheff.) Boerl.) fruit has been used in various traditional medications to cure many diseases. This fruit has many peculier properties. During this time, people consumed it in the form of squeeze but never been made in the form of syrup.
The purpose of this research is to compare the physical stability of syrup that made by 650 g sucrose and 422,5 g sucrose – 227,5 g sorbitol combination as the sweetening agents. The obtained result is about the examination data of syrup physical stability before and after the saving for 6 weeks. The examined syrup physical stability consists of organoleptic properties (colour, smell, clearity), crystallization, the density, pH, rheological properties of syrup.
The changing of density and pH value on weekly storage was analysed statistically with Independent-Sample T Test. The rheological type of syrup was observed from the connection curve between weight addition and the change of shearing rate, while the rheological type was determined by looking the availability of proportional connection between weight addition and the change of shearing rate of syrup which analysed statistically by using linear regression.
The result of this research shows that the organoleptic properties of the two formulas were unstable during storage of 6 weeks. The pH value of syrup using 650 g sucrose is more stable compared with syrup using 422,5 g sucrose-227,5 g sorbitol. Syrup which using sucrose 422,5 g-sorbitol sucrose-227,5 g as the sweetening agents doesn’t experience crystallization and has density value which more stable compared with syrup using 650 g sucrose. The rheological properties of the two formulas was stable during the storage of 6 weeks.
PERBANDINGAN STABILITAS FISIS SIRUP PERASAN DAGING BUAH MAHKOTA DEWA (Phaleria macrocarpa(Scheff.)Boerl.) YANG MENGANDUNG SUKROSA DAN CAMPURAN SUKROSA-SORBITOL
SEBAGAI BAHAN PEMANIS
Skripsi
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Diajukan oleh Brigitta Dharma Shanti
NIM : 02 8114 115
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
“ Janganlah kuatir akan hidupmu,
akan apa yang hendak kamu makan atau minum,
dan janganlah kuatir pula akan tubuhmu,
akan apa yang hendak kamu pakai…….”
“Tetapi Bapamu di surga tahu bahwa kamu memerlukan semuanya itu”
“Sebab itu janganlah kamu kuatir akan hari besok,
karena hari besok mempunyai kesusahannya sendiri.
Kesusahan sehari cukuplah untuk sehari.”
(Mat 6: 25-34)
Kupersembahkan Skripsiku ini kepada:
Tuhan Yesus Kristus dan Bunda Maria yang senantiasa menuntun jalan hidupku serta memberi kekuatan di saat ketidakberdayaanku.
(Alm) Bp. Ig. Sutanto dan Ibu C. Suransih, kedua orangtuaku tercinta, yang selalu mendukung dan ada untukku…ayah, terima kasih atas doa dan restunya dari surga..adik dah selesai lho….
Kedua kakakku tercinta: Mas Wiji dan Mas Nonok. Thank’s atas semuanya.
(Alm) Kakek dan nenekku…kek, terima kasih sudah menjagaku selama ini.
Semua oom, tante dan sepupuku Sahabat-sahabatku
PRAKATA
Puji syukur kepada Allah Bapa di surga atas segala berkat dan karunia
yang telah dianugerahkan kepada penulis sehingga penyusunan skripsi ini dapat
terselesaikan dengan baik.
Penyusunan skripsi ini tidak lepas dari bantuan dan dukungan berbagai
pihak, maka pada kesempatan ini penulis ingin mengucapkan terima kasih yang
sebesar-besarnya kepada:
1. Ibu Sri Hartati Yuliani, M.Si., Apt. selaku dosen pembimbing untuk semua
waktu, dukungan serta pengertian terhadap penulis selama penyusunan
skripsi ini.
2. Ibu Prof. Dr. Sri Sulihtyowati S., Apt. selaku dosen penguji yang telah
bersedia menguji dan memberikan saran kepada penulis.
3. Ibu Erna Tri Wulandari, M.Si., Apt. selaku dosen penguji yang telah
bersedia menguji dan memberikan saran kepada penulis.
4. Semua laboran dari laboratorium lantai satu sampai empat, terutama Pak
Mus, Mas Agung, Pak Iswandi, Mas Otok, Mas Sarwanto, Mas Sigit, Mas
Wagiran dan Mas Andre untuk kerelaannya berbagi waktu dan tenaga
selama penulis melakukan penelitian.
5. Semua pihak yang telah membantu penulis baik secara langsung maupun
Akhirnya, seperti kata pepatah ‘tak ada gading yang tak retak’, skripsi ini
pun tak lepas dari berbagai kekurangan dan kesalahan. Oleh karena itu, penulis
menerima masukan, kritik maupun saran yang membangun terhadap penulisan
DAFTAR ISI
Halaman
HALAMAN JUDUL ………i
HALAMAN PERSETUJUAN PEMBIMBING ………ii
HALAMAN PENGESAHAN ……….iii
HALAMAN PERSEMBAHAN ………..iv
PRAKATA ………v
PERNYATAAN KEASLIAN KARYA………..vii
DAFTAR ISI ………..viii
DAFTAR TABEL ………...xii
DAFTAR GAMBAR ……….…xiii
DAFTAR LAMPIRAN ………..xiv
INTISARI ……….…xv
ABSTRACT ……….…xvi
BAB I. PENDAHULUAN A. Latar Belakang ………1
1. Perumusan Masalah ………3
2. Keaslian Penelitian ………..3
3. Manfaat Penelitian ………..3
B. Tujuan Penelitian ………4
BAB II. PENELAAHAN PUSTAKA A. Mahkota Dewa ………5
C. Sirup ………..…..7
D. Metode Pembuatan Sirup ………7
1. Metode Pemanasan ………..7
2. Metode Agitasi Tanpa Pemanasan ………..9
3. Adisi Sukrosa ………..9
4. Perkolasi ………10
E. Bahan Tambahan dalam Sediaan Obat Cair Oral ……….10
1. Bahan Pemanis ………..10
2. Bahan Perasa ……….11
3. Bahan Pewarna ………..11
4. Pengawet ………...11
5. Buffer ………13
6. Antioksidan ………...13
F. Pemeriksaan stabilitas fisis sirup...………14
1. Penampilan, bau dan kejernihan………14
2. Kristalisasi ……….14
3. Kerapatan ………..14
4. pH ………..15
5. Profil dan Tipe Alir ………...15
G. Landasan Teori ………..18
H. Hipotesis ………19
B. Variabel Penelitian ………20
C. Definisi Operasional ………..21
D. Bahan dan Alat Penelitian ……….22
1. Bahan Penelitian ………22
2. Alat Penelitian ………...22
E. Tata Cara Penelitian ………..22
1. Pengumpulan buah mahkota dewa ………22
2. Determinasi buah mahkota dewa ………..23
3. Pembuatan perasan daging buah mahkota dewa ………...23
4. Penentuan dosis ……….23
5. Pembuatan sirup perasan daging buah mahkota dewa …………..24
6. Pemeriksaan stabilitas sirup perasan daging buah mahkota dewa………..25
a. Uji organoleptis sirup ……….25
b. Pengkristalan ………...25
c. Penentuan pH sirup ………26
d. Penentuan kerapatan sirup ………..26
e. Penentuan tipe alir sirup ……….28
F. Analisis Hasil ………28
BAB IV. HASIL PENELITIAN DAN PEMBAHASAN A. Pengumpulan bahan dan pembuatan perasan daging buah mahkota dewa………...30
C. Pembuatan sirup perasan daging buah mahkota dewa ………..31
D. Pemeriksaan stabilitas fisis sirup ………..33
1. Uji organoleptis sirup ………33
2. Pengkristalan ……….38
3. Penentuan kerapatan sirup ………39
4. Pengukuran pH sirup ………45
5. Penentuan profil dan tipe alir sirup ………...50
BAB V. KESIMPULAN DAN SARAN A. Kesimpulan ………...56
B. Saran ………..57
DAFTAR PUSTAKA ………..58
LAMPIRAN ……….60
DAFTAR TABEL
Halaman
Tabel I. Hasil uji organoleptis sirup selama 6 minggu penyimpanan ……..34
Tabel II. Hasil pengukuran kerapatan sirup ………..41
Tabel III. Nilai t hasil Independent-Sample T Test nilai kerapatan
sirup tiap minggu dibandingkan dengan nilai kerapatan sirup
pada awal penyimpanan ………..42
Tabel IV. Nilai Mean Difference hasil Independent-Sample T Test nilai
kerapatan sirup tiap minggu dibandingkan dengan nilai
kerapatan sirup pada awal penyimpanan ……….44
Tabel V. Data pengukuran nilai pH sirup selama penyimpanan ………46
Tabel VI. Nilai t hasil Independent-Sample T Test nilai pH sirup
tiap minggu dibandingkan dengan nilai pH sirup
pada awal penyimpanan………...47
Tabel VII. Nilai Mean Difference hasil Independent-Sample T Test nilai
pH sirup tiap minggu dibandingkan dengan nilai pH sirup
pada awal penyimpanan ………..49
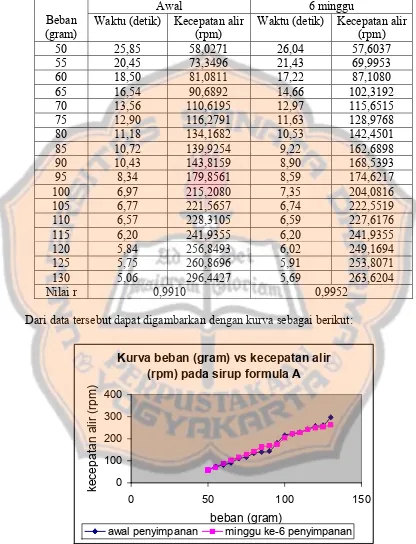
Tabel VIII. Data kecepatan alir pada tiap penambahan beban pada sirup
formula A……….51
Tabel IX. Data kecepatan alir pada tiap penambahan beban pada sirup
DAFTAR GAMBAR
Halaman
Gambar 1. Kurva hubungan beban (gram) vs kecepatan alir (rpm)
pada sirup formula A ………..51
Gambar 2. Kurva hubungan beban (gram) vs kecepatan alir (rpm) pada sirup formula B ………..52
Gambar 3. Foto tanaman mahkota dewa………60
Gambar 4. Foto buah mahkota dewa ……….60
Gambar 5. Foto perasan daging buah mahkota dewa ………...61
Gambar 6. Foto sirup perasan daging buah mahkota dewa formula A dan B…...62
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Foto-foto hasil penelitian ……….60
Lampiran 2. Surat pengesahan determinasi buah mahkota dewa……….63
Lampiran 3. Perhitungan kerapatan sirup perasan daging buah
mahkota dewa………...64
Lampiran 4. Hasil uji Independent-Sample T Test nilai kerapatan sirup
tiap minggu terhadap nilai kerapatan sirup pada
awal penyimpanan………68
Lampiran 5. Hasil uji Independent-Sample T Test nilai pH sirup tiap
minggu terhadap nilai pH sirup pada
INTISARI
Buah Mahkota Dewa banyak digunakan dalam berbagai pengobatan tradisional untuk mengobati berbagai penyakit. Buah ini memiliki banyak khasiat. Selama ini, masyarakat mengkonsumsinya antara lain dalam bentuk perasan dan belum pernah dalam sediaan sirup.
Penelitian ini bertujuan untuk membandingkan stabilitas fisis sirup yang dibuat dengan 650 g sukrosa dan campuran sukrosa 422,5 g – sorbitol 227,5 g sebagai bahan pemanis. Hasil yang diperoleh merupakan data pemeriksaan stabilitas fisis sirup sebelum dan sesudah penyimpanan selama 6 minggu penyimpanan. Stabilitas fisis sirup yang diamati meliputi keadaan organoleptis (warna, bau, rasa, kejernihan), pengkristalan, kerapatan, pH, profil dan tipe alir sirup.
Perubahan nilai kerapatan dan pH sirup pada tiap minggu penyimpanan dianalisis secara statistik dengan uji Independent-Sample T Test. Profil alir sirup diamati dari kurva hubungan antara penambahan beban dan perubahan kecepatan alir sirup, sedangkan tipe alir ditentukan dengan melihat ada tidaknya hubungan yang proporsional antara penambahan beban dan perubahan kecepatan alir sirup.
Hasil penelitian menunjukkan bahwa organoleptis kedua formula sirup perasan daging buah mahkota dewa tidak stabil selama penyimpanan. Sirup dengan 650 g sukrosa memiliki pH yang lebih stabil selama penyimpanan. Tetapi bila ditinjau dari segi kerapatan dan pengkristalan yang terjadi, sirup dengan campuran sukrosa 422,5 g - sorbitol 227,5 g memiliki stabilitas fisis lebih baik dibandingkan sirup dengan 650 g sukrosa. Tipe alir kedua formula sirup tidak mengalami perubahan selama penyimpanan.
ABSTRACT
Crown of God (Phaleria macrocarpa (Scheff.) Boerl.) fruit has been used in various traditional medications to cure many diseases. This fruit has many peculier properties. During this time, people consumed it in the form of squeeze but never been made in the form of syrup.
The purpose of this research is to compare the physical stability of syrup that made by 650 g sucrose and 422,5 g sucrose – 227,5 g sorbitol combination as the sweetening agents. The obtained result is about the examination data of syrup physical stability before and after the saving for 6 weeks. The examined syrup physical stability consists of organoleptic properties (colour, smell, clearity), crystallization, the density, pH, rheological properties of syrup.
The changing of density and pH value on weekly storage was analysed statistically with Independent-Sample T Test. The rheological type of syrup was observed from the connection curve between weight addition and the change of shearing rate, while the rheological type was determined by looking the availability of proportional connection between weight addition and the change of shearing rate of syrup which analysed statistically by using linear regression.
The result of this research shows that the organoleptic properties of the two formulas were unstable during storage of 6 weeks. The pH value of syrup using 650 g sucrose is more stable compared with syrup using 422,5 g sucrose-227,5 g sorbitol. Syrup which using sucrose 422,5 g-sorbitol sucrose-227,5 g as the sweetening agents doesn’t experience crystallization and has density value which more stable compared with syrup using 650 g sucrose. The rheological properties of the two formulas was stable during the storage of 6 weeks.
BAB I PENGANTAR
A. LATAR BELAKANG
Indonesia merupakan negara yang kaya akan berbagai macam tanaman
yang berkhasiat sebagai obat. Salah satu diantaranya adalah mahkota dewa.
Tanaman ini banyak digunakan dalam pengobatan tradisional karena memiliki
berbagai khasiat. Penyakit ringan seperti gatal-gatal, pegal-pegal atau flu hingga
penyakit berat antara lain kanker, diabetes, hipertensi dan asam urat dapat
disembuhkan oleh mahkota dewa.
Salah satu bagian dari tanaman mahkota dewa yang paling banyak
digunakan adalah buahnya, disamping daun dan batang. Buah mahkota dewa
terdiri dari tiga bagian, yaitu kulit dan daging buah, cangkang (batok biji), serta
biji. Dari ketiga bagian tersebut, bagian yang banyak dimanfaatkan adalah kulit
dan daging buah serta cangkangnya. Dalam keadaan segar, kulit dan daging buah
mahkota dewa terasa sepet agak pahit, sedangkan jika sudah tua terasa sepet agak
manis.
Salah satu cara penggunaan buah mahkota dewa untuk pengobatan
secara tradisional adalah dengan diperas. Air perasan tersebut kemudian diminum.
Secara organoleptis, perasan kulit dan daging buah mahkota dewa terasa pahit.
Rasa perasan yang pahit ini akan menimbulkan ketidaknyamanan bagi pasien
maka air perasan kulit dan daging buah mahkota dewa diolah dalam bentuk
sediaan sirup.
Sirup merupakan sediaan cair yang mengandung sukrosa tidak kurang
dari 64% dan tidak lebih dari 66% (Anonim, 1995). Sukrosa merupakan bahan
pemanis yang paling sering digunakan dalam pembuatan sirup. Masalah yang
sering timbul selama proses penyimpanan sirup adalah terjadinya cap-locking.
Cap-locking ini merupakan salah satu manifestasi dari kristalisasi sukrosa yang
ditandai dengan terbentuknya kristal pada leher dan tutup botol. Untuk mencegah
terjadinya cap-locking, sukrosa sering diganti ataupun dikombinasikan dengan
bahan lain seperti gliserin, sorbitol, dan propilen glikol.
Sorbitol merupakan suatu poliol (gula alkohol) yang stabil dan tahan
terhadap panas. Sorbitol dibuat dengan proses hidrogenasi glukosa dan tersedia
dalam bentuk cair maupun kristal. Selain berfungsi sebagai humektan dan
texturizing agent, bahan ini juga dapat berfungsi sebagai anti-crystallizing agent
sehingga diharapkan dapat menghambat laju kristalisasi sukrosa (Anonim,
2006b).
Stabilitas fisis sirup ditentukan dari ada tidaknya perubahan yang terjadi
terhadap kejernihan, warna, bau, rasa, pH, kerapatan, profil dan tipe alir. Selain
itu, juga dilihat dari ada tidaknya kristalisasi sukrosa.
Kombinasi sukrosa-sorbitol yang digunakan dalam penelitian ini
bertujuan untuk mengurangi kecenderungan sukrosa untuk mengkristal. Adanya
pengkristalan sukrosa bisa mempengaruhi nilai kerapatan sirup selama
diharapkan bisa membuat kerapatan sirup menjadi lebih stabil selama
penyimpanan. Namun, apakah dengan adanya penambahan sorbitol, sifat-sifat
fisis sirup yang meliputi: warna, bau, rasa, kejernihan, kerapatan, pH, profil dan
tipe alir menjadi lebih stabil selama penyimpanan ?
1. Perumusan masalah
Bagaimana perbandingan stabilitas fisis sirup perasan daging buah
mahkota dewa yang dibuat dengan 650 g sukrosa dan campuran sukrosa-sorbitol
dengan perbandingan 422,5 g sukrosa : 227,5 g sorbitol ?
2. Keaslian Penelitian
Sejauh penelusuran penulis, pembuatan sirup dari perasan daging buah
Mahkota Dewa belum pernah dilakukan penelitian. Penelitian yang pernah
dilakukan adalah : Wijayanti (2002), Sumastuti (2001), Sisilia (2001), Bestari
(2001) dan Saragih (2001).
3. Manfaat Penelitian
1. Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi tentang
penggunaan campuran sukrosa-sorbitol sebagai bahan pemanis dalam
formulasi sirup perasan daging buah mahkota dewa.
2. Manfaat teoritis
Penelitian ini diharapkan dapat bermanfaat dalam mengembangkan
bidang ilmu kefarmasian terutama dalam formulasi sediaan obat
B. TUJUAN PENELITIAN
Mengetahui perbandingan stabilitas fisis sediaan sirup perasan daging buah
mahkota dewa (yang meliputi: kejernihan, warna, rasa, bau, pengkristalan,
kerapatan, pH serta profil dan tipe alir), yang dibuat dengan 650 g sukrosa dan
campuran sukrosa-sorbitol dengan perbandingan 422,5 g sukrosa : 227,5 g
BAB II
PENELAAHAN PUSTAKA A. Mahkota Dewa
Tanaman ini tumbuh baik di tanah yang gembur dengan bahan organik
yang tinggi pada ketinggian 10-1.200 m di atas permukaan air laut. Penyusun
utama bahan organik adalah unsur karbon. Kedudukan tanaman makuto dewo
dalam sistematika tumbuhan adalah:
Kingdom :Plantae
Divisi :Spermatophyta
Sub divisi :Angiospermae
Kelas :Dikotiledonae
Sub kelas :Archiclhamidae
Bangsa :Thymeleales
Suku :Thymelaceae
(Backer and Backhuizen van den Brink, 1963)
Mahkota Dewa mempunyai nama yang berbeda menurut tempat
tumbuhnya. Di jawa disebut sebagai : Makuto dewo, Makuto rojo, Makuto ratu,
Simalakama. Di Banten disebut Raja obat, dan di Indonesia mempunyai nama
nasional Mahkota dewo (Budiana, 2001).
Kulit dan daging buah mahkota dewa mengandung senyawa alkaloid,
saponin, dan flavonoid (Anonim, 1999a).
Bagian dari tanaman yang banyak dimanfaatkan adalah buahnya. Bagian
khasiat untuk menyembuhkan disentri, eksim, penyakit kulit, dan anti-tumor.
Secara tradisional, dosis yang digunakan adalah tiga buah untuk sehari, direbus
atau diperas. Rebusan buahnya digunakan untuk obat sakit lever, ginjal, tekanan
darah tinggi, dan spasmofilia. Sebagai obat luar, buah dan biji Mahkota Dewa
berkhasiat mengatasi luka, gatal kulit, hingga eksim (Anonim, 2001).
Daun dan kulit buah mahkota dewa mengandung alkaloid, saponin, dan
flavonoid. Selain itu, di dalam daunnya juga terkandung polifenol. Seorang ahli
farmakologi dari Fakultas Kedokteran UGM, dr. Regina Sumastuti, berhasil
membuktikan bahwa mahkota dewa mangandung zat antihistamin. Zat ini
merupakan penangkal alergi (Harmanto, 2005).
B. Pemerasan
Pemisahan cairan dari material padat (seperti buah atau daun) dapat
menggunakan metode peras. Pemerasan dalam teknologi farmasi dijumpai pada
pembuatan sari jamu, dengan maksud agar larutan perasan dapat tepisahkan dari
bahan padat pengotor atau yang tidak diinginkan. Cairan yang diperoleh dengan
cara peras umumnya dibebaskan dari pertikel-partikel kecil melalui cara
penyaringan. Perasan mengandung seluruh bahan yang terkandung dalam
tumbuhan segar, dan yang tertinggal hanyalah bahan yang tidak terlarut
C. Sirup
Sirup adalah larutan yang digunakan secara oral, merupakan sediaan cair
yang mengandung larutan sukrosa (tidak kurang dari 64,0 % dan tidak lebih dari
66,0 % sukrosa) atau gula lain kadar tinggi dengan bahan pengaroma atau
pewarna yang larut dalam air atau campuran kosolven air (Anonim, 1995). Sirup
yang mengandung bahan perasa tanpa mengandung zat aktif disebut “
flavoring/flavored syrup”, sedangkan yang mengandung zat aktif disebut dengan
“medicated syrup” atau sirup obat (Ansel, 1969). Larutan sukrosa hampir jenuh
dalam air dikenal sebagai sirup atau sirup simpleks. Penggunaan istilah sirup juga
digunakan untuk bentuk sediaan cair lain yang dibuat dengan pengental dan
pemanis, termasuk suspensi oral (Anonim, 1995).
Sirup obat dapat dibuat dengan mencampur bahan-bahan, seperti
sukrosa, air murni, bahan pengaroma, bahan pewarna, zat aktif serta bahan lain
yang dibutuhkan dalam pembuatan sirup (Ansel, 1969).
D. Metode Pembuatan Sirup
Sirup dapat dibuat dengan berbagai metode. Pemilihan metode ini
tergantung dari sifat fisika-kimia dari bahan-bahan yang akan digunakan. Secara
umum, ada 4 metode pembuatan sirup, yaitu: metode pemanasan, agitasi tanpa
pemanasan, adisi sukrosa dalam larutan berasa, perkolasi (Ansel, 1969).
1. Metode pemanasan
Pembuatan sirup dengan bantuan pemanasan dilakukan bila dibutuhkan
rusak dengan adanya pemanasan. Pada metode ini, biasanya sukrosa ditambahkan
ke dalam air lalu dipanaskan hingga gula larut. Pemanasan ini akan mempercepat
kelarutan gula. Bahan-bahan lain yang tahan panas kemudian ditambahkan ke
dalam larutan sukrosa yang masih panas. Campuran tersebut kemudian
didinginkan dan ditambah air hingga volume sirup yang dikehendaki. Jika
terdapat bahan-bahan yang tidak tahan terhadap panas/mudah menguap, misal:
minyak atsiri, alkohol, maka bahan-bahan tersebut ditambahkan ke dalam larutan
sukrosa yang telah didinginkan.
Pemanasan yang dilakukan bisa mempercepat kelarutan sukrosa serta
komponen lain yang digunakan dalam pembuatan sirup. Sukrosa, suatu
disakarida, bisa terhidrolisis menjadi monosakarida, dekstrosa (glukosa), dan
fruktosa (levulosa). Reaksi hidrolisis ini disebut inversi, dan kombinasi dari 2
monosakarida disebut gula invert. Inversi sukrosa dapat terjadi saat pemanasan
selama proses pembuatan sirup berlangsung.
Inversi sukrosa meningkat dengan adanya senyawa-senyawa asam. Hal
ini disebabkan karena ion hidrogen dari senyawa asam berfungsi sebagai katalis
dalam reaksi hidrolisis (inversi) tersebut. Peristiwa inversi menyebabkan tingkat
kemanisan sirup berubah dan warnanya menjadi lebih gelap. Sirup dengan
keadaan tersebut akan lebih mudah mengalami fermentasi dan ditumbuhi
mikroorganisme dibandingkan dengan sirup yang tidak mengalami penguraian.
Karena adanya kemungkinan terjadi peristiwa inversi akibat penggunaan panas,
sirup tidak bisa disterilisasi menggunakan autoklaf. Penggunaan air bersih yang
kestabilannya dan bila diperlukan dapat dilakukan penambahan bahan pengawet
untuk melindunginya selama penyimpanan. Penyimpanan sirup sebaiknya dalam
wadah yang tertutup rapat.
2. Metode agitasi tanpa pemanasan
Metode ini digunakan untuk mencegah terjadinya inversi terhadap
sukrosa karena adanya pemanasan. Sirup dalam skala volume yang kecil dapat
dibuat dengan metode ini. Sirup dibuat dengan melarutkan sukrosa dan
bahan-bahan lainnya ke dalam air yang ditampung dalam botol dengan kapasitas volume
yang lebih besar daripada volume sirup yang akan dibuat. Sukrosa akan lebih
lama larut bila menggunakan metode ini dibandingkan dengan bantuan pemanasan
tetapi stabilitas produk yang dihasilkan akan lebih maksimal.
3. Adisi sukrosa dalam medicated liquid atau flavored liquid
Tinktur dan ekstrak cair sering digunakan dalam preparasi/pembuatan
sirup. Sebagian besar tinktur dan ekstrak cair mengandung komponen-komponen
yang larut dalam alkohol. Jika komponen-komponen tersebut tidak dikehendaki
ada di dalam sirup, maka dilakukan proses pemisahan. Caranya adalah dengan
mencampur tinktur atau ekstrak cair dengan air lalu didiamkan hingga
komponen-komponen yang tidak larut dalam air memisah. Setelah pemisahan terjadi
sempurna lalu dilakukan penyaringan, sehingga diperoleh filtrat. Selanjutnya,
4. Perkolasi
Pada metode ini, sukrosa dapat diperkolasi untuk dibuat sirup atau bahan
yang mengandung zat aktif diperkolasi menjadi ekstrak dan sukrosa dapat
ditambahkan ke dalamnya. (Ansel, 1969)
E. Bahan Tambahan dalam Sediaan Obat Cair Oral 1. Bahan pemanis (Sweetening Agents)
Bahan ini berguna untuk menutupi rasa pahit atau rasa yang tidak enak.
Pemanis yang biasa digunakan, antara lain : sukrosa, sorbitol, manitol, cairan
glukosa, madu, sakarin dan aspartam (Ansel,1969).
Sukrosa merupakan bahan pemanis yang paling banyak digunakan.
Sukrosa berupa serbuk kristal putih, larut dalam air dan alkohol. Sukrosa stabil
secara fisik maupun kimia pada pH 4,0 sampai 8,0. Bahan ini akan menghambat
pertumbuhan mikroorganisme dalam larutan pada konsentrasi di atas 65% b/b
dengan mengurangi koefisien aktivitas air. Selama proses pembuatan larutan
sukrosa perlu adanya perhatian khusus untuk mencegah terjadinya karamelisasi
sukrosa karena adanya panas. Sukrosa sering dikombinasikan dengan sorbitol,
gliserin, dan poliol lain untuk mengurangi terjadinya kristalisasi sukrosa (Ansel,
1969). Sukrosa memiliki berat molekul 342,30 (Anonim, 1995).
Sorbitol termasuk suatu poliol (gula alkohol) yang mempunyai tingkat
kemanisan sekitar 60% dari sukrosa. Sorbitol mengandung kalori yang lebih
rendah dari sukrosa. Di alam, sorbitol banyak ditemukan di buah-buahan dan
dalam bentuk cair dan kristal (Anonim, 2006b). Bahan ini memiliki stabilitas yang
baik dan saat digunakan dalam pemakaian oral tidak akan menyebabkan
peningkatan kadar gula darah. Oleh karena itu, sorbitol bisa digunakan dalam
formulasi sirup sederhana untuk penderita diabetes. Dalam penyimpanan,
penggunaan sorbitol ini bisa mencegah terjadinya kristalisasi (Carter, 1975).
Sorbitol memiliki berat molekul 182,17 (Anonim, 2006b).
2. Bahan perasa (Flavoring Agents)
Penggunaan bahan pemanis mungkin tidak mampu menutupi rasa yang
tidak diinginkan pada sediaan. Dalam hal ini dapat diatasi dengan menggunakan
bahan perasa atau flavoring agents. Bahan perasa dapat berupa bahan alam
maupun sintetik. Bahan alam yang bisa digunakan sebagai bahan perasa adalah
sari buah, minyak-minyak aromatis seperti peppermint, herba dan rempah-rempah
(Aulton, 2002).
3. Bahan pewarna (Coloring Agents)
Bahan pewarna yang digunakan disesuaikan dengan rasa yang
diinginkan untuk sediaan, misalnya warna kuning untuk rasa jeruk dan merah
untuk rasa cheery (Swarbick, J. and Boylan, C.J., 1994). Bahan pewarna dapat
dibedakan menjadi pewarna dari bahan alam dan pewarna sintetik. Pewarna
sintetik menghasilkan warna yang lebih terang dan biasanya lebih stabil
dibandingkan pewarna dari bahan alam (Aulton, 2002).
4. Pengawet (Preservatives)
Sebagian besar sediaan cair oral bukan merupakan produk steril
besar dari sediaan ini juga digunakan sebagai obat dosis ganda sehingga resiko
terkontaminasi oleh mikroba sangat besar. Proses pembuatan juga memungkinkan
terjadinya kontaminasi mikroorganisme. Oleh karena itu, perlu adanya bahan
pengawet untuk melindungi produk dari mikroorganisme. (Swarbick, J. and
Boylan, C.J., 1994).
Bahan pengawet harus memenuhi beberapa kriteria tertentu. Faktor
utama adalah menyangkut keamanan dan toksisitasnya sesudah pemakaian per
oral, terutama karena sediaan obat cair sering diberikan kepada anak-anak dan
lansia. Bahan pengawet harus larut, stabil, aktif secara mikrobiologi, dan dapat
campur (compatible) dengan bahan-bahan lainnya. Namun pada kenyataannya,
bahan pengawet yang memenuhi semua kriteria di atas sulit ditemukan. Oleh
karena itu, sering diperlukan kombinasi 2 atau lebih bahan pengawet (Swarbick, J.
and Boylan, C.J., 1994).
Jumlah bahan pengawet yang diperlukan untuk melindungi sirup dari
kontaminasi mikroorganisme bervariasi tergantung pada jumlah air yang tersedia
untuk media tumbuh mikroorganisme, sifat antimikroba yang memang dimiliki
oleh bahan yang diformulasikan dan kemampuan antimikroba itu sendiri (Ansel,
1969).
Bahan pengawet yang banyak digunakan misalnya bentuk garam dari
asam benzoat. Bahan pengawet ini dapat larut dalam air dan dapat berfungsi baik
5. Buffer
Perubahan pH suatu sediaan bisa terjadi selama penyimpanan karena
adanya reaksi degradasi dalam produk, interaksi dengan komponen dari wadah
atau karena adanya disolusi gas dan uap air. Untuk mencegahnya, ditambahkan
buffer untuk menstabilkan pH. Sistem buffer ini harus mempunyai kapasitas yang
cukup baik untuk mempertahankan pH produk selama penyimpanan. Pemilihan
buffer didasarkan pada profil pH dari obat dalam larutan. Buffer yang biasa
digunakan adalah asetat, sitrat, fosfat dan glutamat. Meskipun buffer akan
mempertahankan kestabilan pH, tetapi buffer juga bisa berpengaruh terhadap
bahan lain, misal dalam hal kelarutan. (Swarbick, J. and Boylan, C.J., 1994).
Penggunaan buffer juga bertujuan untuk meningkatkan stabilitas sediaan, karena
pH yang tidak stabil bisa menyebabkan terjadinya dekomposisi senyawa aktif
yang terdapat dalam sediaan solutio (Carter, 1975).
6. Antioksidan
Banyak obat dalam larutan bisa mengalami degradasi karena reaksi
oksidasi. Reaksi ini karena adanya radikal bebas atau molekul oksigen. Suatu
senyawa yang memiliki potensi oksidasi lebih rendah dari obat disebut
antioksidan. Antioksidan ini bisa ditambahkan ke dalam larutan dalam bentuk
tunggal maupun kombinasi dengan chelating agent atau antioksidan lain dan
berfungsi dengan cara teroksidasi terlebih dahulu saat akan dikonsumsi atau
menghambat reaksi oksidasi saat tidak dikonsumsi. Sulfat merupakan antioksidan
F. Pemeriksaan stabilitas fisis sirup
Pemeriksaan stabilitas fisis sirup dapat dilakukan dengan melakukan
pemeriksaan terhadap ada tidaknya perubahan penampilan, bau, kejernihan,
kerapatan, pH serta profil dan tipe alir selama penyimpanan. Selain itu, juga
dilakukan pengamatan terhadap ada tidaknya kristalisasi sukrosa yang terjadi.
1. Penampilan, bau dan kejernihan
Kejernihan, warna, bau dan rasa suatu larutan harus tetap terjaga selama
penyimpanan. Pemeriksaan terhadap kejernihan dan warna dapat dilakukan
dengan pengamatan secara visual (Aulton, 2002).
2. Kristalisasi
Kristalisasi sukrosa sering timbul selama proses penyimpanan sirup.
Salah satu manifestasinya adalah dengan terbentuknya cap-locking, yaitu
terbentuknya kristal-kristal gula pada leher dan tutup botol (Swarbick, J. and
Boylan, C.J., 1994).
3. Kerapatan
Kerapatan adalah massa per unit volume suatu zat pada temperatur
tertentu. Hubungan antara massa dan volume tidak hanya menunjukkan ukuran
dan bobot molekul suatu komponen tetapi juga gaya-gaya yang mempengaruhi
sifat karakteristik pemadatan.
Bobot jenis didefinisikan sebagai ratio kerapatan suatu zat terhadap
kerapatan air pada suhu 4o C atau kerapatan suatu zat terhadap kerapatan air pada
suhu yang sama. Bobot jenis merupakan suatu karakteristik bahan yang penting,
pembantu, khususnya sifat cairan. Penentuan bobot jenis dilakukan dengan
menggunakan metode piknometer, aerometer, timbangan hidrostatik (timbangan
Mohr-Westphal) dan cara manometrik (Voigt, 1995).
4. pH
Power of Hydrogen (pH) atau derajat keasaman digunakan untuk
menyatakan tingkat keasaman atau basa yang dimiliki oleh suatu zat, larutan atau
benda. pH penting dalam formulasi produk obat terkait antara lain dengan
kelarutan obat, kenyamanan pasien. Peningkatan atau penurunan pH bisa
menyebabkan obat dalam larutan mengalami presipitasi. Nilai pH dikatakan
normal jika memiliki nilai 7 sementara bila nilai pH > 7 menunjukkan zat tersebut
memiliki sifat basa sedangkan nilai pH < 7 memiliki sifat asam. Nilai pH 0
menunjukkan derajat keasaman tertinggi, dan pH 14 menunjukkan derajat
kebasaan tertinggi. Umumnya indikator sederhana yang digunakan adalah kertas
lakmus yang berubah menjadi merah bila keasamannya tinggi dan biru bila
keasamannya rendah Selain menggunakan kertas lakmus, indikator asam basa
dapat diukur dengan pH meter yang bekerja berdasarkan prinsip elektrolit suatu
larutan (Anonim, 2006a).
5. Profil dan tipe alir
Istilah rheologi berasal dari bahasa Yunani yaitu rheo yang berarti
mengalir dan logos yang berarti ilmu; digunakan untuk menggambarkan aliran
cairan dan deformasi suatu padatan. Viskositas adalah tahanan suatu cairan untuk
mengalir; semakin tinggi viskositasnya maka makin besar tahanannya (Martin et
pengemasan, pemakaian, konsistensi, dan stabilitas sediaan farmasi (Aulton,
2002).
Sifat alir adalah ratio antara gaya gesek dan sifat gesek. Berdasarkan tipe
alir dan deformasinya, suatu bahan dapat diklasifikasikan termasuk bahan dengan
tipe alir Newtonian dan non-Newtonian tergantung apakah sifat aliran bahan
tersebut sesuai dengan hukum Newton atau tidak (Martin et all, 1983).
Bahan yang termasuk tipe alir Newtonian, memiliki sifat alir yang sesuai
dengan hukum Newton dimana adanya kenaikan gaya gesek (shearing stress)
akan menyebabkan kenaikan kecepatan gesek (shearing rate) yang proporsional.
Semakin besar viskositas cairan suatu cairan, akan makin besar pula shearing
stress yang diperlukan untuk menghasilkan rate of shear tertentu. Oleh karena itu,
rate of shear berbanding langsung dengan shearing stress atau
η = F / G
dimana η : viskositas, F: shearing stress dan G: rate of shear (Martin dkk, 1993).
Banyak alat yang bisa digunakan untuk menentukan sifat alir dari bahan dengan
tipe alir Newtonian, seperti: viskometer Ostwald, suspended-level viscometer dan
falling-sphere viscometer. Namun, tidak semua alat tersebut bisa digunakan untuk
mengukur viskositas (Aulton, 2002).
Bahan yang sifat alirannya tidak mengikuti hukum Newton termasuk
dalam sistem non-Newtonian. Viskositas bahan akan berubah dengan adanya nilai
kecepatan gesek (shearing rate) yang bervariasi. Sistem non-Newtonian dapat
a) Tipe alir plastik
Kurva pada tipe alir plastik tidak melalui titik nol tetapi bergeser ke
kanan dan jika bagian kurva yang lurus diekstrapolasikan terhadap sumbu x
akan memotong pada suatu titik tertentu yang disebut “ Yield value”. Jika gaya
yang diberikan lebih kecil daripada yield value maka bahan yang bersangkutan
tidak akan mengalir dan berkelakuan sebagai zat yang elastik/zat padat
(Aulton, 2002). Contoh cairan yang memiliki tipe alir plastik: saus tomat
(Anonim, 1999b).
b) Tipe alir pseudoplastik
Bahan dengan tipe alir ini akan segera mengalir setelah diberikan gaya
gesek. Viskositas bahan akan menurun dengan adanya penambahan gaya
gesek (Aulton, 2002). Tipe alir pseudoplastik sering disebut dengan tipe
“shear-thinning”. Contoh cairan yang memiliki tipe alir pseudoplastik: cat,
emulsi (Anonim, 1999b).
c) Tipe alir dilatant
Tipe alir ini merupakan kebalikan dari tipe alir pseudoplastik. Adanya
penambahan gaya gesek (shearing stress) akan meningkatkan viskositas bahan
yang bersangkutan (Aulton, 2002). Contoh cairan yang memiliki tipe alir
dilatant: larutan amilum dalam air dan pasir dalam air. Tipe alir dilatant sering
G. Landasan Teori
Bahan utama yang digunakan dalam penelitian ini adalah perasan daging
buah mahkota dewa. Perasan tersebut mengandung berbagai zat aktif yang
terdapat dalam daging buah mahkota dewa dan berasa pahit. Untuk menutupi rasa
pahit tersebut, maka perasan daging buah mahkota dewa dibuat dalam bentuk
sediaan sirup. Sirup mengandung larutan sukrosa tidak kurang dari 64,0 % dan
tidak lebih dari 66,0 %.
Pemeriksaan stabilitas fisis sirup dilakukan dengan melakukan
pemeriksaan terhadap perubahan yang terjadi terhadap sifat-sifat fisis sirup selama
penyimpanan. Pemeriksaan sifat-sifat fisis sirup tersebut meliputi pemeriksaan
terhadap warna, rasa, bau, kejernihan, kristalisasi, kerapatan, pH dan profil serta
tipe alir sirup selama penyimpanan.
Sukrosa merupakan bahan pemanis yang paling banyak digunakan.
Namun demikian, bahan ini mudah mengalami karamelisasi dengan adanya panas
dan juga mudah mengkristal. Pengkristalan sukrosa ini bisa mempengaruhi
sifat-sifat fisis sirup seperti kerapatan.
Sorbitol merupakan salah satu zat tambahan yang bisa dikombinasikan
dengan sukrosa. Bahan ini juga bisa berfungsi sebagai anti-crystallizing agent.
Penambahan sorbitol dalam pembuatan sirup dari perasan daging buah mahkota
dewa ini, diharapkan mampu mengurangi kemungkinan terjadinya pengkristalan
sukrosa. Adanya penghambatan terhadap kristalisasi sukrosa diharapkan bisa
memperbaiki sifat-sifat fisis sirup seperti warna, bau, rasa, kejernihan, kerapatan,
H. Hipotesis
Campuran sukrosa-sorbitol yang digunakan sebagai bahan pemanis
diduga bisa menghambat kristalisasi sukrosa dan memperbaiki sifat-sifat fisis
sirup perasan daging buah mahkota dewa yang meliputi: warna, bau, rasa,
BAB III
METODOLOGI PENELITIAN
A. Jenis Penelitian
Penelitian ini termasuk dalam jenis penelitian eksperimental murni.
B. Variabel Penelitian
1. Variabel bebas
Komposisi bahan pemanis, yaitu sukrosa dan sorbitol, yang digunakan
dalam pembuatan sirup dari perasan daging buah mahkota dewa.
2. Variabel tergantung
Stabilitas fisis sediaan sirup perasan daging buah mahkota dewa yang
dihasilkan, meliputi keadaan warna, bau, rasa, kejernihan, nilai kerapatan, pH,
profil dan tipe alir sirup.
3. Variabel terkendali
- Buah mahkota dewa : buah mahkota dewa yang digunakan sudah masak,
berwarna merah tua, diperoleh dari salah seorang pedagang di pasar
Beringharjo, Yogyakarta.
- Jenis alat dan bahan yang digunakan, seperti: sukrosa, sorbitol, bahan pewarna
sekaligus perasa frambozen.
- Jumlah perasan daging buah mahkota dewa, yaitu sebanyak 150 ml untuk
4. Variabel pengacau tak terkendali
- Panas yang tidak terukur untuk melarutkan sukrosa saat pembuatan sirup
perasan daging buah mahkota dewa.
- Kadar sukrosa pada sirup perasan daging buah mahkota dewa setelah proses
penyaringan.
C. Definisi Operasional
1. Sirup merupakan larutan yang digunakan secara per oral, berupa sediaan cair
yang mengandung larutan sukrosa (tidak kurang dari 64,0 % dan tidak lebih
dari 66,0 %) atau gula lain kadar tinggi dengan bahan pengaroma atau
pewarna yang larut dalam air atau campuran kosolven air (Anonim, 1995).
2. Perasan daging buah mahkota dewa: air perasan yang diperoleh dari hasil
memeras daging buah mahkota dewa menggunakan juicer. Tiga buah mahkota
dewa menghasilkan air perasan sekitar 15 ml.
3. Eksipien merupakan bahan tambahan yang digunakan dalam pembuatan sirup,
antara lain: bahan pemanis, perasa, pengawet.
4. Pemeriksaan stabilitas fisis sirup meliputi pemeriksaan terhadap warna, bau,
rasa, kejernihan, kristalisasi sukrosa, kerapatan, pH, profil dan tipe alir sirup.
5. Sirup dikatakan stabil jika :
a). warna, bau, dan rasanya tidak mengalami perubahan selama penyimpanan
b). tetap jernih selama penyimpanan
d). nilai kerapatan dan pH-nya tidak mengalami perubahan yang bermakna
secara statistik selama penyimpanan
e). profil dan tipe alirnya tidak berubah selama penyimpanan.
6. Mean difference merupakan selisih antara rata-rata nilai kerapatan atau pH
sirup pada tiap minggu penyimpanan dengan rata-rata nilai kerapatan atau pH
sirup pada awal penyimpanan. Semakin besar nilai selisihnya menunjukkan
bahwa sirup semakin tidak stabil.
D. Bahan dan Alat Penelitian
1. Bahan : perasan daging buah mahkota dewa, sukrosa, sorbitol ( produksi PT.
Brataco, Indonesia), aqudest, asam benzoat (produksi PT. Brataco, Indonesia),
bahan pewarna sekaligus perasa frambozen merk Zender.
2. Alat : Alat-alat gelas Merk TE 32 Pyrex (bekker glass, gelas ukur, pengaduk,
pipet, corong), Juicer Kirin KJE-350, Stirrer, Kain kassa putih bersih,
Piknometer 10 ml Merk Duran, pH meter HI 9024/HI 9025, Hotplate,
Viskometer Stomer, Timbangan analitik, Botol wadah, Stopwatch, oven merk
WTC Binder.
E. Tata Cara Penelitian 1. Pengumpulan buah Mahkota Dewa
Bahan yang digunakan yaitu buah mahkota dewa yang sudah masak dan
2. Determinasi buah mahkota dewa
Determinasi buah mahkota dewa dilakukan di laboratorium
farmakognosi fitokimia USD dengan menggunakan Atlas Tumbuhan Obat
Indonesia (Dalimartha, 2003).
3. Pembuatan perasan
Buah mahkota dewa yang sudah masak dan berwarna merah tua menyala
yang masih segar dicuci dengan air mengalir hingga bersih, kemudian daging
buahnya dipotong-potong, dibuang bijinya, dan dimasukkan ke dalam juicer. Air
perasan yang diperoleh dikumpulkan untuk pembuatan sirup.
4. Penentuan dosis
Penentuan kisaran dosis mahkota dewa didasarkan pada dosis
pengobatan yang digunakan dalam masyarakat, yaitu 3 buah mahkota dewa
diperas airnya untuk penggunaan 1 hari. Tiga buah mahkota dewa diambil daging
buahnya dengan berat 70 g untuk manusia Indonesia 50 kg. Perasan yang
dihasilkan dari 70 gram buah mahkota dewa tersebut yaitu sekitar 15 ml. Jadi
dosis penggunaan mahkota dewa untuk 1 hari dalam bentuk perasan yaitu 15 ml
untuk 50 kg manusia Indonesia. Perasan daging buah sebanyak 15 ml digunakan
untuk 100 ml sirup. Perhitungan dosisnya sebagai berikut:
15 ml perasan → untuk 100 ml sirup
→ konsentrasi perasan dalam sirup 15 ml/100 ml
15 ml/100 ml sirup → diminum 3x sehari
1x minum →± 30 ml atau 2 sendok makan
5. Pembuatan sirup
Formula umum sirup yang digunakan adalah sebagai berikut:
Sukrosa………..650 g
Perasan daging buah mahkota dewa……..150 ml
Asam benzoat………1,5 g
Bahan perasa frambozen……….50 ml
Air ad………..1000 ml
Masing-masing formula dibuat sirup sebanyak 1000 ml.
Dalam pembuatan sirup dari perasan daging buah mahkota dewa ini
dibuat dua formula sirup. Kedua formula sirup terdiri dari formula A yang
menggunakan 650 g sukrosa sebagai bahan pemanis dan formula B yang
menggunakan campuran sukrosa-sorbitol sebagai bahan pemanis. Komposisi
sukrosa-sorbitol yang digunakan adalah sbb:
Formula A B
Sukrosa 650 g 422,5 g
Sorbitol - 227,5 g
Pemilihan kedua formula sirup tersebut bertujuan untuk mengetahui dan
membandingkan sifat-sifat fisis sirup antara sirup yang mengandung 100%
sukrosa dengan sirup yang mengandung sukrosa-sorbitol sebagai bahan pemanis.
Sukrosa, menurut Farmakope Indonesia III, termasuk sangat mudah
larut, yaitu 1 g zat dapat larut dalam pelarut kurang dari 1 bagian. Berdasarkan hal
tersebut maka sirup dibuat dengan melarutkan sukrosa dalam air dengan bantuan
pemanasan lalu ditambahkan sorbitol. Larutan sukrosa-sorbitol yang sudah jadi
asam benzoat yang sudah dilarutkan dalam air dan bahan pewarna sekaligus
perasa frambozen. Campuran tersebut kemudian ditambah air hingga 1000 ml dan
dilakukan penyaringan menggunakan kain kassa yang masih bersih. Sirup tersebut
kemudian dimasukkan ke dalam botol-botol dan selanjutnya pemeriksaan
stabilitas sirup.
6. Pemeriksaan stabilitas sirup
Pemeriksaan stabilitas fisis sediaan sirup mahkota dewa dilakukan
sebelum penyimpanan dan sesudah penyimpanan. Pemeriksaan stabilitas fisis
sirup ini dilakukan setiap minggu selama 6 minggu penyimpanan untuk
mengetahui perubahan sifat fisis sirup yang terjadi pada tiap minggu penyimpanan
sehingga bisa digunakan untuk mengetahui kapan sirup mulai menunjukkan
ketidakstabilannya. Pemeriksaan stabilitas yang dilakukan meliputi :
a. Uji organoleptis sirup
Uji organoleptis sirup yang dilakukan meliputi pengamatan terhadap warna
dan kejernihan serta penentuan bau dan rasa sirup. Pengamatan terhadap warna
dan kejernihan dilakukan secara visual. Penentuan bau dan rasa sirup dengan cara
menghirup bau dan mencicipi sirup secara langsung oleh satu orang secara
subyektif.
b. Pengkristalan
Kristalisasi pada sirup diamati secara visual yaitu terbentuknya kristal pada
bagian leher dan tutup botol. Pengamatan dilakukan oleh satu orang secara
c. Penentuan pH sirup
Nilai pH sirup ditentukan dengan menggunakan pH-meter HI 9024/HI
9025. Sebelum digunakan, alat ini perlu dikalibrasi terlebih dahulu dengan
menggunakan larutan buffer yang telah tersedia. Langkah pertama adalah
menekan tombol power pada posisi ON. Tekan tombol CAL maka pada layar
akan terdisplay CAL. Layar juga akan mendisplay nilai dari larutan buffer
“4,01” pH, untuk mengubahnya tekan “ C” atau “ C”. Untuk memulai
kalibrasi, menggunakan larutan buffer dengan pH 7 dahulu kemudian dengan
larutan dengan pH 4. Masukkan elektroda ke dalam larutan buffer 7. Tunggu
selama 30 detik hingga tanda CON muncul dan berkedip-kedip kemudian
tekan tombol CON. Kalibrasi pertama selesai, kemudian elektroda dicuci
dengan aquadest. Gunakan tanda “ C” untuk memperoleh nilai pH yang sama
atau mendekati dengan nilai pH larutan buffer kedua (pH 4) kemudian
elektroda dimasukkan ke dalam larutan buffer kedua. Tunggu 30 detik hingga
layar mendisplay tanda CON, tekan tombol CON. Setelah kalibrasi selesai
elektroda dicuci dan dimasukkan ke dalam sirup untuk mengukur pH sirup.
d. Penentuan kerapatan sirup
i. Penentuan volume piknometer
Timbang piknometer yang bersih dan kering dengan seksama
kemudian isi dengan aquadest hingga penuh lalu rendam dalam air es
sehingga suhunya ±20 C di bawah suhu percobaan (250 C). Piknometer
ditutup, pipa kapiler dibiarkan terbuka dan suhu air dibiarkan naik sampai
suhu air dalam piknometer mencapai suhu kamar, lalu air yang berada di
luar piknometer diusap sampai bersih kemudian ditimbang dengan
seksama. Untuk menghitung volume piknometer (volume air) perlu
diketahui kerapatan air pada suhu percobaan.
Cara perhitungannya :
Misalnya : bobot piknometer + air = a + b gram
bobot piknometer kosong = a gram
bobot air = b gram
dari tabel diketahui kerapatan air = ρair
volume air = volume piknometer = Vp =
(g/ml) (g) b
air
ρ
ii. Penentuan kerapatan sirup
Timbang piknometer yang bersih dan kering dengan seksama
kemudian isi dengan sirup hingga penuh lalu rendam dalam air es
sehingga suhunya ±20C di bawah suhu percobaan (250C). Piknometer
ditutup, pipa kapiler dibiarkan terbuka dan suhu sirup dibiarkan naik
sampai mencapai suhu percobaan, lalu pipa kapiler piknometer ditutup.
Biarkan suhu sirup dalam piknometer mencapai suhu kamar, lalu air yang
berada di luar piknometer diusap sampai bersih kemudian ditimbang
dengan seksama. Untuk penentuan kerapatan sirup perlu diketahui volume
Cara perhitungannya :
Misalnya : bobot piknometer + sirup = a + c gram
bobot piknometer kosong = a gram
bobot sirup = c gram
volume piknometer = Vp
kerapatan sirup = ρsirup =
(ml) V
(g) c
p
e. Penentuan profil dan tipe alir sirup
Masukkan 400 ml sirup ke dalam cup dan diamkan selama beberapa
saat. Tambahkan beban seberat 5 gram pada penggantung dan catat waktu
yang digunakan untuk memutar rotor sebanyak 25 kali putaran. Ulangi lagi
langkah-langkah tersebut dengan menambah beban seberat 5 gram pada
penggantung secara bertahap. Hitung kecepatan alir sirup tiap penambahan
beban dan buat kurva pertambahan beban vs kecepatan alir sirup.
Kecepatan alir sirup ditentukan dengan persamaan :
V = t x
x 60
Keterangan:
V = kecepatan alir (rpm)
t = waktu yang diperlukan untuk memutar rotor sebanyak x (sekon) x = jumlah putaran rotor
7. Analisis hasil
Data diperoleh dengan melakukan pemeriksaan stabilitas fisis setiap
terhadap warna, bau, rasa, kejernihan, kristalisasi, kerapatan, dan pH dilakukan
setiap minggu selama 6 minggu. Sedangkan untuk penentuan profil dan tipe alir
dilakukan pada awal penyimpanan dan minggu keenam penyimpanan.
Data kerapatan sirup dan nilai pH sirup perasan daging buah mahkota
dewa diolah dengan menggunakan Independent-Sample T Test untuk melihat ada
tidaknya perubahan nilai kerapatan dan pH sirup perasan daging buah mahkota
dewa pada tiap minggu penyimpanan dibandingkan dengan awal penyimpanan.
Nilai Mean Difference yang diperoleh dari Independent-Sample T Test digunakan
untuk mengetahui seberapa besar perubahan rata-rata nilai kerapatan dan pH sirup
perasan daging buah mahkota dewa pada tiap minggu penyimpanan terhadap awal
penyimpanan. Semakin besar nilai Mean Difference menunjukkan bahwa
perubahan nilai rata-rata kerapatan dan pH semakin besar sehingga sirup semakin
tidak stabil.
Profil alir sirup dapat diamati pada kurva yang menggambarkan
hubungan antara penambahan beban dan perubahan kecepatan alir. Tipe alir sirup
ditentukan dengan melihat ada tidaknya hubungan yang proporsional antara
penambahan beban dan perubahan kecepatan alir sirup yang dihasilkan. Metode
analisis statistik yang digunakan adalah regresi linear. Nilai koefisien korelasi (r)
yang diperoleh dibandingkan dengan nilai r tabel untuk melihat ada tidaknya
hubungan yang proporsional antara penambahan beban dan perubahan kecepatan
BAB IV
HASIL dan PEMBAHASAN
A. Pengumpulan Bahan dan Pembuatan Perasan Daging Buah Mahkota Dewa
Air perasan daging buah mahkota dewa yang digunakan dalam penelitian
ini diperoleh dari buah mahkota dewa yang sudah masak dan berwarna merah tua
menyala. Hal tersebut disebabkan karena pada buah mahkota dewa yang sudah
masak, kandungan airnya cukup tinggi. Pembuatan air perasan diawali dengan
mencuci buah mahkota dewa yang akan digunakan dengan air mengalir.
Pencucian tersebut bertujuan untuk menghilangkan kotoran-kotoran yang
menempel pada buah mahkota dewa. Buah mahkota dewa yang sudah bersih lalu
diiris menjadi potongan-potongan kecil dan bagian bijinya dipisahkan dari daging
buahnya. Biji mahkota dewa mengandung racun yang bisa menyebabkan lidah
terasa kaku dan mati rasa serta demam, sehingga tidak digunakan dalam penelitian
ini. Irisan dari daging buah mahkota dewa lalu diperas airnya dengan
menggunakan juicer. Tiga buah mahkota dewa menghasilkan air perasan sekitar
15 ml. Air perasan daging buah mahkota dewa yang diperoleh berwarna coklat
keunguan dan berasa pahit.
B. Determinasi Buah Mahkota Dewa
Determinasi buah mahkota dewa dilakukan untuk memastikan kebenaran
dilakukan di laboratorium farmakognosi-fitokimia dengan menggunakan Atlas
Tumbuhan Obat Indonesia (Dalimartha, 2003).
Buah mahkota dewa merupakan buah tunggal, berbentuk bulat/bulat telur.
Buah mahkota dewa memiliki diameter 3-5 cm. Daging buah mahkota dewa
berwarna putih. Setelah masak, daging buahnya berserat dan berair. Biji buahnya
berbentuk bulat, keras, berwarna coklat. Permukaan kulit buah mahkota dewa
licin dan mangkilat. Saat masih muda, kulit buah mahkota dewa berwarna hijau.
Sesudah masak, warna kulit buahnya berubah menjadi merah marun dan menyala.
Ketebalan kulit buah mahkota dewa sekitar 0,5 – 1 mm. Cangkang biji buah
mahkota dewa berwarna putih. Ketebalan cangkang biji mahkota dewa bisa
mencapai 2 mm.
C. Pembuatan Sirup Perasan Daging Buah Mahkota Dewa
Sirup perasan daging buah mahkota dewa dalam penelitian ini dibuat
sebanyak 2 formula, yaitu formula A dan B. Formula A dibuat dengan 650 g
sukrosa, sedangkan formula B dibuat dengan 422,5 g sukrosa : 227,5 g sorbitol.
Adanya penggunaan campuran sukrosa-sorbitol ini bertujuan untuk mengetahui
ada tidaknya pengaruh penambahan sorbitol sebagai bahan pemanis, terhadap
stabilitas fisis sirup perasan daging buah mahkota dewa yang dihasilkan. Metode
yang digunakan dalam pembuatan sirup perasan daging buah mahkota ini adalah
metode pemanasan. Metode pembuatan sirup dalam penelitian ini dapat dibagi
menjadi 3 tahap utama, yaitu: pelarutan sukrosa, pencampuran bahan dan
Tahap pertama pembuatan sirup perasan daging buah mahkota dewa
adalah pelarutan sukrosa. Sukrosa dilarutkan dalam aqudest dengan bantuan
pemanasan di atas penangas listrik. Pemanasan ini bertujuan untuk mempercepat
kelarutan sukrosa.
Tahap kedua yaitu pencampuran bahan. Bahan-bahan selain sukrosa,
seperti: sorbitol, perasan daging buah mahkota dewa, bahan pewarna dan perasa
frambozen serta asam benzoat dicampur setelah larutan sukrosa selesai dibuat.
Sorbitol merupakan bahan yang tahan panas, dan karena bentuknya yang sudah
cair, maka sorbitol bisa dicampurkan ke dalam larutan sukrosa yang masih panas.
Pembuatan sirup perasan daging buah mahkota dewa ini menggunakan metode
pemanasan, dimana pada metode ini bahan pemanis dilarutkan dengan bantuan
pemanasan. Hal inilah yang menjadi alasan sorbitol dicampurkan ke dalam larutan
sukrosa yang masih panas, yaitu bertujuan untuk memberi perlakuan yang sama
terhadap bahan pemanis yang digunakan dalam setiap formula sirup. Perasan
daging buah mahkota dewa dicampurkan ke dalam larutan sukrosa-sorbitol yang
sudah dingin supaya tidak mengalami kerusakan. Setelah itu, ditambahkan bahan
pewarna sekaligus perasa frambozen yang mampu menutupi rasa pahit dan bau
tidak enak dari perasan daging buah mahkota dewa. Langkah selanjutnya adalah
penambahan bahan pengawet. Bahan pengawet yang digunakan adalah asam
benzoat. Penggunaan asam benzoat ini bertujuan untuk mencegah terjadinya
kerusakan fisis sirup akibat mikroorganisme. Jika semua bahan telah tercampur
homogen namun belum mencapai volume yang diinginkan, yaitu 1000 ml, maka
ml supaya tersedia sirup dalam jumlah yang cukup untuk dilakukan pengujian
selama 6 minggu penyimpanan Sirup perasan daging buah mahkota dewa yang
dihasilkan berwarna merah muda.
Tahap ketiga, yaitu penyaringan dilakukan dengan menggunakan kain
kassa yang masih bersih untuk memisahkan bahan-bahan pengotor yang tidak
larut dalam sirup. Penyaringan dilakukan sebanyak 2 kali sehingga diperoleh sirup
yang terlihat bening. Sirup yang telah disaring lalu dimasukkan dalam wadah
botol yang telah disterilisasi dengan menggunakan oven.
D. Pemeriksaan Stabilitas Fisis Sirup 1. Uji Organoleptis Sirup
Uji organoleptis sirup dilakukan tiap minggu mulai dari awal pembuatan
sampai 6 minggu penyimpanan. Uji ini meliputi pemeriksaan warna, bau,
kejernihan dan rasa. Dari hasil uji organoleptis selama 6 minggu penyimpanan
Tabel I. Hasil uji organoleptis sirup selama 6 minggu penyimpanan Lama pe-
nyimpanan
Warna Bau Rasa Kejernihan
0
Merah muda (warna sirup formula B lebih terang di- (warna sirup formula B lebih terang di- (warna sirup formula B lebih terang di-
Formula A: jernih Formula B: sirup
memisah 2
Formula A: jernih Formula B: sirup
memisah 2
Formula A: jernih Formula B: sirup
memisah 2
Formula A: jernih Formula B: sirup
memisah 2 bagian* Ket:
Formula A: sirup yang dibuat dengan 650 g sukrosa
Formula B: sirup yang dibuat dengan 422,5 g sukrosa dan 227,5 g sorbitol
(*):sirup yang memisah ditandai dengan adanya bagian dari sirup yang mengapung.
(-) : berkurang
Pengamatan terhadap organoleptis sirup ini dilakukan oleh satu orang
sehingga bersifat subjektif. Hasil pengamatan organoleptis terhadap sirup yang
diperoleh menunjukkan adanya perubahan warna, bau, rasa serta kejernihan sirup
selama 6 minggu penyimpanan.
Pada awal pembuatan, kedua formula sirup perasan daging buah mahkota
dewa yang dihasilkan memiliki warna yang hampir sama, yaitu merah muda.
Adanya proses pemanasan dalam melarutkan sukrosa memungkinkan terjadinya
inversi yang dapat menyebabkan larutan sukrosa yang dihasilkan cenderung
berwarna jernih agak kecoklatan. Larutan sukrosa kedua formula sirup berwarna
jernih agak kecoklatan, tetapi warna formula A cenderung lebih gelap
dibandingkan formula B. Hal ini disebabkan karena formula A memiliki
kandungan sukrosa yang lebih banyak dibandingkan dengan formula B, sehingga
sukrosa yang mengalami inversi lebih banyak. Penambahan bahan pewarna
sekaligus perasa frambozen yang berwarna merah pada larutan sukrosa kedua
formula dan perasan buah mahkota dewa menjadikan sirup formula A dengan
100% sukrosa berwarna merah muda lebih gelap dibandingkan sirup formula B
dengan campuran sukrosa-sorbitol sebagai bahan pemanis. Namun demikian,
perbedaan warna yang terjadi tidak terlalu mencolok secara visual.
Inversi merupakan reaksi hidrolisis yang mampu memecah sukrosa
menjadi monosakarida-monosakarida penyusunnya, yaitu glukosa (dekstrosa) dan
fruktosa (levulosa). Pemanasan terhadap fruktosa yang merupakan hasil inversi,
dapat menyebabkan warna sirup menjadi lebih gelap. Reaksi inversi yang terjadi
C12H22O11 (sukrosa) + H2O (air) C6H12O6 (glukosa) + C6H12O6 (fruktosa)
Kombinasi dari 2 monosakarida yang dihasilkan dari inversi ini disebut dengan
gula invert. Gula invert ini memiliki tingkat kemanisan yang lebih tinggi
dibandingkan sukrosa. Namun demikian, adanya reaksi inversi yang terjadi ini
menjadi kurang menguntungkan karena glukosa yang dihasilkan merupakan
sumber energi bagi mikroorganisme. Peristiwa inversi ini bisa terjadi karena
lingkungan sirup yang berupa air dan adanya asam yang berfungsi sebagai katalis.
Selain itu, adanya pemanasan akan menyebabkan reaksi inversi berlangsung lebih
cepat. Penambahan asam terjadi saat penambahan asam benzoat yang digunakan
sebagai bahan pengawet.
Peristiwa inversi yang terjadi selama penyimpanan karena adanya air dan
senyawa asam, mempengaruhi penampilan fisik sirup terutama warna dan rasa
sirup. Inversi ini menyebabkan terjadinya diskolorisasi sirup. Hasil pengamatan
menunjukkan bahwa pada minggu ketiga penyimpanan, sirup mulai mengalami
perubahan warna. Warna sirup yang pada awalnya merah muda menjadi semakin
pudar dari minggu ke minggu dan menjadi semakin kecoklatan.
Pada awal pembuatan, sirup perasan daging buah mahkota dewa memiliki
rasa yang manis dan seperti frambozen. Setelah 3 minggu penyimpanan, mulai
terjadi perubahan rasa, yaitu sirup menjadi semakin manis dan muncul aftertaste
yang kurang enak. Hal ini disebabkan karena terbentuknya gula invert (fruktosa
dan glukosa) sebagai hasil inversi, yang memiliki tingkat kemanisan lebih tinggi
Fermentasi merupakan peristiwa digesti glukosa oleh mikroorganisme
yang menghasilkan alkohol (etanol), karbondioksida dan energi. Glukosa bisa
diperoleh dari hasil inversi yang terjadi. Reaksi fermentasi yang terjadi adalah
sebagai berikut:
C6H12O6 (glukosa) 2C2H5OH (etanol) + 2CO2 (karbondioksida) + Energi
Adanya reaksi fermentasi mengindikasikan adanya mikroorganisme di dalam
sirup. Hal tersebut mungkin disebabkan karena bahan pengawet yang digunakan,
yaitu asam benzoat, kurang sesuai untuk sediaan ini. Peristiwa fermentasi yang
terjadi mempengaruhi penampilan fisik sirup, terutama bau.
Sirup perasan mahkota dewa yang dihasilkan mengalami perubahan bau
selama penyimpanan. Mulai pada minggu kedua, aroma frambozen yang terdapat
dalam sirup mulai berkurang bahkan pada minggu keempat mulai tercium adanya
alkohol. Hal ini disebabkan reaksi fermentasi yang terjadi selama penyimpanan.
Adanya proses penyaringan yang dilakukan menyebabkan sirup perasan
daging buah mahkota dewa yang dihasilkan tampak jernih. Selama penyimpanan,
sirup formula A tidak mengalami pemisahan sedangkan sirup formula B
mengalami pemisahan menjadi 2 bagian mulai pada minggu ketiga yang ditandai
dengan adanya bagian yang mengapung. Bagian yang mengapung tersebut
kemungkinan adalah sorbitol. Pemisahan tersebut mungkin disebabkan karena
adanya perbedaan berat molekul dimana berat molekul sorbitol lebih kecil
2. Pengkristalan
Sirup perasan daging buah mahkota dewa yang dibuat dalam penelitian ini
mengandung sukrosa sebagai bahan pemanis. Sukrosa mempunyai sifat yang
mudah mengkristal, oleh karena itu dikombinasikan dengan sorbitol yang bisa
berfungsi sebagai anti-crystallizing agent. Sorbitol sebagai anti-crystallizing
agent ini akan mengurangi kecenderungan mengkristal dari sukrosa. Adanya
sorbitol diharapkan kristalisasi sukrosa dapat dikurangi/dihambat. Maka dari itu,
perlu dilakukan pengamatan akan kristal yang terbentuk. Dalam penelitian ini,
pengamatan kristal hanya dilakukan secara visual yaitu dengan mengamati
terbentuknya kristal pada tutup dan leher botol. Dari hasil pengamatan yang
dilakukan, mulai pada minggu ketiga telah terjadi pembentukan kristal pada sirup
formula A yang mengandung 650 g sukrosa, sedangkan pada formula B yang
menggunakan sorbitol tidak mengalami kristalisasi. Pengkristalan ditandai dengan
adanya kristal-kristal putih di bagian tutup dan leher botol.
Penelitian ini memiliki kelemahan yaitu adanya perbedaan kadar sukrosa
yang digunakan dalam penelitian, dimana sukrosa untuk formula A sebanyak 650
g sedangkan sukrosa untuk formula B sebanyak 422,5 g. Maka dari itu, ada 2
kemungkinan yang bisa menyebabkan sirup formula B tidak mengalami
kristalisasi sukrosa. Kemungkinan pertama adalah karena adanya sorbitol sebagai
kosolven yang akan membantu mencegah terjadinya kristalisasi dengan menjaga
kelarutan sukrosa. Adapun kemungkinan yang kedua adalah karena kadar sukrosa
yang digunakan untuk formula B lebih sedikit dibandingkan kadar sukrosa yang
3. Penentuan Kerapatan Sirup
Kerapatan merupakan massa per unit volume suatu zat pada temperatur
tertentu. Kerapatan ini dapat dipengaruhi oleh faktor konsentrasi zat. Semakin
tinggi konsentrasi suatu zat maka kandungan zat akan lebih banyak sehingga
kerapatan juga semakin besar. Dengan demikian, semakin besar nilai kerapatan
sirup, semakin banyak pula partikel sukrosa yang terdispersi molekuler dalam
larutan tersebut. Jika sirup memiliki nilai kerapatan yang stabil selama
penyimpanan, maka bisa dikatakan bahwa konsentrasi sukrosa dalam sirup tetap
terjaga selama penyimpanan. Namun jika nilai kerapatan sirup mengalami
penurunan berarti bahwa kandungan sukrosa yang terlarut dalam sirup berkurang.
Berkurangnya sukrosa yang terlarut dalam sirup bisa diakibatkan antara lain
karena adanya pengkristalan sukrosa. Penentuan kerapatan sirup perasan daging
buah mahkota dewa perlu dilakukan karena terkait dengan stabilitas fisis sirup,
dimana penurunan kerapatan secara tidak langsung bisa mengindikasikasikan
terjadinya kristalisasi sukrosa.
Penentuan nilai kerapatan sirup perasan daging buah mahkota dewa
dilakukan dengan menggunakan piknometer. Tahap pertama dalam menentukan
nilai kerapatan sirup adalah dengan menentukan volume piknometer terlebih
dahulu. Untuk menentukan volume piknometer dibutuhkan suatu zat yang telah
diketahui nilai kerapatannya, oleh karena itu digunakan air. Dalam penentuan
volume piknometer, suhu air diturunkan ± 2o C di bawah suhu percobaan. Hal ini
bertujuan untuk memudahkan pengamatan saat suhu air naik mencapai suhu
Pengukuran kerapatan sirup dapat dilakukan setelah mengetahui volume
piknometer. Suhu sampel sirup yang akan diukur kerapatannya juga diturunkan ±
2o C di bawah suhu percobaan seperti halnya pada air. Penurunan suhu ini
mempunyai tujuan untuk memudahkan pengamatan saat suhu sampel naik
mencapai suhu percobaan, yaitu 25o C sedangkan penimbangan piknometer
dilakukan saat suhu sampel mencapai suhu kamar, yaitu 28o C. Hal ini bertujuan
untuk mencegah adanya pengembunan pada bagian luar piknometer yang bisa
mempengaruhi hasil penimbangan. Pengembunan bisa terjadi karena suhu
piknometer yang berisi sirup perasan daging buah mahkota dewa lebih rendah
daripada suhu ruangan.
Pengukuran kerapatan sirup perasan daging buah mahkota dewa dilakukan
setiap minggu selama 6 minggu penyimpanan. Berdasarkan pengukuran yang
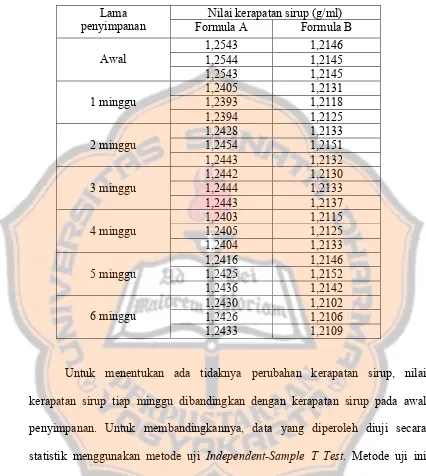
Tabel II. Hasil pengukuran kerapatan sirup:
Nilai kerapatan sirup (g/ml) Lama
penyimpanan Formula A Formula B
1,2543 1,2146
Untuk menentukan ada tidaknya perubahan kerapatan sirup, nilai
kerapatan sirup tiap minggu dibandingkan dengan kerapatan sirup pada awal
penyimpanan. Untuk membandingkannya, data yang diperoleh diuji secara
statistik menggunakan metode uji Independent-Sample T Test. Metode uji ini
digunakan untuk menguji perbedaan nilai rata-rata kerapatan sirup antara dua
sampel sirup yang berbeda (tidak berhubungan). Nilai rata-rata kerapatan sirup
pada awal penyimpanan dilambangkan µ1, sedangkan nilai rata-rata kerapatan
hipotesis alternatif (H1) dan wilayah kritis yang digunakan dalam uji tersebut
Dari analisis statistik yang dilakukan diperoleh hasil seperti tertera dalam tabel
berikut ini:
Tabel III. Nilai t hasil Independent-Sample T Test nilai kerapatan sirup tiap minggu dibandingkan dengan nilai kerapatan sirup pada awal penyimpanan.
Nilai t Lama
penyimpanan Formula A Formula B
1 37,837 5,480
Dari hasil Independent-Sample T Test terhadap nilai kerapatan sirup
formula A selama 6 minggu penyimpanan, diperoleh nilai tuji yang lebih besar