BAB II
TINJAUAN PUSTAKA
2.1. Nanopartikel
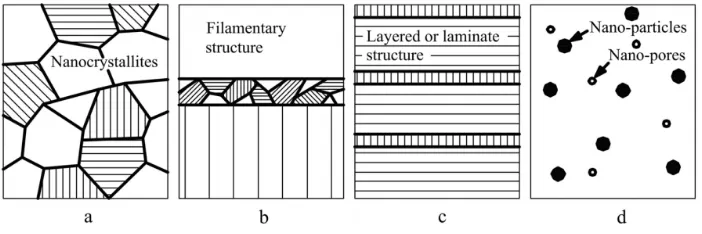
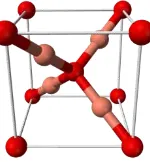
Nanopartikel adalah partikel dalam ukuran nanometer yaitu sekitar 1-100 nm (Hosokawa et al. 2007). Nanopartikel merupakan ilmu dan rekayasa dalam menciptakan material, struktur fungsional, maupun piranti alam skala nanometer.Ditinjau dari jumlah dimensi yang terletak dalam rentang nanometer, material nano diklasifikasikan menjadi beberapa kategori(Gambar 2.1.), yaitu: material nano berdimensi nol (nanoparticle) seperti oksida logam, semikonduktor ,dan fullerenes; material nano berdimensi satu (nanowire, nanotubes, nanorods); material nano berdimensi dua (thin films); dan material nano berdimensi tiga seperti Nanokomposit, nanograined, mikroporous, mesoporous, interkalasi, organik-anorganik hybrids. (Pokropivny,V. et al, 2007).
Nanopartikel menjadi kajian yang sangat menarik, karena material yang berada dalam ukuran nano biasanya memiliki partikel dengan sifat kimia atau fisika yang lebih unggul dari material yang berukuran besar (bulk).(C. R. Vestal et al. 2004; Cao, Guozhong, 2004). Dua hal utama yang membuat nanopartikel
berbeda dengan material sejenis dalam ukuran besar (bulk) yaitu:
1. Karena ukurannya yang kecil, nanopartikel memiliki nilai perbandingan antara luas permukaan dan volume yang lebih besar jika dibandingkan dengan partikel sejenis dalam ukuran besar. Ini membuat nanopartikel bersifat lebih reaktif. Reaktivitas material ditentukan oleh atom-atom di permukaan, karena hanya atom-atom tersebut yang bersentuhan langsung dengan material lain;
2. Ketika ukuran partikel menuju orde nanometer, maka hukum fisika yang berlaku lebih didominasi oleh hukum- hukum fisika kuantum.(Abdullah M., et al, 2008)
sejenis dalam keadaan bulk. Para peneliti juga percaya bahwa kita dapat mengontrol perubahan-perubahan tersebut ke arah yang diinginkan. (Abdullah M.,et al, 2008)
Selain nanopartikel juga dikembangkan material nanostruktur, yaitu material yang tersusun oleh beberapa material nanopartikel. Untuk menghasilkan material nanostruktur maka partikel-partikel penyusunnya harus diproteksi sehingga apabila partikel-partikel tersebut digabung menjadi material yang berukuran besar maka sifat individualnya dipertahankan. Sifat material nanostruktur sangat bergantung pada (a) ukuran maupun distribusi ukuran, (b) komponen kimiawi unsur-unsur penyusun material tersebut, (c) keberadaan interface (grain boundary), dan (d) interaksi antar grain penyusun material nanostruktur.
Quantum dot adalah material berukuran kurang dari 100 nanometer yang mengurung elektron secara 3-dimensi, baik arah x, y dan z. Hal ini dimungkinkan karena diameter dari quantum dot tersebut sebanding dengan panjang gelombang dari elektron. Bahkan, disebut bahwa quantum dot ini merupakan atom buatan (artificial atom). Nanowire adalah material berukuran nanometer yang dapat mengurung elektron secara 2-dimensi dan bebas bergerak di dimensi yang ketiga, yaitu ke depan atau ke belakang. (Astuti, 2007)
2.1.1. Keunggulan Sifat Material Berorde Nano
berukuran nanometer memiliki sifat yang kaya karena menghasilkan sifat yang tidak dimiliki oleh material ukuran besar. Sejumlah sifat tersebut dapat diubah-ubah dengan melalui pengontrolan ukuran material, pengaturan komposisi kimiawi, modifikasi permukaan dan pengontrolan interaksi antar partikel. Material nanopartikel adalah material-material buatan manusia yang berskala nano, yaitu lebih kecil dari 100nm, termasuk didalamnya nanodot, quantum dot, nanowire dan carbon nanotube (Abdullah M., et al, 2008). Berikut merupakan beberapa keunggulan sifat material berorde nano secara umum :
1. Sifat elektrik
Pengaruh size reduction pada sifat elektrik nanopartikel dapat meningkatkan konduktivitas nanometals, membangkitkan konduktivitas nanodielektrik, dan meningkatkan induktansi dielektrik untuk ferroelectrics.
2. Sifat optik
Sistem nanokristalin memiliki sifat optikal yang menarik, yang mana berbeda dengan sifat kristal konvensional. Pengaruh size reduction pada sifat optik nanopartikel dapat meningkatkan penyerapan (absorbansi) dalam range ultraviolet (blue shift), Osilasi penyerapan optik, dan meningkatkan nilai band gap. Kunci peyumbang faktor masuknya quantum tertutup dari pembawa elektrikal pada nanopartikel, energi yang efisien dan memungkinkan terjadinya pertukaran karena jaraknya dalam skala nano serta memiliki sistem dengan interface yang tinggi. Dengan perkembangan teknologi dari material mendukung perkembangan sifat nanofotonik. Dengan sifat optik linear dan non linear material nano dapat dibuat dengan mengontrol dimensi kristal dan surface kimia, teknologi pembuatan menjadi faktor kunci untuk mengaplikasikan.Contoh aplikasi : pada optoelektronik., electrochromik untuk liquid crystal display (LCD).(Pokropivny,V. et al. 2007)
3. Sifat magnetik
Kekuatan magnetik adalah ukuran tingkat kemagnetan. Pengaruh penurunan ukuran butiran patikel (Size reduction) dan kenaikan spesifik surface area per satuan volume partikel pada sifat magnetik ini dapat meningkatkan atau
menurunkan koersivitas magnet, menurunkan temperatur Curie, memiliki sifat paramagnetik atau feromagnetik, membangkitkan temperatur maksimal magnetoresistance, dan meningkatkan permeability magnetik pada sifat
Aplikasinya pada mesin kapal, instrumen ultra sensitiv dan magnetic resonance imaging (MRI) pada alat diagnostik.(Pokropivny,V. et al. 2007)
4. Sifat mekanik
Pengaruh penurunan ukuran butiran patikel (Size reduction) dari partikel pada sifat mekanik dapatmeningkatkan kekerasan (hardness), kekuatan (strength), daktilitas (fracture ductility), dan ketahanan aus (wear resistance). Nanomaterial memiliki kekerasan dan tahan gores yang lebih besar bila dibandingkan dengan material dengan ukuran biasa.Contoh aplikasi : automobil dengan efisiensi greater fuel. Nanomaterial diterapkan pada automobil sejak diketahui sifat kuat, keras dan sangat tahan terhadap erosi, diharapkan dapat diterapkan pada busi.(Pokropivny,V. et al. 2007)
2.1.2. Perkembangan Nanopartikel
Nanoteknologi akan mempengaruhi industri baja, pelapisan dekorasi, industri polimer, industri kemasan, peralatan olahraga, tekstil, keramik, industri farmasi dan kedokteran, transportasi, industri air, elektronika dan kecantikan. Penguasaan nanoteknologi akan memungkinkan berbagai penemuan baru yang bukan sekadar memberikan nilai tambah terhadap suatu produk, bahkan menciptakan nilai bagi suatu produk. Salah satu nanomaterial yang sangat menarik untuk dikembangkan saat ini adalah nanopartikel magnetik.
Nanopartikel saat ini banyak digunakan pada beragam produk komersial mulai dari katalis, media cat dan cairan magnetik, hingga kosmetik dan tabir surya. Suatu review terbaru dari peneliti di Swedia dan Spanyol mendeskripsikan hasil kerja terkini untuk optimasi sintesis, dispersi, dan fungsionalisasi permukaan titania (titanium dioksida), seng oksida, dan seria (serium oksida) — tiga nanopartikel utama yang digunakan pada fotokatalis, penghalau sinar UV (ultraviolet), dan tabir surya. Review mereka dipublikasikan pada 26 April 2013 di jurnal Science and Technology of Advanced Materials. (Gifhari, A.S. 2013).
dalam tubuh dan bereaksi lebih cepat, serta pengembangan obat pintar (smart) yang bisa mencari sel-sel tumor dalam tubuh dan langsung mematikan sel tersebut tanpa mengganggu sel-sel normal), lingkungan (penggunaan partikel skala nanometer untuk menghancurkan polutan organik di air dan udara), dan sebagainya.(Nanoworldindonesia, 2013)
2.2. Metode Sintesis Nanopartikel
Nanopartikel dapat terjadi secara alamiah ataupun melalui proses sintesis oleh manusia. Sintesis nanopartikel bermakna pembuatan nanopartikel dengan ukuran yang kurang dari 100 nm dan sekaligus mengubah sifat atau fungsinya.Dalam sintesis nanopartikel terdapat beberapa faktor yang mempengaruhinya yaitu konsentrasi reaktan, molekul pelapis (capping agent), temperatur dan pengadukan.
Sintesis nanopartikel dapat dilakukan dalam fasa padat, cair, maupun gas. Proses sintesis pun dapat berlangsung secara fisika atau kimia. Proses sintesis secara fisika tidak melibatkan reaksi kimia. Yang terjadi hanya pemecahan material besar menjadi material berukuran nanometer, atau penggabungan material berukuran sangat kecil, seperti kluster, menjadi partikel berukuran nanometer tanpa mengubah sifat bahan. Proses sintesis secara kimia melibatkan reaksi kimia dari sejumlah material awal sehingga dihasilkan material lain yang berukuran nanometer (Abdullahet al. 2008).
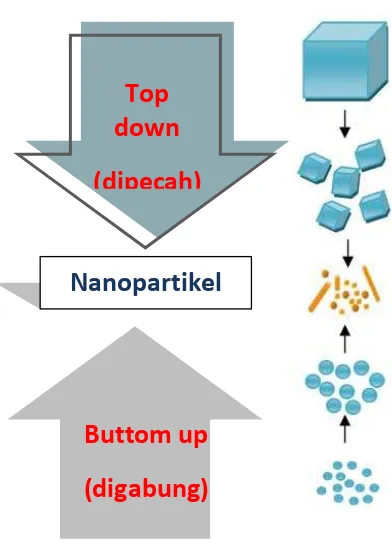
berukuran nanometer. Pendekatan ini kadang disebut pendekatan top-down. Pendekatan kedua adalah memulai dari atom-atom atau molekul-molekul yang membentuk partikel berukuran nanometer yang dikehendaki. Pendekatan ini disebut bottom-up. (Abdullah, M. 2008). Kedua kelompok besar dalam mensintesis nanopartikel telihat pada gambar 2.2.
Gambar 2.2. Sintesis nanopartikel top-down dan bottom-up
Pembentukan nanopartikel dengan keteraturan yang tinggi dapat menghasilkan pola yang lebih seragam dan ukuran yang yang seragam pula.Kebanyakan penelitian telah mampu menghasilkan nanopartikel yang lebih bagus dengan menggunakan metoda-metoda yang umum digunakan, seperti: kopresipitasi, sol-gel, mikroemulsi, hidrotermal/solvoterma, menggunakan
Nanopartikel
Buttom up
(digabung)
Top
down
cetakan (templated synthesis), sintesis biomimetik, metoda cairan superkritis, dan sintesis cairan ionik.
2.3. Metode Kopresipitasi
. Tabel 2.1.Reaksi fisik dan kimia dari metode kopresipitasi
Sifat Fisik Sifat Kimia
Suhu reaksi yang diperlukan , 100o C Proses Kopresipitasi akan meninggakatkan pH Pada Kopresipitasi dilakukan
pengadukan secara terus menerus agar larutan homogen
Kopresipitasi dilakukan pada larutan encer agar memudahkan proses penyaringan
Memiliki ukuran partikel hasil sintetis lebih kecil daripada metode sol state dan lebih besar daripada metode sol gel
Meningkatkan homogenitas dengan penambahan larutan pengendap.
2.3.1. Kemurnian endapan
Setelah proses pengendapan masalah berikut adalah bagaimana cara mendapatkan endapan semurni mungkin untuk mendapatkan hasil analisis seteliti mungkin. Ikut sertanya pengotor pada endapan dapat dibedakan menjadi:
1.Pengendapan bersama (ko-presipitasi)
Pada proses pengotoran ini, zat pengotor mengendap bersama-sama endapan yang diinginkan.Bentuk atau macam pengendapan bersama ini dapat dibedakan:
a. Adsorpsi permukaan; zat pengotor teradsorpsi atau terserap pada permukaan endapan, peristiwa ini dapatterjadi pada endapan berbentuk jel, karena mempunyai luas permukaan cukup besar. Contoh ikut mengendapnya NaCl pada endapan AgCl.
b. Inklusi isomorf; zat pengotor masuk kedalam kisi hablur endapan, dan membentuk hablur campuran
c. Inklusi tak isomorf; zat pengotor larut dalam endapan dan membentuk lapisan endapan. Contoh :pengotoran barium sulfat oleh barium nitrat. d. Oklusi; zat pengotor terkurung dalam hablur endapan
2.Pengendapan susulan (post presipitasi)
pengotor mengendap bersama-sama. Pada proses ini senyawa yang diinginkan mengendap dulu, baru zat pengotor menyusul mengendap. Makin lama endapan dibiarkan dalam induk larutannya, makin meningkat jumlah zat pengotor menyusul mengendap.
2.4. Bahan Nanopartikel 2.4.1. Tembaga (Cu)
Tembagamerupakan suatu unsur kimia dalam tabel periodik yang memiliki lambang Cu dan nomor atom 29. Lambangnya berasal dari bahasa Latin Cuprum.Bahan ini merupakan konduktor panas dan listrik yang baik.Disamping
itu tembaga merupakan salah satu logam non-ferrous yang paling penting dan banyak dipakai mulai dari industri sederhana sampai industri berteknologi tinggi.
Ada dua deret senyawa tembaga. Senyawa-senyawa tembaga(I) diturunkan dari senyawa tembaga(I) oksida (Cu2O), mengandung ion tembaga(I), Cu2+. Senyawa tembaga(I) mudah dioksidasikan menjadi senyawa tembaga(II ), yang dapat diturunkan dari tembaga(II) oksida, CuO.
Tembaga membentuk senyawa dengan tingkat oksidasi +1 dan +2, namun hanya tembaga(II) yang stabil dan mendominasi dalam larutan air. Dalam larutan air, hampir semua garam tembaga(II) berwarna biru, yang karakteristik dari warna ion kompleks koordinasi 6, [��(�2�)6]2+. Kekecualian yang terkenal yaitu tembaga(II) klorida yang berwarna kehijauan oleh karena ion kompleks [����4]2−yang mempunyai bangun geometri dasar tetrahedral atau bujursangkar
Garam-garam tembaga(II) umumnya berwarna biru, baik dalam bentuk hidrat, padat, maupun dalam larutan air. Warna ini benar-benar khas hanya untuk ion tetraakuokuprat(II) saja. Garam-garam tembaga(II) anhidrat, seperti tembaga(II) sulfat anhidrat Cu2SO4, berwarna putih (atau sedikit kuning). Dalam larutan air selalu terdapat ion kompleks tetrakuo (Vogel, 1990).
Gambar 2.3.Tembaga
2.4.2. Sifat Kimia Tembaga
Tembaga merupakan unsur yang relatif tidak reaktif sehingga tahan terhadap korosi. Pada udara yang lembab permukaan tembaga ditutupi oleh suatau lapisan yang berwarna hijau yang menarik dari tembaga karbonat basa, Cu(OH)2CO3.
Tembaga panas dapat bereaksi dengan uap belerang dan halogen. Berekasi dengan belerang membentuk tembaga(I) sulfida dan tembaga(II) sulfida dan untuk reaksi dengan halogen membentuk tembaga(I) klorida , khusus klor yang menghasilkan tembaga(II) klorida.
Tabel 2.2.Data Sifat Kimia Tembaga Data sifat kimia Keterangan Nama, lambang, nomor atom Tembaga, Cu, 29
Deret kimia Logam transisi
Golongan, periode, blok 1B, 4, d
Massa atom (g/mol) 63,546
Konfigurasi elektron [��]3�104�1 Jumlah elektron tiap kulit 2, 8, 18, 1 Bilangan oksida(oksida amfoter) 2, 1 Elektronegatifitas (skala pauling) 1,90
ionisasi (kJ/mol) pertama: 745,5
kedua : 1957,9 ketiga : 3555
Jari-jari atom (pm) 135
Jari-jari kovalen (pm) 138
Struktul kristal Face centered cubic
Tabel 2.3 Beberapa senyawaan yang dibentuk oleh tembaga
Tembaga(II) Nama
2.4.3. Sifat Fisika Tembaga
sehingga mudah dibentuk menjadi pipa, lembaran tipis dan kawat. Konduktor panas dan listrik yang baik, setelah perak.
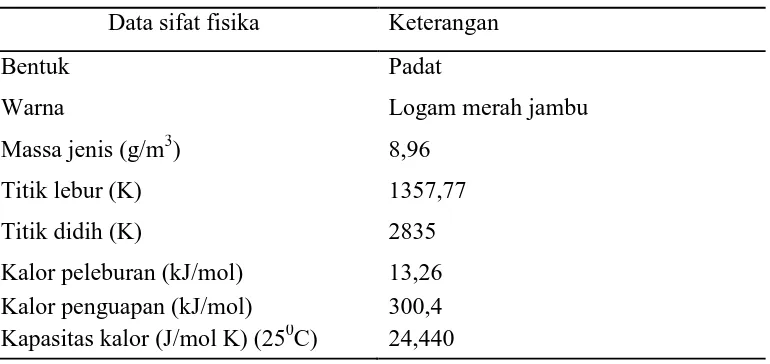
Tabel 2.4.Data Sifat Fisika Tembaga
Data sifat fisika Keterangan
Bentuk Padat
Warna Logam merah jambu
Massa jenis (g/m3) 8,96
Titik lebur (K) 1357,77
Titik didih (K) 2835
Kalor peleburan (kJ/mol) 13,26 Kalor penguapan (kJ/mol) 300,4 Kapasitas kalor (J/mol K) (250C) 24,440
2.4.4. Senyawa Cu2O
Copper(I) oxide atau tembaga oksida adalah senyawa anorganik dengan
mengurangi gula. Gula-gula ini mengurangi larutan alkali dari tembaga(II) garam, memberikan endapan merah cerah dari Cu2O.
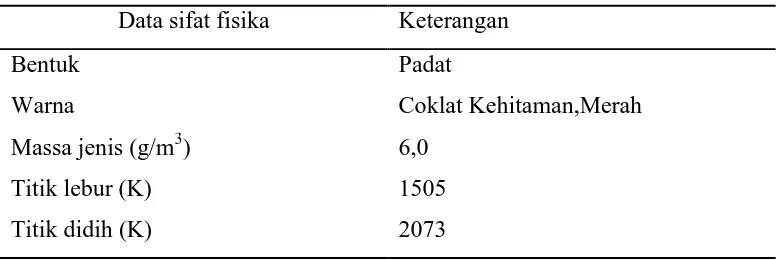
Tabel 2.5.Karakteristik Cu2O
Data sifat fisika Keterangan
Bentuk Padat
Warna Coklat Kehitaman,Merah
Massa jenis (g/m3) 6,0
Titik lebur (K) 1505
Titik didih (K) 2073
Cuprous Oxide (Cu2O) sebagai material semikonduktor merupakan bahan dengan konduktivitas yang berada diantara isolator (penghantar listrik yang buruk) dan konduktor (penghantar listrik yang baik).Material semikonduktor bersifat sebagai isolator pada temperatur yang sangat rendah namun pada temperature ruangan bersifat sebagai konduktor. Semikonduktor sangat berguna karena sifat konduktifitasnya dapat dirubah dan dikontrol dengan memberi materi lain ataumenambahkan ketidakmurnian (doping).Doping merupakan pengotor bahan semikonduktor.
Dalam sejarah semikonduktor, Cu2O adalah salah satu bahan yang paling banyak dipelajari, dan banyak pengamatan eksperimental dan aplikasi semikonduktor telah dibuktikan terlebih dahulu dalam materi semikondukor, semikonduktor dioda. Oksida tembaga umumnya digunakan sebagai pigmen, fungisida dan agent antifrouling untuk cat laut. Rectifier dioda berdasarkan bahan yang telah digunakan industry sejak awal tahun 1924, jauh sebelum silicon menjadi standar.
Gambar 2.4.Cuprous Oxide (Cu2O)
2.5. Semikonduktor
Elektron yang berpindah ke pita konduksi akan menjadi elektron bebas dan akan meninggalkan sejumlah kekosongan di pita valensi yang disebut sebagai lubang (hole) yang nantinya akan berekombinasi kembali dengan elektron. Elektron dan hole inilah yang menjadi penghantar arus listrik pada material semikonduktor. Berdasarkan asal muatan pembawa, semikonduktor dibedakan menjadi dua kelompok yaitu semikonduktor instrinsik dan semikonduktor ekstrinsik. Semikonduktor instrinsik hanya terdiri dari sebuah unsur atau senyawa, electron ataupun hole berasal dari atom itu sendiri.
2.5.1 Semikonduktor Cu2O (Cuprous dioxide)
Semikonduktor Cu2O merupakan semikonduktor tipe-p yang memiliki celah pita enegi yang berkisar antara 2.0-2.1 eV, (He Ping, et al, 2004; Kuo CH,et al, 2007; Lin X.F., et al., 2010; Sekhar, H, et al, 2012;) celah pita energy yang
dimiliki semikonduktor Cu2O ini merupakan rentang yang bisa diterima untuk konversi energy surya, karena material semikonduktor dengan celah pita energy antara 1 eV, sampai 2 eV merupakan material dengan cocok digunakan dalam aplikasi sel surya.Penentuan nilai band gap merupakan salah satu parameter utama dalam menentukan aplikasi yang sesuai untuk suatu material semikonduktor.
Struktur Kristal semikonduktor Cu2O adalah kubik. Nilai parameter kisi a = 4.27 �̇, memiliki massajenis 0.609 g/cm3 dan tidak larut dalam air. Senyawa Cu2O atau cuprous oxide memiliki nama lain copper (I) oxide, cuprite (mineral), atau Read Copper Oxide. (Lestari.,V, 2009)
2.6. Karakterisasi Nanopartikel 2.6.1. X-Ray Diffractometry(XRD)
Difraksi sinar-X digunakan untuk mengidentifikasi struktur kristal suatu padatan dengan membandingkan nilai jarak d (bidang kristal) dan intensitas puncak difraksi dengan data standar. Pengujian ini merupakan aplikasi langsung dari pemakaian sinar X untuk menentukan jarak antara kristal dan jarak antara atom dalam kristal.
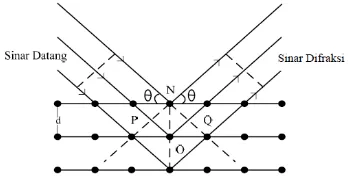
Gambar 2.6. Difraksi Bidang Atom
Gambar 2.6. menunjukkan suatu berkas sinar X dengan panjang gelombang λ,
jatuh pada sudut θ pada sekumpulan bidang atom berjarak d. Sinar yang
dipantulkan dengan sudut θ hanya dapat terlihat jika berkas dari setiap bidang
yang berdekatan saling menguatkan. Oleh sebab itu, jarak tambahan satu berkas dihamburkan dari setiap bidang yang berdekatan, dan menempuh jarak sesuaidengan perbedan kisi yaitu sama dengan panjang gelombang n λ. Sebagai contoh, berkas kedua yang ditunjukkan gambar 2.7. harus menempuh jarak lebih jauh dari berkas pertama sebanyak PO + OQ. Syarat pemantulan dan saling menguatkan dinyatakan oleh :
Persamaan (1.1) disebut dengan hukum Bragg dan harga sudut kritis θ untukmemenuhi hukum tersebut dikenal dengan sudut Bragg.
Prinsip dasar dari XRD adalah hamburan elektron yang mengenai permukaan kristal. Bila sinar dilewatkan ke permukaan kristal, sebagian sinar tersebut akan terhamburkan dan sebagian lagi akan diteruskan ke lapisan berikutnya. Sinar yang dihamburkan akan berinterferensi secara konstruktif (menguatkan) dan destruktif (melemahkan). Hamburan sinar yang berinterferensi inilah yang digunakan untuk analisis.
Difraksi sinar-X hanya akan terjadi pada sudut tertentu sehingga suatu zat akan mempunyai pola difraksi tertentu. Pengukuran kristalinitas relatif dapat dilakukan dengan membandingkan jumlah tinggi puncak pada sudut-sudut tertentu dengan jumlah tinggi puncak pada sampel standar.
Di dalam kisi kristal, tempat kedudukan sederetan ion atau atom disebut bidang kristal. Bidang kristal ini berfungsi sebagai cermin untuk merefleksikan sinar–X yang datang. Posisi dan arah dari bidang kristal ini disebut Indeks Miller. Setiap kristal memiliki bidang kristal dengan posisi dan arah yang khas, sehingga jika disinari dengan sinar-X pada analisis XRD akan memberikan difraktogram yang khas pula.
yang ada pada sampel yang diketahui. Melalui grafik XRD, grain size dari sampel juga dapat diperkirakan. Grain size dihitung dengan menggunakan persamaan Scherrer, yaitu :
�
=
0,9 . ��cos� (2.1)
dengan :
S = grain size
λ = panjang gelombang berkas sinar X B = FWHM (full width half maximum).
� = besar sudut dari puncak dengan intensitas tinggi.
2.6.2. SEM (Scanning Electron Microscope) -EDX
SEM (Scaning Electron Microscope) merupakan mikroskop elektron yang didesain untuk menggambarkan bentuk permukaan dari material yang dianalisis menggunakan berkas electron. Adapun fungsi utama dari SEM antara lain dapat digunakan untuk mengetahui informasi-informasi mengenai topografi (ciri-ciri permukaan), Morfologi (bentuk dan ukuran dari partikel penyusun objek ), dan Informasi kristalografi objek.Pada intrument SEM terintegrasi sebuah detektor Energy Dispersive X-ray (EDX) yang memungkinkan dilakukannya mikroanalisis secara kualitatif dan semi kuantitatif untuk menentukan komposisi unsur-unsur dari suatu objek material.
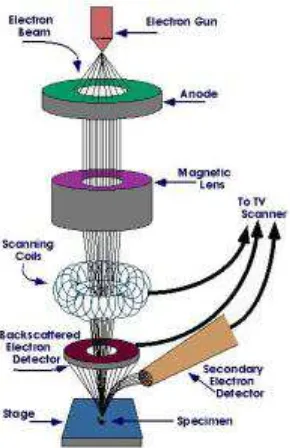
Prinsip kerja SEM yaitu bermula dari electron beam yang dihasilkan oleh sebuah filamen pada electron gun. Pada umumnya electron gun yang digunakan adalah tungsten hairpin gun dengan filamen berupa lilitan tungsten yang berfungsi sebagai katoda. Tegangan diberikan kepada lilitan yang mengakibatkan terjadinya pemanasan. Anoda kemudian akan membentuk gaya yang dapat menarik elektron melaju menuju ke anoda. Elektron berinteraksi dengan sampel komposisi
Gambar 2.8.Prinsip Kerja SEM (Scanning Electron Microscopy)-EDX
Gambar 2.9.Instrumentasi Uji SEM (Scanning Electron Microscopy)-EDX
2.6.3. Konduktivitas Listrik
Konduktivitas listrik σ (S/cm) berhubungan dengan resistivitas ρ (Ω cm)
sesuai dalam persamaan 2.2:
σ
=
1ρ (2.2)Peningkatan konduktivitas listrik disebabkan oleh eksitasi dari penambahan pengisian bebas yang diangkut oleh cahaya energi tinggi pada semikonduktor dan isolator. Material alami maupun buatan yang terdapat di alam dapat diklasifisikan menjadi tiga yaitu konduktor, isolator dan semikonduktor. Nilai dari konduktivitas listrik ketiga material tersebut berbeda. Material
Gambar2.10. Spektrum Konduktivitas Listrik dan Resistivitas
Resistansi suatu material bergantung pada panjang, luas penampang lintang, tipe material dan temperature. Pada material ohmik resistansinya tidak bergantung pada arus dan hubungan empiris ini disebut dengan hukum Ohm yang dinyatakan sesuai dalam persamaan 2.3 :
V = IR; R = konstan (2.3)
Untuk material nonohmik, arus tidak sebanding dengan tegangan. Resistansinya bergantung pada arus, didefinisikan sesuai dalam persamaan 2.4:
�
=
�� (2.4)
Kurva hubungan arus dan tegangan pada material Ohmik adalah linear sedangkan material nonohmik kurva hubungannya tidak linear. Resistansi suatu kawat penghantar sebanding dengan panjang kawat dan berbanding terbalik dengan luas penampang lintang sesuai dalam persamaan 2.4 :
�
=
ρ
�Dimana ρ disebut resistivitas material penghantar. Satuan resistivitasadalah ohm
meter (Ωm). Kebalikan dari resistivitas disebut konduktivitas (σ).Adapun nilai
konduktivitas suatu material bergantung dari sifat material tersebut. Konduktivitas listrik adalah kemampuan suatu bahan untuk menghantarkan arus listrik. Persamaan berikut merupakan hubungan konduktivitas listrik dan resistansi sesuai dalam persamaan 2.6 dan 2.7 :
�
=
σ�� (2.6)
σ
=
��� (2.7)
Nilai konduktivitas pada suatu material dapat diukur dengan mengunakan probe empat titik (four point probe), yaitu suatu jajaran empat probe diletakkan di atas material yang diukur konduktivitasnya. Kemudian sumber tegangan dipasang pada dua probe terluar untuk menghasilkan arus diantara probe dalam, dengan demikian pada probe bagian dalam akan timbul tegangan. (Keithley, 2005). Hasil yang telah didapat dianalisa berdasarkan hukum ohm.
2.6.4. Spektofotometer Ultra Violet-Visible (UV-Vis)
Karakterisasi dengan Spektofotometer Ultra Violet-Visible (UV-Vis) dilakukan untuk membantu penentuan sifat optik seperti besarnya energi gap.Spektroskopi adalah teknik yang digunakan untuk mengeksitasi elektron valensi dalam atom seperti celah pita (band) dari atom atau molekul. (M.M. Grady, 2006) Spektofotometer ini merupakan gabungan antara spektrofotometri UV dan Visible. Menggunakan dua buah sumber cahaya berbeda, sumber cahaya UV dan sumber cahaya Visible. Spektrofotometer UV-Vis mempunyai rentang pengukuran pada panjang gelombang 200-800 nm (Gambar).Gugusan atom yang mengabsorpsi radiasi UV-Vis adalah gugus kromofor. Ketika suatu molekul sederhana dikenakan radiasi elektromagnetik, molekul tersebut akan mengabsorbsi radiasi elektromagnetik yang energinya sesuai. Pada molekul terjadi transisi elektronik dan absorbsi tersebut menghasilkan garis spektrum (Gambar 2.12).
Spektrofotometer Ultraviolet-Visible (UV-Vis) digunakan untuk menentukan lebar celah pita energi dalam semikonduktor.Lebar celah pita energi semikonduktor menentukan sejumlah sifat fisis semikonduktor tersebut.Beberapa besaran yang bergantung pada lebar celah pita energi adalah mobilitas pembawa muatan dalam semikonduktor, kerapatan pembawa muatan, spektrum absorpsi, dan spektrum luminisensi. Ketika digunakan untuk membuat divais mikroelektronik, lebar celah pita energi menentukan tegangan cut off persambungan semikonduktor, arus yang mengalir dalam devais, kebergantunganarus pada suhu, dan sebagainya.
Gambar 2.13. Prinsip Kerja UV Vis Spectroscopy
dapat diloncati electron adalah dasar pita konduksi. Jarak ke dua tingkat energi tersebut sama dengan lebar celah pita energi.
Gambar 2.14.Eksitasi elektron saat di sinari dengan gelombang.
Gambar 2.15.Instrumentasi Spektrofotometer UV-Vis
Pengukuran dengan UV-Vis spektrofotometer dilakukan pada nilaiabsorbansi.Absorbansi dengan simbol A dari larutan merupakan logaritma dari (1/T atau logaritma lo/l).Absorbsi meliputi transisi dari tingkat dasar ke tingkat yang lebih tinggi, yakni tingkat tereksitasi. Dengan menelaah frekuensi bahan yang tereksitasi maka dapatdiidentifikasi dan dianalisis karakteristik dari sebuah bahan.
Pada bahan semikonduktor, kemampuan dalam menyerap radiasiatau energi disebut sebagai absorbansi dimana masing-masing bahan semikonduktor memilki nilai absorbansi dengan rentang panjang gelombang yang berbeda-beda.Absorbansi yang diukur instrument Uv-Vis sesuai dengan hukum Lambert-Berr :
� =�.�.� (2.8)
b = tebal larutan (cm) C = konsentrasilarutan (M)
�= −�1����
0 (2.9)
Dimana : α = koefisien absorbsi b = tebal sampel (cm)
I0 = intensitas cahaya yang menuju sampel (W/m2) I = intensitas cahaya yang keluar dari sampel (W/m2)
Transmitansi didefinisikan sebagai rasio antara intensitas cahaya yang ditransmisikan dengan intensitas cahaya yang menuju sampel.
�= ��
0 (2.10)
hubungan antara absorbansi dan transmitansi sebagai berikut :
A = −logT (2.11)
Penentuan nilai energi gap (celah energi) semikonduktor dapat dilakukan dengan membuat ekstrapolasi pada daerah linier dari grafik hubungan antara (αhυ)2
sebagai absis (sumbu y)terhadap hυsebagai ordinat (sumbu x)berdasarkan persamaan :
αhυ = C(hυ – Eg)n/2 (2.12)
dengan : C = konstanta
n = bilangan yang bergantung sifat transisi α = koefisien absorbansi
Kemudian dalam penentuan nilai energi foton semikonduktor dihitung berdasarkan persamaan :
�
�=
ℎ� λ (2.13)dengan :
h = tetapan Planck (6,63 x 10-34 J.s atau 4.14 ×10–15eV)
c = kecepatan cahaya (3 x 108 m/s)
λ = panjang gelombang (m)
Dengan melakukan ekstrapolasi bagian linier kurva (αhυ)2terhadap hυ memotong absis, diperoleh nilai energi yang dinamakan celah energi (Eg). Ekstrapolasi dilakukan pada daerah kurva yang meningkat tajam, dimana daerah tersebut menyatakan terjadinya transisi langsung. (Sze, S.M., 2007.)
2.6.5. FTIR(Fourier Transform Infra Red)
Sinar infra merah memiliki rentang panjang gelombang dari 2.5 μm
sampai 25 μm. Adapun frekuensi sinar infra red memiliki rentang dari 400 cm -1
sampai 4000 cm-1. FTIR merupakan salah satu pengujian tidak merusak.Dalam spektroskopi sinar infra merah, radiasi sinar infra merah ditembakkan ke arah sebuah molekul.Sebagian radiasi sinar infra merah tersebut diserap (diadsorpsi) oleh molekul dansebagian lagi diteruskan (ditransmisikan) melalui molekul tersebut yangmenghasilkan sebuah spektrum.Hasil spektrum tersebut mewakili nilai adsorpsidan transmisi dari molekul. Seperti sidik jari manusia, tidak ada molekul yangmemiliki nilai spektrum atau vibrasi yang sama. Hal itu menyebabkanspektroskopi infra merah sangat bermanfaat untuk menganalisis dari molekul.Instrumen FTIR memiliki 5 komponen, yaitu Sumber sinar infra merah, Interferometer, Sampel, Detektor, dan komputer.Alat uji FTIR ditunjukkan seperti pada Gambar 2.16.
Pengujian FTIR memiliki 3 fungsi, yaitu (i) untuk mengidentifikasimaterial yang belum diketahui, (ii) untuk menentukan kualitas atau konsistensisampel, dan (iii) untuk menentukan intensitas suatu komponen dalam sebuahcampuran. FTIR merupakan pengujian kuantitatif untuk sebuah sampel.Ukuranpuncak (peak) data FTIR menggambarkan jumlah atau intensitas senyawa yangterdapat didalam sampel.FTIR menghasilkan data berupa grafik intensitas danfrekuensi.Intensitas menunjukkan tingkatan jumlah senyawa sedangkan frekuensimenunjukkan jenis senyawa yang terdapat dalam sebuah sampel. Gambar 2.18menunjukkan hasil proses pengujian instrumental FTIR. (Thermo Nicolet Corp, 2001)