DEHIDRASI
RISINOLEAT
MENJADI
LINOLEAT
YANG
TERDAPAT
DALAM
MINYAK
JARAK
(
Ricinus
communis
L.)
MENGGUNAKAN
MOLEKULAR
SHIEVE
SECARA
REFLUKS
DALAM
BEBERAPA
PELARUT
ORGANIK
Mimpin Ginting, Herlince Sihotang, Keling Ginting*)
Abstract
Castrol oil can be isolated by extraction from kernel castrol using somes organic solvent. The isolation of castrol oil socletation give percentage 49.90 % using 2-propanol as the solvent, 46.00 % using ethanol as the solvent and 17.00% using n-hexana as the solvent.
Ricinoleic has been found as triglyceride in castrol oil can be dehydrated by refluks using moleculer shieve in somes organic solvent to result linoleic as triglyceride. The product of dehydrated give rendement 82.58% using ethanol as the solvent, 68.75% using diethyl eter as the solvent, 80.83% using petroleum eter as the solvent and 81.69% using n-hexana as the solvent. The analysis by iodine value give best product using petroleum eter as the solvent where before dehydrated is 85 and after dehydrated 120.4.5
The product of methenolysis of castrol oil and dehydratyed castrol oil is analyzed using FT-IR spectroscopy and GC-MS. Based on the analysis, we get 5-methyl ester fatty acid, which are methyl hexadecanoic 2.88% methyl 9,10-octadecadienoic 7.09% methyl 9-octadecadienoic 10.60%, methyl octadecanoic 2.35%, and methyl 12-hydroxy 9-octadecadienoic 77.08%. For the dehydrated castrol oil we get 8 methyl ester fatty acid, which are methyl hexadecanoic 2.99%, methyl 9.10-octadecadienoic 17.58%, methyl9-octadecadienoic 31.28%, methyl octadecanoic 7.08%, methyl 9,10-octadecadienoic (trans) 13.02%, methyl 9-octadecadienoic (trans) 10.74%, methyl 12-hydroxy 9-octadecadienoic 10.22% and another fatty acid 7.14%.
Keywords: Castrol oil, Extraction, Ricinoleic, Dehydrated, Refluks, Molecculer shieve, Linoleic
A. PENDAHULUAN
Minyak jarak yang merupakan suatu trigliserida dapat dibedakan dengan gliserida lainnya dari viskositas, bilangan asetil dan kelarutannya dalam alkohol yang relatif tinggi. Biji jarak mengandung 54% minyak yang disusun oleh beberapa asam lemak sebagai gliserida di antaranya asam risinoleat (75–86%), asam oleat (7–12%), asam linoleat (3,5–8%), asam palmitat (2–3%), asam stearat (1–2,5%) (Ketaren, 1986 dan Sujadmaka, 1922).
Asam risinoleat yang merupakan komposisi terbesar dari minyak jarak adalah asam lemak yang memiliki keunikan tersendiri, karena asam lemak ini merupakan turunan
asam oleat yang pada posisi ω = 7 memiliki
gugus hidroksil serta mengandung ikatan π
pada ω = 9. Dengan demikian memberikan
suatu pemikiran untuk mengubah senyawa ini ke berbagai bentuk senyawa kimia lainnya yang diharapkan bermanfaat dalam
bidang kimia oleo. Kandungan asam lemak essensial yang terdapat dalam minyak jarak sangat rendah menyebabkan minyak jarak tidak dapat digunakan sebagai bahan pangan dan minyak goreng. Sebelum digunakan untuk berbagai macam keperluan, minyak jarak perlu diolah terlebih dahulu untuk dapat meningkatkan nilai tambah dari minyak jarak. Salah satu pengolahannya adalah dehidrasi yang mana hasilnya dimanfaatkan sebagai bahan baku untuk industri kimia oleo pengganti linoleat dari minyak kemiri maupun minyak jagung (Ketaren, 1986).
Dehidrasi risinoleat dalam minyak jarak telah pernah dilakukan dengan menggunakan
NaHSO4 1% pada suhu 240 0C tekanan
5 mmHg di mana dapat dihasilkan asam linoleat terkonyugasi dan asam linoleat non konyugasi (Rumamurthi, dkk., 1998). Asam linoleat merupakan asam lemak tak jenuh (PUFA) yang merupakan asam-asam yang diperlukan bagi berlangsungnya pertumbuhan
normal semua jaringan dan ditemukan dalam lipid pembangun struktur sel (Murray, dkk., 1992; Kaban, dan Daniel, 2005).
Asam lemak essensial ω = 6 yaitu linoleat
berperan dalam kesehatan yang telah dibuktikan dari beberapa hasil penelitian, di antaranya dapat mencegah beberapa penyakit kronis (Winarno, 1993). Molekular Shieve adalah bahan pengering pelarut organik di mana sejumlah kecil air dapat memasuki pori-porinya dan terikat kuat pada bagian yang polar dalam molekular shieve (Portfield, 1993). Molekular shive ini mempunyai kemampuan absorbsi yang tinggi pada temperatur tertentu dan tersusun oleh kompleks unsur Al dan Si yang merupakan suatu asam lewis sehingga merupakan suatu katalis dalam reaksi dehidrasi terhadap alkohol sekunder untuk dapat menghasilkan suatu ikatan hidrokarbon tidak jenuh (Thio, 1957). Dari uraian di atas, mengingat kandungan asam lemak essensial dalam minyak jarak sangat rendah, peneliti tertarik untuk meningkatkan asam lemak essensial (linoleat) dan melakukan penelitian dengan judul “Dehidrasi risinoleat menjadi linoleat yang terdapat dalam minyak jarak menggunakan molekular shieve secara refluks dalam beberapa pelarut organik”. Apakah risinoleat yang terdapat dalam minyak jarak dapat didehidrasi menjadi linoleat menggunakan molekular shieve dalam berbagai pelarut organik secara refluks menggunakan alat modifikasi Claisen? Diharapkan hasil penelitian ini dapat meningkatkan nilai tambah dari minyak jarak dalam industri kimia oleo sebagai edible oil, sehingga dapat memberikan informasi di mana sebelumnya tidak dapat digunakan sebagai edible oil tetapi setelah didehidrasi diharapkan dapat digunakan karena risinoleat telah didehidrasi menjadi asam lemak essensial yaitu linoleat.
B. METODE PENELITIAN Bahan-Bahan
Bahan kimia yang digunakan dalam penelitian ini antara lain: metanol, benzena, asam sulfat, N-hexana, natrium sulfat
anhydrous, peteroleum eter, dietil eter, kalium iodida, amilum, wijs solution, karbon tetra klorida, kalium bikromat, natrium tiosulfat, natrium hidroksida, asam asetat anhidrit, kalium hidroksida, dan asam klorida adalah berderajat p.a buatan E. Merck sedangkan biji jarak diperoleh dari tanaman jarak yang tumbuh di daerah Berastagi Kabupaten Karo dan molekular shieve yang digunakan mempunyai
diameter 4,10A yang umum digunakan
sebagai bahan pengering pelarut organik.
Alat-Alat
Peralatan untuk melakukan ekstraksi, reaksi dehidrasi, metanolisis terbuat dari alat gelas yang dirancang sendiri sesuai dengan kebutuhan, penguapan pelarut digunakan rotarievaporator, sedangkan untuk analisis spektroskopi FT-IR dan GC-MS dilakukan di Laboratorium Kimia Organik Universitas Gadjah Mada Yogyakarta.
Prosedur Penelitian
a. Isolasi Minyak Jarak dari Biji Jarak
Biji jarak pertama sekali dipisahkan dari cangkangnya kemudian dikeringkan dan dihaluskan. Serbuk biji halus kemudian diekstraksi secara sokletasi dengan beberapa jenis pelarut organik. Ekstrak yang diperoleh kemudian dikeringkan
dengan Na2SO4 anhidrous untuk
menghilangkan adanya air. Setelah disaring dengan kertas saring whatman filtrat hasil saringan diuapkan dengan rotarievaporator sehingga diperoleh minyak jarak sebagai residu.
b. Dehidrasi Risinoleat Menjadi Linoleat yang Terdapat dalam Minyak Jarak
Sebanyak 46,6 g minyak jarak dimasukkan ke dalam leher dua yang dilengkapi stirrer, penangas minyak, kolom fraksinasi sepanjang 90 cm, pendingin bola dan
corong pisah serta tabung CaCl2 anhidrous.
Kemudian ditambahkan pelarut organik dan sebanyak 2,0 g molekul shieve yang telah diaktifkan. Selanjutnya direfluks pada suhu pelarut selama lebih kurang 24 jam. Hasil refluks didinginkan dan ditambahkan dietil eter. Kelebihan air dihilangkan dengan
penambahan Na2SO4 anhidrous lalu
dengan rotarievaporator. Residu dari hasil penguapan dianalisis harga bilangan Iodin, bilangan asam, bilangan penyabunan, bilangan hidroksil, asam lemak bebas serta komposisi jenis asam lemaknya.
c. Analisis Hasil Dehidrasi
Penentuan Komposisi Asam Lemak Minyak Jarak Terdehidrasi
Sebanyak 10 ml sampel dimasukkan ke dalam labu leher dua yang dilengkapi dengan stirrer dan ditambahkan sebanyak 40 ml metanol. Campuran dalam keadaan dingin sambil diaduk ditetesi sebanyak
2 ml H2SO4 pekat secara perlahan dan
ditambahkan benzena sebanyak 40 ml. Selanjutnya direfluks selama 5 jam. Hasil reaksi diuapkan melalui rotarievaporator,
kemudian residu dilarutkan dalam
n-heksana. Ekstrak dicuci berturut-turut
dengan larutan encer NaHCO3 dan
kemudian dengan aquadest yang
selanjutnya dikeringkan dengan Na2SO4
anhidrous. Dilakukan penguapan melalui rotarievaporator dan residu dari hasil penguapan dianalisis dengan spektroskopi FT-IR yang diikuti analisis GC-MS.
Penentuan Bilangan Iodin
Penetuan bilangan iodin dilakukan secara titrasi iodometri menggunakan pereaksi
Wijs serta larutan penitrasi Na2S3O3 dan
indikator larutan kanji (AOCS. Cd 1–25).
Penentuan Bilangan Asam
Penentuan bilangan asam dilakukan secara titrasi acidi alkalimetri menggunakan larutan KOH dan indicator fenolfetalein (AOCS. Cd 3a–65).
Penentuan Bilangan Penyabunan
Ditentukan secara titrasi asidialkalimetri dengan larutan HCl dan indikator larutan fenolpthalein (AOCS.Cd 3–25).
Penentuan Bilangan Hidroksil
Ditentukan berdasarkan harga bilangan
penyabunan sebelum dan sesudah
diasetilasi (AOCS. Cd 13–60).
Penentuan Asam Lemak Bebas
Sebanyak 10 g minyak hasil dehidrasi ditimbang dengan teliti dalam erlenmeyer 250 ml, ditambahkan 50 ml isopropanol
netral. Lalu dititrasi dengan larutan NaOH 0,1 N dengan menggunakan indikator fenolfetalein hingga warna merah jambu. Kadar asam lemak bebas (ALB) =
% 100 x ) g ( sample Berat BM x N x V di mana:
V = Volume NaOH yang dipakai untuk titrasi
N = Normalitas larutan NaOH yang
digunakan
BM = Berat molekul asam lemak
penyusun minyak.
C. HASIL DAN PEMBAHASAN
Dari sebanyak 1000 g biji jarak diperoleh kernel (daging biji) sebanyak 700 g. Hasil ektraksi minyak jarak diperoleh dengan menggunakan pelarut 2-propanol (49,9%), etanol (46,00%) dan n-heksana (17%). Dalam hal ini menggunakan pelarut 2-propanol diperoleh kandungan minyak terbanyak, disebabkan karena 2-propanol merupakan alkohol sekunder, di mana risinoleat yang terdapat dalam minyak jarak juga digolongkan ke dalam kelompok alkohol sekunder. 2-Propanol dapat mengekstraksi minyak biji jarak lebih banyak dibandingkan dengan etanol yang merupakan alkohol primer dan n-heksan merupakan hidrokarbon yang non-polar sedangkan risinoleat pada minyak jarak karena memiliki hidroksil memiliki sifat yang sedikit lebih polar.
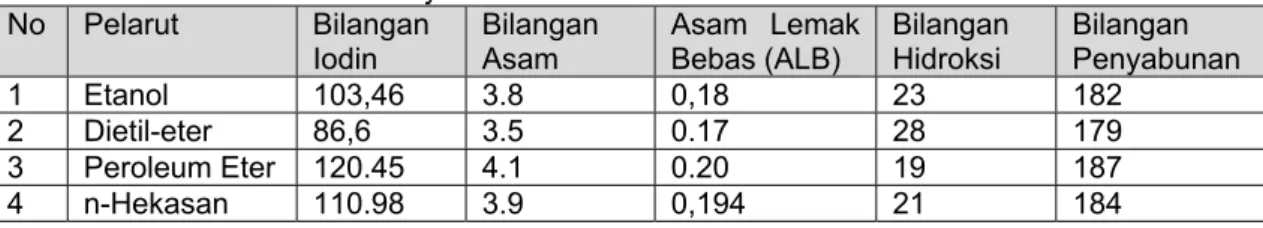
Hasil dehidrasi risinoleat pada minyak jarak menjadi linoleat menggunakan molekular shieve dalam beberapa pelarut organik diperoleh dengan menggunakan pelarut etanol (82,58%), dietileter (68,75%), petroleum eter (80,83%) dan n-heksana (81,69%). Selanjutnya hasil analisis sifat kimia dari minyak jarak terhidrasi diperoleh hasil seperti pada Tabel 1.
Dehidrasi terhadap minyak jarak dengan menggunakan molekular shieve dalam beberapa pelarut organik secara refluks menggunakan alat modifikasi Claisen ternyata terbaik dijumpai menggunakan
pelarut petroleum eter dengan bilangan bilangan iodin sebesar 120,45 yang mana sebelumnya minyak jarak sebesar 85. Hal ini disebabkan karena air yang terlepas dari hasil dehidrasi segera membentuk campuran azeotrop dengan pelarut petroleum eter yang tekanan uapnya lebih besar sehingga dapat diikat oleh pelarut tersebut di bawah titik didih air. Pelarut N-heksan memiliki tekanan uap yang lebih rendah sehingga hasilnya di bawah dari hasil dehidrasi menggunakan petroleum eter. Sedangkan pelarut etanol memiliki titik didih langsung membentuk campuran homogen dengan air sehingga proses dehidrasi terhambat dan untuk pelarut dietil eter yang memiliki titik didih terendah, pelarut ini kemungkinan telah menguap sebelum terjadi dehidrasi.
Molekul shieve yang digunakan dalam
penelitian ini adalah tipe 40A dengan rumus
Na12(Al12Si12O48). Molekular shieve ini
dengan segera dapat menyerap air.
Na12(Al12Si12O48) + xH2O Na12(Al12Si12O48)xH2O
Selanjutnya karena penyusun kompleks dari molekul shieve adalah Al dan Si yang
merupakan alam lewis (Elektrofil, E+),
dalam proses dehidrasi terhadap gugus hidroksil sekunder pada risinoleat yang secara hipotesis mekanismenya diperkirakan seperti pada Gambar 1.
Hasil analisis spektroskopi FT-IR untuk metil ester asam lemak minyak jarak terdehidrasi memberikan spektrum dengan puncak-puncak serapan pada daerah
bilangan gelombang 3448 cm-1
menunjukkan adanya gugus –OH, diperkuat
pada daerah bilangan gelombang 1245 cm
-1, pada 2927 dan 2586 cm-1 menunjukkan
adanya serapan C-H sp3 streaching pada
CH2 dan CH3 dan diperkuat dengan
serapan pada daerah bilangan gelombang
1363 cm-1 merupakan C-H sp3 bending
simetri dan 1458 cm-1 merupakan C-H sp3
simetri. Adanya serapan pada daerah
bilangan gelombang 1741 cm-1
menunjukkan gugus C=O untuk ester, diperkuat pada daerah bilangan gelombang
1172 cm-1 menunjukkan adanya gugus C-C
(=O) ester dan pada 1120 cm-1 adanya
C-O-C. Pada daerah bilangan gelombang
1654 cm-1 merupakan serapan yang lemah
untuk C=C olefin, didukung oleh bilangan
gelombang 3006 cm-1 serta pada daerah
bilangan gelombang 725 cm-1 menunjukkan
puncak vibrasi rocking (CH2)n untuk n lebih
besar 4.
Hasil analisa GC-MS terhadap metil ester asam lemak minyak jarak dan minyak jarak terdehidrasi merupakan suatu campuran asam lemak jenuh dan tak jenuh seperti pada Tabel 2. Hasil analisis GC-MS menunjukkan bahwa sebelum dehidrasi dijumpai sebanyak 5 jenis asam lemak dari penyusun trigrliserida dari minyak jarak dan sesudah terdehidrasi dijumpai 8 jenis senyawa. Hasil dehidrasi menunjukkan bahwa penurunan risinoleat terjadi sebanyak 66,78% dan penambahan linoleat sebanyak 33,51% sedangkan penambahan oleat = 31,42%.
Tabel 1. Hasil Analisis Kimia Minyak Jarak Terdehidrasi No Pelarut Bilangan Iodin Bilangan Asam Asam Lemak Bebas (ALB) Bilangan Hidroksi Bilangan Penyabunan 1 Etanol 103,46 3.8 0,18 23 182 2 Dietil-eter 86,6 3.5 0.17 28 179 3 Peroleum Eter 120.45 4.1 0.20 19 187 4 n-Hekasan 110.98 3.9 0,194 21 184
Tabel 2. Hasil GC-MS Metil Ester Asam Lemak Minyak Jarak Sebelum dan Sesudah Dehidrasi No Nama Rumus Kandungan (%)
Sebelum dehidrasi Sesudah dehidrasi 1 Metil palmitat, C17H34O2 2.88 2.99
2 Unknown 7.14 3 Metil linoleat (cis) C19H34O2 7.09 17.58
4 Metil Oleat ,(cis) C19H36O2 10.60 31.28
5 Metil Stearat, C19H38O2 2.35 7.09
6 Metil linoleat ,(trans) C19H34O2 13.02
7 Metil oleat,(trans) C19H36O2 10.74
8 Metil risinoleat C19H36O2 77,08 10.22
Gambar 1. Mekanisme Dehidrasi Risinoleat Menjadi Linoleat pada Minyak Jarak
Analisis spektroskopi MS dari metil risinoleat yang diperoleh dari hasil esterifikasi minyak jarak dan hasil dehidrasi minyak jarak, memberikan puncak ion molekul pada m/z 312 yang merupakan massa rumus dari metil risinoleat (lampiran 1), sedangkan puncak pada m/z 269 menunjukkan massa ion molekul CH2(CH2)2
CHOHCH2CH=CH(CH2)7COOCH3+
dihasilkan dari pelepasan radikal C3H7,
puncak ion molekul pada m/z 255, 241 dan 227 dan merupakan massa dari ion
CH2(CH2)
CHOHCH2CH=CH(CH2)7COOCH3+.
CH2CHOHCH2CH=CH(CH2)7COOCH3+,dan
CHOHCH2CH=CH(CH2)7COOCH3+,
dihasilklan dari pelepasan radikal, .CH2,
puncak pada ion molekul m/z 157
merupakan massa ion, (CH2)7COOCH3+,
dihasilkan dari pelepasan radikal C4H6O
yang merupakan karakteristik alkohol rantai panjang, puncak ion molekul pada m/z 143 dan 115 merupakan massa ion (CH2)6COOCH3+ dan (CH2)4COOCH3+
dihasilkan dari pelepasan radikal .CH2 dan
.C2H4, puncak pada m/z=101 merupakan
massa ion (CH2)3COOCH3+ dihasilkan dari
pelepasan radikal CH2, puncak pada ion
molekul m/z 88 merupakan massa ion
CH3CH2COOCH3+ dihasilkan dari
pelepasan .CH yang merupakan karakteristik senyawa hidrokarbon tidak jenuh, puncak pada ion molekul m/z 57
merupakan massa ion CH3CH2C=O+
dihasilkan dari pelepasan radikal .OCH3,
puncak pada ion molekul m/z 43
merupakan massa ion CH3C=O+ dihasilkan
dari radikal CH2.
Hasil analisis GC-MS terhadap metil linoleat hasil dehidrasi dari risinoleat pada minyak jarak memberikan spektrum MS dengan puncak ion molekul pada m/z = 294 merupakan massa rumus dari metil linoleat (Lampiran 2). Puncak-puncak selanjutnya diikuti pada m/z 262 yang merupakan massa ion CH3(CH2)4CH=CH2CH=CH(CH2)6
CH=C=O+ dihasilkan dari pelepasan
CH3OH yang merupakan karakteristik senyawa metil ester. Puncak-puncak pada m/z 220 merupakan massa dari ion CH3(CH2)4CH=
CH2CH=CH(CH2)6CH=CH2+., dihasilkan dari
pelepasan radikal CH2C=O. Puncak pada
m/z 178 merupakan massa ion CH3(CH2)4CH=CH2CH=CHCH2CH=CH2+.
dihasilkan dari pelepasan radikal C3H6.
Puncak m/z 164 merupakan massa ion CH3(CH2)4CH=CH2CH=CHCH=CH2+.,
dihasilkan dari pelepasan CH2, puncak m/z
123 merupakan massa ion CH3(CH2)4CH=
CHCH=CH+, dihasilkan dari pelepasan
radikal C2H3 yang merupakan ciri khas
hidrokarbon tidak jenuh. Puncak pada m/z 109, 95, 61, dan 67 merupakan massa dari
ion CH3(CH2)4CH=CHCH=CH+,
CH3(CH2)3CH= CHCH=CH+,
CH3(CH2)2CH=CHCH=CH+,
CH3CH2CH=CHCH=CH+, dihasilkan dari
pelepasan CH2. Yang merupakan karakteristik senyawa hidrokarbon tidak jenuh, puncak pada m/z 41 merupakan massa dari ion CH2CH=CH2+..
D. KESIMPULAN DAN SARAN
Kesimpulan
Berdasarkan hasil penelitian yang dilakukan dapat disimpulkan:
1. Hasil ekstraksi minyak jarak secara sokletasi terhadap biji jarak dari tiga jenis pelarut yang digunakan yakni 2-propanol, etanol, dan N-heksana memberikan hasil yang terbaik adalah menggunakan pelarut 2-propanol.
2. Dehidrasi risinoleat pada minyak jarak menjadi linoleat terhadap minyak jarak menggunakan molekular shieve secara refluks menggunakan pelarut petroleum eter, N-heksana, etanol, dan dietil eter memberikan hasil yang terbaik adalah menggunakan pelarut petroleum eter. 3. Berdasarkan hasil analisis spektroskopi
FT-IR dan GC-MS menunjukkan bahwa dehidrasi minyak jarak terjadi penurunan risinoleat dari 77,08% menjadi 10,22% sedangkan kenaikan linoleat terjadi perubahan dari 7,09% sebelum dehidrasi menjadi 30,60% sesudah dehidrasi yang terdiri dari campuran cis sebesar 17,58% dan trans sebesar 13,02%.
Saran
1. Perlu dibandingkan dehidrasi risinoleat menjadi linoleat yang terdapat dalam minyak jarak menggunakan dehidrator
lain seperti H2SO4(p), H3PO4, dan
alumina.
2. Adanya asam lemak trans yang
terdapat pada hasil dehidrasi, disarankan lebih baik digunakan sebagai bahan industri kimia oleo dan apabila digunakan sebagai bahan pangan perlu dilakukan pemisahan terlebih dahulu.
24
E. DAFTAR PUSTAKA
___ , (1989), “Official Methods And
Recommended Practices Of The American Oil Chemits Society
(AOCS)” , 4th edition Vol.1,
Commercial Fats and Oils.
Rumamurthi, S., Monahar, V. and Mani, V.
V. S., (1998), “Characterization of
Fatty Acid Isomers in Dehydrated Castrol Oil and GC-MS Techniques”,
JAOCS Vol. 75: 1297.
Prtifield, W. W., (1993), “Inorganic Chemistry”,
Seconnd Edition, Academic Press, Inc., Sandiego: 165.
Christie, W. W., (1982), “Lipid
Analysis-Isolation, Separation, Indentification and Structural Analysis Of Lipid”, 2nd
edition, Pergaman Press Ltd., Oxford, England: 73.
Silverstein, (1981), ”Penyelidikan
Spektrometrik Senyawa Oranik”, Edisi
ke-4, Erlangga Jakarta.
Sujadmaka, (1992),. “Prospek Pasar
Budidaya Jarak”, Edisi 1, PT. Penebar
Swadaya, Jakarta: 1–20.
Jhon, M. D., (1980), “Principles of Food
Chemistry”, Van Nostrad Reinhold
Co., New York: 38. Thio, P. A., (1977), ”Molecular Shieve for
Selective Adsorption”, Second
Edition, The British Drug Houses Ltd., England, 10, 21.
Kaban, J. dan Daniel, (2005), “ Sintesis n-6
Etil Ester Asam Lemak dari Beberapa Minyak Ikan Air Tawar, ”Komunikasi
Penelitian , Vol. 17(2): 14–20. Winarno, (1993), Pangan Gizi, Teknologi dan Konsumen”, Edisi I, Penerbit PT.
Gramedia Pustaka Umum, Jakarta.
Ketaren, S., (1986), “Pengantar Teknologi
Lemak dan Minyak Pangan”, Cetakan
1, Penerbit UI-Press, Jakarta: 264– 268.
LAMPIRAN
Lampiran 1. Spektrum MS Metil Risinoleat