LAPORAN TETAP
PRAKTIKUM BIOKIMIA UMUM
Disusun oleh : KELOMPOK III
PROGRAM STUDI TEKNIK PERTANIAN
FAKULTAS TEKNOLOGI PANGAN DAN AGROINDUSTRI UNIVERSITAS MATARAM
KATA PENGANTAR
Puji syukur Penulis panjatkan kepada tuhan Yang Maha Esa atas tersusunnya laporan tetap biokimia umum yang merupakan salah satu syarat telah menyelesaikan mata kuliah Biokimia Umum pada Semester Gasal 2014/2015 di Fakultas Teknoloogi Pangan dan Agroindustri Universitas Mataram. Penulis menyampaikan terima kasih kepada semua pihak yang telah membantu penyusunan laporan dan pelaksanaan praktikum biokimia umum. Penulis menyadari adanya kekurangan dalam penyusunan laporan tetap ini sehingga saran dari pembaca sangat penulis harapkan untuk penyempurnaan laporan biokimia umum ini. Semoga laporan ini dapat bermanfaat untuk meningkatkan wawasan para pembaca tentang biokimia secara umum.
Mataram, 22 Desember 2015
iv
DAFTAR ISI
Halaman
HALAMAN SAMPUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... iv
DAFTAR TABEL ... vi
ACARA I PENGENALAN ALAT DAN BAHAN PENDAHULUAN ... 1 TINJAUAN PUSTAKA ... 3 PELAKSANAAN PRAKTIKUM ... 5 HASIL PENGAMATAN ... 6 PEMBAHASAN ... 12 KESIMPULAN ... 15
ACARA II LARUTAN BUFFER PENDAHULUAN ... 16 TINJAUAN PUSTAKA ... 18 PELAKSANAAN PRAKTIKUM ... 20 HASIL PENGAMATAN ... 22 PEMBAHASAN ... 24 KESIMPULAN ... 26
ACARA III PENGUJIAN KARBOHIDRAT PENDAHULUAN ... 27 TINJAUAN PUSTAKA ... 29 PELAKSANAN PRAKTIKUM ... 32 HASIL PENGAMATAN ... 34 PEMBAHASAN ... 35 KESIMPULAN ... 38
ACARA IV PENGUJIAN PROTEIN PENDAHULUAN ... 39 TINJAUAN PUSTAKA ... 41 PELAKSANAAN PRAKTIKUM ... 43 HASIL PENGAMATAN ... 46 PEMBAHASAN ... 47 KESIMPULAN ... 49
ACARA V PENGUJIAN LEMAK PENDAHULUAN ... 50 TINJAUAN PUSTAKA ... 52 PELAKSANAAN PRAKTIKUM ... 54 HASIL PENGAMATAN ... 57 PEMBAHASAN ... 58 KESIMPULAN ... 61
ACARA VI PENGUJIAN ENZIM PENDAHULUAN ... 63 TINJAUAN PUSTAKA ... 64 PELAKSANAAN PRAKTIKUM ... 66 HASIL PENGAMATAN ... 68 PEMBAHASAN ... 69 KESIMPULAN ... 71
ACARA VII SPEKTROFOTOMETER PENDAHULUAN ... 72 TINJAUAN PUSTAKA ... 74 PEMBAHASAN ... 77 KESIMPULAN ... 79 DAFTAR PUSTAKA LAMPIRAN
vi
DAFTAR TABEL
Halaman
Tabel 1.1 Hasil Pengamatan Alat-alat Praktikum dan Fungsinya ... 6
Tabel 1.2 Hasil Pengamatan Analisis MSDS Bahan Kimia ... 8
Tabel 2.1 Hasil Pengamatan Perubahan pH HCl ... 22
Tabel 2.2. Hasil Pengamatan Perubahan pH H2PO4 ... 22
Tabel 3.1. Hasil Pengamatan Uji Molish ... 34
Tabel 3.2. Hasil Pengamatan Uji Selliwanof ... 34
Tabel 3.3. Hasil Pengamatan Uji Benedict ... 34
Tabel 3.4. Hasil Pengamatan Uji Iodin ... 35
Tabel 4.1. Hasil Pengamatan Uji Ninhidrin ... 46
Tabel 4.2. Hasil Pengamatan Uji Biuret ... 46
Tabel 4.3. Hasil Pengamatan Uji Sulfur ... 46
Tabel 4.4. Hasil Pengamatan Pengendapan Susu ... 46
Tabel 5.1. Hasil Pengamatan Kelarutan Lemak ... 57
Tabel 5.2. Hasil Pengamatan Ketidakjenuhan ... 57
Tabel 5.3. Hasil Pengamatan Penyabunan ... 57
Tabel 6.1. Hasil Pengamatan Perubahan Warna Larutan Pati ... 68
ACARA I
PENGENALAN ALAT DAN BAHAN
PENDAHULUAN
Latar Belakang
Laboratorium merupakan tempat melakukan penelitian dan berbagai percobaan. Pada percobaan biasanya menggunakan alat-alat yang ada di Laboratorium. Alat-alat dalam Laboratorium memiliki fungsi dan prosedur kerja yang berbeda-beda. Percobaan tersebut harus diperhatikan dengan serius karena selama praktikum praktikan akan berhubungan dengan alat tersebut. Selain itu, peralatan yang ada di Laboratorium juga dapat mengakibatkan bahaya yang tak jarang berisiko tinggi bagi praktikum yang sedang melakukan praktikum, jika tidak mengetahui cara dan prosedur penggunaan alat yang akan digunakan (Anonim, 2014).
Alat-alat yang akan digunakan di Laboratorium, harus diperhatikan kebersihannya. Kebersihan dari alat dapat mengganggu hasil praktikum. Apabila alat yang digunakan tidak bersih, maka akan terjadi hal-hal yang tidak diinginkan. Contohnya jika pada alat-alat tersebut masih tersisa zat-zat kimia, maka zat tersebut dapat bereaksi dengan zat yang kita gunakan sesudahnya dan dapat mengakibatkan kegagalan dalam praktikum. Kesalahan dalam penggunaan alat dan bahan dapat menimbulkan hasil praktikum yang didapat tidak akurat dan dapat menyebabkan dampak negatif pada keselamatan diri-sendiri maupun orang lain (Hasrah, 2013).
Pengenalan alat dan bahan ini sangat penting untuk dikuasai oleh praktikan sebelum melakukan praktikum di Laboratorium. Agar dapat
2
mengetahui dan memahami serta menguasai jeni-jenis alat dan bahan, nama masig-masing alat an bahan, dan fungsi masing-masing alat dan bahan yang dilakukan dengan bahan kimia berbahaya. Disamping itu pemilihan jenis alat yang akan digunakan dalam penelitian disesuaikan dengan tujuan, agar penelitian berjalan lancar. Oleh karena itu, dilakukan praktikum ini untuk mengetahui dan memahami serta menguasai jenis-jenis alat dan bahan, nama masing-masing alat dan bahan, dan fungsi masing-masing alat dan bahan yang baik dan benar.
Tujuan Praktikum
Adapun tujuan dari praktikum ini adalah untuk mengetahui dan memahami serta menguasai jenis-jenis alat dan bahan, nama masing-masing alat dan bahan, dan fungsi masing-masing alat dan bahan yang baik dan benar.
TINJAUAN PUSTAKA
Kegiatan praktikum yang dilaksanakan merupakan kegiatan praktikum kimia skala makro. Meskipun tidak diragukan lagi keunggulannya, praktikum skala makro menunjukkan kelemahan yaitu diperlukan zat kimia yang lebih banyak. Sehingga memerlukan biaya yang cukup besar, menuntut kesiagaan dalam pengalaman, karena dapat mengganggu kesehatan dan dapat menimbulkan kecelakaan. Untuk mengatasi permasalahan dalam pelaksanaan dalam pelaksanaan praktikum skala makro Sillberman (1994), Asep dkk (1997) dan Gebi dkk (1999) mengusulkan untuk melakukan praktikum kimia dalam skala mikro. Praktikum yang digunakan dalam penelitian ini adalah praktikum skala mikro dengan alat dan bahan yang digunakan dengan desain ukuran yang lebih kecil dari pralatan yang digunakan pada praktikum biasanya (Sri, 2008).
Percobaan di Laboratorium kimia seseorang akan selalu dihadapkan pada hal-hal yang berhubungan dengan bahan-bahan kimia, peralatan yang dapat berbahaya dan merugikan bagi diri-sendiri, orang lain maupun lingkungan sekitar, bila tidak digunakan dengan baik. Seperti layaknya pekerjaan lain, bekerja dalam Laboratorium kimia juga mempunyai resiko kecelakaan kerja. Resiko ini dapat disebabkan karena faktor ketidaksengajaan, keteledoran dan sebab-sebab lain yang diluar kendali manusia. Terutama disebabkan karena kesalahan penggunaan alat dan bahan. Sehingga menjadi sangat penting untuk mengetahui setiap kemungkinan bahaya (Hala, 2009).
Zat atau bahan hendaknya menggunakan suatu alat untu mengukurnya. Alat yang digunakan untuk mengukur suatu zat kimia adalah gelas ukur. Akan tetapi, pengukuran dari gelas ukur ini penggunaannya tidaklah terlalu teliti. Salah
4
satu contoh alat praktikum pengukuran yang mempunyai tingkat ketelitian tinggi yaitu pipet ukur. Namun pengukuran dengan pipet ukur ini tidak terlepas juga dari ketelitian praktikum (Rohman, 2011).
Praktikum adalah subsistem dari perkuliahan yang merupakan kegiatan terstruktur dan terjadwal yang memberi kesempatan kepada mahasiswa untuk mendapatkan pengetahuan nyata pekerjaan dalam laboratorium sering menggunakan beberapa alat gelas. Penggunaan alat ini dengan tepat untuk diketahui pekerjaan tersebut dapat berjalan baik. Keadaan yang aman dalam suatu laboraatorium dapat diciptakan apabila ada kemauan dari para pekerja, pengguna dan kelompok pekerja laboratorium untuk menjaga dan melindungi diri diperlukan kesadaran bahwa kecelakaan yang terjadi dapat berakibat fatalpada dirinya sendiri ataupun orang lain disekitarnya. Tujuan dari praktikum pengenalan alat adalah untuk mengenal beberapa macam alat gelas yang sering digunakan dalam Laboratorium dan penggunaannya (Ginting, 2011).
Penggunaan alat-alat praktikum dan bahan kimia serta cara pemakaiannya merupakan hal sangat penting dalam praktikum. Banyak bahan kimia yang harus ditangani dengan hati-hati karena sifatnya berbahaya dan beracun. Dari uraian tersirat tersebut bahwa nama setiap alat dan bahan kimia mempunyai ciri-ciri dan kegunaan yang berbeda seperti dilihat dari bentuk alat tersebut. Setiap percobaan selalu menggunakan peralatan yang berbeda meskipun sama tapi ukurannya berbeda (Puja, 2011).
PELAKSANAAN PRAKTIKUM
Waktu dan Tempat Praktikum
Praktikum ini dilaksanakan pada hari Rabu, 04 November 2015 di Laboratorium Kimia dan Biokimia Pangan, Fakultas Teknologi Pangan dan Agroindustri, Universitas Mataram.
Alat dan Bahan Praktikum a. Alat-alat Praktikum
Alat-alat yang digunakan pada praktkum ini adalah Neraca Analitik, Hot Plate, erlenmeyer, Rubber Bulb, pipet gondok, pipet ukur, pipet tetes, tabung reaksi, gelas beaker dan pengaduk kaca.
b. Bahan-bahan Praktikum
Bahan-bahan yang digunakan pada praktikum ini adalah Asam Sulfat, NaCl, NaOH, HCl dan HNO3.
6
HASIL PENGAMATAN
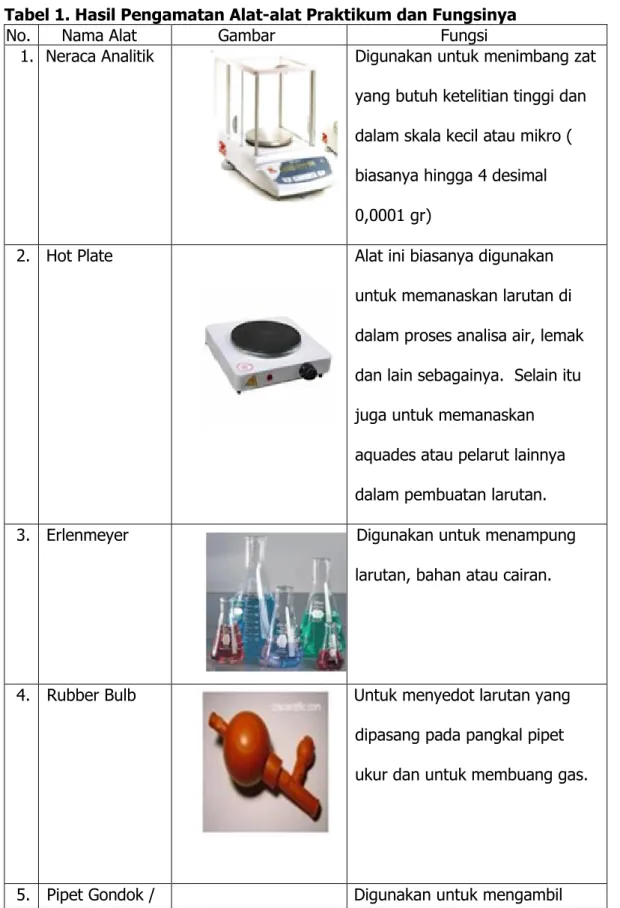
Tabel 1. Hasil Pengamatan Alat-alat Praktikum dan Fungsinya
No. Nama Alat Gambar Fungsi
1. Neraca Analitik Digunakan untuk menimbang zat yang butuh ketelitian tinggi dan dalam skala kecil atau mikro ( biasanya hingga 4 desimal 0,0001 gr)
2. Hot Plate Alat ini biasanya digunakan
untuk memanaskan larutan di dalam proses analisa air, lemak dan lain sebagainya. Selain itu juga untuk memanaskan aquades atau pelarut lainnya dalam pembuatan larutan.
3. Erlenmeyer Digunakan untuk menampung
larutan, bahan atau cairan.
4. Rubber Bulb Untuk menyedot larutan yang
dipasang pada pangkal pipet ukur dan untuk membuang gas.
Pipet Volume larutan dengan volume tepat.
6. Pipet Ukur Untuk mengukur volume larutan.
7. Pipet Tetes Untuk meneteskan atau
mengambil larutan dengan jumlah kecil.
8. Tabung Reaksi Untuk mereaksikan dua atau
8
9. Gelas Beaker Tempat untuk menyimpan dan
membuat larutan. Beaker glass memiliki takaran namun jarang bahkan tidak diperbolehkan untuk mengukur volume suatu zat cair.
10. Pengaduk Kaca Untuk mengocok atau mengaduk
suatu baik akan direaksikan maupun ketika reaksi sementara berlangsung.
Tabel 2. Hasil Pengamatan Analisis Material Safety Data Sheet (MSDS) Bahan Kimia
No. Nama
Dagang Nama Kimia Bahaya (Sifat) Penanganan Pertama 1. Asam Sulfat Asam
Sulfat Reagen ACS (H2SO4) Bahaya : - Menyebabkan iritasi parah dan luka bakar, mungkin bahaya jika tertelan - Hindari mengirup
uap atau debu - Hindari kontak dengan mata, kulitbdan pakaian Sifat :
Terkena pada : - Kulit : cuci daerah
yang terkena dengan sabun dan air. Jika terjadi iritasi, dapatkan bantuan medis.
- Mata : Cuci mata dengan banyak air selama 15 menit, angkat
- Tidak mudah terbakar
- Titik didih : 534-590 ºC
- Tidak berwarna keruh menjadi cair sedikit kuning tutup sesekali. Menari bantuan medis - Terhisap : Hapus dengan udara segar. Berikan napas buatan atau oksigen. - Tertelan : berikan beberapa gelas susu atau air. 2. Garam Dapur Natrium Klorida (NaCl) Bahaya: - Dapat menyebabkan gangguan pernapasan, iritasi mata dan kulit apabila terjadi kontak langsung. Sifat :
- Berbentuk bubuk kristal warna putih. - Mudah larut dalam
air dingin dan panas.
- Apabila terhirup, bawa ketempat yang lebih segar. - Apabila kontak langsung segera membasuh dengan air. 3. Natrium Hidroksida (Soda Api) Hidroksida (NaOH) Bahaya : - Dapat menyebabkan luka bakar pada kulit dan kerusakan mata yang serius, - Dapat merusak
- Menggunakan sarung tangan - Apabila terkena
mata, bilas
dengan air selama beberapa menit.
10
logam-logam. Sifat :
- Tidak mudah terbakar
- Memiliki bau yang tajam 4. Asam Klorida/ Asam Hydrochlonic Hcl Bahaya : - Dapat menyebabkan kerusakan pada jaringan bila terkena kulit. - Dampak menyebabkan kerusakan kornea bila terkena mata. Sifat :
- Tidak mudah terbakar.
- Memiliki bau yang tajam.
- Lepaskan pakaian dan sepatu yang terkena
kontaminasi. - Apabila terkena
mata atau kulit, segera basuh dengan air.
5. Asam Nitrat HNO3 Bahaya :
- Keterpaan uap yang berwarna cokelat
menyebabkan iritasi bahkan luka bakar pada saluran
pernapasan, kulit dan mata.
- Apabila terkena kulit, lepas pakaian yang
terkontaminasi - Apabila terkena
mata, semprot dengan air hati-hati.
- Apabila terhirup, bawa ketempat segar.
Sifat : - Bentuk cair - Tidak berwarna - Korosif - Oksidator Kuat
12
PEMBAHASAN
Larutan adalah campuran homogen yang terdiri dari dua atau lebih zat. Zat yang jumlahnya lebih sedikit di dalam larutan disebut (zat) terlarut atau solut, sedangkan zat yang jumlahnya lebih banyak daripada zat-zat lain dalam larutan disebut pelarut atau solven. Komposisi zat terlarut dan pelarut dalam larutan dinyatakan dalam konsentrasi larutan, sedangkan proses pencampuran zat terlarut dan pelarut membentuk larutan disebut pelarutan atau solvasi (Ani, 2010).
Konsentrasi larutan menyatakan secara kuantitatif komposisi zat terlarut dan pelarut di dalam larutan. Konsentrasi umumnya dinyatakan dalam perbandingan jumlah zat terlarut dengan jumlah total zat dalam larutan, atau dalam perbandingan jumlah zat terlarut dengan jumlah pelarut (Budiansyah, 2011).
1. HCl yang dikonsentrasikan (BM 36,5) memiliki kerapatan 1,19 g/ml dan 37% dari berat HCl. Berapa ml asam konsentrat tersebut yang harus dilarutkan dalam 1 liter air untuk membuat larutan 0,1 M?
Penyelesaian : Diketahui : - Berat = 37% - Massa Jenis = 1,19 g/ml - BM = 36,5 - M2 = 0,1 - V2 = 1 lt = 1000 ml Ditanyakan : V1?
Jawab : M1 = 10 x % berat x = 10 x 37 x = 12,06 Molar V1.M1 = V2.M2 V1 =
=
=
-=
= 8,3 ml
2. Pembuatan larutan NaOH 0,1 M (Volume 50 ml) Diketahui : - m = 0,1 m - V = 50 ml Ditanyakan massa (x)? Jawab : m =
x
0,1 =x
0,1 = x 20
14
0,1 =
0,4 = 2x x =
KESIMPULAN
Berdasarkan hasil pengamatan dan pembahasan, maka dapat ditarik beberapa kesimpulan sebagai berikut :
1. Larutan adalah campuran homogen yang terdiri dari dua atau lebih zat.
2. Konsentrasi larutan menyatakan secara kuantitatif komposisi zat terlarut dan pelarut di dalam larutan.
3. Volume HCl yang dikonsentrasikan dengan 1 ml air dan menghasilkan 8,3 ml untuk larutan 0,1 M.
4. Larutan NaOH yang ditambahkan dengan volume 5 ml menghasilkan 0,2 gram.
16
ACARA II LARUTAN BUFFER
PENDAHULUAN
Latar Belakang
Larutan penyangga sangat penting dalam kehidupan, misalnya dalam analisis kimia, biokimia, bakteriologi, zat warna, fotografi, dan industri kulit. Dalam bidang biokimia, kultur jaringan dan bakteri mengalami proses yang sangat sensitif terhadap perubahan kerja pH. Darah dalam tubuh manusia mempunyai kisaran pH 7,35 sampai 7,45 dan apabila pH darah manusia di atas 7,8 akan menyebabkan organ tubuh manusia dapat rusak, sehingga harus dijaga kisaran pHnya dengan larutan penyangga (Sukirno, 2009).
Untuk menjaga pH larutan agar tidak mengalami perubahan yang mencolok, digunakan zat-zat yang bersifat penyangga. Larutan penyangga atau larutan buffer adalah larutan yang dapat mempertahankan pH pada kisarannya. Jika pada suatu larutan penyangga ditambah sedikit asam atau ditambahkan sedikit basa atau diencerkan maka pH larutan tidak berubah. Hal ini menunjukkan bagaimana sifat dari larutan buffer itu sendiri. Pada percobaan ini, akan digunakan larutan penyangga dari HCl dan H3PO4 yang akan dititrasi dengan NaOH (Poedjani, 2010).
Praktikum ini akan digunakan berbagai macam larutan dan berbagai macam konsentrasi. Hal ini bertujuan untuk dapat membandingkan bagaimana tampilan perubahan pH dan juga kapasitas dari buffer fosfat. Dengan menggunakan berbagai macam larutan dan juga berbagai macam konsentrasi, maka akan didapatkan berbagai perbandingan dari masing-masing percobaan.
Oleh karena itu, praktikan harus menyiapkan alat-alat dan bahan praktikum sebelum memulainya, hal ini bertujuan agar praktikum dapat dilaksanakan.
Tujuan Praktikum
Adapun tujuan dari praktikum ini adalah untuk membandingkan tampilan perubahan pH asam kuat dan asam lemah yang dititrasi dengan NaOH.
18
TINJAUAN PUSTAKA
Larutan adalah campuran yang bersifat homogen antara molekul, atom ataupun ion dari dua zat lebih. Disebut campuran karena susunannya atau komposisinya dapat berubah. Disebut homogen karena susunannya begitu seragam sehingga tidak dapat diamati adanya bagian-bagian yang berlainan, bahkan dengan mikroskop optis sekalipun. Fase larutan dapat berwujud gas, cair, ataupun padat. Komponen larutan terdiri dari pelarut dan zat terlarut (Darma, 2014).
Pengenceran yaitu penambahan pelarut yang mengakibatkan jumlah pelarut yang lebih banyak dibandingkan dengan jumlah zat terlarutnya. Untuk membuat larutan dengan konsentrsi tertentu yang berasal dari larutan pekat, maka diambil dengan volume tertentu larutan pekat yang diperlukan. Setelah itu, diencerkan dengan aquades sampai volume yang ditentukan. Ketelitian dalam pengenceran merupakan salah satu factor untuk memperoleh ketetpan konsentrasi yang diinginkan. Oleh karena itu, pengenceran akan lebih baik jika dilakukan dalam labu takar (Tim Dosen Kimia Universitas Hasanuddin, 2010).
Larutan penyangga adalah larutan yang bersifat mempertahankan pHnya. Jika ditambahkan sedikit asam atau sedikit basa atau diencerkan, pHnya akan tetap dipertahankan. Larutan penyangga merupakan campuran asam lemah dan basa konjugasi atau campuran basa lemah dengan asam konjugasinya. Nilai pH larutan buffer tidak berubah setelah penambahan asam, basa maupun air. Larutan buffer mampu menetralkan penambahan asam ataupun basa luar (Utami, 2009).
Larutan buffer dapat dibuat dengan berbagai cara. Larutan buffer asam dapat dibuat dengan cara mencampurkan sejumlah larutan asam lemah dengan larutan basa konjugasinya secara langsung. Selain itu, larutan buffer asam juga dengan mencampurkan sejumlah larutan basa kuat dengan asam lemah berlebih. Setelah reaksi selesai, campuran dari larutan basa konjugasinya yang terbentuk dan sisa larutan asam lemah membentuk larutan buffer asam. Cara yang serup, larutan buffer basa juga dapat dibuat melalui dua cara. Pertama pencampuran sejumlah larutan basa lemah dengan larutan asam kunjugasinya secara langsung. Cara kedua mencampurkan sejumlah larutan asam kuat dengan larutan basa lemah berlebih (Andy, 2009).
Alkalinitas adalah ukuran kapasitas penyangga ,edium kultur dalam daerah pH netral. Dengan demikian, kapasitas medium untuk menerima proton adalah alkalinitasnya. Alkalinitas medium adalah fungsi bikarbonatnya, carbonate, dan bagian hidroksida. Dari ketiga bagian tersebut, bikarbonat adalah yang paling penitng (Djoko Padmono, 2007).
20
PELAKSANAAN PRAKTIKUM
Waktu dan Tempat Praktikum
Praktikum ini dilaksanakan pada hari Rabu 10 November 2015 di laboratorium Kimia dan Biologi Pangan Fakultas Teknologi Pangan dan Agroidustri, Universitas Mataram.
Alat dan Bahan Praktikum a. Alat-alat Praktikum
Adapun alat-alat yang digunakan pada praktikum ini adalah pH stik, pipet ukur, gelas piala, tabung reaksi, alat titrasi, dan ruble bulp.
b. Bahan-bahan Praktikum
Adapun bahan-bahan yang digunakan pada praktikum ini adalah laruatan HCl 0,1 m, H3PO4,0,5 M, dan NaH2PO4 0,2 M, dan aquades.
Prosedur Kerja a. Titrasi Larutan HCl
Disiapkan HCl 0,1 m, aquades, dan NaOH 0,01 M
Diambil 2 ml HCl 0,1 m, masukkan ke dalam gelas piala 18 ml aquades
Diaduk rata
Diukur pH dengan pH stik
Dititrasi dengan NaOH 0,01 N (30 ml)
Diukur pH dengan pH stik dengan selang pengukuran 5 ml
b. Titrasi Larutan H3PO4
Disiapkan larutan H3PO4 0,05 M, NaOH 0,05 N
Diambil 20 ml H3PO4 0,05 M, masukkan ke dalam gelas piala
Diaduk rata
Diukur pH dengan pH stik
Dititrasi dengan NaOH 0,05 N (30 ml)
Diukur pH setiap penambahan 5 ml sambil diaduk
22
HASIL PENGAMATAN
Tabel 2.1 Hasil Pengamatan Perubahan pH larutan HCl 0,1 dengan Penambahan NaOH 0,01 N
Volume NaOH 0,01 N (ml) yang ditambahkan
0 5 10 15 20 25 30
pH Larutan
HCl 1 2 2 3 3 3 3
Tabel 2.2 Hasil Pengamatan Perubahan pH larutan H2PO4 M dengan Penambahan NaOH 0,01 N
Volume NaOH 0,05 N (ml) yang ditambahkan
0 5 10 15 20 25 30
pH Larutan
H3PO4
2 2 2 3 3 3 3
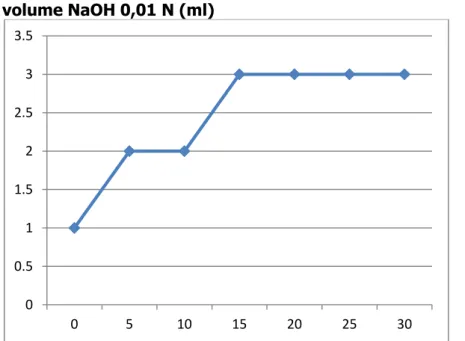
Gambar 1. Kurva Titrasi Hubungan antara Perubahan pH HCl dan volume NaOH 0,01 N (ml) 0 0.5 1 1.5 2 2.5 3 3.5 0 5 10 15 20 25 30
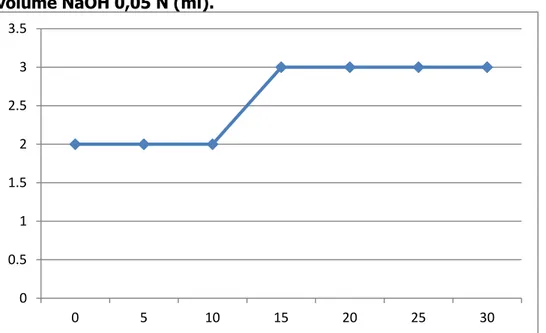
Gambar 2. Kurva titrasi Hubungan antara Perubahan pH H3PO4 dan volume NaOH 0,05 N (ml). 0 0.5 1 1.5 2 2.5 3 3.5 0 5 10 15 20 25 30
24
PEMBAHASAN
Larutan adalah campuran yang bersifat homogen antara molekul, atom ataupun ion dari dua zat atau lebih. Dikatakan campuran karena kompposisinya dapat berubah dan dikatakan homogen karena susunannya begtu seragam sehingga tidak dapat diamati adanya bagian-bagian yang berlainan.Larutan buffer adalah larutan yang bersifat mempertahankan pHnya. Jika ditambahkan sedikit asam atau sedikit basa ataupun diencerkan, pHnya akan tetap dipertahankan (Ani, 2010).
Pada percobaan ini, menggunakan dua campuran yaitu HCl dengan NaOH dan H3PO4 dengan NaOH dengan aquades. Pada percobaan pertama, pH larutan HCl 0,1 m dengan penambahan volume NaOH 0,01 N dengan selang pengukuran 5 ml sampai 30 mldiperoleh pH larutan HCl berturut-turut adalah 1, 2, dan 3. Pada percobaan ini, pH larutan mengalami peningktan sehingga tingkat keasamannya (pH) mengalami pengurangan (karena basa) karena adanya penambahan aquades. Hubungan yang terjadi antara titras perubahan pH dan volume NaOH juga menunjukkan bahwa volume NaOH dengan selang pengukuran 5 ml tingkat keasamannya berkurang.
Pada percobaan kedua, perubahan pH larutan H3PO4 0,05 m dengan penambahan NaOH 0,05 N juga mengalami perubahan. Ketika ditambahkan NaOH dan aquades pada selang pengukuran 0 sampai 30 ml mengalami perubahan pH yang menunjukkan bahwa tingkat keasamannya berbeda.
Dari data percobaan di atas, hasil dari keduanya menunjukkan bahwa perubahan pH larutan buffer dapat berubah, baik dengan penambahan asam
kuat dan basa kuat yang relatif banyak. Dari kedua percobaan juga menunjukkan bahwa larutan HCl dan H3PO4 bersifat asam lemah, karena pHnya kurang dari 7.
26
KESIMPULAN
Berdasarkan hasil pengamatan dan pembahasan, maka dapat ditarik keimpulan sebagai berikut:
1. Larutan adalah campuran yang bersifat homogen antar molekul, atom ataupun ion dari dua zat atau lebih.
2. Larutan penyangga adalah larutan yang bersifat mempertahankan pHnya, jiak ditambahkan sedikit asam, sedikit basa atau diencerkan.
3. Jika ditambahkan dengan asam atau basa dengan volume yang banyak, maka larutan akan cenderung berubah nilai pHnya.
ACARA III
PENGUJIAN KARBOHIDRAT
PENDAHULUAN
Latar Belakang
Karbohidrat sangat akrab dengan kehidupan manusia karena sebagai sumber energy utama manusia. Contoh makanan sehari-hari yang mengandung karbohidrat adalah pada jagung, gandum, tepung, beras, kentang dan sayur-sayuran. Karbohidrat yang berasal dari makanan yang dalam tubuh mengalami perubahan atau metabolisme. Hasil metabolisme karbohidrat merupakan glukosa yang terdapat dalam darah, sedangkan glikogen adalah karbohidrat yang disintesis dalam hati dan digunakan oleh sel-sel pada jaringan otot sebagai sumber energi. Pada umumnya karbohidrat merupakan zat padat berwarna putih yang sukar larut dalam pelarut organik tetapi larut dalam air (Nata, 2009).
Karbohidrat merupakan bahan yang sangat diperlukan tubuh manusia, hewan dan tumbuhan disamping lemak dan protein. Senyawa ini dalam jaringan merupakan cadangan makanan. Karbohidrat yang dihasilkan oleh tumbuhan merupakan cadangan makanan yang disimpan dalam akar,batang dan biji sebagai pati. Karbohidrat dalam tubuh manusia dan hewan dibentuk dari beberapa asam amino dan makanan yang berasal dari tumbuhan (Sirajjudin, 2011).
Kedudukan karbohidrat sangatlah penting pada manusia dan hewan tingkat tinggi lainnya,yaitu sebagai sumber kalori. Karbohidrat juga memiliki fungsi biologi lainnya yang tak kalah penting bagi beberapa makhluk hidup tingkat rendah, ragi misalnya polisakarida terdiri dari rantai panjang yang
28
mempunyai ratusan unit monosakarida. Oleh karena itu, perlu dilakukan praktikum ini untuk mengidentifikasi sifat-sifat umum berbagai jenis karbohidrat berdasarkan terbentuknya furfural, sifat pereduksinya dan mengidentifikasi jenis polisakarida berdasarkan perubahan warna iodine yang terikat pada molekul polisakarida sebelum dan sesudah hidrolisis.
Tujuan Praktikum
Adapun tujuan dari praktikum ini adalah untuk mengidentifikasi sifat-sifat umum berbagai jenis karbohidrat berdasarkan terbentuknya furfural, mengidentifikasi berbagai jenis karbohidrat berdasarkan sifat preduksinya,dan mengidentifikasi jenis polisakarida berdasarkan perubahan warna iodin yang terikat pada molekul polisakarida sebelum dan sesudah terhidrolisis.
TINJAUAN PUSTAKA
Karbohidrat atau sakarida adalah polisakarida aldehid atau polihidroksil keton, atau senyawa hasil hidrolisis keduanya. Penyusu utama karbohidrat adalah C, H, dan O. Perbandingan jumlah atom H dan O adalah 1 : 2 seperti molekul air. Contoh glukosa (12:6), sukrosa (22:11). Karena itu, dahulu penamaan karbohidrat berasal dari sifat y tu g bu g d “k boh d t” d “h d t” H d t d t y K boh d t d p t d golo gk berdasarkan struktur cincin siklisnya yaitu furanosa, karbohidrat dengan cincin siklis segi enam, maupun digolongkan berdasarkan monomer penyusunnya seperti monosakarida, oligosakarida, dan polisakarida (Handito dkk, 2014).
Karbohidrat (CH2O)n adalah sumber energi utama. Kebanyakan karbohidrat yang dikonsumsi adalah tepung/amilum/pati, yng ada dalam gandum, jagung, beras, kentang, dan padi-padian lainnya. Karbohidrat merupakan bahan yang penting dan sumber tenaga yang terdapat dalam tumbuhan dan daging hewan. Selain itu, karbohidrat juga menjdi komponen struktur penting pada makhluk hidup dalam bentuk sert (fiber), seperti selulosa, pektin, serta lignin (Edahwati, 2010).
Glukosa adalah monosakarida dengan rumus kimia C6H12O6 terdapat sebagai glikosida di dalam tubuh binatang, sebagai disakarida-disakarida dan polisakarida-polisakarida di dalam tumbuh-tumbuhan. Glukosa dapat dihasilkan melalui hidrolisis polisakarida atau disakarida, baik dengan asam maupun dengan enzim. Glukosa dapat dibuat dari pati-patian, dan proses pembuatannya dapat dihidrolisa denganasam maupun enzim. Glukosa adalah suatu karbohidrat terpenting yang digunakan sebagai sumber tenaga bagi hewan dan tumbuhan.
30
Analisa kualitatif glukosa dengan uji molisch, uji barfoed, uji benedict, uji seliwanoff, dan uji iodin. Sedangkan uji kuantitatif dengan metode luff schoorl (Mukaromah dan Yusrin, 2010).
Maltosa merupakan gla pereduksi seperti glukosa yang memiliki gugus karbonil yang berpotensi bebas. Sukrosa bukan gula pereduksi, sukrosa tidak mengandung atom karbon anomer bebas, karena karbon anomer kedua unit monosakarida pada sukrosa berikatan satu dengan yang lain. Hal tersebut menyebabkan sukrosa lebih stabil terhadap oksidasi atau hidrolitik enzim-enzim pemecah ikatan glikosida. Karbohidrat sederhana (simple carbohyrate), manosa, atau monosakarida adalah karbohidrat yang molekulnya lebih kecil dari susunannya lebih sederhana dibandingkan dengan molekul karbohidrat yang lain. Nmolekul karbohidrat ini dapat diperkecil lagi dengan cara hidrolisis. Monosakarida adalah suatu persenyawaan yang netral, mudah larut dalam air, kelarutannya dalam alkohol kecil, dan tidak larut dalam dietileter (Sumardjo, 2009).
Pati merupakan simpanan karbohidrat dalam tumbuh-tumbuhan dan merupakan karbohidrat utama yang dimakan manusia di seluruh dunia. Pati terutama terdapat dalam padi-padian, biji-biian, dan umbi-umbian. Jumlah unit glukosa dan susunannya dalam satu jenis pati berbeda satu sama lain bergantung pada jenis tanaman asalnya. Rantai glukosa terikat satu sama lain melalui ikatan alfa yang dapat dipecah dalam proses pencernaan (Almatsier, 2010).
Karbohidrat sendiri terbagi atas dua macam kelompok berdasarkan susunan molekulnya yaitu karbohidrat sederhana dan karbohidrat kompleks.
Karbohidrat sederhana adalah karbohidrat yang tersusun dari 1 (monosakarida) hingga 2 (disakarida) molekul, jenis daro karbohidrat sederhana adalah gula pasir, sirup, dan madu. Sedangkan karbohidrat kompleks adalah karbohidrat yang terbentuk oleh hampir 20.000 unit molekul monosakarida, jenis dari karbohidrat kompleks adalah sumber bahan pokok seperti padi, umbi-umbian, jagung, dan gandum (Anwari, 2007) dalam (Farizi, 2013).
32
PELAKSANAAN PRAKTIKUM
Waktu dan Tempat Praktikum
Praktikum ini dilaksanakan pada hari Rabu, 18 November 2015 di Laboratorium Kimia dan Biokimia Pangan Fakultas Teknologi Pangan dan Agroindustri Universitas Mataram.
Alat dan Bahan Praktikum a. Alat-alat Praktikum
Adapun alat-alat yang digunakan pada praktikum ini adalah tabung reaksi, pipet ukur, penangas air, gelas ukur, rak tabung reaksi, pipet tetes, stopwatch, penjepit kayu, dan tisu.
b. Bahan-bahan Praktikum
Adapun bahan-bahan yang digunakan pada praktikum ini adalah maltose, larutan HCl, larutan H2SO4, larutan ribose 1%, larutan glukosa 1%, larutan fruktosa 1%, larutan laktosa 1%, larutan sukrosa 1%, larutan glikogen 1%, larutan pati 1%, larutan selulosa 1%.
Prosedur Kerja 1. Uji molish
Dimasukkan 2-3 tetes preaksi molisch ke dalam ke 5 tabung. Disiapkan bahan masing-masing 1ml.
Disiapkan 5 buah tabung reaksi dan diberi label.
Diamati cincin ungu yang terjadi.
2. Uji benedict 3. Uji seliwanoff 4. Uji iodin Disiapkan bahan masing-masing 1ml.
Dimasukkan 2-3 tetes benedict
Diamati perubahan warna Digojog
Dipanaskan selama 5 menit
Dimasukkan ke dalam 5 tabung reaksi. Disiapkan masing-masing bahan.
Diamati setiap 1 menit perubahan warna Ditambahkan 1ml pereaksi seliwanoff
Dipanaskan selama 5 menit
Dipanaskan selama 5 menit Disiapkan masing-masing bahan.
Dimasukkan ke dalam 5 tabung reaksi,ditambahkan 3 tetes iodine dan digojog.
Diamati dan dicatat perubahan warna
Ditambahkan 1 ml larutan HCl
34
HASIL PENGAMATAN
Tabel 3.1 hasil uji kualitatif berbagai jenis karbohidrat berdasarkan terbentuknya furfural (uji molish).
Jenis Karbohidrat Terjadinya pembentukan cairan ungu
Glukosa 1% -
Pati 1% -
Sukrosa 1% -
Fruktosa 1% -
Maltose 1% -
Tabel 3.2 hasil pengamatan (uji seliwanoff)
Jenis karbohidrat Sebelum dipanaskan Setelah dipanaskan Glukosa 1% Bening kekuningan Bening kekuningan Pati 1% Bening kekuningan Bening kekuningan Sukrosa 1% Bening kekuningan Bening kekuningan Fruktosa 1% Bening kekuningan Bening kekuningan Maltose 1% Bening kekuningan Bening kekuningan
Tabel 3.3 hasil pengamatan (uji benedict)
Jenis karbohidrat Perubahan warna
Sebelum dipanaskan Sesudah dipanaskan
Glukosa 1% Biru bening Merah bata
Pati 1% Biru bening Biru pekat
Sukrosa 1% Biru bening Biru bening
Fruktosa 1% Biru bening Merah bata
Maltose 1% Biru bening Merah bata
Tabel 3.4 hasil pengamatan (uji iodine) Larutan Warna setelah
ditetesi iodin
Warna setelah ditambah HCl + dipanaskan
Glukosa 1% Kuning Bening kekuningan
Pati 1% Ungu pekat Ungu
Sukrosa 1% Kuning Bening
Fruktosa 1% Kuning bening Bening kekuningan
PEMBAHASAN
Karbohidrat atau sakarida adalah polisakarida aldehid atau polisakarido keton atau senyawa hasil hidrolisis dari keduanya. Penyusun utama karbohidrat adalah C, H dan O. karbohidrat merupakan sumber energi utama yang diperlukan oleh tubuh. Ada dua jenis karbohidrat yaitu karbohidrat sederhana dan karbohidrat kompleks. Karbohidrat sederhana merupakan aneka jenis gula yang langsung membentuk kalori jika dikonsumsi. Karbohidrat kompleks merupakan sumber kalori yang mengandung vitamin, mineral dan serat yang bermanfaat bagi tubuh (Soenardi, 2008).
Uji Molisch adalah uji yang memiliki prinsip hidrolisis karbohidrat menjadi monosakarida, selanjutnya monosakarida jenis pentosa akan mengalami dehidrasi dengan asam tersebut menjadi furfural, sementara golongan heksosa menjadi hidroksi multifultural menggunakan asam organik pekat (Sumardjo, 2006). Percobaan menunjukkan hasil bahwa larutan yang diuji pada glukosa, fruktosa, sukrosa, dan pati,maltosa negative tidak mengandung karbohidrat karena tidak terbentuk cincin ungu,tidak terjadinya perubahan tersebut disebabkan karena kesalahan saat pencampuran bahan sehingga tidak dapat disimpulkan bahwa uji molisch merupakan karbohidrat.
Uji Seliwanoff adalah uji yang spesifik dalam mengidentifikasi gula ketosaheksosa seperti fruktosa. Dalam pengujian ini golongan aldosa tidak bereaksi, sedangkan ketosa mengalami proses dehidrasi untuk memberikan derifat furfuralnya yang kemudian akan mengalami kondensasi dengan dan membentuk senyawa kompleks yang berwarna merah (Sumardjo, 2006). Percobaan menunjukan hasil bahwa larutan yang diuji pada larutan glukosa
36
1%,pati 1%,sukrosa 1%,fruktosa 1% dan maltosa 1%. Jika dipanaskan karbohidrat yang mengandung gugus keton akan menghasilkan warna larutan yang spesifik yakni warna merah bata,namun pada hasil pengamatan menunjukan bahwa sukrosa berwarna kemerahan sedangkan glukosa,pati,fruktosa,dan maltose berwarna bening kekuningan. Warna merah pada sukrosa disebabkan oleh sukrosa yang terhidrolisis menjadi glukosa dan fruktosa.Hal ini sesuai dengan teori yang menyatakan bahwa ketosa dapat didehidrasi lebih cepat daripada aldosa sehingga diperoleh turunan furfural yang selanjutnya berkondensasi dengan resorsinol membentuk kompleks merah.
Uji Benedict berdasarkan pada gula yang mengandung gugus aldehida atau keton bebas akan mereduksi ion Cu2+ dalam suasana alkalis, menjadi Cu+, yang mengendap sebagai Cu2O (kupro oksida) berwarna merah bata. Gula pereduksi merupakan gula yang memiliki gugus alkalis atau keton bebas atau terdapat gugus –OH glikosidis pada strukturnya (Sumardjo, 2006). Percobaan menunjukkan hasil bahwa larutan glukosa,fruktosa dan maltosa menghasilkan warna larutan yang spesifik yakni warna merah bata setelah dipanaskan. Hal ini menunjukkan bahwa larutan glukosa,fruktosa dan maltosa mengalami oksidasi dan mampu mereduksi senyawa yaitu melepaskan O2 sehingga terbentuk tembaga oksida (Cu2O). sukrosa dan pati negatif dengan pereaksi benedict.
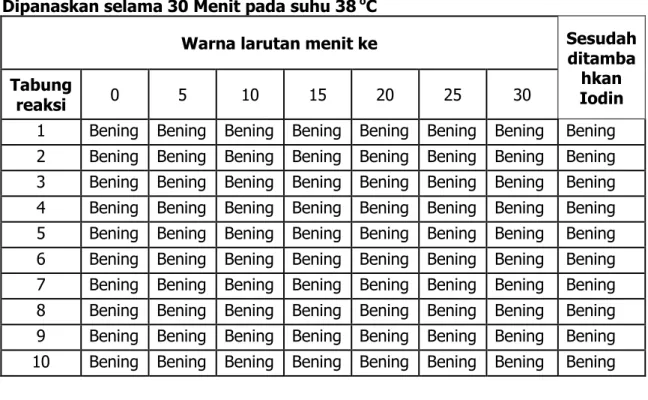
Uji yang terakhir yaitu uji Iodin. Uji Iodin bertujuan untuk mengetahui kandungan polisakarida. Berfungsi untuk mendeteksi kandungan amilosa atau amilum yang ditandai dengan warna biru atau ungu pekat. Hasil pengamatan percobaan menunjukan bahwa pati 1% berwarna ungu pekat. Sedangkan glukosa,sukrosa,fruktosa,dan maltose berwarna kuning. Hal ini sesuai dengan
pendapat yang menyatakan bentuk rantai heliks ini menyebabkan pati dapat membentuk kompleks dengan molekul iodine yang dapat masuk ke dalam spiralnya sehingga menyebabkan warna biru tua pada kompleks tersebut.
38
KESIMPULAN
Berdasarkan hasil pengamatan dan pembahasan, maka dapat disimpulkan sebagai berikut :
1. Karbohidrat merupakan senyawa polihidroksi aldehid dan keton atau senyawa hasil dari keduanya.
2. Pada saat percobaan uji molish tidak terbentuk apa-apa,ini disebabkan karena terjadi kesalahan saat pencampuran bahan.
3. Uji seliwanoff menunjukan hasil yang sama pada semua bahan sebelum dan sesudah dipanaskan.
4. Karbohidrat memiliki gugus keton dapat dibuktikan pada uji seliwanoff yang terbentuknya warna merah orange dilarutan fruktosa 1%.
5. Adanya polisakarida dapat dibuktikan dengan terbentuknya warna biru pada larutan pati 1%.
ACARA IV PENGUJIAN PROTEIN
PENDAHULUAN
Latar Belakang
Hampir setiap fungsi dinamik dalam makhluk hidup bergantung pada protein. Faktanya nilai penting protein digaris bawahi oleh namanya, yang b l d k t Yu P ot ou y g b t ‘t p t p t ’ P ot menyusun lebih dari 50 % massa kering sebagian besar sel, dan protein teramat penting bagi hampir semua hal yang dilakukan organisme. Beberapa protein mempercepat reaksi kimia, sedangkan yang lain berperan dalam penyokongan structural,penyimpanan, transport, komunikasi selular, pergerakan, serta pertahanan melawan zat asing (Raymond, 2010).
Protein memegang peranan yang penting pula dalam kehidupan. Proses kimia dalam tubuh dapat berlangsung dengan baik karena adanya enzim, suatu protein yang berfungsi sebagai biokatalisator. Protein dapat diperoleh dari bahan makanan yang mengandung protein. Contohnya bahan makanan yang mengandung protein adalah pada hewan, terkandung protein hewani, sedangkan pada tumbuhan terkandung protein nabati. Sehingga, protein merupakan salah satu unsur terpenting penyusun makhluk hidup (Rue, 2013).
Protein dalam makanan yang dikonsumsi akan dipecah menjadi asam – asam amino dalam proses pencernaan. Pecahan bahan makanan menjadi asam amino dibantu oleh enzim seperti pepsin dan tripsin. Asam- asam amino yang dihasilkan kemudian diserap oleh usus dan dibawa kearah hati dan didistribusikan ke jaringan-jaringan yang dibutukan. Selain untuk pembentukan
40
sel-sel tubuh protein dapat pula digunakan sebagai bahan bakar apabila keperluan energi tubuh tidak terpenuhi oleh karbohidrat dan lemak. Oleh karena itu, praktikum ini dilaksanakan untuk mengidentifikasikan adanya gugus - asam amino bebas suatu bahan, adanya ikatan peptida suatu larutan, mengidentifikasi gugus R asam amino yang mengandung sulfur, dan mengidentifikasi titik isoelektrik kasein (Sudirman, 2011).
Tujuan Praktikum
Adapun tujuan dari praktikum ini adalah untuk mengidentifikasi adanya gugus - asam amino bebas suatu bahan, adanya ikatan peptida suatu larutan, dan mengidentifikasi gugus R asam amino yang mengandung sulfur, dan mengidentifikasi titik isoelektrik kasein.
TINJAUAN PUSTAKA
Protein berasal dari b h Yu ku o p ot o t y “y g ut ” Dari asal kata ini dapat diambil keputusan bagaimana pentingnya protein dalam kehidupan. Protein terdapat pada semua sel hidup, kira-kira 50 % dari berat keringnya dan berfungsi sebagai pembangun struktur, biokatalis, hormon, sumber energi, penyangga racun, pengatur pH dan bahkan sebagai pembawa sifat keturunan dari generasi-generasi. Protein tersusun dari atom C, H, dan O serta unsur lainnya seperti P dan S yang membentuk unit-unit asam amino (Anwar, 2012).
Peran dan aktivitas protein dalam proses biologis antara lain sebagai enzimatik, bahwa hampir semua reaksi kimia dalam sistem biologi dikatalis oleh makromolekul yang disebut enzim yang merupakan satu jenis protein. Sebagian reaksi seperti hidraksi karbondioksida bersifat sederhana, sedangkan reaksi lainnya seperti reflikasi kromosom sangat rumit. Enzim mempunyai daya katalik yang besar, umumnya meningkatkan kecepatan reaksi sampai jutaan kali ( Katili, 2009).
Asam amino adalah monomer protein yang memiliki dua fungsi yaitu gugus amino dan gugus hidroksil. Jumlah asam amino yang terdapat di alam ada beratus-ratus jumlahnya, namun yang diketahui ikut membangun protein hanya sekitar 20 macam. Sifat asam amino memilki titik leleh diatas 200 ᵒC, larut dalam senyawa polar dan tidak larut dalam senyawa non polar serta memilki momen dipole yang besar. Dicirikan senyawa protein sebagai berikut : berat molekulnya besar, terdiri dari 20 asam amino, terdapat ikatan kimia lain,umumnya reaktif dan sangat spesifik (Aisya, 2011).
42
Struktur asam amino secara umum adalah satu atom c yang mengikat empat gugus : gugus amina (NH2), gugus karboksil (COOH), atom hidroygen (H), dan satu gugus sisa (R, dari residu) atau disebut juga gugus atau rantai samping yang membedakan satu asam amino lainnya. Atom C pusat tersebut dinamai atom C (C- alfa) sesuai dengan penamaan senyawa bergugus karboksil, yaitu atom C yang berikatan langsung dengan gugus karboksil. Oleh karena itu gugus amina juga terikat pada atom C (C-alfa) sesuai dengan penamaan senyawa bergugus karboksil, yaitu atom c ini, senyawa tersebut merupakan asam - amino. Asam amino biasanya diklasifikasikan berdasarkan sifat kimia rantai samping tersebut menjadi empat kelompok. Rantai samping dapat membuat asam amino bersifat asam lemah, basa lemah, hidrofilik jika polar, dan hidrofilik jika non-polar (Khairil, 2010).
Denaturasi suatu protein adalah hilangnya sifat-sifat struktur lebih tinggi oleh terkacaunya ikatan hydrogen dan gaya-gaya sekunder lain yang mengutuhkan moleku itu. Akibat suatu denaturasi adalah hilangnya banyak sifat biologis protein itu. Salah satu faktor yang menyebabkan denaturasi suatu protein ialah perubahan temperature. Memasak putih telur merupakan contoh denaturasi yang tak irreversible. Suatu putih telur adalah cairan tak berwarna yang mengandung albumin, yakni protein globular yang larut. Pemanasan putih telur akan mengakibatkan albumin itu membuka lipatan dan mengendap dihasilkan suatu zat padat putih (Pine, 2013).
PELAKSANAAN PRAKTIKUM
Waktu dan Tempat Praktikum
Praktikum ini dilaksanakan pada hari Rabu, 25 November 2015 di Laboratorium kimia dan Biokimia Pangan, Fakultas Teknologi Pangan dan Agroindustri Universitas Mataram.
Alat dan Bahan Praktikum a. Alat-alat Praktikum
Alat-alat yang digunakan pada praktikum ini adalah tabung reaksi, rak tabung reaksi, penjepit kayu, penangas air, pipet ukur, ruber bulb, gelas ukur, karet gelang, gelas beaker, tisu, dan stopwatch.
b. Bahan- bahan Praktikum
Bahan-bahan yang digunakan pada praktikum ini adalah albumin, glisin, aquades, CuSO4, NaOH 10%, Na Asetat, Pb Asetat.
Prosedur Kerja a. Uji Nidhidrin
Disiapkan 3 tabung reaksi
Ditambahkan 1 ml sampel (aquades, albumin, glisin)
Dipanaskan dengan penangas air selama 5 menit (100 ᵒC) Diamati perubahan warna
44
b. Uji Biuret
Disiapkan 3 tabung reaksi
Ditambahkan 1 ml sampel pada masing tabung
Ditambahkan 1 ml CuSO4 0,5%
Ditambahkan 1 mL NaOH 10%
Dipanaskan selama 5 menit (100 ᵒC)
Diamati perubahan warnanya
Ditambahkan 2 mL larutan Na Asetat
c. Uji Sulfur
Disiapkan 2 tabung reaksi
Ditambahkan 0,5 ml glisin dan albumin
Ditambahkan 1 tetes NaOH 10%
Ditambahkan 2 tetes Pb Asetat
Dipanaskan selama 5 menit (100 ᵒC)
Diamati perubahan warnanya
Ditambahkan 2,5 mL aquades
d. Uji Isoelektrik Protein
Disiapkan 6 tabung reaksi
Ditambahkan 1 ml susu segar dan 1 ml Na asetat 0,1 M
Ditambahkan 1, 3,5, 3,75 ml aquades pada tabung 4,5 dan 6
Ditambahkan 5,2,5, 1,25 ml As. Asetat pada tabung 4, 5 dan 6
Dikocok keenam tabung
Diamati perubahan warna yang terjadi
46
HASIL PENGAMATAN
Tabel 4.1 Hasil Pengamatan Uji Ninhidrin
No Larutan Jenis Hasil Uji Perubahan warna
Sebelum dipanaskan Sesudah dipanaskan
1 Aquades Kuning bening Kuning bening
2 Glisin 1 % Kuning bening Kuning keruh
3 Albumin Kuning bening Ungu pekat
Tabel 4.2 Hasil Uji Kualitatif Peptide dengan Uji Biuret No Jenis Larutan Hasil Uji Perubahan warna
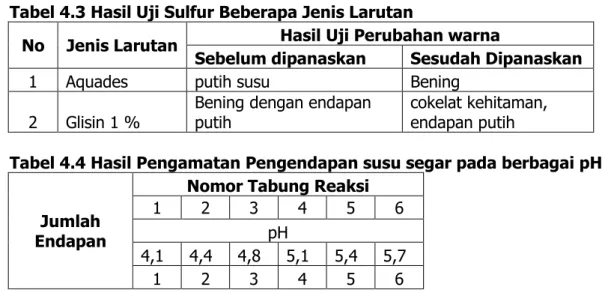
Sebelum dipanaskan Sesudah Dipanaskan 1 Aquades Bening kebiruan bening, endapan hitam 2 Glisin 1 % Biru Keruh bening, endapan biru muda 3 Albumin Ungu,endapan bening kekuningan cokelat bening, endapan putih Tabel 4.3 Hasil Uji Sulfur Beberapa Jenis Larutan
No Jenis Larutan Hasil Uji Perubahan warna
Sebelum dipanaskan Sesudah Dipanaskan
1 Aquades putih susu Bening
2 Glisin 1 % Bening dengan endapan putih cokelat kehitaman, endapan putih
Tabel 4.4 Hasil Pengamatan Pengendapan susu segar pada berbagai pH
Jumlah Endapan
Nomor Tabung Reaksi
1 2 3 4 5 6
pH
4,1 4,4 4,8 5,1 5,4 5,7
PEMBAHASAN
Protein merupakan polimer dari monomer-monomer asam amino yang dihubungkan satu sama lain dengan ikatan peptide. Molekul protein mengandung karbon, hydrogen, oksigen, nitrogen dan kadang kala sulfur serta fosfor. Protein berperan penting dalam struktur dan fungsi semua sel makhluk hidup dan virus. Kebanyakan protein merupakan enzim atau subunit enzim. Jenis protein lain berperan dalam fungsi structural atau mekanis, seperti misalnya protein membentuk batang dan sendi sitoskeleton. Protein terlibat dalam sistem kekebalan (imun) sebagai antibody (Zaini, 2010).
Pada praktikum ini, dilakukan beberapa pengujian pada protein yaitu, uji ninhidrin, uji biuret, uji sulfur, dan uji pengendapan susu segar. Pada pengamatan uji ninhidrin, dapat diketahui uji ninhidrin adalah uji umum protein dan asam amino. Ninhidrin dapat mengubah asam amino menjadi suatu aldehida menurut novita (2010). Ninhidrin bereaksi dengan asam amino bebas dan protein menghasilkan warna biru. Reaksi yang paling umum digunakan untuk analisis kualitatif protein dan produk hasil hidropilisnya. Reaksi ninhidrin dapat pula dilakukan terhadap urin untuk mengetahui adanya asam amino atau mengetahui pelepasan protein pada cairan tubuh menurut Santoso (2012). Pada praktikum diperoleh hasil dari tiga sampel (aquades, glisin 1%, dan albumin) yaitu pada albumin mengalami perubahan warna yang spesifik sesudah dipanaskan, warna yang diperoleh adalah ungu pekat yang menandakan bahwa albumin merupakan protein. Pada sampel aquades dan glisin berwarna keruh dan bening tidak menunjukkan adanya protein.
48
Pada praktikum uji biuret, dapat diketahui pengujian biuret bertujuan untuk mengetahui ada tidaknya rantai peptide pada ketiga sampel (aquades, glisin 1 % dan albumin). Pada pengamatan hanya albumin yang mengalami perubahan menjadi ungu sebelum dipanaskan dengan penambahan NaOH menunjukkan bahwa adanya protein pada albumin. Setelah dipanaskan, NaOH yang bersifat basa molekulnya akan terhidrolisis menjadi molekul asam amino. Pada sampel lainnya (aquades dan glisin 1% menunjukkan perubahan warna biru keruh, bening kebiruan (sebelum dipanaskan) dan perubahan warna dan ada endapan menjadi bening dan ada endapan hitam serta biru muda, menunjukkan adanya protein tetapi sedikit.
Pada praktikum uji sulfur pada sampel (Glisin dan Albumin) pada jenis larutan glisin 1 %dan albumin sebelum dipanaskan menunjjukkan adanya kaandungan sulfur. Pada kedua larutan, hanya larutan sampel albumin yang menunjukkan adanya kandungan sulfur. Pada kedua larutan , hanya larutan sampel albumin yang mengandung sulfur dimana ditujukan warna gelap sesuai dengan literatur menurut Hakim (2010).
Pada pengujian pengendapan susu segar pada berbagai pH dengan nomor tabung 1,4 pH 4,1 dan 5,1 tidak terdapat endapan, pada pH 4,4 dan 5,4 dengan nomer tabung 3 dan 6 dengan pH 4,8 dan 5,7 memiliki endapan paling banyak dari keenam tabung reaksi. Jadi berdasarkan data tersebut titik isoelektriknya pada pH 4,8 dan 5,7 karena pada pH tersebut endapan yang dihasilkan banyak.
KESIMPULAN
Kesimpulan yang dapat diperoleh berdasarkan hasil pengamatan dan pembahasan antara lain:
1. Protein merupakan polimer dari monomer-monomer asam amino yang dihubungkan satu sama lain dengan ikatan peptide.
2. Pengujian yang dilakukan pada praktikum ini antara lain pengujian sulfur, biuret, ninhidrin, dan pengendapan susu segar dengan perubahan pH.
3. Pengujian ninhidrin menunjukkan albumin mengandung protein.
4. Pengujian biuret, albumin menunjukkan adanya kandungan protein dengan berwarna ungu.
5. Pada pengujian sulfur, albumin mengandung sulfur dengan perubahan warna cokelat (warna gelap)
6. Pada pengujian pengendapan susu segar dengan perubahan pH diperoleh endapan yang paling banyak pada pH 4,8 dan 5,7.
50
ACARA V PENGUJIAN LEMAK
PENDAHULUAN
Latar Belakang
Lemak dan minyak sering di temui dalam kehidupan sehari-hari, yaitu sebagai mentega. Lemak berasal dari hewan dan tumbuhan. Contohnya minyak jagung, minyak zaitun, minyak kacang dan lain-lain. Walaupun lemak berbentuk padat dan minyak berbentuk cairan. Keduanya mempunyai struktur dasar yang sama. Perannya dalam kehidupan sehari-hari yang cukup banyak adalah mengetahui lemak dan minyak ini lebih mendalam karena ini dianggap penting dalam bahan pangan (Saad, 2010).
Lipid merupakan senyawa organik berminyak atau berlemak yang tidak larut dalam air, dapat diekstrak dari sel dan jaringan oleh pelarut nonpolar, seperti kloroform, benzena atau eter. Asam lemak adalah komponen unit pembangun kloroform, benzene atau eter. Asam lemak adalah asam organik berantai panjang yang mempunyai atom karbon dari 4 sampai 24. Asam lemak memiliki gugus karboksil tunggal dan ekor hidrokarbon nonpolar yang panjang. Hal ini membuat kebanyakan lipid bersifat tidak larut dalam air dan tampak berminyak atau berlemak. Berbagai kelas lipid dihubungkan satu sama lain berdasarkan komponen dasarnya, sumber penghasilnya, kandungan asam lemaknya, maupun sifat-sifat kimianya (Poedjadi, 2009).
Lemak dibagi menjadi tiga yaitu lemak sederhana, lemak majemuk, dan turunan lemak. Lemak sederhana yaitu apabila dihidrolisis akan menghasilkan alkohol. Lemak majemuk mengandung listrik. Turunan lemak yaitu
berbagai senyawa yang diperoleh dari hidrolisis (Yuni, 2010). Oleh karena itu dilakukan praktikum ini untuk mengetahui pengaruh jenis pelarut terhadap sifat kelarutan lemak, mengetahui tingkat ketidakjenuhan berbagai jenis lemak dan sifat penyabunan dua jenis garam asam lemak.
Tujuan Praktikum
Tujuan dari praktikum ini untuk mengetahui pengaruh jenis pelarut terhadap sifat kelarutan lemak, mengetahui tingkat ketidakjenuhan lemak, dan mengetahui sifat penyabunan dua jenis garam asam lemak.
52
TINJAUAN PUSTAKA
Lipid adalah senyawa biomolekul yang tidak larut dalam air, sehingga terikat pada plasma sebagai mekanisme transport dalam serum. Lipid dapat diekstraksi dengan pelarut organik seperti eter, benzene dan kloroform dan tetraklormetana. Lipid penting karena memilki nilai energi yang tinggi, bahan isolasi dan pelindung yang terdapat pada jaringan-jaringan dibawah kulit dan mengelilingi organ-organ tertentu misalnya jaringan syaraf (Riawan, 2009).
Lemak digolongkan berdasarkan kejenuhan ikatan pada asam lemaknya. Adapun penggolongannya adalah asam lemah jenuh dan asam lemak tak jenuh. Lemak yang mengandung asam lemak jenuh yaitu asam lemak yang tidak memiliki ikatan rangkap. Dalam lemak hewani misalnya lemak sapi, kandungan asam lemak jenuh lebih dominan. Asam lemak tak jenuh adalah asam lemak yang mempunyai ikatan rangkap. Jenis asam lemak ini dapat didefinisikan dengan reaksi adisi, dimana ikatan rangkap terputus sehingga terbentuk asam lemak jenuh (Nazar, 2012).
Lipid dibagi atas 3 golongan yaitu: Lipid sederhana yang terdiri atas ester dari asam-asam lemak gliserol. Ada 3 jenis lemak sederhana yaitu, lemak yang strukturalnnya pada dalam suhu kamar, minyak yang strukturnya cair dalam suhu kamar dan lilin atau malam yang merupakan ester asam lemak dengan alkohol. Lipid campuran fosfolifid ester yang mengandung asam lemak dan yang mengandung gugus lain yang terikat pada alkohol misalnya fosfolipida dan glikopida. Derivat lipid adalah zat yang berasal dari hasil hidrolisis zat-zat tersebut antara lain lemak jenuh dan tidak jenuh, alkohol, gliserol, sterol, dan lemak aldehid (Taufik, 2010).
Salah satu komponen utama makanan yang memberikan dampak positif dan negative terhadap kesehatan adalah lemak yang mempunyai multifungsi, yaitu sebagai penyumbang energy terbanyak (30% atau lebih dari energy total yang diperlukan tubuh) serta merupakan sumber asam lemak esensial linoleat dan linolenat. Selain sebagai pelarut vitamin A, D, E, dan K, lemak memberikan cita rasa dan aroma spesifik pada makanan yang tidak dapat digantikan oleh komponen makanan lainnya (Sartika, 2008).
Asam lemak adalah bagian penting dari seluruh jaringan tubuh dan merupakan bagian utama senyawa fodpolipid membran sel. Dalam tubuh, asam lemak tidak hanya diperkukan untuk sintesa membran, modifikasi protein dan kabohidrat, pembangunan beberapa elemen struktur dalam sel dan jaringan, menghasilkan senyawa penanda dan bahan bakar, tetapi juga untuk melarutkan berbagai macam bagian seluler serta ekstraseluler yang sulit larut dan nonpolar (Tuminah, 2010).
54
PELAKSANAAN PRAKTIKUM
Waktu dan Tempat Praktikum
Praktikum ini dilaksanakan pada hari Rabu, 2 Desember 2015 di Laboratorium Kimia dan Biokimia Pangan, Fakultas Teknologi Pangan dan Agroindustri, Universitas Mataram.
Alat dan Bahan Praktikum a. Alat-alat Praktikum
Alat-alat yang digunakan pada praktikum ini adalah tabung reaksi, pipet ukur, pengaduk gelas, ruber bulb, gelas piala, pipet tetes, dan rak tabung reaksi.
b. Bahan-bahan Praktikum
Bahan-bahan yang digunakan pada praktikum ini adalah minyak nabati, minyak hewani, kloroform, benzene, etanol, NaOH 0,05 M, HCl 0,05 M, aquades, larutan sabun, larutan deterjen, CaCl2 0,5%, MgCl2 0,5%, larutan FeCl3 0,5%, dan larutan wijs.
Prosedur Kerja
b. Uji Tingkat Ketidak jenuhan Lemak
c. Uji Sifat Penyabunan lemak
Disiapkan 5 buah tabung reaksi
Ditambah 2 ml pelarut kloroform pada tabung 1, benzene pada tabung 2, etanol pda tabung 3, NaOH 0,05 M pada tabung 4, dan HCl 0,05 pada
tabung 5
Ditambah 2 ml minyak curah
Digojog
Diamati kelarutan yang terbentuk
Diulangi untuk minyak komersial dan hewani
Disiapkan 4 buah tabung reaksi
Ditambah 1 ml campuran kloroform dan etanol
ditambah 0,5 ml aquades pada tabung 1, minyak hewani pada tabung 2, minyak nabati (komersial) pada tabung 3, dan minyak nabati (curah)
pada tabung 4
56
Disiapkan 8 buah gelas piala
Ditambahkan 25 ml larutan sabun 1 % pada tabung 1 sampai 4 dan 25 ml larutan deterjen 1 % pada tabung 5 sampai 8
Ditambah 5 ml larutan CaCl2 0,5 % pada tabung 1 dan 5 Ditambah 5 ml larutan MgCl2 0,5 % pada tabung 2 dan 6
Ditambah 5 ml larutan FeCl2 0,5 % pada tabung 3 dan 7 Ditambah 10 tetes minyak nabati (komersial) pada tabung 4 dan 8
Diaduk rata
HASIL PENGAMATAN
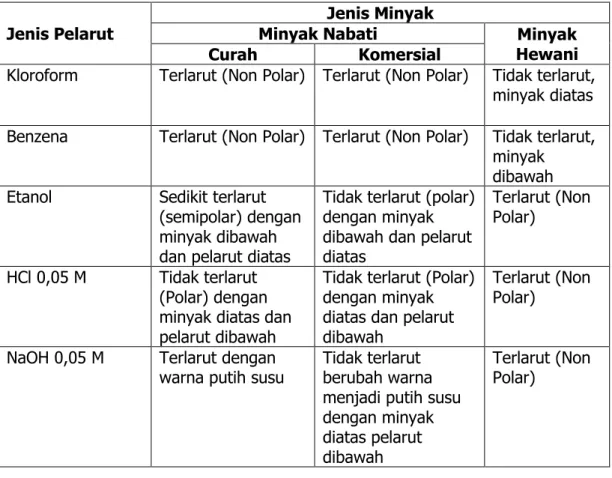
Tabel 5.1 Hasil pengamatan pengaruh jenis pelarut terhadap kelarutan lemak
Jenis Pelarut
Jenis Minyak
Minyak Nabati Minyak
Hewani
Curah Komersial
Kloroform Terlarut (Non Polar) Terlarut (Non Polar) Tidak terlarut, minyak diatas Benzena Terlarut (Non Polar) Terlarut (Non Polar) Tidak terlarut,
minyak dibawah Etanol Sedikit terlarut
(semipolar) dengan minyak dibawah dan pelarut diatas
Tidak terlarut (polar) dengan minyak dibawah dan pelarut diatas
Terlarut (Non Polar)
HCl 0,05 M Tidak terlarut (Polar) dengan minyak diatas dan pelarut dibawah
Tidak terlarut (Polar) dengan minyak diatas dan pelarut dibawah
Terlarut (Non Polar)
NaOH 0,05 M Terlarut dengan
warna putih susu Tidak terlarut berubah warna menjadi putih susu dengan minyak diatas pelarut dibawah
Terlarut (Non Polar)
Tabel 5.2 Hasil pengamatan uji ketidakjenuhan dua jenis minyak Sampel Jumlah tetesan Iodin
Minyak Hewani 60 tetes
Minyak Nabati 24 tetes
Aquades (Kontrol) 41 tetes Minyak nabati curah 57 tetes
Tabel 5.3 Hasil pengamatan sifat penyabunan dari dau jenis garam asam lemak
Larutan Uji Sabun Deterjen
CaCl2 0,5 % +++ +++
MgCl2 0,5 % + ++
FeCl2 0,5 % + ++
58
PEMBAHASAN
Lemak adalah salah satu kelompok yang termasuk pada golongan lipid, yaitu senyawa organik yang terdapat dialam serta tidak larut dalam air, tetapi larut dalam pelarut organik nonpolar, misalnya dietil eter (C2H5OC2H5), kloroform (CHCl3), benzene dan hidrokarbon lainnya. Lemak sederhana merupakan eter dari asam lemak. Hidrolisis dari suatu lemak akan dihasilkan suatu molekul gliserol dan tiga molekul asam lemak. Lemak dan minyak keduanya adalah lemak sederhana, perbedaannya terletak pada banyaknya ikatan rangkap (ketidakjenuhan). Lemak air dalam tempratur kamar disebut minyak (oil), sedangkan yang berbentuk padat disebut lemak (fat) (Andriyanto, 2013).
Pada praktikum ini pengujian lemak dilakukan 3 percobaab yaitu, percobaan sifat kelarutan lemak, uji tingkat ketidakjenuhan lemak, dan sifat penyabunan lemak. Pada percobaan pertama yaitu percobaab sifat kelarutan lemak dengan digunakan pelarut kloroform, benzene, etanolm NaOH 0,05 M, dan HCl 0,05 M. Jenis minyak nabati pada curah, jenis pelarut yaitu kloroform, benzene, etanol, NaOH 0,05 M. Pelarut tersebut termasuk kedalam non polar. Sedangkan etanol termasuk kedalam golongan semipolar yang artinya sedikit terlarut dengan minyak dibawah dan pelarut diatas. Hal inin terjadi karena massa jenis minyak lebih besar dari pelarut. Dan pada HCl 0,05 M tergolong dalam polar yang artinya tidak larut tiak terlarut dengan minyak diatas dan pelarut dibawah. Hal ini terjadi karena massa jenis minyak lebih kecil dari pelarut. Pada minyak nabati komersial kloroform dan benzene terjadi penyatuan atau terlarut, sedangkan pada etanol, HCl 0,05 M, dan NaOH 0,05b M tidak terjadi penyatuan atau tidak terlarut. Penyatuan terjadi karena kloroform dan benzene merupakan
larutan nono polar sehingga adanya momen dipol pada zat terlarut maupun pelarutnya sehingga mampu berikatan dan berinteraksi dengan sesamanya. Ketidaklarutan pada etanoll, HCl 0,05 M, dan NaOH 0,05 M disebabkan karena larutan tersebut merupakan larutan polar sedangkan minyak tidak larut dalam polar sehingga sukar terjadi penyatuan antara larutan dengan minyak. Pada NaOH terjadi penambahan warna menjadi putih susu dengan minyak diatas pelarut dibawah. Pada minyak hewani etanol, HCl 0,05 M, dan NaOH 0,05 M terjadi penyatuan dan termasuk non polar (terlarut). Sedangkan pada kloroform dan benzeba tidak larut (polar) pada kloroform minyak diatas karena massa jenis minyak lebih kecil dari pelarut. pada benzene dengan minyak dibawah disebabkan karena massa jenis minyak lebih besar dari pelarut. Pada kloroform dan benzene menurut literature terjadi penyatuan atau terlarut. Hal inin terjadi karena kesalahan atau kekeliruan pada praktikum sehingga kloroform dan benzene tidak larut (non polar).
Percobaan kedua yaitu pengujian ketidakjenuhan lemak. Pada percobaan ini digunakan 4 jenis sampel yaitu minyak hewani, minyak nabati, aquades, dan minyak nabati curah. Minyak hewani diberikan 60 tetes iodine menghasilkan warna coklat, pada aquades diberikan 41 tetes iodine menghasilkan warna coklat dan minyak nabati curah diberikan 57 tetes menghasilkan warna coklat. Pada sampel yang memiliki sumalh tetesan banyak termasuk larutan jenuh dan sampel yang memiliki jumlah tetesan iodine sedikir termasuk kedalam larutan tak jenuh.
Percobaan ketiga yaitu sifat penyabunan lemak, digunakan 4 larutan yaitu CaCl2 0,5%, MgCl2 0,5%, FeCl3 0,5%,dan minyak nabati. Larutan CaCl2 0,05 % yang diberikan sabun menghasilkan sangat banyak sabun dan menghasilkan
60
banyak busa pada deterjen. Larutan MgCl2 yang diberikan sabun menghasilkan sedikit gelembung sedagkan diberikan deterjen agak banyak gelembung yang dihasilkan. Larutan FeCl3 menghasilkan sedikit gelembung pada sabun dan agak banyak gelembung pada deterjen. Larutan minyak nabati yang diberikan sabun dan deterjen menghasilkan agak banyak gelembung. Dari hasil dapat diketahui bahwa larutan yang diberikan deterjen menghasilkan gelembung lebih banyak dibandingkan sabun. Adanya percobaan jumlah gelembung yang dihasilkan antara sabun dan deterjen memiliki faktor yaitu senayawa yang dapat menurunkan tegangan permukaan air.
KESIMPULAN
Berdasarkan hasil pengamatan dan pembahasan, maka dapat ditarik beberapa kesimpulan sebagai berikut :
1. Tidak semua pelarut dapat melarutkan senyawa lemak karena lemak hanya dapat larut pada larutan non polar.
2. Uji kelarutan lemak pada minyak nabati yang terlarut adalah kloroform, benzene, dan NaOH 0,05 M. Sedangkan pada minyak hewani terjadi penyatuan pada etanol, HCl 0,05 M, dan NaOH 0,05 M.
3. Pada uji ketidakjenuhan minyak hewani mendapatkan jumlah tetesan iodin terbanyak sedangkan minyak nabati mendapatakan tetesan iodin sedikit. 4. Pada uji kelarutan lemak apabila terdapat minyak diatas pelarut artinya
massa jenis lebih kecil dibandingkan pelarut dan apabila minyak dibawah dan pelarut diatas artinya massa jenis minyak lebih besar dari pelarut. 5. Uji penyabunan menghasilkan gelembung pada deterjen lebih besar atau
62
ACARA VI PENGUJIAN ENZIM
PENDAHULUAN
Latar Belakang
Enzim adalah katalisator biologis yang berperan dalam semua reaksi kimia dalam makhluk hidup. Enzim juga memiliki aplikasi industri dan medis berharga, seperti permentasi anggur, roti mengental, keju dan pembuatan bir. Telah di praktekkan sejak dahulu namun tidak sampai abat ke 19 reaksi ini telah dipahami sebagai aktifitas kata titik enzim. Sejak itu enzim diasumsikan peningkatan pentina dalam proses industri yang melibatkan reaksi kimia organic penyebab penyakit mempromosikan luka dan mendiagnosa penyakit tertentu. Enzim juga biasa di sebut sebagai suatu protein yang mempuyai struktur tiga demensi yang mampu menguatalisis reakisi biologis. Untuk mengaktifkan enzim di butuhkan adanya kofaktor seperti ion logam koenzim atau spesies yang lain (Benjamin, 2010).
Enzim yaitu suatu katalisatot protein yang mempercepat reaksi kimia dalam mahkluk hidup atau dalam siatem biologik. Enzim merupakan substansi yang ada dalam jumlah yang amat kecil dan mampu menyebabkan terjadinya perubahan-perubahan yang berkaitan dengan proses-proses seluler dan kehidupan. Nama lain daari enzim adalah fermen, nama enzim sendiri berasal dari bahasa Yu y g b t “d l g ” (Lunita, 2010).
Enzim adalah suatu kelompok protein yang menjalankan dan mengatur perubahan-perubahan kimia dalam sistem biologi. Zat ini dihasilkan oleh organ-organ hewan dan tanaman, yang secara katalitik menjalankan berbagai reaksi,
seperti pemecahan hidrolisis, oksidasi, reduksi, isomerasi, adisi, transfer radikal dan kadang-kadang pemutusan rantai karbon. Pembentukan enzim memerlukan bahan baku asam amino sehingga pembentukannya akan mengalami hambatan jika sumber bahan baku ini berkurang (Ruddi, 2010). Oleh karena itu, perlunya dilakukan pengujian enzim dalam memecah pati dan pengaruh pH, serta menentukan pH optimumnya.
Tujuan Praktikum
Adapun tujuan dari praktikum ini adalah untuk mengetahui kemampuan minimal enzim amilase air liur memecah pati persatuan waktu, dan mengetahui pengaruh pH terhadap aktivitas dan menentukan pH optimum enzim amilase air liur.
64
TINJAUAN PUSTAKA
Enzim adalah suatu kelompok protein yang menjalankan dan mengatur perubahan-perubahan kimia dalam sistem biologi. Kebanyakan enzim yang terdapat didalam alat-alat dan organ-organ organism hidup berupa larutan koloida dalam cairan tubuh, seperti air ludah, darah, cairan lambung, dan cairan pancreas. Enzim terdapat dibagian dalam sel. Hal ini terikat erat dengan protoplasma, gelombang ultrasonik dan radiasi ultraviolet atau pengaruh penambahan asam, basa dan pelarut organik tertentu (Darmin, 2009).
E z gh d ol p t d gl kog α-amylase (Destrinogenik) amilase atau duastasel berperan untuk menghasilkan fargmen dextrin dari pati. Sedangkan amilase (maltogenik amilase) membebaskan maltosa, glukosa bebas dan isomaltosa dari ikatan dalam amiloprotein. Amilase pada air ludah (kadang dinamakan ptyalin) dan amilase pancreas termasuk dalam a-amilase (Atmarita, 2009).
Enzim amilase merupakan salah satu enzim percenaan yang berasal dari getah pancreas. Enzim amilase juga terdapat didalam duodenum, namun sumbernya berasal dari pangkreas, duodenum merupakan muara dari getah pankreas. Enzim ini berfungsi untuk mendegradasi karbohidrat (pati) menjadi monosakarida dalam proses metabolisme tubuh dan sebagai penghasil energi dalam bentuk ATP. Penentuan aktivitas enzim amilase dilakukan dengan menggunakan metode Nelsonsomogyi dengan instrumen spektrotometer (Sesilia dan Yuanita, 2012).
Enzim merupakan suatu makromolekul (protein) mempercepat suatu reaksi kimia dalam tubuh mahluk hidup. Enzim tidak ikut bereaksi, tetapi