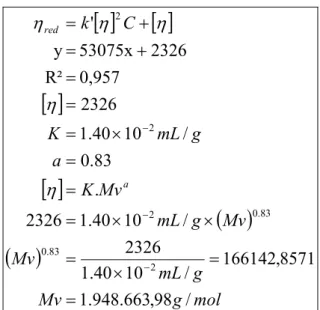Daftar Pustaka
Bilmeyer, F. W., (1971), Textbook of Polymer Science .2nd Edition, Wiley-Interscience Inc., New York, 264-265, 395-397
Chen, S.L. et al., (2004), Ion exchange resin/polystyrene sulfonate composite membranes for PEM fuel cells, J.Membrane Sci, 243, 327–328, 330
Cui, Z. et al., (2007), Polyelectrolyte complexes of chitosan and phosphotungstic acid as proton-conducting membranes for direct methanol fuel cells. Journal of Power
Sources, 167, 94–96, 98
Fessenden, R. J., & Fessenden, J. S., Kimia Organik, Aloysius Hadyana Pudjaatmaka (Penterjemah) (1986), Jilid I edisi 3, Penerbit Erlangga, Jakarta, h. 315-316,480
Focher, B. et al., (1992). Structural Differences Between Chitin Polymorphs and Their Precipitates from Solution Evidence from CP-MAS 13 C-NMR, FT-IR and FT-Raman Spectroscopy, Carbohidrat Polymer, 17 (2), 97 – 102
Fu, R.Q. et al, (2008). Sulfonated polystyrene/polyvinyl chloride composite membranes for PEMFC applications. Journal of Membrane Science. 309. 156–157.
Khan, T. A. et al.,(2002), Reporting Degree of Deacetylation Values of Chitosan:The Influence of Analytical Methods, J.Pharm Pharmaceut Sci, 5 (3) , 202-206
Makowski, H.S et.al., 1975, US pat, 3.870, 841
Martins, C.R. et al, (2003), Synthesis in Pilot Plant Scale and Physical Properties of Sulfonated Polystyrene, J. Braz. Chem. Soc., Vol. 14(5), 797-802
Morimoto, M. et al, (2002), Control of Functions of Chitin and Chitosan by Chemical Modification, 14(78) , 205–206
Rahmawati, F., (2007), Skripsi, Institut Teknologi Bandung, Bandung, 10,13,14-15
Smitha, B. et al., (2003), Synthesis and characterization of proton conducting polymer membranes for fuel cells .J.Membrane Sci ,225,63–65.
49
Won, J. et al., (2003) Structural characterization and surface modification of sulfonatedpolystyrene–(ethylene–butylene)–styrene triblock proton exchange membranes. J.
Membrane Sci, 214, 245–246
Zubir, N.A., Physico-chemical study of sulfonated polystyrene pore-filled electrolyte membranes by electrons induced grafting. 1-3
Lampiran
Lampiran A Sintesis Polistiren dan Kitosan
1. Rendemen polistiren
Tabel A. 1 Data sintesis polistiren
Vol stiren (mL) Massa Stiren (g) Massa PS hasil sintesis (g) Rendemen (%) 15 13,63 12,84 90,97 30 27,27 21,71 79,61 Contoh perhitungan : ρ stiren = 0,909 g/mL Rendemen
=
× 100% = × 100% = 90,97 %2. Penentuan derajat sulfonasi
Tabel A. 2 Data penentuan derajat sulfonasi
Massa PSS awal (g)
Vol NaOH titran rata-rata (mL)
% derajat sulfonasi
0,1511 2,15 24,19 0,1508 2,05 23,11 0,1512 2,60 29,23 Derajat sulfonasi rata-rata 25,33 %
Contoh perhitungan :
mol PSS = mol NaOH
= (2,15x 10-3) L x 0,0924 M = 1,9866x10-4 mol
massa PSS = mol PSS x Mr (unit ulang PSS) = (1,9866x10-4) mol x 184 g/mol = 0,03655 g
51
= × 100%52
Lampiran B Penentuan Massa Molekul Rata-Rata Viskositas (Mv)
1. Penentuan Mv Kitosan
Tabel B. 1 Waktu alir asam asetat dan larutan kitosan
Asam asetat 2% Kitosan 1000 ppm Kitosan 2000 ppm Kitosan 3000 ppm Kitosan 4000 ppm Kitosan 5000 ppm t1 3,82 14,02 31,16 50,4 69 99,1 t2 3,82 14,06 31,17 50,4 69,3 99,2 t3 3,82 14,07 31,17 50,5 69,4 99,4 t4 3,82 14,08 31,02 50,7 68,7 99,9 t5 3,82 14,15 31,08 50,8 68,4 98,4 t rata-rata 3,82 14,076 31,12 50,56 68,96 99,2
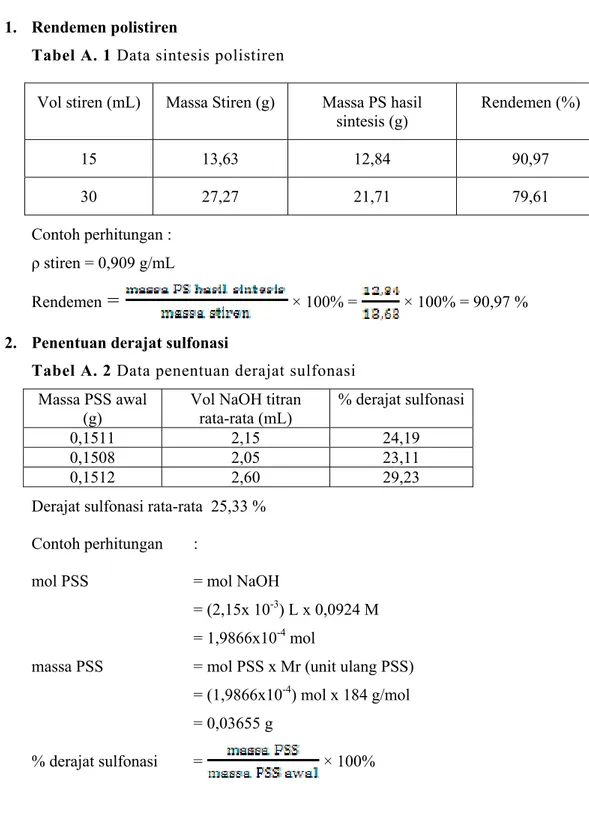
Tabel B. 2 Viskositas larutan kitosan
t
rata-rataC
(g/mL) η
r(t/t
0)
η
sp(η
r-1)
η
red(η
sp/C)
3,82 14,076 0,001 3,68 2,68 2684,82 31,12 0,002 8,14 7,14 3573,30 50,56 0,003 13,23 12,23 4078,53 68,96 0,004 18,05 17,05 4263,09 99,2 0,005 25,97 24,97 4993,7253
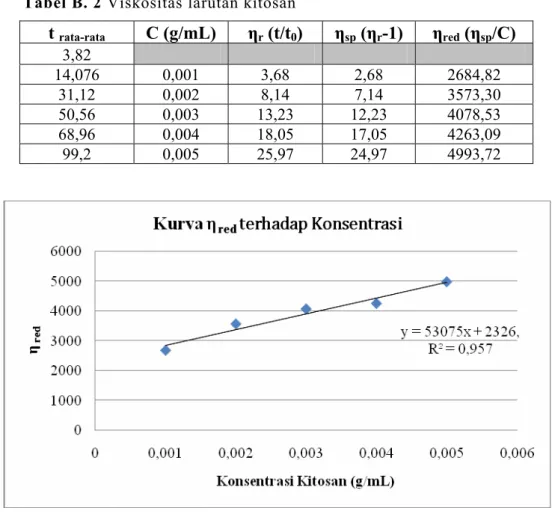
Cara perhitungan :[ ]
[ ]
[ ]
[ ]
( )
( )
mol
g
Mv
g
mL
Mv
Mv
g
mL
Mv
K
a
g
mL
K
C
k
a red/
98
,
663
.
948
.
1
8571
,
166142
/
10
40
.
1
2326
/
10
40
.
1
2326
.
83
.
0
/
10
40
.
1
2326
0,957
R²
2326
53075x
y
'
2 83 . 0 83 . 0 2 2 2=
=
×
=
×
×
=
=
=
×
=
=
=
+
=
+
=
− − −η
η
η
η
η
2. Penentuan Mv Polistiren
Tabel B. 3 Waktu alir toluen dan larutan polistiren
Larutan t
1t
2t
3t
4t
5t
rata-rataToluen 3,08 3,08 3,06 3,07 3,06
3,07
PS1 3,19 3,18 3,18 3,20 3,17 3,18
PS2 3,30 3,30 3,27 3,27 3,26 3,28
PS3 3,38 3,39 3,37 3,37 3,38 3,38
PS4 3,48 3,47 3,47 3,48 3,47 3,47
PS5 3,52 3,57 3,57 3,57 3,50 3,55
Tabel B. 4 Viskositas larutan polistiren
t
rata-rataC
(g/mL)
η
r(t/t
0)
η
sp(η
r-1)
η
red(η
sp/C)
3.07
3.18 0,001
1,04
0,037 37,13
3.28 0,002
1,07
0,068 34,20
3.38 0,003
1,10
0,100 33,44
3.47 0,004
1,13
0,131 32,90
3.55 0,005
1,15
0,155 31,01
54
Gambar B. 2 Kurva phi red terhadap konsentrasi larutan polistiren
Cara perhitungan :
[ ]
[ ]
[ ]
[ ]
( )
( )
mol
g
Mv
g
mL
Mv
Mv
g
mL
Mv
K
a
g
mL
K
C
k
a red/
21
,
743
.
70
5238
,
3469
/
0105
,
0
43
,
36
/
0105
,
0
43
,
36
.
73
.
0
/
0105
,
0
43
,
36
0,920
R²
36,43
x
1011,
-
y
'
73 . 0 73 . 0 2=
=
=
×
=
=
=
=
=
=
+
=
+
=
η
η
η
η
η
55
Lampiran C Data dan Perhitungan Analisis Polyblend
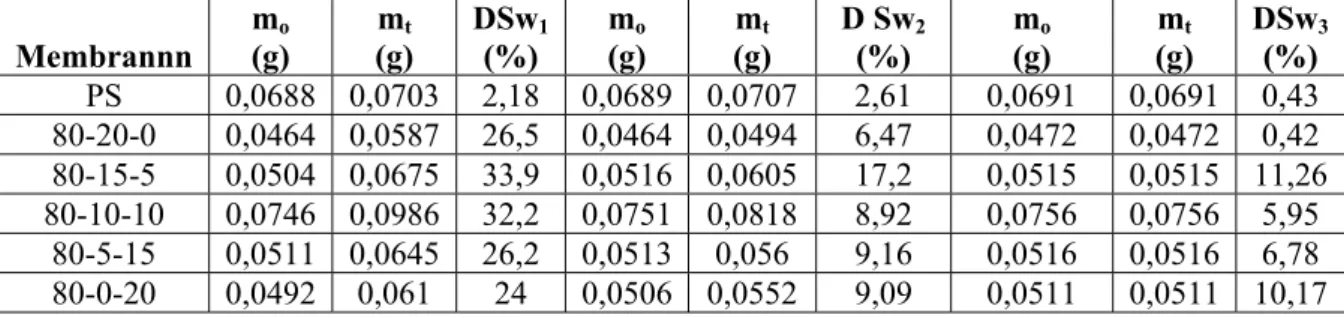
1. Derajat swelling
Tabel C. 1 Data analis swelling Membrannn mo (g) mt (g) DSw1 (%) mo (g) mt (g) D Sw2 (%) mo (g) mt (g) DSw3 (%) PS 0,0688 0,0703 2,18 0,0689 0,0707 2,61 0,0691 0,0691 0,43 80-20-0 0,0464 0,0587 26,5 0,0464 0,0494 6,47 0,0472 0,0472 0,42 80-15-5 0,0504 0,0675 33,9 0,0516 0,0605 17,2 0,0515 0,0515 11,26 80-10-10 0,0746 0,0986 32,2 0,0751 0,0818 8,92 0,0756 0,0756 5,95 80-5-15 0,0511 0,0645 26,2 0,0513 0,056 9,16 0,0516 0,0516 6,78 80-0-20 0,0492 0,061 24 0,0506 0,0552 9,09 0,0511 0,0511 10,17
2. Ion Exchange Capacity
[NaOH] = [HCl] = 0,0972 M Vol NaOH blanko1 = 5,55 mL Vol NaOH blanko2 = 5,60 mL Vol NaOH blanko rata-rata = 5,575 mL
Tabel C. 2 Data analisis IEC
Membran Massa (g) V NaOH rata-rata (mL) IEC (m ekiv/g) 80-20-0 0,04 5,45 1,14 80-15-5 0.05 5,55 0,20 80-10-10 0.04 5,2 3,75 80-5-15 0.06 5,2 2,55 80-0-20 0.05 5,5 0,55
IEC =
56
3. Konduktivitas
Tabel C. 3Data konduktivitas
Membran 1/Rtotal
(µS) Rtotal (Ω) R blanko (Ω) R membran (Ω) Tebal (cm) (µS/cm) σ σ rata-rata (µS/cm)
80-20-0 60 16666,67 156,25 16510,42 0,02 1,94 5,32 24 4166,67 156,25 4010,41 0,02 8,70 80-15-5 12 8333,33 156,25 8177,08 0,05 9,93 7,69 80 12500,00 156,25 12343,75 0,04 5,19 80-10-10 95 10526,31 156,25 10370,06 0,03 4,27 8,22 165 6060,60 156,25 5904,35 0,04 12,173 80-5-15 70 14285,71 156,25 14129,46 0,04 4,14 3,00 35 28571,43 156,25 28415,18 0,03 1,86 80-0-20 340 2941,17 156,25 2784,92 0,05 31,045 3,93 505 1980,20 156,25 1823,95 0,05 47,54
4. Analisis Mekanik
Tabel C. 4Data analisis mekanik
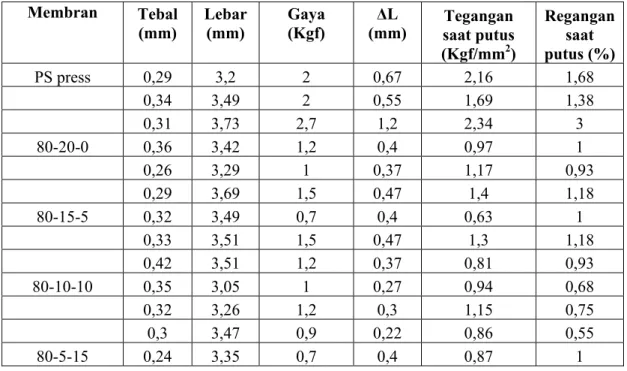
Membran Tebal (mm) Lebar (mm) Gaya (Kgf) ΔL
(mm) saat putus Tegangan (Kgf/mm2) Regangan saat putus (%) PS press 0,29 3,2 2 0,67 2,16 1,68 0,34 3,49 2 0,55 1,69 1,38 0,31 3,73 2,7 1,2 2,34 3 80-20-0 0,36 3,42 1,2 0,4 0,97 1 0,26 3,29 1 0,37 1,17 0,93 0,29 3,69 1,5 0,47 1,4 1,18 80-15-5 0,32 3,49 0,7 0,4 0,63 1 0,33 3,51 1,5 0,47 1,3 1,18 0,42 3,51 1,2 0,37 0,81 0,93 80-10-10 0,35 3,05 1 0,27 0,94 0,68 0,32 3,26 1,2 0,3 1,15 0,75 0,3 3,47 0,9 0,22 0,86 0,55 80-5-15 0,24 3,35 0,7 0,4 0,87 1
57
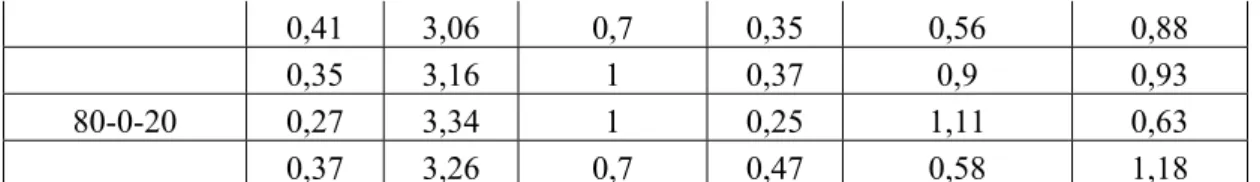
0,41 3,06 0,7 0,35 0,56 0,880,35 3,16 1 0,37 0,9 0,93
80-0-20 0,27 3,34 1 0,25 1,11 0,63
0,37 3,26 0,7 0,47 0,58 1,18
Tabel C. 5 Hasil uji tarik
Membran Tegangan saat
Putus rata-rata (Kgf/mm2) Regangan saat putus rata-rata (%) Modulus Young saat putus PS press 2,06 2,02 1,02 80-20-0 1,18 1,03 1,14 80-15-5 0,91 1,03 0,88 80-10-10 0,98 0,66 1,49 80-5-15 0,78 0,93 0,83 80-0-20 0,69 1,02 0,68
58
Lampiran D Percobaan Pembuatan Polyblend
Sebelum melakukan pembuatan membran secara mekanik, penulis telah melakukan pengujian dan metode lain pembuatan membran, yaitu :
1. Dengan pelarut DMF
Massa polistiren = 0,8005 g Massa kitosan = 0,1118 g Volume DMF = 3,2 mL Massa polistiren tersulfonasi = 0,8029 g Massa kitosan = 0,1055 g Volume DMF = 3,2 mL
Penggunaan pelarut DMF berdasarkan kelarutan polistiren tersulfonasi dalam DMF. Cara kerjanya yaitu, campuran polistiren-kitosan-DMF dimasukkan dalam gelas kimia dan pada gelas kimia yang lain dimasukkan campuran polistiren tersulfonasi-kitosan-DMF. Keduanya kemudian diaduk dengan magnet stirrer selama beberapa jam. Hasilnya dalam percobaan ini DMF tidak dapat melarutkan polistiren-kitosan, dan polistiren tersulfonasi-kitosan karena perbedaan sifat kepolaran polistiren dan kitosan. Kitosan bersifat polar, polistiren bersifat non polar serta polistiren tersulfonasi dalam percobaan ini bersifat cenderung non polar.
2. Penggunaan surfaktan (polietilen glikol)
Berdasar sifat kitosan yang polar dan sifat polistiren tersulfonasi yang cenderung non polar ,dilakukan percobaan menggunakan surfaktan sebagai pelarut kedua molekul polimer ini. Pertama-tama, masing-masing bahan dilarutkan ke dalam pelarutnya terlebih dahulu, PSS dengan DMF dan kitosan dengan asam asetat 2 % lalu setelah kedua larutan polimer terbentuk dilakukan penambahan polietilen glikol (PEG), dengan perbandingan PSS:kitosan:PEG 80:10:10. Larutan kemudian diaduk dan ditempatkan di cawan petri. Setelah satu minggu telah terbentuk padatan namun bersifat seperti gel dan basah sehingga padatan ini tidak dapat diangkat dari cawan karena lengket. Kemudian ditambahkan aquades ke dalam cawan sehingga padatan terendam dan supaya padatan dapat lepas dari cawan karena PSS dan kitosan tidak larut dalam air. Namun setelah berminggu-minggu padatan tetap tidak dapat terangkat dari cawan. Surfaktan yang digunakan hendaknya diuji kompatibilasnya dan pada penambahan berapa surfaktan dalam membantu dalam pembentukan membran PSS-kitosan.
59
3. Uji titik leleh
Uji titik leleh polimer dilakukan untuk menentukan suhu yang diperlukan untuk pembuatan membran dengan metode hotpress. Suhu yang dipakai polimer dalam metode hotpress yaitu berada sedikit di bawah titik leleh polimer tersebut. Alat yang digunakan yaitu electrothermal melting point apparatus. Hasilnya, polistiren leleh pada suhu 184 o C, sementara kitosan tidak memiliki titik leleh namun langsung hancur (hangus) pada suhu 216 o C.
4. Metode hotpress dengan perbandingan PSS-kitosan=2:8
Massa polistiren tersulfonasi = 0,4073 g Massa kitosan = 1,6174 g
Kedua bahan dicampur dan dihaluskan dengan blender, kemudian dilakukan hotpress dengan suhu 120oc dan tekanan 200 kgf selama 5 menit. Hasilnya, kedua bahan tidak homogen, dan masih berbentuk hancuran (tidak saling menempel). Lalu dilakukan pengulangan hotpress dengan menaikkan suhu dan tekanan menjadi 130oc dan 250 kgf. Hasil yang didapat kedua bahan terlihat lebih menempel namun tetap tidak homogen (Gambar D. 1).
Gambar D. 1 Membran dengan komposisi 20% PSS-80% kitosan 5. Dengan pelarut tolen-n butanol = 7:3
PSS larut baik dalam tolen-n butanol = 7:3 namun ternyata kurang baik untuk menghasilkan membran PSS . Pada penelitian tersebut sulfonasi dilakukan selama 1 jam sedangkan pada tugas akhir ini sulfonasi dilakukan selama 20 menit sehingga produk yang dihasilkan berbeda. Pada penelitian ini membran yang dihasilkan berpori besar dan memiliki permukaan yang kasar. Hal ini mungkin terjadi karena kurang cocoknya pelarut dengan polimer serta perbedaan kecepatan menguap antara pelarut toluen dan butanol.
6. Metode perendaman membran PSS dalam larutan kitosan
Berdasar sifat kelarutan polistiren dengan diklorometana, dilakukan percobaan kelarutan PSS dengan diklorometana. Hasilnya, PSS larut baik dalam diklorometana dan cocok sebagai pelarut dalam pembuatan membran karena diklorometana dengan cepat menguap. Membran PSS (6% b/v dalam 10 ml) terbentuk dan kering dalam waktu dua malam sehingga
60
namun hasilnya sedikit berpori, karena kemungkinan terlalu cepatnya diklorometana menguap. Membran PSS kemudian dicelupkan ke dalam larutan kitosan dengan konsentrasi bervariasi. Setelah sekitar lima hari membran kering namun kitosan tidak dapat menempel sempurna pada PSS karena terbentuk lapisan kitosan diatas PSS dengan warna sedikit kekuningan dan hanya menempel di bagian pinggir saja. Hal ini mungkin karena perbedaan kepolaran kedua polimer dan sifat film kitosan yang mudah mengkerut dalam keadaan kering.7. Metode press membran kitosan dengan PSS
Metode ini dilakukan karena pada metode 6 kitosan bersifat mengkerut sehingga tidak menempel sempurna pada PSS. Asumsi jika membran kitosan terlebih dahulu dibuat dengan cara pelarutan, kemudian di press dengan PSS kedua polimer akan lebih tercampur karena bentuk kitosan yang tetap rata (tidak mengkerut). Namun karena sifat pengkerutan membran kitosan sangat kuat, hasil membran PSS-kitosan yang dihasilkan memiliki permukaan kasar karena besarnya sifat pengkerutan kitosan.
61
Lampiran E Penentuan Derajat Deasetilasi Kitosan
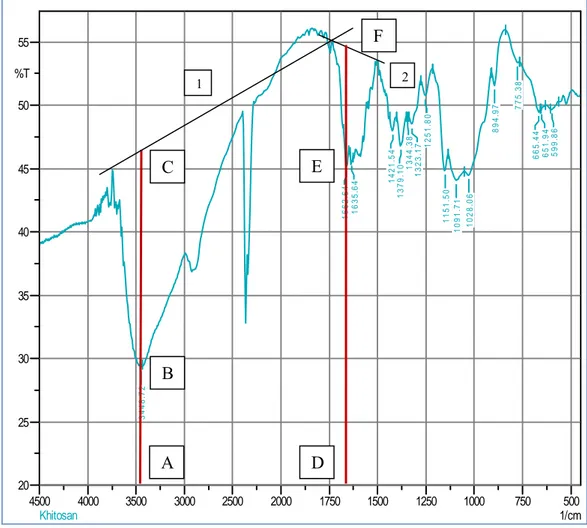
500 750 1000 1250 1500 1750 2000 2500 3000 3500 4000 4500 1/cm 20 25 30 35 40 45 50 55 %T 3448. 72 16 62. 64 16 35. 64 1421. 54 1379. 10 1344. 38 1323. 17 1251. 80 1151. 50 1091. 71 1028. 06 89 4. 97 77 5. 38 665. 44 651. 9 4 599. 86 Khitosan
Gambar E. 1Spektrum IR Kitosan
=