i
KARAKTERISASI EKSTRAK ETANOLIK DAUN TEH HIJAU (Camellia sinensis L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh: Ayu Widya Sari NIM : 068 114 061
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii
KARAKTERISASI EKSTRAK ETANOLIK DAUN TEH HIJAU (Camellia sinensis L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh: Ayu Widya Sari NIM : 068 114 061
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
v
HALAMAN PERSEMBAHAN
Kupersembahkan karya ini bagi:
☺
Allah SWT atas karunia, rahmat, anugerah, kehidupan yang
begitu indah yang telah diberikan bagiku
☺
Orang tuaku tercinta Bapak M.Najamuddin dan Ibu Tedja
Murni atas doa, cinta, kasih sayang, pengertian, kesabaran, dan
yang merupakan tujuan perjuanganku, semangatku,
segala-galanya bagiku, dimana aku tidak akan bisa membalas
semua yang telah diberikan kepadaku.
☺
Ayukku tersayang Indah Pudji Sari yang telah memberikan
kasih sayang, dukungan, dan semangat bagiku.
☺
Kakakku tersayang Zito Kristie Abdi yang telah memberikan
kasih sayang, dukungan, dan semangat bagiku.
☺
Adikku tersayang Reto Minotie Abdi yang telah memberikan
kasih sayang, dukungan, dan semangat bagiku.
☺
Sahabat-sahabat terbaikku yang selalu membantuku,
selalu ada buatku baik suka maupun duka.
☺
Semua orang yang aku sayangi dan menyayangi aku
vii PRAKATA
Puji syukur penulis panjatkan kehadirat Allah Yang Maha Esa yang senantiasa melimpahkan rahmat, karunia dan petunjuk-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul Karakterisasi Ekstrak Etanolik Daun Teh Hijau (Camellia sinensis L.)
Skripsi ini ditulis sebagai salah satu syarat untuk mencapai gelar kesarjanaan pada Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Selama penelitian dan penyusunan skripsi ini tidak lepas dari peran serta berbagai pihak yang telah memberikan bimbingan, dorongan dan saran, maka pada kesempatan ini penulis mengucapkan banyak terima kasih kepada:
1. Ibu Erna Tri Wulandari, M.Si.,Apt. selaku Dosen Pembimbing, yang telah memberikan bimbingan dan pengarahan yang sangat berguna demi terselesaikannya skripsi ini.
2. Bapak Yohanes Dwiatmaka, M.Si. selaku Dosen Penguji atas masukan dan sarannya.
3. Bapak Dr. C.J. Soegihardjo, Apt. selaku Dosen Penguji atas masukan dan sarannya.
4. Seluruh staff Laboratorium Farmakognosi Fitokimia dan Laboratorium Kimia Universitas Sanata Dharma, Yogyakarta: Mas Wagiran, Mas Sigit, Mas Sarwanto, Mas Parlan, Mas Kunto, Mas Bimo yang telah menemani dan membantu selama penelitian.
viii
6. Sahabat terbaikku Grace Litad, Monica Dini Puspita, Inge Maria Wibowo atas kerjasama, suka-duka, kekompakan, bantuan, dan kebersamaan selama proses penelitian dan penyusunan skripsi.
7. Sahabat terbaikku Winny Listyarini Hardi, Tiara Pranasita, Yenni Christina, Sri Yuniarti, Gessi Purnamasari, Ni Nyoman Manik Uliani, Karolina Reni Kristiani, Aroma Mayangsari, Frida Mayasari, Dewi Prasetyaningrum, dan teman-teman Farmasi Klinis Komunitas atas bantuan, dukungan, kerjasama, kebersamaan, suka duka kita selama ini. 8. Teman-teman seperjuanganku angkatan 2006 atas bantuan, kebersamaan,
dan keceriaan kita selama ini.
9. Semua pihak yang tidak dapat disebutkan satu persatu yang telah membantu terwujudnya skripsi ini.
Penulis menyadari masih banyak kekurangan dalam penyusunan skripsi ini, maka ini jauh dari sempurna. Oleh karena itu penulis mengharapkan kritik dan saran yang membangun dari segenap pembaca, semoga skripsi ini bermanfaat bagi perkembangan ilmu pengetahuan khususnya dalam hal penelitian di bidang Farmakognosi dan berguna bagi pembaca.
Yogyakarta, 08 Januari 2010
x INTISARI
Teh (Camellia sinensis L.) merupakan tanaman obat yang telah dikenal sejak lama oleh masyarakat. Bagian tanaman teh yang memiliki banyak khasiat adalah daun teh. Daun teh hijau berkhasiat sebagai antioksidan dan meningkatkan pembakaran kalori dan lemak yang berimplikasi terhadap penurunan berat badan. Pada industri obat tradisional karakterisasi bahan baku perlu dilakukan untuk menjaga kontinuitas kualitas dari segi SQE (Safety, Quality, Efficacy). Penelitian ini bertujuan untuk mengetahui karakter dari ekstrak etanolik daun teh hijau sebagai salah satu bahan baku penyusun jamu pelangsing, sehingga diperoleh produk yang mempunyai standar kualitas yang seragam dan terulang.
Penelitian ini merupakan jenis penelitian non eksperimental, berupa karakterisasi ekstrak yang mengikuti parameter standar umum ekstrak tumbuhan obat. Parameter yang diuji meliputi organoleptik ekstrak, identitas ekstrak, penetapan kadar air, kadar abu, kadar abu tidak larut asam, kadar abu larut air, kadar sari larut air, kadar sari larut etanol, dan penentuan senyawa identitas ekstrak etanolik daun teh hijau secara kualitatif dan kuantitatif.
Hasil penelitian dianalisis secara deskriptif diperoleh organoleptik
ekstrak berwarna cokelat kehitaman, tidak berbau, dan rasa agak kelat; kadar air 27,51 % b/b; kadar abu 2,22 % b/b; kadar abu tidak larut asam 1,40 % b/b; kadar
abu larut air 0,87 % b/b; kadar sari larut air 23,17 % b/b; kadar sari larut etanol 42,98 % b/b; dan kadar senyawa identitas (epigallokatekin galat) 2 x 10-4 ± 0 % b/v.
xi ABSTRACT
Tea (Camellia sinensis L.) was medicinal herbs that has known by people since along time ago. Part of tea herbal that has many functions was tea’s leaves. The green tea’s leaves has a funtion as an antioxidant and also increase of calori burning and fat that have implication to reduce body weight. In traditional medicine industry, the basic material characterization is required to maintain the quality continuity from SQE (Safety, Quality, Efficacy) side. This research aims to find out the character of the green tea’s leaves ethanolic extract as one of the basic materials of slimming herbal medicine, so it is able to get the product that has the same and continual quality standard.
This is a non experimental research, namely characterization the extract that refers to general standard parameter of medicinal herbs extract. The general standard parameter includes extract organoleptic, extract identity, the determination of water degree, ashes degree, acid dissoluble ashes degree, and act of determining identity chemical compound ethanolic extract of green tea’s leaves qualitatively and quantitatively.
The results were analyzed descriptively. As results, organoleptic extract blackish brown, no smell, and taste a little sourish; the water degree score was 27,51 % w/w; the ashes degree was 2,22 % w/w; acid dissoluble ashes degree was 1,40 % w/w; water soluble ashes degree was 0,87 % w/w; water soluble essence degree was 23,17 % w/w; ethanolic soluble essence degree was 42,98 % w/w; extract identity; organoleptic extract that was one of the characteristics of the green tea’s ethanolic extract; and chemical identity (epigallocatechin gallate) degree was 2 x 10-4± 0 % w/v.
xii DAFTAR ISI
HALAMAN JUDUL...ii
HALAMAN PERSETUJUAN PEMBIMBING...iii
HALAMAN PENGESAHAN... iv
HALAMAN PERSEMBAHAN...v
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI……….vi
PRAKATA...vii
PERNYATAAN KEASLIAN KARYA...ix
INTISARI...x
ABSTRACT...xi
DAFTAR ISI ...xii
DAFTAR TABEL...xvi
DAFTAR GAMBAR...xvii
DAFTAR LAMPIRAN...xviii
BAB I. PENGANTAR...1
A. Latar Belakang………...1
1. Permasalahan...3
2. Keaslian penelitian...3
3. Manfaat penelitian...3
B. TujuanPenelitian………...………...4
BAB II. PENELAAHAN PUSTAKA...5
xiii
1. Keterangan botani ...……….…...5
2. Deskripsi...5
3. Penggolongan...6
4. Kandungan kimia teh hijau...6
5. Syarat tumbuh...9
6. Khasiat teh hijau...10
B. Pembuatan Simplisia...10
1. Bahan baku...10
2. Dasar pembuatan...11
3. Tahapan pembuatan...11
C. Ekstrak...15
1. Definisi ekstrak...15
2. Pengelompokan ekstrak...15
3. Metode ekstraksi...15
4. Penguapan...17
D. Standarisasi...18
1. Pembakuan simplisia...19
2. Pembakuan ekstrak...19
3. Pembakuan sediaan obat tradisional...21
E. Kromatografi Lapis Tipis...21
F. KLT-Densitometri...23
G. Keterangan Empiris...24
xiv
A. Jenis dan Rancangan Penelitian...25
1. Jenis penelitian...25
2. Rancangan penelitian...25
B. Definisi Operasional...26
C. Alat...26
D. Bahan...27
E. Jalannya Penelitian...27
1. Determinasi tanaman...27
2. Pengumpulan bahan...27
3. Pembuatan serbuk daun teh hijau...27
4. Pembuatan ekstrak kental...28
5. Uji organoleptik ekstrak...28
6. Identitas ekstrak...28
7. Penetapan kadar air...28
8. Penetapan kadar abu...29
9. Penetapan kadar abu tidak larut asam...29
10. Penetapan kadar abu larut air...29
11. Penetapan kadar sari larut air...30
12. Penetapan kadar sari larut etanol...30
13. Penentuan senyawa identitas secara kualitatif dan kuantitatif...30
F. Analisis Hasil...33
BAB IV. HASIL DAN PEMBAHASAN...34
xv
B. Pengumpulan Bahan dan Pembuatan Serbuk...34
C. Pembuatan Ekstrak Kental...37
D. Organoleptik Ekstrak...39
E. Identitas Ekstrak...39
F. Penetapan Kadar Air...40
G. Penetapan Kadar Abu...41
H. Penetapan Kadar Abu Tidak Larut Asam...42
I. Penetapan Kadar Abu Larut Air...43
J. Penetapan Kadar Sari Larut Air...44
K. Penetapan Kadar Sari Larut Etanol...45
L. Penentuan Senyawa Identitas secara Kualitatif dan Kuantitatif...45
1. Penentuan senyawa identitas secara kualitatif...45
2. Penentuan senyawa identitas secara kuantitatif...52
BAB V. KESIMPULAN DAN SARAN...56
A. Kesimpulan...56
B. Saran...56
DAFTAR PUSTAKA...57
LAMPIRAN...60
xvi
DAFTAR TABEL
Tabel I. USDA database for the flavonoid content of dried teas...8 Tabel II. Hasil KLT standar (epigallokatekin galat) dan sampel (ekstrak
etanolik daun teh hijau)...51 Tabel III. Persamaan kurva baku dari hubungan kadar standar epigallokatekin galat (x) dengan (AUC) (y)...54 Tabel IV. Kadar senyawa epigallokatekin galat (% b/v) yang terdapat dalam
xvii
DAFTAR GAMBAR
Gambar 1. Struktur flavanol teh...7 Gambar 2. Struktur flavonol teh...8 Gambar 3. Ekstrak kental (a) dan ekstrak cair (b) daun teh hijau...38 Gambar 4. Kromatogram standar EGCG dan sampel ekstrak etanolik daun teh hijau dengan deteksi di bawah lampu UV 254 nm...47 Gambar 5. Kromatogram standar EGCG dan sampel ekstrak etanolik daun teh
hijau dengan deteksi di bawah lampu UV 365 nm...48 Gambar 6. Kromatogram standar EGCG dan sampel ekstrak etanolik daun teh
hijau dengan deteksi larutan besi (III) klorida ...49
Gambar 7. Hasil pengukuran λmaks epigallokatekin galat baku.
λmaks epigallokatekin galat terletak pada 280 nm...53
xviii
DAFTAR LAMPIRAN
Lampiran 1. Surat keterangan determinasi...60
Lampiran 2. Data pengentalan ekstrak cair...61
Lampiran 3. Hasil organoleptik ekstrak...63
Lampiran 4. Hasil identitas ekstrak...63
Lampiran 5. Perhitungan penetapan kadar air...64
Lampiran 6. Perhitungan penetapan kadar abu...65
Lampiran 7. Perhitungan penetapan kadar abu tidak larut asam...66
Lampiran 8. Perhitungan penetapan kadar abu larut air...67
Lampiran 9. Perhitungan penetapan kadar sari larut air...68
Lampiran 10. Perhitungan penetapan kadar sari larut etanol...69
Lampiran 11. Hasil kromatografi lapis tipis senyawa identitas...70
Lampiran 12. Perhitungan penetapan kadar senyawa identitas ...72
1
A. Latar Belakang
Seiring dengan berkembangnya ilmu pengetahuan dan teknologi, maka masyarakat semakin selektif dalam memilih obat. Pilihan masyarakat kini beralih dari obat-obatan kimia ke obat tradisional karena diharapkan dapat meminimalkan efek samping yang ditimbulkan (Anonim, 2000).
Salah satu tanaman yang dapat digunakan sebagai obat tradisional adalah tanaman teh. Tanaman teh banyak ditanam di Asia Tenggara termasuk Cina, India, Jepang, Taiwan, Sri Lanka, dan Indonesia. Umumnya tanaman teh diklasifikasikan ke dalam tiga kategori utama yaitu teh hijau yang pada proses produksinya tanpa fermentasi, teh oolong dengan fermentasi sebagian dan teh hitam dengan fermentasi (Kun Lin, 1998). Khasiat utama tanaman teh hijau sebagai antioksidan. Selain itu, teh dapat juga sebagai peluruh lemak. Berdasarkan
American Journal of Clinical Nutrition, teh hijau memiliki potensi dapat
meningkatkan pembakaran kalori dan lemak yang berimplikasi terhadap penurunan berat badan (Craig, 1999).
daun teh hijau menggunakan penyari etanol sehingga diharapkan senyawa polifenol yang ada dalam daun teh hijau dapat tersari dengan optimal. Berdasarkan penelitian tentang teh hijau yaitu uji aktivitas penangkapan radikal hidroksil oleh ekstrak etanol teh hijau dan teh hitam dengan menggunakan metode deoksiribosa, ekstrak etanol teh hijau dan teh hitam memiliki efektif penangkapan radikal hidroksil sebesar 50 % (Kuntari, 2007).
etanol, dan penentuan senyawa identitas ekstrak etanolik daun teh hijau secara kualitatif dan kuantitatif.
1. Permasalahan
Berdasarkan latar belakang tersebut timbul permasalahan, yaitu : Bagaimana karakter dari ekstrak etanolik daun teh hijau ?
2. Keaslian penelitian
Sejauh pengetahuan penulis penelitian mengenai karakteristik ekstrak etanolik daun teh hijau belum pernah dilakukan. Adapun penelitian yang telah dilakukan adalah uji aktivitas penangkapan radikal hidroksil oleh ekstrak etanol teh hijau dan teh hitam dengan metode deoksiribosa (Kuntari, 2007), penetapan kadar flavonoid total terhitung sebagai kuersetin dengan menggunakan metode kolorimetri dalam teh hijau dan teh hitam (merk x) (Pertiwi, 2006), dan perbandingan daya antioksidan infusa teh hijau dari daerah Wonosobo dan daerah Karanganyar dengan menggunakan metode deoksiribosa (Purnamasari, 2009).
3. Manfaat penelitian
Hasil penelitian ini diharapkan dapat memberikan manfaat, yaitu : a. Manfaat teoritis
b. Manfaat praktis
Penelitian ini diharapkan dapat digunakan sebagai informasi kepada masyarakat bahwa ekstrak etanolik daun teh hijau telah sesuai dengan parameter standar ekstrak yang telah ditetapkan oleh Badan Pengawas Obat dan Makanan dan dapat digunakan sebagai komponen penyusun dalam jamu pelangsing.
B. Tujuan Penelitian
5 A. Teh
1. Keterangan botani
Teh berasal dari kawasan Cina Selatan, Indonesia, India, Taiwan, dan Sri Lanka (Kun Lin, 1998). Daun teh adalah daun Camellia sinensis L.
dengan sinonim Thea sinensis L., suku Theaceae (Anonim, 1989). Nama umum atau dagang : Teh. Nama daerah : Teh (Melayu), Nteh (Sunda), Teh (Jawa tengah) (Hutapea, 1994).
2. Deskripsi
3. Penggolongan
Semua jenis teh dibuat dari sumber yang sama, yaitu pucuk dan daun muda tanaman teh. Berdasarkan proses pengolahannya, teh dapat diklasifikasikan menjadi tiga jenis yaitu teh hijau, teh hitam, dan teh oolong. Teh hijau dibuat dengan cara menginaktivasi enzim polifenol oksidase yang ada dalam pucuk teh segar, dengan cara pemanasan atau penguapan menggunakan uap panas sehingga oksidasi enzimatik terhadap katekin dapat dicegah. Teh hitam dibuat dengan cara memanfaatkan terjadinya oksidasi enzimatis terhadap kandungan katekin teh, sedangkan, teh oolong dihasilkan melalui proses pemanasan yang dilakukan segera setelah proses rolling/penggulungan daun, dengan tujuan untuk menghentikan proses fermentasi. Oleh karena itu, teh oolong disebut sebagai teh semi-fermentasi (Hartoyo, 2003). Perbedaan utama yang cukup berarti dari ketiga proses pengolahan teh tersebut adalah pada kandungan katekinnya. Kandungan
katekin tertinggi dimiliki oleh teh hijau, disusul teh oolong, dan teh hitam (Syah, 2006).
4. Kandungan kimia teh hijau
dapat larut dalam pelarut seperti etanol atau air. Teh hijau mengandung kira-kira 30-40% polifenol (bobot kering) (Luper, 1999).
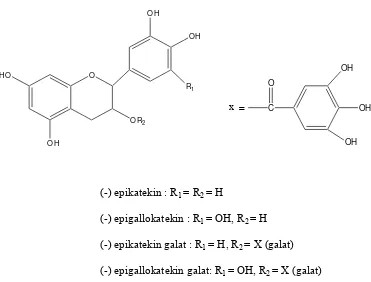
Flavanol dalam secara struktural termasuk subgolongan flavan-3-ol.
Katekin utama dalam teh hijau terdiri dari (-) epikatekin, (-) epigallokatekin, (-) epikatekin galat, (-) epigallokatekin galat. Epigallokatekin galat (EGCG)
Tabel I. USDA database for the flavonoid content of dried teas
Flavon 3-ols Black Tea Green Tea Oolong Tea
Tea Leaves, Dry Tea Leaves, Dry Tea Leaves, Dry
Epicatechin 255,19 811,72 248,42
Epicatechin 3-gallate 688,27 1491,29 627,25
Epigallocatechin 956,81 2.057,98 750,80
Epigallocatechin 3-gallate 1.121,92 7.115,98 3.412,62
Catechin 137,82 57,12 30,63
Catechin 3-gallate 50,83 7,07 19,89
Gallocatechin 91,73 258,11 305,69
Theaflavin 159,20 1,64 15,23
Theaflavin 3-3’-digallate 170,77 1,08 18,62
Theaflavin 3’-gallate 155,77 0,44 -
Theaflavin 3-gallate 132,25 0,47 -
Thearubigins 59,19 137,91 -
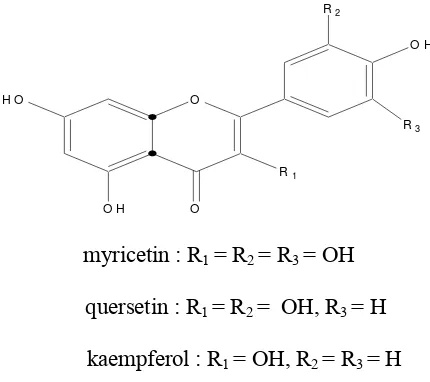
(Indarto, 2009) Flavonol merupakan salah satu antioksidan alami yang terdapat dalam tanaman teh dan mempunyai kemampuan mengikat logam (Syah, 2006). Flavonol utama yang ada di dalam daun teh hijau adalah myricetin, quersetin, dan
kaempferol. Jumlah flavonol dalam teh hijau sebesar 2-3 %. Flavonol ini,
terutama terdapat dalam bentuk glikosidanya (berikatan dengan molekul gula) dan sedikit dalam bentuk aglikonnya (Hartoyo, 2003).
5. Syarat tumbuh
Lingkungan fisik yang paling berpengaruh terhadap pertumbuhan tanaman teh adalah keadaan iklim (curah hujan, suhu udara, tinggi tempat, sinar matahari, kelembaban) dan tanah.
a. Curah hujan : curah hujan tahunan yang diperlukan adalah 2.000 mm-2.500 mm, dengan jumlah hujan pada musim kemarau rata-rata tidak kurang dari 100 mm.
b. Suhu udara : suhu udara yang baik berkisar antara 13oC-25oC, yang diikuti oleh cahaya matahari yang cerah dengan kelembaban relatif pada siang hari tidak kurang dari 70 %.
c. Tinggi tempat : umumnya tanaman teh ditanam pada ketinggian lebih dari 400 meter di atas permukaan laut. Di Indonesia, pertanaman teh dilakukan pada ketinggian antara 400 m-1200 m dari permukaan laut (dpl).
e. Kelembaban : tanaman teh menghendaki kelembaban relatif yang cukup tinggi.
f. Tanah : tanah yang cukup subur dengan kandungan bahan organik cukup, memiliki derajad keasaman (pH) antara 4,5-6,0 (Setyamidjaja, 2000).
6. Khasiat teh hijau
Teh hijau memiliki khasiat yang sangat berpengaruh bagi kesehatan manusia, diantaranya antioksidan, mempertahankan berat tubuh ideal, mereduksi kolesterol, menurunkan LDL (Low Density Lipoprotein), meningkatkan HDL
(High Density Lipoprotein), mengurangi kadar gula darah, menurunkan tekanan
darah, mengurangi stres, antitrombosis, dan antikanker (Hartoyo, 2003).
B. Pembuatan Simpisia
Simplisia adalah bahan alamiah yang dipergunakan sebagai obat yang belum mengalami pengolahan apapun juga dan kecuali dikatakan lain, simplisia merupakan bahan yang dikeringkan. Simplisia dapat berupa simplisia nabati, simplisia hewani, dan simplisia pelikan atau mineral (Anonim, 1985).
Pembuatan simplisia secara umum : 1. Bahan baku
2. Dasar pembuatan
a. Simplisia dibuat dengan cara pengeringan
Pembuatan simplisia dengan cara ini pengeringannya dilakukan dengan cepat, tetapi pada suhu yang tidak terlalu tinggi. Pengeringan yang dilakukan dengan waktu lama akan mengakibatkan simplisia yang diperoleh ditumbuhi kapang. Pengeringan yang dilakukan pada suhu terlalu tinggi akan mengakibatkan perubahan kimia pada kandungan senyawa aktifnya.
b. Simplisia dibuat dengan proses fermentasi
Proses fermentasi dilakukan dengan seksama, agar proses tersebut tidak berkelanjutan kearah yang tidak diinginkan.
c. Simplisia dibuat dengan proses khusus
Pembuatan simplisia dengan cara penyulingan, pengentalan eksudat nabati, pengeringan sari air, dan proses khusus lainnya dilakukan dengan berpegang pada prinsip bahwa simplisia yang dihasilkan harus memiliki mutu sesuai dengan persyaratan.
d. Simplisia pada proses pembuatan memerlukan air
Pati, talk, dan sebagainya pada proses pembuatannya memerlukan air. Air yang digunakan harus bebas dari pencemaran racun serangga, kuman patogen, logam berat, dan lain-lain (Anonim, 1985).
3. Tahapan pembuatan
a. Pengumpulan bahan baku
Kadar senyawa aktif dalam suatu simplisia berbeda-beda antara lain tergantung pada bagian tanaman yang digunakan, umur tanaman atau bagian tanaman pada saat panen, waktu panen, dan lingkungan tempat tumbuh.
b. Sortasi basah
Sortasi basah dilakukan untuk memisahkan kotoran-kotoran atau bahan-bahan asing lainnya dari simplisia. Misalnya, pada simplisia yang dibuat dari akar suatu tanaman obat, bahan-bahan asing seperti tanah, kerikil, rumput, batang, daun, akar yang telah rusak, serta pengotor lainnya yang harus dibuang.
c. Pencucian
Pencucian dilakukan untuk menghilangkan tanah dan pengotor lainnya yang melekat pada bahan simplisia. Pencucian dilakukan dengan air bersih, misalnya air dari mata air, air sumur atau air PAM. Bahan simplisia yang mengandung zat yang mudah larut dalam air yang mengalir, pencucian agar dilakukan dalam waktu yang sesingkat mungkin.
d. Perajangan
Beberapa jenis bahan simplisia perlu mengalami proses perajangan. Perajangan bahan simplisia dilakukan untuk mempermudah proses pengeringan, pengepakan, dan penggilingan.
e. Pengeringan
mutu atau perusakan simplisia. Suhu pengeringan tergantung pada bahan simplisia
dan cara pengeringannya. Bahan simplisia dapat dikeringkan pada suhu 300 C-900C, tetapi suhu yang terbaik adalah tidak melebihi 600C. Bahan simplisia
yang mengandung senyawa aktif yang tidak tahan panas atau mudah menguap harus dikeringkan pada suhu serendah mungkin, misalnya 300 C-450 C.
f. Sortasi kering
Sortasi setelah pengeringan sebenarnya merupakan tahap akhir pembuatan simplisia. Tujuan sortasi ialah untuk memisahkan benda-benda asing seperti bagian-bagian tanaman yang tidak diinginkan dan pengotor-pengotor lain yang masih tertinggal pada simplisia kering. Proses ini dilakukan sebelum simplisia dibungkus untuk kemudian disimpan.
g. Pengepakan dan penyimpanan
Simplisia dapat rusak atau berubah mutunya karena berbagai faktor luar dan dalam, antara lain :
1) Cahaya
Sinar dari panjang gelombang tertentu dapat menimbulkan perubahan kimia pada simplisia, misalnya isomerasi, polimerasi, raseminasi, dan sebagainya.
2) Oksigen
3) Reaksi kimia intern
Perubahan kimiawi dalam simplisia yang dapat disebabkan oleh reaksi kimia intern, misalnya enzim, polimerasi, oto-oksidasi, dan sebagainya.
4) Dehidrasi
Apabila kelembaban luar lebih rendah dari simplisia maka simplisia secara perlahan-lahan akan kehilangan sebagian airnya sehingga semakin lama semakin kecil atau kisut.
5) Penyerapan air
Simplisia yang higroskopis, misalnya agar-agar, bila disimpan dalam wadah yang terbuka akan menyerap langsung udara sehingga menjadi kempal, basah atau mencair (lumer).
6) Pengotoran
Pengotoran pada simplisia dapat disebabkan oleh berbagai sumber, misalnya debu atau pasir, ekskresi hewan, bahan-bahan asing (misalnya minyak yang tertumpah), dan fragmen wadah (karung goni).
7) Serangga
C. Ekstrak 1. Definisi ekstrak
Ekstrak adalah sediaan kering, kental, atau cair yang diperoleh dengan mengekstraksi senyawa aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian sehingga memenuhi standar baku yang telah ditetapkan (Anonim, 2000).
2. Pengelompokan ekstrak
Berdasarkan sifat-sifatnya, ekstrak dapat dikelompokkan menjadi : (a) Ekstrak cair (extractum fluidum) adalah ekstrak yang memiliki konsistensi cair dan mudah dituang.
(b) Ekstrak encer (extractum tenue) adalah ekstrak yang memiliki konsistensi madu dan mudah dituang.
(c) Ekstrak kental (extractum spissum) adalah ekstrak yang memiliki konsistensi liat dalam keadaan dingin, tidak dapat dituang dengan kandungan air mencapai 30%.
(d) Ekstrak kering (extractum siccum) adalah ekstrak yang memiliki konsistensi kering dan mudah digosokkan dengan kandungan lembab tidak lebih dari 5% (Voight, 1994).
3. Metode ekstraksi
karbohidrat, protein, dan lain-lain (Anonim, 1986). Proses penyarian (ekstraksi) secara umum dapat dibedakan menjadi maserasi, infundasi, perkolasi, destilasi uap, dan sering terdapat modifikasi.
a. Maserasi
Maserasi merupakan cara penyarian yang sederhana, dilakukan dengan cara merendam serbuk simplisia atau bahan dalam cairan penyari. Cairan penyari akan menembus dinding sel dan masuk ke dalam rongga sel yang mengandung zat aktif, zat aktif akan larut dan karena adanya perbedaan konsentrasi antara larutan
zat aktif di dalam sel dengan di luar sel, maka larutan yang terpekat didesak ke luar. Peristiwa tersebut berulang sehingga terjadi keseimbangan konsentrasi
antara larutan di luar sel dan di dalam sel.
Maserasi digunakan untuk penyarian simplisia yang mangandung zat aktif yang mudah larut dalam cairan penyari. Cairan penyari yang digunakan dapat berupa air, etanol, air-etanol. Keuntungan dengan cara penyarian ini adalah peralatan yang digunakan sederhana dan cara pengerjaannya mudah dilakukan.
b. Perkolasi
penyari dialirkan hingga di atas permukaan massa masih terdapat lapisan cairan penyari. Setelah 24 jam, keran dibuka dan diatur hingga kecepatan penetesan adalah 1,0 ml per menit. Akhir proses perkolasi ditentukan dengan pemeriksaan secara kualitatif pada perkolat terakhir.
c. Infundasi
Infundasi merupakan proses penyarian yang umumnya digunakan untuk menyari kandungan kimia yang larut dalam air dari bahan-bahan nabati. Sari yang diperoleh dengan cara ini tidak boleh disimpan lebih dari 24 jam karena penyarian dengan cara ini menghasilkan sari yang tidak stabil dan mudah tercemar oleh kuman dan kapang. Infundasi dibuat dengan cara menyari simplisia dengan air pada suhu 90oC selama 15 menit.
d. Penyari berkesinambungan
Proses ini merupakan gabungan antara proses untuk menghasilkan ekstrak cair dan proses penguapan. Pada penyarian ini, cairan penyari dipanaskan hingga mendidih, kemudian uap penyari akan naik ke atas kemudian akan mengembun karena didinginkan oleh pendingin balik. Embun akan turun melalui serbuk simplisia sambil melarutkan zat aktif serbuk simplisia (Anonim, 1986). 4. Penguapan
kecepatan penguapan tergantung pada kecepatan pemindahan panas (Anonim, 1986).
Pengentalan dapat dilakukan melalui penguapan dengan alat
Vacuum Rotary Evaporator di mana ekstrak cair dapat diubah menjadi bentuk
ekstrak kental, yang konsistensinya liat dan kandungan air yang lebih rendah dibandingkan dengan ekstrak cair (Voigt, 1994).
Pada Vacuum Rotary Evaporator, putaran labu dalam sebuah pemanas pada temperatur dan kecepatan putar tertentu, cairan yang terkandung dalam ekstrak akan diuapkan. Melalui pengaturan dalamnya pencelupan ke dalam penangas air, suhu penangas, hampa udara, dan suhu pendingin maka kondisi optimal dapat terpenuhi sehingga proses pengentalan ekstrak dapat berlangsung cepat dan dalam temperatur yang tidak terlalu tinggi (Voigt, 1994).
D. Standarisasi
Standarisasi, yaitu suatu proses pemenuhan persyaratan sebagai bahan baku agar dapat digunakan sesuai dengan standar yang telah ditetapkan. Pada proses standarisasi dilakukan pengukuran parameter untuk mendapatkan mutu yang seragam dan terulang (Anonim, 2000).
Langkah-langkah dalam proses standarisasi adalah : 1. Pembakuan simplisia
Pembakuan simplisia merupakan titik awal yang penting bagi pembakuan obat tradisional secara keseluruhan karena obat tradisional yang bermutu hanya akan dapat diperoleh bila simplisia yang menjadi bahan bakunya juga bermutu. Agar simplisia yang digunakan mempunyai mutu standar, industri obat tradisional disarankan dan didorong untuk melakukan budidaya dan mengembangkan sendiri tanaman sumber simplisia spesifikasi masing-masing industri dengan mutu standar yang relatif homogen (Anonim, 2000).
2. Pembakuan ekstrak
Pembakuan ekstrak sebagai bahan baku obat tradisional juga penting
dilakukan untuk menghasilkan produk obat tradisional yang bermutu (Anonim, 2000).
Pada pembakuan ekstrak sebagai bahan dasar sediaan obat tradisional dilakukan dengan berpedoman pada Parameter Standar Umum Ekstrak Tumbuhan Obat (Anonim, 2000).
Penentuan parameter standar yang dapat dilakukan antara lain : a. Parameter kadar air
dilakukan dengan cara yang tepat sesuai dengan kondisi ekstrak. Beberapa cara yang dapat dilakukan, yaitu titrasi, destilasi atau gravimetri (Anonim, 2000).
b. Parameter kadar abu
Tujuan penetapan kadar abu adalah memberikan gambaran kandungan mineral internal dan eksternal yang berasal dari proses awal sampai terbentuknya ekstrak. Nilai maksimal atau rentang kadar abu yang diperbolehkan terkait secara
langsung dengan kemurnian dan kontaminasi pada bahan atau ekstrak (Anonim, 2000). Abu yang dihasilkan harus memenuhi bobot tetap atau konstan.
Bobot tetap dimaksudkan bahwa dua kali penimbangan berturut-turut berbeda tidak lebih dari 0,5 mg tiap g sisa yang ditimbang. Penimbangan dilakukan setelah zat dikeringkan lagi selama 1 jam (Anonim, 1995).
c. Parameter identitas ekstrak
Tujuan dilakukan identitas ekstrak adalah untuk memberikan identitas objektif dari nama sampai senyawa spesifik yang terkandung dalam ekstrak yang dapat digunakan sebagai senyawa identitas. Parameter identitas ekstrak ditetapkan dengan melakukan deskripsi tata nama ekstrak yang digunakan sebagai bahan baku sediaan obat tersebut (Anonim, 2000).
d. Parameter organoleptik ekstrak
3. Pembakuan sediaan obat tradisional
Obat tradisional terbuat dari bahan alami. Pada formula obat tradisional yang sama dapat digunakan untuk pengobatan berbagai macam penyakit yang berbeda oleh satu daerah dengan daerah yang lain. Hal ini terjadi karena dalam satu tanaman terdapat kemungkinan berbagai kandungan kimia yang mempunyai
khasiat yang berbeda, sehingga dapat dipakai untuk berbagai indikasi (Anonim, 2000).
Tanaman yang ditanam pada kondisi lingkungan yang berbeda, dapat menyebabkan kadar kandungan kimia yang berbeda-beda dan keamanan serta khasiat juga dapat berbeda. Untuk tercapainya keinginan memasukkan obat tradisional dalam pelayanan kesehatan formal, maka perlu dilakukan pembakuan sediaan obat tradisional agar terjamin mutu dan keamanannya, serta sediaan obat tradisional yang memenuhi standar yang berlaku (Anonim, 2000).
E. Kromatografi Lapis Tipis (KLT)
melalui media, hingga terpisah dari zat terlarut lainnya, yang terelusi lebih awal atau lebih akhir. Umumnya zat terlarut dibawa melewati media pemisah oleh aliran suatu pelarut berbentuk cairan atau gas yang disebut eluen. Fase diam dapat bertindak sebagai zat penyerap, seperti halnya penyerap alumina yang diaktifkan seperti silika gel (Anonim, 1995).
Kromatografi lapis tipis sering digunakan karena cara pelaksanaannya sederhana, pemisahannya lebih cepat, dapat memisahkan dalam jumlah relatif kecil sampai beberapa mikrogram dan untuk campuran terdiri dari beberapa komponen dengan cepat dapat dipisahkan. Memisahkan komponen-komponen yang ada dapat digunakan bermacam-macam pelarut dari polar sampai non polar, misalnya air, metanol, etanol, aseton, etil asetat, dietil eter, kloroform, benzena, karbon tetraklorida, sikloheksana, hepatana, n-heksana, atau beberapa campurannya (Stahl, 1969).
Metode kromatografi lapis tipis dapat digunakan untuk analisis baik yang bersifat kualitatif maupun kuantitatif. Dasar analisis yang bersifat kualitatif adalah dengan membandingkan/mengukur jarak Rf (flow rate) dan warna bercak dengan zat baku. Harga Rf ini dipengaruhi oleh beberapa faktor, seperti: tebal lapisan, kejenuhan bejana, kelembaban udara, fase gerak, bahan penyerap, dan suhu (Sastroamidjojo, 1985).
Rf = Jarak yang ditempuh oleh zat Jarak yang ditempuh oleh pelarut
untuk memperkirakan kadar. Penetapan kadar yang diteliti dapat dilakukan dengan cara densitometri (Anonim, 1995).
Untuk analisis kuantitatif dapat dilakukan dengan dua cara yaitu secara langsung dengan membandingkan luas bercak dan kerapatan noda sampel yang telah di-klt dengan densitometri. Dengan cara ini kadar zat ditetapkan dengan mengukur luas dan intensitas bercak yang dibandingkan dengan zat pembandingnya. Cara yang kedua adalah secara tidak langsung, yaitu mengambil bercak pada pelat, kemudian disari dengan penyari yang cocok dan selanjutnya ditetapkan dengan metode spektrofotometri (Stahl, 1969).
F. KLT-Densitometri
KLT-densitometri merupakan salah satu metode analisa KLT kuantitatif yang dilakukan dengan cara mengukur kerapatan bercak senyawa uji yang terlebih dahulu dipisahkan dengan cara KLT, dibandingkan dengan kerapatan bercak senyawa standar yang dielusi bersama-sama (Hardjono, 1985).
Teknik pengukuran dapat didasarkan atas pengukuran intensitas sinar yang diserap (absorbansi), intensitas sinar yang dipantulkan (reflaktansi) atau intensitas sinar yang difluoresensikan (fluoresensi). Teknik pengukuran berdasarkan refleksi di mana sinar datang sebagian diserap dan sebagian lagi dipantulkan. Banyaknya sinar yang diserap sebanding dengan jumlah zat pada bercak yang terkena sinar tersebut (Mintarsih, 1990).
dielusi bersama dalam satu lempeng, kemudian AUC (luas daerah di bawah kurva) sampel dibandingkan dengan harga AUC zat baku. Yang kedua, dengan membuat kurva baku hubungan antara jumlah zat baku dengan AUC. Kurva baku diperoleh dengan membuat totolan zat baku pada pelat KLT dengan bermacam-macam konsentrasi (minimal tiga bermacam-macam konsentrasi). Bercak yang diperoleh dicari AUC nya dengan alat densitometer. Dari kurva baku diperoleh persamaan y = bx + a, dimana x adalah banyaknya zat yang ditotolkan dan y adalah AUC (Supardjan, 1987).
G. Keterangan Empiris
25
A. Jenis dan Rancangan Penelitian 1. Jenis Penelitian
Penelitian ini merupakan jenis penelitian noneksperimental, karena tidak ada perlakuan terhadap subjek uji.
2. Rancangan Penelitian
Penelitian dilakukan melalui beberapa tahap sebagai berikut. a. Determinasi tanaman
b. Pengumpulan bahan
c. Pembuatan serbuk daun teh hijau d. Pembuatan ekstrak kental e. Uji organoleptik ekstrak f. Identitas ekstrak
g. Penetapan kadar air h. Penetapan kadar abu
i. Penetapan kadar abu yang tidak larut asam j. Penetapan kadar abu larut air
k. Penetapan kadar sari larut air l. Penetapan kadar sari larut etanol
B. Definisi Operasional
Definisi operasional yang digunakan dalam penelitian ini adalah :
1. Karakterisasi ekstrak adalah pengukuran ciri-ciri spesifik dan non-spesifik dari ekstrak etanolik daun teh hijau mengikuti parameter standar umum ekstrak tumbuhan obat yang ditetapkan oleh Badan Pengawas Obat dan Makanan meliputi uji organoleptik ekstrak, identitas ekstrak, kadar air, kadar abu, kadar abu tidak larut asam, kadar abu larut air, kadar sari larut air, kadar sari larut etanol, dan penentuan senyawa identitas secara kualitatif dan kuantitatif. 2. Ekstrak etanolik daun teh hijau adalah ekstrak yang dibuat dari serbuk daun
teh hijau secara maserasi dengan penyari etanol 70 %.
3. Penentuan senyawa identitas secara kualitatif dan kuantitatif adalah menentukan ada tidaknya senyawa identitas epigallokatekin galat yang ada pada ekstrak etanolik daun teh hijau menggunakan metode kromatografi lapis tipis dan mengukur kadar senyawa identitas yang terkandung didalamnya menggunakan metode KLT-densitometri.
C. Alat
Alat-alat yang digunakan dalam penelitian ini adalah sebagai berikut.
Vacuum rotary evaporator (Janke & Kunkel Ika Labortechnik), oven (Memmert), timbangan analitik (Model AB-204, Mettler Toledo), eksikator, pemijar (Carbolite), krus platina, penjepit, hot plate (Heidolph MR 2002), penangas air,
vacuum (Robinair High Vacuum Pump Model 15110 seri 11026), corong
D. Bahan
Bahan yang digunakan adalah daun teh dari daerah Boyolali. Bahan kimia yang digunakan meliputi asam klorida p.a (Merck), kloroform p.a (Merck), toluen p.a (Merck), aseton p.a (Merck), asam asetat glasial p.a (Merck), asam formiat p.a (Merck), metanol p.a (Merck), petroleum eter p.a (Merck), etanol p.a
(Merck), besi (III) klorida heksahidrat P, aquades dan kertas saring bebas abu dari laboratorium Farmakognosi Fitokimia Universitas Sanata Dharma Yogyakarta. Sedangkan standar senyawa identitas epigallokatekin galat berasal dari pabrik Sigma-Aldrich.
E. Jalannya Penelitian 1. Determinasi tanaman
Determinasi tanaman teh dilakukan untuk memastikan kebenaran tanaman teh yang digunakan. Determinasi tanaman teh dilakukan di Laboratorium Farmakognosi Fitokimia Universitas Sanata Dharma Yogyakarta dengan menggunakan buku acuan (Backer dan Bakhuizen van den Brink, 1963).
2. Pengumpulan bahan
Pucuk dan daun tanaman teh diambil dari pohon yang sama pada waktu pagi hari, di perkebunan teh di daerah Boyolali, Jawa Tengah pada bulan Juni 2009.
3. Pembuatan serbuk daun teh hijau
serbuk daun teh hijau. Selanjutnya, serbuk daun teh hijau diayak dengan pengayak dengan nomor mesh 12/50.
4. Pembuatan ekstrak kental
Ekstrak dibuat dengan cara maserasi menggunakan etanol 70 %. Sebanyak 15,0 g serbuk daun teh hijau dimasukkan ke dalam erlenmeyer dan ditambah 150,0 ml etanol 70 %, serbuk daun teh hijau dimaserasi selama 6 jam dan kemudian didiamkan selama 18 jam. Maserat dipisahkan dan proses diulangi dua kali dengan jenis dan jumlah pelarut yang sama. Semua maserat dikumpulkan dan diuapkan dengan penguap vakum hingga diperoleh ekstrak kental. Rendemen yang diperoleh ditimbang dan dicatat.
5. Uji organoleptik ekstrak
Dilakukan dengan penggunaan pancaindera, dideskripsikan bentuk, warna, bau, dan rasa dari ekstrak.
6. Identitas ekstrak
Dilakukan dengan study literatur meliputi deskripsi tata nama ekstrak dan senyawa identitas ekstrak.
7. Penetapan kadar air
8. Penetapan kadar abu
Sebanyak 2,0 g ekstrak kental yang telah ditimbang seksama dimasukkan dalam krus platina yang telah dipijarkan dan ditara, kemudian diratakan. Dipijarkan perlahan-lahan hingga arang habis, didinginkan, dan ditimbang. Jika dengan cara ini arang tidak dapat dihilangkan, maka ditambahkan air panas, disaring melalui kertas saring bebas abu. Dipijarkan sisa dalam krus yang sama, diuapkan, dipijarkan hingga bobot tetap, ditimbang. Dihitung kadar abu terhadap bahan yang dikeringkan di udara.
9. Penetapan kadar abu tidak larut asam
Abu yang diperoleh pada penetapan kadar abu, dididihkan dengan 25,0 ml asam klorida encer P selama 5 menit, bagian yang tidak larut dalam asam
dikumpulkan, disaring melalui kertas saring bebas abu, kemudian dicuci dengan air panas dan dipijarkan hingga bobot tetap, ditimbang. Dihitung kadar abu yang tidak larut dalam asam terhadap bahan yang telah dikeringkan di udara.
10. Penetapan kadar abu larut air
Abu yang diperoleh pada penetapan kadar abu, dididihkan dengan 25,0 ml air selama 5 menit, bagian yang tidak larut dalam air dikumpulkan,
11. Penetapan kadar sari larut air
Maserasi selama 24 jam, 2,0 g ekstrak kental dengan 40,0 ml air kloroform P, menggunakan labu bersumbat sambil berkali-kali dikocok
selama 6 jam pertama dan kemudian dibiarkan selama 18 jam. Saring, uapkan sebanyak 30,0 ml filtrat hingga kering dalam cawan porselin berdasar rata yang telah ditara, panaskan sisa pada suhu 1050C hingga bobot tetap. Hitung kadar dalam persen sari yang larut dalam air kloroform, dihitung terhadap bahan yang telah dikeringkan di udara.
12. Penetapan kadar sari larut etanol
Maserasi selama 24 jam, 2,0 g ekstrak kental dengan 40,0 ml etanol 95%, menggunakan labu bersumbat sambil berkali-kali dikocok selama 6 jam pertama dan kemudian dibiarkan selama 18 jam. Saring cepat dengan menghindarkan penguapan etanol (95%), uapkan 30,0 ml filtrat hingga kering dalam cawan porselin berdasar rata yang telah ditara, panaskan sisa pada suhu 1050C hingga bobot tetap. Hitung kadar dalam persen sari yang larut dalam etanol (95%), dihitung terhadap bahan yang telah dikeringkan di udara.
13. Penentuan senyawa identitas secara kualitatif dan kuantitatif
Penentuan senyawa identitas dilakukan secara analisa kualitatif dan kuantitatif. Analisa kualitatif dilakukan dengan metode KLT sedangkan analisa kuantitatif dilakukan dengan penetapan kadar senyawa identitas ekstrak etanolik
Analisis kualitatif dilakukan dengan cara : a. Preparasi standar
Sebanyak 5,0 mg standar epigallokatekin galat dilarutkan dalam 10,0 ml etanol 70 %. Seri larutan standar ditotolkan sebanyak 5,0; 10,0; 15,0;
20,0; 25,0 μl.
b. Preparasi sampel
Sebanyak 200,0 mg ekstrak etanolik daun teh hijau disari dengan petroleum eter 5,0 ml pada suhu 50°C selama 5 menit. Fraksi petroleum eter disingkirkan, kemudian sisanya disari dengan kloroform-asam asetat (99:1) 5,0 ml pada suhu 50°C selama 5 menit. Fraksi kloroform-asam asetat disingkirkan, Kemudian sisanya disari dengan metanol-kloroform-asam asetat (49,5:49,5:1) 5,0 ml pada suhu 50°C selama 5 menit. Fraksi metanol-kloroform-asam asetat kemudian dapat langsung ditotolkan. Larutan sampel ekstrak etanolik daun teh hijau ditotolkan sebanyak 10,0 μl dan dilakukan replikasi tiga kali.
c. Uji kualitatif
Fase diam : silika gel GF254
Fase gerak : toluen-aseton-asam formiat (9 : 9 : 2) Deteksi : UV 254 nm dan UV 365 nm
Larutan besi (III) klorida
a. Penentuan panjang gelombang maksimum
Panjang gelombang maksimum diperoleh dengan cara menelusuri bercak pada panjang gelombang 250 nm sampai 320 nm, sesuai dengan panjang gelombang teoritis senyawa identitas. Panjang gelombang maksimum dicapai pada saat terjadi serapan maksimum yang ditunjukkan dengan terbentuknya puncak kurva.
b. Pembuatan kurva baku
Standar senyawa identitas ditimbang sebanyak 5,0 mg, kemudian dilarutkan dalam 10,0 ml etanol 70 %. Larutan tersebut ditotolkan pada pelat fase diam yang sesuai sebanyak 5,0; 10,0; 15,0; 20,0; 25,0 μl menggunakan pipet mikroliter dan dikembangkan dalam fase gerak yang sesuai. Kemudian dilakukan pengukuran dengan CAMAG TLC Scanner 3 sehingga diperoleh data AUC.
Berdasarkan data AUC dihitung secara regresi linier sehingga diperoleh nilai a,b, r. Nilai a, b, r tersebut kemudian dimasukkan ke dalam persamaan y = bx + a,
dimana a adalah koefisien regresi dan b adalah tetapan regresi, sedangkan x adalah konsentrasi zat yang ingin diketahui.
c. Penetapan kadar sampel secara KLT-densitometri
Sampel yang akan diukur dengan alat densitometer terlebih dahulu dipisahkan menggunakan metode kromatografi lapis tipis.
Fase diam : silika gel GF254
Fase gerak : toluena-aseton-asam formiat (9 : 9 : 2)
disingkirkan, kemudian sisanya disari dengan kloroform-asam asetat (99:1) 5,0 ml pada suhu 50°C selama 5 menit. Fraksi kloroform-asam asetat disingkirkan, Kemudian sisanya disari dengan metanol-kloroform-asam asetat (49,5:49,5:1) 5,0 ml pada suhu 50°C selama 5 menit. Fraksi metanol-kloroform-asam asetat kemudian dapat langsung ditotolkan. Larutan sampel ekstrak etanolik daun teh hijau ditotolkan sebanyak 10,0 μl dan dilakukan replikasi tiga kali.
Konsentrasi sampel yang telah dielusi diukur kerapatan bercaknya dengan KLT-densitometri sehingga didapatkan data AUC dari bercak yang ditotolkan. Penelusuran bercak untuk menetapkan kadar dilakukan pada panjang gelombang maksimum. Kadar masing-masing sampel dihitung menggunakan persamaan kurva baku, sehingga diperoleh harga x (konsentrasi sampel).
F. Analisis Hasil
34
A. Determinasi Tanaman
Determinasi tanaman dilakukan untuk memastikan kebenaran tanaman teh sehingga dapat menghindari kesalahan pemilihan bahan tanaman yang digunakan dalam penelitian. Determinasi dilakukan di Laboratorium Farmakognosi Fitokimia Universitas Sanata Dharma Yogyakarta, dengan menggunakan kunci-kunci determinasi yang terdapat dalam buku acuan (Backer dan Bakhuizen van den Brink, 1963).
Berdasarkan hasil determinasi, tanaman yang digunakan dalam penelitian ini adalah benar-benar tanaman teh dengan nama ilmiah Camellia sinensis (L).O.K (Lampiran 1).
B. Pengumpulan Bahan dan Pembuatan Serbuk
Tanaman yang digunakan dalam penelitian ini adalah teh yang diperoleh dari perkebunan teh di daerah Boyolali, Jawa Tengah pada bulan Juni 2009. Tanaman teh diambil pada bulan Juni, yaitu pada musim kemarau karena sinar
matahari sangat berpengaruh terhadap pertumbuhan tanaman teh. Semakin banyak sinar matahari maka pertumbuhan tanaman teh makin cepat dan
yang masih muda. Pengambilan kuncup dan daun teh dilakukan pada pagi hari agar kuncup dan daun teh yang diambil masih segar dan kandungan senyawa aktifnya masih banyak. Setelah daun dikumpulkan selanjutnya dipisahkan dari kotoran-kotoran yang melekat atau bahan-bahan asing lainnya yang tidak diperlukan. Kotoran-kotoran atau bahan-bahan asing yang dimaksud adalah tanah, batang, debu yang menempel, kerikil, dan akar. Kemudian daun teh dicuci dengan air bersih dan mengalir. Pencucian dilakukan untuk menghilangkan tanah dan pengotor lainnya yang melekat pada daun teh. Tahap selanjutnya, daun dikeringkan ke dalam oven. Pengeringan dilakukan pada suhu 45oC bertujuan untuk mengurangi kadar air dan menghentikan reaksi enzimatik dalam daun teh. Pengeringan dilakukan sampai daun mudah hancur dengan diremas. Setelah dilakukan pengeringan, dilanjutkan dengan sortasi kering. Sortasi kering bertujuan untuk memisahkan benda-benda asing, seperti bagian-bagian tanaman yang tidak diinginkan dan pengotor-pengotor lain yang masih tertinggal pada simplisia kering. Kemudian, daun diserbuk menggunakan blender Retsch sehingga dihasilkan serbuk kering daun teh hijau.
dengan partikel-partikel halus tadi. Selain itu, dinding sel merupakan suatu saringan, sehingga zat yang tidak dapat larut akan tetap berada di dalam sel. Oleh karena itu, penyerbukan yang terlalu halus akan menyebabkan banyak dinding sel yang pecah, sehingga zat yang tidak diinginkan dapat ikut ke dalam hasil penyarian (Anonim, 1986).
maksimal. Selain itu, untuk memperoleh ukuran partikel serbuk yang lebih kecil dan seragam sehingga luas permukaan kontak dengan pelarut semakin besar. Hal ini dimaksudkan agar dalam proses ekstraksi kandungan senyawa aktif yang terlarut semakin banyak. Setelah proses pengayakan, dilakukan pengepakan dan penyimpanan yang bertujuan untuk mencegah berkurangnya mutu dari serbuk daun teh hijau. Selama penyimpanan kemungkinan terjadi kerusakan pada serbuk daun teh hijau yang dapat disebabkan oleh air dan kelembaban sehingga penyimpanan bahan sebaiknya dalam keadaan kering. Selain itu, penyimpanan harus dalam wadah tertutup rapat yang bertujuan untuk melindungi sebuk terhadap masuknya kontaminan dan mencegah kehilangan bahan selama penanganan dan penyimpanan. Oleh karena itu, pengepakan dan penyimpanan serbuk daun teh hijau dilakukan dengan cara memasukkan serbuk ke dalam plastik yang bersih dan disimpan dalam toples yang tertutup rapat.
C. Pembuatan Ekstrak Kental
Dalam proses maserasi, cairan penyari akan menembus dinding sel dan masuk ke dalam rongga sel yang mengandung zat dimana zat akan larut dan karena
adanya perbedaan konsentrasi antara larutan zat di dalam sel dengan di luar sel, maka larutan yang terpekat didesak ke luar. Penelitian ini menggunakan maserasi karena metode ekstraksi dengan maserasi digunakan untuk menyari simplisia yang mempunyai kandungan senyawa aktif yang tinggi, cara pengerjaannya mudah dilakukan, dan peralatan yang digunakan sederhana. Maserat yang dihasilkan dalam proses maserasi berupa ekstrak cair. Ekstrak cair, kemudian dikentalkan menggunakan vacuum rotary evaporator. Pengentalan bertujuan untuk menguapkan pelarut etanol dan menghilangkan kandungan air yang tersisa dalam ekstrak. Penguapan larutan pengekstraksi dengan menggunakan vacuum rotary
evaporator berlangsung cepat dan dapat menjaga stabilitas senyawa yang
dihasilkan karena tekanan dan suhu diatur tidak terlalu tinggi. Kemudian ekstrak di oven pada suhu 45oC dan diperoleh ekstrak kental dengan konsistensi yang liat.
(a) (b) Gambar 3. Ekstrak kental (a) dan ekstrak cair (b) daun teh hijau
dituang. Rendemen ekstrak kental etanolik daun teh hijau yang diperoleh dalam penelitian adalah 24,74 % b/b.
D. Organoleptik Ekstrak
Uji organoleptik ekstrak bertujuan untuk pengenalan awal secara sederhana dan bersifat subyektif. Penilaian bersifat subyektif karena hasil penilaian sangat ditentukan oleh pelaku atau yang melakukan pengukuran. Uji organoleptik ini dapat digunakan untuk mengenal secara sederhana ekstrak yang digunakan pada penelitian, sehingga tidak terjadi kesalahan dalam pemilihan ekstrak yang digunakan sebagai bahan dasar pembuatan obat tradisional.
Uji organoleptik ekstrak dilakukan dengan menggunakan pancaindera untuk mendeskripsikan bentuk, warna, bau, dan rasa dari ekstrak tersebut. Dari hasil uji organoleptik ekstrak kental diperoleh bentuk kental, berwarna cokelat kehitaman, tidak berbau, dan rasa agak kelat. Demikian juga dengan ekstrak cair dengan bentuk cair, berwarna cokelat kehitaman, tidak berbau, dan rasa agak kelat. Hasil uji organoleptik yang diperoleh dalam penelitian tidak dibandingkan dengan standar karena belum ditemukan referensi mengenai organoleptik untuk ekstrak kental etanolik daun teh hijau
E. Identitas Ekstrak 1. Deskripsi tata nama
Nama ekstrak : Camellia Folium Extractum
Nama latin tanaman : Camellia sinensis L. Bagian tanaman yang digunakan : Daun
2. Senyawa identitas ekstrak : Epigallocatechin gallate
Penentuan identitas ekstrak bertujuan untuk mendapatkan identitas obyektif dan spesifik dari senyawa identitas yang terkandung dalam ekstrak. Identitas ekstrak tersebut sangat diperlukan sehingga kita dapat dengan mudah membedakan ekstrak tanaman yang satu dengan yang lain (suatu ekstrak dapat mengandung senyawa identitas dari tanaman penyusunnya). Karakterisasi ekstrak etanolik daun teh hijau dapat dilakukan dengan menetapkan senyawa identitas yang merupakan senyawa tunggal atau kelompok kelas senyawa dalam tanaman obat dan dipakai sebagai acuan kontrol kuantitatif tanpa memperhatikan apakah senyawa atau kelompok senyawa tersebut memiliki aktivitas terapi atau tidak. Secara umum suatu senyawa atau sekelompok senyawa dapat menjadi senyawa identitas bahan tumbuhan obat jika senyawa tersebut stabil, dapat diidentifikasi dan dianalisa secara kuantitatif, serta unik untuk tanaman yang bersangkutan (Sinambela, 2002).
Teh hijau mengandung senyawa epigallokatekin galat yang merupakan senyawa golongan flavonoid. Epigallokatekin galat merupakan konstituen yang utama, memiliki sifat antioksidan tertinggi serta dapat diidentifikasi dan dianalisa secara kuantitatif. Oleh karena itu, epigallokatekin galat yang terkandung dalam ekstrak etanolik daun teh hijau dapat dijadikan sebagai senyawa identitas.
F. Penetapan Kadar Air
ekstrak tersebut. Penetapan kadar air ini berhubungan dengan kemurnian dan kontaminasi. Ekstrak kental yang mengandung kadar air dalam jumlah yang tinggi merupakan media tempat pertumbuhan mikroorganisme. Pada proses ekstraksi menggunakan pelarut etanol 70 % dimana merupakan pelarut dengan kombinasi etanol dan air. Air yang terkandung dalam ekstrak dapat menjadi tempat pertumbuhan mikroorganisme seperti kapang, khamir, dan bakteri.
Penetapan kadar air dilakukan dengan cara gravimetri, yaitu dengan menimbang selisih bobot ekstrak sebelum dan sesudah pengeringan. Pengeringan dilakukan dengan menggunakan oven pada suhu 105°C, yaitu suhu optimal untuk menguapkan air yang terkandung dalam ekstrak. Dari hasil percobaan, diperoleh kadar air ekstrak etanolik daun teh hijau sebesar 27,51 %b/b. Kadar air ekstrak etanolik daun teh hijau yang diperoleh sudah memenuhi syarat dimana kadar air untuk ekstrak kental maksimal 30 % (Voigt, 1994).
G. Penetapan Kadar Abu
kerusakan otak dan ginjal. Cadmium (Cd) dan Kromium (Cr) bersifat karsinogenik dan dalam jangka panjang dapat terakumulasi di hati, ginjal dan pankreas sehingga dapat menyebabkan kerusakan bagi organ tubuh manusia.
Penetapan kadar abu dilakukan dengan alat pemijar dan menggunakan pemijaran dengan temperatur yang tinggi. Pada proses pemijaran digunakan krus platina yang tahan terhadap pemijaran yang tinggi. Pemijaran dengan temperatur tinggi bertujuan mendestruksi senyawa organik yang mengandung karbon sehingga akan menguap dan tertinggal hanya bahan anorganik baik yang logam maupun non logam. Penimbangan dilakukan hingga bobot tetap dan dicapai apabila penimbangan krus dan abu sampai tidak terjadi lagi perbedaan bobot setelah dipanasi lebih lanjut dan selisih penimbangan tidak lebih dari 0,5 mg. Dari hasil penetapan kadar abu ekstrak etanolik daun teh hijau diperoleh gambaran bahwa kandungan bahan anorganik yang terdapat dalam ekstrak etanolik daun teh hijau adalah 2,22 %b/b. Hasil penetapan kadar abu yang diperoleh dalam penelitian ini tidak dibandingkan dengan standar kadar abu untuk ekstrak kental etanolik daun teh hijau karena belum ditemukan referensi mengenai standar kadar abu yang seharusnya diperbolehkan untuk ekstrak kental etanolik daun teh hijau.
H. Penetapan Kadar Abu Tidak Larut Asam
Penetapan kadar abu tidak larut asam dilakukan dengan mendidihkan ekstrak hasil penetapan kadar abu dengan asam klorida encer P yang bertujuan untuk melarutkan bahan anorganik logam yang terlarut dalam asam kuat, sehingga yang tersisa adalah bahan anorganik sisa yang tidak terlarut pada asam kuat yaitu bahan anorganik non logam. Dari hasil penetapan kadar abu tidak larut asam diperoleh gambaran bahwa kandungan bahan anorganik non logam yang terdapat dalam ekstrak etanolik daun teh hijau adalah 1,40 %b/b. Hasil penetapan kadar abu tidak larut asam yang diperoleh dalam penelitian ini tidak dibandingkan dengan standar kadar abu tidak larut asam untuk ekstrak kental etanolik daun teh hijau karena belum ditemukan referensi mengenai standar kadar abu tidak larut asam yang seharusnya diperbolehkan untuk ekstrak kental etanolik daun teh hijau.
I. Penetapan Kadar Abu Larut Air
Penetapan kadar abu larut air bertujuan untuk mengetahui seberapa banyak cemaran yang ada pada ekstrak yang larut dalam air. Ekstrak etanolik daun teh hijau dapat mengandung cemaran baik bahan anorganik logam maupun non logam. Bahan anorganik logam seperti Barium dan Timbal sedangkan non logam seperti silikat atau pasir. Bahan anorganik tersebut memiliki kelarutan rendah dalam air bahkan tidak larut air. Oleh karena itu, penetapan kadar abu larut air digunakan untuk mengetahui cemaran yang larut air.
gambaran bahwa cemaran yang larut air yang terdapat dalam ekstrak etanolik daun teh hijau adalah 0,87 %b/b. Hasil penetapan kadar abu larut air yang diperoleh dalam penelitian tidak dibandingkan dengan standar kadar abu larut air untuk ekstrak kental etanolik daun teh hijau karena belum ditemukan referensi mengenai standar kadar abu larut air untuk ekstrak kental etanolik daun teh hijau.
J. Penetapan Kadar Sari Larut Air
Penetapan kadar sari larut air bertujuan untuk mendapatkan gambaran banyaknya senyawa yang terkandung dalam ekstrak etanolik daun teh hijau yang dapat larut dalam pelarut air. Air yang digunakan adalah air kloroform. Kloroform ditambahkan dalam penyari untuk mencegah terjadinya pembusukan zat selama maserasi, karena air juga mengandung mikroba yang dapat menyebabkan busuk. Dalam penetapan kadar sari larut air, sejumlah ekstrak kental disari dengan pelarut air kloroform. Proses maserasi ini bertujuan agar senyawa dalam ekstrak terekstraksi ke dalam pelarut. Selanjutnya, maserat dipanaskan dengan menggunakan oven pada suhu 105oC bertujuan untuk menguapkan pelarut sehingga diperoleh senyawa dengan bobot tetap.
K. Penetapan Kadar Sari Larut Etanol
Penetapan kadar sari larut etanol bertujuan untuk mendapatkan gambaran banyaknya senyawa yang terkandung dalam ekstrak etanolik daun teh hijau yang dapat larut dalam pelarut etanol. Penelitian dilakukan dengan menyari sejumlah ekstrak kental dengan pelarut etanol 95% sehingga senyawa-senyawa yang tersari akan lebih banyak. Selanjutnya, maserat dipanaskan dengan menggunakan oven pada suhu 105oC bertujuan untuk menguapkan pelarut sehingga diperoleh senyawa dengan bobot tetap.
Dari hasil penetapan kadar sari larut air diperoleh gambaran bahwa senyawa yang terkandung dalam ekstrak etanolik daun teh hijau yang dapat larut dalam pelarut etanol adalah 42,98 %b/b. Hasil yang diperoleh dalam penelitian tidak dibandingkan dengan standar kadar sari larut etanol untuk ekstrak kental etanolik daun teh hijau karena belum ditemukan referensi mengenai standar kadar sari larut etanol untuk ekstrak kental etanolik daun teh hijau.
L. Penentuan Senyawa Identitas secara Kualitatif dan Kuantitatif 1. Penentuan senyawa identitas secara kualitatif
Penentuan senyawa identitas secara kualitatif bertujuan untuk mengetahui dan menentukan ada tidaknya senyawa spesifik dari ekstrak etanolik daun teh hijau serta membandingkan harga Rf (flow rate) dan warna bercak dengan zat baku. Senyawa spesifik yang terkandung dalam ekstrak etanolik daun teh hijau merupakan senyawa identitas dari ekstrak tersebut.
sederhana, pemisahannya lebih cepat, dan dapat memisahkan sampel dalam jumlah yang kecil (mikrosampel). Prinsip pemisahan dengan metode KLT adalah zat terlarut terdistribusi di antara dua fase, yaitu fase diam dan fase gerak. KLT merupakan kromatografi adsorbsi karena penerapan suatu senyawa pada kedua jenis fase yang berbeda. Fase geraknya berupa cairan, pada penelitian ini menggunakan komposisi toluen:aseton:asam formiat (9:9:2). Pengunaan fase gerak tersebut berdasarkan studi CAMAG mengenai Identification of Green Tea
(Anonim, 2005b). Sedangkan fase diamnya adalah silika gel GF254. Silika gel GF254 artinya silika tersebut mengandung gipsum/CaSO4 yang merupakan pengikat dan dapat berfluorosensi kehijauan pada panjang gelombang 254 nm.
dipisahkan sehingga akan mengganggu proses pemisahan. Selain itu, dengan adanya kandungan air dalam silika akan mempengaruhi kepolaran, yaitu silika yang memiliki sifat non polar dapat menjadi polar. Deteksi yang digunakan dalam penelitian ada dua, yaitu deteksi fisika dan kimia. Deteksi fisika menggunakan lampu UV dengan radiasi 254 nm (Gambar 4) dan 365 nm (Gambar 5), sedangkan deteksi kimia menggunakan larutan besi (III) klorida (Gambar 6).
Gambar 4. Kromatogram standar EGCG dan sampel ekstrak etanolik daun teh hijau dengan deteksi di bawah lampu UV 254 nm
Keterangan :
Fase diam : silika gel GF254
1,00
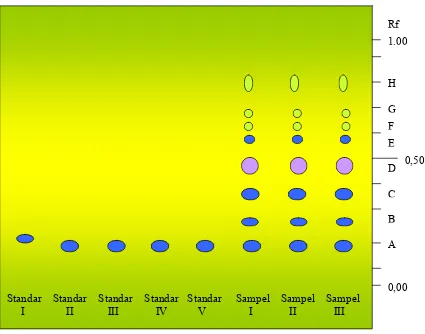
Gambar 5. Kromatogram standar EGCG dan sampel ekstrak etanolik daun teh hijau dengan deteksi di bawah lampu UV 365 nm
Keterangan :
Fase diam : silika gel GF254
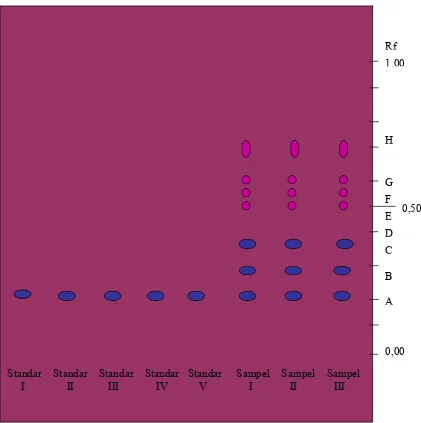
Gambar 6. Kromatogram standar EGCG dan sampel ekstrak etanolik daun teh hijau dengan deteksi larutan besi (III) klorida
Keterangan :
Fase diam : silika gel GF254
Fase gerak : toluena : aseton : asam formiat (9 : 9 : 2) Jarak pengembangan : 10 cm; jarak penotolan: 1,5 cm
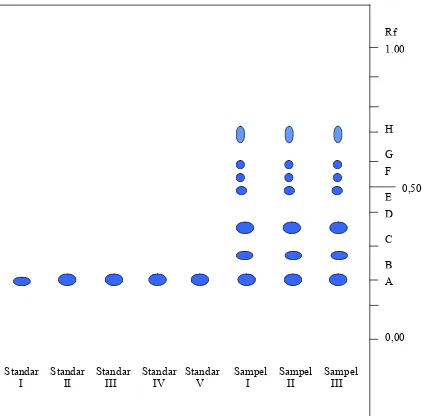
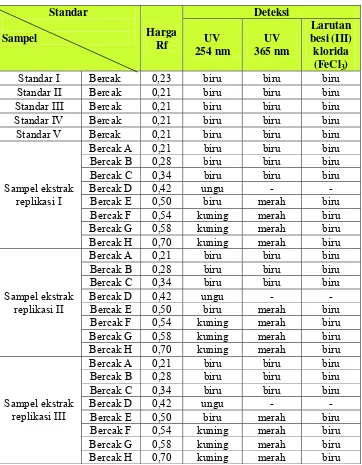
Analisis kualitatif yang digunakan dalam penelitian selain mengamati warna bercak adalah parameter Rf (flow rate). Rf merupakan perbandingan antara jarak rambat yang ditempuh oleh senyawa dengan jarak pengembangan. Nilai Rf dan warna bercak standar dan sampel yang diperoleh dalam penelitian (Tabel II).
Tabel II. Hasil KLT standar (epigallokatekin galat) dan sampel (ekstrak etanolik daun teh hijau)
Berdasarkan pada tabel II, nilai Rf dan warna bercak A pada sampel replikasi I, II, dan III mendekati/mirip nilai Rf dan warna bercak standar I, II, III, IV, dan V yang digunakan dalam penelitian. Ini berarti bahwa dalam ekstrak etanolik daun teh hijau mengandung senyawa epigalokatekin galat. Nilai Rf standar I lebih tinggi dibandingkan dengan keempat standar lainnya karena saat pengembangan terjadi perambatan fase gerak yang tidak merata (miring) sehingga standar I terelusi lebih dahulu. Hal ini dapat disebabkan karena penjenuhan chamber yang kurang optimal, peletakkan plat lempeng yang tidak rata (miring). Selain itu, pada proses elusi terjadi pengekoran baik pada standar maupun sampel. Hal ini dapat dikarenakan jumlah standar maupun sampel yang ditotolkan terlalu banyak atau totolan baik standar maupun sampel belum kering kemudian ditambah lagi jumlah cuplikannya.
2. Penentuan senyawa identitas secara kuantitatif
Pada penelitian ini, setelah menentukan senyawa identitas ekstrak etanolik daun teh hijau secara kualitatif, selanjutnya dilakukan penentuan senyawa identitas secara kuantitatif. Penentuan senyawa identitas secara kuantitatif bertujuan menetapkan dan mengukur kadar senyawa identitas yaitu senyawa epigallokatekin galat yang terdapat dalam ekstrak etanolik daun teh hijau.
Penentuan senyawa identitas secara kuantitatif menggunakan metode KLT-densitometri. Pada penentuan senyawa identitas secara kuantitatif, standar
dan sampel yang telah dipisahkan dengan cara KLT, kemudian diukur kadarnya
dengan menggunakan alat yang bernama CAMAG TLC Scanner 3.
bercak-bercak yang ada pada lempeng tipis atau lempeng tipisnya yang dapat digerakkan menyusuri berkas sinar yang berasal dari sumber sinar. Penelusuran bercak baik standar maupun sampel akan mendapatkan hasil yang baik apabila dilakukan pada panjang gelombang maksimum karena perubahan konsentrasi pada bercak sedikit saja sudah dapat terdeteksi. Panjang gelombang maksimum
(λmaks) merupakan panjang gelombang yang memberikan serapan maksimum.
Oleh karena itu, sebelum dilakukan pengukuran kadar baik pada standar maupun sampel adalah menentukan panjang gelombang maksimum. Panjang gelombang
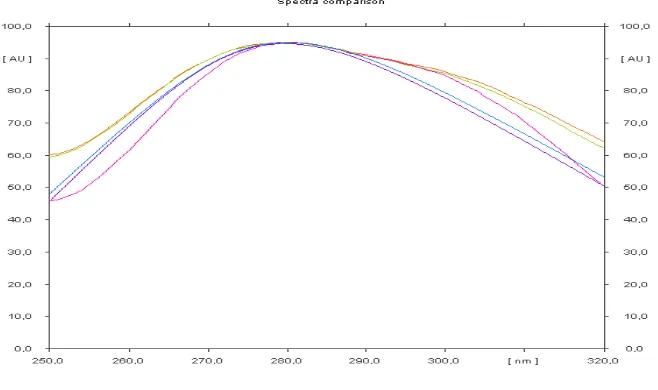
maksimum diperoleh dengan menelusuri bercak pada panjang gelombang 250-320 nm. Dari hasil penelitian diperoleh panjang gelombang maksimum
terletak pada 280 nm (Gambar 7). Berdasarkan Journal of Forestry Research, panjang gelombang maksimum epigallokatekin galat adalah 280 nm (Lei, 2006). Ini berarti bahwa panjang gelombang maksimum yang diperoleh pada penelitian telah sesuai dengan panjang gelombang maksimum berdasarkan teori.
Penelusuran bercak untuk analisis kuantitatif dengan densitometri dilakukan pada panjang gelombang 280 nm. Hasil dari penelusuran bercak tersebut adalah luas daerah di bawah kurva atau disebut juga AUC (Area Under
Curve). Persamaan kurva baku diperoleh dari hubungan kadar standar
epigallokatekin galat yang ditotolkan dengan luas daerah di bawah kurva (Tabel III). Pembuatan kurva baku ini bertujuan untuk mendapatkan persamaan
regresi linier yang selanjutnya digunakan untuk menghitung kadar epigallokatekin galat dalam sampel ekstrak etanolik daun teh hijau.
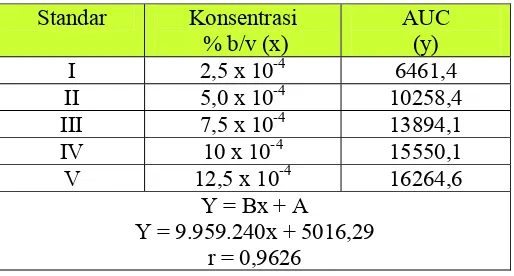
Tabel III. Persamaan kurva baku dari hubungan kadar standar epigallokatekin galat (x) dengan AUC (y)
Persamaan kurva baku yang diperoleh memiliki linearitas yang baik dapat dilihat dari nilai koefisien korelasi (r= 0,9626), menunjukkan bahwa metode analisis memberikan hasil yang linier di mana semakin bertambahnya konsentrasi, luas daerah di bawah kurva semakin besar. Kurva baku yang menunjukkan hubungan antara konsentrasi standar epigallokatekin galat vs AUC (Gambar 8).
Standar Konsentrasi % b/v (x)
AUC (y)
I 2,5 x 10-4 6461,4
II 5,0 x 10-4 10258,4
III 7,5 x 10-4 13894,1
IV 10 x 10-4 15550,1
V 12,5 x 10-4 16264,6
Y = Bx + A Y = 9.959.240x + 5016,29
0
Gambar 8. Kurva antara konsentrasi standar epigallokatekin galat vs AUC
Keterangan
Instrumen : CAMAG TLC Scanner 3
Fase diam : silika gel GF254
Fase gerak : toluena : aseton : asam formiat (9 : 9 : 2) Detektor : UV 280 nm
Penetapan kadar sampel, yaitu senyawa epigallokatekin galat dengan
metode densitometri merupakan pengukuran luas area di bawah kurva. Kadar epigallokatekin galat diperoleh dengan memasukkan data AUC sampel ke dalam persamaan kurva baku sehingga diperoleh kadar senyawa epigallokatekin galat dalam ekstrak etanolik daun teh hijau (Tabel IV).
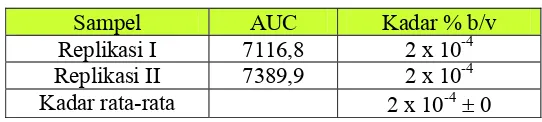
Tabel IV. Kadar senyawa epigallokatekin galat (% b/v) yang terdapat dalam ekstrak etanolik daun teh hijau
Sampel AUC Kadar % b/v
Replikasi I 7116,8 2 x 10-4 Replikasi II 7389,9 2 x 10-4 Kadar rata-rata 2 x 10-4± 0
Dari hasil yang ditunjukkan pada tabel IV, kadar senyawa
56 A. Kesimpulan
Dari hasil penelitian yang dilakukan dapat diambil kesimpulan yaitu : Karakter ekstrak etanolik daun teh hijau adalah organoleptik ekstrak berwarna cokelat kehitaman, tidak berbau, dan rasa agak kelat; kadar air 27,51 %b/b; kadar
abu 2,22 %b/b; kadar abu tidak larut asam 1,40 %b/b; kadar abu larut air 0,87 %b/b; kadar sari larut air 23,17 %b/b; kadar sari larut etanol 42,98 %b/b; dan
kadar senyawa identitas (epigallokatekin galat) 2 x 10-4± 0 %b/v.
B. Saran
Saran yang dapat dipertimbangkan sesuai hasil penelitian ini adalah : 1. Perlu dilakukan penetapan parameter lainnya seperti susut pengeringan dan
bobot jenis, sisa pelarut, residu pestisida, cemaran logam berat, cemaran mikroba, dan uji kandungan kimia ekstrak untuk melengkapi seluruh rangkaian proses standarisasi bahan baku ekstrak etanolik daun teh hijau agar dapat digunakan sebagai bahan baku obat herbal terstandar (OHT).