commit to user
i
MIRA-1 MELALUI PENDEKATAN MEKANIKA KUANTUM
Disusun Oleh :
NINDITA CLOURISA AMARIS SUSANTO
M0307058
SKRIPSI
Diajukan untuk memenuhi sebagian
persyaratan mendapatkan gelar Sarjana Sains Kimia
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SEBELAS MARET
SURAKARTA
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
iii
PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi saya yang berjudul “STUDI INTERAKSI ANTARA SISTEIN (220) PADA p53 DAN MIRA-1 MELALUI PENDEKATAN MEKANIKA KUANTUM” belum pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi, dan sepanjang pengetahuan saya juga belum pernah ditulis atau dipublikasikan oleh orang lain, kecuali yang secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Surakarta, 7 September 2012
NINDITA CLOURISA AMARIS SUSANTO
commit to user
iv
Jurusan Kimia. Fakultas MIPA. Universitas Sebelas Maret.
ABSTRAK
MIRA-1 (Mutant p53-dependent Induction of Rapid Apoptosis 1) diusulkan
membentuk adduct dan menginduksi reaktivasi p53. Kebolehjadian pembentukan adduct antara ikatan rangkap C-C MIRA-1 dan gugus tiol dari sistein (220) dapat
dipengaruhi oleh rantai samping fleksibel dari MIRA-1 dan asam amino protein dari p53 disekitar MIRA-1. Kebolehjadian pembentukan adduct dipelajari dengan
penambahan asam amino bertahap untuk membentuk sebuah konfigurasi terpilih. Hanya asam amino yang mempunyai minimal satu atom dengan jarak maksimum 5 Å dengan satu atom MIRA-1 yang dipilih untuk penelitian ini. Jarak yang relatif dekat diasumsikan memberikan pengaruh besar pada distribusi kerapatan elektron dari MIRA-1. Distribusi kerapatan elektron ditentukan melalui perhitungan single point NBO pada level teori HF (Hartree Fock) dan fungsi basis 6-31G *. Hasil
perhitungan menunjukkan kontribusi rantai samping fleksibel dari MIRA-1 dan asam amino protein dari p53 disekitar MIRA-1 terhadap distribusi kerapatan elektron dari ikatan rangkap C-C dan dapat menyebabkan polarisasi. Polarisasi memberikan karbon bermuatan parsial positif sehingga terdapat kebolehjadian serangan nukleofilik dan pembentukan adduct tiol pada posisi ikatan rangkap C-C
MIRA-1
Kata kunci: MIRA-1, konfigurasi, adduct, QM, NBO, polarisasi
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
v
NINDITA CLOURISA AMARIS SUSANTO
Department of Chemistry. Faculty of Mathematics and Natural Sciences. Sebelas Maret University.
ABSTRACT
MIRA-1 (Mutant p53-dependent Induction of Rapid Apoptosis 1) was proposed to form adduct and induces reactivation of p53. Probability of adduct formation between C-C double bond of MIRA-1 and thiol group of cysteine (220) can be affected by flexible side chain from MIRA-1 and surrounding protein amino acid of p53. The probability of adduct formation were studied by stepwise addition of amino acid to form a selected configurations. Only amino acids which have at least one atom at the distance of maximum 5Å to one atom of MIRA-1 were choosen for this study. Relative proximity is assumed to provide a major influence on the electron density distribution of MIRA-1. Electron density distribution was determined by means of NBO single point calculation at the HF (Hartree Fock) level of theory and 6-31G* basis function. The calculation results demonstrate a contribution of flexible side chain from MIRA-1 and surrounding protein amino acid of p53 to the distribution of electron density of C-C double bond and may induce polarization. Polarization gives a partial positive charge of carbon so there is possibility of nucleophilic attack and the formation of thiol adduct at position C-C double bond of MIRA-1.
Keyword : MIRA-1, configuration, adduct, QM, NBO, polarization
commit to user
vi
selesai (dari sesuatu urusan), kerjakanlah dengan sungguh-sungguh (urusan) yang lain dan hanya kepada Tuhanmulah hendaknya kamu berharap
(Al Insyiraah: 5-8)
Sebaik – baiknya manusia adalah manusia yang bermanfaat bagi orang lain (H. R. Muslim)
You do not really understand something unless you can explain it to your grandmother (Albert Einstein)
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
vii
Karya ini saya persembahkan untuk,
Orangtuaku tersayang, maaf kalau tidak bisa menyelesaikan ini semua tepat waktu. Terimakasih atas
kasih sayang dan do‟a yang selalu tercurah untukku. Adikku tercinta, yang selalu memberikan dukungan untukku.
Semua pembaca, semoga dapat lebih bermanfaat.
commit to user
viii
jalan yang indah bagi penulis sehingga skripsi ini dapat penulis selesaikan dengan baik sebagai salah satu persyaratan dalam memperoleh gelar sarjana sains Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret Surakarta. Atas segala karunia-Nya pulalah penulis menyadari bahwa segala sesuatu memiliki proses dan waktunya masing-masing.
Dalam menyusun skripsi ini penulis menemui berbagai hambatan dan permasalahan yang beragam. Namun, atas bimbingan, kritikan, saran, dan dorongan semangat yang bermanfaat dari berbagai pihak, semua hambatan dan permasalahan tersebut dapat penulis atasi dengan baik. Oleh karena itu, penulis ingin menyampaikan terima kasih kepada pihak-pihak yang telah membantu penulis, yaitu sebagai berikut.
1. Prof. Ir. Ari Handono Ramelan., M.Sc., Ph.D., selaku dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret Surakarta 1. Dr. Eddy Heraldy., M.Si., selaku ketua jurusan Kimia Fakultas Matematika
dan Ilmu Pengetahuan Alam Universitas Sebelas Maret, Surakarta 2. Dr. Khoirina Dwi N., M.Si., selaku pembimbing akademik
3. Dr.rer.nat. Fajar R. Wibowo., M.Si., selaku pembimbing skripsi, yang dengan penuh kesabaran telah memberikan bimbingan dan arahan kepada penulis dari awal hingga akhir
4. I.F. Nurcahyo., M.Si., selaku ketua laboratorium Kimia Dasar, yang telah memberikan akses bagi penulis melakukan penelitian di laboratorium Kimia Dasar bagian Komputasi Kimia
5. Bapak Ibu dosen dan seluruh staf jurusan Kimia yang telah memberikan fasilitas dan pelayanan yang baik bagi penulis
6. Bapak, Mama dan Bela dirumah, terimakasih atas dukungan dan motivasi yang diberikan untuk segera menyelesaikan karya ini
7. Computational Chemistry Comunity, terimakasih atas bantuan dan motivasi yang telah diberikan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
ix
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun dari semua pihak dalam rangka untuk menyempurnakan skripsi ini. Akhirnya penulis berharap, semoga karya kecil ini dapat memberikan manfaat bagi ilmu pengetahuan dan bagi pembaca.
DAFTAR PUSTAKA
Halaman Surakarta, September 2012
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
xi
10. Fungsi Basis ... 19
B. Kerangka Pemikiran ... 20
C. Hipotesis ... 22
BAB III METODOLOGI PENELITIAN... 23
A.Metode Penelitian ... 23
B. Tempat dan Waktu Penelitian ... 23
C.Alat dan Bahan yang Dibutuhkan ... 23
1. Alat ... 23
2. Bahan ... 23
D.Prosedur Penelitian………..……. ... 23
1. Kompleks Protein-Ligan ... 23
a. Pembentukan Konfigurasi ... 23
b. Persiapan Perhitungan ... 24
2. Perhitungan Analisis Populasi ... 24
a. Optimasi Geometri ... 24
b. Single Point ... 25
E. Teknik Pengumpulan dan Analisis Data ... 25
1. Pengumpulan Data ... 25
2. Analisis Data ... 25
BAB IV HASIL DAN PEMBAHASAN ... 27
A. Kompleks Protein-Ligan ... 27
B. Perhitungan Analisis Populasi ... 32
BAB V KESIMPULAN DAN SARAN ... 49
DAFTAR PUSTAKA. ... 50
LAMPIRAN ... 54
DAFTAR TABEL
commit to user
xii
Tabel 2. Jarak antara atom dari asam amino ke atom MIRA-1... 30
Tabel 3. Nilai muatan parsial masing – masing atom penyusun
MIRA-1 ... 34
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
xiii
Halaman Gambar 1. Struktur p53 termutasi yang menunjukkan letak
atau posisi Y220C.. ... 7
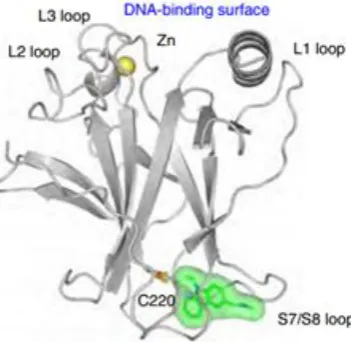
Gambar 2. PhiKan083 (surface warna hijau) berada pada lekukan mutasi (cavity) mutan Y220C ... 7
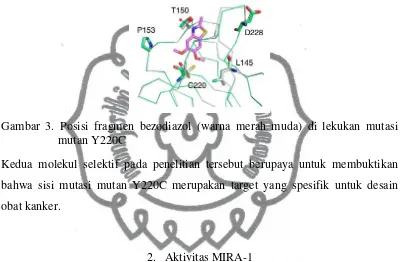
Gambar 3. Posisi fragmen bezodiazol (warna merah muda) di lekukan mutasi mutan Y220C ... 8
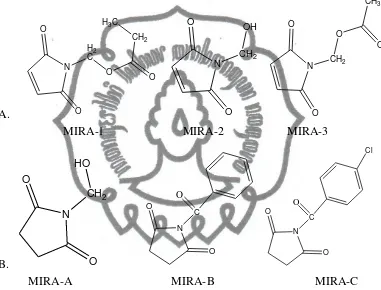
Gambar 4. Struktur turunan maleimida A. Turunan aktif maleimidan B. Turunan tidak aktif maleimida ... 9
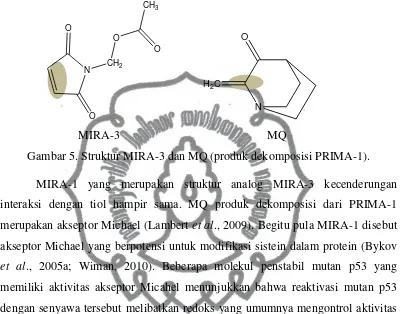
Gambar 5. Struktur MIRA-3 dan MQ (produk dekomposisi PRIMA-1) ... 10
Gambar 6. Mekanisme induced-fit pada enzim ... 12
Gambar 7. Model untuk ilustrasi jarak antar atom ... 14
Gambar 8. Mekanisme reaksi adisi nukeofilik 1,4 (serangan pada C=C) ... 16
Gambar 9. Kompleks p53 termutasi Y220C dengan MIRA-1 hasil docking dan warna hitam menunjukkan MIRA-1 ... 28
Gambar 10. Kompleks p53-MIRA-1 pada daerah mutan Y220C dan warna hitam menunjukkan MIRA-1 ... 29
Gambar 11. Surface bagian asam amino – asam amino dari lekukan mutasi yang berada di sekitar MIRA-1 dan warna hitam menunjukkan MIRA-1.... 31
Gambar 12. Struktur MIRA-1 teroptimasi ... 33
Gambar 13. Struktur MIRA-1 dari kompleks Y220C-MIRA-1 hasil docking ... 36
Gambar 14. Konfigurasi – konfigurasi dengan penambahan asam amino secara parsial dan nilai ∆occupancy C1=C2 dari masing – masing tambahan asam amino... 37
Gambar 15. Konfigurasi ke-2 dengan adanya tarikan elektron yang lebih besar dari salah satu sisi ikatan rangkap C-C... 42
commit to user
xiv
polarisasi tinggi pada ikatan rangkap C-C ... 44 Gambar 18. Struktur MIRA-A, MIRA-B dan MIRA-C ... 46 Gambar 19. Struktur MIRA-1, MIRA-2 dan MIRA-3 ... 47
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
xv
commit to user
1
PENDAHULUAN
A. Latar Belakang Masalah
Protein p53 tumor suppressor berperan dalam pengendalian pertumbuhan
sel sebagai pembatas terhadap adanya pertumbuhan sel menyimpang. Pertumbuhan sel menyimpang dapat diakibatkan oleh kerusakan DNA, aktivasi onkogen dan hipoksia (Bykov et al., 2002a, 2002b; Wiman, 2010). Apoptosis
(bunuh diri sel terprogram) merupakan salah satu upaya untuk pengendalian pertumbuhan sel ketika terjadi kegagalan pada proses perbaikan kerusakan DNA dan kerusakan sel yang lain sebelum pembelahan terjadi pada sel tersebut (Albert
et al., 2002). Mutasi pada p53 akan berakibat hilangnya fungsi p53 sebagai
penekan tumor (Bykov et al.,2002a, 2002b). Hal tersebut dapat memicu kanker
atau cacat lain akibat tidak adanya penghentian pembelahan sel yang disebabkan kerusakan DNA dan kerusakan sel yang lain (Bykov et al., 2002a). Pengembalian
fungsi p53 termutasi berpotensi menghentikan pertumbuhan sel kanker sehingga menjadikan p53 target yang cukup penting untuk terapi kanker (Bykov et al.,
2002a, 2002b; Lambert et al., 2009; Wiman, 2010).
Lazimnya ada enam titik atau hot-spot mutasi yang sering terkait dengan
kanker manusia dan pro-onkogenik. Y220C merupakan mutasi yang sering terjadi di β-sandwich dan jauh dari daerah DNA-binding (Joerger et al, 2006). Mutasi
pada p53 mengubah satu asam amino pada protein menjadi asam amino lain. Mutasi Y220C merupakan mutasi tirosin menjadi sistein dan merupakan satu dari sekian mutasi onkogen yang terjadi pada p53 (Joerger et al., 2006; Basse et al.,
2010). Mutasi Y220C ini menciptakan lekukan pada permukaan protein yang menyebabkan ketidakstabilan protein karena perubahan konformasi protein (Joerger et al., 2006).
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
2
menyerupai wild-type p53. Beberapa molekul kecil yang diidentifikasi dapat
mengembalikan fungsi p53 termutasi diantaranya PRIMA-1 (p53 reactivation
induction of massive apoptosis) (Bykov et al., 2002a, 2002b; Lambert et al., 2009;
Wiman, 2010) dan turunan maleimida (MIRA-1 (Mutant p53-dependent Induction of Rapid Apoptosis I), MIRA-2, MIRA-3) (Bykov et al., 2005). Bykov (2005)
menunjukkan bahwa MIRA-1 mempunyai kestabilan aktivitas pada mutan SKOV-His273, SKOV-His175 dan HI299-His175 dibandingkan MIRA-2 dan MIRA-3 pada konsentrasi yang cukup tinggi.
Interaksi yang terjadi antara p53 dengan MIRA-1 dapat menyebabkan modifikasi pada struktur p53. MIRA-1 dapat mengubah konformasi mutan p53 ke dalam konformasi aktif dengan berikatan secara spesifik pada asam amino tertentu dari DNA dan mempunyai aktivitas antitumor secara in vitro (Bykov et al., 2005).
Modifikasi mutan p53 melalui pembetukan adduct tiol pada satu atau beberapa
asam amino sistein mutan p53 diperkirakan mampu mengembalikan konformasi dan fungsi p53 mendekati wild-type-nya sehingga dapat menginduksi apoptosis
dalam sel yang mengekspresikan mutan p53 (Lambert et al, 2009).
Lambert (2009) melaporkan pembentukan adduct tiol antara PRIMA-1
dengan N-acetylcysteine (NAC). Hal tersebut memungkinkan pembentukan
adduct tiol yang terjadi pada sistein dalam p53. Pembentukan adduct tiol
1 dan NAC melalui substitusi nukleofilik pada salah satu gugus hidroksi PRIMA-1. Lambert (2009) melaporkan juga bahwa pembentukan adduct lebih mudah
melalui konversi PRIMA-1 menjadi MQ (Methylene Quinoclidinone) dimana MQ
mempunyai ikatan rangkap C-C yang reaktif. Sehingga pembentukan adduct tiol
antara MQ dan NAC diperkirakan melalui addisi nukleofilik. MIRA-3 dapat membentuk adduct tiol dengan NAC. Proses reaktivasi p53 dengan MIRA-3
commit to user
B. Perumusan Masalah
1. Identifikasi Masalah
MIRA-1 mempunyai aktivitas antitumor yang hampir sama dengan PRIMA-1 secara in vitro. Aktivitas antitumor kedua senyawa ini diyakini melalui
reaktivasi p53 termutasi. PRIMA-1 diketahui membentuk adduct dengan gugus
tiol dalam proses reaktivasi p53. Konversi PRIMA-1 menjadi MQ diperlukan dalam pembentukan adduct. Gugus hidroksi PRIMA-1 diubah menjadi ikatan
rangkap C-C pada MQ. Ikatan rangkap C-C dengan kondisi yang mirip juga terdapat pada MIRA-3 yang merupakan struktur analog MIRA-1, yaitu ikatan rangkap C-C yang terkonjugasi dengan karbonil. Ikatan rangkap C-C yang terdapat pada MIRA-1 maupun MQ sama - sama mendapat tarikan elektron dari karbonil yang mempunyai atom O dengan keelektronegatifan tinggi. MIRA-3 dipercaya dapat membentuk adduct tiol seperti halnya MQ. MIRA-1
dimungkinkan mempunyai aktivitas yang hampir sama dengan MIRA-3. Namun demikian diduga terdapat perbedaan reaktivitas ikatan rangkap C-C. MIRA-1 dengan MIRA-3 mempunyai perbedaan pada bagian alifatiknya. Seperti halnya MIRA-3, MIRA-1 juga mempunyai dua gugus karbonil disebelah kanan dan kiri ikatan rangkap C-C sehingga tarikan elektron terhadap ikatan rangkap C-C simetris, sedangkan MQ mempunyai satu gugus karbonil maka tarikan elektronnya hanya dari satu arah. Perbedaan polaritas ikatan rangkap C-C pada MIRA-1 atau MIRA-3 dengan MQ menunjukkan kebolehjadian pembentukan adduct turunan maleimida lebih kecil dari MQ. Namun demikian MIRA-3 memiliki aktivitas yang cukup tinggi dibandingkan dengan MQ.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
4
berupa suatu lekukan yang cukup tajam, sempit atau luas maupun hanya berupa lekukan yang landai.
Reaktivitas suatu ikatan rangkap C-C dilihat melalui kerapatan elektron yang dipengaruhi lingkungan. Kerapatan elektron dapat ditunjukkan melalui metode analisis populasi berbantuan komputer yang dikenal antara lain Mulliken, NBO (Natural Bond Orbital) atau ESP (Electrostatic Potential). Analisis populasi
harus dilakukan dengan metode mekanika kuantum mengingat analisis ini melibatkan stuktur elektronik suatu molekul. Metode – metode dari mekanika kuantum mempunyai akurasi dan kecocokan dengan sistem yang berbeda – beda. Akurasi metode mekanika kuantum antara lain ditentukan oleh level teori yang digunakan yaitu: Hartree Fock (HF), Pertubasi Moller-Pleset, Configuration
Interaction (CI), atau Coupled Cluster (CC). Perhitungan komputasi yang
menggambarkan karakter pengaruh lingkungan juga membutuhkan fungsi basis yang sesuai. Fungsi basis diantaranya fungsi basis minimal, fungsi basis yang membagi elektron valensi, fungsi basis yang menambahkan fungsi polarisasi atau yang menambahkan fungsi difusi. Mengingat tingginya sumber daya yang diperlukan, pemilihan metode yang tepat merupakan syarat utama efisiensi perhitungan.
2. Batasan Masalah
1. Reaktivitas MIRA-1 dalam pembentukan adduct ditunjukkan dengan
polarisasi kerapatan elektron pada ikatan rangkap C-C terkonjugasi dengan dua gugus karbonil.
2. Perubahan kerapatan elektron ditinjau dari pengaruh asam amino terdekat dalam lekukan mutasi p53.
3. Struktur interaksi yang digunakan adalah hasil docking dengan MOE kode
PDB 2X0W kompleks p53 termutasi (Y220C) dengan MIRA-1 pada posisi ikatan rangkap C-C dekat dengan gugus tiol.
commit to user
3. Rumusan Masalah
1. Apakah kerapatan elektron ikatan rangkap C-C MIRA-1 dapat menjadi asimetris sehingga terdapat kebolehjadian serangan nukleofil?
2. Apakah ikatan rangkap C-C MIRA-1 dapat terpolarisasi sebagai pengaruh lekukan mutasi sehingga terdapat kebolehjadian pembentukan adduct tiol?
3. Bagaimana bagian alifatik MIRA-1 berpengaruh terhadap kebolehjadian pembentukan adduct tiol?
C. Tujuan Penelitian
1. Mengetahui apakah kerapatan elektron ikatan rangkap C-C MIRA-1 dapat menjadi asimetris sehingga terdapat kebolehjadian serangan nukleofil.
2. Mengetahui pengaruh lekukan mutasi terhadap polarisasi ikatan rangkap C-C MIRA-1 sehingga terdapat kebolehjadian pembentukan adduct tiol.
3. Mengetahui pengaruh bagian alifatik MIRA-1 terhadap kebolehjadian pembentukan adduct tiol.
D. Manfaat Penelitian
Penelitian ini diharapkan mampu memberikan informasi mengenai pengaruh lekukan mutasi Y220C dan bagian alifatik MIRA-1 terhadap kebolehjadian pembentukan adduct tiol dengan menggunakan pendekatan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
6
BAB II
LANDASAN TEORI
A. Tinjauan Pustaka
1. Mutan Y220C
Protein p53 tumor suppressor (penekan tumor) berperan sebagai target
terapi (Bykov et al., 2002a, 2002b; Wiman, 2010). Mutasi pada p53 berakibat
pada hilangnya fungsi p53 sebagai penekan tumor (Bykov et al., 2002a, 2002b).
Protein p53 sebagai target terapi terdapat tiga alasan pertimbangannya. Pertama, p53 berperan penting dalam menentukan nasib sel ketika DNA mengalami kerusakan yakni menentukan sel rusak akan memperbaiki diri atau mengalami apoptosis apabila kerusakan terlalu ekstensif (Wiman, 2010) sehingga p53 yang mengalami mutasi berperan terhadap perkembangan tumor, progesi dan resistensi kemoterapi. Kedua, sebagian besar perubahan genetik dalam tumor baik delesi atau mutasi pada lebih dari 50 % kanker manusia ternyata p53 mengalami mutasi (Joerger et al., 2006). Ketiga, kehilangan p53 mengakibatkan penurunan apoptosis
dan menurunkan sensitivitas terhadap radioterapi dan kemoterapi (Wiman, 2010). Mutasi yang terjadi pada p53 umumnya terdapat enam titik atau hot-spots
yang teridentifikasi terkait kanker manusia yaitu R175H, G245S, R248Q, R249S, R273H dan R282W (Joerger and Fersht., 2007). Selain itu terdapat juga mutasi pada β-sandwich yaitu V143A, L145Q, P151S, V157F, I195T, Y220C, I232T, I255F dan F270C (Bullock, 2000; Joerger et al., 2006). Mutasi pada Y220C
merupakan mutasi yang sering terjadi di β-sandwich sekitar 75000 kasus kanker
baru di dunia (Joerger et al., 2006; Basse et al., 2010). Mutasinya terletak jauh
dari DNA-binding yang dimulai dari loop yang terhubung dengan β-strands S7
dan S8 ditunjukkan Gambar 1.
commit to user
Gambar 1. Struktur p53 termutasi yang menunjukkan letak atau posisi Y220C.
Mutan Y220C dapat dihilangkan sifat onkogen dengan menurunkan stabilitasnya sehingga bisa didenaturasi pada temperatur tubuh akibatnya tidak lagi memicu kanker (Boeckler et al., 2008).
Penempelan molekul selektif dapat mengembalikan konformasi dan fungsi mutan p53 mendekati wild-type (Joerger dan Fersht., 2006; Boeckler, 2008; Basse
et al., 2010)). Molekul selektif salah satunya terdapat PhiKan083 (turunan
karbazol) melalui docking pada lekukan mutasi (cavity) yang diciptakan oleh
Y220C dengan afinitas yang baik dan menstabilkan mutan (Boeckler et al., 2008)
yang ditunjukan Gambar 2.
Gambar 2. PhiKan083 (surface warna hijau) berada pada lekukan mutasi (cavity)
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
8
Selain itu terdapat juga fragmen benzotiazol aromatik pada sistem cincin yang terdapat dalam lekukan mutasi (kode ID PDB 2X0W) pada posisi tegak yang ditunjukkan Gambar 3. Itu diposisikan demikian, nitrogen tiazol berada pada jarak ikatan hidrogen dengan gugus hidroksi Thr150 (threonin 150) dan gugus metoksinya yang mengapit ikatan rangkap C-C berada dekat dengan Cys220 (sistein 220) (Basse et al., 2010)
Gambar 3. Posisi fragmen bezodiazol (warna merah muda) di lekukan mutasi mutan Y220C
Kedua molekul selektif pada penelitian tersebut berupaya untuk membuktikan bahwa sisi mutasi mutan Y220C merupakan target yang spesifik untuk desain obat kanker.
2. Aktivitas MIRA-1
NCI (Natural Cancer Institutes) melaporkan penemuan dua molekul yang
dapat mengaktifkan kembali mutan p53 yaitu PRIMA-1 (p53 Reactivation and
Induction of Massive Apoptosis) dan MIRA-1 (Mutant p53-Dependent Induction of Rapid Apoptosis) (Bykov et al., 2005). Molekul seperti PRIMA-1 dan MIRA-1
atau produk hidrolisisnya dapat bereaksi secara kovalen dengan p53 melalui modifikasi asam amino sistein (Lambert et al., 2009). MIRA-1 mempunyai
aktivitas antitumor lebih baik dibandingkan PRIMA-1 (Bykov et al., 2005).
MIRA-1 merupakan salah satu turunan maleimida yang dapat mengaktifkan kembali mutan p53 in vitro dan mengembalikan
transkripsi-tansaktivasi dengan mutan p53 pada sel hidup (Bykov et al., 2005). MIRA-1
commit to user
strukturnya dapat ditunjukkan pada Gambar 4. Struktur turunan maleimida yang aktif dan mempunyai aktivitas hampir sama dengan MIRA-1 yaitu MIRA-2 dan MIRA-3 ditunjukkan pada Gambar 4A. Selain itu terdapat juga struktur analog MIRA-1 yang tidak aktif yaitu MIRA-A, MIRA-B dan MIRA-C ditunjukkan pada Gambar 4B.
Hasil pengujian terhadap SKOV-His273, SKOV-His175 dan HI299-His175 pada konsentrasi yang tinggi memberikan kestabilan aktivitas dibandingkan MIRA-2 dan MIRA-3. Kedua turunan maleimida tersebut mempunyai aktivitasnya pada konsentrasi yang rendah. MIRA-3 pada konsentrasi yang tinggi dapat memberikan efek toksik (Bykov et al., 2005).
Lambert (2009) melaporkan pembentukan adduct lebih mudah melalui
konversi PRIMA-1 menjadi MQ dimana MQ mempunyai iktan rangkap yang reaktif dan terkonjugasi dengan gugus karbonil sehingga pembentukan adduct tiol
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
10
mempunyai ikatan rangkap C-C yang relatif seperti MQ yang dapat ditunjukkan Gambar 5 sehingga terdapat kecenderungan interaksi dengan tiol seperti pada MQ yaitu melalui reaksi addisi nukleofilik.
Gambar 5. Struktur MIRA-3 dan MQ (produk dekomposisi PRIMA-1).
MIRA-1 yang merupakan struktur analog MIRA-3 kecenderungan interaksi dengan tiol hampir sama. MQ produk dekomposisi dari PRIMA-1 merupakan akseptor Michael (Lambert et al., 2009). Begitu pula MIRA-1 disebut
akseptor Michael yang berpotensi untuk modifikasi sistein dalam protein (Bykov
et al., 2005a; Wiman, 2010). Beberapa molekul penstabil mutan p53 yang
memiliki aktivitas akseptor Micahel menunjukkan bahwa reaktivasi mutan p53 dengan senyawa tersebut melibatkan redoks yang umumnya mengontrol aktivitas p53 wild-type (Wiman, 2010).
3. Reaksi Enzimatis
commit to user
enzim dan merupakan tempat terjadinya ikatan antara enzim dengan substrat. Sisi aktif ini memiliki ukuran yang berkisar hanya tiga sampai empat asam amino. Jauh lebih kecil dibandingkan ukuran enzim secara keseluruhan. Komposisi dan ukuran protein bergantung pada jenis dan jumlah sub unit asam aminonya (Copeland, 2000).
Jenis ikatan yang terjadi antara enzim dan substrat dapat berupa kovalen, ionik, hidrogen dan van der Waals. Ikatan hidrogen dan van der Waals berperan dalam orientasi struktural komplek enzim-substrat (Copeland, 2000). Ukuran polaritas dari suatu ikatan kovalen dari suatu atom dapat dipengaruhi oleh jarak antar inti atom. Interaksi dari satu titik dari protein tidak hanya mempengaruhi daerah tersebut saja, tetapi akan mempengaruhi pada titik yang lain.
Protein dibangun oleh sekitar 20 macam asam amino melalui ikatan peptida. Asam amino mempunyai muatan amino dan muatan karbonil pada ujung – ujungnya yang dinetralkan melalui pembentukan ikatan peptida. Dalam sistem protein penyusunnya disebut asam amino, dimana yang membedakan antara asam amino yang satu dengan asam amino yang lain berupa struktur rantai samping yang berbeda pada asam amino – asam amino tersebut sehingga berpengaruh pada reaktivitas kimia. Beberapa asam amino seperti valin, leusin, alanin dan lain – lain terdiri dari hidrokarbon sehingga bersifat non polar, diharapkan mampu menarik molekul yang polar. Asam amino hidrofobik ini membantu menstabilkan pengikatan molekul substrat non polar ke dalam enzim. Ikatan hidrogen ini dapat menstabilkan struktur protein. Ukuran dan bentuk dari rantai samping asam amino menentukan tipe interaksi dengan gugus aktif tertentu. (Copeland, 2000).
Reaksi enzimatis melibatkan suatu proses pengikatan substrat ke dalam sisi aktif enzim. Terdapat dua mekanisme yang diusulkan untuk menjelaskan proses pengikatan substrat tersebut yaitu mekanisme Lock & Key yang
dikemukakan oleh Emil Fischer pada tahun 1984, dan mekanisme Induced-Fit.
Mekanisme yang terakhir dikemukakan pada tahun 1958 oleh Daniel Koshland. Pada mekanisme Lock & Key, enzim dan substrat dapat dianggap sebagai
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
12
tertentu. Jadi enzim dan substrat memiliki struktur geometrik tertentu yang saling komplemen satu sama lainnya. Model ini mampu menjelaskan sifat spesifik dari suatu enzim namun tidak dapat menjelaskan tingkat kestabilan yang mampu dicapai oleh kompleks teraktifkan enzim-substrat.
Mekanisme Induced-Fit merupakan modifikasi dari mekanisme Lock &
Key. Dalam mekanisme ikut dipertimbangkan struktur enzim yang relatif fleksibel
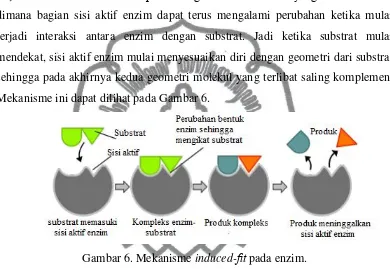
dimana bagian sisi aktif enzim dapat terus mengalami perubahan ketika mulai terjadi interaksi antara enzim dengan substrat. Jadi ketika substrat mulai mendekat, sisi aktif enzim mulai menyesuaikan diri dengan geometri dari substrat sehingga pada akhirnya kedua geometri molekul yang terlibat saling komplemen. Mekanisme ini dapat dilihat pada Gambar 6.
Gambar 6. Mekanisme induced-fit pada enzim.
Gambar 6 yang relevan dengan penelitian ini dibatasi hingga pembentukan kompleks enzim-substrat. Hal tersebut dapat menunjukkan bahwa sisi aktif enzim harus dibantu oleh substrat sehingga membetuk kompleks.
4. Gaya Antar Molekul
commit to user
yang disebut gaya london. Gaya london timbul dari dipol yang diinduksi dalam satu molekul oleh molekul yang lain. Gaya london dapat terjadi bila pasangan elektron suatu molekul, baik yang bebas maupun yang terikat selalu bergerak mengelilingi inti. Elektron yang bergerak dapat mengimbas atau menginduksi sesaat pada tetangga sehingga molekul tetangga menjadi polar terinduksi sesaat. Molekul ini pula dapat menginduksi molekul tetangga lainnya sehingga terbentuk molekul – molekul dipol sesaat (Effendy, 2005).
Molekul polar berada pada jarak tertentu dengan molekul non polar maka molekul polar dapat menginduksi molekul non polar sehingga molekul non polar tersebut menjadi molekul polar induksian. Setelah proses induksian berlangsung antara kedua molekul tersebut terjadi gaya tarik elektrostatik yang disebut gaya dipol – dipol induksi (Effendy, 2005). Elektrostatik merupakan studi interaksi antara muatan benda yang penting untuk memahami interaksi dari elektron yang digambarkan dengan kerapatan elektron. Pendukung utama dari elektrostatik adalah hukum Coulomb yang merupakan deskripsi matematis tentang bagaimana muatan tolak menolak dan tarik menarik. Tarikan dan tolakan terutama timbul dari antaraksi dipol – dipol, tarik menarik antara muatan yang berlainan tanda dan tolak menolak antara muatan yang sama tanda. Persamaan hukum Coulomb untuk kekuatan interaksi antara dua partikel dapat ditunjukkan pada persamaan 1.
.
...persamaan 1.Keterangan :
F = kekuatan interaksi antar dua partikel = muatan partikel pertama
= muatan partikel kedua
= jarak antar dua buah partikel
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
14
A H ---B
Gambar 7. Model untuk ilustrasi jarak antar atom.
Apabila jarak A-H lebih pendek daripada jarak H-B maka ikatan A-H merupakan ikatan kovalen. Ikatan H-B bila jaraknya sama atau lebih besar dari jumlah jari – jari van der Waals atom H dan atom B maka jarak H-B dapat menunjukkan adanya interaksi tanpa ikatan (nonbonded interaction). Tabel 1
menampilkan jari – jari van der Waals beberapa unsur.
Tabel 1. Jari – jari van der Waals beberpa unsur.
Unsur rvdw (Å) Unsur rvdw (Å) Unsur rvdw (Å)
H 1,20 O 1,52 Cl 1,90
C 1,70 S 1,80 Br 2,00
N 1,55 F 1,60 I 2,12
Pada interaksi O dengan O akan memiliki jari – jari van der Waals sebesar 3,04 Å maka bila jarak pada sistem antarmolekul lebih besar daripada jari – jari van der Waals tersebut menunjukkan terdapat interaksi tanpa ikatan berupa dipol – dipol karena sifat dari atom O yang bersifat polar. Namun, semakin jauh jarak antarmolekul tentunya akan mempunyai kekuatan interaksi yang semakin lemah sebab interaksi antar elektronnya semakin sedikit maka polarisasi semakin lemah dan semakin lemah pula kemampuan untuk membentuk ikatan (Effendy, 2005).
5. Reaksi Addisi Nukleofilik Karbon Tak Jenuh-α,β
Reaksi addisi nukleofilik merupakan reaksi pemutusan ikatan rangkap C-C oleh nukleofilik pada rantai karbon tak jenuh (unsaturated). Ikatan rangkap C-C
commit to user
dengan gugus karbonil pada umunya berlangsung makanisme dari Michael
reaction atau Michael addition. Nukleofilik dari mekanisme Michael reaction
akan menyerang pada karbon yang bermuatan parsial positif dimana sistem C=C-C=O ini parsial positif akan terdapat pada karbon-β dan karbon karbonil. Penyerang nukleofil pada C=C mekanismenya melalui addisi 1,4 sedangkan penyerangan nukleofil pada C=O melalui addisi 1,2. Halangan sterik disekitar ikatan rangkap C-C atau sekitar gugus karbonil dapat menyebabkan serangan tertuju pada posisi yang tak terintangi (Laue and Plagens, 2005; Pudjaatmaka, 1999).
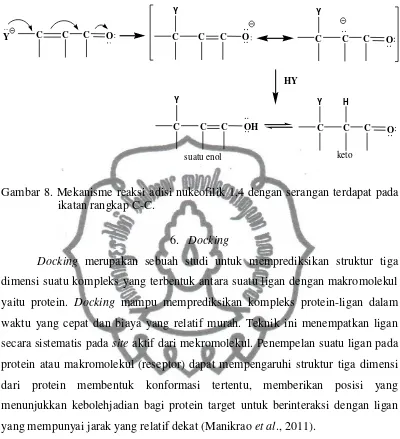
Sistem terkonjugasi seperti keton tak jenuh-α,β addisi nukleofilik yang berlangsung berupa addisi 1,4 dimana tipe addisi ini menyerupai addisi 1,4 diena terkonjugasi. Reaksi addisi 1,4 ini berlangsung melalui dua tahapan reaksi, yang pertama yaitu serangan nukleofil pada ikatan rangkap C-C karbon-α, β yang akan menghasilkan karbanion melalui pemutusan ikatan rangkap C-C. Kemudian nukleofil akan membawa pasangan elektronnya menuju atom karbon-β yang terlibat dalam ikatan rangkap C-C, memaksa elektron π pada ikatan rangkap C-C tersebut menuju atom karbon lainnya membentuk karbanion yang dapat beresonansi. Karbanion dapat beresonansi dengan gugus karbonil membentuk anion pada atom oksigen. Tahap kedua adalah serangan substituen bermuatan positif pada spesi yang bermuatan negatif (March, 1968). Reaksi Michael addition
ini berlangsung melalui rearrangement karbanion pada ikatan rangkap C-C yang
perpustakaan.uns.ac.id digilib.uns.ac.id
Gambar 8. Mekanisme reaksi adisi nukeofilik 1,4 dengan serangan terdapat pada ikatan rangkap C-C.
6. Docking
Docking merupakan sebuah studi untuk memprediksikan struktur tiga
dimensi suatu kompleks yang terbentuk antara suatu ligan dengan makromolekul yaitu protein. Docking mampu memprediksikan kompleks protein-ligan dalam
waktu yang cepat dan biaya yang relatif murah. Teknik ini menempatkan ligan secara sistematis pada site aktif dari mekromolekul. Penempelan suatu ligan pada
protein atau makromolekul (reseptor) dapat mempengaruhi struktur tiga dimensi dari protein membentuk konformasi tertentu, memberikan posisi yang menunjukkan kebolehjadian bagi protein target untuk berinteraksi dengan ligan yang mempunyai jarak yang relatif dekat (Manikrao et al., 2011).
MOE (Molecular Operating Environment) merupakan salah satu aplikasi
yang dikembangkan Chemical Computing Group. Aplikasi ini bersifat
user-friendly sehingga cocok digunakan untuk pembelajaran.
7. Quantum Mechanics (QM)
Quantum Mechanic (QM) atau mekanika kuantum merupakan metode
commit to user
partikel tersebut (menguraikan sifat-sifat dasar partikel yang penting karena elektron terlibat dalam perubahan kimia). Dalam kimia kuantum, sistem digambarkan sebagai fungsi gelombang yang dapat diperoleh dengan menyelesaikan persamaan Schrodinger. Persamaan ini berkait dengan sistem dalam keadaan stasioner dan energi dinyatakan dalam operator Hamiltonian. Operator Hamiltonian dapat dilihat sebagai aturan untuk mendapatkan energi terasosiasi dengan sebuah fungsi gelombang yang menggambarkan posisi dari inti atom dan elektron dalam sistem. Teori QM menggunakan operator Hamiltonian dan fungsi gelombang untuk menghitung energi sistem. Fungsi gelombang berupa fungsi posisi elektron dan nuclear ini dapat digunakan untuk mendeskripsikan
probabilitas elektron pada lokasi tertentu, tetapi tidak dapat memprediksikan secara tepat letak dari elektron tersebut. Muatan atom untuk QM diperoleh dengan skema analisis populasi (Young, 2001).
Metode ini merupakan metode yang paling banyak digunakan dalam permodelan molekul (Leach, 2001). Melalui model Lewis mampu memprediksi pola ikatan kimia dan memberikan indikasi dari kekuatan ikatan (ikatan tunggal, ikatan rangkap C-C). Perhitungan ikatan kovalen yang tanpa pemutusan ikatan dengan Quantum Mechanic (QM) dapat dilakukan dengan menggunakan salah satu metode QM standar (Das, 2002). Akurasi dari perhitungan QM bergantung pada ukuran fungsi basis yang digunakan. Metode QM dapat memberikan penjelasan yang komprehensif untuk fenomena kimia seperti sifat valensi dan ikatan seperti reaktivitas kimia sehingga dapat memberikan penjelasan secara empirik dari kimia. QM (ab initio) pada tingkat dasar dapat memecahkan
persamaan Schrodinger untuk sistem molekul yang mempelajari elektron (Young, 2001). Energi dari keadaan dasar, keadaan tereksitasi dan optimasi geometri dapat dihitung dengan metode QM, tetapi dibatasi pada ukuran sistem (Das, 2002).
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
18
sistem dengan metode QM adalah interaksi elektrostatik dapat dideskripsikan secara realistis (Thiel, 2009). Selain itu perubahan struktur elektronik yang melibatkan interaksi pertukaran muatan dan pengaruh polarisasi tidak diabaikan (Liu et al., 2001). Kelemahan metode ini adalah komputasinya cukup mahal untuk
pembelajaran sistem yang cukup besar, seperti biomolekul (Dolenc and Koller, 2006).
8. Natural Bond Orbital (NBO)
Muatan atom maupun distribusi elektron tidak dapat terlihat dengan QM dan tidak dapat secara langsung dengan perhitungan QM ataupun eksperimen. Terdapat beberapa metode yang berbeda untuk menghitung muatan atom ataupun distribusi elektron dari sistem molekul. Salah satunya adalah NBO yang merupakan teknik analisis yang dapat mendeskripsikan sebuah analisis fungsi gelombang elektronik. NBO menggunakan orbital alami yang merupakan fungsi eigen yang mengurangi orde pertama dari densitas matrik berupa lokalisasi. Prinsip lokalisasi merujuk pada orbital yang menunjukkan pusat atom dan pasangan atom yang menghasilkan muatan dari atom. Analisis dengan NBO dikelompokkan sebagai orbital ikatan, anti ikatan, core dan Rydberg (Young,
2001; Glendening, 2011). Sehingga dengan NBO dapat untuk memahami konsep – konsep ikatan seperti muatan atom, struktur lewis, tipe ikatan, transfer muatan, dan lain – lain. Analisis NBO dalam menunjukkan transfer muatan intramolekul dengan fungsi basis yang menunjukkan akurasi yang tinggi maka nilai - nilai dari muatan inti dan valensi makin negatif yang menunjukkan stabilitas dari struktur molekul (Monajjemi, 2010).
Analisis dengan NBO banyak digunakan karena hasilnya mengklasifikasikan jenis orbital, yang menunjukkan bahwa interaksi orbital lebih berperan penting dalam memutuskan delokalisasi elektron dibandingkan keelektronegatifan. NBO menampilkan occupancy yang menunjukkan berapa
commit to user
umunya menggunakan level teori HF (Hartree-Fock) (Glendening, 2011).
9. Metode komputasi
Metode komputasi perlu dilakukan karena metode eksperimen belum mampu memberikan informasi yang mendalam tentang interaksi antarmolekul dalam skala molekular. Metode eksperimen lebih menjelaskan tentang fenomena yang terjadi dalam sistem makroskopis. Saat ini metode komputasi perhitungan
ab initio telah banyak digunakan untuk menentukan potensial interaksi
antarmolekul secara akurat. Interaksi antarmolekul tergantung pada geometri masing-masing molekul.
Ab initio mengacu pada perhitungan mekanika kuantum melalui beberapa
pendekatan matematis, seperti penggunaan persamaan yang disederhanakan (Born-Oppenheimer approximation) atau pendekatan untuk penyelesaian
persamaan differensial. Ab initio merupakan metode orbital molekul yang paling
akurat dibandingkan semi empirik dan molekul mekanik. Metode ini dapat memberikan prediksi kuantitatif yang akurat untuk berbagai sistem molekular. Namun, membutuhkan sumber daya komputer yang cukup besar (Dorsett and White, 2000). Tipe yang paling terkenal dari metoda ab initio adalah perhitungan
Hartree-Fock (HF) dengan metode pendekatan medan pusat (central field approximation). Ini berarti bahwa tolakan Coulombik antar elektron tidak secara
spesifik dimasukkan dalam perhitungan, tetapi efek total interaksi korelasinya dimasukkan dalam perhitungan sebagai suatu besaran konstant. Dalam teori HF, probabilitas untuk menemukan elektron di suatu daerah dalam atom didefinisikan sebagai jarak dari inti bukan jarak terhadap elektron lainnya (Young, 2001).
10.Fungsi Basis
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
20
orbit atom penyusun molekul tersebut. Dalam kimia komputasi, perhitungan kimia kuantum umumnya dilakukan dalam satu set basis perhitungan yang terdiri atas fungsi gelombang yang ada disusun secara linier (Young, 2001). Fungsi basis yang makin besar menunjukkan peningkatan keakurasian dalam memperkirakan orbital dengan menerapkan pembatasan lokasi elektron dalam ruang. Standar fungsi basis menggunakan kombinasi linier dari fungsi gaussian (Rauk, 2001).
Fungsi basis Split valence merupakan kombinasi dari himpunan fungsi
basis minimal dan himpunan fungsi basis diperluas. Terdapat beberapa fungsi basis untuk masing – masing orbital atomik pada elektron kulit valensi tetapi hanya satu fungsi basis untuk menggambarkan orbital atomik pada kulit dalam. Fungsi basis 6-31G merupakan fungsi basis yang sangat populer untuk perhitungan pada molekul organik. 6-31G mendeskripsikan adanya sebuah
contracted Gaussian yang terdiri dari 6 fungsi Gaussian primitif untuk orbital
atom kulit dalam, sebuah contracted Gaussian yang terdiri dari 3 Gaussian
primitif untuk valensi kulit dalam dan sebuah Gaussian primitif untuk valensi kulit luar (Leach, 2001; Rauk, 2001; Young,2001).
Simbol „*‟ menunjukkan adanya penambahan fungsi polarisasi. Hal tersebut berarti adanya penambahan ke dalam elektron valensi atau penambahan fungsi p untuk atom H dan He untuk sistem dimana hidrogen berperan sebagai atom penghubung atau fungsi d untuk atom besar. Fungsi basis 31G(d) atau 6-31G* merupakan fungsi polarisasi dari fungsi basis 6-31G. Fungsi polarisasi dapat ditambahan pada fungsi basis untuk mendeskripsikan pemindahan yang tidak sama untuk muatan yang jauh dari inti atom sehingga dapat meningkatkan deskripsi dari ikatan kimia. Fungsi polarisasi ini digunakan karena dapat memberikan hasil dengan akurasi lebih baik (Young, 2001).
B. Kerangka Pemikiran
commit to user
ikatan rangkap C-C diapit oleh dua karbonil. Jika tarikan elektron dari kedua karbonil terpusat pada ikatan rangkap C-C MIRA-1 dengan kekuatan yang sama maka kerapatan elektronnya menjadi simetris. Tarikan yang simetris menyebabkan sulit menentukan posisi karbon mana sebagai karbon-β. Ikatan rangkap C-C yang mempunyai kerapatan elektron yang sangat tinggi menyebabkan serangan nukelofil sulit. Sehingga diperlukan faktor yang dapat menurunkan kerapatan elektron dari ikatan rangkap C-C.
Nukleofil umumnya menyerang pada karbon yang mempunyai kerapatan elektron rendah. Kerapatan elektron rendah dapat diperoleh dengan adanya pengaruh dari luar atau dari nukleofil itu sendiri. Tiol yang merupakan nukleofil lemah untuk mempengaruhi polarisasi ikatan rangkap C-C harus ada kombinasi dengan tiol mendekat pada ikatan rangkap C-C dan pengaruh dari luar yang memberikan tarikan elektron lebih kuat pada salah satu sisi karbon. Kemudian elektron ikatan rangkap C-C dapat tertarik ke salah satu sisi karbon dan nukleofil masuk melalui sisi karbon lain. Tarikan elektron yang lebih kuat pada salah satu sisi ikatan rangkap C-C akan memberikan kerapatan elektron asimetris. Pengaruh dari luar dapat diperoleh dari lekukan mutasi karena letak MIRA-1 yang terdapat di dalam lekukan. Lekukan terdiri dari asam amino – asam amino yang mempunyai gugus donor ataupun akseptor elektron. Gugus akseptor sebagai penarik elektron jika posisinya lebih dekat pada salah satu ikatan rangkap C-C dapat memberikan kekuatan tambahan tarikan elektron ke atom karbon tersebut. Sehingga karbon itu kerapatannya lebih besar dibandingkan karbon lain dalam ikatan rangkap C-C. Lekukan mutasi menyelubungi MIRA-1 dari bagian maleimida dan bagian alifatik. Maka pengaruh dari luar dapat pula berpengaruh pada alifatik kemudian secara tidak langsung alifatik tersebut dapat berpengaruh terhadap kerapatan elektron dari ikatan rangkap C-C.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
22
Minimal level yang memenuhi itu adalah HF. Perubahan akibat lingkungan yang berarti ada tarikan, yang dapat mengakomodir tarikan tersebut adalah fungsi basis yang melibatkan polarisasi. Senyawa organik yang melibatkan arom C, N dan O sudah cukup akurat dengan menggunakan fungsi basis split 6-31.
C. Hipotesis
1. Kerapatan elektron ikatan rangkap C-C MIRA-1 dapat dibuat asimetris dengan adanya kekuatan tarikan elektron yang berbeda pada kedua sisi atom karbon ikatan rangkap C-C sehingga dapat terjadi kemungkinan serangan nukleofil. 2. Lekukan mutasi yang terdiri dari asam amino – asam amino yang mempunyai
gugus penarik elektron dapat memberikan pengaruh pada terpolarisasinya ikatan rangkap C-C MIRA-1.
3. Bagian alifatik berpengaruh terhadap kemungkinan pembentukan adduct tiol
commit to user
23
METODOLOGI PENELITIAN
A. Metode Penelitian
Metode yang digunakan dalam penelitian ini adalah metode eksperimental laboratoris.
B. Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Kimia Dasar bagian Komputasi Kimia jurusan Kimia FMIPA UNS selama 6 bulan mulai bulan Oktober 2011 sampai Maret 2012.
C. Alat dan Bahan yang Dibutuhkan
1. Alat
Seperangkat komputer dengan spesifikasi : CPU dengan processor AMD
Phenom (tm) II X 6 1055 T processor, RAM 8 GB dan Hardisk 2 X 500 GB.
Software yang digunakan, yaitu: Gaussian 03 (Frisch et al., 2003), CHIMERA
(Pattersen et al., 2004), molden (Schaftenaar and Noordik, 2000) dan VMD
(Humphrey et al., 1996).
2. Bahan
Struktur hasil docking MOE (Molecular Operating Environment) kode
PDB 2X0W (Basse et al., 2010) yang diperoleh dari perkembangan desain obat
rasional dengan menstabilkan p53 : menyelidiki permukaan mutan onkogen Y220C yaitu kompleks p53 termutasi (Y220C) dengan ligan MIRA-1 (MIRA1-220.pdb)
D. Prosedur Penelitian
1. Kompleks Protein-Ligan a. Perbentukan Konfigurasi
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
24
2X0W sebagai p53 termutasi pada Y220C dengan MIRA-1 sehingga diperoleh kompleks p53-MIRA-1 pada daerah mutan Y220C (unpublished result).
Struktur tersimpan dalam MR1-220 arsip pdb (MR1-220.pdb). Perhitungan sistem dengan kompleks utuh memberikan masalah konvergensi. Hal tersebut kemudian dilakukan pemotongan ukuran kompleks dengan asam amino yang berada disekitar MIRA-1 (dalam lekukan mutasi) yaitu sekitar 20 jumlah asam amino. Itu pun dalam perhitungan memberikan masalah konvergensi. Kemudian dilakukan pembentukan konfigurasi – konfigurasi dengan penambahan asam amino – asam amino secara parsial yang atomnya mempunyai jarak yang relatif dekat dengan atom di MIRA-1. Jarak antar atomnya diperoleh dengan menggunakan CHIMERA. Pembentukan konfigurasi dimulai dari MIRA-1 saja tanpa lingkungan (asam amino) dari MR1-220 arsip pdb kemudian dilanjutkan asam amino pertama yaitu asam amino sistein yang diambil dari MR1-220 arsip pdb sebagai konfigurasi ke-1 dan seterusnya. Asam amino yang diambil dari MR1-220 arsip pdb (MR1-220.pdb) melalui pemutusan ikatan peptida, pada ujungnya terdapat ujung gugus karbonil (C=O) atau ujung N-H. Ujung – ujung tersebut kemudian ditambahkan oleh atom atau gugus yang sesuai dengan struktur standar asam amino dengan gedit dan disimpan kembali sebagai arsip pdb. Tiap konfigurasi disimpan dalam arsip pdb dan dapat divisualisasi dengan CHIMERA.
b. Persiapan Perhitungan
Arsip pdb masing – masing konfigurasi dikonversi menjadi arsip com dengan VMD (Visual Molecular Dynamic) untuk dilakukan eksekusi
perhitungan. Arsip com tiap konfigurasi dibuka dengan gedit untuk mengubah atom type menjadi atom tunggal dan disimpan kembali sebagai arsip com.
Kemudian arsip com tersebut yang digunakan dalam eksekusi perhitungan.
2. Perhitungan Analisis Populasi a. Optimasi Geometri
commit to user
(Hatree Fock) dan fungsi basis 6-31G*. Hasil optimasi geometri tersimpan
sebagai arsip log yang dapat divisualisasi melalui CHIMERA dengan mengubahnya ke dalam arsip pdb melalui molden dan data NBO-nya dapat ditunjukkan melalui gedit.
b. Single Point
MIRA-1 yang diambil dari MR1-220 arsip pdb (MR1-220.pdb) juga dihitung single point NBO-nya dengan Gaussian 03. Single point dilakukan dengan level teori dan fungsi basis yang sama dengan yang dilakukan pada optimasi geometri. Hasilnya tersimpan dalam arsip log sebagai konfigurasi ke-0. Kemudian dilanjutkan perhitungan single point NBO untuk konfigurasi selanjutnya yaitu konfigurasi selanjutnya tergantung jumlah asam amino yang diambil sebagai konfigurasi. Hasilnya juga tersimpan dalam arsip log yang selanjutnya untuk pengumpulan dan analisis data distribusi kerapatan elektronnya dari data NBO yang dapat ditunjukkan melalui gedit.
E. Teknik Pengumpulan dan Analisis Data
1. Pengumpulan Data
Data yang diambil adalah gambar MIRA-1 hasil optimasi geometri dan single point serta gambar konfigurasi yang merupakan tambahan asam amino secara parsial. Selain itu, data NBO yang diambil adalah nilai occupancy dan
muatan parsial.
2. Analisis Data
Interaksi antara sistein dengan MIRA-1 untuk menunjukkan kebolehjadian pembentukan adduct tiol dengan melihat pengaruh lingkungan dalam lekukan
mutasi disekitar MIRA-1 terhadap distribusi kerapatan elektronnya. Hal tersebut dapat ditentukan dengan membandingkan nilai delta occupancy target reaksi di
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
26
dapat memberikan pengaruh pada distribusi kerapatan elektron di MIRA-1 yang berpengaruh pada reaktivitas ikatan rangkap C-C. Kebolehjadian pembentukan
adduct yang dipengaruhi lekukan mutasi dapat juga ditunjukkan melalui
commit to user
27
HASIL DAN PEMBAHASAN
A. Kompleks Protein-Ligan
Mutasi onkogenik Y220C adalah salah satu perubahan genetik yang sering terdapat pada kanker manusia. Mutasi dapat menurunkan stabilitas protein dan menginduksi pembentukan celah di permukaan site mutasi. Mutasi kanker Y220C
menginduksi pembentukan cavity (lekukan mutasi) pada permukaan protein yang
dapat menampung molekul penstabil.
Struktur mutan Y220C diperoleh dari p53 mutan Y220C yang ditambahkan dengan 5,6-dimetoksi-2metilbenzotiazol dengan kode pdb 2X0W. Itu diperoleh dari perkembangan desain obat rasional dengan menstabilkan p53 : menyelidiki permukaan mutan onkogen Y220C. Struktur 5,6-dimetoksi-2metilbenzotiazol berada didekat Y220C kemudian dihilangkan dan digantikan dengan MIRA-1. MIRA-1 masuk ke lekukan mutasi Y220C dengan bantuan
docking MOE (Molecular Operating Environment) (unpublished result).
Struktur 5,6-dimetoksi-2metilbenzotiazol ketika dalam lekukan mutasi Y220C terstabilkan karena posisi dari atom N tiazol dapat membentuk ikatan hidrogen dengan gugus hidroksi dari threonin (150). Gugus metoksi dari struktur 5,6-dimetoksi-2metilbenzotiazol mengapit ikatan rangkap C-C berada jarak yang cukup dekat dengan sistein. Maka model interaksi struktur tersebut dapat dilakukan pada MIRA-1. MIRA-1 dengan 5,6-dimetoksi-2metilbenzotiazol sama – sama mepunyai gugus penarik elektron yang mengapit ikatan rangkap C-C yang dapat mempengaruhi polarisasinya sehingga dapat menunjukkan kebolehjadian pembentukan adduct.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
28
(mutan p53) sehingga dapat mengaktifkan fungsi p53 menyerupai wild-type-nya
melalui kebolehjadian pembentukan adduct tiol. Ikatan rangkap C-C alkena yang
mempunyai orbital ikatan π yang cederung kurang stabil dan memudahkan interaksi dengan sistein sehingga terdapat kebolehjadian pembentukan adduct tiol.
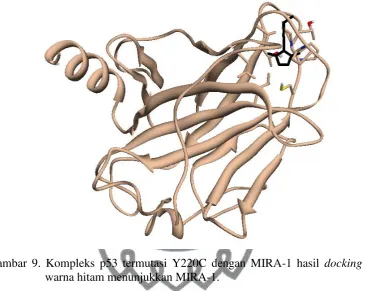
Gambar 9. Kompleks p53 termutasi Y220C dengan MIRA-1 hasil docking dan
warna hitam menunjukkan MIRA-1.
commit to user
semakin banyak antar atom yang tak berikatan dari sisi asam amino yang berbeda sehingga diasumsikan struktur menjadi tidak homogen. Itu menyebabkan perhitungan muncul masalah konvergensi. Oleh karena itu, kompleks p53-MIRA-1 tidak dilakukan perhitungan utuh yang kemudian memperkecil ukuran kompleks pada daerah mutan Y220C yang ditunjukkan Gambar 10.
Gambar 10. Kompleks p53-MIRA-1 pada daerah mutan Y220C dan warna hitam menunjukkan MIRA-1.
Limitasi dari software dan hardware yang tidak diketahui maka dilakukan
percobaan memperkecil ukuran kompleks. Ukuran kompleks yang diperkecil ternyata memberikan masalah yang relatif sama dengan perhitungan dengan ukuran kompleks yang utuh. Ukuran kompleks (Gambar 10) yang sudah diperkecil jumlah atomnya menjadi 314 masih memberatkan ukuran kerja komputasi dan kesulitan dalam mengatur masalah konvergensi.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
30
Tabel 2. Jarak antara atom dari asam amino ke atom MIRA-1
Asam - asam amino yang sederet dengan asam amino sistein (target reaksi) yang mempunyai jarak relatif dekat terdapat atom C dan N asam amino dekat dengan atom O1 MIRA-1 masing – masing berjarak 4,028 Å dan 3,845 Å serta atom C asam amino berjarak 3,288 Å ke C7 MIRA-1 (Tabel 2). Maka asam amino selain sistein pada sisi ini yang diambil adalah asam amino 127 hingga 129 yaitu berturut – turut asam glutamat dan dua asam amino prolin. Asam amino 134 dan 136 mempunyai jarak yang juga dekat dengan MIRA-1, tetapi kedua asam amino berikatan peptida dengan asam amino sebelumnya yang jaraknya relatif jauh. Oleh karena itu, kedua asam amino tersebut tidak dimasukkan pada asam amino pilihan dalam pembentukan konfigurasi.
commit to user
nomor 54 hingga asam amino yang mengarah ke dalam lekukan mutasi yaitu asam amino 51. Asam amino 50 atom C-nya mempunyai jarak yang relatif jauh dengan O3 MIRA-1 sebesar 6,514 Å sehingga dibatasi hingga asam amino 51 yang diambil sebagai konfigurasi nantinya. Jumlah asam amino yang diambil pada sisi ini adalah 4 asam amino. Jadi total keseluruhan asam amino yang diambil sebagai pembentuk konfigurasi dalam perhitungan sebanyak 8 asam amino yaitu sistein, asam glutamat, 2 prolin, asam aspartat, valin, triptofan dan leusin. Dengan menggunakan pola pemilihan tersebut dapat dilihat dalam bentuk surface seperti
Gambar 11.
Gambar 11. Surface bagian asam amino – asam amino dari lekukan mutasi yang
berada di sekitar MIRA-1 dan warna hitam menunjukkan MIRA-1.
Hal tersebut menyebabkan tidak semua asam amino dalam surface tersebut
dihitung, tetapi hanya asam amino – asam amino pada surface warna merah.
Surface warna putih terdiri dari asam amino yang mayoritas mempunyai jarak
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
32
Interaksi spesifik antara MIRA-1 dengan asam amino – asam amino yang merupakan lingkungan dari lekukan mutasi terjadi ketika mempunyai jarak yang relatif dekat sehingga dapat memberikan pengaruh yang lebih besar terhadap distribusi kerapatan elektronnya. Interaksi – interaksi dari asam amino yang dipilih sudah cukup sehingga tidak perlu jarak yang terlalu jauh dan tidak semua asam amino digunakan dalam perhitungan. Oleh karena itu, dapat diasumsikan interaksi yang terdapat dari asam amino – asam amino tersebut telah dapat mewakili sistem protein atau lekukan mutasi.
B. Perhitungan Analisis Populasi
Interaksi spesifik antara sistein dan ikatan rangkap C-C MIRA-1 yang terkonjugasi gugus karbonil dapat menjelaskan kebolehjadian pembentukan
adduct tiol. Adduct merupakan ikatan kovalen yang terbentuk antara suatu
biomolekul dan non biomolekul. Pembentukan adduct mampu mengembalikan
konformasi p53 mendekati konformasi wild-type-nya. Interaksi spesifik dapat
ditunjukkan dengan perhitungan analisis populasi. Perhitungan itu melibatkan struktur elektronik yang dapat dipelajari dengan menggunakan metode mekanika kuantum.
Perhitungan analisis populasi pada penelitian ini menggunakan NBO. Perhitungan menggunakan level teori HF untuk memperoleh hasil perhitungan yang relatif akurat. Fungsi basis yang digunakan adalah 6-31G* yang dapat memberikan hasil perhitungan yang melibatkan pengaruh polarisasi ikatan dari senyawa organik. Perhitungan optimasi geometri dan single point NBO dapat
memberikan informasi distribusi kerapatan elektron yang dapat ditunjukkan melalui data occupancy dan muatan parsial.
commit to user N1. Gugus karbonil dapat mempengaruhi tarikan elektron dari ikatan rangkap C-C. Ikatan π pada ikatan rangkap C-C cenderung kurang stabil dibandingkan ikatan σ sehingga adanya pengaruh tarikan elektron menyebabkan kerapatan elektron pada ikatan π berkurang. Kerapatan elektron ikatan π pada ikatan rangkap C-C semakin rendah sebagai pengaruh dari dua gugus karbonil. Atom N1 juga dapat memberikan efek induksi yang akan mempengaruhi kerapatan elektron ikatan rangkap C-C semakin rendah.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
34
Tabel 3. Nilai muatan parsial masing – masing atom penyusun MIRA-1.
Atom Muatan Parsial Atom Muatan Parsial semakin negatif nilai muatan parsialnya menunjukkan semakin kaya elektron atau kemungkinan ditemukan elektron (kerapatan elektron) semakin besar. Kerapatan elektron ikatan rangkap C-C alkena cukup besar yang ditunjukkan dengan muatan parsial yang cukup negatif sebesar -0,41041. Nilai yang cukup negatif menunjukkan kemungkinan ditemukan elektron pada ikatan rangkap C-C besar. Nilai tersebut dapat menurun kenegatifannya dengan adanya tarikan elektron yang lebih kuat disekitarnya seperti pada ikatan rangkap C-C MIRA-1. Ikatan rangkap C-C pada MIRA-1 yang disimbolkan C1 dan C2 mendapatkan tarikan elektron yang cukup besar dari dua gugus karbonil yang mengapitnya sehingga kerapatan elektron ikatan rangkap C-C-nya menurun menjadi sebesar -0,25872 pada C1 dan -0,25871 pada C2 yang ditunjukkan pada Tabel 3. Perbedaan muatan parsial antar atom C1 dan C2 yang relatif sangat rendah maka diasumsikan polarisasi ikatan rangkap C-C simetris. Ikatan rangkap C-C alkena ataupun pada MIRA-1 teroptimasi sama – sama mempunyai nilai polarisasi simetris karena mempunyai tarikan atau dorongan elektron yang sama besar pada kedua sisinya.
commit to user
elektronnya ke atom C. Hal tersebut yang dapat berakibat atom C atau ikatan rangkap C-C karbon menjadi bernilai sangat negatif muatan parsialnya dengan mendapatkan sumbangan elektron dari atom H. Seperti halnya ikatan rangkap C-C karbon alkena, pada MIRA-1 kedua atom C ikatan rangkap C-C-nya juga sama – sama mendapat donor dari satu atom H. Namun, pada kedua atom C-nya mendapatkan tarikan elektron dari gugus karbonil. Hal tersebut berpengaruh pada nilai muatan parsial yang makin berkurang kenegatifannya. Tarikan elektron dan donor elektron yang sama besar menyebabkan polarisasinya simetris. Gugus karbonil yang mempunyai atom O dengan nilai keelektronegatifan 3,5 yang lebih besar dibandingkan atom C (2,5) sehingga gugus karbonil dapat menarik elektron dari atom karbon ikatan rangkap C-C dan mempengaruh kerapatan elektronnya menjadi lebih rendah. Struktur lingkar 5 simetris yang juga mempengaruhi tarikan elektron dari gugus karbonil sama besar ditunjukkan nilai muatan parsial dari atom O karbonil (O1 dan O3) yang relatif sama berturut – turut yaitu -0,63562 dan -0,63565 yang ditunjukkan pada Tabel 3.
Gugus ester pada bagian alifatik MIRA-1 mempunyai gugus karbonil (C6=O4) mempunyai kecenderungan terdapat tarikan elektron yang mengarah padanya. Atom O2 yang terikat antara atom C5 dan C6 sehingga atom O2 mendapatkan donor elektron dari kedua atom C tersebut. Atom C6 mempunyai muatan parsial yang paling positif (Tabel 3) karena mendapatkan tarikan elektron dari dua atom O (O2 dan O4) yang mempunyai elektronegatif tinggi terutama atom O4 yang berikatan rangkap cenderung lebih polar maka tarikan elektron yang diberikan ke C6 lebih besar dibandingkan O2. Tarikan elektron dari atom O4 gugus karbonil dapat memberikan efek induksi pada atom N yang menghubungkan antara bagian siklis dan alifatik MIRA-1. Atom N yang lebih elektronegatif dibandingkan atom C penyusun kerangka bagian siklis dapat memberikan tarikan elektronya dan mempengaruhi distribusi kerapatan elektron bagian siklis.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
36
11) sehingga dapat memberikan pengaruh besar terhadap distribusi kerapatan elektron MIRA-1 terutama pada ikatan rangkap C-C. Pembentukan konfigurasi dari asam amino terpilih dilakukan melalui penambahan asam amino – asam amino tersebut secara parsial. Hal tersebut dimaksudkan untuk melihat pengaruh tiap asam amino atau lingkungan disekitar MIRA-1 terhadap kerapatan elektron ikatan rangkap C-C MIRA-1 yang berpengaruh pada reaktivitasnya sehingga dapat memberikan informasi tentang kebolehjadian pembentukan adduct tiol.
Informasi distribusi kerapatan elektron ikatan rangkap C-C MIRA-1 sebagai pengaruh lingkungan disekitarnya diperoleh melalui single point NBO.
Single point dilakukan agar target reaksi dari kompleks yang diperoleh tidak
berubah posisinya. Perhitungan dimulai dari konfigurasi ke-0 yang hanya terdiri dari MIRA-1 (ligan). MIRA-1 yang diambil dari kompleks hasil docking yang
terdapat dalam lekukan mutasi ditunjukkan Gambar 13.
C5
Gambar 13. Struktur MIRA-1 dari kompleks Y220C-MIRA-1 hasil docking.
Gambar 13 menunjukkan bagian alifatik pada rantai karbon etil (-C2H5) tertekuk. Bagian alifatik yang fleksibel dapat mempengaruhi kerapatan elektron berbeda antara kedua atom C ikatan rangkap C-C. Kerapatan elektronnya ditunjukkan dengan nilai muatan parsial C1 sebesar -0, 25043 dan C2 sebesar -0,25163 yang menunjukkan terdapat perbedaan sebesar 0,00120.
commit to user
Bagian alifatik yang fleksibel suatu saat berada pada posisi tertentu yang dapat mempengaruhi kerapatan elektron dari ikatan rangkap C-C karbon menjadi asimetris.
Konfigurasi ke-0 yang terdiri dari MIRA-1 merupakan struktur yang selalu ada di semua konfigurasi – konfigurasi. Konfigurasi dibentuk dari lingkungan lekukan mutasi disekitar MIRA-1 yaitu asam amino – asam amino yang ditambahkan secara parsial ditunjukkan Gambar 14.
Gambar 14. Konfigurasi – konfigurasi dengan penambahan asam amino secara parsial dan nilai ∆occupancy C1=C2 dari masing – masing
tambahan asam amino. Warna putih, kuning, merah dan biru berturut – turut menunjukkan atom H (Hidrogen), S (Sulfur), O (Oksigen) dan N (Nitrogen). Hanya atom H polar yang ditampilkan untuk mendukung kejelasan gambar.
Gambar 14 menunjukkan konfigurasi ke-1 hingga ke-8 dengan penambahan asam amino satu per satu melalui ikatan peptidanya. Terdapat nilai ∆occupancy yang dituliskan berurutan kebawah menunjukkan nilai kerapatn
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
38
Nilai ∆occupancy merupakan nilai selisih antara nilai occupancy dari suatu
konfigurasi dengan nilai occupancy dari konfigurasi ke-0 (MIRA-1). ∆occupancy
bernilai positif berarti nilai occupancy konfigurasi yang terdapat pengaruh asam
amino lebih tinggi dibandingan konfigurasi nol. Hal tersebut menunjukan bahwa pengaruh lingkungan disekitar MIRA-1 yaitu asam amino meningkatkan kerapatan elektron dari ikatan rangkap C-C yang berarti reaktivitasnya turun. Nilai ∆occupancy negatif berarti reaktivitas ikatan rangkap C-C dengan adanya
lingkungan disekitar MIRA-1 meningkat karena kerapatan elektronnya lebih rendah sehingga kebolehjadian pembentukan adduct lebih tinggi. Setiap asam
amino – asam amino yang ditambahkan memberikan nilai ∆occupancy yang
berbeda – beda. Hal tersebut menunjukkan setiap asam amino mempunyai kontribusi yang berbeda – beda terhadap ikatan rangkap C-C.
Konfigurasi ke-1 dengan tambahan asam amino sistein terdapat atom S mempunyai jarak rata - rata dengan ikatan rangkap C-C sebesar 3,765 Å. Jarak yang cukup dekat untuk dapat memberikan induksi. Induksi yang diberikan pada ikatan rangkap C-C dapat meningkatkan kekuatan tarikan elektronnya terhadap gugus disekitarnya sehingga menjadikan kerapatan elektronnya meningkat. Itu ditunjukkan dengan nilai ∆occupancy-nya bernilai positif sebesar 0,00021.
Peningkatan kerapatan elektron menunjukkan reaktivitas ikatan rangkap C-C menjadi rendah terhadap serangan nukleofil (gugus tiol) yang diindikasi melalui reaksi addisi. Oleh karena itu, jika dalam sistem hanya terdapat sistein dan MIRA-1 maka kebolehjadian terbentuknya adduct tiol cukup rendah.
commit to user
ikatan rangkap C-C.
Konfigurasi ke-3 dan ke-4, keduanya mempunyai tambahan asam amino prolin yang mempunyai jarak O ke O1 MIRA-1 masing – masing sebesar 5,919 Å dan 7,658 Å. Jarak tersebut cukup jauh untuk asam amino nonpolar dapat memberikan induksinya. Induksi yang dapat diberikan dari asam amino nonpolar lebih lemah dibandingkan asam amino polar atau bahkan tidak dapat memberikan induksi. Oleh karena itu, induksi yang muncul tetap dari atom O gugus karbonil asam amino asam glutamat yang yang bersifat polar dan mempunyai jarak lebih dekat dibandingkan kedua konfigurasi tersebut yaitu 4,108 Å. Induksi dari asam amino pada kedua konfigurasi yang muncul tetap dari gugus karbonil asam amino asam glutamat mempengaruhi kerapatan elektronnya. Asam amino nonpolar gugus penyusunnya pendorong elektron yang ketika berikatan peptida dengan gugus karbonil dapat meningkatkan kepolaran gugus karbonil. Konfigurasi ke-3 asam amino prolin berikatan peptida gugus karbonil asam glutamat sehingga dapat meningkatkan kepolaran gugus karbonil. Hal tersebut mempengaruhi semakin besarnya tarikan elektron atom O karbonil asam glutamat yang dapat ditunjukkan dengan nilai kerapatan elektronnya semakin negatif berturut – turut tanpa atau dengan adanya gugus amino yang mengikatnya dari konfigurasi ke-2, ke-3 dan ke-4 yaitu -0,74354, -0,79603 dan -0,80385. Peningkatan kepolaran atau tarikan elektron atom O gugus karbonil dapat meningkatkan induksi ke atom O1 bagian maleimida MIRA-1 sehingga makin berkurang pula kerapatan elektron ikatan rangkap C-C. Pengaruh asam amino prolin memberikan nilai ∆occupancy
yang cukup rendah berturut – turut pada konfigurasi ke3 dan ke4 sebesar -0,00427 dan -0,00434.