TESIS
UJI DIAGNOSTIK EKUIVALEN HEMOGLOBIN
RETIKULOSIT DAN INDIKATOR RESPON TERAPI
PADA ANEMIA DEFISIENSI BESI
ARUNDINA SANYOTO
NIM : 1114048101
PROGRAM MAGISTER
PROGRAM STUDI BIO-MEDIK
KEKHUSUSAN KEDOKTERAN KLINIK
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
UJI DIAGNOSTIK EKUIVALEN HEMOGLOBIN
RETIKULOSIT DAN INDIKATOR RESPON TERAPI
PADA ANEMIA DEFISIENSI BESI
Tesis untuk Memperoleh Gelar Magister pada Program Magister, Program Combined Degree,
Program Pascasarjana Universitas Udayana
ARUNDINA SANYOTO
NIM : 1114048101
PROGRAM MAGISTER
PROGRAM STUDI ILMU BIOMEDIK
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
DENPASAR
Lembar Persetujuan Pembimbing
TESIS INI TELAH DISETUJUI PADA TANGGAL 11 Juli 2016
Pembimbing I,
DR. dr. Ketut Suega, SpPD-KHOM
NIP. 195704061983121001
Pembimbing II,
dr. Wayan Losen Adnyana, SpPD-KHOM
NIP. 197101192000121005
Mengetahui
Ketua Program Studi Ilmu Biomedik Program Pascasarjana Universitas
Udayana
Dr. dr. G. N. Indraguna Pinatih,MSc,SpGK NIP. 195805211985031002
Direktur Program Pascasarjana
Universitas Udayana
Prof. Dr. dr. A.A. Raka Sudewi,SpS(K)
Tesis Ini Telah Diuji pada
Tanggal 11 Juli 2016
Panitia Penguji Tesis Berdasarkan SK Rektor Universitas Udayana
No :2937/UNI4.4/HK/2016, Tanggal 23 Juni 2016
Panitia Penguji Tesis adalah :
Ketua : DR.dr Ketut Suega, SpPD – KHOM
Sekretaris : dr. I Wayan Losen Adnyana, SpPD – KHOM Anggota :
1. Prof.dr.N. Tigeh Suryadhi, MPH, Ph.D
Pertama-tama perkenankanlah penulis memanjatkan puji syukur ke hadapan
Allah Tritunggal Mahakudus, karena hanya anugerahNya, tesis ini dapat
diselesaikan.
Pada kesempatan ini perkenankanlah penulis mengucapkan terimakasih
yang sebesar- besarnya kepada DR. dr. Ketut Suega, SpPD-KHOM FINASIM
sebagai pembimbing I yang dengan penuh perhatian telah memberikan dorongan,
semangat, bimbingan, dan saran selama penulis mengikuti program magister,
khususnya dalam penyelesaian tesis ini. Terima kasih sebesar-besarnya pula
penulis sampaikan kepada dr. Wayan Losen Adnyana, SpPD-KHOM FINASIM
sebagai pembimbing II yang dengan penuh perhatian dan kesabaran telah
memberikan bimbingan dan saran kepada penulis. Ucapan terima kasih juga
disampaikan kepada Prof. DR. dr. I Made Bakta, SpPD-KHOM, FINASIM yang
telah membimbing, mengkoreksi, dan mengarahkan segala upaya penyelesaian
tesis ini.
Ucapan yang sama juga ditujukan kepada Rektor Universitas Udayana Prof.
Dr. dr. Ketut Suastika SpPD-KEMD, FINASIM atas kesempatan dan fasilitas yang
diberikan kepada penulis untuk mengikuti dan menyelesaikan pendidikan Program
Magister di Universitas Udayana. Ucapan terimakasih ini juga ditujukan kepada
Direktur Program Pascasarjana Universitas Udayana yang dijabat Prof. Dr. dr. A.A.
Raka Sudewi, Sp.S (K) atas kesempatan yang diberikan kepada penulis untuk
menjadi mahasiswa Program S2 pada Program Pascasarjana Universitas Udayana.
kepada penulis untuk mengikuti pendidikan program magister. Pada kesempatan
ini, penulis juga menyampaikan rasa terimakasih kepada Kepala Program Studi
Ilmu Penyakit Dalam, Prof. Dr. dr. IDN. Wibawa SpPD KGEH dan Dr. dr. I Ketut
Suega SpPD KHOM selaku Kepala Laboratorium Ilmu Penyakit Dalam RSUP
Sanglah Denpasar. Ungkapan terima kasih penulis sampaikan pula kepada para
penguji, yaitu Prof. dr. N.Tigeh Suryadhi, MPH, Phd, DR. dr. Desak Made
Wihandani, M. Kes, DR. dr G.N. Indraguna Pinatih, MSc. yang telah memberikan
masukan, saran, sanggahan, dan koreksi sehingga tesis ini dapat terwujud seperti
ini.
Pada kesempatan ini ijinkan juga penulis mengucapkan terima kasih dan
penghormatan yang tulus kepada Prof. Dr. dr Tjok Raka Putra, SpPD-KR, sebagai
mantan Kepala Bagian /SMF Ilmu Penyakit Dalam FK Unud/ RSUP Sanglah dan
Prof. Dr. dr Ketut Suwitra, SpPD-KGH sebagai mantan Ketua Program Studi Ilmu
Penyakit Dalam FK Unud/ RSUP Sanglah yang pada masanya telah memberi
kesempatan kepada penulis untuk mengikuti pendidikan spesialisasi. Penulis juga
memberikan ucapan yang sama kepada Prof. Dr. dr Tjok Raka Putra, SpPD-KR
sebagai pembimbing akademik penulis atas arahan dan bimbingan selama
mengikuti pendidikan spesialis Ilmu Penyakit Dalam.
Pada kesempatan ini penulis menyampaikan ucapan terima kasih yang tulus
disertai penghargaan kepada seluruh guru-guru yang telah membimbing penulis,
mulai dari sekolah dasar sampai perguruan tinggi. Juga penulis ucapkan terima
kasih kepada kedua orang tua, Papa Drs. Y Setyanto Sanyoto (alm) dan Mama Dra.
Indirawati yang senantiasa memberikan dorongan moril dan matriil, motivasi, dan
Papa Yan Sunur dan Mama Flora Krtayasa yang selalu mendukung dalam
penyelesaian studi ini. Suami saya tercinta dr. Yeremias Ronaldy Sunur yang selalu
ada dalam suka dan duka, sehat maupun sakit, berat dan ringan menjalani bahtera
rumah tangga dan pendidikan spesialis ini. Anakku tercinta Alexander Ronaldo
Sunur yang telah memberikan pengertian, penghiburan dan kasih sayang selama
menjalani pendidikan ini, Adik saya Sonia Ardelia Sanyoto, SSn yang selalu
mendukung dan memotivasi penulis agar dapat menyelesaikan pendidikan. Penulis
juga mengucapkan terimakasih pada rekan residen seperjuangan dan sahabat
tercinta atas motivasi dan persahabatan yang kalian berikan selama ini. Juga kepada
paramedis, staf tata usaha Bagian /SMF Ilmu Penyakit Dalam FK Unud/ RSUP
Sanglah atas segala bantuan serta kerjasama yang baik selama menjalani
pendidikan spesialis Ilmu Penyakit Dalam.
Semoga Allah Tri Tunggal Mahakudus selalu melimpahkan rahmat-Nya
kepada semua pihak yang telah membantu pelaksanaan dan penyelesaian tesis ini,
serta kepada penulis sekeluarga.
RETIKULOSIT DAN INDIKATOR RESPON TERAPI PADA ANEMIA DEFISIENSI BESI
ABSTRAK
Latar Belakang : Anemia Defisiensi Besi (ADB) telah menjadi masalah di dunia dan di Indonesia. Dampak dari defisiensi besi beraneka ragam dan sangat merugikan. Diagnosis ADB mudah tapi dapat menyulitkan pada beberapa kondisi tertentu. Feritin yang merupakan tes terbaik dalam menilai cadangan besi merupakan protein fase akut yang kadarnya dapat dipengaruhi oleh kondisi inflamasi. Keberhasilan terapi pada ADB ditandai dengan peningkatan kadar hemoglobin sebesar 1-2 gr/dl setelah diberikan terapi besi selama 4 minggu.
Ret-He (Equivalent Hemoglobin Reticulocyte) adalah modalitas pemeriksaan baru yang
dapat mengetahui ketersediaan cadangan besi untuk eritropoesis pada 3-4 hari kedepan yang relatif tidak dipengaruhi oleh kondisi inflamasi. Kadar Ret-He juga diketahui meningkat lebih awal setelah pemberian terapi besi.
Tujuan : mengetahui akurasi Ret-He dalam mendiagnosis ADB dan sebagai indikator respon terapi pada penderita ADB.
Metode : Terdapat 2 tahap pada penelitian ini yaitu uji diagnostik Ret-He dengan Feritin < 20 ug/L sebagai baku emas dan studi longitudinal analitik untuk mengetahui perubahan Ret-He dibandingkan dengan hemoglobin, retikulosit dan indeks eritrosit sebagai indikator respon terapi ADB. Pengambilan sampel untuk tahap pertama dilakukan secara konsekutif dengan mengikut sertakan penderita yang berusia diatas 18 tahun dengan kadar Hb <10 gr/dl yang berobat ke RSUP Sanglah dan RSU Bangli dan untuk tahap kedua mengikut sertakan penderita ADB yang terdiagnosis pada tahap pertama. Penderita yang telah terdiagnosis ADB diberikan terapi besi oral selama 4 minggu dan diperiksa hemoglobin, hematokrit, retikulosit, Ret-He dan MCV setiap minggu. indikator yang lain dan peningkatan tersebut bermakna yang dinyatakan dengan nilai p<0,001 melalui uji Kruskal Wallis.
Kesimpulan : Ret-He 25 pg memiliki sensitivitas yang terbaik dalam mendeteksi ADB dan Ret-He merupakan indikator respon terapi ADB yang lebih awal dibandingkan hemoglobin, retikulosit dan indeks eritrosit.
DIAGNOSTIC TEST EQUIVALENT HEMOGLOBIN RETICULOCYTE AND AS INDICATOR OF RESPONSE TO THERAPY IN IRON
DEFICIENCY ANEMIA
ABSTRACT
Background: Iron deficiency anemia (IDA) has become a major problem in the world and in Indonesia. The impact of IDA were various and gave many negative effects. Diagnosing IDA was easy but can be tricky in various condition. Ferritin which is the best test to measure iron store is a acute phase protein and its level depends on chronic inflammation. The goal of therapy in IDA condition is increasing of hemoglobin level 1-2 gr/dl after 4 weeks oral iron therapy. Ret-He (Equivalent Hemoglobin Reticulocyte) is a new modality to diagnose iron deficient because it can show the availability iron that was needed for erythropoesis process 3-4 days after. This test also didn’t interfere with inflammation condition. There’s an early increase of Ret-He after having iron therapy.
Aim: to search the acuration of Ret-He on diagnosing IDA and as indicator of response to therapy in IDA.
Study Design and Methods: There were two step in this study, the first was diagnostic test for Ret-He using Ferritin <20 ug/l as gold standard. The second was a analytic longitudinal study to search the alteration of Ret-He compare to hemoglobin, reticulocyte and erithrocyte index as indicator of response therapy in IDA. Sample collecting for the first step was concecutive involving patient with age >18 years old and hemoglobin <10 gr/dl who come to the Sanglah General Hospital and Bangli General Hospital and for the second step involving all IDA patients who were confirmed in the first step. All IDA patients were given oral iron therapy for 4 weeks and every week a Complete Blood Test (CBC), Reticulocyte count and Ret-He were performed.
Results: 87 patient were included in this study (41 men and 46 women) with mean of Hemoglobin 7.42 mg/dL, Serum Iron (SI) 42.71 mg/dl, TIBC 242.82 mg/dL, Ferritin 799 ug/L and Ret-He 23.63 pg. Ret-He value 25 pg had a sensitivity 97.2% (95% CI 83.79%-99.85%), spesificity 66.67% (95% CI 51.97%-78.85%), positive predictive value 67.30% (95% CI 52.77%-79.28%), negative predictive value 97.14% (95% CI 83.38%-99.85%). 26 IDA patients were diagnosed and were given oral iron therapy for 4 weeks. An early increase of Ret-He was found compare to other indicator and it was significant with p <0.001.
Conclusions: Ret-He 25 pg got the best sensitivity when used to screen IDA and Ret-He can be used as early indicator of response to therapy in IDA.
DAFTAR ISI
2.2 Pemeriksaan Kadar Ekuivalen Hemoglobin Retikulosit (Ret-He) dalam Diagnosis ADB ... 22
2.2.1 Pendahuluan ... 22
2.2.3 Automated hematology analyszer ... 23
2.3 Aplikasi Klinis Ret-He dalam Diagnosis ADB ... 25
2.4 Keterbatasan Ret-He dalam Diagnosis ADB ... 26
BAB III KERANGKA BERPIKIR, KONSEP DAN HIPOTESIS PENELITIAN ... 28
4.7 Definisi Operasional Variabel ... 36
4.8 Tempat dan Waktu Penelitian ... 38
5.1 Karakteristik Subyek Penelitian ... 43
DAFTAR TABEL
Halaman
4.1 Perhitungan Jumlah Sampel per Variabel ... 34
5.1 Karakteristik Subyek Penelitian ... 43
5.2 Jenis Anemia ... 44
5.3 Perbandingan Karakteristik Umur pada Kedua Kelompok... 44
5.4 Perbandingan Karakteristik Jenis Kelamin, Pendidikan, dan Pekerjaan pada Kedua Kelompok ... 45
5.5 Cut off Ret-He < 25 pg ... 46
5.6 Cut off Ret-He < 26 pg ... 46
5.7 Cut off Ret-He < 27 pg ... 47
5.8 Cut off Ret-He < 29 pg ... 47
5.9 Data Dasar Parameter Hematologi pada 26 Penderita ADB... 49
5.10 Perbandingan Peningkatan Nilai Indikator Respon Terapi ADB ... 49
5.11 Uji Repeated Anova pada Indikator Hemoglobin ... 50
5.12 Hasil Uji Paired Wise Comparison pada Indikator Hemoglobin ... 50
5.13 Uji Repeated Anova pada Indikator Hematokrit ... 51
5.14 Hasil Uji Paired Wise Comparison pada Indikator Hematokrit ... 51
5.15 Uji Repeated Anova pada Indikator MCV ... 52
5.16 Hasil Uji Paired Wise Comparison pada Indikator MCV ... 52
5.17 Uji Repeated Anova pada Indikator Retikulosit ... 53
5.18 Hasil Uji Paired Wise Comparison pada Indikator Retikulosit ... 53
5.19 Uji Repeated Anova pada Indikator Ret-He ... 54
5.20 Hasil Uji Paired Wise Comparison pada Indikator Ret-He ... 54
5.21 Persentase Peningkatan Nilai Indikator Respon Terapi ADB ... 55
5.22 Perbandingan Persentase Peningkatan Nilai Indikator Respon Terapi ADB pada Minggu I ... 55
DAFTAR GAMBAR
Halaman
2.1 Siklus Pertukaran Besi dalam Tubuh ... 13
2.2 Stadium Patogenesis Defisiensi Besi ... 14
3.1 Kerangka Berpikir I ... 28
3.2 Kerangka Berpikir II ... 29
3.3 Konsep Penelitian ... 29
4.1 Rancangan Penelitian I... 32
4.2 Rancangan Penelitian II ... 32
4.3 Alur Penelitian ... 41
DAFTAR SINGKATAN
SINGKATAN
ADB : Anemia Defisiensi Besi BFU-E : Burst Forming Unit Erythroid
CFU-E : Colony Forming Unit Eryhtroid
CHr : Reticulocyte Hemoglobin Content
CI : Confidence Interval
IDA : Iron Deficient Anemia
IK : Interval Kepercayaan
K/DIGO : Kidney Disease Improving Global Outcome
MCV : Mean Corpuscular Volume
MCH : Mean Corpuscular Hemoglobin
MCHC : Mean Corpuscular Hemoglobin Concentration
RDW : Red Cell Distribution Width
Ret-He : Equivalent Hemoglobin Reticulocyte
PGK : Penyakit Ginjal Kronis
SI : Serum Iron
SKRT : Survei Kesehatan Rumah Tangga sTfR : Soluble or Serum Transferrin Receptor
TfR : Transferrin Receptor
TIBC : Total Iron Binding Capacity
TSAT : Transferrin Saturation
WHO : World Health Organization
DAFTAR LAMPIRAN
No Lampiran Judul Lampiran Halaman
Lampiran 1. Informed Consent ... ... 70
Lampiran 2. Formulir Persetujuan ... 73
Lampiran 3. Jadwal Penelitian ... 74
Lampiran 4. Anggaran Penelitian ... 75
Lampiran 5. Formulir Pengumpulan Data ... 76
Lampiran 6. Prosedur Pemeriksaan Hemoglobin ... 79
Lampiran 7. Prosedur Pemeriksaan Ret-He (Reticulocyte Hemoglobin Equivalent) ... 81
Lampiran 8. Prosedur Pemeriksaan Feritin ... 83
Lampiran 9. Surat Kelaikan Etik ... 85
Lampiran 10. Data Penelitian ... 89
B A B I PENDAHULUAN
1.1Latar Belakang
Indonesia sebagai salah satu negara berkembang saat ini terus melakukan
pembangunan dalam segala bidang. Pertumbuhan ekonomi yang baik,
peningkatan taraf hidup setiap insan dan perbaikan tingkat kesehatan menjadi
target dalam pembangunan. Namun masalah gizi masih menjadi problem utama
dalam perbaikan tingkat kesehatan penduduk Indonesia khususnya zat besi. Besi
memegang peranan penting dalam metabolisme khususnya dalam proses reaksi
transfer elektron (Kaushansky, et al. 2010).
Anemia Defisiensi Besi (ADB) ternyata tidak hanya menjadi masalah di
Indonesia tetapi juga di seluruh dunia. Organisasi kesehatan dunia (WHO) tahun
2005 memperkirakan sekitar 24,8% dari penduduk di dunia terkena ADB dengan
kelompok yang paling tinggi prevalensinya adalah ibu hamil, usia lanjut dan
diikuti oleh bayi dan anak usia dua tahun, anak usia pra sekolah, anak usia sekolah
dan wanita tidak hamil. Di Indonesia berdasarkan Riset Kesehatan Dasar
(Riskesdas) tahun 2007, menunjukkan bahwa prevalensi anemia pada ibu hamil
59%, anak-anak 70,1%, wanita usia subur (WUS) 59,9% dan laki-laki dewasa
sebesar 33,4%. Sedangkan di Bali berdasarkan studi yang dilakukan oleh Suega,
et al. 2002 yang khususnya meneliti prevalensi ADB pada wanita hamil di Bali
menemukan sebesar 46,2% ibu hamil menderita ADB ringan. Dampak dari
defisiensi besi adalah terjadi gangguan perkembangan baik motorik maupun
kognitif, gangguan metabolisme, penurunan daya tahan tubuh dan banyak dampak
Anemia defisiensi besi adalah anemia yang timbul akibat kosongnya
cadangan besi tubuh (depleted iron store) sehingga penyediaan besi untuk
eritropoesis berkurang, yang pada akhirnya pembentukan hemoglobin berkurang.
Diagnosis ditegakkan dengan ditemukannya keadaan kekurangan gizi, kehilangan
darah secara kronis atau adanya penyebab lain dan dengan menggunakan
modifikasi dari kriteria Kerlin (Bakta, 2006).
Pemeriksaan baku emas dalam menegakkan diagnosis ADB adalah
pengecatan sumsum tulang dengan tinta biru prusia dimana akan ditemukan
butir-butir besi atau hemosiderin tetapi karena adanya beberapa kendala seperti
prosedur yang bersifat invasif, variabilitas antar pemeriksa serta kendala biaya
maka pemeriksaan ini mulai digantikan dengan pemeriksaan tes hematologi
seperti hemoglobin, indeks eritrosit dan pemeriksaan biokimia berdasarkan
metabolisme besi seperti feritin, besi serum, saturasi transferin dan Soluble or
Serum Transferrin Receptor (sTfR). Alternatif lain dalam menegakkan diagnosis
ADB adalah berdasarkan respons hematologik setelah pemberian terapi
suplementasi besi yaitu adanya peningkatan jumlah hemoglobin, retikulosit atau
indeks retikulosit setelah pemberian terapi besi oral atau intravena (Brugnara,
2002 ; Kotisaari, et al. 2003 ; Mast, et al. 2008).
Gambaran eritrosit hipokromik melalui pemeriksaan hematologik merupakan
indikator langsung adanya kondisi defisiensi besi fungsional namun pemeriksaan
ini tidak sensitif sebagai indikator awal kondisi iron deficient erythropoiesis.
Sedangkan pemeriksaan biokimia merupakan indikator tidak langsung karena
berdasarkan pengukuran yang mencerminkan kondisi iron deficient
sensitivitas dan spesifisitas pemeriksaan biokimia dan hematologi terhadap
pengecatan besi sumsum tulang sebagai baku emas diagnosis ADB menemukan
feritin merupakan tes terbaik dalam menilai cadangan besi (Thomas dan Thomas,
2002 ; Mast, 2008).
Pada konsensus K/DIGO tahun 2012 (Kidney Disease Improving Global
Outcome) mengenai penatalaksanaan anemia pada penyakit ginjal kronis (PGK),
pemeriksaan feritin dan saturasi transferin digunakan untuk menentukan status
besi pada penderita penyakit ginjal kronis dengan anemia yang mendapatkan
terapi suplementasi besi dan eritropoetin.
Menurut WHO, nilai cut off feritin untuk mendiagnosis ADB digunakan
angka 15 μg/L tetapi untuk daerah tropik dimana angka infeksi dan inflamasi
masih tinggi maka nilai cut off yang diajukan di negeri barat tampaknya perlu
dikoreksi. Hercberg tahun 1991 menganjurkan untuk daerah tropik digunakan
batas nilai serum feritin sebesar <20μg/L. Batasan nilai Feritin yang dipakai untuk
mendiagnosis ADB berdasarkan modifikasi kriteria Kerlin adalah <20 μg/L.
Suega et al. 2007 melalui studinya yang membandingkan beberapa metode
diagnosis ADB pada penderita di RSUP Sanglah menemukan bahwa serum
Feritin memiliki sensitivitas dan spesifisitas paling tinggi dalam mendiagnosis
ADB yaitu sebesar 90,6% dengan nilai cut off 35,4 μg/L.
Ini senada dengan studi yang dilakukan oleh Thomas dan Thomas tahun 2002
yang juga menemukan pemeriksaan feritin memiliki spesifisitas yang tinggi yaitu
sebesar >90% walaupun dengan nilai cut off yang lebih rendah yaitu <21,3 μg/l
Feritin merupakan protein fase akut dan kadarnya akan dipengaruhi oleh
kondisi inflamasi kronis dari pasien seperti kanker dan penyakit kronis yang lain,
maka penggunaannya untuk menegakkan diagnosis ADB terbatas pada beberapa
kondisi (Brugnara, 2002 ; Mast, 2002 ; Thomas dan Thomas, 2002 ; Mast, et al.
2008 ; Swart, et al. 2014).
Beberapa keterbatasan tes biokimia lain bila digunakan dalam mendiagnosis
ADB misalnya : (Wu, 2002 ; Wish, 2006)
1. Total Iron Binding Capacity (TIBC) yang mengukur secara tidak langsung
kadar transferin juga dipengaruhi oleh inflamasi, malnutrisi, infeksi kronis dan
kanker
2. Besi serum dipengaruhi oleh variasi diurnal, jenis diet, inflamasi dan infeksi
3. Saturasi Transferin yang didapatkan berdasarkan pembagian besi serum dan
TIBC dipengaruhi oleh inflamasi dan variasi diurnal
4. Soluble or Serum Transferin Receptor yang mengukur jumlah reseptor
transferin pada retikulosit diketahui merupakan indikator defisiensi besi yang
terbaik tetapi belum terdapat banyak studi mengenai efisiensi tes ini dalam
mendiagnosis defisiensi besi, belum terdapat nilai cut off yang resmi dan
tidak banyak tersedia.
Dengan demikian walaupun diagnosis ADB mudah tetapi dapat cukup
menyulitkan seperti pada kondisi penyakit akut dan kronis. Skrining dengan
tujuan menemukan kondisi defisiensi besi sebelum timbulnya anemia dengan
menggunakan parameter pemeriksaan hematologi dan biokimia menjadi tidak
praktis akibat pengaruh dari faktor tersebut (Brugnara, et al. 1994 ; Brugnara,
Penemuan teknologi flowcytometric memberikan kemudahan dalam
menegakkan diagnosis ADB. Instrumen pemeriksaan hematologi yang diproduksi
oleh Bayer® yaitu ADVIA 120® dan Sysmex® yaitu Sysmex Analysers XE and
XN Series® menyediakan pemeriksaan yang dapat mengukur kadar hemoglobin
yang terkandung dalam sel eritrosit muda atau retikulosit dimana pemeriksaan ini
disebut Reticulocyte Hemoglobin Content (CHr pada ADVIA) atau Equivalent
Hemoglobin Reticulocyte (Ret-He pada Sysmex). CHr merupakan produk
penghitungan volume sel dikalikan konsentrasi hemoglobin di dalam sel
retikulosit sedangkan Ret He mengukur inkorporasi besi di dalam hemoglobin
retikulosit sehingga dapat menghasilkan estimasi langsung dari ketersediaan besi
dalam erythron (Urrechaga, 2014).
Dalam keadaan normal retikulosit merupakan sel eritrosit muda yang
dilepaskan dari sumsum tulang menuju sirkulasi perifer. Proses maturasi
retikulosit berlangsung selama 1-3 hari di sumsum tulang kemudian masuk ke
sirkulasi perifer dan berada di sana selama 1-2 hari sebelum berubah menjadi
eritrosit matur. Atas dasar masa hidup retikulosit yang singkat inilah pengukuran
kadar hemoglobin retikulosit secara tidak langsung dapat memberikan informasi
ketersediaan besi fungsional yang dapat dipakai untuk memproduksi sel darah
merah yang baru dalam jangka waktu 3-4 hari ke depan sehingga pemeriksaan ini
dapat dipakai dalam mendiagnosis ADB (Brugnara, et al. 1994 ; Kotisaari, et al.
2003 ; Brugnara, 2006 ; Mast, 2008).
Bila digunakan dalam menilai respons hematologik setelah pemberian terapi
suplementasi besi, sebuah studi yang dilakukan oleh Kotisaari dkk menemukan
ADB mendapatkan terapi suplementasi besi, dan hal ini juga senada dengan studi
yang dilakukan oleh Brugnara tahun 1994 yang menemukan bahwa terdapat
peningkatan kadar CHr dengan rata-rata 3,2 pg setelah diberikan terapi selama 1
minggu. Bila dibandingkan dengan pemeriksaan hemoglobin yang baru
memberikan peningkatan sebesar 1-2 gr/dL setelah diberikan terapi selama 1
bulan tentunya CHr memberikan hasil yang lebih cepat (Brugnara, et al. 1994 ;
Kotisaari, et al. 2003 ; Mast, 2008).
Pemeriksaan retikulosit juga dapat dipakai untuk pengamatan respons terapi
subtitusi ADB tetapi berdasarkan studi yang dilakukan oleh Buttarello tahun 2004
dan 2008 menunjukkan CHr lebih cepat dalam menunjukkan respons terapi
karena dalam 48 jam setelah diberikan terapi telah terjadi peningkatan (Butarello,
2004).
Kelebihan CHr dan Ret-He adalah pemeriksaan ini relatif tidak dipengaruhi
oleh proses inflamasi, infeksi akut dan kronis, faktor diet dan variasi diurnal, serta
lebih ekonomis dan lebih cepat dalam menunjukkan keberhasilan terapi, sehingga
merupakan indikator yang sensitif dalam mendiagnosis defisiensi besi dan
skrining defisiensi besi sekaligus sebagai indikator respons terapi walaupun belum
ditemukan nilai cut off yang terstandarisasi secara resmi (Mast, et al. 2002 ;
Brugnara, 2003 ; Ullrich, et al. 2005 ; Brugnara, 2006 ; Mast, 2007 ; Urrechaga, et
al. 2009 ; Swart, et al. 2014 ; Urrechaga, 2014).
Brugnara pada tahun 2003 telah melakukan studi untuk mencari nilai cut off
CHr dalam memprediksi defisiensi besi pada beberapa populasi dengan hasil
terdapat perbedaan nilai CHr pada bayi, anak dan dewasa dimana nilai CHr < 27,2
pada anak dipakai nilai <28,4 pg (Brugnara,2003). Studi oleh Ullrich tahun 2005
yang melakukan skrining defisiensi besi pada bayi yang sehat menggunakan nilai
CHr sebesar 27,5 pg (Ullrich, 2005). Variabilitas nilai CHr yang tergantung usia
pada bayi dan anak-anak disebabkan karena adanya perubahan nilai MCV (Mean
Corpuscular Volume) dan MCH (Mean Corpuscular Hemoglobin) pada awal 2
tahun kehidupan (Brugnara, 2003).
Tahun 2006 Brugnara kembali melakukan studi untuk membandingkan nilai
Ret-He pada Sysmex dan CHr pada Bayer ADVIA dan ditemukan hasil yang
senada. Urrechaga tahun 2009 mencoba mencari nilai cut off Ret-He menegakkan
diagnosis ADB pada penderita dewasa dan ditemukan nilai < 29 pg. Sedangkan
studi oleh Karlsson tahun 2011 pada orang tua dengan kondisi anemia
menemukan nilai CHr 30,5 pg sebagai cut off. CHr juga digunakan dalam
mendeteksi defisiensi besi pada penderita yang menjalani hemodialisis dan
digunakan pula sebagai indikator respon terapi eritropoetin pada penderita anemia
pada gagal ginjal (Kaneko, 2003 ; Brugnara, 2006 ; Buttarelo, 2010 ; Karlsson,
2011).
Di Indonesia publikasi tentang penggunaan CHr dan Ret-He untuk
mendiagnosis ADB belum banyak didapatkan. Konsensus Manajemen Anemia
pada Penyakit Ginjal Kronik 2011 menetapkan kadar hemoglobin retikulosit <29
pg sebagai pertanda defisiensi besi. Sebuah penelitian yang dilakukan oleh
Primiastanti pada wanita usia reproduksi ditemukan kadar Ret-He sebesar 33,65
pg sebagai prediktor defisiensi besi walaupun sensitivitas dan spesivisitas kurang
Pemeriksaan Ret-He ini ternyata sangat penting dalam mendiagnosis
defisiensi besi namun belum terdapat standarisasi nilai cut off dan belum sering
digunakan. Atas dasar inilah penelitian ini dilakukan untuk mengetahui apakah
pemeriksaan ekuivalen hemoglobin retikulosit dapat dipakai menjadi salah satu
modalitas pemeriksaan untuk mendiagnosis ADB sekaligus sebagai indikator
keberhasilan terapi pada ADB.
1.2 Rumusan Masalah
1. Berapakah akurasi (sensitivitas, spesifisitas, nilai prediksi positif, nilai
prediksi negatif) dari Ret-He dibandingkan dengan feritin dalam diagnosis
ADB ?
2. Apakah pemeriksaan Ret-He lebih baik sebagai indikator respon terapi
ADB bila dibandingkan dengan hemoglobin, retikulosit dan indeks
eritrosit?
1.3 Tujuan Penelitian 1.3.1 Tujuan umum
Untuk mengetahui peran Ret-He dalam diagnosis ADB dan sebagai
indikator keberhasilan terapi pada ADB
1.3.2 Tujuan khusus
1. Untuk mengetahui akurasi Ret-He (sensitivitas, spesifisitas, nilai
prediksi positif, nilai prediksi negatif) dibandingkan dengan Feritin
dalam mendiagnosis ADB.
2. Untuk menilai peran Ret-He sebagai parameter respons terapi
dibandingkan dengan hemoglobin, retikulosit dan indeks retikulosit.
Mendapatkan pemeriksaan baru untuk diagnostik ADB yang dapat
digunakan sebagai kriteria diagnosis ADB
1.4.2 Manfaat praktis
Proses diagnosis ADB akan lebih mudah karena pemeriksaan ini lebih
cepat, praktis dan ekonomis serta tidak dipengaruhi penyakit kronis. Selain
BAB II
KAJIAN PUSTAKA
1.1Anemia Defisiensi Besi 1.1.1 Definisi
Anemia defisiensi besi adalah anemia yang timbul akibat kosongnya
cadangan besi tubuh (depleted iron store) sehingga penyediaan besi untuk
eritropoesis berkurang, yang pada akhirnya pembentukan hemoglobin berkurang.
Kelainan ini ditandai oleh anemia hipokromik mikrositer, besi serum menurun,
TIBC (Total Iron Binding Capacity) meningkat, saturasi transferin menurun,
feritin serum menurun, pengecatan besi sumsum tulang negatif dan adanya respon
terhadap pengobatan dengan preparat besi (Bakta, 2006).
1.1.2 Epidemiologi
Organisasi kesehatan dunia (WHO) memperkirakan sekitar 24,8% dari
penduduk di dunia menderita anemia dengan kelompok yang paling tinggi
prevalensinya adalah ibu hamil, usia lanjut dan diikuti oleh bayi dan anak usia dua
tahun, anak usia pra sekolah, anak usia sekolah dan wanita tidak hamil. Pada
jumlah absolut anemia terjadi pada 1,62 miliar orang di seluruh dunia dengan
komposisi 293 juta anak usia balita, 56 juta ibu hamil dan 468 juta wanita yang
tidak hamil (WHO, 2005).
Setengah dari kejadian anemia di seluruh dunia merupakan anemia defisiensi
besi. WHO memperkirakan bahwa pada tahun 2004 ADB telah menyebabkan
273.000 kematian dimana 45% terjadi di Asia Tenggara, 31% di Afrika, 9% di
Mediterania timur, 7% di Amerika, 4% di area Pasifik Barat dan 3% di Eropa
rendah sampai menengah. Akibat ADB terjadi penurunan produktivitas kerja yang
berakibat menurunnya pendapatan negara dengan rerata pada 10 negara
berkembang sebesar $16,78 per kapita atau 4% dari pendapatan negara secara
kasar (Pasricha, et al. 2013).
Di Indonesia berdasarkan Riset Kesehatan Dasar (Riskesdas) tahun 2007,
menunjukkan prevalensi anemia pada ibu hamil 59%, anak-anak 70,1%, wanita
usia subur (WUS) 59,9% dan laki-laki dewasa sebesar 33,4%. Untuk prevalensi
ADB di Indonesia belum ada data yang pasti. Martoatmojo et al. memperkirakan
ADB pada laki-laki 16 – 50% dan 25 – 84% pada perempuan tidak hamil. Pada
pensiunan pegawai negeri di Bali didapatkan prevalensi anemia 36% dengan 61%
disebabkan oleh karena defisiensi besi (Martoatmojo, et al. 1973). Survei pada
suatu desa di bali didapatkan angka prevalens ADB sebesar 27% (Bakta, 2015).
Sebuah studi yang dilakukan oleh Suega et al. tahun 2002 yang khususnya
meneliti prevalensi ADB pada wanita hamil di Bali menemukan sebesar 46,2%
ibu hamil menderita ADB ringan.
1.1.3 Metabolisme Besi
Besi merupakan trace element dan mikronutrien esensial yang penting dan
dibutuhkan oleh hampir semua organisme baik mikroba, tanaman, hewan maupun
manusia. Fungsi besi didalam tubuh adalah sebagai katalisator untuk oksigenasi,
hidroksilasi dan proses metabolisme penting lainnya. Selain itu besi juga penting
sebagai kofaktor enzim-enzim pada respirasi mitokondrial. Proliferasi dan aktifasi
dari sel T, sel B dan sel NK juga memerlukan besi. Dalam keadaan normal
seorang laki dewasa mempunyai kandungan besi 50 mg/kgBB sedangkan
Tubuh mendapatkan masukan besi berasal dari makanan dalam usus. Proses
absorpsi besi paling banyak terjadi pada duodenum dan jejunum proksimal.
Membran apikal enterosit di duodenum berperan untuk transport besi dari lumen
intestinal ke dalam sel enterosit dimana molekul transporter yang terpenting
adalah Divalent Metal Transporter 1 (DMT1) (Sharp, 2007 ; Andrews, 2009 ;
Kaushansky, et al. 2010).
Setelah diabsoprsi di duodenum, besi akan beredar di sirkulasi dalam bentuk
transferin menuju sistem portal dari hepar yang merupakan tempat penyimpan
besi yang utama. Sel hepatosit akan mengikat besi melalui Transferrin Receptor 1
(TfR1) yang klasik namun sebagian besar melalui TfR2 yang tersedia dalam
jumlah lebih besar (Flemmig dan Sly, 2001 ; Andrews, 2009).
Tempat utama penggunaan besi adalah sumsum tulang dimana besi diikat
oleh TfR pada sel prekursor eritrosit dan digunakan untuk sintesis heme. Besi
pada heme selanjutnya akan didaur ulang melalui proses tertangkapnya eritrosit
yang sudah tua pada makrofag sistem retikuloendotelial. Besi dalam makrofag
dapat tersimpan di makrofag sebagai feritin atau dilepaskan ke plasma yang
kemudian akan terikat transferin dan beredar di plasma untuk digunakan kembali.
Hati dan sistem retikuloendotelial merupakan tempat utama penggunaan cadangan
besi (Fleming dan Sly, 2001 ; Andrews, 2009).
Setiap hari 1-2 mg besi hilang dari tubuh karena perdarahan, menstruasi atau
eksfoliasi dari epitel yang mengandung besi di kripta usus, traktus urinarius,
rambut dan kulit dan dalam jumlahnya yang samapun setiap harinya diserap.
maka keseimbangan besi dalam tubuh dijaga oleh regulator proses absorpsi besi di
duodenum (Sharp, 2007 ; Gisbert, 2009).
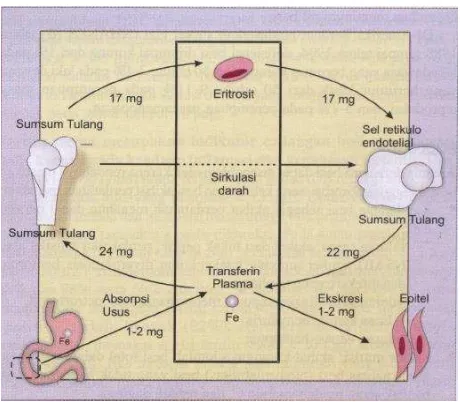
Seluruh proses ini terjadi melalui sirkulasi yang tertutup dimana jumlah yang
diserap dan jumlah yang diekskresi bersifat tetap. Besi yang diserap usus setiap
hari berkisar antara 1-2 mg, ekskresi besi terjadi dalam jumlah yang sama melalui
eksfoliasi epitel (Bakta, 2006 ; Andrews, 2009). Proses ini dapat dilihat pada
gambar berikut :
Gambar 2.1Siklus Pertukaran Besi dalam Tubuh (Bakta, 2015)
1.1.4 Patogenesis
Perdarahan menahun menyebabkan kehilangan besi sehingga cadangan besi
semakin menurun. Jika cadangan besi menurun maka keadaan ini disebut iron
depleted state atau negative iron balance. Keadaan ini ditandai oleh penurunan
kadar serum feritin, peningkatan absorpsi besi dalam usus serta pengecatan besi
dalam sumsum tulang negatif (Bakta, 2015).
Apabila kekurangan besi berlanjut maka cadangan besi menjadi kosong sama
gangguan pada bentuk eritrosit tetapi anemia secara klinis belum terjadi dimana
keadaan ini disebut iron deficient erythropoiesis. Pada fase ini kelainan pertama
yang dijumpai ialah peningkatan kadar free protophorphyrin atau zinc
protophorphyrin dalam eritrosit. Saturasi transferin menurun dan TIBC
meningkat. Akhir-akhir ini parameter yang sangat spesifik ialah peningkatan
reseptor transferin dalam serum (Bakta, 2015).
Kondisi kekurangan besi yang terus berkepanjangan akan menyebabkan
jumlah besi menurun terus dan eritropoesis akan semakin terganggu sehingga
kadar hemoglobin mulai menurun sehingga timbullah anemia hipokromik
mikrositer yang disebut sebagai anemia defisiensi besi. Pada saat ini juga terjadi
kekurangan besi pada epitel serta pada beberapa enzim yang dapat menimbulkan
kelainan pada kuku, epitel mulut dan faring serta berbagai gejala lainnya.
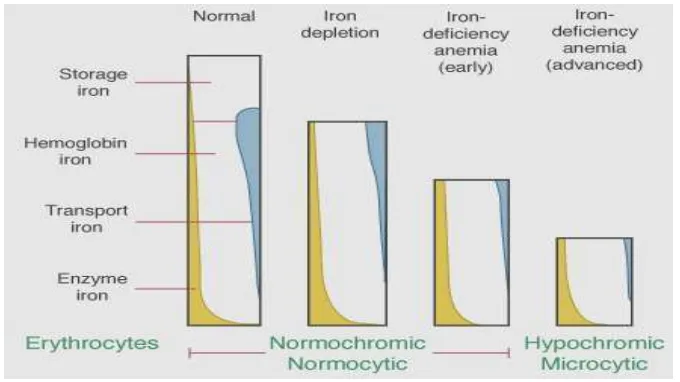
Perjalanan patogenesis defisiensi besi dapat dilihat pada gambar dibawah ini.
Gambar 2.2 Stadium Patogenesis Defisiensi Besi (Kaushansky et al., 2010) 1.1.5 Klasifikasi derajat defisiensi besi
Jika dilihat dari beratnya kekurangan besi dalam tubuh maka defisiensi besi
1. Deplesi besi (iron depleted state) : cadangan besi menurun tetapi penyediaan
besi untuk eritropoesis belum terganggu
2. Eritropoesis defisiensi besi ( iron deficient erythropoiesis) : cadangan besi
kosong penyediaan besi untuk eritropoesis terganggu tetapi belum timbul
anemia secara laboratorik
3. Anemia defisiensi besi : cadangan besi kosong disertai penurunan kadar
hemoglobin.
1.1.6 Komplikasi defisiensi besi
Defisiensi besi selain menyebabkan anemia juga menyebabkan hal negatif
seperti berikut : (Bakta, 2015)
1. Pada sistem neuromuskular menyebabkan gangguan kapasitas kerja
2. Gangguan terhadap proses mental dan kecerdasan
3. Gangguan imunitas dan ketahanan terhadap infeksi.
4. Gangguan terhadap ibu hamil dan janin yang dikandungnya.
Seluruh gangguan ini dapat timbul pada anemia ringan dan bahkan sebelum
anemia bermanifestasi.
1.1.7 Diagnosis anemia defisiensi besi
Diagnosis ADB ditegakkan berdasarkan anamnesa yaitu adanya gejala umum
anemia dan gejala khas defisiensi besi serta adanya penyakit dasar diikuti dengan
pemeriksaan fisik dan pemeriksaan laboratorium. Modifikasi dari Kriteria Kerlin
dipakai sebagai kriteria diagnosis ADB yaitu anemia dengan gambaran hipokrom
fl dan Mean Corpuscular Hemoglobin Concentration (MCHC) < 31% dan salah
satu dari 1, 2, 3, atau 4, yaitu :
1. Dua dari tiga parameter di bawah ini :
a. Besi Serum <50 mg/dl
b.TIBC >350 mg/dl
c. Saturasi Transferin : <15%
2. Serum Feritin <20 g/L
3. Pengecatan sumsum tulang dengan biru prusia (Perl’s Stain) menunjukkan
cadangan besi (butir-butir hemosiderin) negatif.
4. Dengan pemberian sulfas ferosus 3 x 200 mg/hari (atau preparat besi lain yang
setara) selama 4 minggu disertai kenaikan kadar hemoglobin lebih dari 2 g/dl.
Baku emas diagnosis ADB adalah pemeriksaan besi sumsum tulang dengan
pengecatan tinta biru prusia untuk mencari butir-butir hemosiderin (Ann, 2002 ;
Brugnara, 2002 ; Mast, 2008).
1.1.8 Penatalaksanaan dan penilaian respons terapi ADB
Fokus penatalaksanaan anemia defisiensi besi adalah mengatasi penyebab
dan pemberian suplementasi besi agar dapat memenuhi kebutuhan besi tubuh
sekaligus mengisi cadangan besi yang kosong. Pemberian preparat besi dapat
dilakukan secara oral maupun parenteral. Pada umumnya preparat oral yang lebih
sering diberikan sampai dengan kadar hemoglobin normal kemudian dilanjutkan
sampai 6 bulan untuk mengisi cadangan besi tubuh. Besi parenteral dapat
diberikan dengan indikasi adanya intoleransi dengan pemberian obat, kepatuhan
berobat rendah, adanya kondisi kolitis ulseratif, gangguan absorpsi besi di saluran
kondisi defisiensi besi fungsional karena penggunaan eritropoetin yang berulang
(Bakta, 2015).
Terapi lain dengan memberikan diet tinggi protein, pemberian vitamin C
untuk meningkatkan absorpsi besi dan mengatasi penyakit dasar. Transfusi darah
hanya diberikan pada kondisi adanya penyakit jantung anemik dengan ancaman
payah jantung, anemia yang sangat simptomatik misalnya anemia dengan gejala
pusing yang sangat mencolok, penderita memerlukan peningkatan kadar
hemoglobin yang cepat seperti pada kehamilan trimester akhir atau preoperasi.
(Bakta, 2015).
Berdasarkan modifikasi kriteria Kerlin diagnosis ADB dapat ditegakkan pula
dengan adanya kenaikan kadar hemoglobin sebesar 1-2 g/dL setelah mendapatkan
terapi besi dan hal ini dapat menjadi indikator keberhasilan terapi pada ADB
(Bakta, 2015). Respons terhadap terapi sebenarnya dapat dinilai sejak minggu
pertama ditandai dengan peningkatan retikulosit namun kadar retikulosit akan
menurun sehingga tidak dapat dijadikan sebagai prediktor awal (Santen, et.al,
2014 ; Parodi, et.al 2015). Parameter yang lain seperti hematokrit, MCV dan
MCH juga mengalami peningkatan setelah mendapatkan terapi tetapi lebih lambat
sehingga tidak dapat dipakai sebagai indikator keberhasilan terapi (Afzal, et.al
2009).
1.1.9 Problem diagnostik dan penilaian respons terapi ADB
Baku emas diagnosis ADB adalah pemeriksaan besi sumsum tulang untuk
pemeriksa dan biaya pemeriksaan yang tinggi sehingga pemeriksaan ini mulai
digantikan oleh tes hematologi dan tes biokimia yang sesuai dengan metabolisme
besi (Brugnara, 2002 ; Mast, 2008).
Pemeriksaan hematologi yang dipakai adalah hemoglobin, indeks eritrosit,
retikulosit. Pemeriksaan ini lebih umum ditemukan, terjangkau, dan dengan biaya
yang lebih murah. Anemia ditandai dengan kadar hemoglobin <10 gr/dL.
Gambaran eritrosit yang hipokromik merupakan indikator langsung adanya
kondisi iron deficient erythropoiesis. Jumlah retikulosit pada kondisi defisiensi
besi akan menurun tetapi bila kondisi defisiensi yang berat disertai dengan
perdarahan kronis maka jumlah retikulosit akan sedikit meningkat. Diagnosis
ADB dengan hanya menggunakan pemeriksaan hematologi belum dapat
ditegakkan karena anemia pada penyakit kronis juga akan memberikan gambaran
eritrosit yang hipokromik (Thomas dan Thomas, 2002 ; Wu, et al. 2002).
Metabolisme besi dapat dinilai dengan menggunakan pemeriksaan biokimia.
Walaupun dari segi biaya pemeriksaan ini lebih mahal daripada tes hematologi
tetapi dengan kombinasi kedua pemeriksaan ini maka diagnosis ADB dapat
ditegakkan. Pemeriksaan biokimia yang sering dipakai adalah feritin, besi serum,
saturasi transferin, dan serum soluble transferrin receptor (sTfR) (Wu, et al.
2002).
Feritin mengukur ketersediaan cadangan besi. Kadar feritin berkorelasi
langsung dengan total cadangan besi di tubuh. Bila cadangan besi berkurang
maka kadar feritin akan menurun sehingga feritin merupakan penanda yang paling
awal dari kondisi defisiensi besi. Menurut WHO, nilai cut off feritin untuk
angka infeksi dan inflamasi masih tinggi maka nilai cut off yang diajukan di
negeri barat tampaknya perlu dikoreksi. Hercberg tahun 1991 menganjurkan
untuk daerah tropik digunakan batas nilai serum feritin sebesar <20μg/L. Kadar
feritin <20μg/l dikombinasi dengan anemia hipokromik mikrositer secara klinis
paling sensitif dan spesifik dalam mendiagnosis ADB (Bakta, 2015 ; Thomas dan
Thomas, 2002 ; Wu, et al. 2002 ; Hercberg, 1991).
Suega tahun 2007 mencoba mencari nilai cut off feritin untuk mendiagnosis
ADB di RSUP Sanglah Denpasar dengan hasil yaitu feritin memiliki sensitivitas
90,7% dan spesivisitas 90,6% dengan nilai cut off 35,4 g/l.
Feritin merupakan suatu protein fase akut dimana kadarnya akan ikut berubah
pada kondisi penyakit kronis seperti kanker, infeksi atau inflamasi kronis,
penyakit hati, konsumsi alkohol, hipertiroid dan penggunaan kontrasepsi oral serta
dipengaruhi pula oleh jenis kelamin sehingga penggunaannya menjadi terbatas.
Studi oleh Thomas dan Thomas tahun 2002 yang mencoba membandingkan
sensitivitas dan spesifisitas feritin dalam mendiagnosis ADB pada kondisi tanpa
inflamasi dan dengan inflamasi menemukan bahwa terdapat penurunan persentase
sensitivitas dan spesivisitas serta malahan terjadi peningkatan nilai cut off feritin
pada kondisi inflamasi (Mast, et al. 2002 ; Thomas dan Thomas, 2002 ; Brugnara,
2003 ; Karlsson 2011 ; Swart, et al. 2014).
Beberapa keterbatasan tes biokimia lain bila digunakan dalam mendiagnosis
ADB adalah : (Thomas dan Thomas, 2002 ; Wu, et al. 2002; Brugnara, 2003 ;
1. Total Iron Binding Capacity (TIBC) yang mengukur secara tidak langsung
kadar transferin dimana akan meningkat bila kadar besi serum dan cadangan
besi menurun. TIBC ternyata juga dipengaruhi oleh inflamasi, malnutrisi,
infeksi kronis dan kanker yang akan menyebabkan penurunan kadar.
2. Besi serum dapat diukur secara langsung dan kadarnya menurun bila cadangan
besi berkurang. Namun pemeriksaan ini tidak dapat mencerminkan secara
langsung cadangan besi karena dapat dipengaruhi oleh variasi diurnal dimana
konsentrasinya lebih tinggi pada siang hari, jenis diet dan suplementasi besi,
kondisi inflamasi serta infeksi juga ikut mempengaruhi perubahan kadar besi
serum.
3. Saturasi Transferin (TSAT) merefleksikan jumlah besi yang terikat oleh
protein transport dan proses transport besi tersebut. Nilai TSAT didapatkan
berdasarkan pembagian besi serum dengan TIBC dan dengan demikian juga
dipengaruhi oleh inflamasi dan variasi diurnal tetapi berkebalikan dengan
feritin, kadar saturasi transferin akan menurun pada kondisi inflamasi.
4. Serum Soluble Transferin Receptor yang mengukur jumlah reseptor transferrin
pada retikulosit diketahui merupakan indikator defisiensi besi yang terbaik.
Penggunaan rasio sTfR terhadap Feritin (R/F ratio) juga memberikan
gambaran yang cukup baik dalam mengestimasi cadangan besi. Namun tes ini
juga dipengaruhi oleh proses inflamasi dan belum terdapat banyak studi
mengenai efisiensi tes ini dalam mendiagnosis defisiensi besi, belum terdapat
Alternatif lain untuk menegakkan diagnosis ADB adalah berdasarkan respons
hematologi setelah pemberian terapi suplementasi besi. Peningkatan Hb sebesar
1-2 gr/dL baru terjadi setelah terapi diberikan selama 4 minggu. Retikulosit juga
dapat digunakan untuk menilai respons terapi karena peningkatan jumlah telah
terjadi sejak minggu pertama tetapi kemudian jumlahnya akan menetap bahkan
sedikit menurun sehingga tidak dapat digunakan sebagai indikator awal
keberhasilan terapi ADB (Pritchard, 1961 ; Buttarello, 2004 ; Santen, et.al 2014 ;
Parodi, et.al 2015). Indikator lain seperti MCV, MCH juga meningkat tetapi
peningkatan tiap minggu tergolong kecil dan baru terlihat signifikan pada minggu
ke 4 terapi (Afzal, et.al 2009).
Dengan ditemukan hal-hal tersebut diatas, diagnosis ADB walaupun mudah
dapat menyulitkan. Tidak terdapat 1 jenis tes yang paling superior bila
dibandingkan dengan tes-tes yang lain untuk mendiagnosis ADB. Bila digunakan
pada kondisi inflamasi dan penyakit kronis maka hasil yang didapatkan kurang
maksimal sehingga diperlukan sebuah modalitas diagnosis yang lebih praktis,
ekonomis dan tidak terpengaruh oleh kondisi inflamasi. Diperlukan juga
pemeriksaan yang dapat mendeteksi respon terapi lebih cepat sehingga
keberhasilan pengobatan ADB dapat diketahui lebih awal.
1.2 Pemeriksaan Ekuivalen Hemoglobin Retikulosit (Ret-He) dalam Diagnosis ADB
1.2.1 Pendahuluan
Keseimbangan besi terutama diregulasi oleh kecepatan eritropoesis dan
yang dapat menyebabkan anemia. Diagnosis ADB mudah tetapi akibat beberapa
kondisi seperti inflamasi, penyakit kronis, dll sehingga diagnosis menjadi
menyulitkan. Deteksi dini defisiensi besi sebelum terjadi anemia penting
dilakukan untuk mencegah komplikasi namun dikarenakan tidak adanya 1 jenis
tes yang superior dan tidak terpengaruh oleh kondisi penyakit penyerta, proses
deteksi dini menjadi kurang akurat. Diperlukan modalitas diagnosis yang praktis,
ekonomis, dan tidak terpengaruh oleh inflamasi dalam diagnosis dan deteksi dini
defisiensi besi.
1.2.2 Sistem eritroid, eritropoesis dan retikulosit
Sistem eritroid terdiri atas sel darah merah (red cell) atau eritrosit dan
prelursor eritroid. Unit fungsional dari sistem eritroid ini dikenal sebagai eritron
yang mempunyai fungsi penting sebagai pembawa oksigen. Prekursor eritroid
dalam sumsum tulang berasal dari sel induk hemopoetik melalui jalur sel induk
myeloid kemudian menjadi sel induk eritroid yaitu Burst Forming Unit Erythroid
(BFU-E) dan selanjutnya menjadi Colony Forming Unit Erythroid (CFU-E)
(Bakta, 2006).
Perkembangan selanjutnya adalah sel pronormoblast kemudian menjadi
normoblast lalu berkembang menjadi retikulosit yang akan dilepas ke darah tepi
dan menjadi eritrosit dewasa. Retikulosit adalah sel darah merah imatur, tidak
berinti yang berasal dari proses pematangan normoblas di sumsum tulang dengan
masa hidup selama 1-2 hari di sirkulasi darah tepi sebelum mengalami maturasi
menjadi sel darah merah. Peningkatan pelepasan retikulosit ke sirkulasi darah tepi
disebabkan oleh kondisi anemia, kehilangan darah, hemolisis dan lain-lain. Pada
penting karena dapat digunakan sebagai indikator produktivitas dan aktivitas
eritropoesis. Dalam kondisi defisiensi besi jumlah retikulosit akan menurun dan
dengan pemberian terapi subtitusi besi jumlahnya akan meningkat (Wu, et al.
2002 ; Bakta, 2006 ; Suega, 2010).
Bahan pembentuk eritrosit seperti besi, vitamin B12, asam folat juga
diperlukan dalam proses ini. Eritrosit hidup dan beredar dalam darah tepi rata-rata
selama 120 hari dan setelah itu akan mengalami penuaan kemudian dikeluarkan
dari sirkulasi oleh sistem retikuloendotelial (RES). Kadar besi dianggap konstan
pada setiap fase sel saat eritropoesis (Buttarello, 2004 ; Bakta, 2006).
1.2.3 Automatedhematologyanalyser
80 tahun yang lalu seorang ahli hematologi yang bernama Dr Maxwell Myer
Wintrobe menemukan suatu klasifikasi anemia berdasarkan indeks Wintrobe yaitu
penghitungan manual MCV, MCH dan MCHC berdasarkan nilai hemoglobin dan
eritrosit (Brugnara dan Mohandas, 2013 ; Urrechaga, 2014). Tahun 1940 konsep
dari Wintrobe tersebut berusaha diaplikasi dengan ditemukannya alat penghitung
otomatis dari sel-sel darah oleh Wallace H Coulter dan sampai dengan tahun
1980 alat pemeriksaan hematologi mampu memberikan 7 nilai parameter
pemeriksaan darah lengkap dan 3 parameter hitung jenis sel (Urrechaga, 2014).
Pada tahun 1990 ditemukan parameter pemeriksaan yang mampu mengetahui
distribusi dari MCV yaitu Red Cell Distribution Width (RDW). RDW
memberikan informasi mengenai variasi ukuran dari masing-masing sel darah
merah. Dalam 10-15 tahun terakhir teknologi semakin canggih dengan
ditemukannya pengukuran otomatis dari jumlah retikulosit dan parameter selular
dari retikulosit termasuk kandungan hemoglobin serta indeks maturitasnya
Sebuah teknologi analisis retikulosit yang terbaru dapat mengukur kandungan
hemoglobin dalam retikulosit atau ekuivalennya sehingga dapat memberikan
penilaian langsung tentang ketersediaan cadangan besi adekuat untuk proses
eritropoesis (Mast, et al. 2002; Brugnara, 2003 ; Brugnara, et al. 2006; Mast, et al.
2007; Urrechaga, et al. 2009).
Karena masa hidup retikulosit yang singkat maka pemeriksaan ini merupakan
indikator yang sensitif terhadap kondisi iron deficient erythropoiesis bahkan pada
stadium awal karena pemeriksaan ini mencerminkan ketersediaan besi untuk
proses eritropoesis dalam jangka waktu 2-4 hari kedepan sehingga pemeriksaan
ini dapat dipakai untuk mendiagnosis defisiensi besi (Mast, et al. 2002 ; Brugnara,
2003 ; Brugnara, et al. 2006; Mast, et al. 2007 ; Urrechaga, et al. 2009).
Bayer Diagnostic memproduksi Advia® dan memperkenalkan pemeriksaan
kadar hemoglobin retikulosit atau CHr yang merupakan produk konsentrasi
hemoglobin dan volume sel dari retikulosit sedangkan Sysmex Corporation
memproduksi Sysmex seri XE dan XN mengeluarkan pemeriksaan ekuivalen
retikulosit hemoglobin atau Ret-He dengan menggunakan teknologi yang sama
tetapi pada Ret-He langsung mengukur inkorporasi besi di dalam hemoglobin
eritrosit sehingga dapat menghasilkan estimasi langsung dari ketersediaan besi
dalam erythron. Terdapat hasil yang senada antara CHr dan Ret-He menurut studi
yang dilakukan oleh Thomas, et al. tahun 2005, David, et al. tahun 2006 dan
Brugnara, et al. tahun 2006 (Mast, et al. 2002 ; Brugnara, 2003 ; Brugnara, et al.
2006 ; Mast, et al. 2007 ; Urrechaga, et al. 2009).
1.3 Aplikasi Klinis Ret-He dalam Diagnosis ADB
Ret-He telah terbukti sebagai indikator yang sensitif pada stadium awal dari
iron deficient erythropoiesis. Dengan tambahan pemeriksaan seperti HYPO%
Penggunaan Indeks sTfR / Feritin dianggap paling sensitif dalam mendeteksi
defisiensi besi fungsional. Dengan ditemukannya pemeriksaan kadar hemoglobin
retikulosit maka dengan kombinasi nilai pemeriksaan tersebut dan indeks
sTfR/Feritin maka dapat dibuat klasifikasi sebagai berikut : (Brugnara, 2003 ;
Mast, et al. 2007)
a. Eritropoesis normal dengan cadangan besi normal
b. Eritropoesis normal dengan cadangan besi yang menurun
c. Gangguan eritropoesis dengan candangan besi yang cukup
d. Gangguan eritropoesis dengan cadangan besi yang normal
Aplikasi klinis pemeriksaan Ret-He terutama untuk menentukan kebutuhan
pemberian suplementasi besi pada pasien dengan defisiensi besi fungsional.
Misalnya pada pasien hemodialisis regular atau pasien kanker dengan anemia
yang menggunakan eritropoetin karena eritropoetin akan menyebabkan kondisi
iron deficient erythropoiesis. Kondisi defisiensi besi fungsional terjadi pada
anemia penyakit kronik. Hal ini disebabkan oleh beberapa faktor salah satunya
adalah peningkatan hepcidin yang akan mengganggu homeostasis besi. Hal ini
dapat menurunkan respon eritropoetin pada proses eritropoesis dan akan
menghasilkan eritrosit yang hipokromik. (Brugnara, 2003 ; Mast, et al. 2007).
Ret-He juga digunakan pada skrining kondisi defisiensi besi pada bayi dan
anak-anak dan telah terbukti sebagai prediktor yang paling kuat terhadap kondisi
defisiensi besi dengan atau tanpa anemia (Ullrich, et al. 2005).
CHr dan Ret-He juga dapat digunakan sebagai prediktor keberhasilan terapi
besi. Berdasarkan kriteria Kerlin, keberhasilan terapi besi pada ADB ditandai
minggu. Studi yang dilakukan oleh Brugnara menemukan bahwa terdapat
kenaikan kadar CHr dengan rata-rata 3,2 pg setelah diberikan terapi besi oral dan
kenaikan tersebut telah terjadi dalam waktu 1-2 minggu. Pada pemberian terapi
besi intravena, CHr merupakan indikator awal terhadap respons terapi dimana
kadar CHr mulai meningkat dalam 2-4 hari sejak pemberian terapi (Brugnara, et
al. 1994 ; Mast et al., 2002).
1.4Keterbatasan Ret-He dalam Diagnosis ADB
CHr dan Ret-He telah banyak digunakan dalam mendeteksi kondisi defisiensi
besi, namun belum terdapat standar internasional dari nilai cut off-nya. Walaupun
terdapat nilai rentang normal CHr dan Ret-He yang telah ditentukan oleh
produsen namun banyak studi yang menemukan nilai cut-off yang bervariasi
(Urrechaga, 2014 ; Swart , 2014).
Studi oleh Brugnara menemukan nilai CHr < 27,2 pg merupakan prediktor
defisiensi besi yang signifikan pada bayi, sedangkan pada anak dipakai nilai <28,4
pg. Sedangkan Ullrich tahun 2005 melakukan skrining defisiensi besi pada bayi
yang sehat menemukan nilai CHr sebesar 27,5 pg sebagai nilai cut-off. Urrechaga
tahun 2009 mencoba mencari nilai cut off Ret-He menegakkan diagnosis ADB
pada penderita dewasa dan ditemukan nilai < 29 pg. Sedangkan studi oleh
Karlsson tahun 2011 pada orang tua dengan kondisi anemia menemukan nilai CHr
30,5 pg sebagai cut off (Brugnara, 2003 ; Karlsson, 2011).
Keterbatasan yang lain adalah CHr tidak dapat digunakan digunakan pada
pasien dengan thalassemia dan kelainan hemoglobin lainnya karena angka CHr
karena gangguan dari struktur pembentuk hemoglobin. Demikian pula halnya
pada kondisi anemia megaloblastik (Mast, et al. 2002 ; Mast, et al. 2008). Pada
pasien dengan riwayat pemberian transfusi, terapi besi, defisiensi B12 dan folat
serta adanya kelainan dari analisis hemoglobin maka hasil pemeriksaan CHr dan