Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
Isolasi dan Uji Bioaktivitas Senyawa Metabolit Sekunder Ekstrak Metanol Fraksi Non Polar Daun Ungu (Graptophyllum pictum (L.) Griff)
Isolation and Bioactivity Test Secondary Metabolite Compound In Non Polar Fraction of Methanol Extract of Purple Leaves (Graptophyllum pictum (L.) Griff)
1)Merlin Tandi, 2)Iwan Dini, 3)Muharram
1,2.3)Jurusan Kimia FMIPA Universitas Negeri Makassar, Jalan Dg Tata Raya, Makassar
Email : [email protected]
ABSTRAK
Penelitian ini adalah penelitian eksplorasi yang bertujuan untuk mengisolasi senyawa metabolit sekunder dalam ekstrak metanol daun ungu (G.pictum (L.) Griff) serta uji bioaktivitasnya terhadap bakteri S. aureus dan E.coli.
Sampel diperoleh dari desa Pepuro Barat, Kecamatan Wotu, Kabupaten Luwu Timur, Sulawesi Selatan. Isolasi dilakukan dengan beberapa tahap:
maserasi, fraksinasi dan pemurnian sedangkan identifikasi senyawa dilakukan dengan menggunakan alat spektroskopi inframerah dan uji bioaktivitas terhadap bakteri S. aureus dan E. coli dilakukan dengan metode difusi agar. Hasil penelitian berupa isolat murni berbentuk kristal jarum bening dan positif dengan uji Liebermann-Buchard. Spektrum IR menunjukkan adanya serapan gugus C-O, CH2 dan CH3, C=C, dan OH alkohol. Berdasarkan uji pereaksi dan data inframerah disimpulkan bahwa senyawa yang diperoleh adalah golongan steroid yang dapat menghambat pertumbuhan bakteri S. aureus namun tidak pada bakteri E. coli.
Kata kunci : Daun Ungu, Graptophyllum Pictum (L.) Griff, Isolasi, Steroid
ABSTRACT
This study is an exploratory research that aims to isolate the secondary metabolite in methanol extract of purple leaves (G. pictum (L.)Griff) and its bioactivity test against S. aureus and E. coli bacteria. Samples were obtained from the Pepuro Barat village, Wotu District, Luwu Timur regency, South Sulawesi. Isolation was done in several steps: maceration, fractionation and purification, while the identification of compounds were performed using an infrared spectroscopy and bioactivity test to S. aureus and E. coli bacteria was performed using gelatin diffusion method. Results of the research was a pure isolate which has clear needle crystal shaped and showed a positive result in Lieberman Buchard test. IR spectrum showed absorption of C-O, CH2 and CH3, C = C and OH alcohol groups. Based on the reagent tests and infrared data obtained is concluded that the compound is a steroid that can inhibit the growth of S. aureus bacteria but not in E. coli bacteria.
Keywords: Purple leaf, , Graptophyllum Pictum (L.) Griff), Isolation, steroids
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
PENDAHULUAN
Keanekaragaman flora yang tersebar luas mulai dari spesies tingkat tinggi sampai spesies tingkat rendah memiliki senyawa-senyawa bioaktif yang dapat dimanfaatkan sebagai bahan obat. Sebaran senyawa aktif pada tumbuhan biasanya didapatkan dari dua pendekatan, yaitu pendekatan skrining fitokimia dan pendekatan fitofarmakologi. Akan tetapi pendekatan yang sering digunakan yaitu pendekatan fitofarmakologi yang bersumber dari etnobotani yaitu informasi yang terdapat di masyarakat baik secera tertulis maupun informasi dari mulut ke mulut mengenai penggunaan tumbuhan sebagai bahan obat tradisional yang digunakan secara turun menurun di masyarakat (Swantara, 2009).
Senyawa kimia pada tumbuhan yang bersifat bioaktif dapat dijumpai di seluruh bagian tumbuhan seperti daun, batang, bunga, buah atau akarnya. Senyawa metabolit sekunder merupakan hasil metabolisme suatu organisme hidup yang memiliki fungsi berbeda-beda seperti senyawa alkaloid, terpenoid, steroid, flavonoid, dan lain-lain. Metabolit sekunder merupakan biomolekul yang dapat digunakan sebagai lead compounds dalam penemuan dan pengembangan obat-obat baru (Atun, 2010).
Eksplorasi tanaman sebagai bahan obat-obatan masih terus dilakukan oleh peneliti. Salah satu tanaman yang memiliki khasiat obat adalah tanaman ungu. Tanaman Ungu termasuk dalam famili Acanthaceae dengan nama spesies Graptophylum pictum (L.) Griff. Tanaman daun ungu merupakan salah satu tanaman hias, terkhusus di daerah Luwu Timur, desa Pepuro Barat. Tanaman ini biasa
ditanam sebagai tanaman pagar atau pembatas perkarangan rumah karena tanaman ini mudah tumbuh dan memiliki warna yang khas. Bagian tanaman ini yang umum digunakan sebagai obat adalah bagian daun.
Secara empiris daun ungu berkhasiat sebagai obat wasir, obat bisul, luka- luka radang, peluruh air seni, melunakkan feses juga untuk menghilangkan konstipasi. Adapun kandungan senyawa kimia yang diduga berperan menyebabkan efek tersebut adalah turunan senyawa fenol. Secara eksperimental ekstrak daun ungu berkhasiat menghambat pembengkakan dan menurunkan permiabilitas vaskular (Isnawati, 2003; Ozaki dalam Sumarny, 2013).
Daun ungu diketahui mengandung flavonoid, saponin, tanin, alkaloid, steroid. Dari kandungan senyawa kimia ini daun ungu diindikasikan dapat berfungsi sebagai antibakteri dan antioksidan.
Hasil uji ekstrak etanol daun ungu memperlihatkan adanya aktivitas antibakteri terhadap S. Aureus dengan nilai KHM sebesar 0,00375 mg/mL (Arifatin dalam Pidada, 2009; Da’i, 2012; Proboseno, 2011).
Hasil penelitian uji skrining fitokimia daun ungu diketahui bahwa pada ekstrak metanol positif mengandung senyawa triterpenoid sedangkan pada ekstrak n- heksana dan kloroform positif terkandung senyawa steroid, senyawa-senyawa ini bersifat non polar (Tukiran, 2014).
Bioaktivitas tanaman sangat dipengaruhi oleh kandungan senyawa kimia yang terdapat didalamnya.
Perbedaan kandungan senyawa kimia yang ada menunjukkan perbedaan
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
aktifitas farmakologis dari tanaman yang bersangkutan.
Berdasarkan uraian diatas menunjukkan ada potensi ditemukan senyawa metabolit sekunder pada tanaman daun ungu yang dapat dijadikan sebagai senyawa aktif dalam bidang farmasi dari fraksi nonpolar
dengan menggunakan pelarut metanol serta uji bioaktivitasnya terhadap bakteri. Bagian tanaman yang akan diisolasi yaitu bagian daun karena daun merupakan bagian tumbuhan yang sering dimanfaatkan masyarakat sebagai obat tradisional.
METODE PENELITIAN A. Alat dan Bahan 1. Alat
Alat-alat yang digunakan pada penelitian ini terdiri dari alat untuk preparasi sampel yaitu blender, gunting dan wadah sampel. Alat untuk proses ekstraksi dan identifikasi yaitu neraca analitik, wadah kaca tertutup untuk maserasi, evaporator HAHN HS- 2005V-N, corong Buchner, pompa vakum, gelas ukur 100 mL, gelas ukur 50 mL,gelas ukur 10 mL, gelas kimia 1000 mL, gelas kimia 250 mL, gelas kimia 1000 mL, corong biasa, pipet tetes, plat tetes, pipa kapiler, spoit 1 mL, jarum preparat, spatula, hot plate, botol semprot, botol vial, batang pengaduk, lampu UV VL- 4.LC 254-365 nm, oven memmert, chamber, kolom untuk KKCV, kolom untuk KKF, botol kaca kapasitas 100 mL, statif dan klem, spektrofotometer FTIR Shimadzu Prestige-21. Serta alat untuk uji antibakteri meliputi cawan petri, erlenmeyer 250 mL, gelas kimia 500 mL, pinset, batang
pengaduk, hot plate, autoklaf, inkubator, mikropipet, kawat ose, tabung reaksi, dan jangka sorong.
2. Bahan
Bahan yang digunakan adalah serbuk halus daun ungu. Bahan-bahan kimia yang digunakan adalah metanol, n- heksana, etil asetat, kloroform dan aseton. Beberapa reagen seperti pereaksi Liebermann-Burchard, Wagner, Meyer dan FeCl3. Bahan- bahan lain yang digunakan, pelat KLT aluminium berlapis silika gel 60 G F254,, aluminium foil, kertas saring Whatman, tissu, silica gel 60 H (untuk kolom vakum), silica gel 60 (0,2-0,5 mm) untuk imprek sampel, silika gel 60 (0,063-0,200mm) untuk KKT, serium sulfat (CeSO4) dan label. Serta bahan-bahan untuk uji antibakteri meliputi Medium Nutrien Agar, aquades, kapas, aluminiumfoil, NaCl 0,9%, bakteri E. coli, bakteri S.
aureus, dan dimetil sulfoksida (DMSO).
PROSEDUR KERJA
1. Preparasi Sampel dan Ekstraksi
Daun ungu yang telah dibersihkan lalu dikeringkan dengan cara diangin-anginkan pada suhu kamar untuk menghilangkan kandungan air yang terdapat dalam daun ungu, kemudian sampel kering dipotong kecil-kecil dan dihaluskan dengan menggunakan blender. Sampel
serbuk Daun ungu diperoleh sebanyak 2,52 kg
Dimaserasi dengan metanol sebanyak 15 L. Proses maserasi dilakukan selama 3x24 jam disertai dengan sesekali pengadukan. Maserat yang diperoleh kemudian disaring dengan menggunakan corong buncher dan pompa vakum dan diperoleh maserat sebanyak 10 L. Maserat
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
kemudian dipekatkan menggunakan evaporator pada suhu 40oC dan diperoleh ekstrak kental metanol sebanyak 43,9 gram yang berbentuk pasta berwarna hijau. Terhadap ekstrak metanol ini dilakukan uji golongan dengan menggunakan berbagai pereaksi diantaranya
pereaksi Liebermann-
Burchard(terpenoid dan steroid), FeCl3 (flavonoid), Meyer (alkaloid), dan Wagner (alkaloid).
2. Fraksinasi, Pemurnian dan Identifikasi
Ekstrak metanol daun ungu yang diperoleh terlebih dahulu diuji menggunakan kromatografi lapis tipis (KLT) untuk menentukan jenis pelarut yang sesuai pada kromatografi kolom cair vakum dengan larutan pengembang (eluen) n-heksana-etil asetat, n-heksana-aseton dan aseton- etilasetat pada berbagai perbandingan, kemudian dideteksi dibawah lampu UV 254 dan 365 nm dan dilanjutkan dengan penyemprotan penampak noda CeSO4 2% lalu dipanaskan.
Proses fraksinasi pertama dilakukan dengan metode kromatografi kolom cair vakum, sebanyak 8,2675 gram ekstrak kental metanol daun ungu yang berbentuk pasta terlebih dahulu di impregnasi dengan silika gel 60 (0,2-0,5 mm) sebanyak 24,0780 gram hingga tercampur merata dan berbentuk pasir.
Kemudian kedalam kolom ditempatkan secara berturut-turut dari bagian bawah hingga atas yaitu silica gel 60 H merck sebanyak ±60 gram pada bagian paling bawah (fase diam) dan dirapatkan hingga padat, kertas saring whatman, sampel yang telah di impregnasi dan kembali kertas saring whatman. Kolom yang telah terkemas kemudian di elusi, pengelusian
dimulai dari pelarut yang bersifat nonpolar yaitu n-Heksan 100%
kemudian ditingkatkan kepolarnnya dengan campuran pelarut etil asetat dalam n-Heksan mulai dari perbandingan 1: 9 dan ditingkatkan secara bergradien hingga etil asetat 100%. Kemudian dengan eluen aseton dalam etil asetat mulai perbandingan (1:9) hingga eluen aseton 100% dan terakhir dengan pelarut polar yaitu metanol 100%.
Fraksi-fraksi yang dihasilkan kemudian di uji KLT, fraksi 1-52 di uji KLT dengan perbandingan eluen etil asetat dalam n-Heksan (2:8), karena fraksi 32-52 tidak menampakkan noda pada plat KLT maka diuji KLT kembali dengan eluen etil asetat 100%. Kemudian dilakukan penggabungan fraksi dan diperoleh 22 fraksi gabungan. Fraksi gabungan ini kemudian di KLT dengan eluen etil asetat dalam n-Heksan(2:8), karena fraksi gabungan 16-22 tidak menampakan noda maka dilakukan uji KLT kembali dengan eluen etil asetat dalama n-heksan (4:6). Fraksi-fraksi yang memiliki noda, warna dan pola pemisahan yang sama kemudian digabungkan dan diuapkan.
Fraksi E dengan berat 0,2635 gram dipilih untuk difraksinasi dengan metode kromatografi kolom tekan.
Sebelum difraksinasi terlebih dahulu diidentifikasi dengan KLT untuk menentukan eluen yang akan digunakan pada KKT. Kolom untuk fraksinasi dengan KKT diisi dengan gel 60 (0,063-0,200mm) hingga tinggi
±15 cm sebagai fase diam kemudian diisi sampel yang telah diimpregnasi.
Pengelusian dilakukan dengan menggunakan eluen n-heksana 100%, kombinasi n-heksana:etil asetat dengan perbandingan 9:1, 8:2, 6:4,
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
4:6, 2:8 Etil 100%, aseton 100% dan metanol 100% diperoleh sebanyak 25 fraksi. Fraksi- fraksi kemudian di KLT untuk penggabungan fraksi dengan eluen n-heksan : etil asetat (9:1) fraksi yang tidak menampakkan noda ditingkatkan kepolarannya dengan eluen n-heksan: etil asetat (4:6).
Fraksi E5 dengan berat 0,0482 kembali difraksinasi dengan kromatografi kolom tekan , pengelusian dilakukan dengan menggunakan eluen n-heksana 100%, kombinasi n-heksana:etil asetat dengan perbandingan 9:1, 8:2, 6:4, aseton 100% dan metanol 100%
diperoleh sebanyak 9 fraksi. Fraksi- fraksi yang diperoleh kemudian di KLT untuk penggabungan fraksi dengan menggunakan eluen n-heksan:
etil asetat (8:2).
Isolat yang diperoleh dimurnikan. Kemurnian isolat yang diperoleh ditentukan dengan KLT menggunakan sistem tiga eluen dengan menggunakan larutan pengembang atau eluen yang sesuai, jika hasil KLT memperlihatkan noda tunggal, maka senyawa tersebut telah murni.
Isolat diuji menggunakan pereaksi Liebermann-Burchard, FeCl3, Wagner dan Meyer untuk mengetahui golongan senyawa metabolit sekunder yang diperoleh. Identifikasi lebih lanjut dilakukan uji spektroskopi
dengan menggunakan
spektrofotometer FTIR Prestige-21 SHIMADZU untuk mengetahui gugus fungsi yang terdapat dalam senyawa tersebut.
3. Uji Antibakteri
Sampel uji meliputi ekstrak kasar, Fraksi E hasil KKCV dan isolat yang diperoleh. Sampel uji terlebih dahulu dilarutkan dengan menggunakan pelarut dimetil sulfoxida (DMSO) pada konsentrasi 5%, kemudian Paper disc diisi dengan sampel yang telah dilarutkan.
Pengujian aktivitas antibakteri dilakukan dengan metode difusi agar dengan cara menuangkan sebanyak ± 20 ml medium NA ke dalam cawan petri dan dibiarkan hingga memadat.
Kemudian di tuangkan suspensi bakteri kedalam medium NA tersebut dan diratakan hingga seluruh permukaan medium terdapat bakteri.
Meletakan paper disc yang telah berisi sampel uji dan larutan DMSO sebagai kontrol negatif diatas permukaan medium yang telah terinokulasi bakteri. Kemudian di inkubasi selama 1 x 24 jam. Apabila hasil inkubasi menunjukkan zona bening disekitar paper disc, menandakan adanya efek penghambatan larutan uji terhadap bakteri uji. Zona bening yang ada merupakan zona hambat, dapat diukur dengan menggunakan jangka sorong.
HASIL DAN PEMBAHASAN A. Hasil Penelitian
1. Isolasi dan Identifikasi Senyawa Metabolit Sekunder Ekstrak Metanol Daun Ungu.
a. Uji Pendahuluan
Uji pendahuluan bertujuan untuk mengetahui golongan senyawa metabolit sekunder yang terkandung
dalam sampel. Uji dilakukan dengan pereaksi Lieberman-Burchard, Besi (III) klorida (FeCl3), Meyer, dan Wagner, hasilnya pengujian dapat dilihat pada Tabel 4.1 dan perubahan yang terjadi pada masing-masing pereaksi dapat dilihat pada Gambar 1.
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
Tabel 1. Hasil Uji Pendahuluan Ekstrak Metanol Daun Ungu
No Pereaksi Hasil Keterangan
1 Lieberman-Burchard warna biru + Steroid 2 FeCl3 warna hijau kekuningan + Flavonoid
3 Meyer Warna kuning ˗˗ Alkaloid
4 Wagner Warna coklat ˗˗ Alkaloid
(a) (b) (c) (d) (e)
Gambar 1. Hasil Uji Pendahuluan Ekstrak Metanol Daun Ungu (a)Sampel (b)wagner (c)Lieberman-Burchard (d)Meyer (e)FeCl3
b. Fraksinasi, Pemurnian dan Identifikasi
Proses fraksinasi dilakukan dengan tujuan untuk memisahkan senyawa-senyawa yang terdapat pada sampel berdasarkan tingkat kepolarannya. Proses fraksinasi dapat dilakukan dengan berbagai metode, salah satunya adalah metode kromatografi kolom, untuk fraksinasi pada ekstrak kental yang telah diperoleh digunakan teknik kromatografi kolom cair vakum (KKCV). Sebelum dilakukan KKCV ekstrak kasar yang diperoleh terlebih dahulu dilakukan uji KLT.
Perbandingan eluen yang memiliki pola pemisahan yang baik dan memberikan penampakan noda yang jelas yaitu eluen n-heksana:etil asetat (8:2) sebagaimana terlihat pada Gambar 2.
Gambar 2. Kromatogram Lapis Tipis Ekstrak Metanol
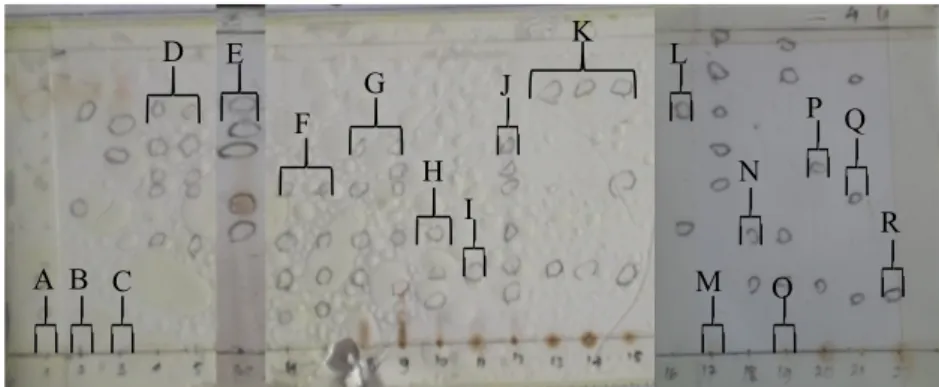
Proses fraksinasi dilakukan dengan menggunakan silika gel 60 H sebagai fase diam dan larutan yang ditingkatkan kepolarannya sebagai fase gerak. Pemisahan dilakukan berdasarkan pita-pita warna yang terdapat pada fase diamnya, dan diperoleh sebanyak 52 fraksi.Fraksi- fraksi tersebut kemudian di uji KLT untuk penggabungan fraksi, berdasarkan kemiripan pola noda dan pemisahan yang terbentuk pada kromatogram maka dihasilkan 18 fraksi gabungan utama (yaitu A-R).
Fraksi 1-15 dengan eluen etil asetat dalam n-Heksana (2:8) serta fraksi 16-22 dengan eluen etil asetat dalam n-Heksana (4:6).
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
Gambar 3. Kromatogram lapis tipis fraksi gabungan hasil KKCV.
Fraksi E kemudian difraksinasi lebih lanjut dengan metode kromatografi kolom tekan (KKT) dan menghasilkan 25 fraksi. Fraksi- fraksi tersebut kemudian di uji KLT
dengan eluen n-Heksan dalam etil asetat (9:1) dan (4:6) dan berdasarkan pola pemisahan yang terbentuk pada kromatogram dihasilkan 10 fraksi gabungan.
Tabel 2. Penggabungan Fraksi Hasil Kromatografi Kolom Tekan E Fraksi Gabungan Berat (g) Wujud
1-4 E1 0,0174 Padatan
5 E2 0,0444 Padatan
6 E3 0,0114 Kristal
7 E4 0,0055 Kristal
8 E5 0,0079 Kristal
9 E6 0,0263 Kristal
10-11 E7 0,0034 Padatan
12-18 E8 0,0278 Padatan
19-21 E9 2,2736 Padatan
22-25 E10 1,6924 Padatan
Fraksi gabungan E5 yang telah terbentuk kristal dipilih untuk dilanjutkan untuk proses KKT karena pada proses penguapan paling cepat terbentuk kristal dan memiliki bobot paling berat. Selanjutnya dilakukan uji KLT dan masih terdapat dua noda. Hal ini menunjukkan kristal tersebut belum
murni sehingga dilakukan kembali proses kromatografi kolom tekan.
Fraksi E5 difraksinasi dengan kromatografi kolom tekan (KKT) diperoleh 9 fraksi, kemudian fraksi di uji KLT dengan menggunakan eluen n-heksan: etil asetat (8:2) dan diperoleh 6 fraksi gabungan seperti terlihat pada Tabel 3.
Tabel 3. Penggabungan Fraksi Hasil Kromatografi Kolom Tekan E5
Fraksi Gabungan Berat (gr) Wujud
1-2 E5.1 0,0064 padatan
3 E5.2 0,0061 Padatan
4 E5.3 0,0349 Kristal
A B C
D E F
G
H I
J
K L
M N
O P Q
R
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
5 E5.4 0,0086 Padatan
6-7 E5.5 0,0080 padatan
8-9 E5.5 0,0290 Cairan
Pelarut fraksi-fraksi gabungan dibiarkan menguap dan diperoleh fraksi E 5.3 yang terbentuk kristal jarum berwarna hijau. Fraksi E 5.3
kemudian didekantasi dengan metanol sehingga menghasilkan kristal jarum bening dapat dilihat pada Gambar 4. berikut:
(a) (b)
Gambar 4. (a)Isolat Fraksi E5.3
sebelum dimurnikan (b)Isolat Fraksi E5.3 setelah dimurnikan
Senyawa murni yang diperoleh dengan bobot 30,9 mg kemudian diuji kemurniannya dengan KLT tiga sistem eluen dengan menggunakan perbandingan pelarut yang berbeda. Kromatogram senyawa murni terlihat setelah pemberian penampak noda CeSO4
dan pemanasan yakni berwarna ungu. Eluen yang digunakan yaitu n- heksan: etil asetat (9:1), kloroform:n- heksan (9:1) dan n-heksan:aseton
(8:2). Hasil kromatogram dapat dilihat pada Gambar 5.
(a) (b) (c)
Gambar 5. Kromatogram Senyawa Murni Hasil KLT Tiga Sistem Eluen
(a) Eluen n-heksan: etil asetat (9:1) (b) Eluen kloroform:n-heksan (9:1) (c) Eluen n-heksan: aseton (8:2)
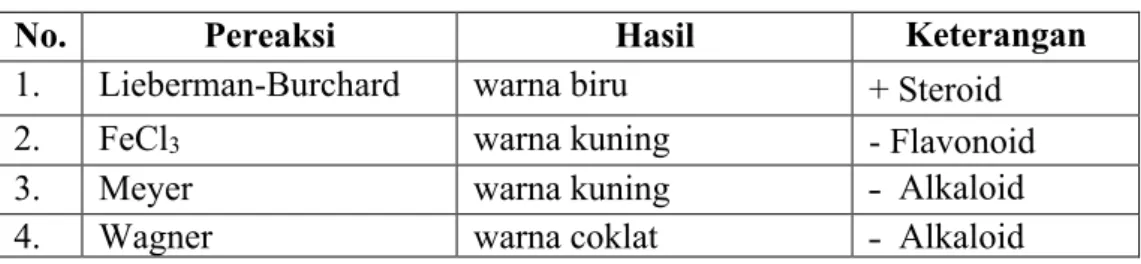
Senyawa murni yang diperoleh kemudiaan diidentifikasi menggunakan spektroskopi FTIR dan uji pereaksi untuk mengetahui golongan senyawanya. Hasil uji pereaksi yang diperoleh menunjukkan bahwa senyawa yang diperoleh merupakan golongan steroid. Hal ini ditunjukkan dengan reaksi positif antara senyawa murni dengan pereaksi Liberman-Burchard yang ditandai dengan perubahan warna dari tidak berwarna menjadi biru dapat dilihat pada tabel 4.
Tabel 4. Hasil Uji Pereaksi Senyawa murni
No. Pereaksi Hasil Keterangan
1. Lieberman-Burchard warna biru + Steroid
2. FeCl3 warna kuning - Flavonoid
3. Meyer warna kuning ˗ Alkaloid
4. Wagner warna coklat ˗ Alkaloid
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
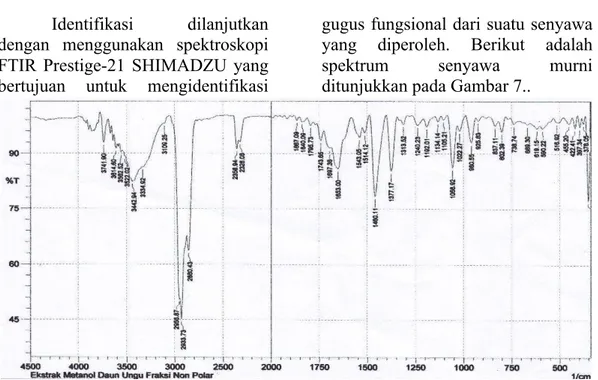
Gambar 6. Uji Golongan Senyawa Murni Identifikasi dilanjutkan
dengan menggunakan spektroskopi FTIR Prestige-21 SHIMADZU yang bertujuan untuk mengidentifikasi
gugus fungsional dari suatu senyawa yang diperoleh. Berikut adalah spektrum senyawa murni ditunjukkan pada Gambar 7..
Gambar 7. Spektrum Inframerah Senyawa Steroid
2. Uji Antibakteri
Ekstrak kasar metanol, fraksi E hasil KKCV dan isolat murni yang diperoleh dari proses isolasi dilakukan uji bioaktivitas terhadap
bakteri S.aureus dan E.coli. Hasil pengujian tersebut terhadap pertumbuhan bakteri S.aureus dan E.coli setelah diinkubasi selama 24 jam dapat dilihat pada Tabel 5.
.
Tabel 5. Rata-rata Diameter Zona hambat pertumbuhan bakteri S. aureus dan E.coli
Bakteri Sampel
(-) DMSO Ekstrak Kental Fraksi E Isolat
S. aureus - 10,27 mm 6,22 mm 6,37 mm
E. coli - - - -
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
Keterangan: Diameter zona hambat tanpa diameter paper disc pada Konsentrasi 5 %
B. Pembahasan
1. Isolasi dan Identifikasi Senyawa Metabolit Sekunder Ekstrak Metanol Daun Ungu.
Uji pendahuluan pada ekstrak metanol daun ungu bertujuan untuk mengetahui golongan senyawa metabolit sekunder yang terkandung di dalam ekstrak daun Pengujian menunjukkan hasil yang positif terhadap pereaksi FeCl3 dan Lieberman Burchard dimana terjadi perubahan warna sehingga dapat disimpulkan bahwa ekstrak metanol positif mengandung senyawa metabolit sekunder golongan steroid dan flavonoid, namun tidak mengandung senyawa alkaloid dan triterpenoid seperti yang dilaporkan oleh Tukiran (2014). Hal ini disebabkan karena kandungan senyawa metabolit sekunder dipengaruhi oleh ekologi tumbuhan yaitu antaraksi tumbuhan- hewan dan antaraksi tumbuhan-tumbuhan sehingga suatu jenis tumbuhan akan memiliki kandungan metabolit sekunder yang berbeda-beda
Pemisahan senyawa
berdasarkan pada sifat kepolarannya.
Hal ini didasarkan pada sifat kepolaran eluen yang berfungsi sebagai fase gerak dan akan menarik senyawa sesuai dari sifat kepolarannya yang melalui silika sebagai fase diamnya sehingga senyawa akan terpisah-pisah dalam beberapa fraksi. Metode KKCV merupakan metode awal fraksinasi yang umum digunakan untuk memisahkan sampel dalam jumlah banyak dan dilanjutkan dengan KKT.
Pada dasarnya pemisahan metode
KKCV dan KKT memiliki prinsip yang sama perbedaannya hanya terdapat pada ukuran kolom dan jumlah sampel yang dipisahkan selain itu pada metode KKCV dikemas secara kering dan vakum sedangkan KKT dikemas basah dan menggunakan tekanan untuk mempercepat laju eluen. Pengelusian dilakukan secara bergradien mulai dari pelarut non-polar sampai pelarut polar. Hal ini dimaksudkan agar semua senyawa non-polar maupun polar dapat terfraksinasi. Fraksinasi dilakukan dengan menggunakan silika gel yang memiliki ukuran partikel yang halus sehingga memiliki kerapatan yang tinggi di dalam kolom.
Fraksi yang dipilih untuk fraksinasi lebih lanjut (KKT) dengan pertimbangan adanya target yang ingin dicapai berdasarkan noda yang tampak pada saat KLT tidak banyak dan pemisahannya jelas, selain itu penampakan ciri fisik kristal. pada proses KKT dilakukan sebanyak dua kali hal ini dikarenakan pada saat KKT pertama kristal masih menampakkan dua noda yang berarti bahwa masih ada dua senyawa didalamnya.
Pemurnian isolat dengan cara dekantasi yaitu dengan melarutkan pengotor yang masih terdapat dalam kristal, namun tidak melarutkan kristal yang sudah ada, selanjutnya isolat diuapkan sampai diperoleh senyawa murni yang ditandai dengan hasil kromatogram yang menujukkan noda tunggal, senyawa murni berbentuk kristal jarum bening.
Senyawa murni yang diperoleh kemudian diuji
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
kemurniannya dengan metode KLT sistem tiga eluen dengan pelarut dan perbandingan yang berbeda. Hal ini dilakukan untuk memastikan kemurnian dari suatu senyawa yang ditunjukkan dengan munculnya satu noda pada tiap KLT. Pemisahan senyawa dianggap cukup apabila telah diperoleh isolat yang menunjukkan noda tunggal pada beberapa uji KLT dengan menggunakan berbagai variasi eluen yang berbeda. Adanya noda tunggal menunjukkan telah diperoleh senyawa dengan kemurnian yang tinggi (Atun, 2014).
Identifikasi dilanjutkan dengan uji pereaksi untuk mengetahui golongan senyawa yang diperoleh.
Hasil uji menunjukkan bahwa isolat memberikan reaksi positif steroid terhadap pereaksi Liebermann- Buchard yang ditandai dengan perubahan warna dari bening membentuk warna biru oleh H2SO4
pekat dengan pelarut asam asetat anhidrat , seperti yang terlihat pada Gambar 4.7.
Asam 3-aseto-5-kolesterol sulfonat (hijau-biru)
Gambar 8. Perkiraan Reaksi Uji Lieberman-Buchard (Hudaya, dkk. 2013) Identifikasi gugus fungsional isolat dilakukan menggunakan spektrofotometer FTIR dengan
metode pellet KBr pada rentang bilangan 4500-500 cm-1. Analisis spektrum IR senyawa murni memberikna pita serapan yang melebar dengan intensitas sedang pada bilangan gelombang (𝜈) 3442,94 cm-1 yang diidentifikasi sebagai vibrasi ulur O-H. Vibrasi ikatan ini merupakan vibrasi dari gugus O-H yang mengalami ikatan hidrogen antarmolekul. Hal ini didukung dengan adanya serapan tajam dengan
intensitas sedang pada daerah 𝜈 1058,92 cm-1 yang diidentifikasi
sebagai vibrasi ulur C–O alkohol sekunder siklik.
Serapan tajam dengan
intensitas kuat tampak pada daerah 𝜈 2956,67 cm-1 yang merupakan vibrasi ulur C–H pada –CH3 yang diperkuat dengan adanya serapan pada 𝜈 2660,43 cm-1. Selanjutnya serapan pada daerah 𝜈 2933,73 cm-1 diidentifikasi sebagai vibrasi ulur C–H pada –CH2– yang ditandai dengan serapan tajam dan kuat. Sifat khas – CH3 dan –CH2– ditandai dengan adanya serapan pada daerah 𝜈 3000–
2700 cm-1, di mana untuk vibrasi ulur –CH3 ( 𝜈 2960 dan 2870 cm-1), sedangkan vibrasi ulur –CH2– (𝜈 2930 dan 2850 cm-1). Hal ini memberi petunjuk bahwa struktur senyawa isolat mengandung gugus metil dan metilena.
Keberadaan gugus metil dan metilena diperkuat dengan adanya vibrasi tekuk –CH2– dan –CH3 pada daerah 𝜈 1460,11 dan 1377,17 cm-1 yang mengindikasikan adanya gugus geminal dimetil –CH(CH3)2 sebagai ciri khas senyawa triterpenoid/steroid.
Serapan oleh geminal dimetil biasanya pecah menjadi dua puncak dengan intensitas yang sama, tapi kedua puncak ini tidak selalu tampak pada
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
semua spektra, yang umum dijumpai hanya satu puncak saja (Sastrohamidjojo, 1992).
Adanya serapan tajam dengan
intensitas lemah pada daerah 𝜈 1653,00 cm-1 mengindikasikan
adanya vibrasi ulur C=C non
konjugasi (1620-1680 cm-1). Hal ini diperkuat dengan adanya vibrasi tekuk
=C–H (1000-650 cm-1) luar bidang pada daerah 𝜈 960,55 cm-1.
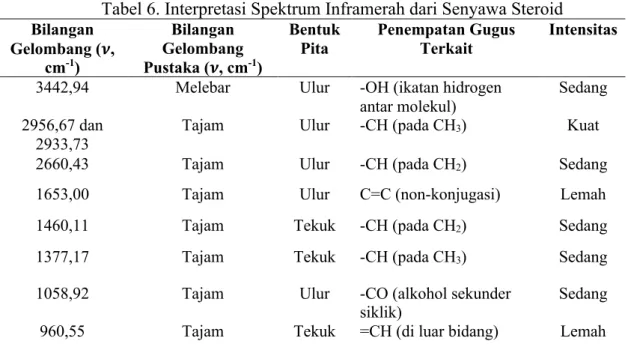
Tabel 6. Interpretasi Spektrum Inframerah dari Senyawa Steroid Bilangan
Gelombang (𝝂, cm-1)
Bilangan Gelombang Pustaka (𝝂, cm-1)
Bentuk Pita
Penempatan Gugus Terkait
Intensitas
3442,94 Melebar Ulur -OH (ikatan hidrogen
antar molekul)
Sedang 2956,67 dan
2933,73
Tajam Ulur -CH (pada CH3) Kuat
2660,43 Tajam Ulur -CH (pada CH2) Sedang
1653,00 Tajam Ulur C=C (non-konjugasi) Lemah
1460,11 Tajam Tekuk -CH (pada CH2) Sedang
1377,17 Tajam Tekuk -CH (pada CH3) Sedang
1058,92 Tajam Ulur -CO (alkohol sekunder
siklik)
Sedang
960,55 Tajam Tekuk =CH (di luar bidang) Lemah
2. Uji Antibakteri
Uji bioaktivitas ini dilakukan dengan tujuan untuk mengetahui kemampuan daya hambat dari sampel daun ungu. adapun bakteri yang digunakan pada uji bioaktivitas ini yaitu E. coli sebagai gram negatif
dan S.aureus sebagai gram positif.
Sebelum dilakukan pengujian terlebih dahulu alat dan bahan disterilisasi dengan tujuan untuk menghilangkan mikroorganisme yang terdapat pada alat dan bahan tersebut.
4
3 1 1 1
2 3
4
4
4
2 3
3 2
1
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
Gambar 9 Hasil Uji Antibakteri (a) S.aureus (b) E. coli.
(1) ekstrak kasar, (2) fraksi E, (3) senyawa murni(4) kontrol (-) DMSO Berdasarkan hasil yang
diperoleh diketahui bahwa ekstrak kasar, fraksi N dan isolat pada konsentrasi 5% dapat menghambat pertumbuhan bakteri S. aureus dan E.coli (Tabel 4.6). Daya hambat paling besar pada ekstrak kasar, hal ini disebabkan karena pada ekstrak masih terdapat banyak senyawa metabolit sekunder yang dapat menghambat pertumbuhan bakteri S.aureus maupun E.coli. Sedangkan pada fraksi N dan Isolat murni daya hambat semakin menurun, hal ini disebabkan karena terjadinya proses fraksinasi sehingga senyawa- senyawa yang memiliki sifat aktif terhadap bakteri telah terpisah-pisah kedalam beberapa fraksi.
Pengamatan pada bakteri S.aureus yaitu terbentuk zona bening yang berada disekitar paper disc setelah diinkubasi selama 24 jam dan begitu pula pada hari berikutnya, hal ini menunjukkan sampel uji bersifat membunuh bakteri S.aureus. Hal ini sejalan dengan penelitian yang telah dilakukan oleh Proboseno (2011), yang melaporkan bahwa pada ekstrak etanol daun ungu bersifat aktif terhadap bakteri S. aureus.
Pengamatan terhadap bakteri E.coli setelah proses inkubasi 24 jam terbentuk zona bening namun bakteri tumbuh kembali, hal ini menunjukkan bahwa sampel uji bersifat aktif dapat menghambat bakteri E.coli.
Kontrol negatif pada pengujian ini adalah dimetil sulfoxida (DMSO), tujuannya yaitu untuk mengetahui pengaruh DMSO dalam proses
pelarutan terhadap daya hambat yang dihasilkan. Pengujian ini menggunakan metode difusi agar dimana sampel yang telah terdapat pada paper disc akan berdifusi pada media Nutrien Agar dan membentuk zona bening setelah diinkubasi selama 24 jam, terbentuknya zona bening menunjukkan bahwa sampel uji bersifat aktif terhadap bakteri.
KESIMPULAN DAN SARAN A. Kesimpulan
Berdasarkan hasil yang diperoleh, maka dapat ditarik kesimpulan bahwa senyawa metabolit sekunder yang terdapat dalam ekstrak metanol fraksi nonpolar daun ungu adalah senyawa steroid berupa kristal bening berbentuk jarum. Hasil uji bioaktivitas ekstrak metanol, fraksi E dan isolat murni dapat menghambat pertumbuhan bakteri S. aureus, namun tidak dapat menghambat pertumbuhan bakteri E. coli
B. Saran
Adapun hal-hal yang disarankan terkait kelengkapan penelitian ini yaitu: Perlu dilakukan identifikasi dengan menggunakan spektrometer UV-Vis, GC-MS, NMR-1H dan NMR-13C untuk memantapkan struktur isolat tersebut, dan Perlu dilakukan penelitian lanjutan terhadap fraksi-fraksi yang tidak dilanjutkan serta menentukan Konsentrasi Hambat Minimum (KHM) terhadap pertumbuhan bakteri S. aureus dan E.coli.
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
DAFTAR PUSTAKA
Atun, S. 2010. Pemanfaatan Bahan Alam Bumi Indonesia Menuju Riset yang Berkualitas Internasional.
Seminar Nasinal Kimia.
Yogyakarta: FMIPA Universitas Negeri Yogyakarta.
Da’i, M., Astrina D. R., dan Arifah S. H. 2012. Uji Aktivitas Antiradikal Ekstrak Etanol Daun Elephantopus schaber L., Ocimum basilicum L.Forma Citratum Back., Graptophyllum pictum Griff, dan Gynura procumbens Merr. Dengan Metode Dpph (1,1-Difenil- 2-Pikril Hidrazil) Serta Penetapan Kadar Fenolik Totalnya. Journal Pharmacon. Vol.13, No.2.
Harborne, J.B. 1987. Metode Fitokimia Penuntun Cara Modern Menganalisa Tumbuhan. Edisi II.
Bandung: Institut Teknologi Bandung.
Hudaya, T., Prasetyo S., & Kristijarti A.P. 2013. Ekstraksi, Isolasi, dan Uji Keaktifan Senyawa Aktif Buah Mahkota Dewa (Phaleria macrocarpa) sebagai Pengawet Makanan Alami.
Hibah Monodisiplin. LPPM Universitas Katolik Parahyangan.
Isnawati, A dan Iwang, S. 2003.
Pemeriksaan Senyawa- Senyawa Turunan Fenol
Daun Handeuleum
(Graptophyllum pictum (L) Griff). Jurnal Media litbag kesehatan. Vol.13, No.1.
Pidada, I.B. Rai dan Suhargo, L.
2009. Peranan Ekstrak Daun Wungu {Graptophyllum pictum (l.) Griff.} untuk Menghambat Atrofi Kelenjar Mammae Mencit Betina Ovariektomi. J.
Penelitian. Med.Eksakta.
Vol. 8, No. 2.
Proboseno, S. 2011. Aktivitas Antibakteri Ekstrak Etanol
Daun Wungu
(graptophyllum pictum (l) griff ) terhadap Bakteri Staphylococcus aureus.
Skripsi. Jember: Fakultas Kedokteran Universitas Jember.
Sastrohamidjojo, H. 1992.
Spektroskopi Inframerah.
Yogyakarta: Liberty.
Sumarny , R., Yuliandini., dan Melly R. 2013. Efek Anti Inflamasi Dan Anti-Diare Ekstrak Etanol Herba Meniran (Phyllanthus niruri L.) dan Daun Ungu (Garptophyllum pictum L.
Griff). Prosiding seminar nasional perkembangan terkini sains farmasi dan klinik. ISSN: 2339-2592.
Swantara, I.M., Dira dan Yenni, C.
2009. Identifikasi Senyawa Antibakteri pada Daun Kecapi Sandoricum koetjape (Burm.f.). Jurnal Kimia. Vol. 3, No.2.
Tukiran, Suyatno, dan Nurul, H.
2014. Skrining Fitokimia pada Beberapa Ekstrak dari Tumbuhan Bugenvil (Bougainvillea glabra),
Jurnal Chemica Vo/. 22 Nomor 2 Desember 2021, 12 - 26
Bunga Sepatu (Hibiscus rosa-sinensis l.), dan Daun Ungu (Graptophylum
pictum griff.). Prosiding Seminar Nasional Kimia.
ISBN : 978-602-0951-00-3.