3
BAHAN DAN METODE
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Juni-Juli 2010 untuk pengambilan cuplikan di perairan laut Kota Tarakan, dan bulan Juli-Desember 2010 untuk analisis cuplikan di laboratorium. Cuplikan dianalisis di Laboratorium Kualitas Air Universitas Borneo Tarakan dan Laboratorium Pangan Universitas Islam Negeri (UIN) Syarif Hidayatullah Tanggerang Selatan.
3.2 Bahan dan Alat
Bahan yang digunakan selama penelitian adalah cuplikan sedimen, air, ikan Nomei (daging dan hati). Alat yang digunakan adalah ekman grab, dissecting set, frezee dried, van dorn water sampler dan pendeteksi PAH spektrometry massa gas kromatograf (GC-MS) tipe Shimadzu QP2010, detection limit 0.001 ppb.
3.3 Pengumpulan Data
3.3.1 Penentuan Stasiun Pengambilan Cuplikan
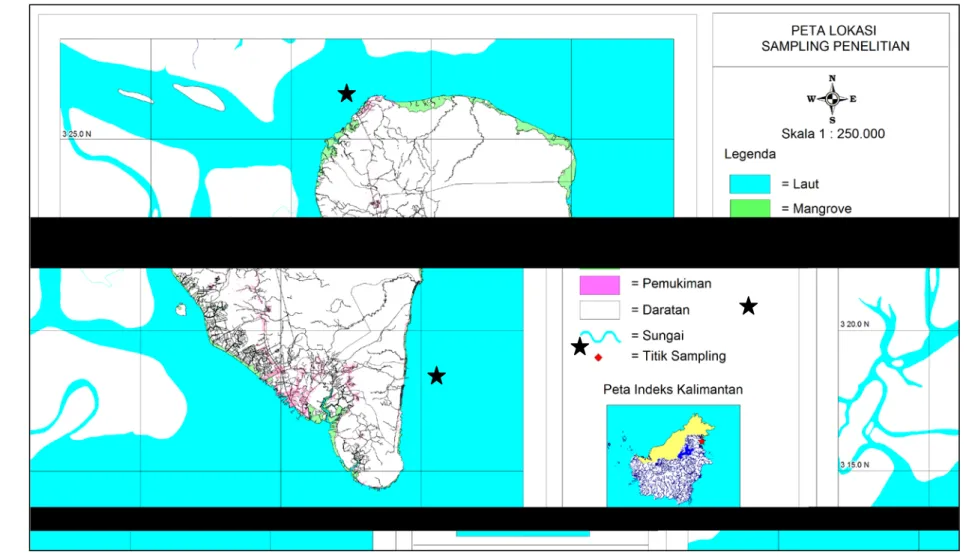
Stasiun pengambilan cuplikan air dan sedimen ditentukan berdasarkan 3 lokasi keterwakilan. Lokasi pertama adalah wilayah yang mewakili daerah kurang banyak kegiatan. Lokasi kedua merupakan lokasi pengambilan cuplikan ikan dan lokasi ketiga mewakili daerah yang aktif/banyak kegiatan. Pengambilan cuplikan ikan hanya dilakukan pada 1 stasiun yaitu lokasi penangkapan di utara (Stasiun 2) karena hanya di wilayah tersebut cuplikan ikan dapat ditemukan (Gambar 10) dan ditangkap pada saat kondisi air laut pasang.
3.3.2 Teknik Pengambilan Cuplikan
1. Air
Cuplikan air diambil dengan menggunakan van dorn water sampler berkapasitas 2 liter, kedalaman 1 meter dari permukaan air dan 1 meter dari permukaan sedimen yang kemudian di komposit. Sebanyak 2 liter
dimasukkan ke dalam botol gelap yang sudah dibersihkan dengan bilasan methanol dan hexan. Dalam trasportasi menuju laboratorium cuplikan dimasukkan dalam boks es, dan setelah di laboratorium disimpan dalam pembeku (freezer).
2. Sedimen
Sedimen dari dasar perairan diambil menggunakan ekman grab, selanjutnya dilakukan pengambilan cuplikan sedimen dengan menggunakan sub core sampai kedalaman 3 cm. Cuplikan sedimen kemudian disimpan dalam plastik yang telah disterilkan dengan prosedur IAEA 1360. Dalam transportasi menuju laboratorium cuplikan dimasukkan dalam boks es, dan kemudian setelah di laboratorium cuplikan disimpan dalam pembeku.
3. Cuplikan ikan Nomei
Cuplikan ikan dapat dibedakan berdasarkan berat badan kecil (27.9 ±79.41), sedang (181±735.9) dan besar (460±103 ) (Liang et al. 2007), berdasarkan ukuran tubuh (Neves et al. 2007), ukuran ikan dewasa (Ramachandran et al. 2006) dan berdasarkan panjang berat (Vuorinen et al. 2006). Dalam penelitian ini ikan dibedakan berdasarkan ukuran tubuh komersil (kecil (<20 cm), sedang (21-25 cm) dan besar (>25 cm)), selain untuk mendapatkan informasi konsentrasi akumulasi PAH berdasarkan ukuran tersebut.
Ikan Nomei diambil dengan menggunakan mini trawl. Kemudian ikan dibedakan berdasarkan tiga kelompok ukuran tubuh yaitu Ukuran kecil (<20 cm), sedang (21-25 cm) dan besar (>25 cm). Setiap ukuran cuplikan kemudian diambil hati dan dagingnya. Daging dipilih dengan pertimbangan bahwa di dalamnya memiliki kandungan lipid yang paling besar sehingga kemungkinan PAH yang terserap cukup banyak, sedangkan hati merupakan organ yang memetabolisme atau sebagai filter semua bahan beracun dalam tubuh ikan termasuk dalam hal ini PAH.
Berat cuplikan yang diambil disesuaikan dengan jumlah standar untuk kebutuhan analisis PAH. Kemudian cuplikan hati dan daging
disimpan dalam boks es selama transportasi ke laboratorium dan dalam laboratorium disimpan dalam pembeku sampai siap untuk dianalisis.
3.4 Analisis Cuplikan 3.4.1 Perlakuan Cuplikan
Sebelum dianalisis cuplikan sedimen, daging dan cuplikan hati ikan Nomei terlebih dahulu dikeringkan dengan pengering beku (freezed dried). Cuplikan air terlebih dahulu di saring untuk menghilangkan partikel sedimen, kemudian disimpan pada kondisi beku sampai analisis dilakukan.
3.4.2 Polycyclic Aromatic Hydrocarbons (PAH)
Prosedur analisis yang digunakan untuk PAH dalam air dilakukan menurut Yu et al. 2009 yang dimodifikasi (Lampiran 1). Cuplikan air sebanyak 2 liter diekstraksi menggunakan 30 ml dicloromethan sebanyak tiga kali. Supernatan kemudian dimurnikan dengan kolom gelas yang diisi dengan alumina/silica (1:2) 30 gr. Fraksi alifatik dielut dengan 20 ml hexan dan fraksi kedua yang merupakan PAH dielut dengan 70 ml diclorometan/hexan (3:7).
Analisis PAH dalam sedimen, daging dan hati ikan Nomei dilakukan dengan metode soxhlet (Liu et al. 2007) yang dimodifikasi (Lampiran 2). Cuplikan sedimen 40 gr kering diekstraksi menggunakan soxhlet ±16 jam dengan pelarut hexan/aseton (1:1) 150 ml. Supernatan kemudian diberikan perlakuan dengan bubuk tembaga untuk menghilangkan sulfur dan dimurnikan di kolom gelas dengan menggunakan silica gel yang diaktifkan/Al2O3
Fraksi alifatik dielut dengan hexan 40 ml dan fraksi aromatik dibilas dengan diclorometan/hexan (3:7). Cuplikan daging yang digunakan adalah 10 gr dan cuplikan hati 5 gr. Standar eksternal yang digunakan dalam penelitian ini adalah fluorin 100 ppm, fenantrena 100 ppm, antrasena 100 ppm dan fluorantena 100 ppm.
(1:2) 10 gr.
Analisis jenis PAH dalam cuplikan sedimen, air, daging dan hati ikan Nomei dilakukan dengan menggunakan GC-MS tipe Shimadzu QP2010, dengan detektor ionisasi nyala (FID), injeksi pisah (split injector) dan menggunakan silica lebur kolom (coulumn fused silica) DB5 MS dengan panjang 30 m, diameter
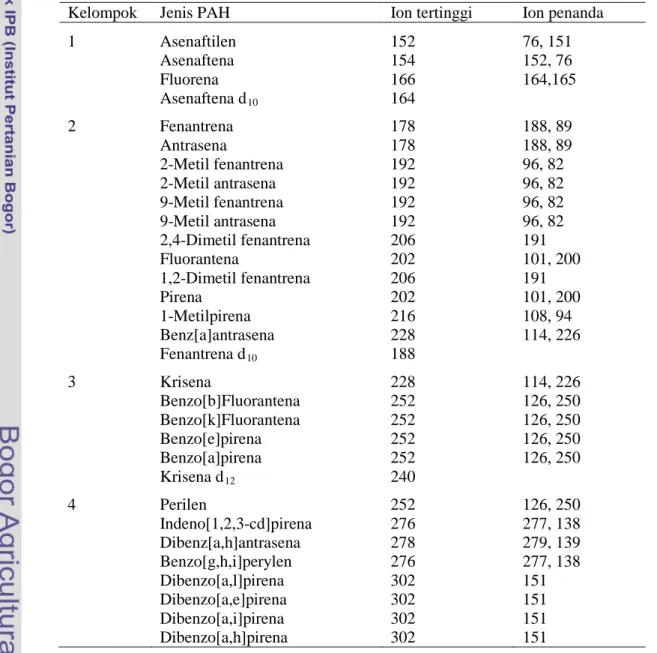
inline 0.32 mm. Temperatur program GC diatur pada 40oC selama 1 min, di naikkan 6 oC/menit sampai 300 oC, kemudian 300oC dipertahankan selama 20 min. Untuk mengidentifkasi jenis dan nama PAH, pada internal sistem GC-MS Shimadzu QP2010 menggunakan library National Institute of Standards and Technology (NIST) 27, NIST147 dan WILEY7. Selain internal library juga digunakan single ion monitoring (SIM) dalam Orecchio et al. 2009 (Tabel 11).
Tabel 11 Daftar 28 jenis PAH, kuantifikasi ion dan konfirmasi ion untuk SIM
(single ion monitoring) GC-MS yang digunakan dalam
mengidentifikasi senyawa PAH selain menggunakan library internal GC-MS (Orecchio et al. 2009).
Kelompok Jenis PAH Ion tertinggi Ion penanda
1 Asenaftilen 152 76, 151 Asenaftena 154 152, 76 Fluorena 166 164,165 Asenaftena d10 164 2 Fenantrena 178 188, 89 Antrasena 178 188, 89 2-Metil fenantrena 192 96, 82 2-Metil antrasena 192 96, 82 9-Metil fenantrena 192 96, 82 9-Metil antrasena 192 96, 82 2,4-Dimetil fenantrena 206 191 Fluorantena 202 101, 200 1,2-Dimetil fenantrena 206 191 Pirena 202 101, 200 1-Metilpirena 216 108, 94 Benz[a]antrasena 228 114, 226 Fenantrena d10 188 3 Krisena 228 114, 226 Benzo[b]Fluorantena 252 126, 250 Benzo[k]Fluorantena 252 126, 250 Benzo[e]pirena 252 126, 250 Benzo[a]pirena 252 126, 250 Krisena d12 240 4 Perilen 252 126, 250 Indeno[1,2,3-cd]pirena 276 277, 138 Dibenz[a,h]antrasena 278 279, 139 Benzo[g,h,i]perylen 276 277, 138 Dibenzo[a,l]pirena 302 151 Dibenzo[a,e]pirena 302 151 Dibenzo[a,i]pirena 302 151 Dibenzo[a,h]pirena 302 151
3.4.3 Analisis Lipid
Prosedur analisis yang digunakan untuk mengetahui kandungan lemak pada daging ikan Horpodon nehereus adalah SEAMIC IMFJ (Southeast Asian Medical Information Center International Medical Foundation of Japan) tahun 1985 (Lampiran. 3). Daging ikan Nomei 5 gr di tambahkan Na2SO4 10 gr kemudian di
campur. Masukkan dalam oven 105oC ± 2 jam, kemudian didinginkan dalam desikator. Cuplikan kemudian di ekstrasi dengan soxhlet dengan pelarut dietil eter 300 ml. Supernatan kemudian diuapkan dengan rotary evaporator sampai ± 10 ml. supernatant kemudian dipindahkan ke gelas beaker yang sudah diketahui beratnya, kemudian dikeringkan dan di timbang kembali.
3.5 Analisis Data
Dalam menentukan sumber pencemar PAH, digunakan beberapa rasio yaitu; rasio antara fluorantena dan pirena (FLA/FLA+PYR), rasio total isomer metilfenantrena terhadap fenantrena (MPHE/PHE), rasio BMR/BMT dan double ratio fenantrena (PHE), antrasena (ANT), fluorantena (FLA) dan pirena (PYR) (Tabel 12).
Tabel 12 Ratio individu PAH penentu sumber pencemar.
Ratio diagnosis Pirolitik Petrogenik Referensi
BMR/BMT <1 >1 Budzinski et al. 1997, Sicre et al. 1987,
Mostafa et al. 2009
∑MPHE/PHE <1 >1 Gschwend dan Hites (1981), Garrigues et al.
1995, Boonyatumanond et al. 2006
FLA(FLA+PYR) >0.5 <0.5 Budzinski et al. 1997, Qiao et al. 2006,
Mostafa et al. 2009.
PHE/ANT <10 >15 Liang et al. 2007, Soclo et al. 2000, Yim et
al. 2007, Tian et al. 2008, Ke et al. 2002, Tang et al. 2005
BMR : Berat molekul rendah; BMT : berat molekul tinggi; MPHE : metilfenantrena; PHE ; fenantrena; FLA : fluorantena; PYR : pirena
Dalam menentukan level konsentrasi di sedimen mengacu pada Baumard et al. (1998) (Tabel 13). Dalam menentukan efek kontaminasi PAH di sedimen terhadap organisme laut dilakukan perbandingan berdasarkan effect range low (ERL) dan effect range median (ERM) (Tabel 14) dan nilai kualitas lingkungan perairan terhadap PAH menggunakan kriteria menurut USEPA (Tabel 16). Dalam mengetahui status kontaminasi PAH pada tubuh, mengacu pada kriteria oleh Varanasi et al. 1993 dalam Gomes et al. 2010 (Tabel 15).
Tabel 13 Tingkatan level konsentrasi PAH pada sedimen (Baumard et al. 1998).
Konsentrasi Kecil Sedang Tinggi Sangat Tinggi
∑PAH (ng/g) 0-100 100-1 000 1 000-5 000 >5 000
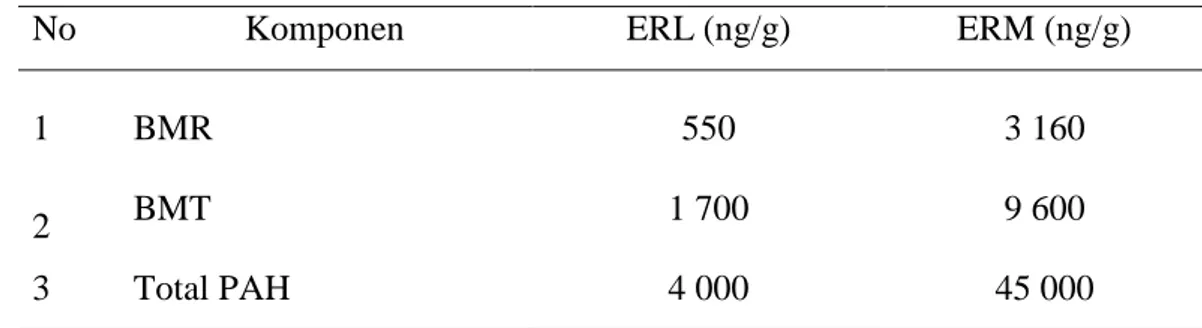
Tabel 14 Konsentrasi ERL (effect range low) dan ERM (effect range median) untuk menentukan status kontaminasi PAH di sedimen terhadap organisme laut (Woodhead et al. 1999; O’connor dan john 2000; Burton 2002).
No Komponen ERL (ng/g) ERM (ng/g)
1 BMR 550 3 160
2 BMT 1 700 9 600
3 Total PAH 4 000 45 000
Tabel 15 Klasifikasi status jaringan ikan yang terkontaminasi PAH (Varanasi et al. 1993 dalam Gomes et al. 2010).
No Klasifikasi Konsentrasi PAH (ng/g)
1 Tidak terkontaminasi <10
2 Nilai kontaminasi kecil 99-100
3 Nilai kontaminasi sedang 100-1 000
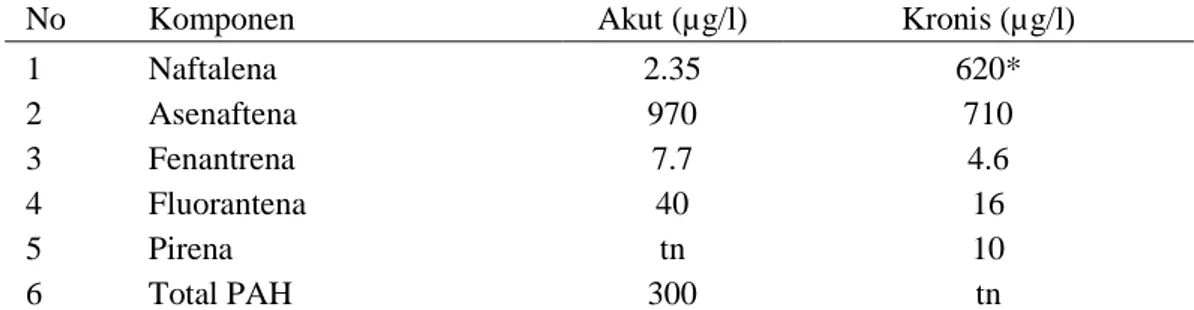
Tabel 16 Kriteria kualitas PAH di perairan laut menurut USEPA (Irwin 1997).
No Komponen Akut (µg/l) Kronis (µg/l)
1 Naftalena 2.35 620* 2 Asenaftena 970 710 3 Fenantrena 7.7 4.6 4 Fluorantena 40 16 5 Pirena tn 10 6 Total PAH 300 tn
Nilai berdasarkan Environmental Protection Agency (EPA), National Oceanic and Atmospheric Administrations (NOAA), Lowest observed effect concentrations (LOEC), tidak ada nilai (tn), (*) tidak ada nilai di perairan laut, nilai yang diberikan adalah perairan tawar.