BAB II
TINJAUAN PUSTAKA
2.1 Dimetil Eter
Dimetil Eter (DME) adalah senyawa eter yang paling sederhana dengan rumus kimia CH3OCH3. Dikenal juga sebagai methyl ether atau wood ether. DME
merupakan gas tak berwarna yang telah banyak digunakan dalam pemakaian sistem pendinginan. Jika DME dioksidasi yang terjadi adalah dekomposisi menjadi bentuk metanol dan formaldehid. DME termasuk bahan kimia tidak beracun, senyawa yang tidak mengandung unsur Sulfur (S) dan Nitrogen (N), sehingga memungkinkan emisi SOx, NOx, particulate matter, dan jelaga yang jauh lebih rendah dari solar. DME tidak bersifat korosif terhadap metal (Mayers, 1982).
Tabel 2.1 Sifat-sifat fisik Dimetil Eter
Sifat Fisik Nilai
Rumus molekul CH3OCH3
Berat molekul 56,069 kg/kmol
Titik beku -138,5°C
Titik didih (pada 760 mmHg) -24,7°C
Densitas (pada 20°C) 677 kg/mol
Indeks bias, pada (-42,5°C) 1,3441
Specific gravity cairan 0,661 (pada 20°C)
Flash point (pada wadah tertutup) -42°F
Panas pembakaran 347,6 kkal/mol
Panas spesifik (pada -27,68°C) 0,5351 kkal/mol Panas pembentukan (gas) -44,3 kal/g Panas laten (gas), (pada -24,68°C) 111,64 kal/g Kelarutan dalam air (pada 1atm) 34 %berat Kelarutan air dalam DME (1 atm) 7 %berat
Fase, 25°C, 1 atm gas
Temperatur kritis 400 K
Sifat kimia dimetil eter :
1. Dimetil eter bereaksi dengan karbon monoksida dan air menjadi asam dengan katalisator Col.
CH3OCH3 + H2O +CO → 2CH3COOH 2. Bereaksi dengan sulfur trioksida membentuk dimetil eter
CH3OCH3 +SO3 → (CH3)2SO4
3. Dengan hidrogen sulfit dengan bantuan katalisator tungsten sulfit (WS2) membentuk dimetil sulfit
CH3OCH3 + H2S → CH3–S–CH3- + H2O
4. Dengan reaksi oksidasi dimetil eter akan menghasilkan formaldehid. CH3OCH3 + O2 → 2CH2O + H2O
(Ketta, 1990)
2.2 Penggunaan DME
DME dikenal sebagai propellant dalam bentuk aerosol yang banyak digunakan sebagai salah satu bahan pendorong dalam industri parfum, obat pembasmi nyamuk, foam (sabun pencukur kumis bagi pria), pengharum ruangan,
colognes, hair sprays, personal care mousses, antiperspirants, room air fresheners. Dan industri coating dan otomotif. Sekarang ini DME sedang diproyeksikan untuk dijadikan salah satu sumber bahan bakar alternatif ramah lingkungan yang nantinya akan menggantikan LPG, LNG, dan bahan bakar diesel (Anonim, 2008). Berikut ini aplikasi penggunaan DME dunia,
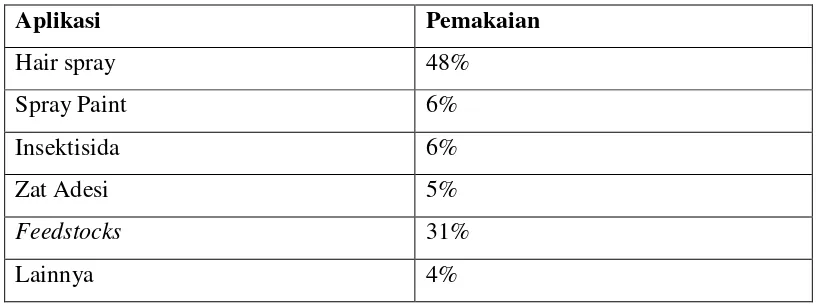
Tabel 2.2 Aplikasi Dimetil Eter dalam berbagai produk
Aplikasi Pemakaian
Hair spray 48%
Spray Paint 6%
Insektisida 6%
Zat Adesi 5%
Feedstocks 31%
Lainnya 4%
Dimetil Eter termasuk salah satu bahan bakar alternatif yang ramah lingkungan. DME dapat digunakan sebagai bahan bakar yang bebas dari sulfur untuk mesin disel tanpa pembentukan partikulat dan rendah emisi NOx jika dibandingkan dengan minyak dan gas. DME juga memiliki sifat yang sama dengan propana dan butana, senyawa pembentuk LPG, sehingga DME dapat didistribusikan dan disimpan menggunakan teknologi penanganan LPG dan DME dapat digunakan sebagai pengganti LPG. DME juga dapat digunakan sebagai aerosol propellant untuk menggantikan chloroflourocarbon, yang diketahui dapat merusak lapisan ozon di atmosfer. DME juga merupakan bahan kimia intermediet yang penting dalam produksi bahan kimia seperti etilen, dimetil sulfat, dan metal asetet (Hermansyah, 2010).
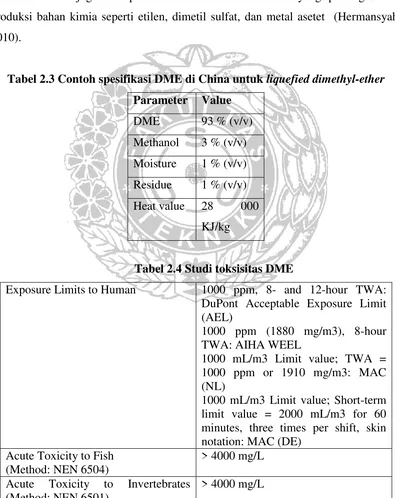
Tabel 2.3 Contoh spesifikasi DME di China untuk liquefied dimethyl-ether Parameter Value DuPont Acceptable Exposure Limit (AEL) Acute Toxicity to Invertebrates
(Method: NEN 6501)
Acute Toxicity to Aquatic Plants (Type: 96-hour EC50)
-
Oral Toxicity -
Inhalation 4-hour LC50 164,000 ppm (95 % confidence limits)
Cardiac Sensitization
Dermal Sensitization -
Eye Irritation -
( Dupont, 2008)
2.3 TKKS (Tandan Kosong Kelapa Sawit)
Tandan kosong kelapa sawit merupakan limbah utama berligniselulosa yang belum termanfaatkan secara optimal dari industri pengolahan kelapa sawit. Basis satu ton tandan buah segar akan dihasilkan minyak sawit kasar sebanyak 0,21 ton (21%), minyak inti sawit sebanyak 0,05 ton (0,5%) dan sisanya merupakan limbah dalam bentuk tandan kosong, serat dan tandan kosong biji yang masing – masing sebanyak 0,23 ton (23%), 0,135 ton (13,5%) dan 0,055 ton (5,5%) (Darnoko, 1992). Padahal tandan kosong kelapa sawit berpotensi untuk dikembangkan menjadi barang yang lebih berguna, salah satunya menjadi bahan baku dimetil eter. Hal ini karena tandan kosong kelapa sawit banyak mengandung selulosa yang dapat dihirolisis menjadi glukosa kemudian difermentasi menjadi dimetil eter. Kandungan selulosa yang cukup tinggi yaitu sebesar 45% menjadikan kelapa sawit sebagai prioritas untuk dimanfaatkan sebagai bahan baku pembuatan dimetil eter (Aryafatta, 2008).
2.4 Komposisi TKKS (Tandan Kosong Kelapa Sawit)
Hasil komposisi Tandan Kosong kelapa sawit dapat diperoleh menggunakan metode Thermogravimetric Analysis (TGA) melalui reaksi pirolisis dalam reaktor batch 200 cm3. Dalam pengerjaannya kira-kira 20 mg sampel dipanaskan pada 25 oC menit-1 sampai 600 oC menggunakan nitrogen sebagai gas pembersih.
Tabel 2.5 Proximate Analysis dari tandan kosong kelapa sawit (% berat)
Parameter nilai
Tabel 2.6 Ultimate Analysis dari tandan kosong sawit (% berat kering) Parameter nilai Tabel 2.7 Analisis gas dari tandan kosong sawit (% berat)
Berat jenis : 1 gr/cm3 (pada suhu 25 0C)
Titik lebur : 0 0C
Titk didih : 100 0C
(Othmer, 1967)
2.5.2. Oksigen
Wujud : Gas
Rumus : O2
Berat Molekul : 32
Titik Didih, oC : -182,95 Temperatur Kriris, oC : -118,38 Tekanan kritis, atm : 50,14
Cp, Joule/mol oC : 29,1 + (1,158*10-2)T - (0,6076*10-5)T2
+ (1,311*10-9) T3
(Othmer, 1967) 2.5.3 Nitrogen
Wujud : Gas
Rumus : N2
Berat Molekul : 28,01
Titik Didih, oC : -195,8 Temperatur Kriris, oC : -146,96 Tekanan kritis, atm : 33,5
Cp, Joule/mol oC : 29 + (0,2199*10-2)T + (0,5723*10-5)T2 (2,871*10-9) T3
2.5.4 Olivine1
Wujud : Solid
Rumus : Tidak Diketahui
Berat Molekul : 89,3
∆Hf (s) : -753,659 kJ/mol
Cp, kJ/kg oK : 1,036 1
Berat molekul dihitung berdasarkan komposisi dari Fuel Processing
Technology 86, Tabel 3 hal. 717, (dalam % berat) MgO=49; SiO2=40;
2.5.5 Katalis Olivine2
Berat molekul dihitung berdasarkan komposisi dari Fuel Processing
Technology 86, Tabel 3 hal. 717, (dalam % berat) MgO=46; SiO2=39;
Fe2O3=9,2; Al2O3=0,4; Cr2O3=0,4; CaO = 0,3 dan NiO=4,7
2.6 Proses Pembuatan Dimetil Eter
Dimetil Eter dapat diperoleh melalui dua cara, yaitu melalui proses langsung dan proses tidak langsung. Melalui proses tidak langsung, metanol disintesis terlebih dahulu, diikuti dengan reaksi dehidrasi Metanol, dan pada reaktor terpisah Dimetil Eter akan disintesis. Pada proses pembentukan langsung, gas sintetis (H2 & CO) disintesis menjadi Dimetil Eter. Proses reaksi Dimetil Eter langsung merupakan hasil sintesa Metanol dari gas sintetis dan dehidrasi Metanol yang terproses dalam reaktor yang sama. Proses yang akan digunakan dalam pabrik ini adalah pembentukan
Tipe reaktor dasar yang digunakan untuk sintesa reaksi langsung mirip dengan reaktor sintesa FT (Fischer-Tropsch) atau reaktor sintesa Metanol. Keuntungan:
Prosesnya sederhana, peralatan yang dipergunakan sedikit. Konversinya tinggi, rata-rata lebih dari 90%.
Kerugian:
Suhu operator cukup tinggi (2500C) b. Indirect synthesis
Metanol sintesis-2 CO2 + 3 H2–> CH3OH +H2O +49.4 kJ/mol (2) Metanol dehydration 2CH3OH –> CH3OCH3 + H2O +23.4 kJ/mol (3) Overall CO + CO2 + 5 H2 –> CH3OCH3 +2H2O +163.5 kJ/mol (4) Kentungan:
Suhu dan tekanan operasi reaktor relatif rendah. Kerugian:
Peralatan yang digunakan lebih banyak.
Menggunaakan asam sulfat yang berfsifat korosif sehingga diperlukan peralatan dengan bahan konstruksi yang tahan terhadap korosi yang harganya lebih mahal.
Konversinya rendah, yaitu : 45% (Galuh, 2011)
2.7 Seleksi Pemilihan Proses
Pada pra rancangan pabrik pembuatan Dimetil Eter, proses yang dipilih adalah proses direct synthesis tandan kosong kelapa sawit. Proses ini dipilih dengan pertimbangan :
- Jumlah Dimetil eter yang dihasilkan lebih besar
- Merupakan proses yang efisien untuk mengubah biomassa TKKS menjadi Dimetil eter
- Jumlah peralatan yang digunakan dapat lebih sedikit
- Dibandingkan dengan proses dehidrasi metanol yang berasal dari gas alam yang tidak dapat diperbaharui, bahan baku untuk proses yang dimulai dari gasifikasi biomassa lebih lebih bersifat renewable.
- Secara komersial dan ekonomis dapat bersaing dengan proses lain.
2.8Deskripsi Proses 2.8.1 Persiapan TKKS
Sebelum memasuki proses gasifikasi, TKKS harus melalui proses perlakuan awal (pre- treatment) seperti pengeringan dan pencacahan. Semakin kering umpan biomassa, efisiensi gasifikasi akan meningkat (Hamelinck, 2001). Kadar air optimum untuk aplikasi gasifikasi biomassa yang akan dilanjutkan dengan siklus kombinasi berkisar antara 10-15% (Faaij, 1998).
diterima kemudian diangkut menggunakan traktor menuju Cutting Machine (CR-101) untuk diseragamkan ukurannya lalu menuju Rotary Dryer (RD-101) untuk dikeringkan dari kandungan air 25% menjadi 12%. Selanjutnya dengan menggunakan ScrewConveyor (C-101) TKKS dikirim ke bejana gasifier.
2.8.1 Produksi Gas Sintetis
Dari bagian penanganan umpan, TKKS masuk kedalam unit gasifier (R-201). Sedangkan hasil pembakaran yang berupa char dikirim ke char combustor (R-202).. Gasifier yang digunakan dalam analisis ini adalah gasifier dengan pemanasan tidak langsung yang bertekanan rendah. Gasifier ini didesain sebanyak 2 buah dengan struktur yang identik. Suhu operasi diatur pada 870°C dan tekanan operasi 23 psia (1,565 atm).
Panas untuk reaksi-reaksi yang terjadi pada gasifier disuplai dengan mensirkulasikan media pemanas (olivine) yang dibakar bersama char di dalam char combustor. Dalam kasus ini, mediumnya adalah olivin sintetik, yang terdiri atas magnesium silikat yang dikalsinasi (Enstatite [MgSiO3], Forsterite [Mg2SiO3], dan
Hematite [Fe2O3]).
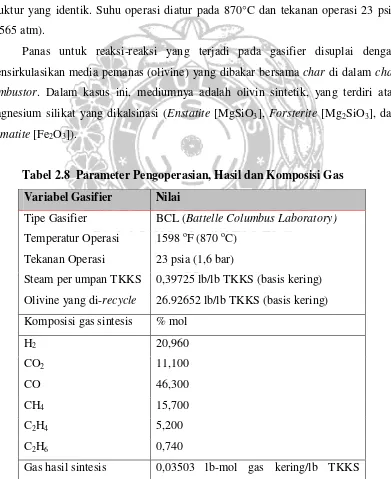
Tabel 2.8 Parameter Pengoperasian, Hasil dan Komposisi Gas Variabel Gasifier Nilai
Tipe Gasifier BCL (Battelle Columbus Laboratory)
Temperatur Operasi 1598 oF (870 oC) Tekanan Operasi 23 psia (1,6 bar)
Steam per umpan TKKS 0,39725 lb/lb TKKS (basis kering) Olivine yang di-recycle 26.92652 lb/lb TKKS (basis kering) Komposisi gas sintesis % mol
H2 20,960
CO2 11,100
CO 46,300
CH4 15,700
C2H4 5,200
C2H6 0,740
(basis kering)
Char yang dihasilkan 0,221 lb/lb TKKS (basis kering)
Sumber : Technical Report NREL/TP-510-37408 May 2005
Catatan : Efisiensi gasifier didefenisikan sebagai energi pembakaran dari gas sintesis dibagi dengan energi pembakaran dari biomassa
Sejumlah kecil MgO harus ditambahkan bersama olivine untuk mencegah pembentukan aglomerasi (penggumpalan seperti kaca) yang dihasilkan dari interaksi kalium dalam TKKS dengan komponen silika. Tanpa penambahan MgO, kalium akan membentuk gelas/kaca (K2SiO4) dengan silika dalam sistem tersebut. K2SiO4 mempunyai titik lebur yang rendah (930oF) dan terbentuknya K2SiO4 tersebut akan menyebabkan media olivine menjadi lengket, terjadi aglomerasi, dan cepat menjadi defluidisasi. Kadar abu dalam umpan diasumsikan terdiri atas 0,2% berat kalium. MgO ditambahkan sebanyak 2 kali aliran mol dari kalium.
Steam bertekanan rendah digunakan sebagai media gasifikasi yang diperoleh dari siklus steam. Perbandingan steam untuk TKKS adalah 0,39725 lb steam/lb TKKS kering. Suhu char combustor di set pada 1800oF (982,22 oC). Laju alir sirkulasi olivine adalah 26.92652 lb olivine/lb TKKS kering. Olivine segar ditetapkan pada laju 0,11% dari laju sirkulasi untuk menutupi kehilangan Olivine dari cyclone. Udara pembakaran dalam simulasi ini adalah 12% udara berlebih.
Pemisahan partikel dilakukan melalui cyclone separator (S-201 dan S-202). Mayoritas dari olivine dan char (99,9% dari keduanya) dipisahkan dalam Gasifier cyclone (S-201) dan selanjutnya dikirim ke char combustor. Combustor cyclone (S-202) memisahkan olivine (99,9%) dari pembakaran gas dan olivine akan dikirim kembali menuju gasifier. Abu dan banyak partikel pasir yang dipindahkan dikirim menuju tempat pengolahan limbah.
thermo-catalytic conversion system dan NREL’s Thermochemical Pilot Process
Development Unit (TCPDU).
Tabel 2.9 Kinerja rancangan dari Reformer Komponen % konversi menjadi CO & H2
CH4 20%
C2H4 50%
C2H6 90%
(Phillips, dkk, 2004)
Dalam rancangan ini, gas yang masuk kedalam reformer adalah pada suhu
gasifier (870oC) dan suhu gas keluaran reformer adalah 1383 F (750,56 oC). Sebelum menuju tahapan pembersihan, gas panas akan didinginkan sampai 300 oF (148,9 oC) dengan alat penukar panas (H-201 dan H-202) yang terintegrasi dalam siklus steam.
2.8.2 Persiapan Gas Sintesis (Gas Clean Up and Compression)
Setelah pendinginan langsung dari gas sintesis pada suhu 300oF, dilanjutkan dengan penambahan pendinginan yang dilakukan melalui Water Scrubbing (M-301 dan M-302). Scrubber juga menghilangkan impuritis seperti partikulat dan residu. Sistem scrubbing terdiri dari Venturi Scrubber dan Quench Chamber. Quench water
didinginkan melalui Heat Exchanger dan disirkulasi kembali menuju Venturi Scrubber (M-302) dan Quench Chamber (M-301). Laju alir quench water ditentukan dengan menyesuaikan laju sirkulasi suhu keluar dari air pendingin Heat Exchanger
(H-301) yaitu sebesar 110 F (43,33oC). Kelebihan water scrubber akan dikirim menuju fasilitas pengolahan air limbah. Jumlah air untuk scrubber sekitar 2 galon per menit dari kelebihan air untuk pabrik ukuran 2000 ton material kering per hari. Untuk tujuan perancangan, kadar air dari aliran lumpur (sludge) diatur pada 50% berat. Suhu pendinginan pada tahap pembersihan gas sintesis adalah pada 140oF. Gas sintesis kemudian dimampatkan atau dikompresi menjadi 2068 kPa menggunakan 3 (tiga) kompresor sentrifugal dengan pendingin interstage (K-301A/B, 301, S-302A/B, S-303, H-S-302A/B, dan H-303). Kompresor yang dimodelkan masing-masing bagian mempunyai efisiensi politropik 78% dan dengan suhu intercooler 140 o
2.8.3 Pembuatan Dimetil Eter
Gas sintesis yang telah dibersihkan dan diatur perbandingan CO/H2 = 1,0, akan memasuki reaktor sintesis DME. Reaksi yang terjadi di dalam reaktor ini adalah:
CO + 2H2 CH3OH
CH3OH CH3OCH3 + H2O CO + H2 CO2 + H2O
Umumnya dimetil eter dapat diperoleh melalui dua cara, yaitu melalui proses langsung dan proses tidak langsung. Melalui proses tidak langsung, metanol disintesis terlebih dahulu, diikuti dengan reaksi dehidrasi metanol, dan pada reaktor terpisah Dimetil Eter akan disintesis. Pada proses pembentukan langsung, gas sintetis
(H2 & CO) disintesis menjadi Dimetil Eter (Sumahamijaya, 2008). Gas sintesis yang telah dibersihkan, diatur perbandingan CO/H2 = 1,0, masuk ke reaktor sintesis Dimetil Eter.
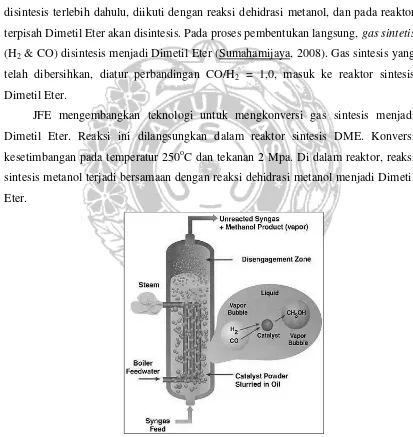
JFE mengembangkan teknologi untuk mengkonversi gas sintesis menjadi Dimetil Eter. Reaksi ini dilangsungkan dalam reaktor sintesis DME. Konversi kesetimbangan pada temperatur 250oC dan tekanan 2 Mpa. Di dalam reaktor, reaksi sintesis metanol terjadi bersamaan dengan reaksi dehidrasi metanol menjadi Dimetil Eter.
Gambar 2.2 Reaktor Sintesis Dme (Ohno, 2001)
Temperatur = 250oC Tekanan = 2.0 MPa
Perbandingan CO/H2 gas sintesis umpan = 1.0
Catalyst loading ratio (= perbandingan berat katalis (kg) terhadap laju alir gas reaktan (kg/jam)) = 0,003
Katalis yang digunakan berbentuk serbuk halus dimasukkan bersamaan dengan minyak sebagai medium. Gas sintesis diumpankan ke reaktor dan membentuk gelembung kecil yang homogen dan bereaksi ketika gelembung tersebut naik. Eksperimen yang dilakukan Khandan, Kazemeini, Aghaziarati (2008) menunjukkan katalis yang baik untuk reaksi ini adalah CuZn/Al2O3. Katalis ini dapat menghasilkan konversi CO sebesar 76% dan selektivitas DME sebesar 97,8% (Ogawa, 2003).
2.8.4 Pemurnian Produk