BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Daun bangun-bangun merupakan tanaman daerah tropis yang daunnya
memiliki aroma tertentu sehingga dikenal sebagai tanaman aromatik. Tanaman
ini banyak ditemukan di India, Ceylon dan Afrika Selatan, memiliki bunga
yang bentuknya tajam dan mengandung minyak atsiri sehingga disebut juga
Coleus aromaticus (Anonim, 2010; Kaliappan, et al., 2008).
2.1.1 Sistematika tumbuhan
Menurut Pandey (2003), sistematika tanaman bangun-bangun adalah
sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Kelas : Dicotyledoneae
Ordo : Solanales
Famili : Lamiaceae
Genus : Plectranthus
Spesies : Plectranthus amboinicus (Lour.) Spreng
2.1.2 Nama daerah
Di beberapa daerah di Indonesia, tanaman ini dikenal dengan nama
yang berbeda-beda. Masyarakat Sumatera menyebutnya bangun-bangun atau
kambing, majha nereng. Di Jawa Tengah disebut daun cumin. Orang Sunda
menyebutnya daun ajeran, di Nusatenggara disebut iwak, kumu etu, bumbu jo
(Depkes, 1989; Anonim, 2010; Jaitun, 2010). Daun ini juga dikenal di Negara
lain misalnya Inggris dengan sebutan country borage, indian mint, mexican
mint, di Vietnam disebut tan day la, sedangkan di Cina disebut zuo shou xiang,
yin du bo he, dao shou xiang. Dan di Jepang disebut kuuban oregano (Jaitun,
2010).
2.1.3 Morfologi tumbuhan
Daun bangun-bangun memiliki ciri-ciri bertulang lunak,
beruas-ruas, melingkar dengan diameter sekitar 15 mm, bagian tengah dan ujungnya
sekitar 10 mm ± 5 mm, dapat berkembangbiak dengan mudah (Anonim, 2010).
Daun tunggal, berwarna hijau, helaian daun berbentuk bundar telur,
kadang-kadang agak membundar, panjang helaian daun 3,5 cm sampai 6 cm, lebar 2,5
cm, pinggir daun beringgit atau agak berombak, tangkai daun panjang 1,5 cm
sampai 3 cm, tulang daun menyirip. Pada keadaan segar helaian daun tebal,
sangat berdaging dan berair, tulang daun bercabang-cabang dan menonjol
sehingga membentuk bangunan menyerupai jala, permukaan atas
berbingkul-bingkul, berwarna hijau muda, permukaan bawah berambut halus berwarna
putih. Pada keadaan kering helaian daun tipis dan sangat berkerut, permukaan
atas kasar, warna coklat sampai coklat tua, permukaan bawah berwarna lebih
muda dari permukaan atas, tulang daun kurang menonjol, pada kedua
permukaan terdapat rambut halus berwarna putih (Depkes, 1989).
Kandungan kimia daun bangun-bangun adalah glikosida, karbohidrat,
asam amino, protein, flavonoid, tanin, senyawa fenol, dan terpenoid, minyak
atsiri (karvakrol, eugenol, limonen, mirsen, pinen, selenen, terpinen, timol, dan
verbenon), vitamin C, vitamin B12, beta karotin, niasin, karvakrol, kalsium,
asam-asam lemak, asam oksalat, dan serat. Terdapat juga apigenin,
cirsimaritin, eriodictyol, genkawanin, luteolin, kuersetin, salvigenin, taxifolin,
asam oksaloasetat, crategolic, asam ursulat, sitosterol (Santosa dan Hertiani,
2005; Rout, et al., 2012).
2.1.5 Khasiat tumbuhan
Daun bangun-bangun berkhasiat sebagai antioksidan, anti tumor, anti
mutagenik, mengobati bronkitis, asma, diare, epilepsi, demam, batuk, sakit
kepala, gangguan pencernaan, dispepsia, konvulsi, batu ginjal, disentri, kolera,
antioksidan, antitumor, antimikroba, antimutagenik, antijamur (Rout, et al.,
2010), sakit gigi, gangguan pendengaran, gangguan saluran cerna (Chandrappa,
et al., 2010), malaria, obat cacing, hepatoprotektif (Kaliappan, et al., 2008),
obat luka, sariawan, mencegah kanker, antivertigo, diuretik, antiinfertilitas,
immunostimulan, hipokolesterolemik, antiradang, meningkatkan total volume
ASI (Santosa dan Hertiani, 2005).
2.2 Kanker
Kanker adalah istilah tidak umum untuk pertumbuhan sel tidak normal,
yaitu suatu kondisi dimana sel telah kehilangan pengendalian dan mekanisme
normal, sehingga mengalami pertumbuhan yang tidak normal, cepat dan tidak
jaringan tubuh normal sehingga mempengaruhi fungsi tubuh. Kanker bukan
merupakan penyakit menular (Diananda, 2009).
Ciri sel kanker yang membedakan dengan sel normal, antara lain
sebagai berikut:
a. Sel kanker mampu mencukupi kebutuhan sinyal pertumbuhannya sendiri.
Sinyal pertumbuhan eksternal (mitogenic growth factor) dibutuhkan
oleh sel normal untuk berproliferasi. Pada kondisi normal terdapat regulasi
terhadap rangsangan sinyal pertumbuhan sehingga proses perkembangan sel
dapat dikontrol. Namun sel kanker dapat memproduksi growth factor sendiri
sehingga tidak bergantung pada rangsangan sinyal pertumbuhan dari luar untuk
melakukan proliferasi. Mutasi yang terjadi pada sel kanker memungkinkan sel
tersebut untuk memperpendek growth factor pathway. Dengan demikian, sel
kanker dapat tumbuh menjadi tidak terkendali (Pecorino, 2005; Kumar, et al.,
2005; Adina, 2009).
b. Sel kanker tidak sensitif terhadap sinyal antiproliferatif
Sinyal antiproliferatif merupakan sinyal antipertumbuhan yang
dibutuhkan oleh sel untuk mengontrol dan menjaga keteraturan sel serta
homeostasis jaringan. Pada kondisi normal, regulasi sinyal pertumbuhan ini
menjadi faktor penentu bagi sel untuk berproliferasi atau istirahat. Sinyal ini
akan mengatur perkembangan sel dengan memblok proliferasi melalui dua
mekanisme, yaitu (1) sel dipaksa keluar dari fase proliferasi yang aktif menuju
fase istirahat atau (2) sel diinduksi untuk melepaskan potensi proliferasi secara
permanen dengan diinduksi untuk memasuki fase post mitotic. Sel kanker
berhubungan dengan daur sel. Hal ini disebabkan oleh adanya mutasi pada
beberapa gen (protoonkogen) (Pecorino, 2005; Kumar, et al., 2005; Adina,
2009).
c. Sel kanker mampu menghindar dari mekanisme apoptosis
Apoptosis merupakan mekanisme fisiologis pengurangan sel untuk
perbaikan jaringan dan pelepasan sel yang rusak yang dapat membahayakan
tubuh (Ruddon, 2007). Resistensi kanker terhadap mekanisme apoptosis dapat
terjadi dengan melibatkan protein regulator apoptosis antara lain: p53 dan
Bcl-2. Protein ini memiliki kemampuan untuk mencegah replikasi DNA yang rusak
dan mendorong penghancuran sel yang mengandung DNA abnormal. Mutasi
gen pada protein regulator ini menyebabkan sel kehilangan kontrol proliferasi
(Kumar, et al., 2005; Adina, 2009).
d. Kemampuan angiogenesis yang dimiliki oleh sel kanker
Sel kanker memiliki kemampuan untuk memacu pertumbuhan darah
baru yang dinamakan angiogenesis. Kemampuan tersebut diinisiasi oleh sinyal
Vascular Endothelial Growth Factor (VEGF) dan Fibroblas Growth Factor
(FGF). Terdapat beberapa regulator proses angiogenesis antara lain:
angiopoietin-1, angiotropin, angogenin, epidermal growth factor, granulocyte
colony-stimulating factor, interleukin (IL-1), IL-6, IL-8, TNF-α, kolagen dan
cathepsin. Faktor-faktor angiogenesis dapat mengaktifkan angiogenic switch,
sehingga pertumbuhan pembuluh darah baru menjadi tidak terkendali (Kumar,
et al., 2005; Adina, 2009).
Selama perkembangannya, kebanyakan kanker pada manusia akan
membentuk massa tumor primer yang mampu membebaskan diri dari jaringan
awalnya, memasuki aliran darah atau pembuluh limfa, dan membentuk tumor
sekunder (metastasis) di bagian tubuh yang lain. Hal ini dapat terjadi akibat
mutasi yang memungkinkan peningkatan aktivitas enzim-enzim yang terlibat
dalam invasi sel kanker dan berkurangnya adhesi antar sel oleh molekul addisi
sel (Pecorino, 2005; Adina, 2009).
f. Sel kanker memiliki potensi tak terbatas untuk melakukan replikasi.
Adanya kemampuan untuk memenuhi kebutuhan sinyal pertumbuhan
dan kemampuan untuk menghindar dari mekanisme apoptosis, sel kanker
memiliki kemampuan tak terbatas untuk bereplikasi. Kemampuan replikasi tak
terbatas ini berkaitan dengan enzim telomerase yang menjaga integritas
telomer pada kromosom, sehingga sel tetap memiliki kemampuan untuk
membelah diri. Pada kondisi normal, telomer akan mengalami degradasi
(pemotongan) pada saat sel mengalami replikasi. Ketidakmampuan sel untuk
meregulasi degradasi telomer inilah yang menyebabkan sel kanker memiliki
kemampuan tidak terbatas untuk bereplikasi (Kumar, et al., 2005; Adina,
2009).
2.2.1 Karsinogenesis
Karsinogenesis merupakan suatu proses terjadinya kanker melalui
mekanisme multitahap dengan adanya perubahan neoplastik pada jaringan
normal yang disebabkan oleh akumulasi multimutasi genetik dan menyebabkan
transformasi progresif sel normal menjadi sel malignan (ganas) (Tsao, et al.,
mengakibatkan perubahan dari normal menjadi hiperplastik, displastik, dan
pada akhirnya menjadi suatu keganasan atau malignansi (memiliki kemampuan
untuk menginvasi jaringan di sekitarnya). Perubahan genetik ini termasuk
perubahan seluler mendasar pada sel kanker yang dipengaruhi oleh beberapa
gen seperti; tumor suppresor genes (pRb, p53, PTEN, E-cadherin) dan
proto-oncogenes (ras, c-myc, Bcl-2). Karsinogenesis dapat dibagi menjadi 4 tahap
utama, yaitu tahap inisiasi, promosi, progresi, dan metastasis (Tsao, et al.,
2004; Adina, 2009).
Secara singkat, pembentukan dan pertumbuhan sel kanker dapat
dijelaskan melalui tahapan-tahapan berikut ini:
a. Fase inisiasi, yaitu ketika sel normal mulai mengalami mutasi oleh
karsinogen.
b. Fase induksi, yaitu ketika sel normal yang sedang bermutasi mulai
berubah menjadi sel kanker. Fase inisiasi dan induksi tidak bisa diketahui dan
sangat sulit untuk dideteksi. Fase-fase ini berlangsung hingga puluhan tahun.
c. Fase in situ, yaitu ketika pertumbuhan kanker terbatas pada jaringan
tempat asalnya tumbuh. Fase ini lamanya sangat bervariasi. Mungkin saja
penderita penyakit kanker berada dalam fase ini selamanya, tetapi umumnya
berlangsung sampai 5 tahun.
d. Fase invasif, yaitu sel kanker telah menembus membran basal dan
masuk ke jaringan atau organ sekitar yang berdekatan. Fase ini lebih cepat dari
fase lain dan berlangsung kurang dari 5 tahun.
e. Fase metastasis, yaitu penyebaran kanker ke kelenjar getah bening
hati). Penyebaran ini dapat melalui aliran darah, aliran getah bening, atau
langsung dari tumor (Diandana, 2009; Harianto, 2009).
Pada tahap promosi, sel-sel akan memperoleh beberapa keuntungan
selektif untuk tumbuh sehingga pertumbuhannya menjadi cepat dan berubah
menjadi tumor jinak. Tahap promosi tidak melibatkan perubahan struktural dari
genom secara langsung, tetapi biasanya terjadi perubahan ekspresi gen yang
terinisiasi (Tsao, et al., 2004).
Adanya mutasi pada satu sel tunggal normal sebagai akibat terpapar oleh
karsinogen (tahap inisiasi), akan menyebabkan perkembangan sel menjadi
hiperplasi (tahap promosi), diplasi (tahap progresi) dan pada akhirnya memiliki
kemampuan invasi ke jaringan sekitarnya (metastasis) (Tsao, et al., 2004;
Adina, 2009).
Pada tahap progresi, kemampuan pembelahan yang tinggi menuntun
terbentuknya koloni sel yang lebih besar melalui perubahan genetik lebih lanjut
dan munculnya keistimewaan-keistimewaan lain seperti peningkatan mobilitas
dam angiogenesis (Kumar, et al., 2005). Pada tahap ini sel-sel tumor dikatakan
sebagai sel malignan. Pada fase ini juga akan terjadi karsinoma dan metastasis
melalui aktivasi onkogen dan malfungsi dari enzim topoisomerase (Pecorino,
2005; Adina, 2009).
Tahap metastasis merupakan tahap akhir dalam karsinogenesis. Pada
tahap ini, sel kanker melakukan invasi ke jaringan-jaringan lain di dalam tubuh
melalui pembuluh darah, pembuluh limpa, atau rongga tubuh. Sel malignan
yang bermetastasis ini masuk melalui basement membran menuju saluran
sebagai inangnya. Selanjutnya sel kanker akan masuk ke jaringan lainnya
membentuk tumor sekunder dengan didukung kemampuan neoangiogenesis
yang dimilikinya (Kumar, et al., 2005).
Tahap metastasis dapat berlangsung karena melemahnya ikatan antarsel
yang disebabkan oleh terdegradasinya CAMs (Cell-cell Adhesion Molecules)
dan E-cadherin sebagai molekul yang menjaga pertautan antarsel.
Molekul-molekul tersebut diketahui sudah sangat sedikit bahkan tidak ditemukan lagi
pada sel kanker, sehingga proses metastasis dapat terus berlangsung. Selain itu,
kemampuan angiogenesis yang telah dimiliki sel kanker mampu menjaga agar
sel tetap hidup selama proses metastasis berlangsung (Kumar, et al., 2005).
2.2.2 Siklus sel
Siklus sel merupakan proses perkembangbiakan sel yang
memperantarai pertumbuhan dan perkembangan makhluk hidup. Setiap sel
baik normal maupun kanker mengalami siklus sel. Siklus sel memiliki dua fase
utama, yakni fase S (sintesis) dan fase M (mitosis). Fase S merupakan fase
terjadinya replikasi DNA kromosom dalam sel, sedangkan pada fase M terjadi
pemisahan 2 set DNA kromosom tersebut menjadi 2 sel (Nurse, 2000; Adina,
2009).
Selain itu terdapat fase yang membatasi kedua fase tersebut yang
dinamakan Gap. G-1 (Gap-1) terdapat sebelum fase S dan setelah fase S
dinamakan G-2 (Gap-2). Pada fase G-1, sel melakukan persiapan untuk sintesis
DNA. Fase ini merupakan fase awal cell cycle progression yang diatur oleh
faktor ekstraselular seperti mitogen dan molekul adhesi. Penanda fase ini
Pada fase G-2, sel melakukan sintesis lebih lanjut yang memadai untuk proses
pembelahan, sehingga sel siap melakukan pembelahan pada fase M (Ruddon,
2007).
Siklus sel dikontrol oleh beberapa protein yang bertindak sebagai
regulator positif dan negatif. Kelompok cyclin khususnya cyclin D, E, A, dan B
merupakan protein yang levelnya fluktuatif selama proses siklus sel. Cyclin
bersama dengan kelompok cyclin dependent kinase (CDK), khususnya CDK 4,
6, dan 2, bertindak sebagai regulator positif yang memacu terjadinya siklus sel.
Pada mammalia ekspresi kinase (CDK4, CDK2 dan CDC2/CDK1) terjadi
bersamaan dengan ekspresi cyclin (D, E, A dan B) secara berurutan seiring
dengan jalannya siklus sel (G1-S-G2-M) (Nurse, 2000). Aktivasi CDK
dihambat oleh regulator negatif siklus sel, yakni CDK inhibitor (CKI), yang
terdiri dari Cip/Kip protein (meliputi p21, p27, p57) dan keluarga INK4
(meliputi p16, p18, p19). Selain itu, tumor suppresion protein yaitu p53 dan
pRb juga bertindak sebagai protein regulator negatif (Adina, 2009).
Aktivasi CDK memerlukan ekspresi cyclin (Cyc). Kompleks
cyclin-CDK dengan protein CKI dan adanya fosforilasi oleh Weel (tyrosin15)/Myt1
(threonin14) dapat menyebabkan inaktivasi CDK. Aktivasi kompleks
Cyc-CDK diawali dengan proteolisis CKI oleh ubiquitin, kemudian fosforilasi Cyc-CDK
oleh CDK-activating kinase (CAK) pada threonin1611 dan penghilangan fosfat
(defosforilasi) oleh Cdc25 fosfatase pada target fosforilasi Weel
(tyrosin15)/Myt1 (CDK bekerja pada awal G-1 untuk mengaktifkan E2F
-dependent transcriptiongene yang diperlukan untuk fase S (di akhir G-1 untuk
Checkpoint pada G-2 terjadi ketika ada kerusakan DNA yang akan
mengaktivasi beberapa kinase termasuk ataxia telangictasia mutated (ATM)
kinase. Hal tersebut menginisiasi dua kaskade untuk menginaktivasi
Cdc2-CycB baik dengan jalan memutuskan kompleks Cdc2-Cdc2-CycB maupun
mengeluarkan kompleks Cdc2-CycB dari nukleus atau aktivasi p21 (Ruddon,
2007).
Checkpoint ini akan menghambat progresi siklus sel ke fase mitosis,
sedangkan checkpoint pada fase M terjadi jika benang sprindle tidak terbentuk
atau jika semua kromosom tidak dalam posisi yang benar dan tidak menempel
dengan sempurna pada spindle. Kontrol checkpoint sangat penting untuk
menjaga stabilitas genomik. Kesalahan pada checkpoint akan meloloskan sel
untuk berkembang biak meskipun terdapat kerusakan DNA atau replikasi yang
tidak lengkap ataupun kromosom tidak terpisah sempurna sehingga akan
menghasilkan kerusakan genetik. Hal ini kritis bagi timbulnya kanker, proses
regulasi siklus sel mampu berperan dalam pencegahan kanker (Ruddon, 2007).
2.2.3 Benzo(α)piren
Benzo(α)piren, C20H12, adalah hidrokarbon aromatik polisiklik lima
cincin yang memiliki sifat mutagenik dan sangat karsinogenik. Benzo(α)piren
merupakan produk dari proses pembakaran yang tidak sempurna pada suhu
300-600°C (Desissenko, et al., 1996).
Beberapa penelitian menunjukkan bahwa benzo(α)piren menjadi
penyebab terjadinya toksisitas saraf akut melalui proses stres oksidatif dan
terjadinya diferensiasi pembelahan sel saraf. Komponen asap tembakau yaitu
benzo(α)piren secara molekuler menjadi penyebab munculnya kanker
paru-paru melalui kerusakan genetik (DNA) sel paru-paru-paru-paru (Saunders, et al., 2006;
Slotkin dan Seidler, 2009; Desissenko, et al., 1996).
Benzo(α)piren merupakan prokarsinogen, yang berarti mekanisme
karsinogenesis dari benzo(α)piren tergantung dari metabolisme
enzimatik benzo(α)piren menjadi senyawa mutagen, yaitu benzo(α)piren diol
eposida. Senyawal ini akan berinteraksi dengan DNA dengan berikatan secara
kovalen pada basa guanin di posisi atom N2. Hal ini akan mengakibatkan
terjadinya mutasi pada struktur ganda helik DNA. Enzim CYP450 1A1, dan
CYP 450 1B1 merupakan dua enzim yang bersifat protektif terhadap toksisitas
dari benzo(α)piren. Toksisitas benzo(α)piren diperoleh akibat dari bioaktivasi
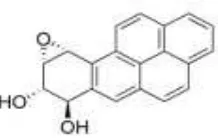
benzo(α)piren menjadi benzo(α)piren-7,8-dihidrodiol-9,10-epoksida. Senyawa
karsinogenik benzo(α)piren-7,8-dihidrodiol-9,10-epoksida akan berikatan
dengan DNA, maka DNA sel mengalami mutasi, atau memasuki tahap inisiasi
(Saunders, et al., 2006; Slotkin dan Seidler, 2009; Desissenko, et al., 1996).
Gen yang bertanggungjawab terhadap pertumbuhan kanker ada tiga
yaitu: gen reparasi DNA, gen penekan tumor (tumor suppressor gen) dan
protoonkogen. Kegagalan gen reparasi DNA dalam memperbaiki kerusakan
DNA dan mutasi pada gen penekan tumor serta onkogen, atau karena mutasi
tercapai, merupakan tahap inisiasi dalam pembentukan sel kanker. Mutasi pada
gen penekan tumor berakibat aktifasi protoonkogen menjadi onkogen yang
menyebabkan hilangnya kontrol terhadap pertumbuhan sel. Onkogen
mengkode protein-protein yang berperan dalam berbagai fungsi fisiologis sel,
diantaranya adalah protein permukaan membran, protein sitoplasma yang
terlibat dalam transduksi sinyal, dan protein inti pengikat DNA yang dapat
mengubah ekspresi genetik dari berbagai gen. Gen penekan tumor mengkode
berbagai protein termasuk protein yang mengatur siklus sel, protein adesi yang
mengurus komunikasi sel dan protein sitoplasma yang mengatur transduksi
sinyal (Pfeifer, et al., 2002).
Benzo(α)piren diol epoksida akan mentransversi G (guanine) ke T
(timidin) sehingga terjadi inaktivasi kemampuan supresor tumor dan akhirnya
mendorong pembelahan sel menjadi kanker (Pfeifer, et al., 2002).
2.2.4 Kanker payudara
Kanker payudara merupakan kanker yang menyerang jaringan epitelial
payudara, yaitu membran mukosa dan kelenjar. Kanker payudara merupakan
kanker yang paling umum diderita oleh wanita, disamping kanker serviks.
a. Kerusakan pada DNA yang menyebabkan mutasi genetik. Kerusakan
ini dapat disebabkan oleh paparan agen kimiawi (karsinogen) dan radiasi yang
berlebihan.
b. Kegagalan immune surveillance dalam pencegahan proses malignan
pada fase awal.
c. Malfungsi DNA repairs seperti: BRCA1, BRCA2, dan p53.
Kanker payudara terjadi ketika sel-sel pada payudara tumbuh tidak
terkendali dan dapat menginvasi jaringan tubuh yang lain baik yang dekat
dengan organ tersebut maupun bermetastasis ke jaringan tubuhnya yang
letaknya berjauhan. Semua tipe jaringan pada payudara dapat berkembang
menjadi kanker, namun pada umumnya kanker muncul baik dari saluran
(ducts) maupun kelenjar (glands). Perkembangannya memerlukan waktu
berbulan-bulan ataupun bertahun-tahun sampai tumor tersebut cukup besar
untuk dirasakan pada payudara. Deteksi dapat dilakukan dengan mammograms
yang kadang-kadang dapat mendeteksi tumor sejak dini (Elwood, 1993;
Dolinsky, 2002; Adina, 2009).
Faktor resiko kanker payudara dapat dibedakan menjadi faktor yang
dapat diubah (reversible) dan faktor yang tidak dapat diubah (irreversible).
Faktor yang tidak dapat diubah termasuk jenis kelamin, bertambahnya umur,
ada-tidaknya riwayat keluarga menderita kanker, pernah-tidaknya menderita
kanker payudara, pernah-tidaknya mendapat radiasi pada bagian dada, suku
bangsa Kaukasian, orang yang mengalami menstruasi pertama pada usia sangat
muda (sebelum 12 tahun), yang mengalami menopause terlambat (setelah 50
mengalami mutasi genetik. Dari berbagai macam faktor tersebut, 3%-10%
penyebab kanker payudara diduga berkaitan dengan perubahan baik gen
BRCA1 maupun gen BRCA2 (Dolinsky, 2002; Adina, 2009).
Beberapa faktor yang menaikkan resiko menderita kanker payudara
yang dapat diubah, yakni mendapatkan terapi pengganti hormon (penggunaan
estrogen dan progesteron dalam jangka waktu lama untuk mengatasi gejala
menopause), menggunakan pil kontrasepsi (pil KB), tidak menyusui,
mengkonsumsi minuman beralkohol 2-5 gelas per hari, menjadi gemuk
terutama setelah menopause, dan tidak berolahrga (Dolinsky, 2002; Adina,
2009). Perlu diingat bahwa faktor-faktor resiko tersebut hanyalah berdasarkan
pada kemungkinan. Seseorang tetap dapat terkena kanker payudara meskipun
ia tidak mempunyai satupun faktor resiko tersebut. Menghindari faktor resiko
tersebut dan deteksi awal adalah cara terbaik untuk mengurangi kematian
berkaitan dengan kanker ini (Dolinsky, 2002; Adina, 2009).
Peningkatan insidensi kanker payudara disebabkan oleh kegagalan
terapi terhadap kanker itu sendiri. Kegagalan ini diakibatkan oleh adanya
multidrug resistance (MDR) dan terjadi hingga 71% dibandingkan dengan
faktor penyebab lainnya (Mechetner, et al., 1998). Multidrug resistance atau
resistensi obat ini disebabkan oleh adanya breast cancer resistance protein
(BRCP) yang salah satunya adalah P-glycoprotein (Pgp) (Imai, et al., 2005).
Aktivasi Pgp dan peningkatan ekspresinya dapat menurunan efikasi dari
beberapa agen kemoterapi seperti taxol dan doxorubicin. Penekanan aktivitas
Pgp dan ekspresinya mampu meningkatkan efektivitas agen kemoterapi
Selain itu paparan estrogen endogen yang berlebihan juga dapat
berkontribusi sebagai penyebab kanker payudara. Sekitar 50% kasus kanker
payudara merupakan kanker yang bergantung pada estrogen dan sekitar 30%
kasus merupakan kanker yang positif mengekspresikan HER-2 berlebihan
(Gibbs, 2000; Adina, 2009).
2.2.5 Fitoestrogen
Isoflavon, kumestan, lignan dan metabolitnya, flavonoid, dan stilbenoids
semua adalah golongan senyawa yang termasuk fitoestrogen karena mereka
dapat berinteraksi dengan reseptor estrogen, mengubah ekspresi gen,dan
sebaliknya mempengaruhi hormon. Isoflavon dan kumestan sangat tinggi
dalam kacang-kacangan, seperti kedelai, kacang polong dan kacang hijau, dan
tanaman medis umum antara lain Trifolium, Medicago, serta Glycyrrhiza.
Flavonoid dengan aktivitas estrogenik berlimpah, termasuk yang paling sering
dipelajari dan dibahas adalah rutin, catechin, apigenin, kaempferol, luteolin,
chrysin dan subtipe dari flavonoid termasuk flavanon, flavon, dan flavonols,
banyak yang dilaporkan memiliki aktivitas estrogenik. Kumestan dilaporkan
memiliki efek estrogenik paling menonjol dari semua fitoestrogen. Yang paling
umum dan paling banyak dipelajari dari golongan kumestan adalah kumestrol,
ditemukan di Trifolium, Pisum, Medicago, serta Glycyrrhiza.(Ososki dan Kennely, 2003; Opolski, et al., 2005).
Banyak studi epidemiologis menunjukkan bahwa diet kaya fitoestrogen
(PE), khususnya kedelai dan produk gandum yang tidak dimurnikan,
berhubungan dengan risiko rendah beberapa jenis kanker, terutama kanker
makanan kedelai dan risiko kanker payudara masih kontroversial. Meskipun
isoflavon, seperti yang ditemukan dalam kedelai, telah terbukti dapat
menghambat kanker payudara dalam penelitian laboratorium, korelasi antara
konsumsi makanan yang mengandung isoflavon-dan risiko kanker payudara
tidak konsisten dalam beberapa penelitian. Beberapa studi telah menunjukkan
bahwa negara-negara dengan konsumsi PE tertinggi memiliki tingkat terendah
kanker payudara kanker, namun studi epidemiologi lain menunjukkan
kurangnya hubungan kausatif (Ososki dan Kennely, 2003; Opolski, et al., 2005).
Hubungan antara asupan tinggi kedelai dan risiko penurunan pola
parenkim mammographic yang berkorelasi dengan risiko kanker payudara
yang tinggi telah ditunjukkan. Selain itu, setelah mengkonsumsi 2 tahun dari
makanan kedelai, yang setara 50 mg isoflavon, oleh perempuan premenopause,
rata-rata kepadatan persentase parenkim mammographic mengalami penurunan
sebesar 2,8 dan 4,1% pada intervensi dan kontrol. Dalam studi lain hubungan
antara konsumsi isoflavon tapi bukan dari makanan kedelai, pada perempuan di
Jepang, adalah berbanding terbalik terkait dengan risiko kanker payudara
(Ososki dan Kennely, 2003; Opolski, et al., 2005).
Sebagian besar penelitian tentang fitoestrogen melibatkan kemampuan
mereka untuk menghambat perkembangan kanker hormonal, kegiatan yang
dikenal sebagai chemoprevention. Ratusan penelitian telah menunjukkan
fitoestrogen mampu mengurangi efek proliferatif steroid alami manusia dan
sintetis zat pada jaringan yang sensitif terhadap hormon. Flavonoid telah
chemoprevention yang dimilikinya mencakup mekanisme hormonal.Penelitian
telah menunjukkan bahwa tidak hanya isoflavon bertindak sebagai SERM
alami, tetapi mereka juga menginduksi terjadinya apoptosis, mempengaruhi
ekspresi gen, dan mempengaruhi berbagai sistem enzim dalam cara yang
positif. Semua mekanisme membantu mengurangi stimulasi estrogen yang
berlebihan pada jaringan sensitif terhadap hormon ini. Sistem enzim steroid
tertentu yang dapat dipengaruhi oleh fitoestrogen termasuk aromatase,
dehidrogenase, sulfotransferase, dan enzim reduktase. Sulfotransferase terlibat
dengan produksi estradiol dan fitoestrogen diketahui mampu mengurangi
sulfotransferase bila berlebihan sehingga mengurangi kelebihan hormon yang
terjadi (Ososki dan Kennely, 2003; Opolski, et al., 2005).
2.3 Metode Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair
(Depkes, 2000)
Ekstraksi dengan menggunakan pelarut dapat dilakukan dengan
beberapa cara yaitu :
Cara dingin
a. Maserasi
Maserasi adalah proses ekstraksi simplisia dengan menggunakan pelarut
dengan beberapa kali pengadukan pada temperatur ruangan (Depkes, 2000).
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar.
Proses ini terdiri dari tahapan pengembangan bahan, tahap maserasi antara,
tahap perkolasi sebenarnya (penetasan/penampungan ekstrak) (Depkes, 2000).
Cara panas
a. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya,
selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan
dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada
residu pertama sampai 3-5 kali sehingga dapat termasuk proses ekstraksi
sempurna (Depkes, 2000).
b. Soxhletasi
Soxhletasi adalah ekstraksi menggunakan pelarut yang umumnya
dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah
pelarut relatif konstan dengan adanya pendingin balik (Depkes, 2000).
c. Digesti
Digesti adalah maserasi dengan pengadukan kontinu pada temperatur
yang lebih tinggi dari temperatur ruangan, yaitu secara umum dilakukan pada
temperatur 40-50 (Depkes, 2000).
d. Infus
Infus adalah sediaan cair yang dibuat dengan menyari simplisia nabati
dengan air pada suhu 90 selama 15 menit (Depkes, 1979).
Dekok adalah sediaan cair yang dibuat dengan menyari simplisia nabati
dengan air pada waktu yang lebih lama ± 30 menit dan temperatur sampai titik