SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Oki Christina NIM : 078114035
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH PROPORSI DRUG LOAD TERHADAP DISOLUSI DISPERSI PADAT VACUUM DRIED ISOLAT EKSTRAK RIMPANG KUNYIT
(Curcuma domestica C-95)-GOM GUAR
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Oki Christina
NIM : 078114035
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
PADAT VACUUM DRIED ISOLAT EKSTRAK RIMPANG KUNYIT (Curcuma domestica C-95)-GOM GUAR
Skripsi yang diajukan oleh:
Oki Christina
NIM : 078114035
telah disetujui oleh:
Pembimbing Utama
tanggal 11 Februari 2011
Pembimbing Pendamping
Lucia Wiwid Wijayanti, M.Si.
iv
-Anyone who stops learning is old, whether at twenty or
eighty. Anyone who keeps learning stays young. The greatest
thing in life is to keep your mind young
Henry Ford -
With Jesus I can take it
With Him I know I can stand
No matter what may come my way
My life is in his hands
v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Oki Christina
Nomor Mahasiswa : 07 8114 035
Demi perkembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan
Universitas Sanata Dharma karya ilmiah saya yang berjudul:
PENGARUH PROPORSI DRUG LOAD TERHADAP DISOLUSI DISPERSI
PADAT VACUUM DRIED ISOLAT EKSTRAK RIMPANG KUNYIT (Curcuma
domestica C-95)-GOM GUAR
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan
kepada
Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan
dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data,
mendistribusikan secara terbatas, dan mempublikasikannya di internet atau media
lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya ataupun
memberi royalti kepada saya selama tetap mencantumkan nama saya sebagai
penulis.
Demikian pernyataan ini yang saya buat dengan sebenamya.
Dibuat di Yogyakarta
Pada tanggal: 17 Februari 2011
Yang menyatakan
vi
tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah
ini, maka saya bersedia menanggung segala sanksi sesuai peraturan
perundang-undangan yang berlaku.
Yogyakarta, 2 Februari 2011
Penulis
vii
PRAKATA
Puji syukur kepada Tuhan Yesus atas berkat dan penyertaan-Nya kepada
penulis, sehingga penulis dapat menyelesaikan skripsi ini dengan baik. Skripsi ini
disusun untuk memenuhi salah satu syarat untuk memperoleh gelar kesarjanaan
Program Studi Ilmu Farmasi (S.Farm.).
Dalam penyelesaian skripsi ini penulis banyak mengalami kesulitan,
namun penulis banyak mendapat bantuan dari berbagai pihak. Oleh karena itu,
pada kesempatan ini penulis ingin mengucapkan banyak terima kasih kepada:
1. Bapak Ipang Djunarko, M.Sc., Apt. selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma.
2. Ibu Dewi Setyaningsih, M.Sc., Apt. selaku Dosen Pembimbing Utama,
yang dengan sabar memberikan bimbingan, saran, pengarahan, dan telah
menanggung biaya penelitian.
3. Ibu Lucia Wiwid Wijayanti, M.Si. selaku Dosen Pembimbing
Pendamping, yang telah memberikan waktu dan bimbingan kepada
penulis.
4. Ibu Rini Dwiastuti, M.Sc., Apt. selaku Dosen Penguji atas waktu, kritik,
dan saran yang diberikan.
5. Bapak Dr. C.J. Soegihardjo, Apt. selaku Dosen Penguji atas waktu, kritik,
dan saran yang diberikan.
6. Bapak Prof. Dr. Sudibyo Martono, M.S., Apt. atas pemberian eksklusif
viii
semangat, kerjasama dan kebersamaannya selama ini.
9. I Gusti Ngurah Agung Windra Wartana Putra, Lia Natalia Setiomulyo, dan
Benny Nugroho, yang telah memberikan waktu, tenaga, dan pikiran untuk
membantu penulis dalam menyelesaikan skripsi ini.
10.Teman-teman angkatan 2007, khususnya teman-teman seperjuangan FST
07 jumawa, atas dukungan, semangat, dan kebersamaannya selama ini.
11.Keluargaku di kos Difa yang kusayangi Mba Dini Puspita, Kak Grace
Litad, Kak Ayu Widyasari, Flavia Sungkit, Ayu Ningsih, Maria Larizza,
Putri Adrenari, Melantina, Evina, Eka Permatasari, Sari, Putu Dyana,
Defilia, Leni atas kebersamaan, keceriaan, dukungan dan semangat yang
diberikan kepada penulis.
12.Semua pihak yang tidak dapat disebutkan satu-persatu yang telah
membantu dalam penyelesaian skripsi ini.
Penulis menyadari bahwa masih banyak kekurangan dalam penulisan
skripsi ini mengingat keterbatasan yang ada. Oleh karena itu penulis
mengharapkan kritik dan saran dari segenap pembaca. Semoga skripsi ini dapat
bermanfaat bagi pihak yang membutuhkan dan perkembangan ilmu kefarmasian.
ix
DAFTAR ISI
HALAMAN JUDUL ...……… i
HALAMAN PERSETUJUAN PEMBIMBING ………. ii
HALAMAN PENGESAHAN ………... iii
HALAMAN PERSEMBAHAN ………. iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ……… v
PERNYATAAN KEASLIAN KARYA ……….…………... vi
PRAKATA ………..………. vii
DAFTAR ISI ………... ix
DAFTAR TABEL ………... xiii
DAFTAR GAMBAR ……….. xiv
DAFTAR LAMPIRAN ………... xv
INTISARI ……… xvi
ABSTRACT ……….. xvii
BAB I. PENGANTAR ……….... 1
A.Latar Belakang ………... 1
1. Permasalahan ……….………... 4
2. Keaslian penelitian ………... 4
3. Manfaat penelitian ………... 4
x
C.Gom guar ... 8
D.Dispersi Padat ………... 10
1. Definisi ……….. 2. Metode pembuatan dispersi padat ……….………….. 10 11 E. Uji Disolusi ... 11
1. Disolusi ………...………... 11
2. Peralatan uji disolusi ………... 12
F. Spektrofotometri Visibel ………..…... 13
G.Validasi Metode Analisis ………..…... 14
H.Landasan Teori ………... 20
I. Hipotesis ……… 21
BAB III. METODE PENELITIAN ……… 22
A.Jenis dan Rancangan Penelitian ………... 22
B.Variabel Penelitian ………... 1. Variabel utama ……….. 2. Variabel pengacau ………. 22 22 22 C.Definisi Operasional ………... 23
D.Bahan Penelitian ………... 23
E. Alat Penelitian ………... 24
xi
1. Pembuatan dispersi padat isolat ekstrak rimpang kunyit-gom guar 24
2. Pembuatan campuran fisik ………... 25
3. Pengujian disolusi ………... 4. Validasi metode analisis ……… 25 26 G.Analisis Hasil ………... 1. Validasi metode ……….... 2. Pengaruh proporsi drug load terhadap disolusi kurkumin ... 28 28 29 BAB IV. HASIL DAN PEMBAHASAN ………...….. 30
A.Pembuatan Dispersi Padat ………..……... 30
B.Pembuatan Campuran Fisik ………... 31
C.Penetapan Panjang Gelombang Maksimum ………... 31
xiii
DAFTAR TABEL
Tabel I. Elemen-elemen data yang dibutuhkan untuk uji validasi .... 16
Tabel II. Nilai persyaratan koefisien korelasi pada tiap pengujian …. 19 Tabel III. Proporsi drug load dalam dispersi padat ………... 25
Tabel IV. Hasil pengukuran seri kurva baku ……… 33
Tabel V. Rentang % recovery yang diijinkan pada setiap konsentrasi analit pada matriks………. 34
Tabel VI. Persyaratan nilai presisi (CV) ………... 35
Tabel VII. Hasil perhitungan koefisien variasi (CV) ……... 35
Tabel VIII. Hasil pengukuran kurva baku... 36
Tabel IX. Persyaratan nilai linieritas ……… 36
Tabel X. Hasil uji statistik disolusi dispersi padat dan campuran fisik proporsi drug load 1,72% ………. 39
Tabel XI. Hasil uji statistik disolusi dispersi padat dan campuran fisik proporsi drug load 3,38% ………. 40
Tabel XII. Hasil uji statistik disolusi dispersi padat dan campuran fisik proporsi drug load 5,11% ………. 42
xiv
Gambar 1. Rimpang kunyit (Curcuma domestica Val.) ……… 6
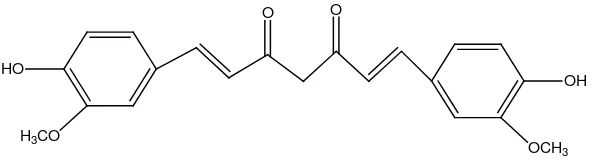
Gambar 2. Struktur kimia kurkumin ……...…… 7
Gambar 3. Degradasi kurkumin dalam larutan ...……….. 8
Gambar 4. Struktur gom guar ……...……… 9
Gambar 5. Kurva baku ………... 33
Gambar 6. Grafik dispersi padat dan campuran fisik drug load 1,72% 38 Gambar 7. Grafik dispersi padat dan campuran fisik drug load 3,38% 39 Gambar 8. Grafik dispersi padat dan campuran fisik drug load 5,11% 41 Gambar 9. Grafik dispersi padat berbagai proporsi drug load ... 42
xv
DAFTAR LAMPIRAN
Lampiran 1. Certificate of Analysis (CoA) isolat ekstrak rimpang
kunyit (Curcuma domestica Rhizome) ………...….. 50
Lampiran 2. Certificate of Analysis (CoA) baku standar kurkumin …... 51
Lampiran 3. Scan λ maksimum ... 52
Lampiran 4. Kurva baku, linieritas dan LOD ... 56
Lampiran 5. Perhitungan recovery dan CV ... 58
Lampiran 6. Penimbangan untuk pembuatan dispersi padat dan
campuran fisik …... 59
Lampiran 7. Hasil uji disolusi campuran fisik dan dispersi padat ……. 64
Lampiran 8. Grafik dispersi padat dan campuran fisik ... 73
Lampiran 9. Uji normalitas, korelasi, dan regresi linier proporsi drug
load dan persentase kurkumin terdisolusi …………... 76
Lampiran 10. Perbandingan disolusi dispersi padat dan campuran fisik 78
xvi
Penelitian ini bertujuan untuk mengetahui pengaruh proporsi drug load terhadap disolusi dispersi padat vacuum dried isolat ekstrak rimpang kunyit-gom guar. Penelitian ini dilakukan dengan pembuatan campuran fisik dan dispersi padat menggunakan pembawa gom guar pada proporsi drug load 1,72%, 3,38%, dan 5,11%. Disolusi campuran fisik dan dispersi padat dilihat melalui uji disolusi menggunakan medium cairan lambung buatan tanpa pepsin (pH 1,2), lalu diukur dengan spektrofotometer visibel λ 421,6 nm.
Kandungan utama rimpang kunyit adalah kurkuminoid, yang terdiri dari kurkumin, demetoksikurkumin, dan bisdemetoksikurkumin. Kurkumin memiliki banyak efek farmakologi, seperti antioksidan, antiinflamasi, antimikrobia, dan antikanker. Namun, kurkumin mempunyai kelarutan yang sangat rendah dalam air. Kelarutan senyawa dapat ditingkatkan dengan pembuatan dispersi padat.
Hasil uji disolusi dibuat kurva antara waktu dan persentase kurkumin terdisolusi. Disolusi kurkumin pada dispersi padat meningkat secara signifikan dibandingkan dengan campuran fisik, dilihat dari nilai p<0,05. Korelasi antara proporsi drug load dan disolusi kurkumin dianalisis dengan korelasi Spearman dan regresi. Korelasi Spearman menunjukkan adanya korelasi yang kuat (r= -0,685). Pada analisis regresi didapatkan persamaan y=-2,7204x+18,047 dengan nilai signifikansi 0,028. Peningkatan proporsi drug load berpengaruh terhadap penurunan disolusi kurkumin.
xvii
ABSTRACT
Turmeric (Curcuma domestica Val.) widely used in society. The main content of turmeric are curcuminoids, consisting of curcumin, demetoksikurkumin, and bisdemetoksikurkumin. Curcumin has many pharmacological effects, such as antioxidant, antiinflammatory, antimicrobial, and anticancer. However, curcumin has very low solubility in water. Solubility of compounds can be enhanced by making solid dispersions.
This study aims to determine the influence of the proportion of drug load on the dissolution of solid dispersion vacuum dried isolate turmeric rhizome extract-guar gum. Research was conducted by making physical mixtures and solid dispersions using guar gum on the proportion of carriers of drug load 1,72%, 3,38%, and 5,11%. Dissolution of physical mixture and solid dispersion seen through the dissolution testusing the medium of artificial gastric fluid without pepsin (pH 1,2), then measured by visible spectrophotometer λ 421,6 nm.
Dissolution test results made the curve between time and percentage of curcumin terdisolusi. Dissolution of curcumin on solid dispersion increased significantly compared with physical mixture, judging from the value of p < 0,05. The correlation between the proportion of drug load and dissolution of curcumin were analyzed with Spearman correlation and regression. Spearman correlation showed a strong correlation (r= -0,685). In the regression analysis equation y = -2,7204 x + 18,047 with a value of significance 0,028. Increasing the proportion of drug load reduction effect on the dissolution of curcumin.
1
A. Latar Belakang
Kunyit (Curcuma domestica Val.) secara empiris telah digunakan oleh masyarakat untuk mengobati berbagai penyakit, seperti antikoagulan, antiedemik,
obat sakit perut, memperbanyak ASI, stimulan, mengobati keseleo, memar dan
rematik (The Medical News, 2010). Bagian tanaman kunyit yang paling sering
digunakan adalah rimpang kunyit. Rimpang kunyit mengandung senyawa yang
berkhasiat obat, yaitu kurkuminoid, yang terdiri dari kurkumin (sebanyak 60%),
desmetoksikurkumin, dan bisdesmetoksikurkumin (Parinussa dan Timotius,
2010). Kurkumin (1,7-bis-(4-hidroksi-3-metoksifenil)-1,6-heptadiena-3,5-dion)
adalah senyawa golongan polifenol berwarna kuning yang memiliki banyak efek
farmakologi, seperti antioksidan, antiinflamasi, antimikrobia, antikanker, dan
anti-HIV (Xu, Wang, Jin, Mei, dan Xu, 2006).
Kurkumin mempunyai stabilitas yang baik pada pH asam, namun pada
pH basa kurkumin mudah mengalami dekomposisi atau degradasi (Tonnesen dan
Karlsen, 1985). Produk utama dekomposisi kurkumin adalah asam ferulat dan
4-fenil-3-butena-2-on, yang secara cepat mengalami kondensasi retroaldol menjadi
vanilin dan aseton. Selain mudah terdegradasi dalam suasana basa, kurkumin juga
mudah terdekomposisi oleh cahaya menjadi ferulat aldehid, asam ferulat,
adihidrosinaftalen, vinilguaiacol, vanilin, dan asam vanilat. Faktor dekomposisi
2
Kurkumin mempunyai kelarutan dalam air yang sangat rendah sehingga
kurkumin tidak terabsorpsi sempurna dan bioavailabilitas oral kurkumin rendah
(Kaewnopparat, Kaewnopparat, Jangwang, Maneenaum, Chucome, dan
Panichayupakaranant, 2009). Bioavailabilitas oral senyawa tergantung pada
kelarutan dan/ atau kecepatan disolusi, sehingga seringkali diperlukan
peningkatan disolusi dari senyawa yang sukar larut dalam air (Malviya,
Srivastava, Bansal, dan Sharma, 2010). Kelarutan senyawa dapat ditingkatkan
dengan beberapa cara, yaitu dengan micronization, dispersi padat, pembentukan garam, dan penyisipan gugus polar ke dalam molekul (Voigt, 1984).
Dispersi padat merupakan salah satu metode yang sering digunakan dan
berhasil digunakan untuk meningkatkan kelarutan, kecepatan disolusi, dan pada
akhirnya dapat meningkatkan bioavailabilitas senyawa dengan kelarutan rendah
(Malviya et al., 2010). Umumnya, dispersi padat mengandung pembawa hidrofilik, dimana obat terdispersi secara molekular atau sebagai partikel yang
sangat kecil. Dengan ukuran partikel yang kecil, luas permukaan kontak partikel
saat disolusi meningkat sehingga dapat meningkatkan kelarutan obat. Selain itu,
senyawa yang semula berbentuk kristal akan berubah menjadi amorf. Senyawa
berbentuk amorf mempunyai energi yang lebih tinggi dibandingkan bentuk kristal,
sehingga kelarutannya lebih besar (Srinarong, Kouwen, Visser, Hinrichs, dan
Frijlink, 2009).
Ada beberapa macam metode pembuatan dispersi padat, antara lain
electrostatic spinning method, dan super critical fluid technology (Sharma dan Joshi, 2007). Pembuatan dispersi padat pada penelitian ini menggunakan metode
vacuum drying, dimana cara ini adalah cara yang sederhana dan dapat dilakukan di Laboratorium Fakultas Farmasi Universitas Sanata Dharma.
Pada pembuatan dispersi padat, bahan pembawa dan isolat ekstrak
rimpang kunyit yang didispersikan sesuai dengan proporsi drug load. Peningkatan drug load dan/ atau saat pembawa terlarut dengan cepat, akan menyebabkan penurunan laju disolusi. Hal ini menunjukkan terjadinya kristalisasi obat yang
tidak terkontrol, yang disebabkan oleh supersaturasi pada daerah pelepasan obat
tersebut. Kristalisasi yang tidak terkontrol ini menghasilkan bentuk kristal dalam
jumlah besar, yang akan terlarut dengan lambat (Srinarong et al., 2009). Bahan pembawa yang digunakan dalam pembuatan dispersi padat adalah gom guar.
Gom guar adalah suatu hidrokoloid yang diperoleh dari endosperma biji
tanaman guar (Srichamroen, 2007). Gom guar dapat terdispersi dan mengembang
dalam air membentuk larutan dengan viskositas yang tinggi (Rowe, Sheskey, dan
Owen, 2006). Dalam pembuatan dispersi padat, gom guar dan isolat ekstrak
kunyit akan terdispersi dalam ukuran yang lebih kecil dan menjadi bentuk amorf
sehingga kelarutannya meningkat. Peningkatan kelarutan kurkumin diketahui
dengan mengukur disolusi kurkumin dalam dispersi padat, menggunakan
4
1. Permasalahan
Berdasarkan latar belakang di atas timbul permasalahan, yaitu:
Bagaimana pengaruh proporsi drug load terhadap disolusi dispersi padat isolat ekstrak rimpang kunyit-gom guar?
2. Keaslian penelitian
Sejauh pengetahuan penulis, penelitian mengenai pengaruh proporsi drug load terhadap laju disolusi kurkumin pada dispersi padat isolat ekstrak rimpang kunyit (Curcuma domestica C-95)-gom guar belum pernah dilakukan. Penelitian terkait yang pernah dilakukan adalah Solubility and Dissolution Rate Enhancement of Licofelone by Using Modified Guar Gum.
3. Manfaat penelitian
a. Manfaat teoritis
b.
. Penelitian ini diharapkan dapat menambah informasi
mengenai cara peningkatan disolusi kurkumin dengan pembuatan
dispersi padat isolat ekstrak rimpang kunyit-gom guar.
Manfaat Metodologis
c.
. Penelitian ini diharapkan dapat menambah
informasi mengenai jenis bahan pembawa dan proporsi drug load yang dapat digunakan dalam pembuatan dispersi padat.
Manfaat Praktis. Penelitian ini diharapkan dapat menambah
pengetahuan mengenai pembuatan dispersi padat isolat ekstrak
B. Tujuan Penelitian
Berdasarkan latar belakang dan perumusan masalah, tujuan dari
6 BAB II
PENELAAHAN PUSTAKA
A. Ekstrak Kunyit
Kunyit secara empiris telah digunakan masyarakat untuk mengobati
berbagai penyakit. Bagian yang sering dimanfaatkan sebagai obat adalah rimpang;
dimanfaatkan untuk antikoagulan, antiedemik, obat sakit perut, memperbanyak
ASI, stimulan, mengobati keseleo, memar dan rematik (The Medical News, 2010).
Bagian tanaman kunyit yang paling sering digunakan adalah rimpang kunyit.
Komponen utama yang terpenting dalam rimpang kunyit adalah kurkuminoid dan
minyak atsiri (Wahyuni dan Yamrewav, 2004). Kurkuminoid terdiri dari
kurkumin (sebanyak 60%), desmetoksikurkumin, dan bisdesmetoksikurkumin
(Parinussa dan Timotius, 2010).
B. Kurkumin
Kurkumin (1,7-bis-(4-hidroksi-3-metoksifenil)-1,6-heptadiena-3,5-dion)
adalah senyawa polifenol berwarna kuning yang diperoleh dari ekstrak rimpang
kunyit (Curcuma longa). Kurkumin merupakan suatu sistem cincin aromatis dengan polifenol yang dihubungkan oleh dua α, β gugus karbonil tak jenuh yang
berasal dari rantai diketon. Kurkumin memiliki banyak efek farmakologi, antara
lain sebagai antitumor, antiartritik, amylod, antioksidan, antiinflamasi,
anti-HIV, antikanker, dan antimikrobia (Najib, 2009).
Namun demikian, kendatipun aplikasi klinis sudah cukup luas dan
dikenal manjur sebagai bahan antikanker dan penyakit lainnya, kurkumin
memiliki sifat yang terbatas dari segi kelarutan. Hal ini mengakibatkan kurkumin
mempunyai bioavailabiltas sistemik yang minim (Meiyanto, 2010).
Kurkumin berwarna kuning terang, mempunyai bobot molekul 368,37 (C
= 68,47 %; H = 5,47 %; O = 26,06 %). Titik lebur kurkumin adalah 183°C.
kurkumin larut dalam alkohol dan asam asetat glasial dan tidak larut dalam air
(Wahyuni dan Yamrewav, 2004). Nilai log P kurkumin adalah 3,62 (Genome
Alberta, 2009).
Gambar 2. Struktur kimia kurkumin (Najib, 2009)
Apabila kurkumin diinkubasi dalam buffer fosfat 0,1 M dan serum, pH
8
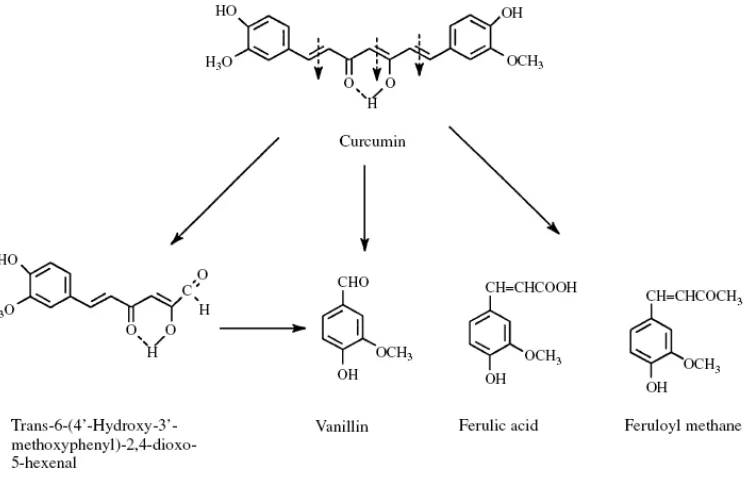
Produk degradasi kurkumin yang utama diidentifikasikan sebagai
trans-6-(4’-hidroksi-3’-metoksifenil)-2,4-diokso-5-heksenal. Produk degradasi yang lain
(vanillin, asam ferulat, dan ferulol metana) hanya terbentuk sedikit. Dekomposisi
terjadi dipengaruhi oleh pH dan terjadi lebih cepat pada kondisi pH netral (Wang,
Pan, Chang, Hsieh, dan Lin, 1997).
Gambar 3. Degradasi kurkumin dalam larutan (Wang et al., 1997)
C. Gom Guar
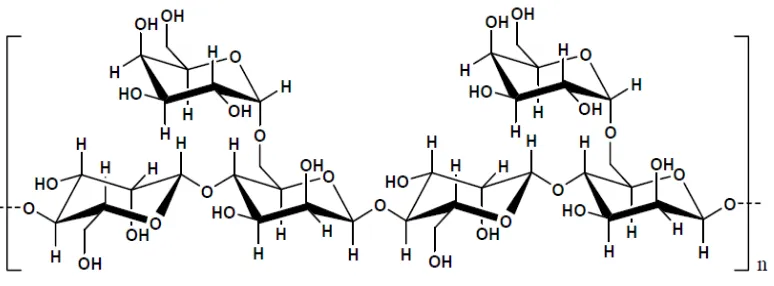
Gom guar adalah suatu hidrokoloid yang diperoleh dari endosperma biji
tanaman guar, Cyamopsis tetragonolobus, yang termasuk dalam famili Leguminosae (Srichamroen, 2007). Tanaman ini banyak tumbuh di India dan
Pakistan. Tanaman ini juga tersebar di belahan bumi bagian selatan, pada daerah
selatan, seperti Texas dan Arizona (Kawamura, 2008). Gom guar sebagian besar
terdiri dari polisakarida dengan bobot molekul tinggi (kira-kira
50.000-8.000.000), terdiri dari galaktomanan. Gom guar berwarna putih sampai putih
kekuningan, tidak berbau atau hampir tidak berbau dengan rasa yang lemah
(Kawamura, 2008).
Gambar 4. Struktur gom guar (Kawamura, 2008)
Gom guar tidak larut dalam pelarut organik. Gom guar terdispersi dan
mengembang dalam air dingin atau air panas, membentuk larutan dengan
viskositas yang tinggi. Akan tetapi, pemanasan yang lama dapat mengurangi
viskositas larutan gom guar. Larutan gom guar mempunyai kemampuan sebagai
buffer dan sangat stabil pada rentang pH 4,0-10,5. Gom guar umumnya digunakan
dalam kosmetik, produk makanan, dan formulasi sediaan farmasi. Gom guar
digunakan sebagai pengikat dan penghancur dalam sediaan padat. Pada sediaan
10
D. Dispersi Padat
1. Definisi
Dispersi padat didefinisikan sebagai dispersi satu atau lebih zat aktif
dalam pembawa hidrofilik atau matriks inert pada bentuk padat, yang dibuat
dengan metode peleburan (fusion), pelarut, atau peleburan pelarut (Kaewnopparat
et al., 2009).
Dispersi padat yang amorf dapat digunakan untuk meningkatkan laju
disolusi dari obat yang kelarutannya rendah. Pada umumnya, dispersi padat
mengandung pembawa hidrofilik, dimana obat terdispersi secara molekular atau
sebagai partikel yang sangat kecil. Mekanisme peningkatan laju disolusi obat
adalah sebagai berikut.
a. Penurunan ukuran partikel obat, sehingga luas permukaan partikel
saat terdisolusi menjadi lebih besar.
b. Peningkatan sifat pembasahan dari obat.
c. Tingkat energi bentuk amorf lebih tinggi dibandingkan bentuk
kristalin, sehingga terjadi peningkatan kelarutan obat (Srinarong et al., 2009).
Bila dispersi padat kontak dengan air, pembawa akan terlarut, dan obat
dilepaskan dengan ukuran partikel yang kecil. Oleh karena terjadi peningkatan
luas permukaan partikel obat, laju disolusi dan bioavailabilitasnya juga
mengalami peningkatan (Chaudhari, Sharma, Badagale, Dave, Kaulkarni, dan
Obat dapat terdispersi secara molekular dalam pembawa membentuk
larutan solid atau dapat terdispersi sebagai partikel. Selain itu, obat juga dapat
sebagian terlarut dan sebagian lagi terdispersi dalam pembawa. Untuk obat
dengan banyak lapisan, lebih baik jika terdispersi molekular, sedangkan bila
terdispersi sebagai partikulat, obat akan lebih mudah lepas dari matriks
pembawanya (Chaudhari et al., 2006).
Peningkatan drug load dan/ atau saat pembawa terlarut dengan cepat, akan menyebabkan penurunan laju disolusi. Hal ini menunjukkan terjadinya
kristalisasi obat yang tidak terkontrol, yang disebabkan oleh supersaturasi pada
daerah pelepasan obat tersebut. Kristalisasi yang tidak terkontrol ini menghasilkan
bentuk kristal dalam jumlah besar, yang akan terlarut dengan lambat (Srinarong et al., 2009).
2. Metode Pembuatan Dispersi Padat
Beberapa metode yang dapat dilakukan untuk membuat dispersi padat
adalah fusion method, solvent evaporation method, liofilisasi, melt agglomeration method, extruding method, spray drying, penggunaan surfaktan, electrospinning, super critical fluid technology (Sharma dan Joshi, 2007).
E. Uji Disolusi
1. Disolusi
Disolusi didefinisikan sebagai proses dimana substansi padat masuk ke
dalam pelarut menghasilkan suatu larutan. Secara sederhana, disolusi adalah
12
afinitas antara substansi padat dan pelarut. Faktor-faktor yang mempengaruhi
karakter disolusi suatu obat, antara lain sifat fisik bentuk sediaan, kemampuan
pembasahan sediaan, kemampuan penetrasi medium disolusi, proses swelling, disintegrasi dan deagregasi sediaan (Troy, 2005).
Umumnya, disolusi obat terjadi tidak hanya dari partikel halus obat yang
dihasilkan dari pemecahan sediaan, tetapi juga pada tingkat yang kecil dari
sediaan sebelum disintegrasi dan dari fragmen dan agregat setelah disintegrasi.
Bukti ilmiah menunjukkan bahwa uji disolusi sangat berarti dalam mengevaluasi
parameter kritis seperti bioavailabilitas yang memadai dan memberikan informasi
yang dibutuhkan formulator pengembangan bentuk sediaan yang optimal secara
terapetik dan efikasinya lebih besar (Banakar, 1992).
2. Peralatan uji disolusi
Metode laju disolusi diklasifikasikan menurut berbagai macam faktor.
Jika luas permukaan obat tetap, laju disolusi obat diukur dari jumlah obat yang
dilepaskan per unit area dan per unit waktu (Banakar, 1992).
Banyak peralatan yang telah digunakan untuk menentukan laju disolusi.
Prosedurnya berbeda pada prinsip dasarnya. Kondisi umum pada kebanyakan uji
in vitro adalah sebagai berikut :
a. Penggunaan cairan lambung dan cairan usus buatan pada suhu 37°C.
b. Penggunaan peralatan untuk mengaduk komponen dan produk pada
kecepatan tetap.
c. Penggunaan kasa untuk memisahkan partikel yang terdisintegrasi dari
Macam-macam metode pengujian disolusi adalah rotating basket method, rotating paddle method, reciprocating cylinder, flow-through cell, paddle over disk, dan cylinder (Troy, 2005)
F. Spektrofotometri Visibel
Spektrofotometri UV-Visibel adalah salah satu teknik analisis
fisika-kimia yang mengamati interaksi atom atau molekul dengan radiasi
elektromagnetik pada panjang gelombang 190-380 nm (UV) dan 380-780 nm
(visibel) dengan menggunakan instrument spektrofotometer (Mulja dan
Suharman, 1995).
Pada umumnya, semua molekul dapat menyerap radiasi elektromagnetik
di daerah UV dan visibel karena memiliki elektron, baik berkelompok maupun
tunggal yang dapat terkeksitasi ke tingkat energi yang lebih tinggi. Panjang
gelombang yang menunjukkan terjadinya serapan tergantung pada kekuatan
ikatan elektron pada molekul tersebut (Day dan Underwood, 1986).
Instrumentasi spektrofotometer meliputi sumber radiasi kontinyu pada
panjang gelombang tertentu, monokromator untuk memilih berkas sempit dari
14
Untuk sampel yang berupa larutan perlu diperhatikan beberapa persyaratan
pelarut yang dipakai yaitu :
1. Pelarut tidak mengandung sistem ikatan rangkap terkonjugasi pada
struktur molekulnya dan tidak berwarna
2. Tidak terjadi interaksi dengan molekul senyawa yang dianalisis
3. Kemurnian harus tinggi atau derajat untuk analisis (Mulja dan Suharman,
1995).
Pada umunya, pelarut yang sering dipakai adalah air, etanol, sikloheksan,
dan isopropanol. Hal lain yang perlu diperhatikan dalam masalah pemilihan
pelarut adalah polaritas pelarut yang dipakai, karena akan berpengaruh terhadap
pergeseran spektrum molekul yang dianalisis (Mulja dan Suharman, 1995).
Keuntungan teknik spektrofotometri yaitu banyak substansi dapat diukur
pada kisaran part per million (ppm) rendah pada pelarut yang tidak memberikan serapan. Selain itu, spektrofotometri memiliki sensitivitas yang baik serta
didukung oleh cara yang sederhana dan akurat (Schirmer, 1982).
G. ValidasiMetode Analisis
Validasi metode menurut United States Pharmacopeia (USP) dilakukan untuk menjamin bahwa metode analisis bersifat akurat, spesifik, reprodusibel, dan
tahan pada kisaran analit yang akan dianalisis. Tujuan utama validasi metode
adalah untul menghasilkan hasil analisis yang paling baik. Untuk memperoleh
dipertimbangkan. Banyaknya parameter yang harus di validasi tergantung pada
tujuan analisis (Rohman, 2009).
Suatu metode analisis untuk mengamati adanya pengotor-pengotor
(impurities) atau produk degradasi dalam suatu produk akhir obat, harus menentukan nilai batas deteksi (limit of detection, LOD) dan batas kuantifikasi (limit of quantification, LOQ); karena adanya suatu fakta bahwa senyawa-senyawa pengotor dan hasil degradasi biasanya berada dalam jumlah sekelumit
(trace elements). Meskipun demikian, untuk uji senyawa aktif farmasetik (Active Pharmaceutical Ingredients, API), maka tidak disyaratkan untuk menentukan nilai LOD dan LOQ, Karena metode analisis untuk API tidak ditujukan untuk
analisis senyawa pada konsentrasi rendah (Rohman, 2009).
Kategori yang terdapat dalam USP dan ICH adalah sebagai berikut:
1. Kategori I
Metode untuk kuantifikasi komponen mayor dalam produk ruahan API,
termasuk senyawa-senyawa pengawet dalam produk akhir obat,
diklasifikasikan dalam kategori I. Metode uji dan keseragaman kandungan
masuk dalam kategori ini.
Analisis sekelumit ini tidak diisyaratkan pada uji keseragaman kandungan
ini, karenanya penentuan LOD dan LOQ dalam uji ini tidaklah penting
(Rohman, 2009).
2. Kategori II
Metode kategori II ditujukan untuk menentukan pengotor/ pengganggu
16
produk akhir obat atau dalam proses pembersihan (cleanng process). Metode ini lebih lanjut dibagi menjadi 2 yaitu ke dalam uji kuantitatif dan uji batas
(limit test) (Rohman, 2009). 3. Kategori III
Metode-metode yang digunakan untuk menentukan karakteristik kinerja
produk akhir jatuh pada kategori III. Uji disolusi (tidak termasuk
pengukurannya) dan uji-uji pelepasan obat merupakan contoh metode yang
masuk kategori ini (Rohman, 2009).
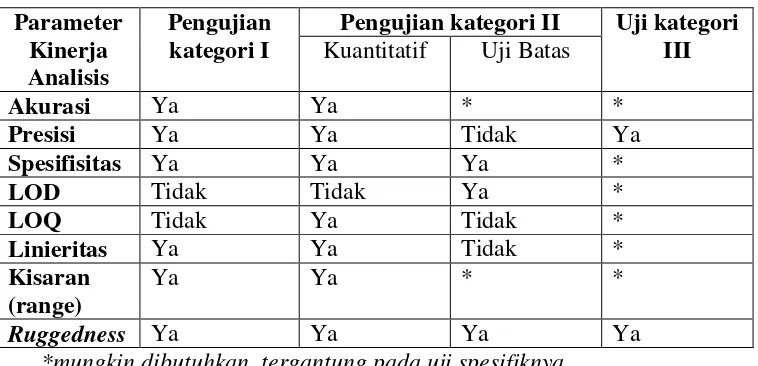
Tabel I. Elemen-elemen data yang dibutuhkan untuk uji validasi
Parameter Kinerja Analisis
Pengujian kategori I
Pengujian kategori II Uji kategori III Kuantitatif Uji Batas
Akurasi Ya Ya * *
*mungkin dibutuhkan, tergantung pada uji spesifiknya
Parameter-parameter dalam validasi metode analisis adalah sebagai
berikut.
1. Presisi
Presisi suatu metode analisis merupakan sejumlah pencarian hasil yang
diperoleh dari analisis berulangkali pada suatu sampel homogen. Presisi biasanya
memberikan presisi yang bagus, sedangkan untuk bioanalisis, CV = 15% - 20%
masih dapat diterima (Mulja dan Hanwar, 2003).
Nilai SD dihitung dengan:
SD =
Nilai CV dihitung dengan rumus:
CV = x 100%
Keterangan:
x = nilai dari masing-masing pengukuran = rata-rata (mean) dari pengukuran
N = banyaknya data
N-1 = derajat kebebasan (Rohman, 2009).
2. Akurasi
Akurasi merupakan keterdekatan antara nilai pengukuran dengan nilai
yang sebenarnya dari analit dalam sampel. Indikasi yang paling umum untuk
menyatakan akurasi yang tinggi adalah perolehan kembali (% recovery) (Mulja dan Hanwar, 2003).
3. Batas deteksi (LOD)
Batas deteksi didefinisikan sebagai konsentrasi analit terendah dalam
sampel yang masih dapat terdeteksi, meskipun tidak selalu dapat dikuantifikasi.
LOD merupakan batas uji yang secara spesifik menyatakan apakah analit di atas
atau di bawah nilai tertentu (Rohman, 2009).
18
Keterangan :
Sy/x = simpangan baku (SD)
Sl = arah garis linier dari kurva antara respon terhadap konsentrasi (slope)
(Harmita, 2004).
4. Batas kuantifikasi (LOQ)
Batas kuantifikasi didefinisikan sebagai konsentrasi analit terendah
dalam sampel yang dapat ditentukan dengan presisi dan akurasi yang dapat
diterima pada kondisi operasional metode yang digunakan. Sebagaimana LOD,
LOQ juga diekspresikan sebagai konsentrasi (dengan presisi dan akurasi juga
dilaporkan) (Rohman, 2009).
LOQ =
Keterangan :
Sy/x = simpangan baku (SD)
Sl = arah garis linier dari kurva antara respon terhadap konsentrasi (slope)
(Harmita, 2004).
5. Spesifisitas
Spesifisitas suatu metode analisis adalah kemampuan suatu metode
analisis untuk mengukur analit yang dituju secara tepat dan spesifik dengan
adanya komponen-komponen lain dalam matriks (Rohman, 2009).
6. Linieritas
Linieritas merupakan kemampuan suatu metode untuk memperoleh
hasil-hasil uji yang secara langsung proporsional dengan konsentrasi analit pada kisaran
kalibrasi yang menghubungkan antara respon (y) dengan konsentrasi (x)
(Rohman, 2009).
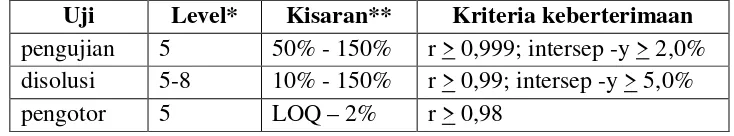
Tabel II. Nilai persyaratan koefisien korelasi pada tiap pengujian (Rohman, 2009)
Uji Level* Kisaran** Kriteria keberterimaan
pengujian 5 50% - 150% r > 0,999; intersep -y > 2,0% disolusi 5-8 10% - 150% r > 0,99; intersep -y > 5,0% pengotor 5 LOQ – 2% r > 0,98
7. Kekasaran (Ruggedness)
Kekasaran merupakan tingkat reprodusibilitas hasil yang diperoleh di
bawah kondisi yang bermacam-macam, yang diekspresikan sebagai persen standar
deviasi relatif (% RSD). Kondisi ini meliputi laboratorium, analisis, alat, reagen,
dan waktu percobaan yang berbeda. Kekasaran suatu metode mungkin tidak akan
diketahui jika suatu metode dikembangkan pertama kali, akan tetapi kekasaran
suatu metode akan kelihatan jika digunakan berulang kali. Suatu pengembangan
metode yang bagus mensyaratkan suatu evaluasi yang sistematik terhadap
faktor-faktor penting yang mempengaruhi kekasaran suatu metode (Rohman, 2009).
8. Ketahanan (Robustness)
Ketahanan merupakan kapasitas metode analisis untuk tetap tidak
terpengaruh oleh adanya variasi parameter metode yang kecil. Ketahanan
dievaluasi dengan melakukan variasi parameter-parameter metode seperti
persentase pelarut organik, pH, kekuatan ionik, suhu, dan sebagainya (Rohman,
20
H. Landasan Teori
Kunyit (Curcuma domestica Val.) telah banyak digunakan oleh masyarakat untuk mengobati berbagai penyakit, seperti antikoagulan, antiedemik,
obat sakit perut, memperbanyak ASI, stimulan, mengobati keseleo, memar dan
rematik. Bagian dari tanaman kunyit yang paling sering digunakan adalah bagian
rimpang. Rimpang kunyit mengandung senyawa yang berkhasiat obat, yaitu
kurkuminoid, yang terdiri dari kurkumin (sebanyak 60%), desmetoksikurkumin,
dan bisdesmetoksikurkumin.
Kurkumin merupakan senyawa polifenol yang berwarna kuning dan
diperoleh dari kunyit. Kurkumin mempunyai banyak efek farmakologi, seperti
antiinflamasi, antitumor, antiartritik, antikanker, antimikroba, dan anti-HIV.
Meskipun demikian, kurkumin mempunyai bioavailabilitas yang rendah. Hal ini
disebabkan oleh kelarutan kurkumin dalam air yang rendah dan terdegradasi pada
pH basa. Faktor degradasi kurkumin ini disebabkan oleh gugus metilen aktifnya.
Ada berbagai macam cara meningkatkan kelarutan suatu senyawa. Salah
satu cara yang akan dilakukan dalam penelitian ini adalah pembentukan dispersi
padat. Dispersi padat adalah dispersi satu atau lebih zat aktif dalam pembawa atau
matriks inert pada bentuk padat. Dispersi padat yang amorf dapat digunakan untuk
meningkatkan laju disolusi dari obat yang kelarutannya rendah. Pada umumnya,
dispersi padat mengandung pembawa hidrofilik, dimana obat terdispersi secara
molekular atau sebagai partikel yang sangat kecil. Bahan pembawa yang
Gom guar merupakan suatu hidrokoloid yang diperoleh dari endosperma
tanaman guar. Gom guar sebagian besar terdiri dari polisakarida dengan bobot
molekul yang tinggi, yang terdiri dari galaktomanan. Gom guar dapat terdispersi
dan mengembang dalam air dingin atau air panas, membentuk larutan dengan
viskositas yang tinggi.
Peningkatan laju disolusi obat dapat diketahui dengan melakukan
pengujian disolusi, yang kemudian akan diukur dengan spektrofotometer visibel.
I. Hipotesis
22 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan jenis penelitian eksperimental. Penelitian ini
disebut eksperimental karena peneliti menambahkan bahan pembawa untuk
meningkatkan disolusi kurkumin.
B. Variabel Penelitian
1. Variabel Utama
a. Variabel bebas
Proporsi drug load b. Variabel tergantung
Persen kurkumin terdisolusi
2. Variabel Pengacau
a. Variabel pengacau terkendali
Intensitas cahaya selama penyimpanan kurkumin
b. Variabel pengacau tak terkendali
C. Definisi Operasional
1. Ekstrak rimpang kunyit mempunyai kandungan utama kurkuminoid, yang
terdiri dari kurkumin (sebanyak 60%), desmetoksikurkumin, dan
bisdesmetoksikurkumin
2. Kurkumin adalah senyawa polifenol yang berwarna kuning, yang mempunyai
banyak efek farmakologi. Kurkumin memiliki kelarutan dan disolusi yang
rendah dalam air sehingga bioavailabilitasnya juga rendah.
3. Gom guar adalah suatu hidrokoloid yang sebagian besar terdiri dari
polisakarida dengan bobot molekul tinggi. Gom guar dapat terdispersi dan
mengembang dalam air dingin atau air panas, membentuk larutan dengan
viskositas yang tinggi.
4. Dispersi padat adalah dispersi satu atau lebih zat aktif dalam pembawa yang
inert, dalam bentuk padat. Dispersi padat dibuat dengan metode vacuum drying.
5. Uji disolusi dilakukan dengan menggunakan cairan lambung buatan tanpa
pepsin (pH 1,2). Peralatan uji disolusi yang digunakan adalah rotatingpaddle method.
6. Pengukuran kelarutan dan disolusi kurkumin pada dispersi padat dilakukan
dengan spektrofotometer visibel.
D. Bahan Penelitian
Bahan baku yang digunakan adalah isolat ekstrak rimpang kunyit (PT.
24
(pemberian eksklusif dari Prof. Dr. Sudibyo Martono, M.S., Apt.), gom guar (PT.
Brataco), etanol 70% (PT. Brataco), metanol p. a (E. Merck), dan aquadest.
E. Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah sebagai berikut:
timbangan analitik (Ohaus, Carat Series), oven (Memmert), desikator, Vacuum Rotary Evaporator (Janke & Kunkel, IKA Labortechnik), alat-alat gelas, blender (Philips), mortar, stemper, alat uji disolusi, spektrofotometri visibel (Perkin-Elmer
Lambda 20).
F. Tata Cara Penelitian
1. Pembuatan dispersi padat isolat ekstrak rimpang kunyit-gom guar
Dispersi padat isolat ekstrak rimpang kunyit-gom guar dengan drug load 1,72%; 3,38%; 5,11% dibuat dengan metode vacuum drying. Isolat ekstrak rimpang kunyit (100,0228 mg) dilarutkan dalam etanol 70% dengan suhu ±50°C
(40 ml). Ke dalam larutan gom guar ditambahkan larutan isolat ekstrak rimpang
kunyit tersebut, sesuai dengan dengan drug load 1,72%; 3,38%; 5,11%. Pelarut dihilangkan di bawah tekanan 72 mbar pada suhu 50°C dan dikeringkan dengan
oven pada suhu 50°C selama 4 hari. Hasil dispersi padat kering dihaluskan
menggunakan blender, serta diayak dengan nomor mesh 60. Hasil dispersi padat
dibungkus dengan aluminium foil dan disimpan selama 24 jam dalam desikator.
Kemudian, hasil ayakan ditimbang sebanyak 250 mg dan dimasukkan ke dalam
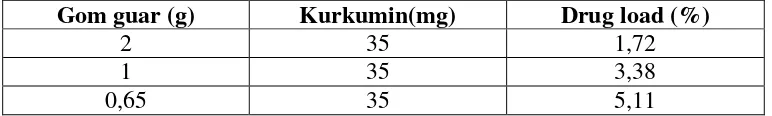
Tabel III. Proporsi Drug Load dalam Dispersi Padat
Gom guar (g) Kurkumin(mg) Drug load (%)
2 35 1,72
1 35 3,38
0,65 35 5,11
2. Pembuatan campuran fisik
Campuran fisik dibuat dengan mencampurkan isolat ekstrak rimpang
kunyit dan gom guar, yang masing-masing telah diayak sebelumnya dengan
ayakan no. mesh 60. Jumlah isolat ekstrak rimpang kunyit dan gom guar yang
dicampurkan dihitung berdasarkan jumlah dispersi padat yang diperoleh tiap
replikasinya. Pencampuran isolat ekstrak rimpang kunyit dan gom guar dilakukan
dengan mortar dan stemper hingga homogen. Kemudian, hasil campuran fisik
tersebut dibungkus dengan aluminium foil dan disimpan selama 24 jam dalam
desikator.setelah 24 jam, campuran fisik dimasukkan ke dalam kapsul dan
disimpan lagi selama 24 jam dalam desikator sebelum diuji disolusi.
3. Pengujian disolusi
a.
Medium disolusi yang digunakan adalah cairan lambung buatan LP tanpa
pepsin. Larutkan 2,0 g Natrium Klorida P dalam 7,0 ml Asam Klorida P dan air
hingga 1000 ml. Larutan mempunyai pH ±1,2. Pembuatan medium disolusi
b.
Disolusi dispersi padat diukur menggunakan peralatan disolusi. Media
disolusi terdiri dari 900 ml cairan lambung buatan tanpa pepsin pada pH 1,2.
26
Kapsul yang berisi dispersi padat dan campuran fisik dimasukkan ke dalam
medium disolusi. Setiap 5, 10, 20, 30, 45, 60, 90, 120, 150, dan 180 menit,
cuplikan sebanyak 5 ml diambil dan disaring, medium disolusi diganti dengan 5
ml medium disolusi yang baru setelah pengambilan sampel. Kurkumin dalam
cuplikan diukur dengan spektrofotometer visibel pada λ 421,6 nm. Kadar
kurkumin dihitung dan dinyatakan sebagai persentase kurkumin terdisolusi dari
rata-rata 3 replikasi pengujian disolusi.
4. Validasi metode analisis
a.
Sebanyak 10,0 mg serbuk kurkumin ditimbang lebih kurang seksama,
masukkan ke dalam labu ukur 25,0 ml. Encerkan dengan metanol p.a hingga
tanda. Simpan dalam wadah terlindung cahaya. Larutan stok kurkumin
b.
Larutan stok kurkumin diambil sebanyak 1,0 ml, masukkan ke dalam
labu ukur 10,0 ml. Encerkan dengan metanol p.a hingga tanda. Larutan
intermediet dibuat sebanyak 3 kali. Larutan intermediet
c. Penentuan panjang gelombang maksimum (λmaks
Larutan intermediet diambil sebanyak 0,4; 0,8; 1,2 ml dan masukkan ke
dalam labu ukur 10,0 ml. Encerkan dengan metanol p.a hingga tanda. Pengukuran
panjang gelombang maksimum dilakukan pada λ 300-600 nm, sebanyak 3 kali. Pengukuran juga dilakukan pada larutan intermediet II dan III. Panjang
gelombang dicari yang memberikan serapan maksimum dan memberikan profil
kurva yang mirip.
d.
Larutan intermediet diambil sebanyak 0,4 ml; 0,6 ml; 0,8 ml; 1,0 ml dan
1,2 ml, masukkan ke dalam labu ukur 10,0 ml, kemudian diencerkan dengan
metanol p.a hingga tanda. Kelima larutan tersebut diukur serapannya pada
panjang gelombang maksimum. Pengukuran dilakukan sebanyak 3 kali, untuk
kurva baku intermediet I, II, dan III. Data yang diperoleh dihitung dengan regresi
linier sehingga diperoleh persamaan kurva baku kurkumin. Pembuatan kurva baku
e.
Larutan intermediet diambil sebanyak 0,4 ml; 0,8 ml; dan 1,2 ml,
masukkan ke dalam labu ukur 10,0 ml, kemudian diencerkan dengan metanol p.a
hingga tanda. Ketiga larutan tersebut diukur serapannya pada panjang gelombang
maksimum. Pengukuran ulang dilakukan untuk larutan intermediet II dan III. Penetapan parameter akurasi (recovery)
Cara perhitungannya adalah sebagai berikut.
% recovery = x 100%
f.
Larutan intermediet diambil sebanyak 0,4 ml; 0,8 ml; dan 1,2 ml,
masukkan ke dalam labu ukur 10,0 ml, kemudian diencerkan dengan metanol p.a
hingga tanda. Kelima larutan tersebut diukur serapannya pada panjang gelombang
maksimum. Pengukuran ulang dilakukan untuk larutan intermediet II dan III.
Serapan yang diperoleh dimasukkan ke dalam persamaan kurva baku untuk
mengetahui kadar terukur, kemudian dihitung standar deviasi. Data yang
diperoleh dimasukkan ke dalam rumus berikut.
Penetapan parameter presisi (koefisien variasi)
28
Keterangan :
SD = standar deviasi
= kadar rata-rata
CV = koefisien variasi
g.
Larutan intermediet diambil sebanyak 0,4 ml; 0,6 ml; 0,8 ml; 1,0 ml dan
1,2 ml, masukkan ke dalam labu ukur 10,0 ml. Encerkan dengan metanol p.a
hingga tanda. Kelima larutan tersebut diukur serapannya pada panjang gelombang
maksimum. Pengukuran ulang dilakukan untuk larutan intermediet II dan III.
Hitung nilai linearitas serapan dan konsentrasi baku kurkumin dengan
menggunakan regresi linier.
Penetapan parameter linearitas
G. Analisis Hasil
1. Validasi metode
Validasi metode yang digunakan berdasarkan parameter berikut.
a.
Akurasi metode analisis dinyatakan sebagai recovery dan dihitung
dengan rumus berikut. Akurasi
% recovery = x 100%
Metode digunakan untuk menganalisis bahan obat dengan kadar lebih
b.
Presisi dinyatakan dengan koefisien variasi, dengan rumus: Presisi
CV = x 100%
Metode ini dikatakan baik bila nilai CV yang diperoleh < 2%. Semakin
kecil nilai CV, presisi metode yang digunakan semakin baik.
c.
Parameter linearitas dilihat dari nilai koefisien korelasi (r) hasil
pengukuran larutan seri baku kurkumin. Metode dikatakan memiliki linearitas
yang baik bila r > 0,99 atau r Linieritas
2
2. Pengaruh proporsi drug load terhadap disolusi kurkumin
≥ 0,997.
Data uji disolusi kurkumin dibuat dalam bentuk kurva hubungan
persentase pelepasan kurkumin terhadap waktu. Kemudian, korelasi keduanya
dilihat dengan menggunakan Korelasi Spearman dan regresi linier dengan taraf
30 BAB IV
HASIL DAN PEMBAHASAN
A. Pembuatan Dispersi Padat
Dispersi padat adalah dispersi satu atau lebih zat aktif dalam pembawa
atau matriks inert pada bentuk padat. Tujuan pembuatan dispersi padat adalah
untuk meningkatkan kelarutan kurkumin dalam air. Dalam penelitian, dispersi
padat dibuat menggunakan metode vacuum drying dengan gom guar sebagai pembawa, dalam berbagai proporsi drug load, yaitu 1,72%, 3,38%, dan 5,11%.
Dalam pembuatan dispersi padat, isolat ekstrak rimpang kunyit yang
digunakan berasal dari PT. Phytochemindo Reksa dengan komponen 97,20%
kurkuminoid, yang tertera pada Certificate of Analysis. Dalam kurkuminoid terdapat kandungan kurkumin sebesar 60% (Parinussa dan Timotius, 2010). Isolat
ekstrak rimpang kunyit yang dilarutkan dalam etanol 70% (suhu 50°C)
didispersikan ke dalam gom guar yang dilarutkan dalam aquadest, hingga
homogen. Etanol yang digunakan sebagai pelarut serbuk kunyit sebelumnya
dipanaskan terlebih dahulu hingga suhu 50°C karena bila tidak dipanaskan gom
guar yang terdispersi akan menggumpal. Pelarut pada campuran tersebut
dihilangkan dengan menggunakan vacuum rotary evaporator.
Hasil yang didapat dikeringkan dalam oven selama 4 hari pada suhu
50°C. Hasil yang sudah kering dihaluskan dengan blender menjadi serbuk dan
desikator selama 24 jam, kemudian dimasukkan dalam kapsul ukuran 0. Kapsul
tersebut akan dilakukan uji disolusi setelah penyimpanan 24 jam.
B. Pembuatan Campuran Fisik
Campuran fisik dibuat dengan mencampurkan isolat ekstrak rimpang
kunyit dan gom guar, yang masing-masing telah diayak sebelumnya dengan
ayakan no. mesh 60. Masing-masing serbuk diayak terlebih dahulu agar ukuran
partikelnya homogen dan sama dengan ukuran partikel dispersi padat. Jumlah
isolat ekstrak rimpang kunyit dan gom guar yang dicampurkan dihitung
berdasarkan jumlah dispersi padat tiap replikasinya. Serbuk kunyit dan gom guar
dihomogenkan dengan mortar dan stemper. Hasil campuran fisik dibungkus
dengan aluminium foil dan disimpan dalam desikator selama 24 jam. Setelah
penyimpanan 24 jam, serbuk campuran fisik dimasukkan dalam kapsul dan
disimpan selama 24 jam. Setelah penyimpanan dalam kapsul 24 jam, kapsul
tersebut diuji disolusi.
C. Penetapan Panjang Gelombang Maksimum
Panjang gelombang maksimum adalah panjang gelombang dari suatu
larutan yang mempunyai absorbansi atau serapan maksimum. Panjang gelombang
maksimum digunakan karena pada panjang gelombang maksimum, perubahan
absorbansi untuk setiap satuan konsentrasi, paling besar. Dengan demikian,
sensitivitas pengukuran lebih baik dan saat dilakukan pengukuran ulang hasilnya
32
Dalam menentukan panjang gelombang maksimum, digunakan larutan
baku kurkumin pada tiga konsentrasi yang berbeda (rendah, tengah, tinggi),
dimana masing-masing konsentrasi direplikasi sebanyak tiga kali. Panjang
gelombang maksimum diukur mulai dari 300 nm sampai 600 nm. Dari hasil
penelitian, diperoleh panjang gelombang maksimum pada 421,6 nm. Panjang
gelombang maksimum yang diperoleh tidak berbeda jauh dengan yang tertera
pada penelitian Kaewnopparat (2009), dimana pengukuran kadar kurkumin dalam
medium cairan lambung buatan (pH 1,2), menggunakan panjang gelombang 421
nm. Dengan demikian, kurkumin yang digunakan dalam pengukuran panjang
gelombang maksimum ini dapat digunakan sebagai baku (standar) dan panjang
gelombang maksimum 421,6 nm dapat digunakan untuk pengukuran larutan baku
maupun sampel yang akan dianalisis.
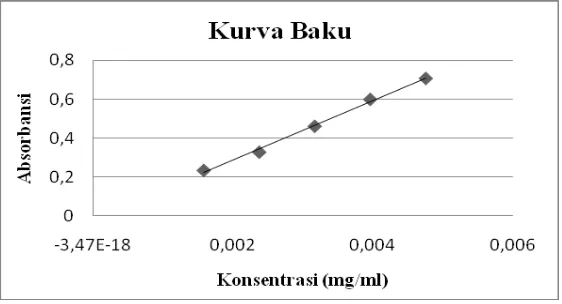
D. Pembuatan Kurva Baku
Dalam pembuatan kurva baku digunakan satu seri larutan baku
kurkumin dengan lima konsentrasi yang berbeda, yaitu 1,584∙10-3; 2,376∙10-3;
3,168∙10-3; 3,960∙10-3, dan 4,752∙10-3 mg/ml. Seri larutan baku kurkumin diukur
absorbansinya pada panjang gelombang maksimum, kemudian dibuat kurva
hubungan antara konsentrasi dan absorbansi. Dari kurva hubungan antara
konsentrasi dan absorbansi, dapat dilihat korelasi dari keduanya. Korelasi yang
baik antara konsentrasi dan absorbansi dapat dilihat dari nilai r yang mendekati
adalah r ≥ 0,99. Persamaan kurva baku yang memiliki nilai r ≥ 0,99, yang akan digunakan dalam penetapan kadar pada uji disolusi.
Tabel IV. Hasil pengukuran seri kurva baku
I II III
Dari data pada tabel di atas, maka persamaan kurva baku yang
digunakan dalam pengukuran kadar pada uji disolusi adalah y = 152,3990 x –
0,017 dengan nilai r = 0,9981.
34
E. Validasi Metode Analisis
Suatu metode analisis harus divalidasi untuk memastikan bahwa
metode analisis yang digunakan sesuai dengan tujuan yang diinginkan. Parameter
validasi yang digunakan pada suatu metode analisis berbeda-beda, disesuaikan
dengan tujuan yang diinginkan. Pada penelitian ini digunakan
parameter-parameter sebagai berikut.
1. Akurasi
Akurasi metode dilihat dari nilai % recovery. Persyaratan akurasi yang diperbolehkan pada setiap metode tergantung pada konsentrasi analit dalam
matriks sampel.
Tabel V. Rentang % recovery yang diijinkan pada setiap konsentrasi analit pada matriks (Guideline, 2004)
% Active/ impurity content Acceptable mean recovery ≥ 10
Hasil dari perhitungan recovery untuk larutan seri baku 1,584∙10-3 mg/ml adalah 96,52%; untuk seri 3,168∙ 10-3 mg/ml adalah 93,48% ; dan untuk seri
2. Presisi
Presisi suatu metode dinyatakan dengan koefisien variasi (CV).
Umumnya, presisi dikatakan baik bila nilai CV < 2%, namun menurut Guideline
(2004), persyaratan nilai CV tergantung pada jumlah analit yang diukur.
Tabel VI. Persyaratan nilai presisi (CV) (Guideline, 2004)
Component measured in sample Precision
>10.0% ≤ 2%
1.0 up to 10.0% ≤ 5%
0.1 up to 1.0% ≤ 10%
< 0.1% ≤ 20%
Tabel VII. Hasil perhitungan koefisien variasi (CV)
Recovery (%) SD CV(%)
96,52 7,19 7,44
93,48 4,85 5,19
98,41 1,39 1,42
Pada penelitian ini, kadar analit sampel >0,1% atau dalam rentang 0,1 –
1,0%, maka persyaratan CV yang digunakan adalah CV ≤ 10%. Dari hasil
perhitungan didapatkan bahwa semua nilai CV yang diperoleh memenuhi syarat
CV ≤ 10%. Dengan demikian, metode yang digunakan memenuhi persyaratan
presisi.
3. LOD
LOD merupakan batas terkecil analit yang masih dapat dideteksi pada
suatu metode. Bila kadar yang diukur berada di bawah LOD, maka kadar tersebut
tidak dapat dideteksi. Nilai LOD dihitung dengan rumus berikut:
36
Tabel VIII. Hasil pengukuran kurva baku
SD = 1,2522 x 10
LOD =
-3
=
= 2,4649 x 10-5
Dari hasil perhitunngan LOD, didapatkan LOD sebesar 2,4649 x 10 mg/ml
-5
4. Linieritas
mg/ml. Hal ini menunjukkan bahwa jumlah kurkumin dalam dispersi padat dan
campuran fisik berada di atas LOD pengukuran.
Linieritas metode dilihat dari nilai koefisien korelasi pada kurva baku.
Nilai koefisien korelasi yang baik adalah yang mendekati ±1, karena pada nilai r
±1, peningkatan konsentrasi akan diikuti dengan peningkatan absorbansinya.
Tabel IX. Persyaratan nilai linieritas (Rohman, 2009)
Uji Level* Kisaran** Kriteria keberterimaan
pengujian 5 50% - 150% r > 0,999; intersep -y > 2,0% disolusi 5-8 10% - 150% r > 0,99; intersep -y > 5,0% pengotor 5 LOQ – 2% r > 0,98
Menurut Rohman (2009), persyaratan nilai koefisien korelasi pada uji
disolusi adalah r ≥ 0,99. Persamaan kurva baku memiliki nilai r = 0,9981 sehingga Konsentrasi (mg/ml) Absorbansi
dapat dikatakan mempunyai linieritas yang baik. Dengan demikian, metode
analisis yang digunakan dalam pengujian disolusi ini memenuhi persyaratan
linieritas.
F. Uji Disolusi
Uji disolusi sangat penting dalam mengevaluasi parameter kritis seperti
bioavailabilitas yang memadai, sehingga dapat dibuat bentuk sediaan yang
efikasinya lebih besar. Dalam penelitian ini, uji disolusi dilakukan secara in vitro menggunakan medium cairan lambung buatan tanpa pepsin (pH 1,2). Uji disolusi
dilakukan untuk mengetahui disolusi kurkumin dalam dispersi padat dan
campuran fisik.
Uji disolusi dilakukan menggunakan peralatan uji disolusi tipe 2
(rotating paddle method) dengan kecepatan putar paddle 50±1 rpm, pada suhu 37±0,5°C. Pengujian dilakukan selama 3 jam dengan waktu pengambilan cuplikan
pada menit ke-5, 10, 20, 30, 45, 60, 90, 120, 150, dan 180. Cuplikan diambil
sebanyak 5 ml, yang diikuti dengan penggantian medium disolusi sebanyak 5 ml.
Cuplikan tersebut diukur absorbansinya dan dimasukkan ke dalam persamaan
kurva baku sehingga diperoleh kadar kurkumin yang terdisolusi. Dari kadar
tersebut, dihitung kadar dalam 900 ml, dan kemudian dihitung persentase
kurkumin yang terdisolusi. Kemudian, dibuat kurva hubungan antara waktu dan
38
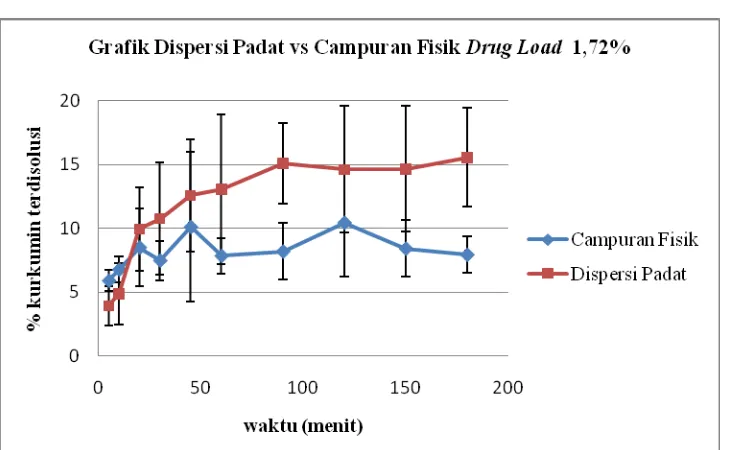
Gambar 6. Grafik Dispersi Padat dan Campuran Fisik Drug Load 1,72% Dari grafik di atas dapat diketahui bahwa dispersi padat isolat ekstrak
rimpang kunyit-gom guar dapat meningkatkan disolusi kurkumin, tetapi tidak
signifikan dibandingkan dengan campuran fisik. Hal ini dapat dilihat dari rentang
± SD yang saling tumpang tindih antara dispersi padat dan campuran fisik.
Perbandingan disolusi dispersi padat dan campuran fisik drug load 1,72% juga dilihat dengan uji statistik, dengan uji T tidak berpasangan dan uji
Mann-Whitney. Uji statistik dilakukan dengan uji T tidak berpasangan dan uji Mann-Whitney karena distribusi data pada waktu-waktu yang diuji, ada yang normal dan ada yang tidak normal. Uji normalitas dilakukan dengan
Tabel X. Hasil uji statistik disolusi dispersi padat dan campuran fisik proporsi drug load 1,72%
Waktu
(menit) Nilai p Signifikan/ tidak
5 0,121 Tidak signifikan
10 0,275 Tidak signifikan
20 0,607 Tidak signifikan
30 0,290 Tidak signifikan
45 0,591 Tidak signifikan
60 0,513 Tidak signifikan
90 0,036 Signifikan
120 0,331 Tidak signifikan
150 0,116 Tidak signifikan
180 0,033 Signifikan
Dari hasil perhitungan uji statistik diperoleh nilai signifikansi > 0,05;
hanya pada menit ke-90 dan 180 nilai signifikansi < 0,05. Oleh karena itu, dapat
dikatakan bahwa terdapat perbedaan yang tidak bermakna antara disolusi dispersi
padat dan campuran fisik.
40
Grafik di atas menunjukkan peningkatan disolusi kurkumin yang
signifikan antara dispersi padat dan campuran fisik. Hal ini dapat dilihat dari
rentang ± SD yang tidak tumpang tindih diantara keduanya. Oleh karena rentang
± SD tidak tumpang tindih, maka rentang persentase kurkumin yang terdisolusi
berbeda signifikan antara dispersi padat dan campuran fisik.
Tabel XI. Hasil uji statistik disolusi dispersi padat dan campuran fisik proporsi drug load 3,38%
Waktu
(menit) Nilai p Signifikan/ tidak
5 0,872 Tidak signifikan
10 0,232 Tidak signifikan
20 0,226 Tidak signifikan
30 0,098 Tidak signifikan
45 0,021 Signifikan
Perbandingan disolusi dispersi padat dan campuran fisik drug load 3,38% juga dilakukan dengan uji T tidak berpasangan karena data terdistribusi
normal (p < 0,05). Uji normalitas dilakukan dengan menggunakan Shapiro-Wilk,
karena data yang diuji jumlahnya kurang dari 50.
Dari hasil perhitungan uji T tidak berpasangan menunjukkan bahwa pada
menit ke-5 sampai menit ke-30 disolusi kurkumin pada dispersi padat dan
campuran fisik tidak ada perbedaan yang signifikan. Namun, pada menit ke-45
sampai menit ke-180 terdapat perbedaan yang signifikan antara dispersi padat dan
terjadi pemecahan kapsul dan kurkumin yang terdisolusi masih sedikit sehingga
tidak ada perbedaan yang signifikan antara dispersi padat dan campuran fisik.
Oleh karena itu, dapat dikatakan bahwa disolusi antara dispersi padat dan
campuran fisik pada proporsi drug load 3%, terdapat perbedaan yang signifikan.
Gambar 8. Grafik Dispersi Padat dan Campuran Fisik Drug Load 5,11% Grafik di atas menunjukkan bahwa terjadi sedikit peningkatan disolusi
kurkumin antara dispersi padat dan campuran fisik, namun peningkatan disolusi
tersebut tidak signifikan. Hal ini dapat dilihat dari rentang ± SD yang
berdekatan, bahkan tumpang tindih antara dispersi padat dan campuran fisik.
Perbandingan disolusi dispersi padat dan campuran fisik drug load 5,11% juga dilakukan dengan uji T tidak berpasangan karena data menunjukkan
distribusi normal (p > 0,05). Uji normalitas dilakukan menggunakan
42
Tabel XII. Hasil uji statistik disolusi dispersi padat dan campuran fisik proporsi drug load 5,11%
Waktu
(menit) Nilai p Signifikan/ tidak
5 0,863 Tidak signifikan
10 0,992 Tidak signifikan
20 0,380 Tidak signifikan
30 0,304 Tidak signifikan
45 0,297 Tidak signifikan
60 0,360 Tidak signifikan
90 0,233 Tidak signifikan
120 0,308 Tidak signifikan
150 0,123 Tidak signifikan
180 0,101 Tidak signifikan
Dari hasil perhitungan uji T tidak berpasangan diperoleh nilai
signifikansi > 0,05; hal ini menunjukkan adanya perbedaan yang tidak signifikan
antara disolusi dispersi padat dan campuran fisik.
Grafik tersebut menunjukkan bahwa semakin besar drug load, maka disolusi kurkumin akan semakin menurun. Peningkatan drug load dan/ atau saat pembawa terlarut dengan cepat,maka akan menyebabkan penurunan laju disolusi.
Hal ini menunjukkan terjadinya kristalisasi obat yang tidak terkontrol, yang
disebabkan oleh supersaturasi pada daerah pelepasan obat tersebut. Kristalisasi
yang tidak terkontrol ini menghasilkan bentuk kristal dalam jumlah besar, yang
akan terlarut dengan lambat (Srinarong et al., 2009).
G. Korelasi Proporsi Drug Load dan Disolusi Kurkumin
Dari hasil disolusi tersebut, kemudian dilihat hubungan korelasi antara
proporsi drug load dengan persentase kurkumin terdisolusi pada waktu 60 menit. Korelasi antara proporsi drug load dengan persentase kurkumin terdisolusi dihitung dengan menggunakan korelasi Spearman dan analisis regresi. Korelasi
dilakukan dengan korelasi Spearman karena data yang ada tidak terdistribusi
normal (p < 0,05). Uji normalitas data dilakukan menggunakan Shapiro-Wilk,
karena data yang diuji jumlahnya kurang dari 50.
Dari hasil perhitungan korelasi Spearman, diperoleh nilai signifikansi
0,042. Nilai signifikansi yang diperoleh tersebut < 0,05; maka dapat dikatakan
bahwa ada korelasi yang bermakna antara proporsi drug load dengan persentase kurkumin yang terdisolusi. Nilai koefisien korelasi yang diperoleh adalah -0,685.
44
terdisolusi. Koefisien korelasi sebesar 0,685 menunjukkan bahwa ada korelasi
yang kuat antara proporsi drug load dan persentase kurkumin terdisolusi. Tabel XIII. Kekuatan korelasi (Dahlan, 2009)
Koefisien korelasi Kekuatan korelasi
0,00-0,199 sangat lemah
0,20-0,399 lemah
0,40-0,599 sedang
0,60-0,799 kuat
0,80-1,000 sangat kuat
Pengaruh proporsi drug load terhadap persentase kurkumin terdisolusi juga dihitung dengan analisis regresi linier. Dengan melakukan analisis regresi
linier, dapat diprediksi nilai proporsi drug load dan persentase kurkumin terdisolusi, yang berada diluar nilai yang diteliti melalui persamaan matematis.
Gambar 10. Kurva Proporsi Drug Load vs %Kurkumin Terdisolusi
Dari perhitungan analisis regresi diperoleh persamaan regresi
0,026. Nilai signifikansi yang diperoleh < 0,05; hal ini menunjukkan bahwa
persamaan tersebut layak digunakan untuk meramalkan besarnya persentase
kurkumin terdisolusi bila proporsi drug load diturunkan kurang dari 1,72% dan ditingkatkan lebih dari 5,11%. Nilai Adjusted R Square yang diperoleh adalah 0,464, yang berarti 46,4% dari persentase kurkumin terdisolusi dipengaruhi oleh
46 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Dispersi padat dapat meningkatkan disolusi kurkumin secara signifikan
dibandingkan dengan campuran fisik. Peningkatan proporsi drug load akan berpengaruh terhadap penurunan disolusi dispersi padat ekstrak rimpang kunyit
(Curcuma domestica Rhizome)-gom guar.
B. Saran
1. Perlu dilakukan uji stabilitas terhadap dispersi padat pada rentang waktu
tertentu untuk melihat pengaruhnya terhadap disolusi kurkumin.
2. Pengukuran kadar pada uji disolusi dilakukan dengan metode yang lebih
47
DAFTAR PUSTAKA
Banakar, U.V., 1992, Pharmaceutical Dissolution Testing, Marcel Dekker Inc., New York, United States of America, pp. 15-17, 53.
Chaudhari, P.D., Sharma, P.K., Badagale, M.M., Dave, K.D., Kaulkarni, P.A., dan Baharte, N.S., 2006, Current Trends in Solid Dispersions Techniques,
Christian, G.D., 2004, Analytical Chemistry, 6th
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995, Farmakope Indonesia, jilid IV, Departemen Kesehatan Republik Indonesia, Jakarta, pp. 1143.
ed., John Wiley & Sons, Inc., United States of America, pp. 65-66, 483-484.
Day, R.A. dan Underwood, A.L., 1986, Quantitative Analysis, diterjemahkan oleh Pudjaatmaka, A. H., Erlangga, Jakarta, pp. 388-390.
Guideline, 2004, Guidelines for the Validation of Analytical Methods Active Constituent, Agricultural and Veterinary Chemical Producta, Australian Pesticides & Veterinary Medicines Authority, 1-9.
Genome Alberta, 2009, Curcumin,
Harmita, 2004, Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya, Majalah Ilmu Kefarmasian, Vol. I, No. 3, 117-135.
Kaewnopparat, N., Kaewnopparat, S., Jangwang, A., Maneenaum, D., Chucome, T., dan Panichayupakaranant, P., 2009, Increased Solubility, Dissolution, and Physicochemical Studies of Curcumin-Polyvinylpyrrolidone K-30 Solid Dispersions, World Academy of Science, Engineering and Technology, 55, 229-234.
Kawamura, Y., 2008, Guar Gum, Chemical and Technical Assessment, diakses tanggal 5 September 2010.
Malviya, R., Srivastava, P., Bansal, M., dan Sharma, P.K., 2010, Improvement of Dissolution Behavior of Paracetamol Using Solid Dispersion Technique, International Journal of Pharmaceutical Science and Research, 1, 95-99. Meiyanto, E., 2010, Kurkumin Sebagai Obat Kanker; Menelusuri Mekanisme