i
PENGARUH PROPORSI DRUG LOAD TERHADAP PROFIL DISOLUSI
DISPERSI PADAT KURKUMIN EKSTRAK TEMULAWAK (Curcuma
xanthorrhiza Roxb.) DALAM POLIVINIL PIROLIDON DENGAN VACCUM ROTARY EVAPORATOR
Skripsi
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Ilmu Farmasi
Diajukan Oleh: Nama : Jati Panantya NIM : 098114087
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
PERSEMBAHAN
Kupersembahkan skripsi ini untuk……
Tuhan Yesus dan Bunda Maria yang selalu menjaga dan memberiku kekuatan,
berkat dan jalan keluar dari segala persoalan,
Bapak Ibuku, dan kakak serta dosen-dosenku sebagai orangtua kedua,
Maria Rosalia Biri Koni Tiala,
yang selalu memberiku dukungan dan doa,
Sahabat-sahabat dan teman-temanku tersayang,
Alm. Filipus Joko Pamungkas, atas persahabatan terbaik dalam hidupku,
vii PRAKATA
Puji dan syukur ke hadirat Tuhan Yang Maha Esa atas berkat, kasih dan
pertolongan-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul
“Pengaruh Proporsi Drug Load Terhadap Profil Disolusi Dispersi Padat Kurkumin
Ekstrak Temulawak (Curcuma Xanthorrhiza Roxb.) Dalam Polivinil Pirolidon
Dengan Vaccum Rotary Evaporator”. Skripsi ini disusun guna memenuhi salah satu
syarat untuk mendapatkan gelar Sarjana Strata Satu Program Studi Ilmu Farmasi
(S.Farm.).
Selama masa perkuliahan hingga penelitian dan penyusunan skripsi, penulis
banyak mendapatkan bantuan dari berbagai pihak baik berupa bimbingan, doa,
dorongan, nasehat maupun sarana dan prasarana. Pada kesempatan ini penulis ingin
menyampaikan ucapan terima kasih yang sebesar-besarnya kepada:
1. Ipang Djunarko, M.Sc., Apt., selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
2. Prof. Dr. H. Achmad Fudholi, DEA., Apt. selaku Dosen Pembimbing yang
telah memberikan bimbingan, saran dan nasehat..
3. Enade Perdana Istyastono, Ph.D., Apt., selaku Dosen Pembimbing
Pendamping atas segala segala arahan, saran dan bimbingannya.
4. C.M. Ratna Rini Nastiti, M.Pharm., Apt., selaku dosen penguji atas segala arahan, masukan, kritik, dan saran yang telah diberikan kepada penulis.
5. Yohanes Dwiatmaka, M.Si., selaku dosen penguji atas segala arahan,
viii
6. Dewi Setyaningsih, M.Sc., Apt., selaku pendukung penelitian yang telah
memberikan bimbingan, saran, nasehat, serta bantuan material dan
nonmaterial.
7. Prof. Dr. Sudibyo Martono, M.S., Apt., atas pemberian eksklusif kurkumin
baku dan membimbing kami dalam metode analisis.
8. Pak Musrifin, Pak Wagiran, Pak Iswandi, Pak Agung, Pak Yuwono, Mas
Bimo Doblo, Mas Otto, Pak Parlan, Mas Kunto, Mas Sigit, Pak Pardjiman,
Pak Heru, Pak Ketul dan segenap jajaran keamanan kampus atas bantuan dan
kelancaran yang telah diberikan dalam pelaksanaan penelitian ini.
9. Felix Pradana, Saka Adhiyuda selaku teman seperjuangan dalam penelitian
atas bantuan, dukungan, dan persahabatannya dalam susah, senang, dan
pusing bersama selama ini.
10.Teman-teman Genk Galak atas semua senyum, canda, dan tawanya.
11.Semua pihak dan teman-teman yang tidak dapat penulis sebutkan satu per
satu, yang telah membantu terselesaikannya skripsi ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, oleh karena
itu penulis sangat mengharapkan kritik dan saran yang bersifat membangun dari para
pembaca demi kesempurnaan skripsi ini.
Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi
perkembangan ilmu farmasi khusunya dan kemajuan ilmu pengetahuan pada
umumnya.
Yogyakarta, 15 Juni 2013
ix DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN PERSETUJUAN PUBLIKASI ... v
PERNYATAAN KEASLIAN KARYA ... vi
PRAKATA ... vii
DAFTAR ISI ... ix
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
INTISARI ... xv
ABSTRACT ... xvi
BAB I. PENGANTAR... 1
A.Latar Belakang ... 1
B. Rumusan Masalah ... 2
C. Keaslian Penelitian ... 3
D.Manfaat Penelitian ... 3
E. Tujuan Penelitian ... 3
BAB II. PENELAAHAN PUSTAKA ... 5
A.Kurkumin... 5
x
C. Rotary Evaporator ... 7
D.PVP K30 ... 9
E. Disolusi... 11
F. Alat Uji Disolusi Rotating Paddle ... 15
G.KLT- Densitometri ... 16
H.Landasan Teori ... 17
I. Hipotesis ... 19
BAB III. METODE PENELITIAN ... 20
A.Jenis dan Rancangan Penelitian ... 20
B. Variabel Penelitian dan Definisi Operasional ... 20
C. Bahan Penelitian ... 21
D. Alat Penelitian ... 21
E. Tata Cara Penelitian ... 22
1. Pembuatan Dispersi Padat ... 22
2. Pembuatan Campuran Fisik ... 22
3. Uji Disolusi ... 23
4. Penetapan Kadar Kurkumin dengan KLT-Densitometri ... 23
F. Validasi Metode ... 24
G.Analisis Hasil ... 26
BAB IV. PEMBAHASAN ... 28
A.Pembuatan Dispersi Padat ... 28
B. Pembuatan Campuran Fisik ... 29
C. Pembuatan Fase Gerak ... 30
xi
E. Pembuatan Kurva Baku Kurkumin ... 31
F. Validasi Metode ... 32
1. Selektivitas ... 33
2. Linearitas ... 33
3. Akurasi ... 34
4. Presisi ... 34
5. Range ... 35
G.Penentuan Akurasi dan Presisi Baku Kurkumin dalam Sampel ... 35
H.Uji Disolusi ... 37
I. Pengukuran Kadar Kurkumin ... 38
J. Hubungan Proporsi Drug Load Terhadap Disolusi Kurkumin ... 41
BAB V. KESIMPULAN DAN SARAN ... 44
A.Kesimpulan ... 44
B.Saran ... 44
Daftar Pustaka ... 45
Lampiran ... 48
xii
DAFTAR TABEL
Tabel I. Formula Dispersi Padat ... 22
Tabel II. Formula Dispersi Padat ... 28
Tabel III. Kurva Baku Kurkumin ... 31
Tabel IV. Kadar Baku Kurkumin ... 34
Tabel V. Recovery Baku Kurkumin ... 34
Tabel VI. Data Coefficient of Variation (CV) Kadar kurkumin ... 34
Tabel VII. Recovery dan CV Baku Kurkumin dalam Matriks Sampel ... 36
Tabel VIII. Dispersi Padat Kurkumin ... 37
Tabel IX. Disolusi Efisiensi Formula Dispersi Padat Menit 120 ... 41
xiii
DAFTAR GAMBAR
Gambar 1. Struktur Kurkumin ... 5
Gambar 2. Rotary Evaporator... 8
Gambar 3. Grafik Persen Terdisolusi vs Waktu Formula SD F1 ... 38
Gambar 4. Grafik Persen Terdisolusi vs Waktu Formula SD F2 ... 39
Gambar 5. Grafik Persen Terdisolusi vs Waktu Formula SD F3 ... 39
xiv
DAFTAR LAMPIRAN
Lampiran 1. Data Penimbangan Baku dan Ekstrak Temulawak ... 48
Lampiran 2. Pembuatan Seri Baku Kurkumin ... 49
Lampiran 3. Data Rf dan Baku Kurkumin ... 50
Lampiran 4. Pengecekan Kadar Kurkumin dalam Ekstrak Temulawak... 51
Lampiran 5. Data Kromatogram Baku Kurkumin... 52
Lampiran 6. Data Validasi Metode ... 54
Lampiran 7. Data Kromatogram Adisi ... 58
Lampiran 8. Data Perhitungan Hasil Disolusi... 60
xv INTISARI
Kurkumin adalah salah satu kandungan utama dalam ekstrak temulawak (Curcuma xanthorriza Roxb.) yang telah diketahui aktivitasnya farmakologisnya sebagai antioksidan, antiinflamasi, antimikrobia, dan antikanker. Penggunaan kurkumin dalam dunia farmasi telah dilakukan dan ditemui permasalahan yaitu kelarutannya yang rendah di dalam air. Penelitian ini dilakukan untuk melihat pengaruh proporsi drug load pada dispersi padat kurkumin ekstrak temulawak (Curcuma xanthorriza Roxb.) dalam polimer polivinil pirolidon (PVP K30) yang dibuat dengan instrumen vaccum rotary evaporator sebagai usaha untuk meningkatkan kelarutan kurkumin dalam air.
Ekstrak temulawak yang mengandung kurkumin didispersi padat dengan pembawa polimer PVP K30 dengan vaccum rotary evaporator. Dispersi padat ekstrak dibuat pada 3 formula, yaitu formula SD F1 dengan perbandingan ekstrak temulawak : PVP K30 (1:1), SD F2 dengan perbandingan ekstrak temulawak : PVP K30 (1:2), dan SD F3 dengan perbandingan ekstrak temulawak : PVP K30 (1:4). Diperoleh dispersi padat yang kemudian dibuat dalam sediaan kapsul. Uji disolusi dilakukan pada semua variasi drug load. Sampel diambil pada waktu 5, 10, 20, 30, 45, 60, dan 120 menit. Analisis sampel dilakukan dengan metode KLT-densitometri untuk melihat kadar kurkumin dan didapatkan persentase kurkumin yang terdisolusi. Analisis data dilakukan dengan menghitung Disolusi Efisiensi (DE) masing-masing formula dan diuji statistik dengan metode Anova dan post hoc dengan uji T.
Hasil uji disolusi menunjukkan adanya perbedaan profil disolusi antar formula ditunjukkan dengan hasil disolusi efisiensi. Formula SD F3 memiliki disolusi efisiensi paling tinggi dengan 78.86% diikuti formula SD F2 69.44% dan SD F1
39.70%.
xvi ABSTRACT
Curcumin is one of the main content in the extract of curcuma (Curcuma xanthorriza Roxb.) which has pharmacological activity as an antioxidant, anti-inflammatory, antimicrobial, and anticancer. The use of curcumin in the pharmaceutical world has been known and the problem encountered is their low solubility in water. This study was conducted to obtain the effect on the proportion of drug-loaded solid dispersion of curcumin extract of curcuma (Curcuma xanthorriza
Roxb.) in the polymer polyvinyl pyrrolidone (PVP K30) that were made with a rotary vacuum evaporator instruments in an effort to increase the solubility of curcumin in water.
Curcuma extract containing curcumin was solid dispersed with PVP K30 as carrier using a rotary vacuum evaporator. Extract solid dispersions were made on 3 formula, the formula F1 with extract ratio: PVP K30 (1:1), F2 with extract ratio: PVP K30 (1:2), and F3 with extract ratio: PVP K30 (1: 4). Solid dispersion obtained was then made in the capsule. Dissolution test was performed on all drug load variations. Samples were taken at 5, 10, 20, 30, 45, 60, and 120 minutes. Sample analysis was conducted using TLC-densitometry to obtain the levels of dissolved curcumin and dissolved percentage were obtained. Data analysis was performed by calculating the Dissolution Efficiency (DE) of each formula and statistically tested by Anova and T test post hoc methods.
The dissolution test results showed a difference in dissolution profiles inter the formula in terms dissolution efficiency. Formula SD F3 had the highest value
78.86%, followed by the formula SD F2 69.44%, and SD F1 39.70%.
1
BAB I PENGANTAR
A. Latar Belakang
Kurkumin adalah sebuah polifenol hidrofobik yang dapat ditemukan
dalam ekstrak temulawak (Curcuma xanthorrhiza Roxb.). Secara tradisional,
kurkumin pada temulawak telah digunakan sebagai ramuan untuk mengobati
bengkak (inflamasi). Penelitian terkait aktivitas kurkumin telah dilakukan, seperti
Kuttan, Bhanumathy, Nirmala, dan George, (1985) menyebutkan bahwa kurkumin
memiliki sifat sebagai antioksidan dan memiliki aktivitas sebagai antikanker.
Babu dan Srinivisan (1997) mengemukakan kurkumin memiliki sifat hepato dan
nephro-protektif. Shoba, Joy, Joseph, Majeed, Rajendran, dan Srinivas (1998)
mengungkapkan keamanan kurkumin yang digunakan pada dosis tinggi.
Berdasarkan aktivitas farmakologisnya, kurkumin menjadi obyek
penelitian yang menarik dalam pengembangan obat. Selain itu kurkumin juga
merupakan bahan alam yang saat ini sedang marak untuk dikembangkan.
Keterbatasan yang secara alami melekat pada kurkumin adalah ketersediaan
hayati yang rendah karena sifat kelarutannya yang buruk dalam air. Tonnesen dan
Karlsen (1985) mengatakan bahwa kelarutan yang rendah dalam air, suasana
asam, dan pH fisiologis sebagai penyebab rendahnya ketersediaan hayati
kurkumin yang dikonsumsi secara oral. Wang, Pan, Cheng, Lin, Ho, Hsieh, dan
Lin (1997) mencoba untuk melarutkan kurkumin pada larutan pH tinggi dan
Salah satu usaha untuk meningkatkan kelarutan kurkumin adalah dengan
metode dispersi padat. Vasconcelos, Sarmento, dan Costa (2007) menyebutkan
metode dispersi padat sebagai strategi untuk meningkatkan bioavailabilitas obat
oral dengan kelarutan rendah. Kurkumin dalam sistem dispersi padat akan
mengalami peningkatan kelarutan melalui mekanisme reduksi ukuran partikel
yang akan meningkatkan luas permukaan partikel dan pembawaan oleh polimer
hidrofilik. Peningkatan kelarutan dan disolusi dari kurkumin melalui sistem
dispersi padat akan berakibat pada peningkatan bioavalabilitasnya secara oral.
Polivinil pirolidon (PVP) adalah polimer yang diketahui dapat membantu
kelarutan obat sukar larut dalam air. PVP bekerja dengan membentuk matrik yang
akan menjebak zat aktif obat dan selanjutnya dilepaskan dalam medium disolusi.
Dari penelitian terdahulu telah dilakukan penelitian untuk mengevaluasi
parameter farmakokinetika dispersi padat kurkumin dengan pembawa solutol
HS15. Dalam studi ini digunakan PVP K30 sebagai pembawa dan dilakukan
variasi drug load untuk dilakukan uji disolusi kemudian dilakukan pengukuran
dengan densitometri.
B. Rumusan Masalah
Dari uraian diatas, dapat ditarik rumusan permasalahan, adakah pengaruh
variasi proporsi drug load pada profil disolusi dispersi padat kurkumin dengan
pembawa PVP K30 yang dibuat dengan vaccum rotary evaporator dan jika ada,
C. Keaslian Penelitian
Berdasarkan penelusuran literatur, studi disolusi kurkumin ekstrak
temulawak dengan pembawa PVP belum pernah dilakukan. Penelitian mengenai
disolusi kurkumin yang pernah dilakukan adalah “Preparation and
pharmacokinetic evaluation of curcumin solid dispersion using solutol HS15 as a
carrier” (Seo, Han, Chun, dan Choi, 2012).
D. Manfaat Penelitian 1. Manfaat Teoretis
Penelitian ini diharapkan dapat menambah pengetahuan tentang disolusi
dispersi padat kurkumin sebagai usaha mengatasi sifat kurkumin yang sukar
larut di dalam air.
2. Manfaat Praktis
Penelitian ini diharapkan memberikan bukti ilmiah yang menunjukkan
dengan metode dispersi padat memperbaiki disolusi dan memberikan
fleksibilitas, variasi, dan efisiensi yang lebih baik dalam formulasi oral obat
bahan alam kurkumin.
E. Tujuan Penelitian 1. Tujuan umum
Meningkatkan disolusi kurkumin ekstrak temulawak melalui metode
2. Tujuan Khusus
Mengetahui pengaruh proporsi drug load pada dispersi padat kurkumin
ekstrak temulawak dalam PVP K30 yang dibuat dengan metode vacuum
5 BAB II
PENELAAHAN PUSTAKA
A. Kurkumin
Kurkumin adalah suatu polifenol dengan rumus kimia C21H206.
Kurkuminoid terdiri dari kurkumin (deferuloil metan), demetoksikurkumin
(feruloil-phidroksi-sinnamoiletan) dan bis-demetoksi-kurkumin (bis-(
p-hidroksisinnamoil)-metan) (Bermawie,Rahardjo, Wahyuno, dan Ma‟mun, 2007).
Gambar 1. Struktur Kurkumin (Gordon dan Tristan, 1999).
Kurkumin juga merupakan suatu pigmen alami yang larut dalam minyak,
praktis tidak larut air pada pH asam dan netral. Kurkumin memiliki titik lebur
183oC dan massa molekulnya 368,38 g/mol. Kurkumin memiliki berwarna kuning
terang atau jingga (Budavari, O‟Neill, Smith, Heckelman, dan Kinneary, 1996).
Kurkumin diketahui memiliki aktivitas antioksidan, anti-inflamasi,
antiviral, dan antifungal. Kurkumin dapat menghambat pertumbuhan bakteri
Heliobacter pylori yang dapat menyebabkan tukak lambung. Kurkumin juga dapat
berikatan dengan logam berat seperti cadmium sehingga dapat mengurangi
toksisitas dari logam berat. Dengan sifatnya yang dapat mengikat logam berat,
kurkumin ditengarai memiliki aksi protektif terhadap otak. Kurkumin berperan
sebagai inhibitor cyclooxygenase, 5-lipoxygenase dan glutathione S-transferase
B. Dispersi Padat
Dispersi padat merupakan suatu sistem dispersi yang memiliki prinsip di
mana satu atau lebih dari satu bahan aktif terdispersi dalam suatu matrik pembawa
pada fase padat. Kondisi dispersi padat merujuk pada pada keadaan obat
hidofobik terdispersi dalam matrik hidrofilik. Dispersi padat dilakukan dengan
metode pelelehan, metode pelarutan, dan metode pelarutan-pelelehan (Beringer,
2005).
1. Metode Pelelehan
Metode pelelehan adalah metode dispersi padat dengan pencampuran
secara fisika antara zat aktif obat dengan larutan pembawa yang kemudian
dipanaskan sampai meleleh. Campuran ini kemudian dipadatkan dengan cepat
dengan cara dibekukan pada penangas es disertai pengadukan kuat. Kemudian
campuran padat yang terbentuk tersebut dihancurkan, diserbuk dan diayak. Massa
padat tersebut membutuhkan penyimpanan satu hari atau lebih dalam desikator
pada suhu kamar untuk mencapai kekerasan tertentu sehingga mudah diserbuk
(Goldberg, Gibaldi, dan Kanig, 1965).
Keuntungan metode ini adalah sederhana dan ekonomis. Sebagai
tambahan dapat dicapai supersaturasi zat terlarut atau obat pada sistem dengan
mengkristalkan lelehan langsung secara cepat dari temperatur tinggi (Fudholi,
2013). Pada kondisi seperti itu, molekul zat terlarut tertahan pada matriks pelarut
dengan proses pemadatan langsung. Sehingga didapat dispersi kristalit yang lebih
Kekurangannya adalah banyak zat baik obat atau pembawa, dapat terurai atau
menguap selama proses peleburan pada suhu tinggi (Chiou dan Riegelman, 1971).
2. Metode Pelarutan
Metode pelarutan secara singkat adalah campuran fisik dari obat dan
matriks larut dalam pelarut biasa dan diikuti dengan penguapan pelarut.
Keuntungan dari metode pelarutan adalah cara dekomposisi termal dari
obat-obatan dapat dicegah karena suhu relatif rendah yang diperlukan untuk penguapan
pelarut organik (Leuner dan Dressman, 2000).
Salah satu syarat penting untuk pembuatan dispersi padat dengan metode
pelarutan adalah bahwa obat dan pembawa cukup larut dalam pelarut. Suhu yang
digunakan untuk penguapan pelarut biasanya terletak pada kisaran 23-65º C
(Leuner dan Dressman, 2000).
3. Metode Pelarutan-Pelelehan
Sistem dispersi padat dibuat dengan melarutkan dahulu obat dalam pelarut
yang sesuai dan mencampurnya dengan lelehan polietilen glikol, dapat dicapai
dibawah suhu 70º C, tanpa memisahkan pelarut (Chiou dan Riegelman, 1971).
C. Rotary Evaporator
Rotary evaporator adalah sebuah alat yang digunakan di laboratorium
kimia untuk menghilangkan pelarut secara efisien dan perlahan-lahan serta untuk
preparasi destilasi dan penemuan ekstrak. Rotary evaporator sederhana pertama
kali ditemukan oleh Lyman C. Craig yang kemudian dipasarkan secara komersil
Gambar 2.Rotary Evaporator (Anonim, 2012)
Komponen utama dari sebuah vacuum rotary evaporator adalah :
1. Motor yang memutar vial atau flask sampel yang dievaporasi.
2. Saluran uap sebagai sumbu rotasi dan jalur uap yang ditarik dari sampel.
3. Sistem vakum yang secara bertahap mengurangi tekanan pada sistem
evaporator.
4. Bak cairan panas untuk memanaskan sampel.
5. Kondensor dan koil pendingin di mana zat pendingin seperti aseton atau dry
ice ditempatkan.
6. Labu kondensator di bawah kondensor untuk menangkap pelarut yang sudah
didestilasi setelah mengalami kondensasi kembali (Laurence dan Christopher,
1989).
Rotary evaporator adalah alat dengan sistem vakum yang berfungsi
menurunkan tekanan di sekitar cairan sampel yang akan menurunkan titik didih
pada komponen pelarut yang akan dihilangkan dari sampel setelah ekstraksi
segera setelah isolasi dari produk ekstrak tersebut. Dengan rotary evaporator akan
didapatkan cara penguapan pelarut tanpa pemanasan berlebih dan terhindar dari
resiko merusak sampel yang biasanya merupakan molekul kombinasi yang
sensitif dan kompleks antara pelarut dan zat terlarutnya. Rotary evaporator
diterapkan untuk memisahkan pelarut yang telah diturunkan titik didihnya dengan
komponen yang akan berwujud padat pada suhu dan tekanan kamar (Laurence dan
Christopher, 1989).
Keuntungan penggunaan rotary evaporator antara lain adanya gaya
sentrifugal dan gaya friksional antara dinding labu atau vial yang berotasi dengan
cairan sampel akan menghasilkan pembentukan lapisan film tipis yang merupakan
pelarut yang tersebar seluas area labu atau vial (Laurence dan Christopher, 1989).
Gaya yang tercipta dari rotasi akan meminimalkan terjadinya bumping
atau tabrakan dari molekul dalam sampel. Pelarut yang masih tersisa setelah
evaporasi dapat dihilangkan dengan mengkondisikan sampel pada tekanan yang
lebih tinggi atau kondisi yang lebih vakum pada suhu yang lebih tinggi dari
sebelumnya. Jadi, secara umum dapat dikatakan rotary evaporator relatif mudah
digunakan karena tidak memerlukan metode lanjutan yang rumit (Laurence dan
Christopher, 1989).
D. PVP K30
PVP (Polyvinylpyrrolidone) adalah suatu polimer yang larut dalam air dan
pelarut polar lainnya dan terdiri dari monomer N-vinylpyrrolidone (Haaf, Sanner,
air di udara hingga 40% bobotnya. PVP memiliki sifat sebagai wetting agent yang
baik dalam larutan dan dengan mudah dapat membentuk suatu film sehingga
sangat baik digunakan untuk coating zat aktif obat. PVP terdiri dari ratusan
hingga ribuan monomer di mana atom-atomnya terikat secara kovalen (Fischer
dan Bauer, 2009).
PVP memiliki rumus kimia (C6H9NO)n dengan bobot molekul 2.500 –
25.000.000 g/mol. PVP memiliki kenampakan serbuk amorf, bersifat higroskopik,
dan berwarna putih atau kuning terang. PVP meleleh pada suhu 150 – 180oC yang merupakan glass temperaturenya (Budavari, dkk, 1996).
Di dunia kefarmasian, PVP biasa digunakan sebagai pengganti plasma
darah dan sebagai bahan-bahan tambahan dalam formulasi produk obat. Polimer
ini digunakan sebagai bahan pengikat pada tablet yang digunakan secara oral.
Penggunaaan PVP yang cukup efektif saat ini adalah pada pembentukan kompleks
povidone-iodine yang memiliki sifat desinfektan. Obat yang diproduksi dapat
berwujud larutan, salep, dan sabun cair. Kompleks ini dinilai cukup efektif dan
aman, selain itu juga merupakan bahan yang cukup murah dan mudah didapatkan
(Santhi, 2003).
PVP adalah bahan kimia yang dikategorikan aman namun diketahui
adanya kasus alergi terhadap penggunaan PVP secara subkutan dan bila terjadi
kontak dengan membran mukosa. Alergi yang terjadi adalah anaphylaxis. PVP
digunakan sebagai bahan tambahan dalam obat, penyebab alergi pertama kali
ditujukan pada iodine, namun setelah dilakukan uji klinik diketahui bahwa PVP
E. Disolusi
Disolusi didefinisikan sebagai proses dimana suatu zat padat masuk ke
dalam pelarut menghasilkan suatu larutan. Secara sederhana, disolusi adalah
proses dimana zat padat melarut. Secara prinsip disolusi dikendalikan oleh afinitas
antara zat padat dengan pelarut. Dalam penentuan kecepatan disolusi dari berbagai
bentuk sediaan padat terlibat berbagai proses dan faktor yang mempengaruhi.
Karakteristik fisik sediaan, proses pembasahan sediaan, kemampuan penetrasi
media disolusi ke dalam sediaan, proses pengembangan, proses disintegrasi, dan
degradasi sediaan, merupakan sebagian dari faktor yang mempengaruhi
kerakteristik disolusi obat dari sediaan (Beringer, 2005).
Secara sederhana kecepatan pelarutan didefinisikan sebagai jumlah zat
yang terlarut dari bentuk sediaan padat dalam medium tertentu sebagai fungsi
waktu (Fudholi, 2013). Dapat juga diartikan sebagai kecepatan larutan bahan obat
dari sediaan farmasi atau granul atau partikel-partikel sebagai hasil pecahannya
bentuk sediaan obat tersebut setelah berhubungan dengan cairan medium. Dalam
hal tablet biasanya diartikan sebagai mass transfer, yaitu kecepatan pelepasan
obat atau kecepatan larut bahan obat dari sediaan tablet kedalam medium
penerima (Beringer, 2005).
Untuk mengerti mekanisme dari disolusi digunakan salah satu model atau
gabungan dari beberapa model antara lain adalah:
1. Model Lapisan Difusi (Diffusion Layer Model)
Pada permukaan padat terdapat satu lapisan tipis cairan dengan ketebalan
permukaan padat.Reaksi pada permukaan padat–cair berlangsung cepat. Begitu model solut melewati antar muka liquid film–bulk film, pencampuran secara cepat
akan terjadi dan gradien konsentrasi akan hilang. Karena itu kecepatan disolusi
ditentukan oleh difusi gerakan Brown dari molekul dalam liquid film.
2. Model Barrier Antar Muka (Interfacial Barrier Model)
Model ini menggambarkan reaksi yang terjadi pada permukaan padat dan
dalam hal ini terjadi difusi sepanjang lapisan tipis cairan. Sebagai hasilnya, tidak
dianggap adanya kesetimbangan padatan–larutan, dan hal ini harus dijadikan pegangan dalam membahas model ini. Proses pada antar muka padat–cair sekarang menjadi pembatas kecepatan ditinjau dari proses transpor. Transpor yang
relatif cepat terjadi secara difusi melewati lapisan tipis statis (stagnant).
3. Model Dankwert (Dankwert Model)
Model ini beranggapan bahwa transpor solut menjauhi permukaan padat
terjadi melalui cara paket makroskopik pelarut mencapai antar muka–cair karena terjadi pusaran difusi secara acak. Paket pelarut terlihat pada permukaan padatan.
Selama berada pada antar muka, paket mampu mengabsorpsi solut menurut
hukum difusi biasa, dan kemudian digantikan oleh paket pelarut segar. Jika
dianggap reaksi pada permukaan padat terjadi segera, proses pembaharuan
permukaan tersebut terkait dengan kecepatan transpor solut ataudengan kata lain
disolusi (Beringer, 2005).
Metode pengujian disolusi antara lain adalah metode Khan yang dikenal
dengan konsep dissolution efficiency (DE) area di bawah kurva disolusi di antara
Dirumuskan dengan persamaan sebagi berikut :
DE = 0t∫(Y dt/ Y100.t) x 100%...(1)
(Fudholi, 2013)
Penggunaan DE sebaiknya mendekati 100% zat yang terlarut. Keuntungan
metode ini adalah :
1. Dapat menggambarkan seluruh proses percobaan yang dimaksud dengan
harga DE
2. Dapat menggambarkan hubungan antara percobaan in vitro dan in vivo
karena penggambaran dengan cara DE ini mirip dengan cara
penggambaran pecobaan in vivo (Fudholi, 2013).
Kecepatan disolusi suatu zat dapat dipengaruhi oleh beberapa faktor antara
lain adalah:
1. Suhu
Semakin tinggi suhu maka akan memperbesar kelarutan suatu zat yang bersifat
endotermik serta akan memperbesar harga koefisien kelarutan zat tersebut.
2. Viskositas
Turunnya viskositas suatu pelarut juga akan memperbesar kelarutan suatu zat.
3. pH
Nilai pH sangat mempengaruhi kelarutan zat-zat yang bersifat asam maupun basa
lemah. Zat yang bersifat basa lemah akan lebih mudah larut jika berada pada
suasana asam sedangkan asam lemah akan lebih mudah larut jika berada pada
4. Ukuran Partikel
Semakin kecil ukuran partikel, maka luas permukaan zat tersebut akan semakin
meningkat sehingga akan mempercepat kelarutan suatu zat.
5. Polimorfisme dan Sifat Permukaan Zat
Polimorfisme dan sifat permukaan zat akan sangat mempengaruhi kelarutan suatu
zat, adanya polimorfisme seperti struktur internal zat yang berlainan, akan
mempengaruhi kelarutan zat tersebut dimana kristal metastabil akan lebih mudah
larut daripada bentuk stabilnya. Dengan adanya surfaktan dan sifat permukaan zat
yang hidrofob, akan menyebabkan tegangan permukaan antar partikel menurun
sehingga zat mudah terbasahi dan lebih mudah larut (Beringer, 2005).
Selain faktor-faktor tersebut juga terdapat faktor-faktor yang
mempengaruhi laju disolusi obat secara in vitro antara lain adalah:
1. Sifat Fisika Kimia Obat
Sifat fisika kimia obat berpengaruh besar terhadap kinetika disolusi. Luas
permukaan efektif dapat diperbesar dengan memperkecil ukuran partikel. Laju
disolusi akan diperbesar karena kelarutan terjadi pada permukaan solut. Kelarutan
obat dalam air juga mempengaruhi laju disolusi. Obat berbentuk garam, pada
umumnya lebih mudah larut dari pada obat berbentuk asam maupun basa bebas.
Obat dapat membentuk suatu polimorfi yaitu terdapatnya beberapa kinetika
pelarutan yang berbeda meskipun memiliki struktur kimia yang identik. Obat
bentuk kristal secara umum lebih keras, kaku dan secara termodinamik lebih stabil
daripada bentuk amorf, kondisi ini menyebabkan obat bentuk amorf lebih mudah
2. Faktor Formulasi
Berbagai macam bahan tambahan yang digunakan pada sediaan obat dapat
mempengaruhi kinetika pelarutan obat dengan mempengaruhi tegangan muka
antara medium tempat obat melarut dengan bahan obat, ataupun bereaksi secara
langsung dengan bahan obat. Penggunaan bahan tambahan yang bersifat hidrofob
seperti magnesium stearat, dapat menaikkan tegangan antar muka obat dengan
medium disolusi. Beberapa bahan tambahan lain dapat membentuk kompleks
dengan bahan obat, misalnya kalsium karbonat dan kalsium sulfat yang
membentuk kompleks tidak larut dengan tetrasiklin. Hal ini menyebabkan jumlah
obat terdisolusi menjadi lebih sedikit dan berpengaruh pula terhadap jumlah obat
yang diabsorpsi.
3. Faktor alat dan kondisi lingkungan
Adanya perbedaan alat yang digunakan dalam uji disolusi akan
menyebabkan perbedaan kecepatan pelarutan obat. Kecepatan pengadukan akan
mempengaruhi kecepatan pelarutan obat, semakin cepat pengadukan maka
gerakan medium akan semakin cepat sehingga dapat menaikkan kecepatan
pelarutan. Selain itu temperatur, viskositas dan komposisi dari medium, serta
pengambilan sampel juga dapat mempengaruhi kecepatan pelarutan obat (Fudholi,
2013).
F. Alat Uji Disolusi Rotating Paddle
Rotating paddle adalah salah satu alat pengujian disolusi. Pada metode ini
digunakan suatu dayung yang berputar dalam suatu basket atau wadah yang
obat dalam tablet yang terdisolusi dengan mengaduk cairan dalam wadah tersebut.
Diperlukan dayung-dayung dengan dimensi atau ukuran dan bentuk yang sama
untuk mendapatkan hasil yang konsisten pada uji-uji yang dilakukan. Dayung
tidak boleh mengalami perubahan kecepatan saat berotasi mengaduk cairan dan
juga tidak boleh terlalu cepat berotasi karena dapat menyebabkan turbulensi
selama proses disolusi. Pada advanced researcher atau peneliti tingkat lanjut
disarankan melapisi dayung dan porosnya dengan polyfluorocarbon untuk
mencegah korosi dayung dan menggunakan nomor seri tertentu untuk satu kali uji
disolusi yang kemudian diganti untuk uji disolusi yang berbeda (Beringer, 2005).
G. KLT–Densitometri
KLT (Kromatografi Lapis Tipis) merupakan teknik kromatografi yang
masuk dalam kromatografi planar. Pada KLT digunakan fase diam berupa lapisan
yang seragam (uniform) pada permukaan bidang datar yang didukung oleh pelat
aluminium, pelat plastik, atau lempeng kaca. Fase gerak yang disebut juga pelarut
pengembang akan bergerak sepanjang fase diam karena pengaruh kapiler pada
proses pengembangan (Gandjar dan Rohman, 2007).
Keuntungan dari KLT :
1. Dapat digunakan untuk tujuan analisis.
2. Identifikasi pemisahan komponen dapat dilakukan dengan pereaksi warna,
fluorosensi, atau radiasi sinar ultra violet.
3. Dapat dilakukan elusi secara menaik dan menurun.
4. Ketepatan penentuan kadar akan lebih baik karena komponen yang akan
Fase diam pada KLT merupakan penjerap berukuran kecil dengan
diameter partikel antara 10-30 µm. Kinerja KLT akan semakin baik bila ukuran
rata-rata partikel fase diam semakin kecil. Fase diam yang sering digunakan
adalah silika dan serbuk selulosa dengan mekanisme sorpsi partisi dan adsorpsi
(Gandjar dan Rohman, 2007).
Fase gerak pada KLT dapat menggunakan campuran 2 pelarut organik
karena daya elusi campuran kedua pelarut ini dapat diatur sedemikian rupa
sehingga pemisahan terjadi dengan optimal. Fase gerak harus memiliki kemurnian
tinggi karena KLT adalah teknik yang sensitif. Selain itu fase gerak diharapkan
dapat memberikan daya elusi yang baik sehingga diperoleh harga Rf antara
0,2-0,8. Air atau metanol dapat ditambahkan dalam campuran fase gerak untuk
solut-solut ionik dan solut-solut-solut-solut polar (Gandjar dan Rohman, 2007).
Martono (1996) melakukan pemisahan kurkumin dari kunyit dengan fase
gerak kloroform: etanol: air (25:0,96:0,04), dengan fase diam silica gel 60 F254
dan dilakukan scanning densitometri pada λ 420 nm. KLT-Densitometri
merupakan metode yang efektif dan ekonomis dibandingkan dengan metode
KCKT dalam pemisahan dan analisis kuntitatif kurkumin (Martono, 1996).
H. Landasan Teori
Kurkumin ekstrak temulawak adalah salah satu obat bahan alam dengan
sifat bioaktifnya diketahui memiliki kelarutan yang buruk dalam air dan pelarut
polar lainnya yang menyebabkan biovailabilitas yang rendah bila diformulasikan
kurkumin yang sukar larut, diperlukan upaya untuk meningkatkan laju disolusi
kurkumin, yaitu dengan metode dispersi padat.
PVP adalah polimer yang biasa digunakan sebagai bahan tambahan dalam
produk sediaan obat (Fischer dan Bauer, 2009). PVP memiliki kemampuan untuk
berperan sebagai pembawa yang akan memfasilitasi kurkumin melalui mekanisme
penyelubungan partikel kurkumin sehingga laju disolusinya meningkat. Polimer
PVP yang merupakan polimer polar dan hidrofilik akan bertugas sebagai matrik
yang membawa molekul-molekul kurkumin di dalamnya dan menembus membran
biologis dengan lebih mudah karena sifat PVP yang dapat terlarut dalam air (van
Ketel dan van den Berg, 1990). Dalam perannya sebagai pembawa PVP K30
membentuk sistem matrik dengan ikatan O-H dan N-H pada setiap unit PVP K30
secara berulang sehingga diperlukan dalam jumlah yang cukup untuk membawa
zat aktif (Wang, 2009).
Dispersi padat dapat dilakukan dengan beberapa cara, salah satunya
dengan instrumen rotary evaporator yang bekerja dengan sistem vakum (Leuner
dan Dressman, 2000). Rotary evaporator bertanggung jawab untuk
mendispersikan kurkumin ke dalam matrik polimer PVP dengan bantuan pelarut
dan selanjutnya akan menghilangkan pelarutnya sehingga akan didapatkan bahan
obat yang merupakan dispersi kurkumin dalam PVP. Pelarut dapat dihilangkan
dari dispersi karena rotary evaporator dengan sistem vakum akan membentuk
kondisi pada suhu dan tekanan tertentu hanya pelarut saja yang akan ditarik keluar
dari sistem dispersi (Laurence dan Christopher, 1989). Sehingga yang didapatkan
bentuk sediaan kapsul. Dispersi padat dapat dibuat dalam berbagai macam
perbandingan jumlah zat aktif dan pembawa. Srinarong (2009) menyebutkan
bahwa dengan menurunnya proporsi drug load, persen terdisolusi akan
meningkat.
Uji disolusi dilakukan dengan alat rotating paddle dan akan dianalisis
dengan densitometri untuk melihat profil disolusi dispersi kurkumin. Data dari
analisis densitometri akan diolah dan diketahui apakah kurkumin yang sudah
didispersi padat memiliki profil disolusi yang baik.
I. Hipotesis
Berdasarkan landasan teori, dapat dihipotesiskan bahwa dispersi padat
kurkumin ekstrak temulawak dengan pembawa PVP K30 dengan berbagai
proporsi drug load yang dihasilkan dengan metode vacuum rotary evaporator
akan meningkatkan disolusi efisiensi kurkumin ekstrak temulawak, dengan
20
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental karena adanya
perlakuan terhadap senyawa uji. Rancangan penelitian ini adalah rancangan
penelitian acak pola searah.
B. Variabel dan Definisi Operasional 1. Variabel
a. Variabel bebas : Proporsi drug load yang digunakan
b. Variabel tergantung : Persentase kurkumin terdisolusi
c. Variabel pengacau terkendali : Suhu dan kelembaban selama
penyimpanan
d. Variabel pengacau tak terkendali : Suhu dan kelembaban ruangan
2. Definisi Operasional
a. Dispersi padat adalah mendispersikan kurkumin sebagai zat aktif dalam
ekstrak temulawak pada pembawa PVP K30, yang disiapkan dengan
metode pelarutan. Dispersi padat dibuat dengan 3 variasi drug load; SD F1
dengan drug load 6%, SD F2 dengan drug load 4%, dan SD F3 dengan
drug load 2,4%.
b. Evaporasi adalah metode yang digunakan untuk menghilangkan etanol
sebagai pelarut dalam pembuatan dispersi padat. Campuran ekstrak
suhu 50o-60o C dalam kondisi vakum. Pelarut akan dievaporasi akan
menguap dan membentuk tetesan kembali setelah terjadi kontak dengan
pendingin Liebig. Tetesan tertampung pada wadah tertentu sehingga
terpisah dari bahan sehingga didapatkan bahan yang tidak lagi disertai
pelarut.
c. Disolusi adalah suatu proses melarutnya kurkumin dari sediaan dispersi
padat ke dalam suatu medium buffer phospat menghasilkan larutan
berwarna kuning yang bening. Disolusi diukur dengan menghitung
disolusi efisiensi, yaitu area di bawah kurva persentase kurkumin
terdisolusi.
d. Pengukuran persentase disolusi kurkumin pada dispersi padat dilakukan
dengan KLT-densitometri sehingga dapat diketahui kadar kurkumin dari
dispersi padat tersebut yang telah terpisah dari senyawa lain yang
menyerupai kurkumin (demetoksikurkumin dan bisdemetoksikurkumin).
C. Bahan Penelitian
Ekstrak Temulawak C15, baku kurkumin, kloroform, metanol, PVP K30,
Etanol, kloroform, aquabidest, kapsul cangkang keras gelatin No.00.
D. Alat Penelitian
Dissolution tester (Erweka), vacuum rotary evaporator, neraca analitis
E. Tata Cara Penelitian 1. Pembuatan Dispersi Padat
Sistem dispersi padat ini dibuat dengan menggunakan metode pelarutan.
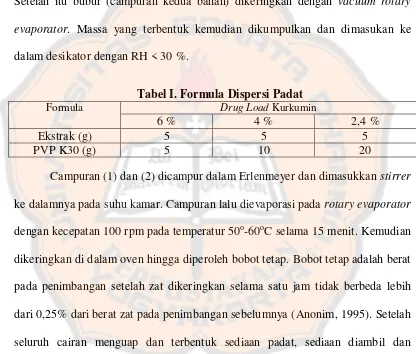
Setelah masing-masing bahan ditimbang sesuai dengan perbandingan, ekstrak
temulawak dengan kadar 12,12% dan PVP K30 dilarutkan dalam sejumlah etanol.
Setelah itu bubur (campuran kedua bahan) dikeringkan dengan vacuum rotary
evaporator. Massa yang terbentuk kemudian dikumpulkan dan dimasukan ke
dalam desikator dengan RH < 30 %.
Tabel I. Formula Dispersi Padat
Formula Drug Load Kurkumin
6 % 4 % 2,4 %
Ekstrak (g) 5 5 5
PVP K30 (g) 5 10 20
Campuran (1) dan (2) dicampur dalam Erlenmeyer dan dimasukkan stirrer
ke dalamnya pada suhu kamar. Campuran lalu dievaporasi pada rotary evaporator
dengan kecepatan 100 rpm pada temperatur 50o-60oC selama 15 menit. Kemudian
dikeringkan di dalam oven hingga diperoleh bobot tetap. Bobot tetap adalah berat
pada penimbangan setelah zat dikeringkan selama satu jam tidak berbeda lebih
dari 0,25% dari berat zat pada penimbangan sebelumnya (Anonim, 1995). Setelah
seluruh cairan menguap dan terbentuk sediaan padat, sediaan diambil dan
disimpan pada desikator atau dry box dengan kelembaban ≤ 30%.
2. Pembuatan Campuran Fisik
Campuran fisik dibuat dengan mencampurkan serbuk ekstrak temulawak
dan PVP K30, yang masing-masing telah diayak sebelumnya dengan ayakan no.
dihitung berdasarkan jumlah dispersi padat yang diperoleh tiap replikasinya.
Pencampuran kedua serbuk dilakukan dengan mortir dan pengaduk hingga
homogen.
3. Uji Disolusi
Uji disolusi dilakukan dalam medium aquadest sebanyak 500 mL pada
suhu 37 ± 0,5oC. Metode yang digunakan adalah rotating paddle. Pedal disolusi
diatur pada kecepatan putaran 100 rpm
Sediaan uji dimasukkan ke dalam tabung disolusi, lalu alat uji disolusi
dihidupkan. Kemudian setiap 5, 10, 15, 30, 45, 60, dan 120 menit dipipet cuplikan
sebanyak 5 ml dan medium disolusi diganti dengan 5 ml medium disolusi yang
baru setelah pengambilan sampel. Setiap pengambilan cuplikan diganti dengan
medium disolusi dalam jumlah yang sama. Larutan diukur kadarnya dengan
KLT-densitometri dan dihitung disolusi efisiensinya dengan metode Khan dengan
membandingkan area di bawah kurva persentase terdisolusi.
4. Penetapan Kadar Kurkumin dengan KLT-Densitometri
Sejumlah 5 mL cuplikan yang didapatkan dari disolusi akan dipekatkan
dengan cara ekstraksi cair-cair dengan etil asetat untuk selanjutnya dimasukkan
flakon, diuapkan, dan didapatkan kurkumin padat pada flakon. Efisiensi dan
reprodusibilitas ekstraksi dilihat dengan metode adisi.
Padatan kurkumin yang didapatkan dilarutkan dengan 500 µL etanol.
Diambil 1 µL larutan kurkumin kemudian ditotolkan pada plat KLT dan dianalisis
Kondisi Densitometer untuk analisis ini adalah :
Fase diam : Silica gel 60 GF 254
Tebal plat : 0,2 mm
Fase gerak : kloroform : etanol : air suling
Panjang pengembangan : 6,5 cm
Durasi pengembangan : ±15 menit
Volume sampel : 1 μL Panjang gelombang : 425 nm
Detektor : UV
Dihitung luas area yang didapatkan kemudian dihitung kadar
kurkuminnya dengan kurva baku yang telah dibuat.
F. Validasi Metode 1. Larutan Stok Kurkumin
Sejumlah 50,0 mg serbuk kurkumin ditimbang dengan seksama,
dimasukkan ke dalam labu ukur 25,0 mL. Diencerkan dengan etanol p.a hingga
tanda, kemudian disimpan dalam wadah yang terlindung dari cahaya.
2. Pembuatan Kurva Baku
Larutan stok diambil sebanyak 0,125 mL; 0,25 mL; 0,5 mL; 0,75 mL; 1
mL; 1,25 mL; 1,5 mL; dan 1,75 mL dimasukkan ke dalam labu ukur 10,0 mL.
Diencerkan dengan etanol p.a hingga tanda. Kelima seri pengenceran tersebut
ditotolkan sebanyak 1 µL pada plat KLT, dikembangkan, dan selanjutnya diukur
yang diperoleh dihitung dengan regresi linier sehingga diperoleh persamaan kurva
baku kurkumin.
3. Penentuan recovery dan Coefficient of Variations (CV) baku
Penetapan parameter akurasi dilakukan dengan metode adisi. Larutan stok
diambil sebanyak 0,125 mL; 1 mL; dan 1,75 mL, masukkan ke dalam labu ukur
10,0 mL. Encerkan dengan etanol p.a hingga tanda. Ketiga larutan tersebut
ditotolkan sebanyak 1 µL pada plat KLT, dikembangkan, dan kemudian diukur
pada panjang gelombang maksimum. Replikasi dilakukan sebanyak 5 kali.
Selanjutnya dihitung kadar terukur dengan menggunakan persamaan kurva baku
yang telah dibuat pada poin 2. Berdasarkan data ini dapat ditentukan recovery dan
CVnya. Perhitungan dilakukan dengan cara sebagai berikut:
% recovery = 𝑘𝑎𝑑𝑎𝑟𝑡𝑒𝑟𝑢𝑘𝑢𝑟
𝑘𝑎𝑑𝑎𝑟𝑡𝑒𝑟 ℎ𝑖𝑡𝑢𝑛𝑔 x 100%...(2)
(Gandjar dan Rohman, 2007).
4. Penentuan recovery dan Coefficient of Variations (CV) baku dalam matriks sampel
i. Pembuatan larutan sampel (LS)
Sejumlah lebih kurang 50 mg ekstrak temulawak dilarutkan etanol
hingga volume 50 mL. Replikasi dilakukan sebanyak 5 kali.
ii. Pembuatan larutan sampel dengan penambahan baku kurkumin (LSK).
Sejumlah 2,25 mL larutan baku kurkumin dengan konsentrasi 90 μg/ml dimasukkan dalam labu takar 50 mL, kemudian ditambahkan 50 mg ekstrak
ekstraksi menggunakan etil asetat kemudian dikeringkan dengan udara mengalir,
setelah itu ditambahkan etanol hingga tanda . Replikasi dilakukan sebanyak 5 kali.
iii. Pengembangan dan pengukuran.
LSdan LSK ditotolkan sebanyak 1 µL pada plat KLT, dikembangkan,
dan kemudian diukur pada panjang gelombang maksimum. Setelah itu dihitung
kadar baku kurkumin dalam sampel menggunakan persamaan kurva baku yang
telah dibuat pada poin 2. Kadar baku kurkumin dalam sampel adalah selisih kadar
LSKdengan kadar LS. Selanjutnyadihitung recovery dan CV nya.
5. Penetapan Parameter Linearitas
Larutan stok diambil sebanyak 0,125 mL; 0,25 mL; 0,5 mL; 0,75 mL; 1
mL; 1,25 mL; 1,5 mL; dan 1,75 mL, masukkan ke dalam labu ukur 10,0 ml.
Encerkan dengan metanol p.a hingga tanda. Kelima larutan tersebut ditotolkan
sebanyak 1 µL pada plat KLT, dikembangkan, dan selanjutnya diukur pada
panjang gelombang maksimum. Replikasi dilakukan sebanyak 3 kali. Hitung nilai
linieritas luas area dan konsentrasi baku kurkumin dengan menggunakan regresi
linier. Persyaratan data linearitas yang dapat diterima jika memenuhi nilai
koefisien korelasi r > 0,99 (Gandjar dan Rohman, 2007).
G. Analisis Hasil 1. Validasi Metode
Validasi metode yang digunakan berdasarkan parameter berikut.
a. Akurasi
% recovery = 𝑘𝑎𝑑𝑎𝑟𝑡𝑒𝑟𝑢𝑘𝑢𝑟
𝑘𝑎𝑑𝑎𝑟𝑡𝑒𝑟 ℎ𝑖𝑡𝑢𝑛𝑔 x 100%...(4)
Metode adisi digunakan untuk menganalisis bahan obat dengan kadar
lebih dari 0,1% dan kurang dari 1%, maka rentang recovery yang digunakan yaitu
80-120% (Gandjar dan Rohman, 2007).
b. Presisi
Presisi dinyatakan dengan koefisien variasi, dengan rumus:
CV = 𝑆𝐷
× x 100%...(5)
Metode ini dikatakan baik bila nilai CV yang diperoleh < 2%. Semakin
kecil nilai CV, presisi metode yang digunakan semakin baik (Gandjar dan
Rohman, 2007).
c. Linearitas
Parameter linearitas dilihat dari nilai koefisien korelasi (r) hasil
pengukuran larutan seri baku kurkumin. Metode dikatakan memiliki linearitas
yang baik bila r > 0,99 atau r (Gandjar dan Rohman, 2007).
2. Analisis Statistik Penetapan Kadar Kurkumin Terlarut
Data uji disolusi kurkumin dibuat dalam bentuk kurva hubungan antara
jumlah persentase kurkumin terdisolusi terhadap waktu. Dihitung area di bawah
kurva untuk mendapatkan nilai disolusi efisiensi sesuai dengan metode Khan.
Kemudian dilakukan perhitungan statistik korelasi proporsi drug load terhadap
28 BAB IV PEMBAHASAN
A. Pembuatan Dispersi Padat
Tujuan dari pembuatan dispersi padat adalah meningkatkan disolusi obat
yang memiliki kelarutan rendah. Kurkumin dapat ditingkatkan kelarutannya
dengan didispersi padat. Dispersi padat dibuat dengan melarutkan terlebih dahulu
ekstrak temulawak pada etanol 96% dan dicampurkan dengan PVP K30 yang
telah dilarutkan juga pada etanol 96%. Dispersi padat dibuat dalam 3 formula.
Etanol 96% digunakan untuk melarutkan ekstrak maupun PVP K30. Berikut
merupakan tabel formulasi pembuatan dispersi padat.
Tabel II. Formula Dispersi Padat
PVP K30 (mg) EtOH 96% (mL) Ekstrak (mg) EtOH (mL)
5000 100 5000 100
10000 200 5000 100
20000 400 5000 100
Dispersi padat ekstrak temulawak dibuat dengan vacuum rotary
evaporator dengan pengkondisian suhu air 50o-70oC, dan rotation speed 100 rpm.
Vacuum rotary evaporator bekerja dengan mengevaporasi pelarut (etanol 96%)
dengan waterbath yang dikendalikan suhunya dan kondisi vakum sehingga suhu
untuk mengevaporasi pelarut akan lebih rendah dan tidak merusak komponen
yang terkandung dalam larutan (kurkumin).
Larutan ditempatkan pada labu alas bulat dan dipasangkan pada suatu
dan meninggalkan labu alas bulat. Uap tersebut akan memasuki pendingin dan
akan berubah menjadi cair kembali dan ditampung pada labu penampung.
Setelah larutan pada labu alas bulat hampir teruapkan semua, suhu air
diturunkan dan alat dimatikan. Akan diperoleh hasil dispersi padat berupa
campuran semipadat dengan viskositas tinggi. Campuran tersebut dimasukkan
oven dengan suhu 30o-50oC selama beberapa hari hingga bobot konstan dan
diperoleh padatan yang adalah hasil dispersi padat ekstrak temulawak.
Padatan digerus hingga halus dan diayak dengan ayakan no. mesh 50,
kemudian didapatkan serbuk dan disimpan dalam desikator dan tertutup
aluminium foil karena dalam serbuk terbuat dari PVP K30 yang bersifat sangat
higroskopis serta kurkumin yang fotosensitif. Serbuk dalam jumlah 500 mg
dimasukkan dalam kapsul no. 00 untuk dilakukan uji disolusi.
B. Pembuatan Campuran Fisik
Campuran fisik dibuat dengan mencampurkan ekstrak temulawak dengan
PVP K30 secara homogen menggunakan mortar dan pengaduk kaca. Tidak
digunakan stemper untuk mengurangi resiko adanya tekanan saat pengadukan
yang dapat mengubah bentuk partikel ekstrak temulawak.
Campuran fisik dibuat sama pada proporsi yang sama dengan formula
dispersi padat, yaitu 1:1, 1:2, dan 1:4 (ekstrak temulawak : PVP K30). Campuran
fisik kemudian dimasukkan ke dalam kapsul no. 00 dan diuji disolusinya untuk
C. Pembuatan Fase Gerak
Fase gerak pada penelitian ini menggunakan komposisi fase gerak dari
penelitian Sudibyo Martono pada tahun 1996, yaitu dengan kloroform : etanol :
aquadest (25 : 0,96 : 0,004). Pemilihan fase gerak mempengaruhi waktu retensi
pemisahan komponen-komponen di dalam formula dispersi padat yang dibuat.
Sistem kromatografi KLT-Densitometri pada penelitian ini merupakan
kromatografi dengan fase normal, karena fase gerak bersifat non polar, sedangkan
fase diamnya, yaitu silika gel 60 GF254 bersifat lebih polar dari fase geraknya.
D. Penetapan Panjang Gelombang Maksimum
Tujuan dari penetapan panjang gelombang maksimum adalah
mendapatkan panjang gelombang yang paling baik untuk pengukuran kurkumin
secara KLT-densitometri dalam artian panjang gelombang yang mampu
menunjukkan sensitifitas yang baik saat dilakukan pengukuran berulang dengan
panjang gelombang tersebut.
Penentuan panjang gelombang maksimum dilakukan dengan melakukan
pengukuran menggunakan seri baku kurkumin 50 μg/ml, 200 μg/ml, dan 350 μg/ml dan direplikasi sebanyak 3 kali. Dari hasil pengukuran diamati absorbansi
maksimum yang diberikan, dan akan digunakan sebagai panjang gelombang untuk
pengukuran selanjutnya. Tujuan dari penggunaan 3 seri konsentrasi ini untuk
melihat apakah pada konsentrasi yang dianggap mewakili seluruh konsentrasi
pada seri baku ini dihasilkan spektrum serapan maksimum yang sama. Scanning
panjang gelombang maksimum kurkumin dilakukan pada panjang gelombang
nm. Panjang gelombang maksimum ditentukan dari nilai yang memberikan
pengukuran luas area paling besar dan paling sering muncul. Dari hasil
pengukuran didapatkan bahwa panjang gelombang maksimumnya adalah 425 nm.
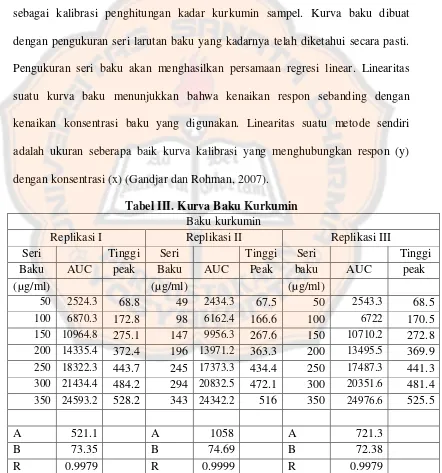
E. Pembuatan Kurva Baku Kurkumin
Kurva baku atau kurva kalibrasi adalah kurva yang akan digunakan
sebagai kalibrasi penghitungan kadar kurkumin sampel. Kurva baku dibuat
dengan pengukuran seri larutan baku yang kadarnya telah diketahui secara pasti.
Pengukuran seri baku akan menghasilkan persamaan regresi linear. Linearitas
suatu kurva baku menunjukkan bahwa kenaikan respon sebanding dengan
kenaikan konsentrasi baku yang digunakan. Linearitas suatu metode sendiri
adalah ukuran seberapa baik kurva kalibrasi yang menghubungkan respon (y)
dengan konsentrasi (x) (Gandjar dan Rohman, 2007).
Tabel III. Kurva Baku Kurkumin
Baku kurkumin
Replikasi I Replikasi II Replikasi III
Seri larutan baku yang digunakan adalah larutan dengan konsentrasi 50
μg/ml, 100 μg/ml, 150 μg/ml, 200 μg/ml, 250 μg/ml, 300 μg/ml dan 350 μg/ml
dan dilakukan replikasi 3 kali, didapatkan nilai (r) yang baik dan memenuhi
persyaratan kurva baku, yaitu 0,99.
F. Validasi Metode
Validasi metode adalah ukuran kesahihan suatu metode yang digunakan.
Validasi digunakan dalam suatu pengembangan metode pengukuran untuk
menjamin kesahihan metode tersebut, selain itu validasi juga diperlukan dalam
verifikasi metode. Verifikasi metode berbeda dengan pengembangan metode,
validasi yang dibutuhkan pada verifikasi metode meliputi linieritas, akurasi, dan
presisi.
1. Selektivitas
Selektivitas adalah parameter yang menyatakan kemampuan metode
penetapan kadar untuk mengukur respon analit dalam sampel secara akurat
diantara semua komponen yang terdapat dalam matriks sampel.
Selektivitas metode diperlukan untuk mengukur analit secara akurat tanpa
terganggu oleh senyawa-senyawa lain yang terdapat dalam sampel. Pengukuran
parameter selektivitas metode KLT-Densitometri ini dilakukan dengan
membandingkan Rf dari baku dan Rf dari sampel dalam campuran pada kondisi
yang sama. Nilai Rf merupakan parameter analisis kualitatif suatu senyawa dalam
campuran pada metode KLT, sehingga dapat digunakan sebagai parameter
baku adalah 0,62 dan Rf rata-rata dari analit dalam sampel adalah 0,61. Selain itu
resolusi juga dihitung dan didapatkan nilai resolusi > 1,5. Maka metode ini
diketahui memenuhi syarat selektivitas yang baik untuk analisis kurkumin.
2. Linearitas
Linearitas yang baik ditunjukkan dengan nilai (r) yang baik, yaitu r ≥ 0,99 (Gandjar dan Rohman, 2007). Linearitas diperoleh dengan pengukuran seri baku
kurkumin dengan konsentrasi 50 μg/ml, 100 μg/ml, 150 μg/ml, 200 μg/ml, 250 μg/ml, 300 μg/ml dan 350 μg/ml yang direplikasi 3 kali. Dari seri larutan baku
tersebut akan diperoleh kurva kalibrasi dan persamaan regresinya, lalu dihitung
nilai (r). Hasil nilai (r) yang diperoleh replikasi I = 0,9979 replikasi II = 0,9999
dan replikasi III = 0,9979.
3. Akurasi
Akurasi adalah parameter validasi yang menggambarkan apakah suatu
metode menghasilkan nilai pengukuran yang tepat atau mendekati nilai
sebenarnya. Akurasi dinyatakan dengan persen recovery (% recovery) / persen
perolehan kembali. Persen recovery merupakan persen perolehan kembali kadar
terukur terhadap kadar sebenarnya. Recovery dari baku kurkumin adalah faktor
penting dalam analisis kuantitatif kurkumin karena sangat menentukan kebenaran
pengukuran sampel. Suatu metode dikatakan memiliki akurasi yang baik apabila
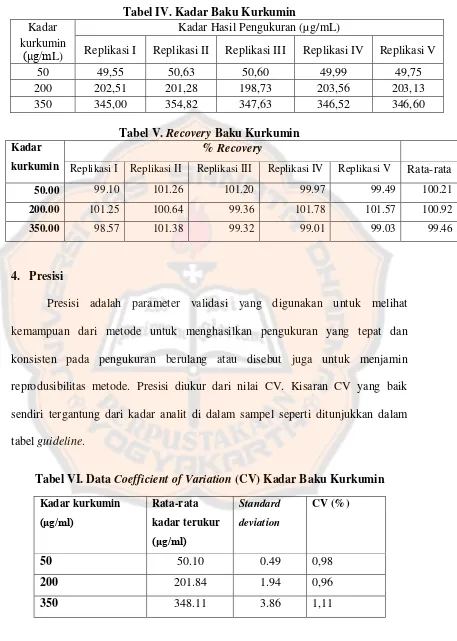
nilai % recoverynya antara 98-102% (Harmita, 2004). Berikut hasil pengukuran %
Tabel IV. Kadar Baku Kurkumin
Kadar Kadar Hasil Pengukuran (µg/mL) kurkumin
(μg/mL) Replikasi I Replikasi II Replikasi III Replikasi IV Replikasi V 50 49,55 50,63 50,60 49,99 49,75 200 202,51 201,28 198,73 203,56 203,13 350 345,00 354,82 347,63 346,52 346,60
Tabel V. Recovery Baku Kurkumin Kadar
Presisi adalah parameter validasi yang digunakan untuk melihat
kemampuan dari metode untuk menghasilkan pengukuran yang tepat dan
konsisten pada pengukuran berulang atau disebut juga untuk menjamin
reprodusibilitas metode. Presisi diukur dari nilai CV. Kisaran CV yang baik
sendiri tergantung dari kadar analit di dalam sampel seperti ditunjukkan dalam
tabel guideline.
Nilai CV pada konsentrasi 50 μg/ml, 200 μg/ml, dan 350 μg/ml kurang
dari 2 %. Hasil tersebut menunjukkan bahwa CV sudah sesuai persyaratan dan
menunjukkan bahwa metode yang digunakan memiliki presisi yang baik.
5. Range
Range adalah interval antara konsentrasi analit pada level bawah dan level
atas dalam pengukuran sampel secara kuantitatif yang masih memenuhi parameter
linearitas, akurasi, dan presisi sehingga hasilnya dapat dipertanggungjawabkan
validitasnya. Pada penelitian ini, range konsentrasinya adalah 50-350 μg/ml. Range ini menunjukkan area analisis yang memenuhi parameter linearitas,
akurasi, dan presisi.
G. Penentuan Akurasi Dan Presisi Baku Kurkumin Dalam Sampel
Akurasi dan presisi baku kurkumin dalam sampel ditentukan dengan
melihat AUC hasil penambahan baku kurkumin ke dalam matriks sampel. Metode
pengukuran dilakukan dengan metode adisi. Luas area dari peak baku yang
ditambahkan akan menambah luas area pada peak yang dihasilkan sampel.
Apabila luas area pada peak tersebut bertambah ketika baku kurkumin
ditambahkan maka dapat dipastikan bahwa peak tersebut merupakan peak
kurkumin.
Luas area yang bertambah harus berada pada nilai Rf yang identik dengan
Rf baku kurkumin sehingga dapat disimpulkan bahwa peak tersebut merupakan
kurkumin. Setelah dapat dipastikan bahwa peak tersebut adalah peak kurkumin
sampel ditambah baku, maka dilakukan penentuan akurasi dan presisi baku
mengetahui kemampuan metode dalam mengukur respon baku kurkumin dalam
matriks sampel secara akurat dan reprodusibilitas metode.
Tabel VII. Recovery dan CV baku kurkumin dalam matriks sampel Rep % Recovery CV (%)
1 98.72
2 103.07
3 104.01 2.74
4 97.86
5 99.37
Kadar baku kurkumin yang ditambahkan pada sampel adalah 90 μg/ml.
Berdasarkan ketentuan dalam UNODC, batas nilai recovery yang dapat diterima
95-105% dengan nilai CV<15% (Anonim,2009),. Oleh karena itu, dari tabel VII
dapat disimpulkan bahwa metode KLT-Densitometri ini dapat mengukur analit
dalam matriks sampel secara akurat dan metode memiliki presisi yang bagus.
H. Uji Disolusi
Uji disolusi adalah uji untuk melihat pelepasan obat pada jangka waktu
tertentu dan akan menghasilkan profil disolusi dari sampel tersebut. Pengujian
disolusi pada penelitian bertujuan untuk membandingkan profil disolusi dari
masing-masing formula dispersi padat yang dibuat dan juga melihat profil disolusi
campuran fisik ekstrak temulawak – PVP K30. Uji disolusi dilakukan dengan menggunakan metode rotating paddle.
Sampel dispersi padat kurkumin dan campuran fisik masing-masing
dimasukkan ke dalam kapsul no. 00 dan diujikan dalam medium disolusi berisi
buffer fosfat dengan pH 6 sebanyak 500 mL yang dibuat dengan mencampurkan
dengan pH 6 dan di tambah aquadest hingga 1000 mL. Pencuplikan sampel
dilakukan pada 0, 5, 10, 15, 30, 45, 60, dan 120 menit. Uji disolusi dilakukan pada
medium bersuhu ± 37oC dengan kecepatan rotasi dayung 100 rpm. Cuplikan
diambil sebanyak 5 mL dan langsung ditambahkan kembali 5 mL larutan buffer
yang sama ke dalam medium disolusi untuk mempertahankan jumlah 500 mL.
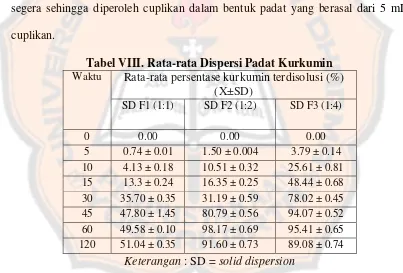
Cuplikan pada menit-menit yang telah ditentukan tersebut langsung
diekstraksi cair-cair dengan etil asetat untuk menarik kurkuminoid di dalam 5 mL
medium disolusi. Setelah diekstraksi, dilakukan penguapan etil asetat dengan
segera sehingga diperoleh cuplikan dalam bentuk padat yang berasal dari 5 mL
cuplikan.
Tabel VIII. Rata-rata Dispersi Padat Kurkumin Waktu Rata-rata persentase kurkumin terdisolusi (%)
(X±SD)
SD F1 (1:1) SD F2 (1:2) SD F3 (1:4)
0 0.00 0.00 0.00
5 0.74 ± 0.01 1.50 ± 0.004 3.79 ± 0.14 10 4.13 ± 0.18 10.51 ± 0.32 25.61 ± 0.81 15 13.3 ± 0.24 16.35 ± 0.25 48.44 ± 0.68 30 35.70 ± 0.35 31.19 ± 0.59 78.02 ± 0.45 45 47.80 ± 1.45 80.79 ± 0.56 94.07 ± 0.52 60 49.58 ± 0.10 98.17 ± 0.69 95.41 ± 0.65 120 51.04 ± 0.35 91.60 ± 0.73 89.08 ± 0.74
Keterangan : SD = solid dispersion
Campuran fisik tidak dapat dianalisis jumlah yang terdisolusi, karena pada
saat uji disolusi tidak terdisolusi dan membentuk semacam suspensi sehingga
pada pengambilan cuplikan dan ekstraksi menghasilkan jumlah yang tidak
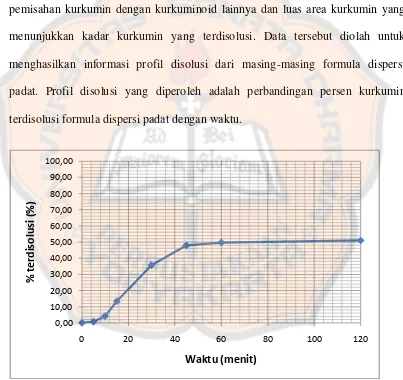
I. Pengukuran Kadar Kurkumin
Pengukuran kadar kurkumin dilakukan dengan metode KLT-densitometri.
Kadar kurkumin yang terukur kemudian akan dihitung persen kurkumin
terdisolusi. Pengukuran dilakukan pada tiap cuplikan formula dispersi padat dan
juga campuran fisik kemudian dilakukan replikasi 3 kali untuk setiap formula
dispersi padat. Pengukuran dengan KLT-densitometri akan menghasilkan data
pemisahan kurkumin dengan kurkuminoid lainnya dan luas area kurkumin yang
menunjukkan kadar kurkumin yang terdisolusi. Data tersebut diolah untuk
menghasilkan informasi profil disolusi dari masing-masing formula dispersi
padat. Profil disolusi yang diperoleh adalah perbandingan persen kurkumin
terdisolusi formula dispersi padat dengan waktu.
Gambar 3. Grafik Persen Terdisolusi vs Waktu Formula SD F1
Formula SD F1 adalah formula dengan perbandingan ekstrak temulawak :
PVP K30 (1:1) dengan kadar kurkumin dalam formula 6 %.
Gambar 4. Grafik Persen Terdisolusi vs Waktu Formula SD F2
Formula SD F2 adalah formula dengan perbandingan ekstrak temulawak :
PVP K30 (1:2) dengan kadar kurkumin dalam formula 4 %.
Gambar 5. Grafik Persen Terdisolusi vs Waktu Formula SD F3
Formula SD F3 adalah formula dengan perbandingan ekstrak temulawak :
PVP K30 (1:4) dengan kadar kurkumin dalam formula 2,4 %.
Gambar 6. Grafik Persen Terdisolusi vs Waktu Formula SD F1, SD F2, SD F3 Gambar diatas menunjukkan bahwa formula SD F3 menghasilkan profil
disolusi yang lebih baik dibandingkan formula yang lain diliat dari persen
kurkumin terdisolusi di tiap menit. Srinarong (2009) menyebutkan bahwa dengan
menurunnya proporsi drug load, persen terdisolusi akan meningkat.
Pada gambar 7 digambarkan profil disolusi masing-masing formula, dan
ditemukan hasil yang menarik di mana hingga menit kelimabelas F2 menunjukkan
persen terdisolusi yang lebih besar daripada F1, namun pada menit ketigapuluh F1
menunjukkan persen terdisolusi yang lebih banyak daripada F2. Pada menit
keempatpuluh lima kembali F2 menunjukkan persen terdisolusi yang lebih tinggi
daripada F1. Fenomena tersebut juga terjadi pada F3, hingga menit keempatpuluh
lima F3 menunjukkan persen terdisolusi yang lebih tinggi daripada F2, tetapi
sejak menit keenampuluh hingga seratus duapuluh F2 menunjukkan persen
terdisolusi yang sedikit lebih tinggi daripada F3.
J. Hubungan Proporsi Drug Load Terhadap Disolusi Kurkumin
Fenomena yang terjadi menunjukkan adanya perubahan kecepatan disolusi
pada F1, F2, dan F3 pada waktu tertentu. Pengambilan kesimpulan pada hasil
disolusi harus dilakukan dengan metode Disolusi Efisiensi (DE) sehingga tidak
didapat kesimpulan yang bias dari hasil disolusi formula-formula tersebut. DE
adalah metode untuk mengungkapkan hasil pengamatan kecepatan disolusi obat
dalam suatu medium dengan cara membandingkan luas area di bawah kurva
disolusi dengan luas segiempat seratus persen zat aktif larut dalam medium pada
saat tertentu (Fudholi, 2013).
DEt = ( ydt / y100t )x 100% ………(6)
(Fudholi, 2013)
ydt = luas area di bawah kurva zat aktif terlarut pada saat t
y100t = luas segiempat 100% zat aktif larut dalam medium untuk waktu t
Harga DE dinyatakan dalam kurun waktu pengamatan tertentu sehingga semakin
besar harga t akan semakin besar juga harga DE karena artinya semakin banyak
titik-titik pengamatan yang digunakan. Berikut merupakan tabel formulasi
pembuatan dispersi padat.
Tabel IX. Disolusi Efisiensi Formula Dispersi Padat Menit 120 Formula DE120 (%) Rata- rata
DE120 (%)
Replikasi 1 Replikasi 2
Replikasi 3