i
EFEK HEPATOPROTEKTIF INFUSA DAUN
Macaranga tanarius
L. PADA TIKUS JANTAN GALUR WISTAR
TERINDUKSI PARASETAMOL
SKRIPSI
Disusun untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
EFEK HEPATOPROTEKTIF INFUSA DAUN
Macaranga tanarius
L. PADA TIKUS JANTAN GALUR WISTAR
TERINDUKSI PARASETAMOL
SKRIPSI
Disusun untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
EFEK HEPATOPROTEKTIF INFUSA DAUN
Macaranga tanarius
L. PADA TIKUS JANTAN GALUR WISTAR
TERINDUKSI PARASETAMOL
SKRIPSI
Disusun untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
iii
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
iv
HALAMAN PERSEMBAHAN
”
Kemarin sudah berlalu, hari esok belum datang, hanya hari ini yang
menjanjikan sukses bagi orang yang mau dan mampu
mengaktualisasikan dirinya dengan totalitas”
Karya kecil ini aku persembahkan untuk:
Yesus Penerangku karena Engkau adalah sumber kekuatanku
Bapak, Ibu,mbak Heni tercinta atas kasih sayang, dukungan dan doa
v
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
vii
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa atas berkat dan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi dengan judul “ Efek Hepatoprotektif Infusa Daun Macaranga tanarius L. pada Tikus Jantan Galur Wistar Terinduksi Parasetamol” ini.
Skripsi ini disusun untuk memenuhi salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S. Farm.) Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Penyelesaian skripsi ini tentunya tidak lepas dari bantuan dari berbagai pihak, baik secara langsung maupun secara tidak langsung. Oleh karena itu penulis hendak mengucapkan terima kasih kepada :
1. Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Phebe Hendra, M.Si., Ph.D., Apt., selaku Dosen Pembimbing skripsi ini atas segala kesabaran untuk selalu membimbing, memberi motivasi, dan memberi masukan kepada penulis dalam menyusun skripsi ini.
3. Dr. C. J. Soegihardjo, Apt., selaku Dosen Penguji skripsi atas bantuan dan masukkan kepada penulis demi kemajuan skripsi ini.
4. Yosef Wijoyo, M.Si., Apt., selaku Dosen Penguji skripsi atas bantuan dan masukkan kepada penulis demi kemajuan skripsi ini.
5. Mas Parjiman, Mas Heru dan Mas Kayat selaku laboran bagian farmakologi serta Mas Wagiran, selaku laboran farmakognosi fitokimia, atas segala bantuan dan dinamika selama di laboratorium.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
viii
6. Rekan-rekan penelitian tim macaranga, Aryanti Prima Andini, Elisa Eka Adrianto, Ari Widya Nugraha, Dina Wulandari, atas bantuan, kerjasama, perjuangan dan suka duka yang telah kita alami bersama selama penelitian.
7. Teman-teman tim kerja kelompok, Bimo Tiar Nugroho, Hendrika Toi Doja, Agustina Nila, Maria Ratri Damarini atas kesabaran, kekompakan, dan dukungannya selama ini.
8. Teman-teman angkatan 2007 kelas B serta teman-teman kelas FKK A angkatan 2007 atas kebersamaan kita.
9. Pihak-Pihak lain yang turut membantu penulis namun tidak dapat disebutkan satu persatu.
Penulis menyadari bahwa setiap manusia tidak ada yang sempurna. Oleh karena itu, penulis mengharapkan adanya kritik, saran dan masukan demi kemajuan di masa yang akan datang.
Akhir kata, penulis berharap bahwa skripsi ini dapat bermanfaat bagi semua pihak, baik mahasiswa, lingkungan akademis, masyarakat serta memberikan sumbangan kecil bagi perkembangan ilmu pengetahuan khususnya di bidang kefarmasian.
Yogyakarta, 14 Desember 2010
ix
DAFTAR ISI
HALAMAN JUDUL………... i
HALAMAN PERSETUJUAN PEMBIMBING………... ii
HALAMAN PENGESAHAN………... iii
HALAMAN PERSEMBAHAN………... iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH. v PERNYATAAN KEASLIAN KARYA………... vi
PRAKATA………... vii
DAFTAR ISI………... ix
DAFTAR TABEL………... xii
DAFTAR GAMBAR... xiii
DAFTAR LAMPIRAN………. ... xiv
INTISARI………... xv
ABSTRACT………... xvi
BAB I. PENGANTAR………... 1
A. Latar Belakang………..……….... 1
1. Perumusan masalah...………...………... 3
2. Keaslian penelitian………...……... 3
3. Manfaat penelitian………..…... 4
B. Tujuan Penelitian... 4
BAB II. PENELAHAAN PUSTAKA... 5
A. TanamanMacaranga tanariusL. ... 5
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
x
1. Sinonim…………... 5
2. Nama daerah... ... 5
3. Taksonomi………..………..………... 5
4. Penyebaran ………. ……….... 6
5. Morfologi ………. ……….... 6
6. Kandungan ………. ……….... 6
7. Khasiat dan kegunaan ………... 8
B. HATI ... 8
1. Anatomi fisiologi hati………... 8
2. Kerusakan sel-sel hati………... 10
3. Hepatotoksin………. 13
4. ALT dan AST………... 13
C. Parasetamol ... 14
D. Infusa ... 17
1. Definisi……….……..……….….. 17
2. Pembuatan……….. 17
E. Landasan Teori... 17
K. Hipotesis ... 18
BAB III. METODE PENELITIAN... 19
A. Jenis dan Rancangan Penelitian... 19
B. Variabel dan Definisi Operasional ... 19
xi
D. Alat Penelitian………... 22
E. Tata Cara Penelitian ... 23
F. Tata Cara Analisis Hasil ... 26
BAB IV. HASIL DAN PEMBAHASAN ... 28
A. Penyiapan Bahan... 28
B. Uji Pendahuluan... 29
C. Hasil uji Hepatoprotektif Infusa DaunM. tanarius…….... 35
BAB V. KESIMPULAN DAN SARAN... 47
A. Kesimpulan... 47
B. Saran... 47
DAFTAR PUSTAKA... 48
LAMPIRAN... 51
BIOGRAFI PENULIS... 69
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xii
DAFTAR TABEL
Tabel I Rata-rata aktivitas ALT-serum tikus akibat perlakuan parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah... 30 Tabel II Hasil uji Scheffeaktivitas ALT-serum aktivitas ALT-serum tikus akibat
perlakuan parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah………... 31 Tabel III Rata-rata aktivitas AST-serum tikus akibat perlakuan parasetamol dosis
2,5 g/kgBB pada orientasi waktu pencuplikan
darah... 31 Tabel IV Hasil uji Scheffeaktivitas ALT-serum aktivitas ALT-serum tikus akibat
perlakuan parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah... 32 Tabel V Pengaruh praperlakuan jangka panjang pemberian infusa daun M.
tanarius terhadap hepatotoksisitas parasetamol dilihat dari aktivitas ALT-serum ………... 35 Tabel VI Pengaruh praperlakuan jangka panjang pemberian infusa daun M.
xiii
DAFTAR GAMBAR
Gambar 1. Struktur senyawa yang terdapat dalam daun
M.tanarius………... 7 Gambar 2. Struktur mikroskopik hati……... 9 Gambar 3. Struktur parasetamol…... 14 Gambar 4. Mekanisme biotransformasi dan oksidasi parasetamol oleh sitokrom
P450... 16 Gambar 5. Diagram batang rata-rata aktivitas ALT-serum tikus akibat perlakuan
parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah. ... 30 Gambar 6. Diagram batang rata-rata aktivitas ALT-serum tikus akibat perlakuan
parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah. ………. 32 Gambar 7. Diagram batang rata-rata pengaruh praperlakuan jangka panjang
pemberian infusa daunM. tanariusterhadap hepatotoksisitas parasetamol dilihat dari aktivitas ALT-serum... 36 Gambar 8. Diagram batang rata-rata pengaruh praperlakuan jangka panjang
pemberian infusa daunM. tanariusterhadap hepatotoksisitas parasetamol dilihat dari aktivitas AST-serum... 37 Gambar 9. Perpindahan elektron oleh karena protonasi pada ikatanα-βunsaturated
pada senyawa macarangiosida A... 46
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xiv
DAFTAR LAMPIRAN
Lampiran 1. Foto daunM. tanarius...51 Lampiran 2. Foto infusa daunM. tanarius……... 51 Lampiran 3. Analisis statistik aktivitas serum ALT pada uji pendahuluan penentuan
dosis hepatotoksik parasetamol... 52 Lampiran 4. Analisis statistik aktivitas serum AST pada uji pendahuluan penentuan
dosis hepatotoksik parasetamol………... 55 Lampiran 5. Analisis statistik aktivitas serum ALT perlakuan infusa daunM. tanarius
setelah induksi parasetamol dosis 2,5 g/kgBB... 58 Lampiran 6. Analisis statistik aktivitas serum AST perlakuan infusa daunM. tanarius
setelah induksi parasetamol dosis 2,5 g/kgBB... 62 Lampiran 7. Perhitungan efek hepatoprotektif………... 65 Lampiran 8. Perhitungan penetapan peringkat dosis infusa daunM. tanarius pada
xv
INTISARI
Penelitian efek hepatoprotektif infusa daunMacaranga tanarius(L.) pada tikus jantan terinduksi parasetamol dilakukan dengan tujuan untuk memperoleh bukti ilmiah tentang efek hepatoprotektif dari infusa daun M. tanarius akibat perlakuan hepatotoksin parasetamol.
Penelitian ini termasuk eksperimental murni rancangan acak lengkap pola searah menggunakan 30 ekor tikus putih jantan galur Wistar. Tikus yang ada kemudian dibagi sama banyak ke dalam enam kelompok. Tikus kelompok I diberi aquadest dosis 10 g/kgBB selama 6 hari berturut-turut sebagai kontrol negatif. Tikus kelompok II diberi Parasetamol dosis 2,5 g/kgBB sebagai kontrol hepatotoksik parasetamol. Tikus kelompok III diberi infusa daunM. tanarius dosis 10 g/kgBB selama 6 hari beturut-turut sebagai kontrol negatif infusa daun M. tanarius. Tikus kelompok IV sampai VI diberi infusa daunM. tanarius berturut-turut dengan dosis 10 g/kgBB; 5 g/kgBB; 2,5 g/kgBB selama 6 hari berturut-turut dan pada hari ke-7 diberi parasetamol dosis 2,5 g/kgBB, kemudian pada kelompok I hingga VI setelah 48 jam diambil darahnya dari sinus obitalis untuk ditetapkan aktivitas serum ALT dan AST.
Berdasarkan hasil penelitian dari data ALT serum yang diperoleh, dari tatacara analisis hasil yang ditetapkan, infusa daun M. tanarius memberikan efek hepatoprotektif pada dosis 10 g/kgBB; 5 g/kgBB; 2,5 g/kgBB secara berturut-turut sebesar 63,6%, 82,2%, dan 26,3%.
Kata kunci: efek hepatoprotektif, parasetamol, infusaMacaranga tanarius
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xvi
ABSTRACT
The research of hepatoprotective effect of aqueous extract from Macaranga tanariusL. leaf on male wistar strain rats induced paracetamol has been done in order to find scientific evidence of the hepatoprotective effect of M. tanarius leaf induced 2.5 g/kgBB doses of paracetamol.
This research is included to experimental study with one way-complete-random design using 30 male wistar strain rats. The rats were divided into six groups. Rats in group I were given 10 g/kgBB doses of aquadest continually in 6 days as a negative control. Group II rats were given 2.5 g/kgBB doses of Paracetamol as a hepatotoxic control. Group III rats were given 10 g/kgBB doses of M. tanarius leaf’s aqueous extract in 6 days as a negative control ofM. tanarius leaf’s aqueous extract. In group IV, V and VI, the rats were given 10 g/kgBB; 5 g/kgBB; 2.5 g/kgBB doses of M. tanariusleaf’s aqueous extract continually in 6 days and on the 7thday, the rats were given 2.5 g/kgBB doses of paracetamol. Then, the blood of the rats on group I up to group VI were taken from sinus obitalis to measure the ALT and AST serum activities.
Based on the result of the data of ALT serum taken, and oneway ANOVA test which is followed by Scheffe test, M. tanarius leaf’s aqueous extract has given hepatoprotective effect on 10 g/kgBB; 5 g/kgBB; 2.5 g/kgBB doses continually as big as 63.6%, 82.2%, and 26.3%.
1
BAB I PENGANTAR
A. Latar Belakang Penelitian
Hati merupakan organ dengan peranan yang penting dalam mempertahankan hidup dan dalam hampir setiap metabolisme dalam tubuh (Price dan Wilson, 2005). Apabila terjadi kerusakan pada hati manusia, tentu saja akan sangat berbahaya bagi kelangsungan hidup manusia tersebut.
Penyebab utama munculnya penyakit hati adalah karena induksi obat, infeksi virus dan reaksi imunologi (Williamson, David, dan Fred, 1996). Di Indonesia penelitian obat baru untuk masalah kerusakan hati belum banyak dilakukan, sehingga perlu dicari alternatif obat baru yang berasal dari sumber daya alam hayati. Macaranga tanarius L. (M. tanarius) merupakan tanaman asli Indonesia dan dapat dikembangkan di daerah tropis di seluruh dunia (Starr, Kim, dan Lloyd, 2003). Berdasarkan hasil penelitian dari Matsunami, Takamori, Shinzato, Aramoto, Kondo, Otsuka, dkk. (2006),M. tanariusdilaporkan memiliki beberapa kandungan glikosida yaitu macarangiosida A, macarangiosida B, macarangiosida C, macarangiosida D, dan malofenol B. Macarangiosida A, macarangiosida B, macarangiosida C, dan malofenol B menunjukkan aktivitas penangkapan radikal terhadap DPPH. Penelitian terbaru dari Matsunami, Otsuka, Kondo, Shinzato, Kawahata, Yamaguchi, dkk, (2009) melaporkan kandungan lignan glukosida yang diisolasi dari ekstrak metanol daunM. tanarius mempunyai aktivitas antioksidan terhadap penangkapan DPPH. Phommart, Pakawadee, Nitirat, Somsak, dan Somyote (2005) menyebutkan bahwa dalam daun M.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
tanarius terdapat tanariflavanon C, dan tanariflavanon D, nymphaeol A, nymphaeol B, nymphaeol C, yang sudah terbukti sebagai senyawa antioksidan
dalam menghambat radikal DPPH dan sebagai agen antiinflamasi pada uji siklooksigenase-2.
Parasetamol merupakan obat analgesik yang dikenal di masyarakat sebagai obat yang paling aman. Parasetamol sangat dikenal di masyarakat karena adanya catatan yang menyebutkan bahwa parasetamol merupakan obat yang lebih aman dari aspirin. Sekarang ini, parasetamol dipertimbangkan sebagai obat analgesik yang paling aman diantara semua analgesik yang ada (Madan, 1977). Akan tetapi, bila parasetamol diberikan dalam jumlah melebihi dosis terapeutik parasetamol diubah dalam tubuh menjadi NAPQI, suatu metabolit parasetamol yang bersifat toksik. Munculnya NAPQI akan merangsang terjadinya kerusakan pada hati (Forrest, 2006). Karena sifatnya yang dapat merusak hati pada penggunaan yang berlebihan maka parasetamol digunakan sebagai senyawa model untuk menggambarkan bagaimana kerusakan hati yang terjadi pada penelitian ini.
Adanya kandungan M. tanarius sebagai senyawa antioksidan baik dari ekstrak metanol dan ekstrak n-heksan dan kloroform, menunjukkan kandungan M. tanarius berpotensi untuk menghambat oksidasi parasetamol menjadi NAPQI
3
Pada penelitian ini digunakan bentuk sediaan infusa karena pada penelitian Matsunami dkk, (2006) dilaporkan bahwa senyawa antioksidan dari daun M. tanarius dapat diperoleh dari ektrak metanol yang merupakan pelarut polar. Oleh karena itu, diharapkan dengan menggunakan air sebagai pelarut infusa, diharapkan dapat diperoleh senyawa antioksidan pula. Selain alasan di atas, proses pembuatan infusa yang relatif cepat dan sederhana menjadi dasar pemilihan sediaan infusa.
1. Perumusan masalah
Berdasarkan latar belakang tersebut muncul permasalahan sebagai berikut: a. Apakah pemberian infusa daun M. tanarius dapat memberi efek
hepatoprotektif pada tikus jantan terinduksi parasetamol?
b. Berapakah dosis pemberian infusa daun M. tanarius yang dapat menimbulkan efek hepatoprotektif pada tikus jantan terinduksi parasetamol?
2. Keaslian penelitian
Penelitian yang menggunakan M. tanarius pernah dilakukan oleh Phommart dkk, (2005) dan Matsunami dkk, (2006, 2009). Phommart dkk, (2005) melaporkan kandungan tanaman M. tanarius berupa tanariflavanon B, tanariflavanon C, tanariflavanon D, nymphaeol A, nymphaeol B, nymphaeol C, blumenol A dan blumenol B. Matsunami dkk, (2006, 2009) melaporkan adanya
macarangiosida A, macarangiosida B, macarangiosida C, dan malofenol B yang mempunyai aktivitas antioksidan pada tanamanM. tanarius.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Sepanjang pengetahuan penulis, penelitian ini berbeda dengan penelitian-penelitian sebelumnya karena penelitian-penelitian ini melihat aspek lain, yakni kemampuan infusa daun M. tanarius dalam menurunkan aktivitas serum Alanine Aminotransferase (ALT) dan serum Aspatartate Aminotransferase (AST) pada
kerusakan hati tikus jantan yang terinduksi parasetamol.
3. Manfaat penelitian
a. Manfaat teoritis
Penelitian ini diharapkan dapat memberikan sumbangan bagi ilmu pengetahuan khususnya bidang kefarmasian tentang efek hepatoprotektif infusa daunM. tanariusdengan mekanisme penurunan serum ALT dan AST.
b. Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi tentang alternatif obat hepatitis baru bagi masyarakat.
B. Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. Membuktikan bahwa pemberian infusa daun M. tanariusdapat menimbulkan efek hepatoprotektif pada tikus jantan terinduksi parasetamol.
5
BAB II
PENELAAHAN PUSTAKA
A. TanamanMacaranga tanariusL.
1. Sinonim
Ricinus tanarius L. (Wagner, Herbst, dan Sohmer, 1999), Macaranga molliuscula Kurz, Macaranga tomentosa Druce, Mappa tanarius Blume (World
Agroforestry Centre, 2002).
2. Nama daerah
Pohon senu, mara, tutup merah, sapat (Anonim, 2010).
3. Taksonomi
Kingdom :Plantae Subkingdom :Tracheobionta Divisio :Spermatophyta Sub-Divisi :Magnoliophyta Classis :Magnoliopsida Sub-classis :Rosidae
Ordo :Euphorbiales
Familia :Euphorbiaceae
Genus :Macaranga
Spesies :Macaranga tanariusL. (Anonim, 2010).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
4. Penyebaran
M. tanariustersebar di hampir seluruh daerah tropis di dunia, antara
lain: Australia, Brunei, Kamboja, Cina, Indonesia, Jepang, Laos, Malaysia, Myanmar, Papua Nugini, Filipina, Taiwan, Thailand, dan Vietnam (World Agroforestry Centre, 2002).
5. Morfologi
Tanaman pohon dengan tinggi sekitar 4-20 m, daun berwarna hijau dengan bentuk jantung dan pangkal daun berbentuk bulat, panjang petiole 6-25 cm, kelopak bunga berwarna hijau hingga hijau kekuningan, kepala sari berbentuk tetrahecal, tangkai putik berukuran 5-8 mm, kapsul 2-3 ruang dengan diameter 10-12 mm, ditutupi dengan kelenjar lilin yang halus (Wagner dkk., 1999).
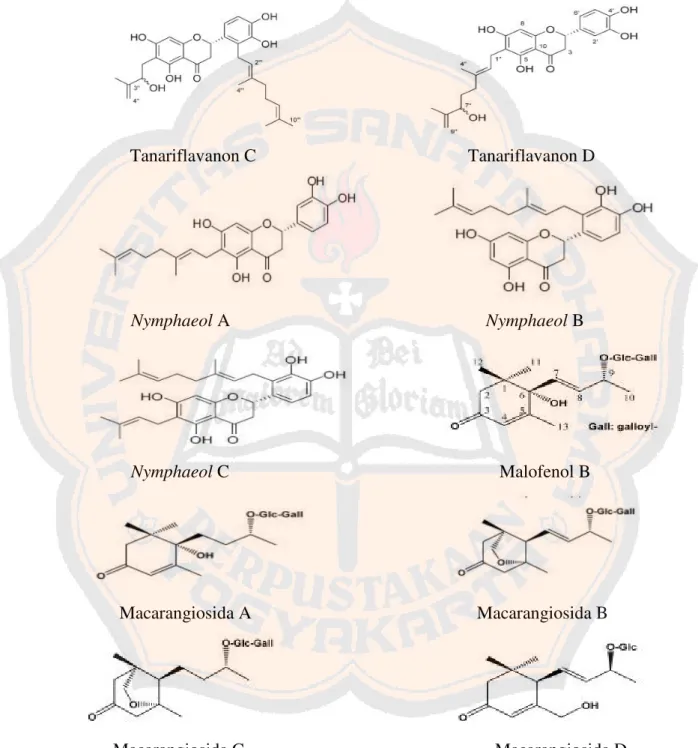
6. Kandungan
Dari daun M. tanarius dilaporkan dan diidentifikasi bahwa ditemukan tiga kandungan senyawa baru yaitu tanarifuranonol, tanariflavanon C, dan tanariflavanon D bersama dengan tujuh kandungan yang telah diketahui yaitunymphaeolA,nymphaeolB,nymphaeolC,tanariflavanoneB, blumenolA (vomifoliol),blumenol B (7,8dihydrovomifoliol, danannuionone
7
Sturktur senyawa yang terdapat dalam daun M. tanarius dapat dilihat pada gambar 1.
Tanariflavanon C Tanariflavanon D
NymphaeolA NymphaeolB
NymphaeolC Malofenol B
Macarangiosida A Macarangiosida B
Macarangiosida C Macarangiosida D
Gambar 1. Struktur senyawa dalam daun M. tanarius (Phommart dkk., 2005) dan (Matsunami dkk., 2006).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
7. Khasiat dan kegunaan
Berdasarkan penelitian yang dilakukan oleh Phommart dkk., (2005), dekok akar M. tanarius sudah digunakan di Thailand sebagai antipiretik dan antitusif, akar kering digunakan sebagai agen emetik, dan daun segarnya dapat digunakan sebagai antiinflamasi.
B. Hati
1. Anatomi fisiologi hati
Hati merupakan kelenjar terbesar dan salah satu yang terumit dalam tubuh manusia dengan berat rata-rata sekitar 1500 g atau sekitar 2% dari berat badan orang dewasa normal. Bentuk hati menyesuaikan struktur di sekitarnya. Bagian atas hati berbentuk cembung dan terletak di bagian kanan bawah diafragma dan sebagian di sebelah kiri bawah. Bagian bawah hati berbentuk cekung dan melindungi pankreas, ginjal kanan, lambung, dan usus (Price dan Wilson, 2005).
9
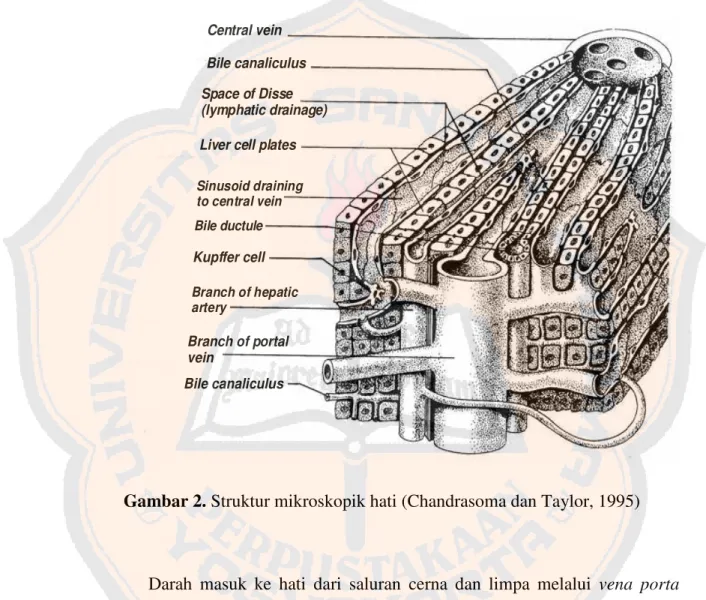
vena porta dan arteria hepatika. Sebagai pembatas sinusoid terdapat sel Kupffer, yaitu sel yang berfungsi menelan bakteri dan benda asing dalam darah (Price dan Wilson, 2005). Gambaran dari bagian-bagian hati dapat dilihat pada gambar 2.
Central vein
Gambar 2.Struktur mikroskopik hati (Chandrasoma dan Taylor, 1995)
Darah masuk ke hati dari saluran cerna dan limpa melalui vena porta hepatica dan dari aorta melaluiarteria hepatica. Darah dari vena yang masuk ke
hati berkisar duapertiga dan darah yang berasal dari arteri berkisar sepertiga dari jumlah seluruh darah yang masuk ke hati. Jumlah total darah yang masuk ke hati setiap menitnya kurang lebih 1500 mL (Price dan Wilson, 2005).
Hati mempunyai peranan yang penting dalam mempertahankan hidup, penting pula dalam hampir setiap metabolisme dalam tubuh dan bertanggung
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
jawab dalam 500 aktivitas yang berbeda. Fungsi utama dari hati adalah untuk membentuk dan mengekresi empedu. Selain itu hati berfungsi untuk metabolisme protein, lemak dan karbohidrat. Fungsi metabolisme lainnya adalah untuk penyimpanan vitamin, besi, dan tembaga, konjugasi dan eksresi steroid adrenal, dan detoksifikasi beberapa senyawa eksogen dan endogen. Di hati, fungsi detoksifikasi dilakukan oleh enzim hati dengan cara oksidasi, hidrolisis, reduksi, atau konjugasi senyawa-senyawa berhaya bagi tubuh kemudian mengubahnya menjadi bentuk yang tidak aktif (Price dan Wilson, 2005).
Peran penting hati dalam eliminasi obat adalah dengan memetabolisme obat induk dan merubahnya menjadi senyawa metabolit. Kapasitas dari hati untuk mengubah obat induk menjadi metabolit sangat dipengaruhi oleh aktivitas enzim pemetabolisme yang terdapat pada retikulum endoplasma halus dan sitosol pada hepatosit, jumlah protein pengikat obat di dalam darah yang akan mempengaruhi jumlah obat bebas yang tersedia untuk kemudian dibawa ke hepatosit, dan aliran darah di hati yang membawa obat ke hepatosit (DiPiro, Robert, Gary, Gary, Barbara, Michael, 2008).
2. Kerusakan sel-sel hati
Kerusakan sel hati dibagi menjadi dua, yakni: a) Kerusakan sel hati akut
11
adalah hipokalemia), enselophati hati, sindrom hepatorenal, dan kenaikan serum enzim (ALT, LDH, AST) pada kasus terjadinya nekrosis hati (Chandrasoma dan Taylor, 1995).
b) Kerusakan sel hati kronik
Kerusakan sel hati kronik biasanya merupakan hasil dari sirosis yang merupakan tahap lanjut dari nekrosis, fibrosis, dan regenerasi nodular. Efek dari kerusakan sel hati kronik dapat digambarkan sebagai berikut:
(1) penurunan sintesis albumin yang menyebabkan nilai serum albumin yang rendah dan edema.
(2) penurunan jumlah protombin dan faktor VII, IX, dan X yang menyebabkan terjadinya perdarahan.
(3) hipertensi portal, yakni kenaikan tekanan darah pada vena porta di atas batas normal. Hipertensi porta dapat terjadi karena gangguan aliran darah dari sistem porta.
(4) enselophati hati dapat terjadi jika darah yang mengalir dari vena porta tidak melalui saluran yang seharusnya dan tidak melalui detoksifikasi hati.
(5) sindrom hepatorenal, yakni terjadinya gagal ginjal pada orang yang memiliki penyakit di hati.
(6) perubahan sistem endokrin karena terjadi penyimpangan metabolisme dari hormon-hormon tertentu (Chandrasoma dan Taylor, 1995).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Berdasarkan manifestasi klinis yang terjadi dan pola spesifik pada histopatologi, kerusakan sel hati dapat dibagi lebih lanjut menjadi:
a) nekrosis sentrolobuler
Sering terjadi pada induksi obat hepatotoksik yang bergantung pada dosis. Nekrosis sentrolobuler biasanya terjadi karena produksi metabolit beracun dari suatu senyawa. Kerusakan yang terjadi menyebar ke luar mulai dari tengah lobus.
b) steatonecrosis
Merupakan suatu kerusakan sel hati akut yang ditandai dengan penumpukan lemak pada sel-sel hati. Obat-obat dapat menyebabkan terjadinya steatonecrosis dengan cara mempengaruhi proses oksidasi asam lemak di dalam
mitokondria.
c) phospholipidosis
Merupakan akumulasi dari phospholipid sebagai pengganti asam lemak. fosfolipid biasanya menelan badan lisosom dari sel hati.
d) nekrosis hepatoselular tergeneralisasi
13
3. Hepatotoksin
Obat dan senyawa yang dapat menyebabkan kerusakan hati dibedakan menjadi dua, yaitu:
a. hepatotoksin teramalkan (tipe A).
Merupakan obat atau senyawa yang bila diberikan dapat mempengaruhi sebagian besar orang yang menelan senyawa tersebut dalam jumlah yang cukup untuk menimbulkan efek toksik. Hepatotoksin teramalkan bergantung kepada dosis pemberian. Contoh dari obat-obat tipe ini adalah Parasetamol, salisilat, tetrasiklin (Forrest, 2006).
b. hepatotoksin tak teramalkan (tipe B).
Merupakan obat atau senyawa yang tidak bersifat toksik pada hati tetapi jika diberikan kepada orang tertentu akan dapat menimbulkan efek toksik. Hepatotoksin jenis ini tidak bergantung pada dosis pemberian. Frekuensi terjadinya sangat jarang, hanya terjadi pada 1 : 1000 orang. Contoh obat-obat yang tipe ini adalah isoniazid, halothane, dan chlorpromazine (Forrest, 2006).
4. ALT dan AST
Kerusakan sel-sel hati dapat dilihat dari peningkatan serum aminotransferase secara signifikan yang mendahului terjadinya kenaikan jumlah bilirubin total dan alkaline phospatase. Kebanyakan dari kerusakan hati dapat terjadi satu tahun setelah pemaparan agen hepatotoksik (DiPiro dkk., 2008).
Saat terjadi nekrosis pada hepatosit, kebocoran pada associated plasma membrane dapat dideteksi secara biokimia dengan cara menganalisa plasma atau
serum untuk melihat enzim turunan sitosol yakni, lactate dehydrogenase (LDH),
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
alanine aminotransferase (ALT atau SGPT), aspartate aminotransferase (AST atau SGOT) (Casarett dan Doull, 1996). Beberapa enzim lain yang dapat digunakan sebagai penanda untuk mengetahui adanya kerusakan hati adalah enzim-enzim golongan hidrogenase seperti laktat dehidrogenase, glutamate dehidrogenase, isositrat dehidrogenase, dan malat dehidrogenase. Enzim-enzim tersebut jarang digunakan untuk mendeteksi kerusakan hati dan kurang sensitif dibandingkan kombinasi AST dan ALT (Hodgson dan Levi 2000). Enzim ALT lebih spesifik untuk organ hati karena proporsinya paling banyak berada pada organ ini dibanding organ tubuh lainnya (Edem dan Akpanabiatu, 2006).
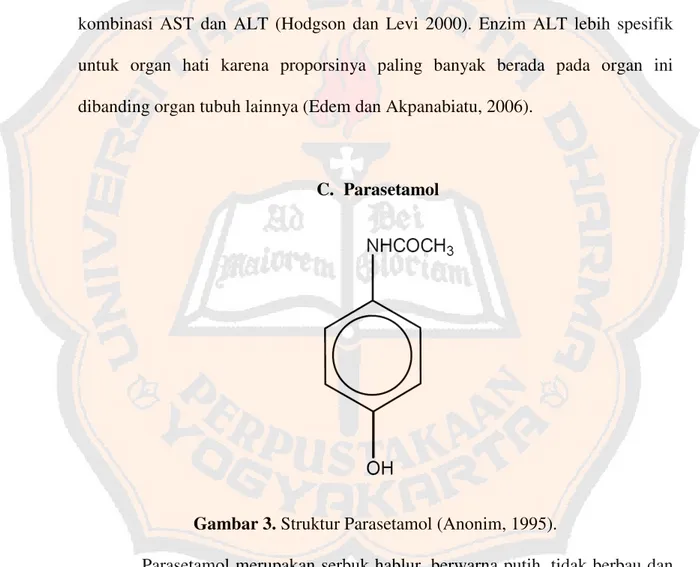
C. Parasetamol
Gambar 3.Struktur Parasetamol (Anonim, 1995).
15
Parasetamol merupakan obat analgesik yang dikenal di masyarakat sebagai obat yang paling aman. Parasetamol sangat dikenal di masyarakat karena adanya catatan yang menyebutkan bahwa parasetamol merupakan obat yang lebih aman dari aspirin. Sekarang ini, parasetamol dipertimbangkan sebagai obat analgesik yang paling aman diantara semua analgesik yang ada (Madan, 1977).
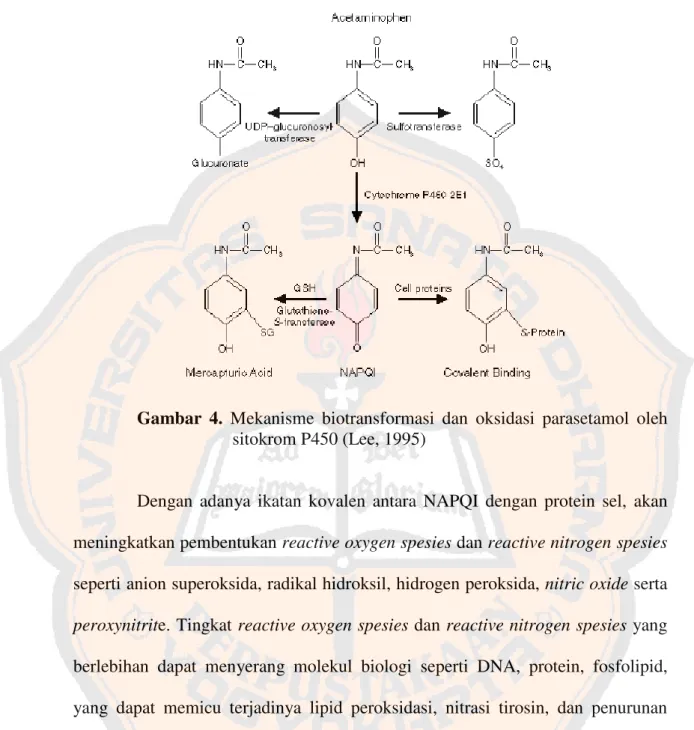
Penggunaan parasetamol pada dosis terapeutik secara umum sangat aman, tetapi pada penggunaan yang overdosis, akan sangat beresiko terjadi hepatotoksisitas. Pada dosis terapeutik, parasetamol dimetabolisme dengan cara konjugasi menjadi senyawa dengan kandungan glukoronida dan sulfat yang kemudian dikeluarkan melalui urin. Sebagian kecil (5-10%) parasetamol dioksidasi oleh mixed-function enzymes menjadi metabolit yang sangat reaktif yakni N-acetyl-p-benzoquinoneimine (NAPQI). Penggunaan parasetamol yang berlebihan dapat menyebabkan nekrosis sentrolobuler dan bahkan kegagalan hati baik pada manusia maupun hewan uji (Gujral, Tamara, Anwar, Mary, dan Hartmut , 2002). Pada keadaan overdosis, jalur konjugasi akan jenuh dan jumlah parasetamol yang dioksidasi menjadi semakin banyak. Hasilnya glutathione (GSH) simpanan di hati menjadi semakin habis dan hati menjadi tidak dapat menonaktifkan NAPQI. Jumlah NAPQI yang berlebihan dapat berikatan kovalen dengan sel hati yang dapat menyebabkan terjadinya nekrosis (Forrest, 2006). Berikut akan digambarkan mekanisme biotransformasi dan oksidasi parasetamol oleh sitokrom P450:
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Gambar 4. Mekanisme biotransformasi dan oksidasi parasetamol oleh sitokrom P450 (Lee, 1995)
Dengan adanya ikatan kovalen antara NAPQI dengan protein sel, akan meningkatkan pembentukanreactive oxygen spesiesdanreactive nitrogen spesies seperti anion superoksida, radikal hidroksil, hidrogen peroksida, nitric oxide serta peroxynitrite. Tingkat reactive oxygen spesies dan reactive nitrogen spesies yang
17
D. Infusa
1. Definisi
Infusa didefinisikan sebagai sediaan cair yang dibuat dengan mengekstraksi simplisia nabati dengan air pada suhu 90°C selama 15 menit (Anonim, 1995).
2. Pembuatan
Infusa dapat dibuat dengan cara mencampur simplisia dengan derajat halus yang sesuai dalam panci dengan air secukupnya, panaskan di atas tangas air selama 15 menit terhitung mulai suhu mencapai 90°C sambil berkali-kali diaduk. Serkai selagi panas melalui kain flannel, tambahkan air panas secukupnya melalui ampas hingga diperoleh volume infus yang dikehendaki (Anonim, 1995).
E. Landasan teori
Pada keracunan parasetamol, telah diketahui bahwa yang menyebabkan terjadinya nekrosis bukanlah karena senyawa induk yang ada, melainkan karena metabolit aktif (NAPQI) yang terbentuk. Pada penggunaan dosis terapeutik parasetamol, NAPQI akan didetoksifiksi dengan efektif oleh GSH dengan cara pembentukan konjugasi parasetamol-GSH. Pada penggunaan parasetamol yang melebihi dosis terapeutik, terjadi penurunan GSH hingga sebesar 90 %, dan sebagai hasilnya, NAPQI akan berikatan dengan gugus sistein pada protein (James, Philip, dan Jack, 2003)..
Pada pembentukan NAPQI karena overdosis parasetamol, konsentrasi GSH pada sentrilobular sel hati akan sangat rendah. Rendahnya konsentrasi GSH
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
akan menyebabkan enzim utama yang berperan dalam detoksifikasi peroksidase (enzim GSH peroksidase) yang bekerja dengan tidak efisien. Sedangkan pada saat terjadinya pembentukan NAPQI, terbentuk pula anion superoksida yang dapat mengarah pada pembentukan hidrogen peroksida. Mekanisme ini dapat menyebabkan meningkatnya toksisitas dari parasetamol (James dkk., 2003).
Kerusakan sel-sel hati dapat dilihat dari peningkatan serum aminotransferase secara signifikan yang mendahului terjadinya kenaikan jumlah bilirubin total dan alkaline phospatase (ALP). Kebanyakan dari kerusakan hati dapat terjadi satu tahun setelah pemaparan agen hepatotoksik (DiPiro dkk., 2008).
Hasil penelitian dari Matsunami dkk., (2006) melaporkan kandungan dari M. tanarius, yaitu macarangiosida A, macarangiosida B, macarangiosida C, dan
malofenol B yang diisolasi dari ekstrak metanol daun M. tanarius menunjukkan aktivitas penangkapan radikal terhadap DPPH yang berpotensi sebagai zat antioksidan. Macarangiosida A, dan malofenol B memiliki ikatanα-βunsaturated. Kemungkinan pada atom C-β inilah radikal bebas terikat karena sifat ikatan α-β
unsaturatedyang khas. Senyawa-senyawa antioksidan yang diperoleh dari ekstrak
polar tersebut diharapkan dapat meningkatkan sintesis GSH, menghambat serta mengurangi hasil proses oksidasi pada metabolisme parasetamol menjadi NAPQI, sehingga ketoksikan pada hati dapat dihindari.
F. Hipotesis
19
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni dengan rancangan penelitian acak lengkap pola searah.
B. Variabel Penelitian dan Definisi Operasional
1. Variabel penelitian
Variabel-variabel yang ada dalam penelitian ini, antara lain: a. Variabel bebas:
Dosis infusa daun M. tanarius, dosis infusa daun M. tanarius, adalah volume tertentu (ml) infusa daunM. tanarius, tiap kg berat badan subjek uji yang digunakan.
b. Variabel tergantung
Efek hepatoprotektif infusa daun M. tanarius, terhadap sel hati tikus terinduksi parasetamol ditandai dengan tolok ukur kuantitatif berupa penurunan aktivitas serum ALT dan AST.
c. Variabel pengacau terkendali
1. Kondisi hewan uji, yakni tikus dengan galur Wistar, berjenis kelamin jantan, berat badan 150 hingga 250 g, umur 2-3 bulan.
2. Frekuensi pemberian infusa daun M. tanarius, satu kali sehari selama enam hari berturut-turut, dengan waktu pemberian yang sama.
3. Cara pemberian obat pada tikus dilakukan secara per oral.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
4. Bahan uji yang digunakan berupa daunM. tanarius, yang berasal dari Kebun Tanaman Obat Fakultas Farmasi Universitas Sanata Dharma dan diambil pada tanggal 10 Agustus 2010.
d. Variabel pengacau tak terkendali
1. Keadaan patologi dari tikus jantan galur wistar yang digunakan.
2. Definisi operasional
a. Infusa daunM. tanarius100%.
Infusa serbuk kering daun M. tanarius 100% didapatkan dengan cara menginfudasi 100,0 g serbuk kering daunM. tanariusdalam 100,0 ml air pada suhu 90°C selama 15 menit.
b. Efek hepatoprotektif infusa daunM. tanarius.
Didefinisikan sebagai kemampuan infusa daun M. tanariusuntuk melindungi hepar dari hepatotoksin.
C. Bahan Penelitian
Penelitian ini menggunakan bahan uji sebagai berikut:
1. Hewan uji yang digunakan berupa tikus jantan galur Wistar dengan umur 2-3 bulan dan berat badan 150 hingga 250 g yang diperoleh dari Laboratorium Imono Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Daun M. tanarius yang diperoleh dari Kebun Tanaman Obat Fakultas Farmasi Universitas Sanata Dharma Yogyakarta pada 10 Agustus 2010. 3. Bahan hepatotoksin yang digunakan adalah suspensi parasetamol
21
Laboratorium Farmakologi-Toksikologi Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
4. Pelarut untuk pembuatan sediaan uji adalah air suling yang diperoleh dari Laboratorium Farmakologi-Toksikologi Fakultas Farmasi Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
5. Blanko pengujian ALT dan AST menggunakan aqua bidestilata yang diperoleh dari PT. IKAPHARMINDO PUTRAMAS, Jakarta
6. Reagen serum ALT
Reagen serum yang digunakan adalah reagen serum ALT diasys. Komposisi dan konsentrasi dari reagen serum ALT adalah sebagai berikut:
R1: TRIS pH 7.15 140 mmol/L
L-Alanine 700 mmol/L
LDH (lactate dehydrogenase) ≥2300 U/L
R2: 2-Oxoglutarate 85 mmol/L
NADH 1 mmol/L
Pyridoxal-5-phosphate FS:
Good’s buffer pH 9.6 100 mmol/L
Pyridoxal-5-phosphate 13 mmol/L
7. Reagen serum AST
Reagen serum yang digunakan adalah reagen serum AST diasys. Komposisi dan konsentrasi dari reagen serum AST adalah sebagai berikut:
R1: TRIS pH 7.65 110 mmol/L
L-Aspartate 320 mmol/L
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
MDH (malate dehydrogenase) ≥800U/L LDH (lactate dehydrogenase) ≥1200 U/L
R2: 2-Oxoglutarate 65 mmol/L
NADH 1 mmol/L
Pyridoxal-5-phosphate FS:
Good’s buffer pH 9.6 100 mmol/L
Pyridoxal-5-phosphate 13 mmol/L
D. Alat Penelitian
1. Alat-alat pembuatan serbuk kering daun M. tanarius antara lain: oven, mesin penyerbuk, timbangan elektrik.
2. Alat-alat pembuatan infusa daun M. tanarius antara lain: panci lapis alumunium,heater, termometer, gelas ukur,Stopwatch, timbangan elektrik, kain flanel.
23
E. Tata Cara Penelitian
1. Determinasi daunM. tanarius
Tanaman M. tanarius yang digunakan dalam penelitian ini telah dideterminasi dengan cara mencocokkan ciri-ciri tanaman yang ada dengan buku acuan (Koorders dan Valeton, 1918) hingga ke tingkat spesies. Determinasi dilakukan oleh Bapak Ign. Y. Kristio Budiasmoro, M.Si., Dosen Jurusan Pendidikan Biologi, Fakultas JP MIPA, Universitas Sanata Dharma Yogyakarta.
2. Pengumpulan bahan uji
Penelitian ini menggunakan daun tanaman M. tanarius sebagai bahan uji. Daun yang dipilih adalah daun yang masih segar dan berwarna hijau. Daun yang dipetik hanya berasal dari Kebun Tanaman Obat Fakultas Farmasi Universitas Sanata Dharma pada 10 Agustus 2010.
3. Pembuatan serbuk
Daun M. tanarius yang telah dipetik dicuci dan dikering anginkan. Setelah kering, daun dimasukkan ke dalamovendengan suhu 50°C selama 24 jam. Daun yang sudah kering kemudian diserbuk dan diayak dengan ayakan no. 50.
4. Pembuatan infusa daunM. tanarius
Untuk membuat infusa daun M. tanarius dengan konsetrasi 100%, Serbuk kering daun M. tanarius diambil sejumlah 100,0 g ditambahkan dengan 150,0 mL air. Campuran ini kemudian dipanaskan di atas heaterpada suhu 90°C selama 15 menit. Waktu 15 menit dihitung ketika suhu pada
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
campuran mencapai 90°C. Jika air yang diperoleh kurang, maka air dapat ditambahkan selagi panas melalui ampas rebusan hingga volume yang diinginkan tercapai.
5. Pembuatansuspending agentCMC Na 1%
CMC Na ditimbang seksama hingga 1,0 g, kemudian dimasukkan ke dalam air mendidih, biarkan mengembang lalu diaduk hingga larut, tambahkan air hingga 100,0 ml.
6. Pembuatan suspensi parasetamol konsentrasi 25%
Suspensi parasetamol dibuat dengan cara mencampurkan 25,0 g parasetamol dengan 100,0 mlsuspending agent(CMC Na 1%).
7. Uji pendahuluan
Uji yang dilakukan sebelum penelitian ini dilaksanakan adalah:
a) penetapan dosis hepatotoksik parasetamol.
Dosis hepatotoksik parasetamol yang digunakan untuk menginduksi kerusakan hati pada tikus jantan galur wistar diperoleh dari penelitian Linawati, Apriyanto, Susanti, Wijayanti, dan Donatus (2006) yang melaporkan bahwa pada pemberian parasetamol dosis 2,5 g/kg BB secara peroral sudah dapat menginduksi terjadinya kerusakan hati tikus.
b) penetapan waktu pencuplikan darah
25
ke 24 dan kelompok II akan diambil darahnya pada jam ke 48 dan kelompok III diambil darahnya 72 jam setelah pemejanan parasetamol.
8. Pengelompokan dan perlakuan hewan uji
Sebanyak 30 tikus jantan dibagi secara acak ke dalam 6 kelompok. Masing-masing kelompok terdiri lima ekor tikus. Tikus kelompok I diberi aquadest dosis 10 g/kgBB selama enam hari berturut-turut sebagai kontrol negatif. Tikus kelompok II diberi Parasetamol dosis 2,5 g/kgBB sebagai kontrol hepatotoksik parasetamol. Tikus kelompok III diberi infusa daun M. tanarius dosis 10 g/kgBB selama enam hari beturut-turut sebagai kontrol
negatif infusa daun M. tanarius. Tikus kelompok IV sampai VI diberi infusa daun M. tanarius berturut-turut dengan dosis 10 g/kgBB; 5 g/kgBB; 2,5 g/kgBB selama enam hari berturut-turut dan pada hari ke-7 diberi parasetamol dosis 2,5 g/kgBB, kemudian pada kelompok I hingga VI setelah 48 jam diambil darahnya dari sinus obitalis untuk ditetapkan aktivitas serum ALT dan AST.
9. Pembuatan serum
Darah diambil melalui sinus orbitalis mata tikus, kemudian ditampung dalam tabung Effendorf yang telah ditetesi dengan heparin. Darah kemudian disentrifugasi selama 10 menit dengan kecepatan 3500 rpm. Bagian supernatan kemudian diambil.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
10. Pengukuran serum ALT dan AST
Pengukuran aktivitas serum ALT dan AST dilakukan pada panjang gelombang 340 nm dengan suhu 37°C. Aktivitas serum ALT dan AST dinyatakan dalam u/l. Pengukuran serum ALT dan AST dilakukan di laboratorium Farmakologi-Toksikologi, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
F. Tata Cara Analisis Hasil
1. Penetapan dosis toksik parasetamol
Serum ALT dan AST yang diperoleh dianalisis dengan uji Kolmogorov Smirnov untuk melihat distribusi data tiap kelompok. Jika
didapat distribusi data yang normal maka analisis dilanjutkan dengan analisis pola searah (One Way ANOVA) dengan taraf kepercayaan 95% yang dilanjutkan dengan uji Scheffe untuk mengetahui perbedaan masing-masing kelompok. Tetapi jika didapat distribusi yang tidak normal, analisis dilanjutkan dengan analisis non parametrik, yaitu uji Kruskal Wallis untuk melihat perbedaan aktivitas serum ALT dan AST antar kelompok. Selanjutnya, diuji dengan ujiMann Whitneyuntuk melihat perbedaan uji tiap kelompok.
2. Penetapan waktu pencuplikan darah
Data serum ALT dan AST dianalisis dengan uji Kolmogorov Smirnov untuk melihat distribusi data tiap kelompok. Jika didapatkan
27
3. Perlakuan hewan uji
Data serum ALT dan AST dianalisis dengan uji Kolmogorov Smirnov untuk melihat distribusi data tiap kelompok. Jika didapat distribusi
normal maka analisis dilanjutkan dengan analisis pola searah pola searah (One Way ANOVA) dengan taraf kepercayaan 95% yang dilanjutkan dengan uji Scheffe untuk mengetahui perbedaan masing-masing kelompok. Tetapi jika didapat distribusi yang tidak normal, analisis dilanjutkan dengan analisis non parametrik, yaitu uji Kruskal Wallis untuk melihat perbedaan aktivitas serum ALT dan AST antar kelompok. Selanjutnya, diuji dengan uji Mann Whitneyuntuk melihat perbedaan uji tiap kelompok.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
28
BAB IV
HASIL DAN PEMBAHASAN
A. Penyiapan Bahan
1. Hasil determinasi tanaman
Penelitian ini menggunakan serbuk daun yang berasal dari tanaman M.
tanarius. Tujuan dari determinasi tanaman adalah untuk memastikan bahwa bagian dari tanaman yang digunakan memang benar berasal dari tanaman M. tanarius, sehingga tidak terjadi kesalahan dalam penyiapan bahan yang akan digunakan. Determinasi dilakukan di Laboratorium Farmakognosi-Fitokimia Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Determinasi dilakukan dengan mencocokkan kesamaan ciri tanaman dari batang, daun, bunga, buah dari tanaman dengan buku acuan (Koorders dan Valeton, 1918) hingga ke tingkat spesies. Hasil determinasi membuktikan bahwa tanaman yang diuji memang benarM. tanarius.
2. Penetapan kadar air serbuk daunM. tanarius
Tujuan dilakukan penetapan kadar air adalah untuk memenuhi persyaratan serbuk yang baik, yakni kurang dari 10% (Anonim, 1995). Penetapan kadar air serbuk daun M. tanarius dilakukan dengan metode Gravimetri dengan menggunakan alat
29
kadar air sebesar 8,18%. Dari pengujian ini, menunjukkan bahwa kadar air sebuk daun M. tanarius telah memenuhi persyaratan kadar air, yaitu kurang dari 10% (Anonim, 1995).
B. Uji Pendahuluan
1. Penentuan dosis hepatotoksik parasetamol
Tujuan dari penentuan dosis hepatotoksik dari parasetamol adalah untuk menentukan dosis parasetamol yang dapat menyebabkan kerusakan pada hati tikus. Hal ini dapat diketahui dari adanya peningkatan aktivitas ALT-serum, minimal 10 kali lipat terhadap kontrol negatif (Ladoangin, 2004). Linawati, dkk (cit. Bergmeyer dan Bernt, 1971) melaporkan bahwa kerusakan hati, juga terlihat dari peningkatan AST-serum 10-20 kali lipat dari nilai normal.
Pada penelitian ini, dosis hepatotoksik diperoleh dari penelitian Linawati, dkk (2006) yang melaporkan bahwa pada dosis 2,5 g/kgBB tikus sudah menimbulkan efek hepatotoksik.
2. Penentuan waktu pencuplikan darah
Penentuan waktu pencuplikan darah dilakukan untuk melihat kehepatotoksikan parasetamol dosis 2500 mg/kgBB mencapai maksimal. Hal ini ditunjukkan oleh aktivitas ALT-serum tertinggi pada selang waktu tertentu. Parasetamol dosis 2,5 g/kgBB diujikan pada tikus jantan dengan selang waktu pengambilan cuplikan darah 24 jam, 48 jam dan 72 jam. Hasil uji ini berupa aktivitas serum ALT yang dapat dilihat pada tabel I serta gambar 5 dan aktivitas serum AST yang dapat dilihat pada tabel III serta gambar 6 berikut.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
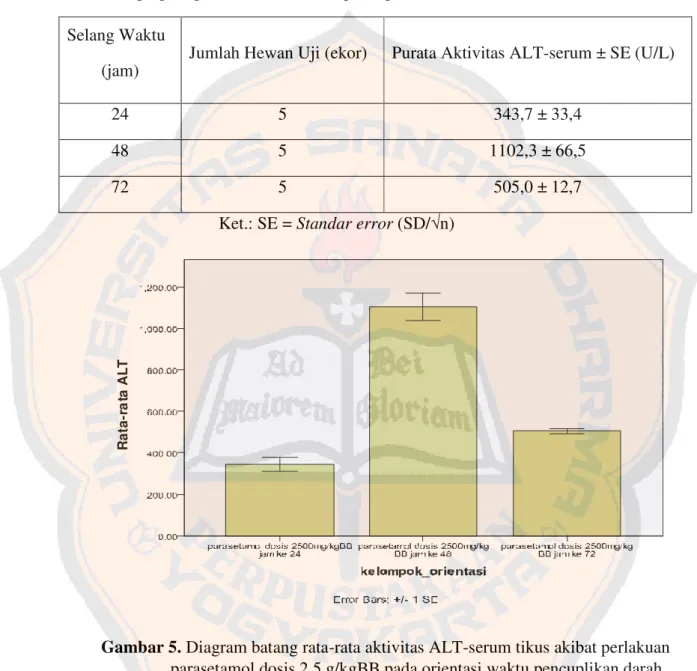
Tabel I.Rata-rata aktivitas ALT-serum tikus akibat perlakuan parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah
Selang Waktu (jam)
Jumlah Hewan Uji (ekor) Purata Aktivitas ALT-serum ± SE (U/L)
24 5 343,7 ± 33,4
48 5 1102,3 ± 66,5
72 5 505,0 ± 12,7
Ket.: SE =Standar error(SD/√n)
R
a
ta
-r
a
ta
A
L
T
Gambar 5.Diagram batang rata-rata aktivitas ALT-serum tikus akibat perlakuan parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah
31
antar kelompok maka dilanjutkan dengan uji Scheffe. Data dan analisisnya dapat dilihat di tabel II.
Tabel II. Hasil uji Scheffe aktivitas ALT-serum aktivitas ALT-serum tikus akibat perlakuan parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah
Selang waktu 24 jam 48 jam 72 jam
24 jam - B TB
48 jam B - B
72 jam TB B
-Keterangan :
B = Berbeda bermakna (p < 0,05) TB = Berbeda tidak bermakna (p > 0,05)
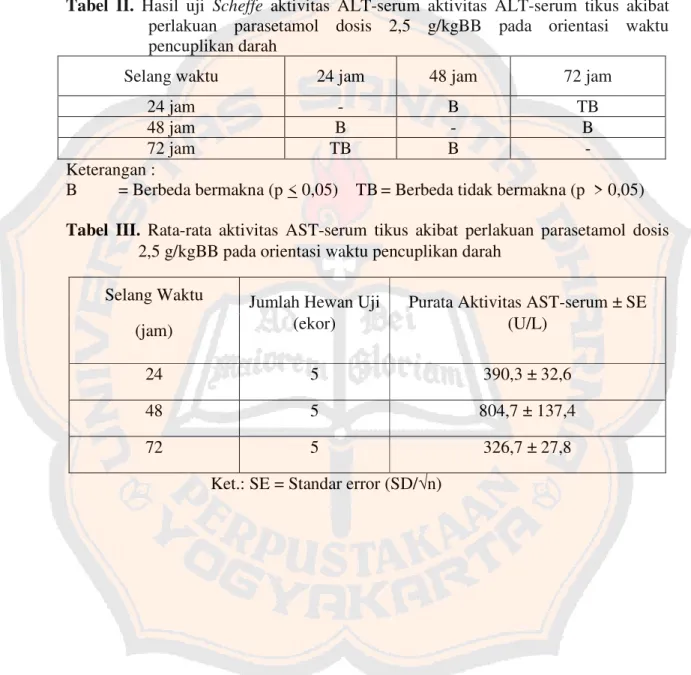
Tabel III. Rata-rata aktivitas AST-serum tikus akibat perlakuan parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah
Selang Waktu (jam)
Jumlah Hewan Uji (ekor)
Purata Aktivitas AST-serum ± SE (U/L)
24 5 390,3 ± 32,6
48 5 804,7 ± 137,4
72 5 326,7 ± 27,8
Ket.: SE = Standar error (SD/√n)
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
R
a
ta
-r
a
ta
A
S
T
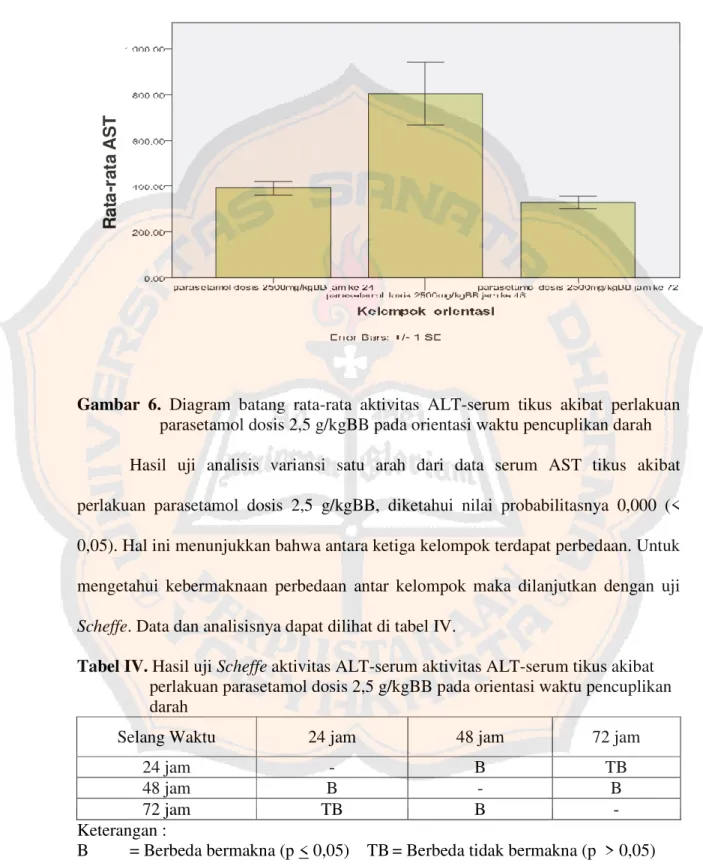
Gambar 6. Diagram batang rata-rata aktivitas ALT-serum tikus akibat perlakuan parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah Hasil uji analisis variansi satu arah dari data serum AST tikus akibat perlakuan parasetamol dosis 2,5 g/kgBB, diketahui nilai probabilitasnya 0,000 (< 0,05). Hal ini menunjukkan bahwa antara ketiga kelompok terdapat perbedaan. Untuk mengetahui kebermaknaan perbedaan antar kelompok maka dilanjutkan dengan uji
Scheffe. Data dan analisisnya dapat dilihat di tabel IV.
Tabel IV.Hasil ujiScheffeaktivitas ALT-serum aktivitas ALT-serum tikus akibat perlakuan parasetamol dosis 2,5 g/kgBB pada orientasi waktu pencuplikan darah
Selang Waktu 24 jam 48 jam 72 jam
24 jam - B TB
48 jam B - B
72 jam TB B
-Keterangan :
33
Hastuti, (cit. Pilichos, dkk, 2004) melaporkan nilai normal AST-serum dan ALT-serum padar tikus normal berturut-turut adalah 19,3-68,9 U/l dan 29,8-77,0 U/l. Berdasarkan tabel I, ternyata pengambilan darah pada jam ke 48 mencapai jumlah aktivitas ALT yang paling tinggi, yakni 1102,3 ± 66,5 U/l hal ini didukung pula dari tabel III yang menunjukkan aktivitas AST tertinggi pada jam ke 48 yang mencapai 804,7 ± 137,4 U/l. Dari gambar 5 dan gambar 6 dapat dilihat bahwa pada jam ke 48 terjadi peningkatan aktivitas serum ALT dan AST secara signifikan. Hal ini menunjukkan bahwa parasetamol memiliki efek hepatotoksik maksimal pada waktu ke-48 jam. Berdasarkan hasil uji, penelitian ini menggunakan waktu pencuplikan darah pada jam ke 48.
3. Penetapan lama preperlakuan infusaM. tanarius
Dalam penelitiannya, Ladoangin (2004) dalam penelitian efek hepatoprotektif jus buah apel hijau dan Linawati dkk (2006) dalam penelitian efek hepatoprotektif rebusan herba putri malu, menjelaskan bahwa praperlakuan pemberian jus buah apel hijau dan rebusan diberikan kepada kelompok hewan uji selama enam hari dan pada hari ke 7 diberikan parasetamol dosis hepatotoksik.
Penetapan waktu praperlakuan infusa daun M. tanarius didasarkan penelitian Ladoangin (2004) dan Linawati dkk (2006) yang mengikuti model pemberian praperlakuan selama 6 hari dan pada hari ke7 diberi parasetamol dosis 2,5 g/kgBB. Hal ini dikarenakan penelitian ini merupakan skrining awal untuk melihat efek
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
hepatoprotektif dari infusa daun M. tanarius sehingga hasil yang diperoleh dapat dibandingkan dengan penelitian-penelitian tentang hepatoprotektif yang sudah ada.
4. Penetapan dosis infusa daunM. tanarius
Tujuan dari penetapan dosis infusa M. tanarius adalah untuk menentukan besarnya dosis infusa daun M. tanarius yang akan digunakan dalam penelitian ini. Penentuan dosis infusa daun M. tanarius didasarkan pada konsentrasi maksimal infusa daun M. tanarius yang mampu dibuat dan volume maksimal infusa daun M. tanarius yang dapat dipejankan pada tikus jantan secara peroral. Dari orientasi diketahui bahwa konsentrasi tertinggi infusa daun M. tanarius yang dapat dibuat adalah 100%. Dari hasil ini, diperoleh dosis maksimal infusa daunM. tanariusadalah sebesar 10 g/kgBB. Kemudian ditentukan 3 tingkatan dosis infusa daunM. tanarius
35
C. Hasil uji efek hepatoprotektif Infusa DaunM. tanarius
Efek hepatoprotektif infusa daun M. tanarius dinilai dari penurunan aktivitas serum ALT dan serum AST. Aktivitas serum ALT dan AST dinyatakan dalam satuan U/l yang disajikan dalam bentuk purata ± SE yang tersaji dalam tabel V dan VI serta gambar 7 dan 8 berikut.
Tabel V.Pengaruh praperlakuan jangka panjang pemberian infusa daunM. tanarius
terhadap hepatotoksisitas parasetamol dilihat dari aktivitas ALT-serum
Kel. Perlakuan
I Kontrol Negatif Aquadest
10 g/kgBB 79,2 ± 5,3 - (-) 91,9
(B)
-II Kontrol Hepatotoksik
Parasetamol 2,5 g/kgBB 977,2 ± 85,2 (+) 1133,8 (B)
-
-III IDM 10 g/kgBB 59,8 ± 4,0 (-) 24,5(TB) (-) 93,8(B)
-IV IDM 10 g/kgBB +
Parasetamol 2,5 g/kgBB 356,2 ± 12,3 (+) 349,8 (B)
(-) 63,6(B) 63,6
V IDM 5 g/kgBB +
Parasetamol 2,5 g/kgBB 174,0 ± 17,1 (+) 119,7 (TB)
(-) 82,2(B) 82,2
VI IDM 2,5 g/kgBB +
Parasetamol 2,5 g/kgBB 720,2 ± 18,8 (+) 809,3 (B)
(-) 26,3(B) 26,3
Ket.: TB= berbeda tidak bermakna (p > 0,05) B=Berbeda Bermakna (p<0,05) IDM=Infusa Daun Macaranga
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
R
Gambar 7. Diagram batang rata-rata pengaruh praperlakuan jangka panjang pemberian infusa daun M. tanarius terhadap hepatotoksisitas parasetamol dilihat dari aktivitas ALT-serum
Tabel VI.Pengaruh praperlakuan jangka panjang pemberian infusa daunM. tanarius
terhadap hepatotoksisitas parasetamol dilihat dari aktivitas AST-serum
Kel. Perlakuan
I Kontrol Negatif Aquadest
10 g/kgBB 138,4 ± 4,9 - (-) 79,441
(B)
-II Kontrol Hepatotoksik
Parasetamol 2,5 g/kgBB 673,2 ± 110,4 (+) 386,4 (B)
-
-III IDM 10 g/kgBB 127,4 ± 10,5 (-) 7,9(TB) (-) 81,1(B)
-IV IDM 10 g/kgBB +
Parasetamol 2,5 g/kgBB 667,8 ± 58,1 (+) 382,5 (B)
(-) 0,8(TB) 0,8
V IDM 5 g/kgBB +
Parasetamol 2,5 g/kgBB 198,8 ± 16,9 (+) 43,6 (TB)
(-) 70,5(B) 70,5
VI IDM 2,5 g/kgBB +
Parasetamol 2,5 g/kgBB 856,0 ± 68,3 (+) 518,5 (B)
(+)27,2(TB) (-) 27,2
37
Gambar 8. Diagram batang rata-rata pengaruh praperlakuan jangka panjang pemberian infusa daun M. tanarius terhadap hepatotoksisitas parasetamol dilihat dari aktivitas AST-serum
1. Kontrol negatif (aquadest 10 g/kgBB)
Pengujian kelompok kontrol negatif aquadest bertujuan untuk melihat apakah penggunaan aquadest sebagai pelarut infusa daun M. tanarius
menyebabkan peningkatan serum ALT dan AST pada tikus jantan terinduksi parasetamol. Digunakan dosis aquadest sebesar 10 g/kgBB sesuai dengan dosis terbesar infusa daun M. tanarius dengan harapan hasil kelompok ini berlaku untuk kelompok praperlakuan infusa daun M. tanarius dari dosis terendah (2,5 g/kgBB) hingga dosis tertinggi (10 g/kgBB).
Hasil pengukuran aktivitas serum ALT dan AST yang diperoleh dari kelompok kontrol negatif ini tidak menunjukkan peningkatan aktivitas serum ALT dan AST yang signifikan dibanding nilai normal ALT dan AST dari
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
hasil penelitian Hastuti cit. Pilichos, dkk., (2004). Tabel V menunjukkan bahwa aktivitas serum ALT kontrol negatif adalah sebesar 79,2±5,3 U/l dan dari tabel VI dapat dilihat bahwa aktivitas AST sebesar 138,4±4,9 U/l. Hasil pengujian terhadap aktivitas serum ALT dan AST menunjukkan bahwa pemberian aquadest 10 g/kgBB pada tikus tidak menaikkan aktivitas serum AST dan ALT, artinya bila pada kelompok kontrol maupun perlakuan terjadi kenaikan serum ALT maupun AST itu bukan dikarenakan penggunaan aquadest sebagai pelarut.
Kelompok kontrol negatif nantinya akan dipakai sebagai dasar nilai aktivitas serum AST dan ALT normal pada penelitian ini.
2. Kontrol hepatotoksik parasetamol 2,5 g/kgBB
Parasetamol digunakan sebagai hepatotoksin karena parasetamol dalam jumlah yang melebihi dosis lazim dapat menyebabkan kerusakan hati yang khas, karenanya, parasetamol sering digunakan sebagai senyawa model kerusakan hati oleh induksi senyawa obat.
39
terdapat perbedaan yang bermakna antara kelompok kontrol hepatotoksik parasetamol dengan kelompok kontrol negatif.
Hasil pengukuran aktivitas serum ALT menunjukkan telah terjadi kerusakan sel hati tikus, sedangkan nilai serum AST yang meningkatnya belum mencapai 10 kali lipat dikarenakan kerusakan yang terjadi belum mencapai mitokondria, sehingga kenaikan serum AST belum terlalu tinggi.
Nilai kenaikan serum ALT dan AST pada kelompok kontrol hepatotoksik parasetamol dosis 2,5 g/kgBB pada penelitian ini akan digunakan sebagai dasar dalam melihat besarnya efek hepatoprotektif yang dimiliki oleh infusa daunM. tanariuspada kelompok praperlakuan.
3. Kontrol negatifM. tanariusdosis 10 g/kgBB
Kontrol negatif M. tanarius juga diuji untuk melihat bagaimana pengaruh pemberiannya terhadap aktivitas serum ALT dan AST. Pada tabel V terlihat bahwa tidak terjadi kenaikan aktivitas serum ALT yakni sebesar 59,8±4,0 U/l. Aktivitas ALT yang cenderung turun dibanding kontrol negatif ini setelah diuji menggunakan analisis variasi satu arah yang dilanjutkan dengan uji Scheffe ternyata menunjukkan perbedaan yang tidak bermakna. Aktivitas serum AST kontrol negatif pada tabel VI sebesar 127,4±10,5 U/l. Hasil ini tidak jauh berbeda dari kontrol negatif sebesar 138,4±4,9 U/l. Data aktivitas serum AST kemudian diuji secara statistik menggunakan analisis variasi satu arah dan dilanjutkan dengan ujiScheffe. Hasil yang diperolah dari uji statistik menunjukkan terdapat perbedaan tidak bermakna antara aktivitas
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
serum AST kontrol negatif aquadest dengan kontrol negatif infusa daun M. tanarius. Dapat disimpulkan bahwa pemberian infusa daun M. tanariusdosis 10 g/kgBB tidak menaikkan aktivitas serum ALT maupun AST. Artinya, bila terjadi peningkatan serum ALT maupun AST pada tikus semata-mata karena pengaruh dari parasetamol yang diberikan.
4. Kelompok perlakuan infusa daunM. tanariusdosis 10 g/kgBB, 5 g/kgBB, 2,5 g/kgBB pada tikus jantan galur Wistar terinduksi parasetamol 2,5 g/kgBB.
Kelompok IV adalah perlakuan infusa daun M. tanarius dosis 10 g/kgBB. Aktivitas serum ALT kelompok ini adalah sebesar 356,2±12,3 U/l. Aktivitas serum ALT kelompok IV bila dibandingkan dengan kelompok kontrol hepatotoksik parasetamol 2,5 g/kgBB mengalami penurunan sebesar 63,6 %. Perbedaan yang bermakna ditunjukkan secara statistik oleh kelompok perlakuan infusa daun M. tanarius10 g/kgBB terhadap kontrol hepatotoksik parasetamol 2,5 g/kgBB. Aktivitas serum ALT kelompok IV mengalami kenaikan sebesar 349,7 % bila dibandingkan dengan kelompok kontrol negatif aquadest 10 g/kgBB. Perbedaan yang bermakna terlihat antara kelompok IV dan kontrol negatif aquadest 10 g/kgBB setelah melalui uji statistik.
41
Perbedaan yang bermakna terlihat pada aktivitas serum AST kelompok IV dan kelompok kontrol negatif aquadest 10 g/kgBB setelah keduanya diuji secara statistik.
Kelompok IV memiliki efek hepatoprotektif sebesar 63,6% dilihat dari aktivitas serum ALT. Kelompok IV memiliki efek hepatoprotektif sebesar 0,8% jika dilihat dari aktivitas serum AST. Dibandingkan dengan kelompok V, kelompok VI memiliki efek hepatoprotektif yang lebih rendah. Hal ini kemungkinan karena antioksidan yang ada pada infusa daunM. tanariusdosis 10 g/kgBB terlalu jenuh, sehingga kemungkinan menjadi prooksidan yang justru mampu menyebabkan kerusakan pada sel hati tikus.
Kelompok V adalah kelompok perlakuan infusa daun M. tanarius
dosis 5 g/kgBB. Aktivitas serum ALT kelompok ini mengalami penurunan sebesar 82,2% dibandingkan kelompok kontrol hepatotoksik parasetamol 2,5 g/kgBB dilihat dari tabel V. Perbedaan yang bermakna antara kedua kelompok ini terlihat berdasarkan hasil uji statistik. Dibandingkan dengan kelompok kontrol negatif aquadest 10 g/kgBB, aktivitas serum ALT mengalami kenaikan sebesar 119,7%. Kedua kelompok ini berbeda tidak bermakna bila dilihat secara statistik, artinya kedua kelompok ini memiliki aktivitas serum ALT yang sama.
Kelompok V mengalami penurunan sebesar 70,5% dibandingkan dengan kelompok kontrol hepatotoksik parasetamol 2,5 g/kgBB bila dilihat dari aktivitas serum AST pada tabel VI. Perbedaan yang bermakna diantara
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
kedua kelompok ini terlihat setelah melalui uji statistik. Aktivitas serum AST kelompok V mengalami kenaikan sebesar 43,6% dibandingkan dengan kelompok kontrol negatif aquadest 10 g/kgBB. Kenaikan ini berbeda tidak bermakna secara statistik, artinya aktivitas serum AST kelompok V sama dengan aktivitas serum AST kelompok kontrol negatif aquadest 10 g/kgBB.
Kelompok V memiliki efek hepatoprotrektif sebesar 82,2% jika dilihat dari aktivitas serum ALT dan bila dilihat dari aktivitas serum AST, kelompok V memiliki efek hepatoprotektif sebesar 70,5%.
Kelompok VI adalah kelompok perlakuan infusaM. tanariusdosis 2,5 g/kgBB. Aktivitas serum ALT kelompok ini bila dibandingkan dengan kelompok kontrol hepatotoksik parasetamol mengalami penurunan sebesar 26,3%. Penurunan aktivitas serum ALT kelompok VI berbeda bermakna dengan kontrol hepatotoksik parasetamol jika dilihat secara statistik. Aktivitas ALT kelompok VI bila dibandingkan dengan kontrol negatif aquadest 10 g/kgBB menunjukkan kenaikan sebesar 809,3%. Kenaikan aktivitas serum ALT kelompok V dibanding kontrol aquadest 10 g/kgBB secara statistik menunjukkan perbedaan yang bermakna.
43
kelompok kontrol hepatotoksik parasetamol dosis 2,5 g/kgBB. Aktivitas serum AST kelompok VI mengalami peningkatan sebesar 518,5% bila dibandingkan dengan kelompok kontrol negatif aquadest 10 g/kgBB. Peningkatan aktivitas serum AST ini secara statistik berbeda bermakna.
Efek hepatoprotektif kelompok VI adalah sebesar 26,3% jika dilihat dari aktivitas serum ALT, sedangkan bila dilihat dari aktivitas serum AST, efek hepatoprotektif kelompok VI adalah sebesar (-)27,2%. Dibandingkan dengan kelompok IV atau V, kelompok VI memiliki efek hepatoprotektif yang paling rendah.
D. Rangkuman Pembahasan
Penelitian ini menggunakan tiga variasi dosis infusaM. tanarius yakni kelompok dosis 10 g/kgBB, 5 g/kgBB, 2,5 g/kgBB. Hasil yang diperoleh berupa efek hepatoprotektif (%). Kelompok infusa dosis M. tanarius 10 g/kgBB, 5 g/kgBB, 2,5 g/kgBB memiliki efek hepatoprotektif berturut-turut 63,6%, 82,2%, 26,3% jika dilihat dari aktivitas serum ALT. Efek hepatoprotektif dilihat dari aktivitas serum AST kelompok infusa dosis M. tanarius 10 g/kgBB, 5 g/kgBB, 2,5 g/kgBB berturut-turut adalah 0,8%, 70,5%, (-) 27,2%. Hasil pengujian yang diperoleh menunjukkan bahwa pemberian infusa daun M. tanarius mampu memberikan efek hepatoprotektif pada tikus terinduksi parasetamol. Hal ini sesuai dengan hipotesis yang disusun, yakni infusa daun M. tanarius mampu memberikan efek hepatoprotektif pada tikus terinduksi parasetamol.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Pada pengukuran aktivitas serum ALT dan AST pada kelompok kontrol negatif M. tanarius dosis 10 g/kgBB diperoleh hasil yang berbeda tidak bermakna dengan kelompok kontrol negatif Aquadest dosis 10 g/kgBB. Artinya pemberian infusa daun M. tanarius tidak menaikkan aktivitas serum AST maupun ALT. Dengan demikian kenaikan aktivitas serum ALT maupun AST disebabkan karena induksi parasetamol.
Dosis perlakuan infusa daunM. tanariusyang memberikan efek paling baik adalah dosis 5 g/kgBB. Hasil pengukuran dan uji statistik terhadap aktivitas serum ALT dan AST, dosis 5 g/kgBB memberikan hasil yang berbeda tidak bermakna terhadap kontrol negatif aquadest 10 g/kgBB. Hal ini menunjukkan bahwa pemberian infusa daun M. tanarius memperlambat aktivitas serum ALT dan AST dalam batas normal.
45
nekrosis pada hati tikus. Keberadaan NAPQI akan meningkatkan pembentukan reactive oxygen spesies dan reactive nitrogen spesies seperti anion superoksida, radikal hidroksil, hidrogen peroksida, nitric oxide serta
peroxynitrite. Tingkat reactive oxygen spesies dan reactive nitrogen spesies
yang berlebihan dapat menyerang molekul biologi seperti DNA, protein, fosfolipid, yang dapat memicu terjadinya lipid peroksidasi, nitrasi tirosin, dan penurunan jumlah enzim-enzim antioksidan (superoksida dismutase, katalase, dan glutathion peroksidase) dan akhirnya menghasilkan (oxdative stress) tekanan oksidasi.
Di dalam daunM. tanariusterdapat kandungan berupa macarangiosida A, macarangiosida B, macarangiosida C, dan malofenol B yang semuanya dapat tertarik oleh pelarut yang sifatnya polar. Pada penelitian ini digunakan air sebagai pelarut infusa, jadi kemungkinan besar zat yang tertarik dalam infusa daunM. tanariusadalah keempat senyawa di atas. Keempat kandungan di atas, oleh Matsunami (2006) dilaporkan memiliki aktivitas penangkapan radikal bebas DPPH, artinya keempatnya dapat digunakan sebagai zat antioksidan.
Efek hepatoprotektif infusa daun M. tanarius dapat dicapai kemungkinan besar karena pemberian infusa daun M. tarariusselama 6 hari yang mengarah ke sintesis GSH dari komponen-komponen senyawa yang ada pada infusa daun M. tararius. Mekanisme hepatoprotektif lainnya diprediksikan akibat adanya aktivitas antioksidan dari macarangiosida A,
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
macarangiosida B, macarangiosida C, dan malofenol B. Zat antioksidan tersebut bekerja sebagai hepatoprotektor dengan cara menghambat oksidasi NAPQI oleh sitokrom P450. Kemungkinan lain, macarangiosida A, macarangiosida B, macarangiosida C, dan malofenol B memberikan efek hepatoprotektif dengan cara menangkap radikal bebas yang terbentuk akibat ikatan NAPQI pada protein.
Dilihat dari strukturnya, macarangiosida A, dan malofenol B memiliki ikatan α-β unsaturated. Ikatan α-β unsaturated memiliki ciri khas elektron sigma yang ikatannya kuat serta elektron phi yang ikatannya lemah, serta dapat berpindah tempat. Jika ikatan α-β unsaturated terprotonasi, maka kemungkinan akan terjadi perpindahan elektron seperti pada gambar 9.
Gambar 9.Perpindahan elektron oleh karena protonasi pada ikatanα
-βunsaturatedpada senyawa macarangiosida A.
Atom C pada posisiβ akan bermuatan positif sebagai akibat loncatan elektron pada ikatan phi. Kemungkinan besar atom C pada posisi β inilah yang akan menangkap radikal bebas yang terbentuk sehingga kehepatotoksikan parasetamol menurun.
O O
+
- -OH
47
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan hasil yang diperoleh dan analisis statistik yang telah dilakukan, maka dapat disimpulkan:
1. Pemberian infusa daun M. tanarius pada dosis 10 g/kgBB, 5 g/kgBB, 2,5 g/kgBB terbukti mampu menghasilkan efek hepatoprotektif pada tikus terinduksi parasetamol dosis 2,5 g/kgBB.
2. Pemberian infusa daun M. tanarius dosis 5 g/kgBB menimbulkan efek hepatoprotektif yang paling besar pada tikus jantan terinduksi parasetamol dosis 2,5 g/kgBB.
B. Saran
Perlu dilakukan penelitian lebih lanjut tentang:
1. Uji hepatoprotektif dengan infusa daun M. tanarius untuk induksi hepatotoksin lain seperti karbon tetraklorida atau galaktosamin.
2. Uji hepatoprotektif dengan infusa daunM. tanariuspada tikus jantan galur Wistar terinduksi parasetamol 2,5 g/kgBB, dengan kisaran dosis infusa daunM. tanariuspada kisaran dosis 2,5 g/kgBB hingga 5 g/kgBB.
3. Perlu dilakukan penelitian terhadap pengaruh infusa daun M. tanarius pada jumlah asam merkapturat yang terbentuk pada tikus jantan terinduksi parasetamol 2,5 g/kgBB.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Daftar Pustaka
Anonim, 2010,Plantamor, situs dunia tumbuhan
http://www.plantamor.com/index.php?plant=804, diakses tanggal 19 Maret 2010
Anonim, 1995, Farmakope Indonesia, edisi IV,9, 649, Departemen Kesehatan Republik Indonesia, Jakarta
Casarett and Doull, 1996, The Basic Science of Poisons, 5th edition, 403-414, McGraw-Hill, New York
Chandrasoma, P., and Taylor C. R., 1995, Concise Pathology, 2nd edition, 621-628, FRC Path Prentice Hall International, USA.
DiPiro, J. T., Robert L. T., Gary C. Y., Gary R. M., Barbara G. W., dan, L. Michael P., 2008, Pharmacotherapy : Apathiphysiologic Approach, 7th ed., 651-656, Mc Graw Hill, New York.
Edem DO and Akpanabiatu MI. 2006. Effects of palm oil-containing diets on enzyme activities of rats.Pakistan J Nutr5(4):301- 305.
Forrest, E., 2006, Hepatic Disorders, in Lee, A., (Ed.), Adverse Drug Reaction, 2nded, 193, 201-202, Pharmaceutical Press, London
Gujral, J. S., Tamara S. K., Anwar F., Mary L. B., and Hartmut J., 2002, Mode of Cell Death after Acetaminophen Overdose in Mice: Apoptosis or Oncotic Necrosis?,Toxicological Sciences,67, 322-328.
Hastuti, T., 2008, Aktivitas Enzim Transaminase dan Gambaran Histopatologi Tikus yang Diberikan Kelapa Kopyor Pasca Induksi Parasetamol, Fakultas Matematika dan Ilmu Pengetahuan Alam, skripsi, Institut Pertanian Bogor, Bogor.
Hinson JA, Bucci TJ, Irwin LK, Michael SL, and Mayeux PR, 2002, Effect Of Inhibitors Of Nitric Oxide Synthase On Acetaminophen-Induced Hepatotoxicity In Mice,Nitric oxide,6: 160-167
Hodgson E, and Levi PE. 2000. A Textbook of Modern Toxicology. Ed ke-2. Singapore: McGraw-Hill.
James L. P., Philip R. M., and Jack A. H., 2003, Acetaminophen-Induced Hepatotoxicity,Drug Metabolism and Dispotition31, 1499-1506. Koorders, S.H.,andTh. Valeton, 1918,Atlas Der Baumarten Von Java, Buch und
49
Ladoangin, A. A., 2004, Efek Hepatoprotektif Jus Buah Apel Hijau (Pyrus malus L.) pada Mencit Jantan Terinduksi Parasetamol, Skripsi, Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta.
Lee WM. 1995. Drug-induced hepatotoxicity.Med Progress333,17:1118-1127 Linawati, Y., Apriyanto, A., Susanti, E., Wijayanti, I., dan Donatus, A., 2006,
Efek Hepatoprotektif Rebusan Herba Putri Malu (Mimosa pigra, L.) Pada Tikus Terangsang Parasetamol, Risalah Seminar Ilmiah Nasional Hasil Penelitian "Fitofarmaka: Imunomodulator Masa Kini", 207-217, Universitas Sanata Dharma, Yogyakarta.
Madan, P. L., 1977, Acetaminophen Toxicity, The Journal of Clinical Pharmacology,17, 555-560.
Matsunami, K., Ichiko T., Takakazu S., Mitsunori A., Kazunari K., Hideaki O,et al, 2006, Radical-Scavenging Activities of New Megastigmane Glucosides fromMacaranga tanarius(L.) MÜLL.-ARG.,Chemical and Pharmaceutical Bulletin,54, No. 10, 1403-1406
Matsunami, K., Otsuka, H., Kondo, K., Shinzato, T., Kawahata, M., Yamaguchi, K., dkk 2009, Absolute configuration of (+)-pinoresinol 4-O-[600-O-galloyl]-b-D-glucopyranoside, macarangiosides E, and F isolated from the leaves of Macaranga tanarius, Phytochemistry 70 (2009) 1277-1285
Olson, K. R., 2006,Poisoning & Drug Overdose, Mc Graw Hill, San Fransisco. Phommart, S., Pakawadee Sutthivaiyakit, Nitirat Chimnoi, Somsak Ruchirawat,
and Somyote Sutthivaiyakit, 2005, Constituents of the Leaves of Macaranga tanarius,J. Nat. Prod., 68, 927-930
Price, S.A., Lorraine M.W, 2005, PATOFISIOLOGI : Konsep Klinis Proses-Proses Penyakit, Edisi 6, Vol1, 473-476 Penerbit EGC, Jakarta
Puteri, M.G., dan Kawabata, J., 2010, Novel alfa-glucosidase inhibitors from Macaranga tanarius leaves,Food Chemistry,123 (2010), 384-389 Robinson, T., 1991,Kandungan Organik Tumbuhan Tinggi, 6th ed., Penerbit ITB,
Bandung
Starr, F., Kim S., and Lloyd L., 2003, Macaranga tanarius, United States Geological Survey, Haleakala Field Station, Mau’I, 1 - 2