STUDI MEKANISME ANTIKANKER
SENYAWA ANALOG CALKON 3,5-BIS
-(2,3-DIMETOKSIBENZILIDIN)-1-METILPIPERIDIN-4-ON TERHADAP GUANIN
SKRIPSI
INES KOMALA SITI HANIFA
DEPARTEMEN KIMIA
FAKULTAS SAINS DAN TEKNOLOGI UNIVERSITAS AIRLANGGA
SURABAYA 2012
ADLN Perpustakaan Universitas Airlangga
ii
STUDI MEKANISME ANTIKANKER
SENYAWA ANALOG CALKON 3,5-BIS
-(2,3-DIMETOKSIBENZILIDIN)-1-METILPIPERIDIN-4-ON TERHADAP GUANIN
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Bidang Kimia Pada Fakultas Sains dan Teknologi
Universitas Airlangga
Disetujui oleh :
Pembimbing I
Drs. Hery Suwito, M.Si NIP. 19630308 198701 1 001
Pembimbing II
Dr. Alfinda Novi Kristanti, DEA NIP. 19671115 199102 2 001
iii
LEMBAR PENGESAHAN NASKAH SKRIPSI
Judul : Studi Mekanisme Antikanker Senyawa Analog Calkon 3,5-
bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on terhadap
Guanin
Penyusun : Ines Komala Siti Hanifa
NIM : 080810512
Pembimbing I : Drs. Hery Suwito, M.Si
Pembimbing II : Dr. Alfinda Novi Kristanti, DEA Tanggal Ujian : 2 Agustus 2012
Disetujui oleh :
Pembimbing I
Drs. Hery Suwito, M.Si NIP. 19630308 198701 1 001
Pembimbing II
Dr. Alfinda Novi Kristanti, DEA NIP. 19671115 199102 2 001
Mengetahui, Ketua Departemen Kimia Fakultas Sains dan Teknologi
Universitas Airlangga
Dr. Alfinda Novi Kristanti, DEA NIP. 19671115 199102 2 001
ADLN Perpustakaan Universitas Airlangga
iv
PEDOMAN PENGGUNAAN SKRIPSI
Skripsi ini tidak dipublikasikan, namun tersedia di perpustakaan dalam lingkungan Universitas Airlangga. Diperkenankan untuk digunakan sebagai referensi kepustakaan dengan pengutipan seijin penulis serta harus menyebutkan sumbernya.
Dokumen skripsi ini merupakan hak milik Universitas Airlangga
v
KATA PENGANTAR
Puji syukur kehadirat Allah SWT atas segala rahmat dan hidayah-Nya, sehingga penulis dapat menyelesaikan skripsi yang berjudul Studi Mekanisme Antikanker Senyawa Analog Calkon 3,5-bis-(2,3-dimetoksibenzilidin)-1-
metilpiperidin-4-on terhadap Guanin. Penulis menyadari bahwa penulisan skripsi ini tidak lepas dari bantuan berbagai pihak, untuk itu penulis menyampaikan terima kasih kepada :
1. Drs. Hery Suwito, M.Si selaku pembimbing I yang telah memberikan bimbingan selama proses pengerjaan skripsi ini.
2. Dr. Alfinda Novi Kristanti, DEA selaku pembimbing II dan Ketua Departemen Kimia Fakultas Sains dan Teknologi, Universitas Airlangga yang telah memberikan bimbingan selama proses pengerjaan skripsi ini.
3. Dra. Aning Purwaningsih, M.Si selaku dosen wali yang telah memberikan bimbingan selama proses perkuliahan.
4. Dr. Afaf Baktir, MS., Drs. Hamami, M.Si dan Dr. Nanik Siti Aminah, S.Si., M.Si yang telah memberikan banyak saran, inspirasi, dan motivasi.
5. Seluruh staf pengajar Departemen Kimia yang telah membantu selama proses perkuliahan dan pengerjaan skripsi ini.
6. Mama, nenek, dan kakak-kakak tercinta yang telah memberikan doa, kepercayaan, dan motivasi secara penuh.
7. Sahabat-sahabatku tercinta (A’yunil, Rohis, Ike, Nia, Mala, Nera, Bela, Riris dan Wahyu) yang telah memberikan banyak inspirasi.
8. Teman – teman angkatan 2008 (yang tidak bisa disebutkan satu persatu), kakak kelas angkatan 2007 serta adik – adik angkatan 2009 dan 2010 yang terus memberikan dukungan dan doa dalam penyelesaian skripsi ini.
9. Pihak – pihak yang tidak dapat disebutkan satu persatu yang banyak memberikan saran, bantuan dan pengalaman.
Penulis menyadari bahwa skripsi ini masih memiliki banyak kekurangan. Oleh karena itu, kritik dan saran yang membangun sangat diharapkan untuk
ADLN Perpustakaan Universitas Airlangga
vi
perbaikan dan pengembangan penulisan naskah skripsi ini. Penulis berharap skripsi ini dapat bermanfaat bagi perkembangan ilmu pengetahuan.
Surabaya, Agustus 2012 Penulis
Ines Komala Siti H.
vii
Hanifa, I.K.S., 2012, Studi Mekanisme Antikanker Senyawa Analog Calkon 3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on terhadap Guanin,
skripsi ini dibawah bimbingan Drs. Hery Suwito, M.Si dan Dr. Alfinda Novi Kristanti, DEA, Departemen Kimia Fakultas Sains dan Teknologi, Universitas Airlangga, Surabaya.
ABSTRAK
Telah dilakukan sintesis senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dalam suasana basa. Hasil penelitian menunjukkan bahwa senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on terbukti mempunyai aktivitas antikanker dengan IC50 sebesar
1.77 µg/ml. Berdasarkan struktur utamanya, senyawa analog calkon diduga bekerja sebagai senyawa antikanker melalui mekanisme alkylating agent terhadap basa guanin. Penelitian ini bertujuan untuk mengetahui reaksi antara senyawa analog calkon dengan basa guanin. Reaksi antara senyawa analog calkon dengan guanin berlangsung selama 14 jam pada suhu 78°C. Hasil kromatografi lapis tipis menunjukkan terdapatnya noda baru pada filtrat hasil reaksi. Campuran yang diperoleh dimurnikan menggunakan kromatografi lapis tipis preparatif sehingga diperoleh senyawa murni. Analisis menggunakan spektrofotometer UV-Vis menunjukkan 2 puncak pada panjang gelombang 259 dan 308,5 nm, yang diduga mengindikasikan terjadinya reaksi antara senyawa analog calkon dengan guanin. Berdasarkan hasil tersebut, senyawa analog calkon diduga mempunyai mekanisme antikanker sebagai alkylating agent terhadap guanin.
Kata kunci : analog calkon, alkilasi guanin, mekanisme antikanker ADLN Perpustakaan Universitas Airlangga
viii
Hanifa, I.K.S., 2012, Study Anticancer Mechanism of
Chalcone Analogue 3,5-bis-(2,3-dimethoxybenzylidine)-1-methylpiperidine-4-on toward Guanine, final project was under guidance of Drs. Hery Suwito, M.Si and Dr. Alfinda Novi Kristanti, DEA, Chemistry Departement, Faculty of Science and Technology, Airlangga University, Surabaya.
ABSTRACT
Synthesis of chalcone analogue 3,5-bis-(2,3-dimethoxybenzylidine)-1-methylpiperidine-4-on compound under alkaline condition had been done. The result showed that the compound had anticancer activity with IC50 of 1.77 µg/ml.
Based on its primary structure, this compound was expected to work as anticancer compound through alkylating agent mechanism toward guanine. This research aimed to determine the reaction between chalcone analogue compound and guanine. The reaction between chalcone analogue and guanine occurred at 78 ° C for 14 hours. The result of thin layer chromatography showed the presence of a new spot on the filtrate. The mixture obtained was purified using preparative thin layer chromatography in order to obtain pure compounds. Analysis using UV-Vis spectrophotometer showed two peaks at 259 and 308.5 nm. This result was thought to indicate the occurrence of the reaction between chalcone analogue compound with guanine. Based on these results, chalcone analogue compound was thought to have anticancer mechanism as an alkylating agent toward guanine.
Keywords : chalcone analogue, alkylating guanine, anticancer mechanism
ix
BAB I PENDAHULUAN 1.1 Latar Belakang Masalah ... 1
1.2 Rumusan Masalah ... 4
1.3 Tujuan Penelitian ... 4
1.4 Manfaat Penelitian ... 5
BAB II TINJAUAN PUSTAKA 2.1 Calkon ... 6
2.2 Guanin ... 7
2.3 Reaksi Kondensasi Aldol ... 8
2.3.1 Reaksi kondensasi aldol silang ... 9
2.4 Reaksi Pembentukan Enamina ... 9
2.5 Kromatografi ... 10
2.5.1 Kromatografi lapis tipis ... 10
2.5.2 Kromatografi lapis tipis preparatif ... 11
2.6 Spektroskopi ... 11
2.6.1 Spektroskopi ultraviolet-visibel (UV-Vis) ... 13
2.6.2 Spektroskopi 1H-NMR ... 13
2.6.3 Spektroskopi 13C-NMR ... 14
2.7 Kanker ... 14
2.8 Antikanker... 15
BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ... 19
3.2 Alat dan Bahan Penelitian ... 19
3.2.1 Alat-alat penelitian ... 19
3.2.2 Bahan-bahan penelitian ... 19
3.3 Tahapan Penelitian ... 20
3.3.1 Sintesis senyawa 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on ... 20
3.3.2 Reaksi antara senyawa 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dengan guanin ... 20
3.3.3 Pemisahan senyawa hasil sintesis tahap 2 menggunakan kromatografi lapis tipis preparatif ... 21
ADLN Perpustakaan Universitas Airlangga
x
3.3.4 Uji sifat fisika senyawa hasil sintesis ... 21
3.3.4.1 Uji titik leleh ... 21
3.3.5 Kromatografi lapis tipis ... 22
3.3.6 Analisis spektroskopi ... 22
3.3.6.1 Uji spektroskopi ultraviolet-visibel (UV-Vis) ... 22
3.3.6.2 Uji spektroskopi resonansi mangetik inti (NMR). ... 22
3.4 Skema Kerja ... 24
BAB IV HASIL DAN PEMBAHASAN 4.1 Sintesis Senyawa 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on ... 25
4.2. Hasil Analisis Spektroskopi ... 29
4.2.1 Hasil analisis spektroskopi UV-Vis... ... 29
4.2.2 Hasil analisis spektroskopi resonansi magnet inti... . 29
4.3 Reaksi antara Senyawa Analog Calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dengan Guanin.... 32
4.4 Pemisahan Campuran Senyawa menggunakan Kromatografi Lapis Tipis Preparatif... ... 36
4.5. Hasil Analisis Spektroskopi ... 38
4.5.1 Hasil analisis spektroskopi UV-Vis ... 38
4.6 Senyawa Pengalkilasi dalam Mekanisme Alkylating Agent... ... 39
BAB V KESIMPULAN DAN SARAN 5.1 Kesimpulan ………... 40
5.2 Saran ……….... 40
DAFTAR PUSTAKA ... 41
LAMPIRAN
xi
DAFTAR GAMBAR
No. Judul Gambar Halaman
1.1 Struktur senyawa analog calkon 3,5-bis
-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on ... 3
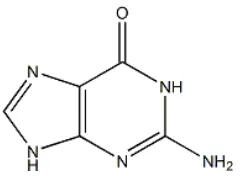
1.2 Struktur guanin ... 3
2.1 Struktur umum senyawa calkon ... 6
2.2 Struktur senyawa analog calkon 3,5-bis-(2,3- dimetoksibenzilidin)-1-metilpiperidin-4-on ... 7
2.3 Struktur guanin ... 8
2.4 Spektrum elektromagnetik ... 12
4.1 Kristal senyawa analog calkon ... 26
4.2 Reaksi kondensasi aldol silang ... 27
4.3 Mekanisme reaksi pembentukan senyawa analog calkon.. ... 28
4.4 Bagian sinamoil dari struktur senyawa 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on ... 29
4.5 Penomoran atom C/H senyawa 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on ... 30
4.6 Struktur dan pergeseran kimia 13C-NMR senyawa hasil sintesis tahap 1 ... 31
4.7 Struktur dan pergeseran kimia 1H-NMR senyawa hasil sintesis tahap 1 ... 32
4.8 Prediksi mekanisme reaksi adisi nukleofilik antara senyawa analog calkon dengan guanin ... 34
ADLN Perpustakaan Universitas Airlangga
xii
DAFTAR TABEL
No. Judul Halaman
4.1 Nilai Rf senyawa hasil sintesis tahap 1... 26
4.2 Data pergeseran kimia (δ, ppm) spektrum 1H
dan 13C-NMR (CDCl3, 400 MHz)... 30
4.3 Nilai Rf hasil sintesis tahap 2... 36
4.4 Data nilai Rf senyawa hasil sintesis... 37
xiii
DAFTAR LAMPIRAN
No. Judul
1 Hasil kromatografi lapis tipis senyawa hasil sintesis tahap 1 2 Spektrum UV senyawa analog calkon
3 Spektrum 1H-NMR senyawa hasil sintesis tahap 1 4 Spektrum 13C-NMR senyawa hasil sintesis tahap 1
5 Spektrum 13C-NMR (BB dan DEPT 45, 90 dan 135) senyawa hasil
sintesis tahap 1
6 Pemisahan senyawa hasil sintesis tahap 2 menggunakan KLTP 7 Kromatogram senyawa hasil sintesis tahap kedua yang telah murni 8 Spektrum UV senyawa hasil sintesis tahap 2
ADLN Perpustakaan Universitas Airlangga
1
BAB I
PENDAHULUAN
1.1 Latar Belakang Masalah
Kanker merupakan salah satu penyakit yang patut diperhitungkan sebagai penyebab kematian terbesar di dunia. Faktanya, kanker mendapat predikat sebagai
penyakit yang paling umum terjadi di Amerika Serikat pada tahun 2005, dengan total korban 500.000 jiwa (Katzung, 2006). Di negara berkembang seperti Indonesia, penyakit kanker menduduki peringkat kelima sebagai penyebab
kematian utama setelah penyakit kardiovaskuler, infeksi, pernapasan, dan pencernaan. Namun, yang paling dikhawatirkan adalah data penelitian dari
Organisasi Penanggulangan Kanker Dunia (UICC) dan Organisasi Kesehatan Dunia (WHO) yang memperkirakan bahwa angka kejadian kanker di dunia dapat mengalami peningkatan hingga 40 % pada tahun 2020, terutama di negara-negara
berkembang seperti Indonesia (Mortara, 2007). Berdasarkan data tersebut, tidak menutup kemungkinan peringkat penyakit kanker sebagai penyebab kematian di
Indonesia akan mengalami kenaikan pada tahun 2020.
Penanganan penyakit kanker (terutama sebelum mencapai stadium yang
lebih berbahaya) sangat penting guna menghambat pembelahan sel-sel abnormal. Berbagai metode telah dilakukan untuk mengatasi hal tersebut antara lain menggunakan pembedahan (operasi), radioterapi, kemoterapi, terapi hormon dan
immunoterapi (Breiner, 2011). Salah satu metode terapi kanker yang banyak
2
mengalami perkembangan hingga saat ini adalah kemoterapi. Kemoterapi
merupakan proses pemberian obat-obatan antikanker dalam bentuk kapsul atau melalui infus. Kemoterapi menggunakan bahan aktif berupa senyawa kimia yang bersifat sitotoksik yang bertujuan untuk menghambat pertumbuhan sel kanker
(Blows, 2005). Berbagai penelitian untuk menemukan obat baru telah dilakukan baik dengan cara mensintesis senyawa yang berpotensi sebagai antikanker
maupun mengisolasinya dari sumber-sumber alam.
Salah satu senyawa antikanker yang cukup banyak diteliti hingga saat ini adalah calkon. Struktur kimiawi senyawa calkon (1,3-difenil-2-propen-1-on)
secara umum terdiri dari dua cincin aromatis yang dihubungkan oleh 3 atom
karbon dengan sistem karbonil-,-tak jenuh. Beberapa penelitian yang telah
dilakukan menunjukkan bahwa senyawa calkon dan turunannya memiliki aktivitas
sebagai antikanker terhadap berbagai macam sel tumor (Achanta et al., 2005). Handika (2011) telah berhasil mensintesis senyawa antikanker analog
calkon 3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on yang merupakan hasil reaksi kondensasi aldol silang antara N-metilpiperidin-4-on dengan 2,3-dimetoksibenzaldehid dalam suasana basa. Uji antikanker senyawa tersebut
terhadap sel kanker payudara T47D menunjukkan nilai IC50 sebesar 1.77 µg/ml.
Berdasarkan hasil tersebut, dapat diketahui bahwa senyawa analog calkon 3,5-bis
-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on berpotensi untuk dikembangkan sebagai bahan aktif dalam terapi.
ADLN Perpustakaan Universitas Airlangga
Gambar 1.1 Struktur senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on
Penelitian lebih lanjut terkait mekanisme antikanker dari senyawa analog calkon 3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on sangat diperlukan
sebagai salah satu data pendukung untuk merealisasikan senyawa hasil sintesis tersebut sebagai obat antikanker yang efektif. Dimmock (1998) menyatakan bahwa salah satu aktivitas senyawa calkon sebagai antikanker disebabkan oleh
kemampuan alkilasi dari gugus olefin terkonjugasi yang dapat berikatan dengan basa guanin. Guanin merupakan salah satu basa purin yang terdapat pada untaian
DNA yang memiliki beberapa sisi yang rentan diserang oleh zat pengalkil. Kemampuan senyawa calkon sebagai agen pengalkilasi basa guanin terjadi melalui pembentukan ikatan kovalen dengan DNA (Meric et al., 2002). Oleh
karena itu, prediksi mekanisme antikanker yang paling mendukung dari senyawa analog calkon 3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on adalah
sebagai alkylating agent.
Gambar 1.2 Struktur guanin
4
Berdasarkan uraian tersebut, pada penelitian ini akan dilakukan studi
terkait kemampuan senyawa analog calkon sebagai alkylating agent terhadap basa guanin melalui reaksi kimia. Produk yang dihasilkan dari reaksi alkilasi guanin tergantung dari struktur senyawa pengalkilasi yang digunakan. Keberadaan gugus
enon dalam senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dan sifat nukleofil dari guanin diduga akan mengarah pada
terbentuknya senyawa siklik sebagai produk hasil reaksi tersebut (Sturla, 2007).
1.2 Rumusan masalah
1. Apakah senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dapat bereaksi dengan basa guanin?
2. Bagaimana mekanisme reaksi antara senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dengan basa guanin?
1.3 Tujuan Penelitian
1. Mengetahui kemampuan senyawa analog calkon 3,5-bis
-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on untuk bereaksi dengan basa guanin.
2. Mengetahui mekanisme reaksi antara senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dengan basa guanin.
ADLN Perpustakaan Universitas Airlangga
1.4 Manfaat Penelitian
Dengan melakukan penelitian terkait mekanisme senyawa analog calkon 3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on sebagai antikanker, diharapkan dapat menambah pengetahuan dan informasi tentang mekanisme
antikanker, khususnya senyawa calkon dan alkylating agent.
6
Bab II
TINJAUAN PUSTAKA
2.1 Calkon
Calkon merupakan salah satu senyawa golongan flavonoid yang memiliki gugus enon dalam strukturnya. Senyawa yang memiliki nama IUPAC
1,3-difenil-2-propen-1-on ini secara umum membentuk sol dalam eter, kloroform, karbon bisulfida, dan benzena, agak larut dalam alkohol, dan sedikit larut dalam petroleum eter dingin (Budavari, 2001).
Hasil penelitian Kamei et al. (1997) menunjukkan bahwa senyawa calkon dapat menginduksi DNA secara abnormal yang berhubungan dengan aktivitas
antikanker (Meric et al., 2002). Selain sebagai antikanker, calkon juga memiliki aktivitas biologis lainnya meliputi antimalaria, antiinflamasi, antioksidan dan antibakteri (Chiaradia, 2008). Sifat farmakologi senyawa calkon tersebut berasal
dari keberadaan gugus karbonil-,-tak jenuh dalam strukturnya seperti yang
tampak pada gambar 2.1 (Curti et al., 2007).
O
Gambar 2.1 Struktur umum senyawa calkon
Senyawa calkon dapat disintesis melalui reaksi kondensasi Claisen Schmidt antara suatu aldehid dan keton yang sesuai dalam suasana basa dengan
pelarut seperti metanol (Hijova, 2006).
ADLN Perpustakaan Universitas Airlangga
Senyawa analog calkon 3,5-bis
-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on merupakan salah satu senyawa yang telah terbukti memiliki aktivitas antikanker terhadap sel kanker payudara T47D. Uji sitotoksisitas secara in vitro dilakukan berdasarkan prinsip reduksi senyawa MTT oleh enzim
dehidrogenase mitokondria menjadi formazan, suatu garam yang berwarna biru (Doyle, 1988).
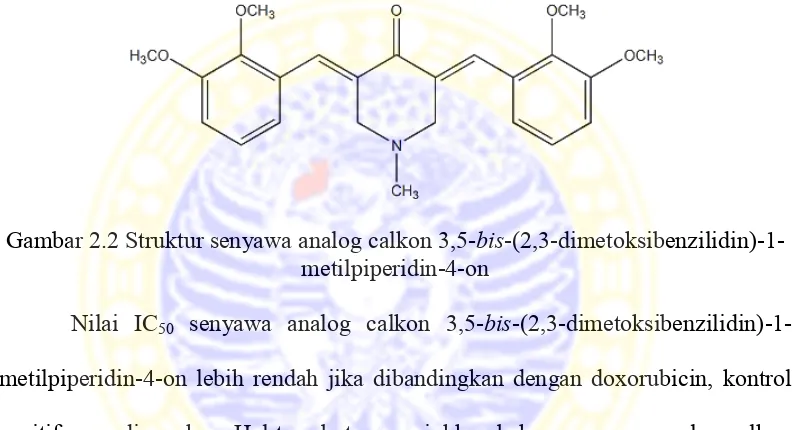
Gambar 2.2 Struktur senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on
Nilai IC50 senyawa analog calkon 3,5-bis
-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on lebih rendah jika dibandingkan dengan doxorubicin, kontrol
positif yang digunakan. Hal tersebut menunjukkan bahwa senyawa analog calkon 3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on memiliki keaktifan yang lebih baik sebagai antikanker (Handika, 2011).
2.2 Guanin
Guanin merupakan salah satu dari empat basa penyusun DNA dan RNA. Secara umum, guanin berbentuk amorf, dapat larut dalam larutan kalium hidroksida, larutan asam, agak sukar larut dalam air dan alkohol, serta hampir
tidak larut dalam eter (Sumardjo, 2008).
8
Gambar 2.3 Struktur guanin
Residu guanin dalam DNA terutama terdapat dalam bentuk tautomer keto,
dan dengan mudah akan membentuk pasangan basa Watson-Crick dengan residu sitosin melalui pembentukan ikatan hidrogen (Brunton et al., 2010). Secara
umum, guanin biasanya terlibat dalam proses alkilasi pada pengobatan antikanker. Pembentukan alkilguanin yang disusul dengan pembentukan tautan silang ( cross-link) menandakan sitotoksiksitas (Harahap, 2003).
2.3 Reaksi Kondensasi Aldol
Kondensasi aldol merupakan reaksi antara dua molekul aldehid maupun
keton dalam suasana basa. Dalam reaksi ini, sebuah proton pada posisi C dari
gugus karbonil lepas oleh serangan basa, sehingga terbentuk C yang bersifat
nukleofil. Selanjutnya C yang bersifat nukleofil menyerang atom C gugus
karbonil yang bersifat elektrofil dari molekul kedua (Bruice, 2003). Berikut
adalah reaksi antara dua molekul asetaldehid dalam suasana basa KOH . ADLN Perpustakaan Universitas Airlangga
Produk yang dihasilkan disebut aldol (dinamakan demikian karena
mengandung gugus alkohol dan karbonil dalam sebuah senyawa) (Hart et al., 2010).
2.3.1 Reaksi kondensasi aldol silang
Reaksi kondensasi aldol antara dua senyawa karbonil yang berbeda disebut kondensasi aldol silang (Pellegrini, 2011). Apabila salah satu senyawa
karbonil yang digunakan tidak memiliki hidrogen alfa, maka hasil reaksi kondensasi aldol silang yang terjadi dapat dikontrol menjadi hanya satu produk. Hal tersebut dapat terjadi apabila senyawa karbonil tanpa hidrogen alfa terdapat
berlebih dalam reaksi, sehingga karbanion lebih memilih untuk menyerang senyawa karbonil tanpa hidrogen alfa karena kelimpahannya. Berikut adalah
reaksi antara benzaldehid dan butanal dalam suasana basa (Bruice, 2003).
Dalam reaksi tersebut, hanya butanal yang dapat membentuk ion enolat
sedangkan tidak pada benzaldehid (karena benzaldehid tidak memiliki H). Jika
ion enolat menyerang atom C karbonil benzaldehid, maka kondensasi aldol silang akan terjadi (Hart et al., 2010).
2.4 Reaksi Pembentukan Enamina
Reaksi antara senyawa calkon dengan guanin melibatkan pembentukan
suatu enamina. Enamina merupakan amina tersier dengan ikatan rangkap ,-tak
jenuh ditinjau dari posisi atom nitrogen. Enamina dapat terbentuk apabila suatu
10
aldehid atau keton direaksikan dengan amina sekunder. Dalam reaksi
pembentukan enamina, dibutuhkan asam lemah maupun basa sebagai katalis. Misalnya reaksi antara sikloheksanon dengan dimetilamin (Bruice, 2003) :
Kromatografi merupakan proses pemisahan berdasarkan afinitas komponen suatu campuran terhadap fasa diam dan fasa gerak. Komponen akan
terdistribusi secara tidak sama dalam dua fasa yaitu fasa diam dan fasa gerak. Fasa diam dapat berbentuk padat atau cair yang ditunjang suatu zat padat. Fasa diam
tersebut dapat ditempatkan dalam kolom, tersebar dalam lapisan, atau terdistribusi sebagai film. Sedangkan fasa gerak dapat berbentuk gas maupun cair. Apabila fasa gerak berbentuk gas (disebut gas pembawa) tekniknya disebut sebagai
kromatografi gas, sedangkan apabila fasa gerak berbentuk cair tekniknya disebut kromatografi cair (Sewell and Clark, 2008).
2.5.1 Kromatografi lapis tipis
Kromatografi lapis tipis merupakan teknik penting dalam pemisahan dan analisis kualitatif komponen dalam suatu sampel (Pavia, 2005). Apabila
komponen-komponen dalam campuran bergerak melalui fasa diam pada laju yang berbeda maka pemisahan dapat terjadi. Parameter yang digunakan untuk
+ HN
CH3
H3C + H2O
H+
ADLN Perpustakaan Universitas Airlangga
Rf =
mengetahui posisi solut dalam KLT adalah Retardation factor (Rf) dengan rumus
(Sewell and Clark, 2008) :
Jarak yang ditempuh komponen Jarak yang ditempuh pelarut
Noda yang tidak menimbulkan warna pada kromatogram dapat dilihat
menggunakan bantuan sinar UV. Selain itu, deteksi dapat dilakukan menggunakan reagen chromogenic maupun fluorogenic (Sherma and Fried, 2003).
2.5.2 Kromatografi lapis tipis preparatif
Kromatografi lapis tipis perparatif merupakan suatu metode pemisahan senyawa dalam skala miligram-gram. Secara umum, fasa diam yang sering
digunakan adalah silika yang tersebar dalam pelat. Ukuran dari pelat kromatografi lapis tipis preparatif tergantung pada jumlah sampel dan ukuran bejana
pengembang. Ukuran pelat 20 x 20 cm dengan tebal 1 mm dapat digunakan untuk pemisahan 10-100 mg sampel. Fasa gerak yang digunakan dapat diketahui dari hasil elusi terbaik yang digunakan pada kromatografi lapis tipis. Sampel ditotol
sepanjang garis bawah pelat silika secara berulang-ulang hingga membentuk pita, kemudian dielusi dengan pelarut yang sesuai untuk mencapai pemisahan (Xu,
2011).
2.6 Spektroskopi
Spektroskopi merupakan ilmu yang mempelajari tentang interaksi materi dengan radiasi elektromagnetik. Radiasi elektromagnetik merupakan energi
radiasi yang memiliki sifat-sifat partikel dan gelombang. Karena radiasi elektromagnetik memiliki sifat-sifat partikel dan gelombang, maka dapat
Skripsi Studi Mekanisme Antikanker Senyawa Analog Calkon
3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on terhadap Guanin
12
E =
dihubungkan dengan frekuensi dan panjang gelombang. Spektrum
elektromagnetik terbagi dalam beberapa daerah sesuai dengan kegunaannya dalam spektroskopi, seperti yang tampak pada gambar 2.4.
Gambar 2.4 Spektrum elektromagnetik
Hubungan antara energi (E) suatu foton dan frekuensi dapat dijelaskan
melalui persamaan (Bruice, 2003) :
E = h v
Persamaan tersebut menjelaskan bahwa frekuensi suatu radiasi berbanding lurus dengan energinya sehingga semakin besar frekuensi maka energinya juga semakin besar. Konstanta proporsionalitas antara energi dan frekuensi disebut konstanta
Planck’s dengan simbol h. Secara umum, frekuensi suatu radiasi berbanding terbalik dengan panjang gelombang sehingga persamaan di atas dapat dituliskan
dalam bentuk :
hc λ
dengan λ adalah panjang gelombang cahaya dan c adalah kecepatan cahaya (Hart
et al., 2010).
2.6.1 Spektroskopi ultraviolet-visibel (UV-Vis)
Spektroskopi UV-Vis dapat memberikan informasi tentang komponen
yang memiliki sistem elektron terkonjugasi. Bagian sinar ultraviolet terletak
pada panjang gelombang antara 180-400 nm, sedangkan sinar tampak terletak
pada panjang gelombang 400-780 nm. Apabila suatu molekul mengabsorbsi radiasi pada daerah tersebut, maka akan terjadi transisi elektronik. Pada transisi ini, semakin banyak jumlah ikatan rangkap terkonjugasi maka panjang gelombang
senyawa semakin besar. Pengaruh gugus auksokrom yang terikat pada ikatan tersebut dapat menggeser panjang gelombang ke arah yang lebih besar.
Pergeseran ini disebut efek batokromik (Bruice, 2003).
2.6.2 Spektroskopi 1H-NMR
Spektroskopi 1H-NMR dapat digunakan untuk menentukan karakteristik
proton suatu senyawa. Perbedaan posisi serapan suatu proton dengan posisi serapan standart disebut pergeseran kimia. Pada dasarnya, proton yang memiliki
kondisi lingkungan yang sama memiliki pergeseran kimia yang sama. Sebaliknya, proton dengan kondisi lingkungan kimia yang berbeda memiliki pergeseran kimia yang berbeda. Nilai pergeseran kimia proton bergantung pada lingkungan kimia di
sekitar atom C yang mengikat proton tersebut. Selain itu, pergeseran kimia juga dipengaruhi oleh resonansi dan efek anisotropi. Sebagai contoh proton pada C
alkena muncul pada pergeseran kimia 4,5-7,5 ppm, proton pada C aromatis dan heteroaromatis muncul pada 6-9 ppm, dan proton pada C aldehid muncul pada 9-10 ppm (Silverstein et al., 2005).
14
2.6.3 Spektroskopi 13C-NMR
Spekroskopi 13C-NMR dapat digunakan untuk menentukan kerangka suatu senyawa (Bruice, 2003) berupa jumlah, posisi, dan jenis atom karbon (Hart et al., 2010). Dalam spektroskopi 13C-NMR, nilai pergeseran kimia pada umumnya
terletak antara 0-200 ppm. Nilai pergeseran kimia yang khas untuk gugus fungsi tertentu yakni : atom karbon pada CH3 alifatis muncul pada pergeseran kimia
antara 10-30 ppm, atom karbon pada senyawa aromatis muncul pada pergeseran kimia antara 120-150 ppm, dan atom karbon pada gugus karbonil muncul pada pergeseran kimia sekitar 200 ppm (Silverstein et al., 2005).
2.7 Kanker
Kanker adalah segolongan penyakit yang ditandai dengan pembelahan sel yang tidak terkendali dan kemampuan sel-sel tersebut untuk menyerang jaringan biologis lainnya, baik dengan pertumbuhan langsung di jaringan yang
bersebelahan (invasi) maupun dengan migrasi sel ke tempat yang jauh (metastasis). Pertumbuhan yang tidak terkendali tersebut disebabkan oleh
kerusakan DNA dan menyebabkan mutasi di gen vital yang mengontrol pembelahan sel pada jaringan dan organ (Lodish et al., 2000).
Kejadian, distribusi, dan perilaku dari jenis tertentu kanker berkaitan dengan beberapa faktor, antara lain jenis kelamin, usia, ras, dan paparan zat karsinogen dari lingkungan. Faktor yang paling berperan dalam memicu
timbulnya kanker adalah paparan zat karsinogen dari lingkungan (Katzung, 2006). ADLN Perpustakaan Universitas Airlangga
2.8 Antikanker
Antikanker merupakan zat kimia yang dapat menghambat atau mengganggu pertumbuhan sel tumor ganas. Senyawa-senyawa antikanker juga disebut sebagai agen-agen kemoterapeutik atau antineoplastik. Obat-obat
antikanker dapat dibagi menjadi dua golongan sederhana yaitu golongan sitotoksik dan hormon. Obat golongan sitotoksik bertujuan untuk menghambat
pertumbuhan sel, terutama sel-sel yang membelah. Contoh dari obat golongan ini adalah senyawa pengalkil, antibiotik, antimetabolit, serta berbagai obat lain. Sedangkan senyawa - senyawa hormonal digunakan untuk tumor-tumor pada
jaringan yang sensitif hormon seperti payudara dan prostat (Stringer, 2008). Berdasarkan mekanisme kerjanya, obat-obatan antikanker pada umumnya
dibagi dalam beberapa golongan sebagai berikut : 1. Agen pengalkilasi
Agen pengalkilasi merupakan senyawa reaktif yang dapat mentransfer
alkil untuk membentuk ikatan kolvalen dengan DNA (Lullmann et al., 2000). Zat pengalkil digunakan dalam kemoterapi kanker secara luas karena efektif dalam
mematikan sel kanker melalui reaksinya yang langsung dengan DNA dalam sel kanker. Hal ini menyebabkan DNA kehilangan kemampuannya untuk melakukan
replikasi sel (Harahap, 2003).
Di dalam tubuh, obat pengalkil dengan mudah dapat berinteraksi dengan basa-basa yang terdapat pada DNA dan mencegah pembelahan sel dengan
membuat tautan silang (cross-link) dari untai heliks ganda (Neal, 2006). Situs utama dari alkilasi DNA adalah guanin, namun basa lain juga dapat mengalami
16
alkilasi dengan derajat yang lebih rendah. Pembentukan tautan silang (cross-link)
DNA merupakan faktor yang sangat penting dalam mekanisme alkilasi dan sel-sel yang sedang mengalami replikasi paling rentan terhadap agen pengalkilasi. Proses tersebut sangat berpengaruh selama fase S dalam siklus sel (Brunton et al., 2010).
Peristiwa alkilasi dapat terjadi pada sel sehat dan pada umumnya berupa yang dapat menimbulkan beberapa efek samping. Hal tersebut dipengaruhi oleh
dosis toksisitas senyawa golongan pengalkilasi yang dapat memberikan efek terhadap jaringan yang sedang berkembang dengan cepat seperti sumsum tulang, saluran pencernaan, dan sistem reproduksi (Harahap, 2003).
2. Golongan antimetabolit
Golongan antimetabolit juga disebut sebagai agen antiproliferasi. Obat
golongan ini dapat dibagi menjadi 3 kelompok yaitu antagonis asam folat, pirimidin, dan purin. Dalam mekanismenya, senyawa antikanker golongan antimetabolit bekerja sebagai antagonis asam folat, purin dan pirimidin. Hal
tersebut berkaitan dengan strukur obat yang mirip dengan tiga metabolit tersebut. Selektivitas obat golongan antimetabolit berhubungan dengan fakta bahwa sel-sel
tumor dapat tumbuh lebih cepat daripada sel-sel normal (pengecualian sumsum tulang, folikel rambut, dan bagian dari saluran gastrointestinal) (Thurston, 2007).
3. Golongan antibiotik
Hasil uji skrining dari produk mikroba telah mendorong tercetusnya penemuan sejumlah obat antibiotik yang terbukti secara klinis dapat bermanfaat
dalam kemoterapi kanker. Secara umum, senyawa golongan antibiotik bekerja melalui mekanisme interkalasi pada pasangan basa. Hal tersebut dapat
ADLN Perpustakaan Universitas Airlangga
menyebabkan terpotongnya untai DNA dan mengganggu replikasi sel (Katzung,
2006).
4. Agen antitubulin
Senyawa golongan alkaloid vinca dan taxan memiliki mekanisme
antikanker sebagai antitubulin. Agen antitubulin menghambat siklus sel pada fasa M (mitosis sel) dengan cara terikat pada protein mikrotubulus yang penting dalam
pembentukan spindel (Neal, 2006). Agen ini dapat mengganggu dinamika mikrotubulus (pembentukan maupun peruraian spindel) tepatnya pada tahap metafase. Mikrotubulus adalah polimer dari tubulin yang tidak dapat dipisahkan
dari fase mitosis sel. Sebuah struktur yang dihasilkan dari mikrotubulus adalah gelendong mitosis, yang digunakan dalam pembelahan sel (Thurston, 2007).
5. Antibodi monoklonal
Antibodi monoklonal merupakan molekul antibodi yang berasal dari produk klon tunggal sel. Obat golongan ini merupakan obat baru yang dapat
bereaksi dengan antigen yang diekspresikan secara khusus pada sel kanker (Neal, 2006). Apabila antigen di permukaan sel tumor dapat diidentifikasi, antibodi dapat
dibentuk untuk menyerang dan menghancurkan sel tumor tersebut (Brooker, 2005). Misalnya Herceptin, sejenis antibodi yang direkayasa secara genetik, dan
dapat menghambat kanker payudara dengan cara berikatan dengan reseptor faktor pertumbuhan yang terdapat dalam sel kanker (Campbell et al., 2004).
6. Golongan hormonal
Obat golongan hormonal digunakan untuk mengobati tumor-tumor yang sensitif hormon seperti tumor pada payudara, prostat, dan uterus. Tujuan
18
penggunaan obat ini adalah mengurangi kadar hormon yang merangsang
pertumbuhan tumor atau memblok reseptor untuk hormon. Misalnya penghambat aromatase yang dapat memblok pembentukan estrogen dan digunakan untuk mengobati tumor-tumor yang bergantung pada estrogen (Stringer, 2008).
Antihormon jenis ini khusus digunakan pada kanker mamma yang tersebar pada wanita menopause (Tjay dan Raharja, 2007).
ADLN Perpustakaan Universitas Airlangga
19
BAB III
METODE PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan di Laboratorium Kimia Organik Departemen Kimia Fakultas Sains dan Teknologi Universitas Airlangga, mulai bulan Januari
2012 sampai Juni 2012.
Analisis Spektroskopi UV-Vis dilakukan di Laboratorium Kimia Analitik Departemen Kimia Fakultas Sains dan Teknologi Universitas Airlangga. Analisis
1H-NMR dan 13C-NMR dilakukan di Phytochemistry Laboratory, Faculty of
Science and Food, University Kebangsaan Malaysia, Bangi, Malaysia.
3.2 Alat dan Bahan Penelitian
3.2.1 Alat-alat penelitian
Alat-alat yang digunakan pada penelitian meliputi seperangkat alat gelas yang biasa digunakan di laboratorium kimia organik. Sedangkan instrumen yang
digunakan untuk keperluan analisis adalah Fisher John Melting Point Apparatus, spektrofotometer UV-Vis (Shimadzu PharmaSpec-1770) dan spektrometer
resonansi magnetik inti (NMR Bruker 400 MHz).
3.2.2 Bahan-bahan penelitian
Bahan-bahan kimia yang digunakan pada penelitian ini adalah
2,3-dimetoksibenzaldehid, N-metilpiperidin-4-on, etanol, NaOH, n-heksana, etil asetat, guanin, HCl pekat, dan Silika gel.
20
3.3 Tahapan Penelitian
3.3.1 Sintesis senyawa 3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin 4-on
(tahap 1)
Sejumlah 1,4840 gram (9 mmol) 2,3-dimetoksibenzaldehid, 0,3690 gram (3 mmol) N-metilpiperidin-4-on dan 10 ml etanol dimasukkan ke dalam labu alas
bulat leher tiga secara berurutan. Campuran tersebut diaduk menggunakan pengaduk magnetik sampai larut. Selanjutnya, bagian luar labu alas bulat leher
tiga direndam dalam air es hingga tercapai suhu 7-10°C, kemudian dilakukan penambahan 4 ml NaOH 40 % tetes demi tetes. Campuran direfluks selama 1 jam dan suhu dipertahankan antara 7-10°C. Setelah 1 jam, proses refluks dilanjutkan
pada suhu kamar (sekitar 29-30°C) selama 4 jam. Selanjutnya, larutan dalam labu alas bulat dituang ke dalam gelas beker yang berisi air es selama beberapa menit
sampai terbentuk endapan. Endapan yang terbentuk disaring menggunakan corong Buchner, kemudian dilakukan reksristalisasi menggunakan pelarut etanol (Suwito dan Puspaningsih, 2010).
3.3.2 Reaksi antara senyawa 3,5-bis
-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dengan guanin (tahap 2)
Sejumlah 0,2260 gram (1,5 mmol) guanin, 0,4100 gram
3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on (1 mmol), 20 ml etanol, dan 5 ml HCl pekat dimasukkan ke dalam labu alas bulat leher tiga. Campuran tersebut direfluks
pada suhu 78°C selama 14 jam. Setelah proses refluks selesai, campuran didiamkan pada suhu kamar. Endapan yang terbentuk disaring menggunakan corong Buchner. Filtrat hasil penyaringan dimasukkan ke dalam botol vial dan
ADLN Perpustakaan Universitas Airlangga
dievaporasi sampai kering. Selanjutnya dilakukan pemisahan terhadap campuran
yang diperoleh (Fathalla, 2005).
3.3.3 Pemisahan senyawa hasil sintesis tahap 2 menggunakan kromatografi lapis tipis preparatif
Senyawa hasil sintesis tahap 2 yang masih dalam keadaan campuran
ditotol sepanjang garis bawah pelat silika secara berulang-ulang hingga membentuk pita. Setelah kering, pelat silika tersebut dimasukkan ke dalam bejana
besar yang telah jenuh oleh uap eluen. Aliran fasa gerak yang telah mencapai bagian atas pelat adalah tanda untuk menghentikan proses elusi. Selanjutnya, dilakukan pembacaan noda pada pelat menggunakan bantuan sinar ultraviolet.
Noda senyawa hasil sintesis pada plat silika dikerok dan direndam dalam kloroform selama beberapa jam, kemudian disaring. Setelah itu, dilakukan
penguapan terhadap filtrat yang diperoleh pada suhu kamar (Sherma and Fried, 2003).
3.3.4 Uji sifat fisika senyawa hasil sintesis
3.3.4.1 Uji titik leleh
Titik leleh senyawa hasil sintesis ditentukan menggunakan Fisher John Melting Point Apparatus. Sejumlah kecil sampel ditempatkan dalam blok
pemanas dengan pengontrol suhu. Selanjutnya, suhu dinaikkan secara perlahan dan dilakukan pengamatan terhadap senyawa saat mulai meleleh sampai tepat
meleleh secara keseluruhan. Perbedaan suhu suatu senyawa antara mulai meleleh dengan tepat meleleh seluruhnya tidak boleh melebihi 2°C (Shah, 2007).
22
3.3.5 Kromatografi lapis tipis
Uji kemurnian suatu senyawa dapat dilakukan menggunakan kromatografi lapis tipis. Senyawa yang berbentuk padat dilarutkan terlebih dahulu dalam pelarut yang sesuai. Selanjutnya, sampel senyawa dalam pipa kapiler ditotolkan di
atas plat KLT yang telah diberi tanda (origin) dan didiamkan sejenak untuk mengeringkan pelarut. Setelah kering, plat KLT tersebut dimasukkan ke dalam
chamber yang telah dijenuhkan dengan eluen atau fasa gerak. Selanjutnya, fasa
gerak akan mengalir ke bagian atas plat TLC. Plat tersebut diambil saat eluen tepat mencapai garis batas atas (solvent front). Setelah proses pemisahan selesai,
dilakukan proses pembacaan noda pada plat KLT dengan menggunakan bantuan lampu ultraviolet (Hamilton, 2008).
3.3.6 Analisis spektroskopi
3.3.6.1 Uji spektroskopi ultraviolet-visibel (UV-Vis)
Senyawa hasil sintesis dilarutkan dalam pelarut yang sesuai, kemudian
dimasukkan ke dalam kuvet dan diukur panjang gelombang maksimum menggunakan spektrofotometer UV-Vis. Sebelum pengukuran terhadap sampel
dilakukan, terlebih dahulu dimasukkan larutan blanko ke dalam instrumen tersebut.
3.3.6.2 Uji spektroskopi resonansi magnetik inti (NMR)
Senyawa hasil sintesis dilarutkan dalam pelarut aprotik yang sesuai, misalnya CDCl3. Kemudian larutan dalam tabung gelas kecil dimasukkan ke
dalam bagian tengah dari kumparan pada frekuensi gelombang radio. Hasil plot ADLN Perpustakaan Universitas Airlangga
dari energi yang diadsorbsi oleh sampel dengan frekuensi dari kumparan dapat
memberikan spektrum NMR (Hart et al., 2010).
24
- Refluks selama 4 jam (29-30°C) - Refluks selama 1 jam (7-10°C)
3.4 Skema Kerja
2,3-dimetoksibenzaldehid + N-metilpiperidin-4-on + etanol - + NaOH 40 % (7-10°C) Refluks (suhu 78°C) 14 jam
PLC
25
BAB IV
HASIL DAN PEMBAHASAN
4.1 Sintesis Senyawa 3,5-bis
-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on
Pada proses sintesis senyawa 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on digunakan dua bahan utama yakni 2,3-dimetoksibenzaldehid
dan N-metilpiperidin-4-on. Apabila ditinjau dari struktur kimia, secara teoritis kedua senyawa tersebut dapat mengalami reaksi kondensasi aldol silang dengan bantuan katalis basa kuat. Perbandingan mol kedua senyawa yang digunakan
dalam reaksi tersebut adalah 3:1 karena struktur senyawa target yang diharapkan
berbentuk bis. Senyawa yang memiliki H harus lebih sedikit jumlahnya supaya
benzaldehid dapat terikat pada kedua sisi N-metilpiperidin-4-on. Secara teoritis
perbandingan yang diperlukan hanya 2:1, namun pada penelitian ini perbandingan 3:1 lebih dipilih untuk menghindari reaksi antar senyawa N-metilpiperidin-4-on
yang dikhawatirkan masih dapat terjadi apabila perbandingannya 2:1.
Penambahan NaOH 40% sebagai katalis untuk membentuk ion enolat dilakukan pada suhu 7-10°C. Pengaturan suhu yang rendah dan penambahan
NaOH yang dilakukan tetes demi tetes bertujuan supaya suhu campuran reaksi tidak naik terlalu ekstrim. Awalnya proses refluks dilakukan dalam waktu 1
jam pada suhu 7-10°C, setelah itu dilanjutkan pada suhu ruang selama 4 jam.
26
Pergantian suhu ini dimaksudkan untuk mempercepat proses dehidrasi yang
merupakan tahap akhir reaksi. Selanjutnya, larutan dituang ke dalam air es dengan tujuan untuk mengendapkan senyawa hasil reaksi yang masih terdapat dalam cairan, sehingga diperoleh endapan dengan jumlah yang lebih maksimal.
Rekristalisasi endapan dilakukan menggunakan etanol (pelarut tunggal). Setelah dilakukan rekristalisasi, diperoleh padatan berbentuk kristal jarum kuning
sebanyak 1,006 gram dengan rendemen sebesar 81,79 %.
Gambar 4.1 Kristal senyawa analog calkon
Uji kemurnian terhadap senyawa hasil sintesis dilakukan menggunakan kromatografi lapis tipis. Proses uji dengan KLT dilakukan menggunakan 3 macam sistem eluen, yaitu n-heksana : etil asetat 7:3, 5:5, dan 3:7. Dari masing-masing
eluen yang digunakan, muncul satu noda pada senyawa hasil sintesis seperti yang tampak pada lampiran 1. Tabel 4.1 merupakan daftar nilai Rf yang diperoleh pada
masing-masing elusi.
Tabel 4.1 Nilai Rf senyawa hasil sintesis tahap 1
Eluen Nilai Rf
n-heksana : etil asetat (7:3) 0,25
n-heksana : etil asetat (5:5) 0,46
n-heksana : etil asetat (3:7) 0,76 ADLN Perpustakaan Universitas Airlangga
NaOH
Penentuan titik leleh senyawa hasil sintesis dilakukan menggunakan alat
Fisher-John Melting Point Apparatus. Selisih suhu sebesar 2°C saat zat mulai
dengan tepat meleleh merupakan suatu patokan yang sekaligus menandakan kemurnian suatu senyawa. Titik leleh senyawa hasil sintesis yang diperoleh
adalah sebesar 139,5- 141 °C.
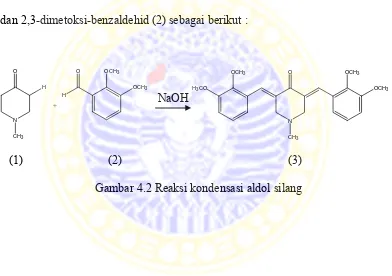
Reaksi dan mekanisme reaksi pembentukan senyawa 3,5-bis
-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on (3) dari N-metil-piperidin-4-on (1) dan 2,3-dimetoksi-benzaldehid (2) sebagai berikut :
N O
H
CH3
H
O OCH3
OCH3
+
N OCH3
H3CO
O OCH3
OCH3
CH3
(1) (2) (3)
Gambar 4.2 Reaksi kondensasi aldol silang
28
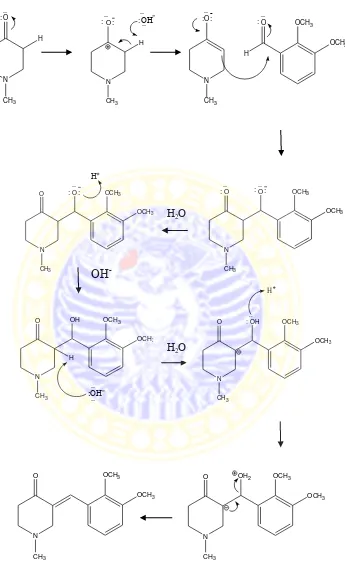
Gambar 4.3 Mekanisme reaksi pembentukan senyawa analog calkon
H2O
OH
H2O
ADLN Perpustakaan Universitas Airlangga
4.2. Hasil Analisis Spektroskopi
4.2.1 Hasil analisis spektroskopi UV
Senyawa hasil sintesis dianalisis menggunakan spektrofotometer UV-Vis dengan blanko metanol. Seperti yang dapat dilihat pada lampiran 2, panjang
gelombang maksimum senyawa hasil sintesis yang diperoleh dari pengukuran secara spektrofotometri UV-Vis adalah 329 nm. Daerah tersebut termasuk dalam
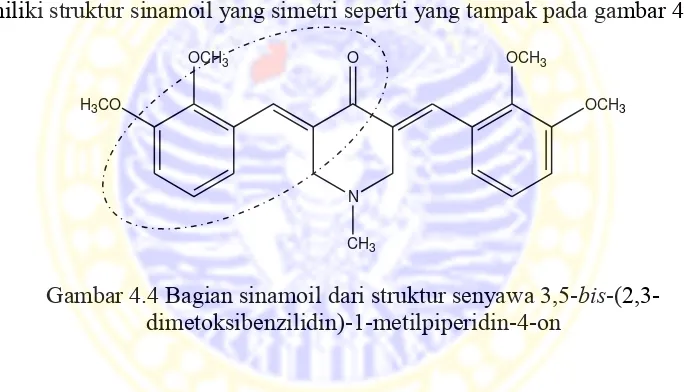
rentang serapan sinamoil yakni 300 - 550 nm (Bruice, 2003). Hal ini sesuai dengan senyawa 3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on yang memiliki struktur sinamoil yang simetri seperti yang tampak pada gambar 4.4.
N OCH3
H3CO
O OCH3
OCH3
CH3
Gambar 4.4 Bagian sinamoil dari struktur senyawa 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on
4.2.2 Hasil analisis spektroskopi resonansi magnetik inti (NMR)
Spektrum NMR terdiri dari dua jenis yakni 1H-NMR dan 13C-NMR. Pembacaan spektrum NMR senyawa hasil sintesis dapat dimulai dari spektrum karbon (13C-NMR) karena dapat menunjukkan jumlah atom karbon yang terdapat
pada senyawa tersebut. Dalam spektrum 13C-NMR senyawa hasil sintesis terdapat 13 sinyal yang muncul, seperti yang tampak pada lampiran 3. Namun, atom
karbon dalam senyawa tersebut berjumlah 23. Perbedaan jumlah tersebut menunjukkan terdapat beberapa atom karbon yang berada pada kondisi
30
lingkungan kimia yang sama dan ditunjukkan oleh intensitas ketinggian sinyal
yang muncul. Tabel 4.2 menunjukkan data pergeseran kimia dari spektrum 1H dan
13C-NMR senyawa 3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on.
Tabel 4.2 Data pergeseran kimia (δ, ppm) spektrum 1H dan 13C-NMR (CDCl3,
Keterangan : s = singlet, d = doublet, dd = doublet-doublet, dan t=triplet
N
Gambar 4.5 Penomoran atom C/H senyawa 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on
ADLN Perpustakaan Universitas Airlangga
Pada DEPT 135 terdapat 1 sinyal mengarah ke bawah pada pergeseran kimia 55,7 ppm yang menunjukkan metilen dan 7 sinyal mengarah ke atas.
Selanjutnya pada DEPT 90 muncul 4 sinyal yang menunjukkan keberadaan metin. Sinyal yang paling khas dalam spektrum 13C-NMR terdapat pada pergeseran
kimia 187 ppm yang menunjukkan adanya gugus karbonil dari keton. Gugus =CH- dan C= yang terletak di sebelah gugus karbonil mengalami deshielding
sehingga muncul pada pergeseran kimia 134,1 dan 129,7 ppm. Atom karbon
gugus metoksi ditunjukkan pada pergeseran kimia 57,1 dan 61,7 ppm. Atom C tersier (=CH-) benzena masing-masing ditunjukkan pada pergeseran kimia
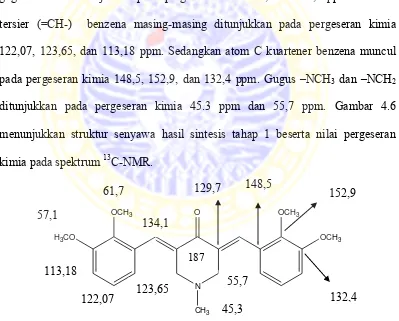
122,07, 123,65, dan 113,18 ppm. Sedangkan atom C kuartener benzena muncul pada pergeseran kimia 148,5, 152,9, dan 132,4 ppm. Gugus –NCH3 dan –NCH2
ditunjukkan pada pergeseran kimia 45.3 ppm dan 55,7 ppm. Gambar 4.6
menunjukkan struktur senyawa hasil sintesis tahap 1 beserta nilai pergeseran kimia pada spektrum 13C-NMR.
Gambar 4.6 Struktur dan pergeseran kimia 13C-NMR senyawa hasil sintesis tahap 1
Spektrum H-NMR menunjukkan sinyal pada pergeseran kimia 3,84 dan
3,91 ppm yang merupakan sinyal suatu metoksi dengan lingkungan kimia yang
32
berbeda. Gugus –NCH3 dan –NCH2 ditunjukkan pada pergeseran kimia 2,39 ppm
dan 3,6 ppm. Sedangkan pada pergeseran kimia 6,83 (dd, 2H), 6,97 (dd, 2H), dan 7,11 (t, 2H) ppm terdapat sinyal yang menunjukkan proton senyawa aromatis. Pergeseran kimia yang paling deshielding adalah =CH- yakni sebesar 8,04 ppm
karena terpengaruh oleh gugus karbonil. Gambar 4.7 menunjukkan struktur senyawa hasil sintesis tahap 1 beserta nilai pergeseran kimia dari spektrum 1
H-Gambar 4.7 Struktur dan pergeseran kimia 1H-NMR
senyawa hasil sintesis tahap 1
4.3 Reaksi antara Senyawa Analog Calkon 3,5-bis
-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dengan Guanin
Jika ditinjau dari strukturnya, reaksi yang terjadi antara senyawa analog
calkon dan guanin diawali oleh adisi nukleofilik. Hal yang mendasari reaksi
terletak pada gugus karbonil-,-tak jenuh senyawa analog calkon dan sifat
nukleofilik yang dimiliki oleh guanin. Secara keelektronegatifan, atom oksigen pada gugus karbonil (suatu enon) mempunyai kemampuan menarik elektron yang
jauh lebih besar dari karbon sehingga elektron lebih tertarik ke arah oksigen. Hal 6,83
tersebut menyebabkan atom karbon gugus karbonil semakin kekurangan elektron
dan bermuatan positif sehingga elektron pada ikatan rangkap yang terdapat di sebelah atom tersebut langsung berpindah untuk menetralkan muatan tersebut. Perpindahan elektron pada ikatan rangkap menyebabkan atom karbon yang
ditinggalkan bermuatan positif karena kekurangan elektron sehingga dalam kondisi tersebut, gugus amina bebas pada guanin akan menyerang atom karbon
tersebut. Sebelumya dapat dilakukan protonasi terlebih dahulu pada gugus karbonil oleh suatu elektrofil seperti ilustrasi pada gambar 4.8.
Protonasi terhadap gugus karbonil dapat terjadi dengan penambahan suatu
asam. Pada penelitian ini digunakan HCl pekat sebagai katalis yang bekerja sebagai agen protonasi untuk mempermudah terjadinya reaksi adisi. Pemilihan
HCl pekat dalam penelitian ini juga didasarkan pada pertimbangan kelarutan guanin (Sumardjo, 2008). Guanin sebagai bahan utama dalam reaksi hanya sebagian larut dalam etanol (pelarut senyawa analog calkon). Keberadaan asam
kuat seperti HCl pekat dimaksudkan untuk mempermudah kelarutan guanin dalam campuran reaksi.
34
N
Gambar 4.8 Prediksi mekanisme reaksi adisi nukleofilik antara senyawa analog calkon dengan guanin
Reaksi antara senyawa analog calkon dan guanin dalam penelitian ini
berlangsung pada suhu sekitar 78°C. Penggunaan suhu reaksi pada titik didih etanol (pelarut), selain untuk mempermudah kelarutan, juga dimaksudkan untuk mempercepat reaksi yang terjadi antara analog calkon dengan guanin.
Salah satu faktor penting dalam sintesis adalah waktu reaksi. Saat awal proses, terdapat sebagian campuran yang tidak larut. Pada jam ke-6, warna
campuran berubah menjadi kuning agak kecoklatan. Kemudian pada jam ke-10 terjadi perubahan warna menjadi kecoklatan yang konstan sampai jam ke 14. Dalam selang waktu 14 jam, campuran yang direaksikan tidak larut secara
sempurna melainkan masih terdapat endapan berwarna putih. Uji awal yang dapat digunakan untuk mengetahui terbentuknya suatu produk adalah dengan
melakukan KLT terhadap filtrat dan endapan. Setelah dilakukan KLT terhadap filtrat, didapatkan noda baru yang posisinya berbeda dengan bahan dasar. Noda baru pada analisis KLT jam ke-10 dan jam ke-14 menunjukkan intensitas yang
tidak jauh berbeda (dapat dikatakan hampir sama). Oleh karena itu, reaksi dihentikan pada jam ke -14. Setelah dilakukan pemisahan terhadap filtrat dan
36
endapan yang diperoleh menggunakan corong Buchner, dilakukan uji KLT
terhadap endapan. Hasil KLT menunjukkan bahwa endapan putih yang terdapat pada akhir reaksi memiliki hasil Rf yang sama dengan guanin. Selain itu, massa endapan putih tersebut juga tidak jauh berbeda dengan jumlah guanin yang
direaksikan, sehingga dapat disimpulkan bahwa guanin yang direaksikan hampir sebagian besar tidak bereaksi.
Proses KLT filtrat dilakukan menggunakan 3 macam eluen yang berbeda yaitu klorofom, n-heksana : etilasetat (7:3), dan n-heksana : etilasetat (9:1). Proses KLT menunjukkan bahwa hasil yang diperoleh masih berupa campuran senyawa
sehingga perlu dilakukan pemisahan lebih lanjut untuk memperoleh senyawa target. Tabel 4.3 merupakan daftar nilai Rf noda baru yang diperoleh pada
masing-masing elusi.
Tabel 4.3 Nilai Rf hasil sintesis tahap 2
Eluen Nilai Rf
n-heksana : etilasetat (7:3) 0,73
Kloroform 0,82
n-heksana : etil asetat (9:1) 0,51
4.4 Pemisahan Campuran Senyawa menggunakan Kromatografi Lapis Tipis Preparatif
Campuran kental hasil evaporasi dilarutkan dalam etanol kemudian ditotol pada plat KLTP. Setelah plat tersebut dielusi menggunakan eluen n-heksana : etil asetat (9:1), terlihat noda seperti yang tampak pada lampiran 4. Noda baru pada
plat dikerok menggunakan ujung pengaduk besi kemudian dilarutkan dalam ADLN Perpustakaan Universitas Airlangga
kloroform. Setelah campuran disaring dan diuapkan, diperoleh padatan dengan
jumlah yang sangat sedikit. Untuk menguji kemurnian, dilakukan proses KLT terhadap senyawa yang telah diperoleh menggunakan 3 sistem eluen yang berbeda seperti tampak pada lampiran 5. Tabel 4.4 merupakan daftar nilai Rf senyawa
hasil sintesis tahap kedua yang telah murni. Tabel 4.4 Data nilai Rf senyawa hasil sintesis
No. Eluen Rf
1. n-heksana : etil asetat (9:1) 0,51
2. Kloroform 0,77
3. n-heksana : etil asetat (5:5) 0,86
Setelah dilakukan proses pemisahan, diperoleh senyawa murni sebesar 3,2
mg dengan rendemen 0,59 %. Rendemen senyawa yang dihasilkan pada reaksi ini sangat kecil. Salah satu faktor yang mendasari hal tersebut adalah halangan ruang
dari senyawa calkon yang dapat menjadi penyebab utama sulitnya reaksi berlangsung. Selain itu, pH katalis yang digunakan dalam reaksi terlalu rendah.
Sebenarnya untuk reaksi pembentukan enamina atau imina diperlukan katalis pada pH 3-4. Apabila pHnya terlalu rendah, sebagian besar H+ justru akan
memprotonasi agen nukleofil yang digunakan sehingga gugus tersebut menjadi
tidak bersifat nukleofil lagi. Namun, pemilihan HCl dalam reaksi ini lebih diutamakan karena selain sebagai katalis, HCl juga dapat mempermudah kelarutan guanin dalam larutan.
38
4.5. Hasil Analisis Spektroskopi
4.5.1 Hasil analisis spektroskopi UV
Senyawa hasil sintesis dianalisis menggunakan spektrofotometer UV-Vis dengan blanko metanol. Spektrum UV menunjukkan 2 puncak pada panjang
gelombang 259 dan 308,5 nm seperti yang tampak pada lampiran 5. Intensitas puncak pada panjang gelombang 259 nm lebih tinggi dari pada puncak kedua.
Puncak tersebut merupakan bagian serapan dari basa guanin yang terdapat dalam struktur molekul karena basa-basa asam nukleat menyerap dengan kuat cahaya pada panjang gelombang 260 nm (Yuwono, 2002), sedangkan puncak kedua
merupakan bagian dari senyawa analog calkon yang mengalami penghalangan konjugasi oleh guanin, sehingga panjang gelombangnya turun menjadi 308,5 nm.
Berdasarkan spektrum UV yang diperoleh, diduga telah terjadi reaksi antara senyawa analog calkon 3,5-bis-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dengan guanin. Oleh karena itu, senyawa analog calkon 3,5-bis
-(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on dapat diduga mempunyai mekanisme reaksi sebagai alkylating agent terhadap basa guanin.
4.6 Senyawa Pengalkilasi dalam Mekanisme Alkylating Agent
Apabila senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on telah terbukti mempunyai mekanisme alkylating agent
terhadap guanin, maka senyawa ini dapat dikatakan masuk dalam golongan baru
dari senyawa pengalkilasi yang telah ditemukan (sebagai analog). Ilustrasi mekanisme reaksi yang terjadi antara senyawa analog calkon dengan basa guanin
ADLN Perpustakaan Universitas Airlangga
dapat dilihat pada gambar 4.8. Mekanisme tersebut terutama berlangsung pada
fase S, saat proses replikasi terjadi. Saat enzim helikase memisahkan untai ganda DNA menjadi untai tunggal DNA, maka pada saat inilah senyawa pengalkilasi tersebut bekerja dengan membentuk hubungan dengan basa DNA. Namun, proses
tersebut tidak sepenuhnya terjadi pada fasa replikasi karena senyawa-senyawa golongan agen pengalkilasi bersifat tidak spesifik terhadap siklus sel (Burke,
2006).
40
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on diduga dapat bereaksi dengan basa guanin.
2. Senyawa analog calkon 3,5-bis -(2,3-dimetoksibenzilidin)-1-metilpiperidin-4-on diduga mempunyai mekanisme reaksi sebagai alkylating agent terhadap basa guanin.
5.2 Saran
Dari penelitian ini perlu dilakukan studi dan penelitian lebih lanjut untuk menemukan metode reaksi yang sesuai antara senyawa analog calkon dan guanin
guna mendukung informasi penentuan struktur senyawa yang dihasilkan. ADLN Perpustakaan Universitas Airlangga
Achanta, G., Modzelewska, A., Feng, L., Khan, S., and Huang, P., A. 2006.
Boronic-Chalcone Derivative Exhibits Potent Anticancer Activity through Inhibition of the Proteasome. Mol Pharmacol., 70:426-433.
Blows, W. 2005. The Biological Basis of Nursing : Cancer.London: Routledge. Breiner, K., 2011. Tackling the Tumour Vasculature with Vaccines.Mednous.,
Vol 5, page 9.
Brooker, C. 2005. Ensiklopedia Keperawatan, Alih bahasa : Andry Hartono, Brahm U. Pendit, dan Dwi Widiarti. Jakarta : Penerbit Buku Kedokteran EGC.
Bruice, P.Y. 2003. Organic Chemistry, Fourth Edition. New Jersey: Prentice Hall. Brunton, L.L, Chabner, B.A., Knollmann, B.C.2010. Goodman and Gilman’s The
Pharmacological Basis of Therapeutics, 12th edition. California :
McGraw-Hill Companies, Inc.
Budavari, S. 2001. The Merck Index, An Encyclopedia of chemicals, Drugs and Biologicals, Thirdteen edition. USA : Merck & Co., Inc.
Burke, M.B., Wilkes, G.M. 2006. Cancer Therapies. Sudbury : Jones and Bartlett Publishers, Inc.
Campbell, N.A., Reece, J.B., and Mitchell, L.G. 2004. Biologi, Edisi kelima, terjemahan : Wasmen Manalu. Jakarta : Erlangga.
Chiaradia, L., 2008. Synthetic Chalcones as Efficient Inhibitors of Imycobacterium tuberculosis Protein Tyrosine Phosphatase PtpA.
Bioorg. Med. Chem. Lett 18: 6227-6230.
Curti, C., Gellis, A., and Vanelle, P., 2007.Synthesis of α,β-Unsaturated Ketones as Chalcone Analogues via a SRN1 Mechanism. Molecules,
12, 797-804.
Doyle, A and R.S.J.B. Griffith. 1988. Cell and Medical Research. New York: John Willey and sons Ltd.
Fathalla, O.A., Awad, S.M., Mohamed, M.S.,2005, Synthesis of New 2-thiouracyl-5-sulphonamide Derivates with Antibacterial and Antifungal Activity. Arch Pharm, res, 28, 1205-1212
Hamilton, R. 2008. Thin Layer Chromatography. London : John Wiley and sons.
42
Handika, H. 2010. Sintesis Calkon 3,5-Bis-(2,3-Dimetoksibenzilidin)-1-Metilpiperidin-4-On sebagai Senyawa Antikanker. Skripsi Program Studi S-1 Kimia Fakultas Sains dan Teknologi, Universitas Airlangga.
Harahap, Y. 2003. Rasio O6-alkilguanin dan tautan silang terhadap N7-alkilguanin yang terbentuk pada reaksi zat pengalkil dengan DNA In vitro Disertasi Program S3, Farmasi ITB, Bandung, 125–126.
Hart, H., Hadad, C.M., Craine, L., Hart, D. 2010. Organic Chemistry : a Short Course, Thirdteen Edition. Belmont: Brooks/Cole.
Hijova, E., 2006. Bioavailibility of Chalcones. Bratisl Lek Listy 107 (3): 80-84. Katzung, B.G. 2006. Basic and Clinical Pharmacology, 10th Edition.San
Francisco: Mc Graw Hill.
Krupadanam, G.L.D, Prasad, D.V., Rao, K.V., Reddy, K.L.N., Sudhakar, C. 2001.
Analytical Chemistry. Hyderabad : Universities Press.
Lodish, H., Berk, A., Matsuaira, P., Kaiser, C.A., Krieger, M., Scott, M.P., Zipursky, S.L., Darnell, J. 2004. Molecular Cell Biology, Fifth Edition. New York : WH Freeman.
Lullmann, H., Mohr, K., Ziegler, A., Bieger, D. 2000. Color Atlas of Pharmacology second edition revised and expanded. New York : Thieme.
Meric, B., Kerman, K., Ozkan, D., Kara, P., Erdem, A., Kucukoglu, O., Erciyas, E., and Ozsoz, M., 2002. Electrochemical Biosensor for the Interaction of DNA with the Alkylating Agent 4,4’-dihydroxy chalchone Based on Guanine and Adenine Signals.J. Pharm. Biomed. Anal., 30: 1339-1346.
Mortara, I. 2007. The International Union Against Cancer. International Union Against Cancer (UICC), Geneva : usoncologicaldisease.
Neal, M.J. 2006. At a Glance Farmakologi Medis, Edisi kelima, terjemahan : Juwalita Surapsari. Jakarta : Penerbit Erlangga.
Pavia, D.L., Lampman, G.M., Kriz, G.S. 2001. Introduction to Spectroscopy a Guide for Student of Organic Chemistry, Third Edition. London : Thomson Learning.
Pavia, D.L. 2005. Introduction to organic laboratory techniques: a small scale approach. Belmont : Brooks/Cole-Thomson Learning.
Pellegrini, F.2011.CliffsQuickReview Organic Chemistry II. Hoboken: Wiley Publishing, Inc.
ADLN Perpustakaan Universitas Airlangga
Shah, V. 2007. Handbook of plastics testing and failure analysis, Third Edition. New Jersey : John Wiley & Sons, Inc.
Sherma, J., Fried, B. 2003. Handbook of Thin Layer Chromatography, Third Edition, Revished, and Expanded. New York : Marcel Dekker, Inc. Silverstein, R.M., Webster F.X., Kiemle, D.J. 2005. Spectrometric Identification
of Organic Compound, Seventh Edition.Danvers: John Willey and Sons.
Singh, R. 2002. Chromatography.New Delhi : Mittal Publications.
Singh, P., Negi, J.S., Rawat, M.S.M., Pan, G.J., Bishoyi, A.K. 2011. Syntheses, Characterization and Antimicrobial Activity of
3-(Aminophenyl)-1,3-diphenylpropanones, Novel Aza-michael Products. Int.J.
ChemTech Res, Vol.3, No.2.
Stringer, J.L. 2006. Konsep Dasar Farmakologi Panduan untuk mahasiswa, terjemahan oleh Huriawati Hartanto. Jakarta : EGC.
Sturla, S.J. 2007. DNA adduct profiles: chemical approaches to addressing the biological impact of DNA damage from small molecules. Current Opinion in Chemical Biology, 11:293-299.
Stuart, B. 2004. Infrared Spectroscopy:Fundamentals and Application. Chichester :John Wiley & Sons.
Sumardjo, D. 2008. Pengantar Kimia Buku Panduan Kuliah Mahasiswa Kedokteran. Jakarta : Penerbit Buku Kedokteran EGC.
Suwito,H., Puspaningsih, N.N.T. 2010. Calkon Teranulasi sebagai Antagonis Onkoprotein MDM2 pada Terapi Antikanker. Laporan Hibah Penelitian Strategis Nasional: UNAIR.
Thurston, D.E. 2007.Chemistry and Pharmacology of Anticancer Drugs. Danvers: CRC Press.
Tjay, T.H., Raharja, K. 2007.Obat-obat Penting, Khasiat, Penggunaan, dan Efek Sampingnya, Edisi keenam. Jakarta : Gramedia.
Williamson, K.L., Masters, K.M. 2011. Macroscale and Microscale Organic Experiment, Sixth Edition. Belmont : Brooks/Cole.
Xu, R., Ye, Y., Zhao, W. 2011. Introduction to Natural Products Chemistry. Beijing : Science Press .
44
Yuwono, T. 2002. Biologi Molekular. Jakarta : Erlangga ADLN Perpustakaan Universitas Airlangga
LAMPIRAN
Lampiran 1
Hasil kromatografi lapis tipis senyawa hasil sintesis tahap 1
Keterangan : A= eluen n-heksana : etil asetat (7:3) B= eluen n-heksana : etil asetat (5:5) C= eluen n-heksana : etil asetat (3:7)
Lampiran 2
Spektrum UV senyawa analog calkon
ADLN Perpustakaan Universitas Airlangga
Lampiran 3
Spektrum 1H-NMR senyawa hasil sintesis tahap 1
Spektrum 13C-NMR senyawa hasil sintesis tahap 1
Spektrum 13C-NMR (BB dan DEPT 45, 90 dan 135) senyawa hasil sintesis tahap 1
ADLN Perpustakaan Universitas Airlangga
Lampiran 4
Pemisahan senyawa hasil sintesis tahap 2 menggunakan KLTP
Lampiran 5
Kromatogram senyawa hasil sintesis tahap kedua yang telah murni ADLN Perpustakaan Universitas Airlangga
Lampiran 6
Spektrum UV senyawa hasil sintesis tahap 2