INTISARI
Telah dilakukan penelitian tentang alopurinol dalam sampel obat, matriks biologis dan penelitian BKO dalam sediaan jamu sebelumnya pernah dilakukan dengan menggunakan sampel metampiron. Penelitian ini ingin mengetahui optimasi isolasi alopurinol dalam sampel tablet dan jamu untuk mengurangi berbagai matriks yang terdapat dalam sampel tablet dan jamu sehingga dapat digunakan untuk determinasi alopurinol. Optimasi isolasi dilakukan dengan optimasi penyaringan, ektraksi cair-cair dan Solid Phase Extraction (SPE).
Pada sampel tablet isolasi alopurinol dilakukan dengan penyaringan dan dideterminasi dengan metode Spektrofotometri UV karena alopurinol memiliki gugus kromofor dan auksokrom, sedangkan pada sampel jamu isolasi alopurinol dilakukan dengan clean up yang meliputi ekstraksi cair-cair dan Solid Phase Extraction (SPE) dan dideterminasi dengan metode High Performance Liquid Chromatography (HPLC).
Pada sampel tablet, volume penyaringan yang digunakan 10 mL x 2. Pada sampel jamu, volume kloroform yang digunakan pada ekstraksi cair-cair adalah 3x3 mL, pada SPE volume loading sampel yang digunakan adalah 1000 µL, volume eluen yang digunakan adalah 10 mL amonium hidroksida 5% dalam metanol. Kondisi tersebut merupakan kondisi optimal dalam isolasi alopurinol dari sampel tablet dan jamu.
ABSTRACT
There had been research on allopurinol in drug samples, biological matrix and BKO research in herbal preparations using sample methampyrone. This research investigates the optimal isolation of allopurinol in tablet and herbal samples to reduce the matrix contained in tablet and herbal samples, so later they can be used for the determination of allopurinol. Isolation optimization is done with filtration optimization, liquid-liquid extraction and Solid Phase Extraction (SPE).
In tablet samples, allopurinol isolation was performed by filtration and determined by UV spectrophotometry method because allopurinol has a chromophore and auxochrome group, whereas the allopurinol isolation of herbal samples performed with clean up that includes liquid-liquid extraction and Solid Phase Extraction (SPE) and determined by the High Performance Liquid Chromatography (HPLC).
In tablet samples, the filtration volume used was 10 mL x 2. In herbal samples, the volume of chloroform used in liquid-liquid extraction is 3x3 mL, at SPE sample loading volume used was 1000 mL, while the volume of eluent used was 10 mL ammonium hydroxide 5% in methanol. This condition is the optimal condition in allopurinol isolation from tablet and herbal samples.
OPTIMASI ISOLASI ALOPURINOL DALAM SEDIAAN TABLET DAN JAMU
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Sugiarto Adji Soenarso NIM: 108114020
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
OPTIMASI ISOLASI ALOPURINOL DALAM SEDIAAN TABLET DAN JAMU
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Sugiarto Adji Soenarso NIM: 108114020
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
Persetujuan Pembimbing
OPTIMASI ISOLASI ALOPURINOL DALAM SEDIAAN TABLET DAN JAMU
Skripsi yang diajukan oleh: Sugiarto Adji Soenarso
NIM: 108114020
Telah disetujui oleh:
Pembimbing Utama
iii
Pengesahan Skripsi Berjudul
OPTIMASI ISOLASI ALOPURINOL DALAM SEDIAAN TABLET DAN JAMU
Oleh:
Sugiarto Adji Soenarso NIM: 108114020
iv
HALAMAN PERSEMBAHAN
Jangan pernah menganggap belajar sebagai suatu
kewajiban, tetapi anggaplah ia sebagai suatu kesempatan
menyenangkan untuk membebaskan diri dalam mempelajari
alam dan kehidupan. Belajar adalah untuk kebahagiaanmu
sendiri dan akan memberikan keuntungan bagi masyarakat
tempatmu bekerja nanti
–
Albert Einstein
Kita hidup dalam dunia yang penuh dengan keindahan dan
petualangan. Tidak ada akhir dari
petualangan-petualangan yang dapat kita jalani hanya jika kita
mencari petualangan-petualangan baru dengan mata yang
terbuka
–
Jawaharlal Nehru
Orang-orang serius hanya punya ide-ide terbatas.
Orang-orang yang punya banyak ide tidak pernah serius
– Paul Vallery
Iman akan Allah tidak memberikan solusi instan atas
semua persoalan dan ketidakpastian hidup, tetapi
melengkapi kita untuk mengatasinya – Daniel Louw
Karya ini kudedikasikan untuk orang tuaku, adikku,
v
PERNYATAAN KEASLIAN KARYA
Penulis menyatakan dengan sesungguhnya bahwa skripsi yang ditulis ini tidak memuat karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila dikemudian hari ditemukan indikasi plagiarism dalam naskah ini, maka penulis bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 7 Januari 2015
Penulis
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertandatangan di bawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Sugiarto Adji Soenarso
NIM :108114020
Demi pengembangan ilmu pengetahuan, saya memberikan kepada perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
OPTIMASI ISOLASI ALOPURINOL DALAM SEDIAAN TABLET DAN JAMU
Beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikan di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang mana saya buat dengan sebenarnya. Dibuat di Yogyakarta
Pada tanggal: Yang menyatakan
vii PRAKATA
Segala pujian dan syukur penulis haturkan kepada Tuhan karena hanya dengan anugerah, berkat, cinta, kasih, dan pertolongan-Nya, penulis dapat menyelesaikan penelitian dan penyusunan skripsi yang berjudul ”Optimasi Isolasi Alopurinol Dalam Sediaan Tablet dan Jamu”. Skripsi ini disusun guna
memenuhi salah satu syarat untuk memperoleh gelar Sarjana Strata Satu Program Studi Farmasi (S.Farm).
Terselesaikannya penulisan laporan akhir ini tidak lepas dari bantuan berbagai pihak, karena itu penulis mengucapkan terima kasih kepada:
1. Aris Widayati, M.Si., Apt. PhD. selaku Dekan dan segenap staf serta karyawan Laboratorium Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Prof. Dr. Sri Noegrohati, Apt. selaku Dosen Pembimbing yang telah memberikan petunjuk, saran, arahan, dan bimbingan kepada penulis dalam proses penyusunan skripsi ini.
3. Jeffry Julianus, M.Si. selaku Dosen Penguji skripsi yang telah memberikan saran dan masukan demi kesempurnaan skripsi ini.
4. Florentinus Dika Octa Riswanto, M.Sc. selaku Dosen Penguji skripsi yang telah memberikan saran dan masukan demi kesempurnaan skripsi ini.
viii
6. PT IFARS Solo yang telah memberikan baku kepada penulis untuk penulis dapat menyelesaikan skripsi ini.
7. Phebe Hendra, M.Si., Apt., Ph.D. selaku dosen pembimbing akademik atas pendampingan dan perhatiannya terhadap perkembangan saya selama perkuliahan ini.
8. Dewi Setyaningsih dan Sanjaya, M.Si. atas bantuan selama menghadapi masalah dalam penelitian dan mau membagi ilmu yang tidak didapatkan selama kuliah.
9. Seluruh dosen dan karyawan Fakultas Farmasi Universitas Sanata Dharma atas ilmu, pengalaman, semangat, dan persahabatan yang telah dibagikan. 10. Mas Bimo, Mas Kunto, dan Pak Parlan yang telah banyak membantu selama
penelitian di laboratorium.
11. Keluarga tercinta Papa, Mama, dan Sugeng terima kasih atas dukungan doa yang selalu tulus untukku yang membuatku berani bangkit lagi di kala terpuruk.
12. Keluarga Papa dan Mama yang selalu mendoakan segala perjuanganku.
13. Ria Kusuma Dewi dan Meta Kartika Sari teman seperjuangkanku yang telah dengan sabar menghadapi semua kemalasanku, mendukung dan menyemangati aku selama masa-masa terpuruk di lab.
14. Kawan-kawan seperjuangan di lab: Bakti, Naomi, Kezia, Ita atas kerja sama dan kebersamaan, dukungan dan keceriaan di lab selama penelitian ini.
ix
16. Jo dan Nety atas bantuannya yang mau membantu aku saat aku bertanya tentang skripsiku ini.
17. Agatha Herny Sekar Natalia untuk momen-momen kebersamaan kita dan terima kasih buat dukungan dan doa serta semangat yang diberikan.
18. Teman-teman FST dan FKK 2010 yang selalu memberi bantuan, dukungan, dan berbagi keceriaan untuk selesainya skripsi ini.
19. Teman-teman KKN terima kasih atas keluangan waktu untuk bersama pergi sejenak dari penatnya skripsi.
20. Serta semua pihak yang telah banyak membantu penyusunan skripsi ini baik dalam bentuk doa, semangat yang menyertai penulis dari awal penelitian sampai penyelesaian skripsi ini yang tidak dapat disebutkan satu per satu.
Penulis menyadari bahwa penulisan skripsi ini masih banyak kekurangan dan kelemahan karena keterbatasan pikiran, tenaga, dan waktu penulis. Untuk itu penulis mengharapkan saran dan kritik yang membangun dari semua pihak. Akhir kata semoga skripsi ini dapat berguna dan bermanfaat bagi pembaca semua.
x DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
HALAMAN PERSETUJUAN PUBLIKASI ... vi
xi
H.High Performance Liquid Chromatography (HPLC) ... 19
I. Landasan Teori ... 26
J. Hipotesis ... 28
BAB III METODE PENELITIAN ... 29
A.Jenis dan Rancangan Penelitian ... 29
B.Variabel Penelitian dan Definisi Operasional ... 29
xii
2. Definisi operasional ... 29
C.Bahan Penelitian... 30
D.Alat Penelitian ... 30
E.Tata Cara Penelitian ... 31
1. Optimasi isolasi alopurinol dalam tablet dengan menggunakan spektrofotometri UV ... 31
2. Optimasi ekstraksi cair-cair tanpa SPE ... 33
3. Optimasi isolasi alopurinol dalam jamu asam urat merek X ... 34
4. Identifikasi alopurinol dalam sampel jamu dengan menggunakan HPLC ... 37
5. Validasi metode clean up SPE MCX ... 40
6. Penggunaan kembali SPE MCX ... 42
F. Analisis Hasil ... 43
1. Analisis hasil optimasi penyaringan dengan spektrofotometri UV ... 43
2. Analisis hasil optimasi clean up yang dilanjutkan dengan HPLC .... 43
BAB IV HASIL DAN PEMBAHASAN ... 44
1. Optimasi isolasi alopurinol dalam tablet dengan menggunakan spektrofotometri UV ... 44
2. Optimasi ekstraksi cair-cair tanpa SPE ... 50
3. Optimasi isolasi alopurinol dalam jamu asam urat merek X ... 52
4. Identifikasi alopurinol dalam sampel jamu dengan menggunakan HPLC ... 66
xiii
6. Penggunaan kembali SPE MCX ... 73
BAB V KESIMPULAN DAN SARAN... 77
A.Kesimpulan ... 77
B.Saran ... 77
DAFTAR PUSTAKA ... 78
LAMPIRAN ... 82
xiv
DAFTAR TABEL
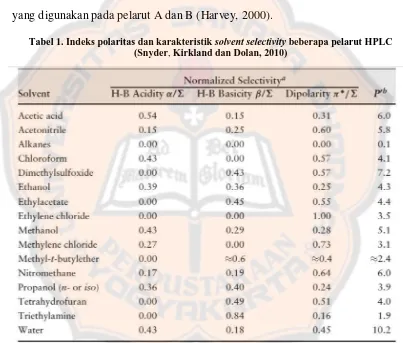
Halaman Tabel I. Indeks polaritas dan karakteristik solvent selectivity
beberapa pelarut HPLC ... 22
Tabel II. Optimasi loading sampel dan volume eluen SPE MCX ... 35
Tabel III. Pengulangan pencucian SPE ... 42
Tabel IV. Penyimpangan bobot rata-rata pada tablet ... 45
Tabel V. Hasil bobot alopurinol, SD, dan % CV ... 49
Tabel VI. Optimasi kapasitas kolom ... 56
Tabel VII. Optimasi volume eluen ... 60
Tabel VIII. Tabel tR dan AUC hasil ekstraksi cair-cair ... 65
Tabel IX. Perbandingan tR dan AUC blanko dan sampel adisi ... 68
Tabel X. Hasil perolehan kembali dan CV ... 71
Tabel XI. Perolehan kembali yang dapat diterima pada beberapa tingkat konsentrasi analit ... 72
xv
DAFTAR GAMBAR
Halaman Gambar 1. Struktur alopurinol ... 10 Gambar 2. Proses skematik prosedur SPE ... 13 Gambar 3. Diagram tingkat energi elektronik... 16 Gambar 4. (A) Pengaruh pelarut polar terhadap transisi π → π* (B) Transisi n → π* ... 18 Gambar 5. Dasar pemisahan kromatografi partisi ... 20 Gambar 6. Diagram sistem HPLC secara umum ... 20 Gambar 7. Skema sampler KCKT. (A) – posisi load, sampel diinjeksikan
dan terisolasi dari fase gerak. (B) – posisi inject, sampel terbawa fase gerak dan memasuki kolom ... 24 Gambar 8. Reaksi antara kalium biftalat dengan NaOH ... 46 Gambar 9. Perubahan warna indicator fenolftalein dari bening menjadi Gambar 12. Interaksi antara alopurinol dengan fase diam SPE ... 54 Gambar 13. Kromatogram alopurinol dalam fraksi asam asetat setelah
xvi
Gambar 15. Kromatogram alopurinol pada optimasi kapasitas kolom SPE MCX (A) 500 L (B) 750 L (C) 1000 L (D) baku alopurinol dengan fase gerak metanol : aquabidest/amonium hidroksida 0,1% (10:90) ... 57 Gambar 16. Kurva hubungan volume eluen VS AUC ... 60 Gambar 17. Kromatogram alopurinol pada optimasi volume eluen
(A) 5 mL (B) 7.5 mL (C) 12.5 mL yang dilakukan dengan mengelusi 10 mL (C1) dan dilanjutkan dengan elusi 2.5 mL (C2) (D) baku alopurinol dengan fase gerak metanol :
aquabidest/amonium hidroksida 0,1% (10:90) ... 61 Gambar 18. Reaksi pembentukkan garam alopurinol ... 63 Gambar 19. Reaksi pembentukkan ion alopurinol ... 64 Gambar 20. Kromatogram alopurinol hasil ekstraksi cair-cair dengan variasi
pengulangan penambahan kloroform (A) 2x3 mL (B) 3x3 mL (C) 4x3 mL dengan fase gerak HPLC metanol : aquabidest/ amonium hidroksida 0,1% (10:90) ... 64 Gambar 21. Perbandingan puncak (A) puncak baku alopurinol (B1 dan B2)
puncak blanko dan sampel alopurinol yang sudah ditambahkan dengan baku alopurinol dalam 3 level konsentrasi ... 67 Gambar 22. Kromatogram alopurinol hasil clean up dengan menggunakan
xvii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Sertifikat analisis baku alopurinol ... 83
Lampiran 2. Sertifikat analisis SPE MCX ... 84
Lampiran 3. Penimbangan keseragaman bobot tablet alopurinol ... 85
Lampiran 4. Penimbangan sampel A tiap kemasan untuk perhitungan keseragaman bobot ... 86
Lampiran 5. Penimbangan sampel B tiap kemasan untuk perhitungan keseragaman bobot ... 87
Lampiran 6. Penimbangan sampel C tiap kemasan untuk perhitungan keseragaman bobot ... 88
Lampiran 7. Penimbangan kalium biftalat ... 89
Lampiran 8. Standarisasi NaOH 0.1 N ... 89
Lampiran 9. Gambar hasil pembakuan NaOH 0.1 N ... 89
Lampiran 10. Perhitungan penimbangan sampel tablet alopurinol ... 90
Lampiran 11. Penimbangan optimasi penyaringan ... 90
Lampiran 12. Bobot alopurinol, SD dan %CV hasil ... 91
Lampiran 13. Penimbangan sampel tanpa SPE... 91
Lampiran 14. Kromatogram sampel tanpa SPE ... 92
Lampiran 15. Penimbangan optimasi kapasitas kolom SPE ... 93
Lampiran 16. Kromatogram optimasi kapasitas kolom SPE ... 94
Lampiran 17. Tabel optimasi kapasitas kolom SPE ... 100
xviii
Lampiran 19. Kromatogram optimasi volume eluen SPE ... 101
Lampiran 20. Tabel optimasi volume eluen SPE ... 105
Lampiran 21. Penimbangan optimasi volume kloroform ... 106
Lampiran 22. Kromatogram optimasi volume kloroform ... 107
Lampiran 23. Penimbangan baku untuk validasi SPE ... 110
Lampiran 24. Penimbangan sampel untuk validasi SPE ... 110
Lampiran 25. Kromatogram validasi SPE ... 111
Lampiran 26. Hasil recovery dan % CV validasi SPE ... 119
Lampiran 27. Penimbangan baku untuk pencucian SPE ... 120
xix INTISARI
Telah dilakukan penelitian tentang alopurinol dalam sampel obat, matriks biologis dan penelitian BKO dalam sediaan jamu sebelumnya pernah dilakukan dengan menggunakan sampel metampiron. Penelitian ini ingin mengetahui optimasi isolasi alopurinol dalam sampel tablet dan jamu untuk mengurangi berbagai matriks yang terdapat dalam sampel tablet dan jamu sehingga dapat digunakan untuk determinasi alopurinol. Optimasi isolasi dilakukan dengan optimasi penyaringan, ektraksi cair-cair dan Solid Phase Extraction (SPE).
Pada sampel tablet isolasi alopurinol dilakukan dengan penyaringan dan dideterminasi dengan metode Spektrofotometri UV karena alopurinol memiliki gugus kromofor dan auksokrom, sedangkan pada sampel jamu isolasi alopurinol dilakukan dengan clean up yang meliputi ekstraksi cair-cair dan Solid Phase Extraction (SPE) dan dideterminasi dengan metode High Performance Liquid Chromatography (HPLC).
Pada sampel tablet, volume penyaringan yang digunakan 10 mL x 2. Pada sampel jamu, volume kloroform yang digunakan pada ekstraksi cair-cair adalah 3x3 mL, pada SPE volume loading sampel yang digunakan adalah 1000 µL, volume eluen yang digunakan adalah 10 mL amonium hidroksida 5% dalam metanol. Kondisi tersebut merupakan kondisi optimal dalam isolasi alopurinol dari sampel tablet dan jamu.
xx
ABSTRACT
There had been research on allopurinol in drug samples, biological matrix and BKO research in herbal preparations using sample methampyrone. This research investigates the optimal isolation of allopurinol in tablet and herbal samples to reduce the matrix contained in tablet and herbal samples, so later they can be used for the determination of allopurinol. Isolation optimization is done with filtration optimization, liquid-liquid extraction and Solid Phase Extraction (SPE).
In tablet samples, allopurinol isolation was performed by filtration and determined by UV spectrophotometry method because allopurinol has a chromophore and auxochrome group, whereas the allopurinol isolation of herbal samples performed with clean up that includes liquid-liquid extraction and Solid Phase Extraction (SPE) and determined by the High Performance Liquid Chromatography (HPLC).
In tablet samples, the filtration volume used was 10 mL x 2. In herbal samples, the volume of chloroform used in liquid-liquid extraction is 3x3 mL, at SPE sample loading volume used was 1000 mL, while the volume of eluent used was 10 mL ammonium hydroxide 5% in methanol. This condition is the optimal condition in allopurinol isolation from tablet and herbal samples.
1 BAB I
PENDAHULUAN
A. Latar Belakang
Akhir-akhir ini kesadaran masyarakat akan kesehatan semakin meningkat, itu terlihat dari usaha masyarakat untuk mencegah penyakit baik secara modern maupun tradisional. Pada sebagian masyarakat, usaha untuk mencegah penyakit masih menggunakan cara tradisional. Selain itu kecenderungan masyarakat untuk kembali ke alam (back to nature) yang dalam beberapa hal lebih menguntungkan jika dibandingkan dengan pengobatan dengan obat sintetik atau obat modern, membuat penggunaan obat tradisional semakin meningkat. Selain itu, harga obat tradisional juga lebih terjangkau dibandingkan dengan obat sintetik. Obat tradisional adalah bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik) atau campuran dari bahan tersebut yang secara turun temurun telah digunakan untuk pengobatan, dan dapat diterapkan sesuai dengan norma yang berlaku di masyarakat (PerMenKes, 2012).
Produk obat tradisional yang telah banyak digunakan oleh masyarakat adalah jamu. Banyak masyarakat minum jamu untuk mencegah penyakit tertentu karena mudah penggunaannya dan harganyapun juga terjangkau oleh masyarakat. Selama beberapa tahun terakhir, penggunaan obat tradisional di dunia semakin meningkat. Menurut WHO, 65-80% populasi dunia menggunakan obat tradisional sebagai perlindungan untuk kesehatan (Yee, 2003).
Namun banyak kendala yang terjadi pada produk sediaan jamu seperti, pengolahan bahan baku yang belum terstandar terutama mutu dan kualitasnya, serta industri jamu yang tidak jujur sering kali menambahkan bahan kimia obat (BKO) ke dalam jamu sehingga menimbukan efek yang merugikan.
Karena tidak semua bahan baku untuk jamu dibudidayakan dengan baik dan benar sehingga seringkali tanaman obat tertentu hilang di pasaran karena ketidaktersediaan bahan baku yang dibutuhkan. Kurangnya penelitian ilmiah mengenai keefektifan dari jamu dan juga efek samping yang ditimbulkan melalui uji praklinis dan uji klinis oleh pihak terkait.
Menurut PerMenKes RI no. 007 tahun 2012 obat tradisional tidak boleh mengandung bahan kimia obat atau hasil sintesis yang berkhasiat sebagai obat. BKO yang biasanya ditambahkan dalam sediaan obat tradisional antara lain parasetamol (menghilangkan rasa sakit), fenilbutazon (mengatasi rematik dan menyegarkan tubuh), natrium diklofenak (mengatasi rematik), sildenafil sitrat (mengatasi disfungsi ereksi dan meningkatkan libido), sibutramin HCl (melangsingkan tubuh), dan alopurinol (menghilangkan asam urat).
Banyak masyarakat menggunakan obat modern untuk menyembuhkan penyakit yang mana pada obat modern dosis obatnya sudah diketahui secara pasti karena melihat bahaya jamu yang ditambahkan BKO. Salah satu penyakit yang biasa dialami oleh sebagian masyarakat adalah asam urat, sehingga banyak masyarakat menggunakan obat asam urat yaitu alopurinol untuk menyembuhkan asam urat.
Menurut Depkes RI (1974), metode baku analisis alopurinol dilakukan dalam sampel tablet dan diukur secara spektrofotometri UV. Pada sampel tablet memiliki matriks yang lebih sederhana, oleh karena itu untuk dapat mengisolasi alopurinol dari matriks dapat dilakukan dengan menggunakan penyaringan. Pada penelitian ini dilakukan pengembangan metode analisis alopurinol dalam sampel jamu.
Extraction (SPE) serta dilanjutkan dengan High Performance Liquid Chromatography (HPLC).
Metode clean up alopurinol dalam jamu dengan ekstraksi cair-cair dan
Solid Phase Extraction (SPE) diperlukan optimasi. Pada optimasi ekstraksi cair-cair dilakukan dengan mengubah komposisi volume kloroform, sedangkan pada optimasi SPE dilakukan dengan mengubah komposisi volume loading ekstrak dan volume eluen.
Penelitian ini merupakan bagian dari serangkaian penelitian yang
meliputi “Optimasi dan Validasi Penetapan Kadar Alopurinol Dalam Matriks
Tablet Obat Secara Spektrofotometri UV dan Matriks Sampel Jamu Asam Urat
Secara Kromatografi Cair Kinerja Tinggi” dan “Validasi Metode Analisis
Alopurinol Dalam Matriks Tablet Secara Spektrofotometri dan Matriks Jamu
Asam Urat Secara KCKT Fase Terbalik serta Aplikasinya.”
Sejauh penelusuran literatur oleh penulis penelitian tentang penetapan kadar alopurinol dalam jamu belum pernah dilakukan, sedangkan untuk penelitian bahan BKO lain seperti parasetamol dan fenilbutason sudah banyak dilakukan dan penelitian alopurinol dalam matriks biologis menggunakan metode cation exchange chromatography sudah pernah dilakukan. Untuk penelitian alopurinol di dalam tablet sudah pernah dilakukan.
1. Permasalahan
UV dan isolasi alopurinol dalam sediaan jamu asam urat dengan menggunakan SPE MCX yang dilanjutkan dengan HPLC fase terbalik?
2. Keaslian penelitian
Sejauh penelusuran literatur, penelitian terhadap alopurinol telah dilakukan dalam suatu obat. Namun penelitian sejenis yaitu penetapan kadar bahan kimia obat metampiron dalam jamu yang pernah dilakukan oleh Mayasari (2009), penelitian tentang alopurinol dalam metabolit biologis dengan cation exchange chromatography pernah dilakukan oleh Sweetman dan Nyhan (1969), dan penelitian tentang alopurinol dalam tablet secara spektrofotometer menggunakan CT Complex pernah dilakukan oleh Refat, dkk (2010). Demikian, maka dapat dipastikan bahwa perbandingan optimasi metode analisis secara HPLC dan Spektrofotometri UV alopurinol dalam jamu asam urat dan dalam sediaan tablet belum pernah dilakukan sebelumnya.
3. Manfaat penelitian
a. Manfaat metodologis. Penelitian ini diharapkan dapat memberikan informasi mengenai optimasi isolasi alopurinol dalam sediaan tablet secara spektrofotometer UV dan isolasi alopurinol dalam jamu asam urat dengan menggunakan SPE MCX yang dilanjutkan dengan HPLC.
B. Tujuan Penelitian
7 BAB II
PENELAAHAN PUSTAKA
A. Obat Tradisional
Obat tradisional adalah bahan atau ramuan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik) atau campuran dari bahan tersebut yang secara turun-temurun telah digunakan untuk pengobatan dan dapat diterapkan sesuai dengan norma yang berlaku di masyarakat (PerMenKes RI No. 007 Tahun 2012).
Sediaan obat tradisional ini perlu dilakukan berbagai jenis pengujian untuk mengetahui mutu dari sediaan obat tradisional yang akan diproduksi. Jenis pengujian ini meliputi pengujian mutu dan pengujian keamanan. Pengujian mutu meliputi organoleptik, kemasan, makroskopis, kebenaran simplisia, kadar air dan keseragaman bobot. Pengujian keamanan meliputi uji cemaran logam berat, cemaran pestisida, cemaran mikroba, zat tambahan yang diizinkan seperti bahan pengawet, cemaran aflatoksin dan penetapan ada tidaknya bahan kima obat yang ditambahkan dalam sediaan obat tradisional (KepMenKes RI no 661/MENKES/SK/VII/1994).
1. Jamu (obat tradisional warisan nenek moyang).
2. Obat Herbal Terstandar (telah dikembangkan berdasarkan bukti-bukti ilmiah, uji praklinis dan standarisasi bahan baku).
3. Fitofarmaka (telah melewati uji klinis dan standariasasi bahan baku).
B. Jamu
Jamu merupakan obat tradisional warisan nenek moyang yang dapat dibedakan menjadi 2 yaitu obat dalam dan obat luar. Obat dalam biasa dijumpai dalam bentuk herbal kering siap rebus, dalam bentuk segar rebusan dalam bentuk jamu gendong, dalam bentuk serbuk kering siap seduh. Obat luar bisa dimanfaatkan dengan cara dioles, digosok, direndam atau ditempel (Harmita, 2006).
Menurut PerMenKes No. 003 Tahun 2010, jamu harus memenuhi kriteria:
1. Aman sesuai dengan persyaratan yang ditetapkan. 2. Klaim khasiat dibuktikan berdasarkan data empiris. 3. Memenuhi persyaratan mutu yang berlaku.
Menurut Keputusan Kepala Badan POM No. HK.00.05.41.1384 tahun 2005 di dalam jamu dilarang digunakan:
1. Bahan kimia hasil isolasi atau sintetik yang berkhasiat obat. 2. Narkotika atau psikotropika.
Persyaratan mengenai jamu belum begitu mantap dan tegas, namun pemerintah telah mengeluarkan beberapa petunjuk yaitu:
1. Kadar air tidak lebih dari 10%. Ini untuk mencegah berkembangnya bakteri, kapang, dan khamir.
2. Jumlah kapang dan khamir tidak lebih dari 10000 3. Jumlah bakteri non patogen tidak lebih dari 1 juta 4. Bebas dari bakteri patogen
5. Tidak boleh tercemar atau diselundupi bahan kimia berkhasiat (Harmita, 2006).
C. Asam Urat
Asam urat merupakan senyawa kimia hasil akhir dari metabolism nucleic acid atau metabolisme purin dalam tubuh. Berdasarkan penyelidikan bahwa 90% dari asam urat merupakan hasil katabolisme purin yang dibantu oleh enzim guanase dan xanthine oksidase (Suhendi, Nurcahyanti, Muhtadi, Sutrisna, 2011).
D. Alopurinol
Gambar 1. Struktur alopurinol (1H-Pirazolo[3,4-d]pirimidin-4-ol) (DepKesehatan RI, 1995)
1. Sifat fisika kimia
Alopurinol mengandung tidak kurang dari 98% dan tidak lebih dari 101,0% C5H4N4O dihitung terhadap zat yang telah dikeringkan. Pemerian
berupa serbuk halus putih hingga hampir putih dan berbau lemah. Alopurinol sangat sukar larut dalam air dan etanol, larut dalam larutan kalium dan natrium hidroksida, praktis tidak larut dalam kloroform dan dalam eter (DepKes RI, 1995).
2. Dosis
Pada dewasa, dosis harian rata-rata adalah 2-10 mg/kgBB, 100-200 mg untuk kondisi ringan, 300-600 mg untuk kondisi cukup parah dan 700-900 mg untuk kondisi parah (Apotex NZ Ltd, 2011).
3. Peringatan dan pencegahan
Hati-hati pemberian pada penderita yang hipersensitif dan wanita hamil. Hindari penggunaan pada penderita dengan gagal ginjal atau penderita hiperurisemia asimptometik. Hentikan pengobatan dengan alopurinol bila timbul kulit kemerahan atau demam. Penggunaan jangka panjang dapat menyebabkan katarak. Selama pengobatan dianjurkan melakukan pemeriksaan mata secara berkala, hentikan pengobatan jika terjadi kerusakan lensa mata. Penggunaan pada wanita hamil, hanya bila ada pertimbangan manfaat dibandingkan resikonya. Alopurinol dapat meningkatkan frekuensi serangan artritis gout akut sehingga sebaiknya obat antiinflamasi atau kolkisin diberikan bersama pada awal terapi. Hati-hati bila diberikan bersama dengan vidarabin (DechaCare, 2014).
4. Efek samping
Reaksi hipersensitifitas: ruam mokulopapular didahului pruritus, urtikaria, eksofoliatif dan lesi pupura, dermatitis, nefritis, faskulitis dan syndrome poliartrtis. Demam, eosinophilia, kegagalan hati dan ginjal, mual, muntah, diare, rasa mengantuk, sakit kepala dan rasa logam (DechaCare, 2014).
5. Penetapan kadar
E. Ekstraksi
Ekstraksi adalah proses pemisahan satu atau lebih komponen dari suatu campuran homogen menggunakan pelarut cair (solven) sebagai separating agent
(Harborne, 1987). Pemilihan pelarut dan cara ekstraksi yang tepat dapat dipermudah dengan mengetahui terlebih dahulu zat aktif yang dikandung simplisia (Departemen Kesehatan Republik Indonesia, 1986).
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian sehingga memenuhi baku yang telah ditetapkan (Departemen Kesehatan Republik Indonesia, 1995).
F. Solid Phase Extraction (SPE)
1. Prosedur SPE
Tahap pertama menggunakan SPE adalah dengan mengkondisikan penjerap dengan pelarut yang sesuai. Penjerap nonpolar seperti C18 dan
penjerap penukar ion dikondisikan dengan mengalirinya menggunakan metanol lalu dengan akuades. Pencucian yang berlebihan dengan air akan mengurangi
recovery analit. Penjerap - penjerap polar seperti diol, siano, amino, dan silika harus dibilas dengan pelarut nonpolar seperti metilen klorida (Gandjar dan Rohman, 2010).
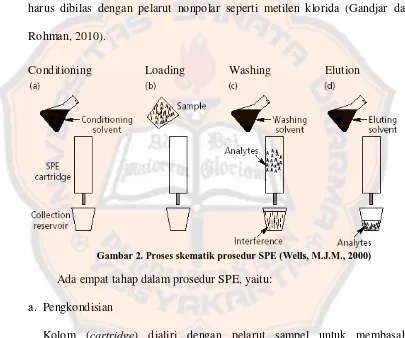
Gambar 2. Proses skematik prosedur SPE (Wells, M.J.M., 2000)
Ada empat tahap dalam prosedur SPE, yaitu: a. Pengkondisian
Kolom (cartridge) dialiri dengan pelarut sampel untuk membasahi permukaan penjerap dan untuk menciptakan nilai pH yang sama, sehingga perubahan-perubahan kimia yang tidak diharapkan ketika sampel dimasukkan dapat dihindari.
b. Retensi (tertahannya) sampel
Larutan sampel dilewatkan ke cartridge baik untuk menahan analit yang diharapakan, sementara komponen lain terelusi atau untuk menahan komponen yang tidak diharapkan sementara analit yang diharapkan terelusi. c. Pembilasan
Tahap ini penting untuk menghilangkan seluruh komponen yang tidak tertahan oleh penjerap selama tahap retensi.
d. Elusi
Tahap ini merupakan tahap terakhir untuk mengambil analit yang dikehendaki jika analit tersebut tertahan pada penjerap (Gandjar dan Rohman, 2010).
2. Pengembangan metode
Pendekatan empirik untuk melakukan pengembangan metode SPE melibatkan screening penjerap yang tersedia. Langkah pertama adalah menetukan penjerap mana yang paling baik dalam hal menahan analit yang dituju. Pertimbangan kedua adalah pelarut apa yang dibutuhkan untuk mengelusi analit yang dituju. Langkah ketiga adalah menguji matriks sampel blanko untuk mengevaluasi adanya pengganggu yang mungkin ada, dan akhirnya (langkah keempat) adalah menentukan recovery dengan menambah analit dalam jumlah tertentu harus dilakukan (Gandjar dan Rohman, 2010).
dalam penjerap nonpolar (seperti C18) digunakan pelarut nonpolar (Gandjar dan
Rohman, 2010).
G. Spektrofotometri UV
Spektrofotometeri UV merupakan salah satu teknik analisis spektroskopik yang menggunakan radiasi elektromagnetik UV dekat dengan menggunakan alat spektrofotometer (Skogg, West dan Holler, 1994). Radiasi elektromagnetik pada daerah UV dan visibel biasanya ditulis dalam satuan nanometer. Ketika sampel mengabsorbsi radiasi elektromagnetik (foton), terjadi perubahan energi pada sampel tersebut. Energi yang diserap mempunyai hubungan terhadap Persamaan Planck (Harvey, 2000).
Molekul yang dikenakan gelombang radiasi elektromagnetik pada frekuensi yang sesuai dapat terjadi penyerapan/absorpsi, adanya serapan tersebut menghasilkan perbedaan energi serapan. Selisih energi tersebut setara dengan energi foton yang diserap. Energi yang melompat dari keadaan dasar (ground state) ke keadaan tereksitasi (excited state) disebut dengan transisi.
Dimana, E1= energi pada keadaan dasar/lebih rendah E2= energi pada keadaan tereksitasi/lebih tinggi h = konstanta Planck
υ = frekuensi foton yang diabsorpsi/diserap
= panjang gelombang
c = kecepatan
Transisi yang terjadi antar molekul tidaklah sama, hal ini menyebabkan perbedaan spektra absorpsinya. Dengan demikian, spektra dapat digunakan sebagai bahan analisis kualitatif dan banyaknya molekul yang menyerap radiasi pada panjang gelombang tertentu setara dengan sinar yang diabsorpsi sehingga spektra juga dapat digunakan sebagai bahan analisis kuantitatif (Gandjar dan Rohman, 2010).
Pada analisis dengan spektrofometer, dilakukan pembacaan absorbansi yang disebut sebagai absorban (A) yang tidak memiliki satuan (Mulja dan Suharman, 1995). Spektrum absorpsi merupakan plot absorbansi analit yang merupakan fungsi dari panjang gelombang (Skogg, West dan Holler, 1994).
Gambar 3. Diagram tingkat energi elektronik (Gandjar dan Rohman, 2010)
Penyerapan foton yang dialami molekul mengakibatkan terjadinya eksitasi elektron-elektron ikatan. Transisi elektronik yang terjadi antara tingkat energi suatu molekul ada empat, yakni:
1. Transisi sigma–sigma star (σ → σ*)
Energi pada transisi ini terletak pada daerah < 180nm atau terjadi pada daerah UV vakum dan kurang begitu bermanfaat untuk analisis spektrofotometri UV-VIS (Gandjar dan Rohman, 2010).
2. Transisi non bonding elektron–sigma star (n → σ*)
Energi yang diperlukan untuk jenis transisi ini lebih kecil dibandingkan
yang lebih panjang (150–250nm). Kebanyakan transisi ini terjadi pada panjang gelombang < 200nm (Gandjar dan Rohman, 2010).
3. Transisi n → π* dan transisi π → π*
Transisi ini terjadi pada molekul organik yang memiliki gugus fungsional tidak jenuh, ikatan rangkap dalam gugus tersebut memberikan orbital phi yang diperlukan. Transisi jenis ini paling cocok digunakan dalam analisis menggunakan spektrofotometri UV–visibel karena berada diantara panjang gelombang 200–700 nm (Gandjar dan Rohman, 2010).
Pelarut dapat memberikan pengaruh transisi n → π* dan π → π*, hal ini
berkaitan dengan adanya perbedaan kemampuan dari pelarut untuk mensolvasi antara keadaan dasar dengan keadaan tereksitasi. Pada transisi π → π*, molekul yang berada dalam keadaan dasar akan relatif non polar dan keadaan tereksitasinya lebih polar dibandingkan dari keadaan dasar. Penggunaan pelarut polar akan menyebabkan interaksi lebih kuat saat keadaan tereksitasi
dibandingkan keadaan dasar sehingga perbedaan energi transisi π → π* lebih
kecil. Akibat yang ditimbulkan atas peristiwa ini ialah pergeseran ke panjang
gelombang yang lebih besar dari semula. Berbeda dengan transisi n → π*, pada
lebih pendek dibandingkan semula akibat kemampuan membentuk interaksi hidrogen (polaritas) pelarut meningkat (Gandjar dan Rohman, 2010).
Gambar 4. (A) Pengaruh pelarut polar terhadap transisi π → π* dan (B) Transisi n → π* (Gandjar dan Rohman, 2010)
Dalam memilih panjang gelombang terkait hubungan sifat optik cuplikan dan pelarut. Penyerapan radiasi UV atau visibel terkait dari elektron terluar atau elektron valensi dari molekul dan tergantung pula pada jenis ikatan kimia dalam molekul, adanya ikatan kimia penyebab terjadinya serapan sinar UV-Vis disebut kromofor (Johnson dan Stevenson, 1978). Sinar UV mempunyai panjang gelombang 200-400 nm, sedangkan sinar visibel mempunyai panjang gelombang 400-750 nm (Gandjar dan Rohman, 2010).
(A)
Kromofor merupakan ikatan rangkap tak jenuh selang-seling yang menyerap radiasi pada daerah UV dan visibel, sedangkan aukosokrom merupakan gugus jenuh yang terikat pada kromofor dapat menyebabkan adanya perubahan panjang gelombang dan intensitas serapan maksimum. Ciri auksokrom adalah gugusan heteroatom seperti –OCH3, -Cl, OH, dan NH2. Penambahan auksokrom
menyebabkan pergeseren batokromik. Pergeseran batokromik merupakan pergeseran panjang gelombang ke arah yang lebih panjang akibat adanya subsitusi gugus atau atom atau adanya pengaruh pelarut (Sastrohamidjojo, 2001).
H. High Performance Liquid Chromatography (HPLC)
Kromatografi merupakan teknik yang mana solut atau zat-zat terlarut terpisah oleh perbedaan kecepatan elusi, karena solut-solut ini melewati suatu kolom kromatografi. Pemisahan ini diatur oleh distribusi solut dalam fase gerak dan fase diam (Gandjar dan Rohman, 2010).
Gambar 5. Dasar pemisahan kromatografi partisi (Lennan, 2010)
Kromatografi partisi merupakan metode pemisahan analit berdasarkan kemampuan partisinya diantara fase diam dan fase gerak yang melewati fase diam. Analit yang mempunyai afinitas lebih besar pada fase diam (gambar 3 - bulatan merah) relatif lebih tertahan di fase diam daripada analit yang kurang tertahan pada fase diam (gambar 3 - bulatan hijau) (Lennan, 2010).
Gambar 6. Diagram sistem HPLC secara umum (Harvey, 2000)
kolom, detektor, wadah penampung buangan fase gerak, tabung penghubung, dan suatu komputer atau integrator atau perekam (Gandjar dan Rohman, 2010).
Wadah fase gerak harus bersih dan inert. Wadah ini biasanya mampu menampung fase gerak antara 1-2 liter pelarut. Fase gerak harus di degasing (penghilangan gas) dulu sebelum digunakan karena adanya gas akan berkumpul dengan komponen lain terutama di pompa dan detektor sehingga akan mengacaukan analisis. Pada saat membuat fase gerak, maka sangat dianjurkan untuk memilih fase gerak dengan kemurnian yang tinggi agar tingkat pengotor rendah dan tidak merusak sistem HPLC (Gandjar dan Rohman, 2010).
Fase gerak pada HPLC biasanya terdiri atas campuran pelarut yang dapat bercampur dan secara keseluruhan berperan dalam daya elusi dan resolusi. Daya elusi dan resolusi ini ditentukan berdasarkan polaritas pelarut, polaritas fase diam dan sifat komponen-komponen sampel. Untuk fase normal (fase diam lebih polar daripada fase gerak), kemampuan elusi meningkat dengan meningkatnya polaritas pelarut. Sedangkan untuk fase terbalik (fase diam kurang polar daripada fase gerak), kemampuan elusi akan menurun dengan meningkatnya polaritas pelarut (Gandjar dan Rohman, 2010).
Dasar pemilihan fase gerak dalam suatu metode pemisahan yaitu
berdasarkan pada indeks polaritas (P’) campuran fase gerak tersebut. Semakin
gerak tersebut akan menghasilkan nilai polaritas tersendiri yang disebut indeks polaritas fase gerak (Harvey, 2000).
�′ Φ . �′ + Φ . �′ (2)
Dengan ΦA dan ΦB merupakan fraksi volume pelarut yang digunakan
pada pelarut A dan B, sedangkan P’A dan P’B merupakan indeks polaritas pelarut
yang digunakan pada pelarut A dan B (Harvey, 2000).
Tabel 1. Indeks polaritas dan karakteristik solvent selectivity beberapa pelarut HPLC (Snyder, Kirkland dan Dolan, 2010)
berlangsung dengan tepat, reprodusibel, konstan dan bebas gangguan (Gandjar dan Rohman, 2010).
Metode pencampuran fase gerak dibedakan menjadi dua, yakni metode isokratik dan metode gradien. Metode isokratik merupakan metode pencampuran fase gerak secara manual dengan tangan dan saat memasuki sistem HPLC tidak dibutuhkan adanya pencampuran fase gerak kembali dan dilakukan dengan satu pompa. Metode gradien merupakan metode pencampuran fase gerak yang dilakukan di dalam sistem HPLC, dimana beberapa pompa digunakan untuk memompa pelarut ke dalam wadah pencampuran fase gerak dan hasil pencampuran fase gerak tersebut yang dialirkan ke dalam kolom (Snyder, Kirkland, dan Dolan, 2010).
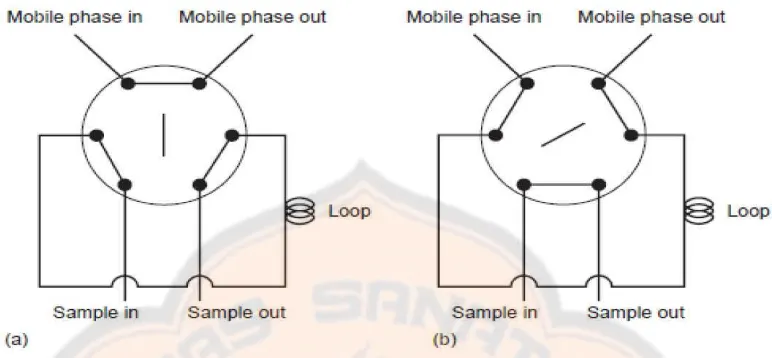
Penyuntikan sampel pada HPLC dilakukan secara langsung ke dalam fase gerak yang mengalir menuju kolom (Gandjar dan Rohman, 2010).
Gambar 7. Skema sampler KCKT. (A) – posisi load, sampel diinjeksikan dan terisolasi dari fase gerak. (B) – posisi inject, sampel terbawa fase gerak dan memasuki kolom (Harvey,
2000)
Kolom pada HPLC memuat fase diam, kebanyakan merupakan silika yang dimodifikasi secara kimiawi. Permukaan silika merupakan permukaan yang polar dan sedikit asam karena adanya residu gugus silanol (Si-OH). Modifikasi secara kimia akan menutupi gugus silanol dan menggantinya dengan gugus fungsional lain. Hasil reaksi kimiawi tersebut akan menghasilkan silika yang stabil terhadap hidrolisis karena terbentuk ikatan siloksan (Si-O-Si) (Gandjar dan Rohman, 2010).
Oktadesil silika (C18) merupakan fase diam yang paling banyak
Deteksi pada KCKT dibagi menjadi empat secara umum, yakni bulk property, sample specific, mobile-phase modification, dan hyphenated techiniques.
a. Bulk property detector. Detektor ini dianggap sebagai detektor universal yang dapat mengukur banyak komponen. Detektor ini memiliki keuntungan karena dapat mendeteksi semua senyawa, sekaligus memiliki kelemahan karena semua senyawa dari sampel yang terelusi akan terbaca sebagai sinyal. Secara umum, detektor universal memiliki sensitivitas yang rendah (Snyder, Kirkland, dan Dolan, 2010).
b. Sample specific detectors. Detektor ini merespon terhadap keunikan karakteristik yang dimiliki suatu analit karena beberapa karakteristik sampel mempunyai sifat unik yang mana tidak secara umum dimiliki oleh semua analit. Detektor UV merupakan detektor yang paling banyak digunakan dan merespon analit yang mengabsorbsi sinar UV pada panjang gelombang tertentu. Selain detektor UV, terdapat detektor lain seperti fluoresen dan detektor conduct electricity (Snyder, Kirkland, dan Dolan, 2010). Detektor UV-VIS dapat mengukur analit yang memiliki struktur kromoforik pada daerah panjang gelombang 190 – 800 nm. Detektor UV-VIS ini dapat berupa detektor dengan panjang gelombang tetap ataupun bervariasi (Gandjar dan Rohman, 2010).
perubahan reaksi analit dan detektor spektrometrik masa (Snyder, Kirkland, dan Dolan, 2010).
d. Hyphenated techniques. Teknik ini mengacu pada kopling dari analisis HPLC yang dipadukan dengan teknik lain, seperti LC-MS dan LC-IR (Snyder, Kirkland, dan Dolan, 2010).
Detektor pada HPLC idealnya memiliki beberapa karakteristik sebagai berikut:
Respon terhadap analit cepat dan reprodusibel
Mampu mendeteksi analit hingga kadar yang sangat kecil Stabil saat dioperasikan/digunakan
Memiliki sel volume yang kecil sehingga mampu meminimalkan pelebaran
pita.
Sinyal yang dihasilkan berbanding lurus dengan konsentrasi analit pada kisaran
luas/AUC
Tidak peka terhadap perubahan suhu dan kecepatan alir fase gerak.
Komputer atau integrator merupakan alat yang dihubungkan dengan detektor unuk mengukur sinyal yang dihasilkan dan diplotkan sebagai suatu kromatogram sehingga dapat dievaluasi oleh peneliti (Gandjar dan Rohman, 2010).
I. Landasan Teori
belum diterapkan secara semestinya sehingga mendorong beberapa pihak yang kurang bertanggung jawab untuk meningkatkan omsetnya dengan menambahkan bahan-bahan kimia obat untuk dapat memperoleh efek terapi yang cepat.
Penyakit asam urat banyak dialami oleh banyak masyarakat, oleh karena itu agar penyembuhannya cepat banyak masyarakat menggunakan obat. Obat untuk menyembuhkan asam urat adalah alopurinol.
Pada sampel tablet, digunakan pengukuran secara spektrofotometri UV untuk mengukur kadar alopurinol dalam matriks tablet. Sampel tablet disaring lalu diencerkan dan diukur dengan spektrofotometer UV. Parameter pengukuran dengan spektrofotometer UV, yaitu nilai presisi yang baik.
Sampel dipisahkan dengan cara ekstraksi cair-cair, dimana sampel jamu dilarutkan dalam NaOH karena kelarutan alopurinol terbesar terdapat dalam NaOH, kemudian diekstraksi dengan kloroform agar senyawa-senyawa organik larut dalam klorofom tetapi tidak melarutkan analit karena perbedaan polaritas, lalu dibuang fase organiknya kemudian dipisahkan lagi dengan Solid Phase Extraction MCX (Mixed Cation Exchanger) karena analit akan berikatan dengan SO3- dari fase diam SPE. Setelah analit berikatan dengan fase diam MCX, matriks
sampel dikeluarkan dengan mengaliri asam asetat dan metanol kemudian dilakukan elusi dengan amonium hidroksida 5% dalam metanol.
dengan SPE yang menunjukkan hasil optimum yaitu berkurangnya puncak-puncak senyawa selain alopurinol, Area Under Curve (AUC) alopurinol yang terbesar, resolusi tercapai ≥ 1,5 pada kromatogram
J. Hipotesis
1. Isolasi alopurinol dalam sampel tablet dilakukan dengan ekstraksi berulang dapat menghasilkan presisi yang baik.
2. Isolasi alopurinol dalam sampel jamu dilakukan dengan ekstraksi cair-cair dan dilanjutkan dengan SPE MCX dapat memberikan efisiensi clean up yang baik dengan berkurangnya puncak-puncak selain alopurinol, AUC terbesar, dan
29 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Jenis dan rancangan penelitian ini adalah eksperimental karena terdapat perlakuan terhadap subjek uji.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel
a. Variabel bebas
Variabel bebas dalam penelitian ini adalah komposisi volume kloroform, loading sampel, fase gerak (eluen), dan volume penyaringan.
b. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah absorbansi alopurinol, efisiensi clean up, nilai resolusi, dan AUC alopurinol.
c. Variabel pengacau terkendali
Kemurnian pelarut yang digunakan, dapat diatasi dengan mengunakan pelarut pro analysis yang memiliki kemurnian tinggi, sediaan tablet alopurinol, dan sampel jamu asam urat.
2. Definisi operasional
a. Alopurinol yang dianalisis merupakan senyawa aktif yang berada dalam sediaan tablet dan sampel jamu asam urat.
c. Sistem SPE yang digunakan adalah seperangkat alat Solid Phase Extraction
(SPE) dengan fase diam Mixed Cation Exchanger (MCX).
d. Optimasi volume ekstraksi kloroform dilakukan dengan memvariasikan volume kloroform, optimasi volume fase gerak dilakukan dengan mengubah volume fase gerak (eluen) dan optimasi kapasitas kolom dilakukan dengan mengubah volume (loading) sampel yang masuk ke dalam kolom SPE. e. Parameter pemisahan komponen dengan metode SPE dilanjutkan dengan
HPLC fase terbalik adalah dengan jumlah impurities yang sedikit, bentuk
peak, retention time, nilai resolusi, nilai tailing factor, dan nilai AUC alopurinol.
C. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah baku alopurinol yang diperoleh dari PT IFARS Solo, metanol p.a (E, Merck), ammonium hidroksida p.a (E, Merck), aquabides, aquadest yang diperoleh dari Laboratorium Farmasi USD, tablet alopurinol dan sampel jamu asam urat.
D. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah neraca analitik (OHAUS Carat Series PAJ 1003, max 60/120g, min 0,1 mg, d=0,01/0,1 mg, e = 1 mg), seperangkat alat KCKT fase terbalik dengan sistem isokratik dengan detektor ultraviolet, Shimadzu LC-2010C, kolom C-18 merek KNAUER C-18 (No. 25EE181KS (B115Y620), Dimensi 250 x 4,6 mm), seperangkat komputer (merk Dell B6RDZIS Connexant System RD01-D850 A03-0382 JP France S.A.S, printer
935922013), Spektrofotometer UV-Vis Mini Shimadzu, seperangkat catridge
SolidPhase Extraction (SPE) dengan fase diam Mixed Cation Exchanger (MCX) merek Waters (60 mg, 3 cc, ukuran partikel 30 m), desilator aquabidest merek Thermo Scientific, organic and anorganic solvent membrane filter (Whatman)
dengan ukuran pori 0,45 m, syringe, mikropipet Socorex, milipore filter, rotary
evaporator dan seperangkat alat-alat gelas (Pyrex).
E. Tata Cara Penelitian
1. Optimasi isolasi alopurinol dalam tablet dengan menggunakan spektrofotometri UV
a. Penyiapan sampel tablet alopurinol
Menyiapkan 20 tablet alopurinol. Tablet kemudian ditimbang satu per satu untuk menguji keseragaman bobot. Setelah dilakukan uji keseragaman bobot, tablet alopurinol dihomogenkan dengan menggunakan mortir dan stamper. Serbuk kemudian disimpan dalam wadah yang kering.
b. Pembuatan dan pembakuan larutan NaOH 0,1 N
Sejumlah 1 gram pelet NaOH dilarutkan dengan aquadest hingga semua larut sempurna dan dimasukkan ke dalam labu ukur 250 mL lalu diencerkan dengan aquadest hingga tanda batas.
Ditimbang lebih kurang 400 mg kalium biftalat secara seksama yang sebelumnya telah dihaluskan dan dikeringkan pada suhu 120oC selama 2 jam dan larutkan dalam 75 mL air bebas CO2 lalu tambahkan 2 tetes indikator fenolftalein
N NaOH =
(DepKes RI, 1995)
c. Optimasi penyaringan alopurinol
1) Optimasi penyaringan dengan menggunakan baku alopurinol
Penyaringan tanpa pembilasan. Baku sejumlah 50,0 mg ditimbang, dilarutkan dengan 20 mL NaOH lalu disaring dengan kertas saring dan dimasukkan ke dalam labu 50 mL diencerkan dengan NaOH hingga tanda batas. Larutan hasil penyaringan diambil 1,0 mL lalu diencerkan dengan NaOH ke dalam labu ukur 10 mL. Dari labu 10 mL yang pertama diambil lagi 1,0 mL diencerkan dengan NaOH ke dalam labu ukur 10 mL hingga tanda batas. Kemudian larutan ini disebut dengan larutan A.
Penyaringan diikuti dengan pembilasan. Baku sejumlah 50,0 mg ditimbang, dilarutkan dengan 10 mL NaOH lalu disaring dengan kertas saring, di dalam beaker glass dibilas lagi dengan 10 mL NaOH lalu disaring lagi dan dimasukkan ke dalam labu 50 mL dan diencerkan dengan NaOH hingga tanda batas. Larutan hasil penyaringan diambil 1,0 mL lalu diencerkan dengan NaOH ke dalam labu ukur 10 mL. Dari labu 10 mL yang pertama diambil lagi 1,0 mL diencerkan dengan NaOH ke dalam labu ukur 10 mL hingga tanda batas. Kemudian larutan ini disebut dengan larutan B.
Absorbansi larutan A dan B dibandingkan untuk mengetahui pengaruh perbedaan cara penyaringan larutan baku alopurinol.
2) Optimasi penyaringan dengan menggunakan tablet alopurinol
dimasukkan ke dalam labu 25 mL diencerkan dengan NaOH hingga tanda batas. Larutan hasil penyaringan diambil 1,0 mL lalu diencerkan dengan NaOH ke dalam labu ukur 10 mL. Dari labu 10 mL yang pertama diambil lagi 1,0 mL diencerkan dengan NaOH ke dalam labu ukur 10 mL hingga tanda batas. Kemudian larutan ini disebut dengan larutan C.
Penyaringan diikuti dengan pembilasan. Sampel tablet sejumlah 77 mg ditimbang, dilarutkan dengan 10 mL NaOH lalu disaring dengan kertas saring, di dalam beaker glass dibilas lagi dengan 10 mL NaOH, disaring lagi dan dimasukkan ke dalam labu 25 mL dan diencerkan dengan NaOH hingga tanda batas. Larutan hasil penyaringan diambil 1,0 mL lalu diencerkan dengan NaOH ke dalam labu ukur 10 mL. Dari labu 10 mL yang pertama diambil lagi 1,0 mL diencerkan dengan NaOH ke dalam labu ukur 10 mL hingga tanda batas. Kemudian larutan ini disebut dengan larutan D.
Absorbansi larutan C dan D dibandingkan untuk mengetahui pengaruh perbedaan cara penyaringan tablet alopurinol.
2. Optimasi ekstraksi cair-cair tanpa SPE
Sampel disaring dengan menggunakan kertas saring untuk menghilangkan pengotor yang masih ada. Volume sampel setelah disaring adalah 4 mL. Setelah disaring, sampel tidak dilewatkan pada SPE MCX. Sampel dipekatkan seluruhnya lalu dilarutkan dengan amonium hidroksida 5% dalam metanol sebanyak 10 mL, disaring dengan milipore dan diultrasonifikasi 15 menit. Sampel diinjeksikan ke dalam HPLC fase terbalik dengan kolom C18, komposisi fase gerak metanol : aquabidest/amonium hidroksida 0,1% (10:90), kecepatan alir 0,5 mL/menit, detektor UV dengan panjang gelombang 274 nm dan volume injeksi sebanyak 20 L (Sari, 2014). Hasil kromatogram yang didapat dibandingkan dengan kromatogram yang diperoleh pada langkah 3c.
3. Optimasi isolasi alopurinol dalam jamu asam urat merek X a. Penyiapan sampel jamu asam urat merek X
Menyiapkan 20 bungkus jamu asam urat merek X. Serbuk jamu kemudian ditimbang satu per satu untuk menguji keseragaman bobot. Setelah dilakukan uji keseragaman bobot, serbuk jamu dihomogenkan dengan menggunakan mortir dan stamper. Serbuk kemudian disimpan dalam wadah yang kering.
b. Optimasi clean up SPE MCX
Pada penelitian ini dilakukan optimasi kapasitas kolom dan volume eluen dengan menggunakan metode SPE penukar kation dengan fase diam MCX (Mixed Cation Exchanger) (Waters).
dengan memvariasi volume eluen yang digunakan untuk mengelusi SPE MCX. Kedua variasi tersebut dilakukan sesuai dengan Tabel II.
Langkah kerja yang dilakukan adalah menimbang sebanyak 0,5 g sampel jamu asam urat merek X kemudian dilarutkan ke dalam 10 mL NaOH 0,1 N. Sampel diekstraksi dengan menggunakan volume kloroform 3x3 mL, fase NaOH diambil dan ditambahkan HCl 0,1 N hingga pH menjadi 2.
Sampel disaring dengan menggunakan kertas saring untuk menghilangkan pengotor yang masih ada. Volume sampel setelah disaring adalah 4 mL. SPE MCX disiapkan, dikondisikan (conditioning) dengan berturut-turut mengaliri 1 mL metanol p.a. dan 1 mL aquabidest ke dalam kolom SPE MCX kemudian tetesan ditampung pada flakon.
Tabel II. Optimasi loading sampel dan volume eluen SPE MCX
Loading ekstrak sampel ( L) Volume eluen (mL)
Sampel hasil pengelusian diinjeksikan ke dalam HPLC fase terbalik dengan kolom C18, komposisi fase gerak metanol : aquabidest/amonium hidroksida 0,1% (10:90), kecepatan alir 0,5 mL/menit, detektor UV dengan panjang gelombang 274 nm dan volume injeksi sebanyak 20 L (Sari, 2014). Hasil kromatogram yang didapat, diamati bentuk peak dan nilai AUC untuk mengetahui hasil yang optimal dari proses optimasi clean up SPE MCX.
c. Optimasi ekstraksi cair-cair
Pada penelitian ini dilakukan optimasi clean up cair-cair dengan memvariasi pengulangan ekstraksi cair-cair dengan pelarut organik, yaitu 2x3 mL, 3x3 mL, dan 4x3 mL.
Langkah kerja yang dilakukan adalah menimbang sebanyak 0,5 g sampel jamu asam urat merek X kemudian dilarutkan ke dalam 10 mL NaOH 0,1 N. Sampel diekstraksi dengan menggunakan jumlah pengulangan ekstraksi dengan pelarut organik yang berbeda-beda, yaitu 2x3 mL, 3x3 mL, dan 4x3 mL, fase NaOH diambil dan ditambahkan HCl 0,1 N hingga pH menjadi 2.
Sampel disaring dengan menggunakan kertas saring untuk menghilangkan pengotor yang masih ada. Volume sampel setelah disaring adalah 4 mL. Setelah disaring, sampel diloading ke dalam SPE dan dielusi sesuai dengan hasil optimasi pada langkah 3b. Sampel dipekatkan seluruhnya lalu dilarutkan dengan amonium hidroksida 5% dalam metanol sebanyak 10 mL, disaring dengan
milipore dan diultrasonifikasi 15 menit.
kecepatan alir 0,5 mL/menit, detektor UV dengan panjang gelombang 274 nm dan volume injeksi sebanyak 20 L (Sari, 2014). Hasil kromatogram yang didapat, diamati bentuk peak dan nilai AUC untuk mengetahui hasil yang optimal dari proses optimasi ekstraksi cair-cair.
4. Identifikasi alopurinol dalam sampel jamu dengan menggunakan HPLC
Pada penelitian ini dilakukan identifikasi alopurinol dalam sampel jamu dengan menggunakan HPLC. Cara yang dilakukan adalah dengan cara membandingan waktu retensi, bentuk puncak, dan nilai AUC antara baku alopurinol, blanko sampel jamu, dan sampel jamu yang ditambah baku alopurinol yang bertujuan untuk mengetahui apakah dalam sampel jamu terdapat alopurinol.
Langkah kerja yang dilakukan adalah
a. Pembuatan larutan stok baku alopurinol. Ditimbang secara seksama lebih kurang 25 mg baku alopurinol, lalu dimasukkan ke dalam labu ukur 25 mL dan dilarutkan dengan dengan amonium hidroksida 5% dalam metanol hingga tanda.
b. Pembuatan larutan intermediet alopurinol. Larutan intermediet dibuat dengan konsentrasi 500 g/mL dengan cara mengambil sebanyak 5 mL dari larutan stok baku alopurinol, dimasukkan labu ukur 10 mL dan diencerkan dengan amonium hidroksida 5% dalam metanol hingga tanda.
c. Pembuatan larutan baku alopurinol dengan konsentrasi 30 g/mL. Diambil
sejumlah 600 L larutan intermediet alopurinol kemudian dimasukkan ke
Larutan baku alopurinol diinjeksikan ke dalam HPLC fase terbalik dengan kolom C18, komposisi fase gerak metanol : aquabidest/amonium hidroksida 0,1% (10:90), kecepatan alir 0,5 mL/menit, detektor UV dengan panjang gelombang 274 nm (Sari, 2014).
d. Penyiapan blanko sampel jamu
Sebanyak 0,5 g sampel jamu asam urat merek X ditimbang dilarutkan dengan 10 mL NaOH 0,1 N. Sampel diekstraksi dengan kloroform 3 mL sebanyak 3x. Didapatkan 2 fase pemisahan, diambil fase air (bagian atas), tampung dalam beaker glass. Fase air ditambah HCl 0,1 N hingga pH 2. Sampel disaring dengan menggunakan kertas saring untuk menghilangkan endapan yang timbul saat penambahan HCl sedemikian rupa sehingga hasil penyaringan adalah 4 mL.
e. Penyiapan sampel dalam matriks jamu
Sebanyak 0,5 g sampel jamu asam urat merek X ditimbang dilarutkan dengan 10 mL NaOH 0,1 N. Sampel diekstraksi dengan kloroform 3 mL sebanyak 3x. Didapatkan 2 fase pemisahan, diambil fase air (bagian atas), tampung dalam beaker glass. Fase air ditambah HCl 0,1 N hingga pH 2. Sampel disaring dengan menggunakan kertas saring untuk menghilangkan endapan yang timbul saat penambahan HCl sedemikian rupa sehingga hasil penyaringan adalah 4 mL.
Sampel ditambah dengan seri larutan baku alopurinol sebanyak 200
L pada konsentrasi 5 g/mL, 15 g/mL, 30 g/mL dan 100 L, 200 L, dan
300 L dari larutan intermediet sehingga diperoleh massa alopurinol yang ditambahkan sebanyak 51 ng, 103 ng, dan 156 ng. SPE dikondisikan dengan mengaliri 1 mL metanol p.a. dan 1 mL aquabidest, lalu dilakukan loading
ekstrak sampel sebanyak 1000 L ke dalam kolom SPE. Kolom SPE MCX dicuci dengan mengaliri 2 mL asam asetat 2% dan 2 mL metanol. Selanjutnya dielusi dengan 10 mL amonium hidroksida 5% dalam metanol. Fraksi hasil elusi diuapkan seluruhnya lalu dilarutkan kembali dengan amonium hidroksida 5% dalam metanol sebanyak 10 mL lalu disaring dengan menggunakan
Hasil kromatogram yang didapat dari langkah 4c, 4d, dan 4e, diamati waktu retensi, bentuk peak, dan nilai AUC alopurinol lalu dibandingkan antara baku alopurinol, blanko sampel jamu, dan sampel yang ditambah baku alopurinol.
5. Validasi metode clean up SPE MCX
Validasi dilakukan pada hasil optimasi kapasitas kolom dan volume eluen. Proses validasi dilakukan dengan menghitung akurasi dan presisi. Akurasi dinyatakan dengan % perolehan kembali. Sampel ditambah dengan baku sebanyak 200 µl pada 3 level konsentrasi yaitu 5 µg/mL, 15 µg/mL, 30 µg/mL, dan 100 L, 200 L, dan 300 L dari larutan intermediet sehingga diperoleh massa alopurinol yang ditambahkan sebanyak 51 ng, 103 ng, dan 156 ng (dilakukan 5 kali replikasi). % perolehan kembali dihitung dengan menggunakan rumus:
% perolehan kembali =
x 100%
Presisi dinyatakan dengan % CV yang menunjukkan persentase penyimpangan data yang terjadi. Koefisien variasi (CV) dihitung pada setiap replikasi dengan rumus:
% CV =
x 100%
Langkah kerja yang dilakukan adalah
b. Pembuatan larutan intermediet alopurinol. Larutan intermediet dibuat dengan konsentrasi 500 g/mL dengan cara mengambil sebanyak 5 mL dari larutan stok baku alopurinol, dimasukkan labu ukur 10 mL dan diencerkan dengan amonium hidroksida 5% dalam metanol hingga tanda.
c. Pembuatan seri larutan baku alopurinol. Diambil sejumlah 100 L, 300 L, dan 600 L larutan intermediet alopurinol kemudian masing-masing dimasukkan ke dalam labu ukur 10 mL. Masing-masing labu ukur diencerkan dengan amonium hidroksida 5% dalam metanol hingga tanda, sehingga diperoleh
konsentrasi 5 g/mL, 15 g/mL, dan 30 g/mL.
d. Penyiapan sampel dalam matriks jamu
Sebanyak 0,5 g sampel jamu asam urat merek X ditimbang dilarutkan dengan 10 mL NaOH 0,1 N. Sampel diekstraksi dengan kloroform hasil optimasi ekstraksi cair-cair. Didapatkan 2 fase pemisahan, diambil fase air (bagian atas), tampung dalam beaker glass. Fase air ditambah HCl 0,1 N hingga pH 2. Sampel disaring dengan menggunakan kertas saring untuk menghilangkan endapan yang timbul saat penambahan HCl sedemikian rupa sehingga hasil penyaringan adalah 4 mL.
Sampel ditambah dengan seri larutan baku alopurinol sebanyak 200
L pada konsentrasi 5 g/mL, 15 g/mL, 30 g/mL dan 100 L, 200 L, dan
300 L dari larutan intermediet sehingga diperoleh massa alopurinol yang ditambahkan sebanyak 51 ng, 103 ng, dan 156 ng. SPE dikondisikan dengan mengaliri 1 mL metanol p.a. dan 1 mL aquabidest, lalu dilakukan loading
Kolom SPE MCX dicuci dengan mengaliri 2 mL asam asetat 2% dan 2 mL metanol. Selanjutnya dielusi dengan 10 mL amonium hidroksida 5% dalam metanol. Fraksi hasil elusi diuapkan seluruhnya lalu dilarutkan kembali dengan amonium hidroksida 5% dalam metanol sebanyak 10 mL lalu disaring dengan menggunakan milipore kemudian diultrasonifikasi selama 15 menit. Diinjeksikan sebanyak 9 µ l untuk adisi 5 µg/mL, 20 µl untuk adisi 15 µg/mL dan 21 µl untuk adisi 30 µg/mL ke dalam HPLC fase terbalik dengan kolom C18, komposisi fase gerak metanol : aquabidest/amonium hidroksida 0,1% (10:90), kecepatan alir 0,5 mL/menit, detektor UV dengan panjang gelombang 274 nm dan volume injeksi sebanyak 20 L (Sari, 2014). Hasil kromatogram yang didapat, diamati nilai AUC lalu dihitung nilai akurasi dan presisi.
6. Penggunaan kembali SPE MCX
Tujuan penelitian ini adalah untuk mengetahui apakah SPE yang telah dipakai dapat digunakan kembali dengan cara melakukan pencucian SPE bekas/yang sudah pernah dipakai kembali setelah dicuci menurut suatu siklus pencucian. Pada penelitian ini digunakan variasi pengulangan pencucian SPE seperti yang tertera pada tabel III.
Tabel III. Pengulangan pencucian SPE
Variasi pengulangan
Urutan siklus pencucian
1x Dalam 1x siklus pencucian SPE dilakukan dengan cara berturut-turut mengaliri SPE dengan metanol p.a.; aquabidest;
NaOH 0,1N; HCl 0,1N; aquabidest; dan metanol p.a. 2x
Setelah pencucian SPE, SPE digunakan sesuai dengan tata cara penelitian langkah 3b. Tahap loading ekstrak sampel dimasukkan 1000 L larutan baku alopurinol dengan konsentrasi 30 g/mL yang akan dijelaskan berikutnya pada langkah 4.
Fraksi hasil elusi diinjeksikan ke dalam HPLC fase terbalik dengan kolom C18, komposisi fase gerak metanol : aquabidest/amonium hidroksida 0,1% (10:90), kecepatan alir 0,5 mL/menit, detektor UV dengan panjang gelombang 274 nm dan volume injeksi sebanyak 20 L (Sari, 2014).
Hasil kromatogram yang didapat pada pencucian SPE 1x, 2x, dan 3x dibandingkan untuk mengetahui sampai berapa kali pencucian SPE dilakukan agar SPE dapat dipakai kembali.
F. Analisis Hasil
1. Analisis hasil optimasi penyaringan dengan spektrofotometri UV
Data absorbansi yang diperoleh dari hasil optimasi penyaringan ditetapkan nilai presisi dari penyaringan alopurinol dalam matriks tablet.
2. Analisis hasil optimasi clean up yang dilanjutkan dengan HPLC
Data kromatogram yang diperoleh dari hasil optimasi clean up
44 BAB IV
HASIL DAN PEMBAHASAN
1. Optimasi isolasi alopurinol dalam tablet dengan menggunakan spektrofotometri UV
Penetapan kadar alopurinol dalam tablet (DepKes RI 1974) dilakukan pengembangan metode dengan melarutkan alopurinol dalam NaOH 0,1 N dan dilakukan pengenceran 2500 kali. Larutan intermediet disaring dan diukur pada panjang gelombang maksimum secara spektrofotometri UV.
a. Penyiapan sampel tablet alopurinol
Sampel yang digunakan dalam penelitian ini adalah sediaan tablet alopurinol yang banyak beredar di pasaran. Analit yang ingin dianalisis adalah alopurinol yang terdapat dalam tablet. Pertama-tama menyiapkan 20 tablet alopurinol, lalu kemudian sampel ditimbang satu per satu untuk uji keseragaman bobot dimana fungsi dari uji keseragaman bobot adalah untuk memastikan bobot tablet yang seragam karena dengan seragamnya bobot tablet maka dosis yang terkandung juga seragam.



![Gambar 1. Struktur alopurinol (1H-Pirazolo[3,4-d]pirimidin-4-ol) (DepKesehatan RI, 1995)](https://thumb-ap.123doks.com/thumbv2/123dok/857132.609390/33.595.98.513.97.544/gambar-struktur-alopurinol-h-pirazolo-pirimidin-depkesehatan-ri.webp)