5
I. TINJAUAN PUSTAKA
1.1 Kacang Gude (Cajanus cajan (L.) Millsp.)
Kacang gude atau pigeon pea memiliki banyak nama lokal di Indonesia yaitu kacang hiris (Sunda), kacang Bali, ritiklias (Sumatera), kacang kayu (Jawa), kance (Bugis), kacang kaju (Madura), kacang undis (Bali), lebui, legui, kacang iris, kacang turis, puwe jai (Halmahera), dan fou hate (Ternate dan Tidore). Tanaman ini diduga berasal dari Afrika. Pusat keanekaragaman yang kedua adalah India, dan sekarang sudah tersebar hingga Negara-Negara tropika dan sub tropika. Daerah penanaman kacang gude di Indonesia adalah Yogyakarta, Surakarta, Madiun, Bondowoso, Malang, Probolinggo, Bali, Nusa Tenggara Barat, dan Nusa Tenggara Timur (Susila et al., 2012).
Klasifikasi kacang gude adalah sebagai berikut (Anon., tt): Kingdom : Plant
Sub Kingdom : Tracheobionta Super Divisi : Spermatophyta Divisi : Magnoliophyta Kelas : Magnoliopsida Sub Kelas : Rosidae Ordo : Fabales Famili : Fabaceae Genus : Cajanus Adans
Spesies : Cajanus cajan (L.) Millsp.
Kacang gude dapat tumbuh pada ketinggian 0-1800 m di atas permukaan laut, pH tanah 5-7, suhu lingkungan 18-300C. Tanaman ini cukup toleran terhadap kekeringan. Penanaman dilakukan menggunakan benih dengan jarak tanam 40 x 30 cm. Pemberian unsur S dapat meningkatkan hasil panen. Sebenarnya tanaman dapat menghasilkan sampai 3 – 5 tahun, namun hasilnya akan lebih kecil dibandingkan panen tahun pertama (Susila et al., 2012). Tanaman dan biji kacang gude dapat dilihat pada Gambar 1.
Gambar 1. Tanaman Kacang Gude (Emefiene et al.,2014)
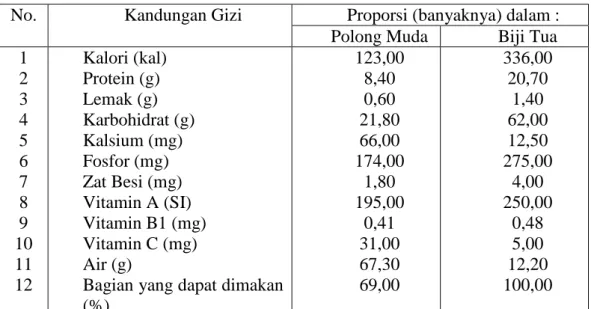
Kacang ini memiliki kandungan protein sebesar 21% dan karbohidrat sebesar 62% (Damardjati dan Widowati, 1985). Kandungan senyawa-senyawa tersebut sangat dipengaruhi oleh beberapa faktor, antara lain ; varietas, kemasakan biji, iklim, dan pemupukan (Makfoeld, 1977). Kandungan gizi kacang gude polong muda dan biji tua dapat dilihat pada Tabel 1.
Tabel 1. Kandungan gizi kacang gude polong muda dan biji tua
No. Kandungan Gizi Proporsi (banyaknya) dalam :
Polong Muda Biji Tua 1 2 3 4 5 6 7 8 9 10 11 12 Kalori (kal) Protein (g) Lemak (g) Karbohidrat (g) Kalsium (mg) Fosfor (mg) Zat Besi (mg) Vitamin A (SI) Vitamin B1 (mg) Vitamin C (mg) Air (g)
Bagian yang dapat dimakan (%) 123,00 8,40 0,60 21,80 66,00 174,00 1,80 195,00 0,41 31,00 67,30 69,00 336,00 20,70 1,40 62,00 12,50 275,00 4,00 250,00 0,48 5,00 12,20 100,00 Sumber : Anon., (1981)
Protein kacang gude tersusun atas asam amino esensial dan asam amino non esensial. Odeny (2007), melaporkan bahwa kacang gude merupakan salah satu sumber asam amino yang baik. Salah satu asam amino esensial yang secara signifikan menyusun protein kacang gude adalah sistin dan metionin . Komposisi asam amino yang menyusun protein kacang gude dapat dilihat pada Tabel 2.
Tabel 2. Komposisi asam amino penyusun protein kacang gude
No. Asam Amino Persentase (%)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Arginin Sistein* Histidin Isoleusin* Leusin* Lisin* Methionin* Fenilalanin* Threonin* Tirosin* Valin* Asam Aspartat Asam Glutamat Alanin Glisin Prolin Serin 6,7 1,2 3,4 3,8 7,6 7 1,5 8,7 3,4 2,2 5 9,8 19,2 6,4 3,6 4,4 5 Sumber : Duke (1981)
Keterangan : * Asam amino esensial
1.2 Konsentrat Protein
Konsentrat protein adalah produk pekatan protein yang memiliki kandungan protein minimal 70% (Koswara, 2009). Konsentrasi gula yang rendah menyebabkan konsentrat protein lebih mudah dicerna dan lebih sedikit menyebabkan flatulensi (Riaz, 2004). Spesifikasi konsentrat protein secara umum dapat dilihat pada Tabel 3.
Tabel 3. Spesifikasi konsentrat protein
Item Range
Protein (%) 65-75%
Lemak (%) 0,3-1,2%
Air (%) Maksimal 9%
Abu (%) 4-6%
Polisakarida tak larut (%) 15-25%
Sumber : Cheftel et al., (1985)
Konsentrat protein dapat diproduksi dari berbagai bahan pangan yang merupakan sumber protein baik hewani (misalnya susu, ikan dan daging) maupun nabati (misalnya kacang-kacangan dan serelia). Beberapa jenis kacang-kacangan yang biasa digunakan sebagai bahan pembuatan konsentrat protein yaitu kacang
kedelai, kacang tanah, kanola, kacang almond, wijen, dam kacang methe (cashew nut) (Garba dan Kaur, 2014). Kadar protein bahan yang dijadikan sebagai bahan baku pembuatan konsentrat protein cukup bervariasi. Baberapa bahan tersebut yaitu kacang merah dengan kadar protein 21-27% (Rusiani, 2016), chasew nut dengan kadar protein 21% (Ogunwolu et al., 2009), wijen dengan kadar protein 20-25% (Onsaard, 2012), shorgum dengan kadar protein 10% (Illaningtyas et al., 2012), dedak padi dengan kadar protein 14-16% (Wang et al., 2015) dan lain sebagainya.
1.3 Isolasi Protein
Konsentrat protein dapat diperoleh dari proses isolasi (pemisahan) protein dalam bahan pangan. Natarajan (1980) menyebutkan bahwa isolasi protein pada prinsipnya terdiri dari tahap-tahap ekstraksi protein dalam medium pengekstrak, penghilangan bahan tidak larut dengan sentrifugasi, filtrasi atau kombinasinya, pengendapan, pencucian dan pengeringan konsentrat.
Isolasi protein dapat dilakukan pada bahan berupa tepung yang sudah dihilangkan lemaknya (defatted flour) maupun tepung yang belum dihilangkan lemaknya (full fat flour). Penghilangan lemak bisa dilakukan dengan menggunakan pelarut organik misalnya n-hexan dan petroleum eter. Perbandingan bahan dengan pelarut organik disesuaikan dengan kadar lemak dalam bahan. Budijanto et al., (2011), melaporkan bahwa dengan kandungan lemak sebesar 17,51% - 21,75% pada biji kecipir, dihilangkan melalui proses defatting menggunakan pelarut n-hexan dengan perbandingan bahan dan pelarut 1 : 5. Kandungan lemak pada kacang komak yang lebih kecil yaitu 0,8% dihilangkan menggunakan pelarut n-hexan dengan perbandingan 1 : 1,5 (Purwitasari et al., 2014).
Pemisahan protein menggunakan pelarut alkali (alkaline extraction) yang diikuti dengan proses pengendapan protein pada pH isoelektrik (isoelectric precipitation) adalah cara yang banyak dilakukan sekarang ini (Wang et al., 1999). Kemampuan ekstraksi protein dipengaruhi oleh beberapa faktor, antara lain: ukuran partikel tepung, umur tepung, perlakuan panas sebelumya, rasio pelarutan serta suhu , pH, dan kekuatan ion dari medium pengekstrak (Kinsella, 1979).
Menurut Cheftel et al., (1985) pemilihan suasana basa sebagai pH selama ekstraksi berdasarkan pada kenyataan bahwa sebagian besar asam amino akan bermuatan negatif pada pH di atas titik isoelektriknya, muatan yang sejenis cenderung untuk tolak menolak, hal ini menyebabkan minimnya interaksi antara residu-residu asam amino yang berarti kelarutan protein akan meningkat. Oleh sebab itu, kelarutan protein lebih besar pada suasana basa dibandingkan pada suasana asam. Sugijanto dan Manullang (2001), menyatakan bahwa jenis basa yang digunakan untuk mengekstrak protein yaitu NaOH (basa kuat) dan NH4OH (basa lemah). Penggunaan NaOH jauh lebih efisien dari segi jumlah penggunaannya dan tidak menimbulkan bau dibandingkan NH4OH. Menurut Saunders et al., (1975), penggunaan NH4OH bermanfaat ketika produk atau residu hasil ekstrak diberikan sebagai pakan ternak. NH4OH memiliki kelemahan yaitu jumlah yang digunakan untuk mencapai kondisi ekstraksi lebih banyak dibandingkan NaOH, bau ammonia yang ditimbulkan selama proses tetap tertinggal di dalam produk, walaupun produk sudah dikeringkan, dan senyawa N pada NH4OH dapat memberikan tambahan % N pada penentuan kadar protein metode kjeldahl.
Tahapan setelah ekstraksi adalah sentrifugasi. Prinsip utama sentrifugasi adalah memisahkan substansi berdasarkan berat jenis molekul dengan cara memberikan gaya sentrifugal sehingga substansi yang lebih berat akan berada di dasar, sedangkan substansi yang lebih ringan akan terletak di atas.
Prinsip dari proses isoelectric precipitation adalah pengendapan seluruh protein bahan pada titik isoelektriknya. Suciono (1995), menyebutkan bahwa dalam larutan asam (pH rendah), gugus amino bereaksi dengan H+ sehingga protein bermuatan positif dengan gugus bermuatan negatif. Interaksi elektrostatik antar asam amino akan maksimum karena muatan yang tidak sejenis cenderung untuk tarik menarik, fenomena ini dapat diamati dengan terjadinya koagulasi protein. Koagulasi dan pengendapan dilakukan dengan penambahan asam, agar mencapai pH tertentu (pH isoelektrik), terjadi penggumpalan, dan endapan (protein). Koagulan yang digunakan dalam proses isoelectric precipitation dapat merupakan asam kuat. Salah satu asam kuat yang biasa digunakan adalah asam klorida. pH isoelektrik adalah pH dimana protein bermuatan nol sehingga protein
cenderung saling tarik menarik membentuk agregat dan mengendap. pH isoelektrik protein sangat tergantung pada komposisi asam amino penyusunnya (Garba dan Kaur, 2014).
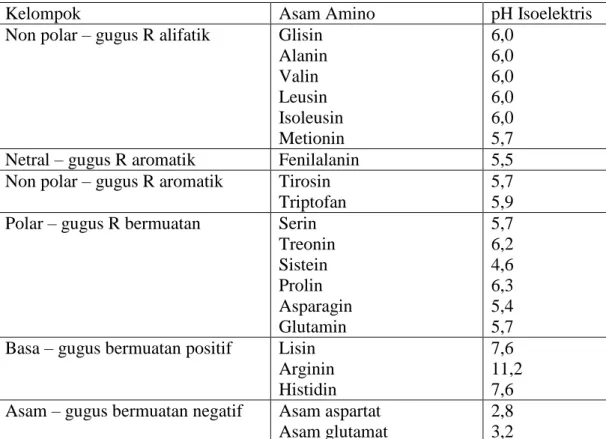
Protein dibangun dari rangkaian 20 asam amino yang berikatan kovalen dalam urutan yang khas. Semua asam amino yang ditemukan pada protein mempunyai ciri sama yaitu gugus karboksil sama, dan gugus amino yang sama serta gugus R (rantai samping) yang bervariasi dalam struktur, ukuran, muatan listrik, dan kelarutannya dalam air. Gugus R pada asam amino bervariasi polaritasnya, mulai dari gugus R yang sama sekali tidak polar atau hidrofobik sampai bersifat amat polar atau hidrofilik. Menurut Suhardi (1991), pH isoelektrik berkisar antara 4,8 – 6,3. Beberapa nilai pH presipitasi isoelektrik yang menghasilkan rendemen dan kadar protein optimum berbagai jenis konsentrat protein kacang yaitu kacang kedelai 4,2 (Garba dan Kaur, 2014), kacang merah 4,5 (Rusiani, 2016), kecipir 3,45 (Budijanto et al., 2011), koro benguk 4,4 (Sudradjat et al., 2016), dan lain sebagainya. Pengelompokan dan pH isoelektris masing-masing asam amino dapat dilihat pada Tabel 4.
Tabel 4. Pengelompokan dan pH isoelektrik asam amino
Kelompok Asam Amino pH Isoelektris
Non polar – gugus R alifatik Glisin Alanin Valin Leusin Isoleusin Metionin 6,0 6,0 6,0 6,0 6,0 5,7
Netral – gugus R aromatik Fenilalanin 5,5
Non polar – gugus R aromatik Tirosin Triptofan
5,7 5,9 Polar – gugus R bermuatan Serin
Treonin Sistein Prolin Asparagin Glutamin 5,7 6,2 4,6 6,3 5,4 5,7 Basa – gugus bermuatan positif Lisin
Arginin Histidin
7,6 11,2 7,6 Asam – gugus bermuatan negatif Asam aspartat
Asam glutamat
2,8 3,2 Sumber : Kusnandar (2010)
Pengeringan konsentrat protein dilakukan pada suhu 450C menggunakan pengering oven. Krisnantoko (2012), melaporkan bahwa pada kondisi suhu rendah < 500C sudah mulai terjadi reaksi Maillard, namun reaksi tersebut berjalan lambat. Perlakuan pemanasan dapat memberikan pengaruh terhadap terjadinya pencoklatan Selama proses pengeringan dan pemanasan tepung, kadar gula reduksi akan meningkat tajam, sehingga terjadilah reaksi pencokelatan (Maillard) yang semakin meningkat (Gil et al., 1994).
1.4 Sifat Fisik Kimia dan Fungsional 1.4.1 Sifat fisik
Warna merupakan salah satu atribut penampilan pada suatu produk tersebut secara keseluruhan. Suatu bahan dinilai bergizi, enak, dan teksturnya sangat baik tidak akan dimakan apabila memiliki warna yang tidak menarik untuk dipandang dan memberi kesan menyimpang dari warna yang seharusnya (Winarno, 2004).
Salah satu alat yang digunakan untuk uji warna adalah colorimeter. Terdapat 3 parameter yaitu nilai L, a, dan b dimana L memiliki interval antara 0-100 untuk warna kecerahan, a memiliki interval untuk warna hijau hingga merah dan b untuk interval biru hingga kuning. Pada parameter L apabila semakin positif (+), warna semakin cerah. Apabila nilai L semakin positif (+), warna akan semakin cerah. Parameter a apabila semakin negatif (-) warnanya semakin hijau dan positif (+) warnanya semakin merah. Parameter b semakin negatif (-), warna semakin biru dan semakin positif (+) warnanya semakin kuning. Dalam sistem pembacaan colorimeter akan keluar 4 digit dimana 4 digit tersebut dibagi 100 untuk hasil kuantitatifnya.
1.4.2 Sifat kimia
Reaksi kimia yang terjadi pada tahap-tahap proses pengolahan menyebabkan terjadinya perubahan pada bahan pangan, baik yang diharapkan maupun yang tidak diharapkan. Proses pengolahan dengan suhu tinggi dapat mengakibatkan peningkatan nilai gizi bahan pangan (misalnya karena terjadinya dekstruksi senyawa anti-nutrisi, terjadinya denaturasi molekul, sehingga meningkatkan daya cerna dan ketersediaan zat gizi). Akan tetapi proses pengolahan dengan suhu tinggi bila tidak terkontrol akan menurunkan nilai gizi bahan pangan (misalnya terjadi reaksi reaksi antar molekul nutrien, hancurnya
nutrien yang tidak tahan panas, atau terbentuknya molekul kompleks yang tidak dapat diuraikan atau dicerna oleh enzim tubuh) (Muchtadi, 1989). Faktor-faktor yang berpengaruh dalam ekstraksi protein juga dapat mempengaruhi sifat kimia konsentrat protein yang dihasilkan.
1.4.3 Sifat fungsional
Sifat fungsional protein dapat didefinisikan sebagai sifat-sifat fisiko-kimia di luar sifat nutrisi yang memungkinkan protein menyumbang karakteristik yang diinginkan pada makanan (Cheftel et al., 1985), yang didasarkan pada komponen protein bila berinteraksi dengan komponen lain dalam sistem pangan yang kompleks (Phillips dan Beuchat, 1981). Sifat-sifat fungsional protein dipengaruhi oleh tiga faktor, yaitu sifat intrinsik, faktor lingkungan, dan perlakuan selama proses. Menurut Demodaran dan Kinsella (1982) yang termasuk sifat intrinsik adalah komposisi protein, bentuk protein, jumlah penyusun protein serta keragaman komponen penyusun protein. Adanya air, ion, lemak, gula, suhu, dan pH lingkungan merupakan faktor lingkungan, sedangkan perlakuan selama proses pembuatan produk yang mempengaruhi sifat fungsionalnya adalah pemanasan, pengeringan, pendinginan, serta modifikasi protein.
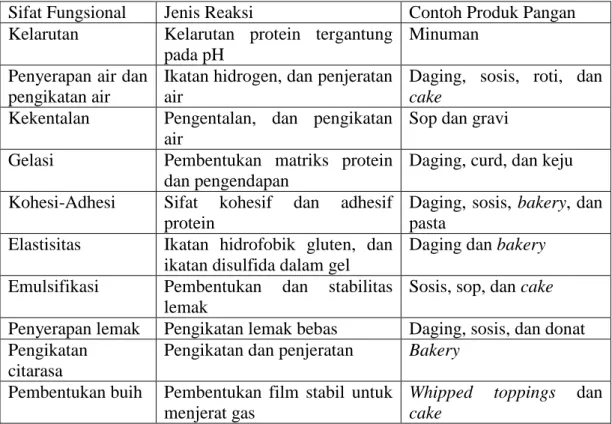
Dalam suatu sistem pangan, sifat fungsional protein penting untuk diketahui. Tabel 5. menyajikan beberapa sifat fungsional konsentrat protein, jenis reaksi yang terjadi dan contoh penggunaanya dalam sistem pangan. Konsentrat protein kedelai juga banyak digunakan untuk memproduksi daging analog seperti meatless ham, meatless bacon, dan meatless hot dog untuk para vegetarian (Koswara, 2009). Masing-masing sifat fungsional protein tidak berdiri sendiri, melainkan saling berkaitan satu sama lain. Keberadaan sifat-sifat fungsional protein kedelai sangat potensial untuk dimanfaatkan dalam industri pangan, seperti daya serap air, daya serap minyak, kapasitas dan stabilitas emulsi serta kapasitas dan stabilitas buih.
Tabel 5. Jenis-jenis sifat fungsional protein dalam sistem pangan
Sifat Fungsional Jenis Reaksi Contoh Produk Pangan Kelarutan Kelarutan protein tergantung
pada pH
Minuman
Penyerapan air dan pengikatan air
Ikatan hidrogen, dan penjeratan air
Daging, sosis, roti, dan cake
Kekentalan Pengentalan, dan pengikatan air
Sop dan gravi
Gelasi Pembentukan matriks protein dan pengendapan
Daging, curd, dan keju
Kohesi-Adhesi Sifat kohesif dan adhesif protein
Daging, sosis, bakery, dan pasta
Elastisitas Ikatan hidrofobik gluten, dan ikatan disulfida dalam gel
Daging dan bakery
Emulsifikasi Pembentukan dan stabilitas lemak
Sosis, sop, dan cake
Penyerapan lemak Pengikatan lemak bebas Daging, sosis, dan donat Pengikatan
citarasa
Pengikatan dan penjeratan Bakery
Pembentukan buih Pembentukan film stabil untuk menjerat gas
Whipped toppings dan cake
Sumber : Kinsella dan Srinivasan (1981) a. Daya serap air (water holding capacity)
Daya serap air suatu protein didefinisikan sebagai kemampuan untuk menahan air melawan perlakuan gravitasi dan fisikokimia. Air berinteraksi dengan protein dalam beberapa cara dan sejumlah signifikan air terikat oleh protein melalui ikatan hidrogen. Interaksi antara molekul air dan gugus hidrofilik pada rantai protein terjadi melalui ikatan hidrogen. Pengikatan air dengan protein dipengaruhi oleh gugus hidrofilik polar seperti imino, amino, karboksil, hidroksil, karbonil, dan sulfihidril. Kapasitas protein untuk menahan air dipengaruhi oleh jenis dan jumlah dari gugus polar pada rantai polipeptida protein (Zayas, 1997).
Asam amino diklasifikasikan berdasarkan kemampuannya untuk mengikat air yaitu : 1) asam amino polar dengan daya pengikatan air paling tinggi, 2) asam amino yang tidak mengion, mengikat sejumlah air dalam jumlah yang medium, 3) gugus hidrofobik yang hanya dapat mengikat sedikit air atau tidak sama sekali. Gugus asam amino polar pada molekul protein adalah sisi utama dalam interaksi protein-air (Zayas, 1997).
Penyerapan air oleh beberapa jenis protein dapat mengakibatkan pembengkakan. Pembengkakan mencerminkan pengambilan air oleh jaringan protein
sambil melonggarkan polipeptida. Tingkat pembengkakan dipengaruhi oleh gaya-gaya antar molekul, ikatan hidrogen, interaksi elektrostatik antara polipeptida yang berdekatan dan fasilitas tertentu yang dengannya air akan memberikan gangguan dan menggantikan ikatan protein-protein dengan protein-air (Muchtadi, 1991).
Penambahan protein kedelai ke dalam adonan produk panggang akan meningkatkan penyerapan air yang membantu menahan kelembaban produk, sehingga menjaga kesegaran produk lebih lama. Ini penting untuk jenis-jenis makanan yang memiliki umur simpan pendek seperti roti. Pada produk pudding dan yoghurt, daya serap air sangat berperan dalam menghasilkan tekstur yang kental dan mencegah terjadinya pemisahan. Selain itu, protein juga dapat meningkatkan rendemen akhir produk seperti pada produk daging olahan. Hal ini karena protein akan mengikat air yang ditambahkan sehingga mengurangi penyusutan saat pemasakan (Wolf dan Cowman, 1971).
b. Daya serap minyak (oil holding capacity)
Daya serap minyak merupakan pengikatan minyak secara fisik oleh protein. Kemampuan penyerapan minyak/lemak tergantung pada struktur protein. Struktur yang bersifat lipofilik disebabkan oleh kandungan cabang protein nonpolar yang lebih dominan, sehingga berkontribusi terhadap meningkatnya daya serap minyak. Protein hidrofobik yang tidak larut air memiliki kemampuan menyerap lemak dalam jumlah besar (NAS, 1981 ).
Daya serap minyak suatu protein dipengaruhi oleh sumber protein, ukuran partikel protein, kondisi proses pengolahan, zat tambahan lain, suhu, dan derajat denaturasi protein. Ukuran partikel dan tekstur yang lebih halus, lebih seragam dan lebih porus menyebabkan isolat protein lebih mudah menyerap dan mengikat minyak. Denaturasi protein dapat meningkatkan kemampuan protein mengikat minyak. Hal ini dikarenakan terbukanya struktur protein sehingga memaparkan asam-asam amino nonpolar. Namun, denaturasi protein yang berlebihan akan menurunkan daya serap minyak karena rusaknya rantai hidrofobik protein (Zayas, 1997).
Protein hidrofobik efektif pada tegangan permukaan yang lebih rendah dan mengikat banyak materi lipofilik seperti lipid, emulsifier, dan materi flavor. Kapasitas protein untuk mengikat lemak sangat penting dalam produksi meat extenders dan
meningkatkan mouth feel. Lemak diserap terutama melalui pemerangkapan secara fisik. Penyerapan lemak dapat ditingkatkan jika protein dimodifikasi secara kimia untuk meningkatkan densitas kambanya (Pomeranz, 1991).
Daya serap minyak oleh protein kedelai pada produk daging olahan seperti frankfurters atau luncheon meat, dapat memperbaiki formasi serta menstabilkan emulsi dan matriks gel yang menghalangi migrasi lemak kepermukaan. Pada produk lainnya seperti pancake dan donat, penambahan tepung kedelai dapat membantu menjaga kelebihan lemak selama penggorengan. Hal ini akibat denaturasi protein yang membentuk barrier untuk menahan lemak di permukaan donat (Wolf dan Cowman, 1971).
c. Kapasitas dan stabilitas emulsi
Emulsi adalah suatu sistem yang terdiri dari dua fase cairan yang tidak saling melarutkan, dimana salah satu cairan terdispersi dalam bentuk globula-globula di dalam cairan lainnya. Cairan yang terpecah menjadi globula-globula dinamakan fase terdispersi sedangkan cairan yang mengelilingi globula-globula tersebut dinamakan fase kontinyu atau medium dispersi (Muchtadi, 1991).
Daya emulsi merupakan kemampuan protein untuk menurunkan tegangan permukaan antara dua fase (tegangan interfasial) sehingga mempermudah terbentuknya emulsi. Kemampuan ini disebut kemampuan protein sebagai emulsifier. Menurut Subarna, et al. (1990), daya emulsi ini dipengaruhi oleh konsentrasi protein, kecepatan pencampuran, jenis protein, jenis lemak, dan sistem emulsi. Daya kerja emulsifier disebabkan oleh bentuk molekulnya yang dapat terikat baik pada minyak (nonpolar) maupun air (polar).
Emulsifier mengandung dua gugus yaitu gugus hidrofilik dan gugus lipofilik. Di dalam molekul emulsifier, salah satu gugus harus lebih dominan jumlahnya. Bila gugus polar lebih dominan, maka molekul emulsifier tersebut akan diadsorpsi lebih kuat oleh air dibandingkan dengan minyak. Akibatnya tegangan permukaan air menjadi lebih rendah sehingga mudah menyebar dan menjadi fase kontinyu. Demikian juga sebaliknya jika gugus nonpolar lebih dominan, maka molekul emulsifier akan lebih kuat diadsorpsi oleh minyak dibandingkan dengan air (Muchtadi, 1991).
Daya kerja emulsifier disebabkan oleh bentuk molekulnya yang dapat terikat baik pada minyak maupun air. Bila emulsifier lebih terikat pada air (polar)
maka dapat lebih membantu terjadinya dispersi minyak dalam air (o/w) seperti pada susu. Sebaliknya bila emulsifier lebih larut dalam minyak (nonpolar) maka akan terbentuk dispersi air dalam minyak, contohnya mentega dan margarin (Kartika, 2009).
Suryani (2000), menyebutkan bahwa suatu sistem emulsi pada dasarnya adalah suatu sistem yang tidak stabil, karena masing-masing partikel mempunyai kecenderungan untuk bergabung dengan partikel lainnya. Kekuatan dan kekompakan lapisan antar muka adalah sifat yang penting yang dapat membentuk stabilitas emulsi. Faktor-faktor yang mempengaruhi sistem emulsi akan berdampak apabila dilakukan perubahan atau modifikasi pada lapisan antar muka tersebut. Emulsi yang baik tidak membentuk lapisan-lapisan, tidak terjadi perubahan warna dan konsistensi tetap. Stabilitas emulsi merupakan salah satu karakter terpenting dan mempunyai pengaruh besar terhadap mutu produk emulsi ketika dipasarkan.
d. Kapasitas dan Stabilitas Buih
Buih suatu protein yaitu suatu struktur terdispersi yang mengandung cairan koloid yaitu larutan protein sebagai medium pendispersi dan udara atau gas sebagai fase terdispersi (Subarna, et al.,1990 dalam Hapsari, 2009). Kapasitas buih protein berarti kemampuan protein untuk membentuk lapisan film tebal pada permukaan gas-cair sehingga sejumlah besar gelembung udara dapat bergabung dan terstabilkan. Sedangkan stabilitas buih berarti kemampuan protein untuk menstabilkan buih melawan gravitasi dan stres mekanis (Damodaran, 1996).
Pembentukan buih terjadi dengan tiga tahap yaitu pertama protein globular yang larut berdifusi ke antar fasa udara dan air, mengalami peningkatan konsentrasi dan menurunkan tegangan permukaan. Kedua protein membuka pada antar fasa dengan orientasi molekul polar ke air, dan ketiga polipeptida berinteraksi membentuk film. Faktor-faktor yang mempengaruhi pembentukan dan stabilitas buih protein meliputi kelarutan, laju difusi ke arah permukaan dan penyerapan. Faktor-faktor tersebut tergantung pada sifat-sifat hidrofobik, orientasi dan asosiasi polipeptida, viskoelastisitas, kesetimbangan agregasi konjugasi, muatan permukaan dan hidrasi (Pomeranz, 1991).