UJI EFEK ANTI INFLAMASI EKSTRAK ETANOL AKAR KROKOT BELANDA (Talinum triangulare (Jacq.)Willd)
PADA MENCIT PUTIH BETINA
SKRIPSI
Disusun untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S. Farm)
Program Studi Ilmu Farmasi
Oleh :
Agnes Meiriana NIM : 038114121
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
UJI EFEK ANTI INFLAMASI EKSTRAK ETANOL AKAR KROKOT BELANDA (Talinum triangulare (Jacq.)Willd)
PADA MENCIT PUTIH BETINA
SKRIPSI
Disusun untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S. Farm)
Program Studi Ilmu Farmasi
Oleh :
Agnes Meiriana NIM : 038114121
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2007
HALAMAN PERSEMBAHAN
^xà|~t }tÄtÇ {tÅÑt? t~â ^tâ ÑâÄ|{~tÇ
^xà|~t Ñâàâá tát? t~â ^tâ ~âtà~tÇ
^xà|~t ÄxÄt{? t~â ^tâ áxztÜ~tÇ
fx}tâ{ ÑxÜ}tÄtÇtÇ çtÇz àxÄt{ ~âàxÅÑâ{
gt~ áxwxà|~ ÑâÇ t~â ~x{|ÄtÇztÇ ~tá|{`â
`âÇz~|Ç àt~ ~âÑt{tÅ|
TÑt çtÇz ~|Ç| t~â tÄtÅ|
atÅâÇ ~â àtâ Ñtáà|
^tá|{ TÄÄt{~â àt~ t~tÇ uxÜ{xÇà|
^tÇ ~â ~âáxÜt{~tÇ áxÅât ÑxÜzâÅâÄtÇ~â ÑtwtÅâ lxáâá
^tÜxÇt ~â àtâ Ñtáà| TÄÄt{~â ux~xÜ}t ÅxÇwtàtÇz~tÇ ~xut|~tÇ utz|
çtÇz ÅxÇztá|{|açt
^âÑxÜáxÅut{~tÇ ~tÜçt ~xv|Ä~â |Ç| utz|
UtÑt? câàÜt wtÇ eÉ{ ^âwâá áxutzt| cÜ|utw| gÜ|àâÇzztÄ tàtá
~tá|{ áxà|taçt
^xÄâtÜzt~â çtÇz ~âv|Çàt|AAA
ft{tutà@át{tutà~â çtÇz ~âátçtÇz|‹
TÄÅtÅtàxÜ~âAAAA
PRAKATA
Puji dan syukur ke hadirat Tuhan Yang Maha Kuasa berkat kasih karuniaNya lah, penulis dapat menyelesaikan skripsi dengan judul “Uji Efek Anti Inflamasi Ekstrak Etanol Akar Krokot Belanda (Talinum triangulare (Jacq.) Willd) pada Mencit Putih Betina“ ini dengan baik. Skripsi ini disusun untuk memenuhi salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S. Farm.) Fakultas Farmasi Universitas Sanata Dharma.
Penyelesaian skripsi ini tentunya tidak lepas dari bantuan berbagai pihak baik secara langsung maupun tidak langsung. Pada kesempatan ini, penulis mengucapkan terima kasih kepada :
1. Rita Suhadi, M.Si., Apt, selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Drs. Mulyono, Apt selaku pembimbing utama skripsi ini atas segala dukungan, bimbingan, kritik dan masukkan kepada penulis demi kemajuan skripsi ini.
3. Erna Tri Wulandari, M.Si., Apt. selaku penguji skripsi atas bantuan dan masukkan kepada penulis demi kemajuan skripsi ini.
4. Yosef Wijoyo, M.Si., Apt. selaku penguji skripsi atas bantuan dan masukan kepada penulis demi kemajuan skripsi ini.
5. Mas Parjiman, Mas Heru dan Mas Kayat selaku laboran bagian Farmakologi-Toksikologi, serta Mas Wagiran selaku laboran bagian Farmakognosi-Fitokimia atas segala bantuan dan kerja sama selama di laboratorium.
6. Papa, Mama dan Kak Nina yang selalu menemani dan mendukung terutama dukungan moral, semangat dan kasih sayang selama ini serta adik Putra (Alm) yang telah lebih dahulu dipanggil untuk menikmati keindahan dan kedamaian surga.
7. Nike, Jenny, Erma, Nia, Indri, Ratna, Tyas, Marlin, Yenny, Ndari, dan Sigit, atas kebersamaan, dukungan dan persahabatan yang telah memberi makna hidupku
8. Iin, Margie, Nunik, Joan yang jauh di mata tetapi dekat di hati atas canda tawa, kekonyolan, dan dukungan yang sangat menghibur penulis selama ini 9. Teman-teman Amakusa : Nova, Inchan, Deka, C’dian, Henny, C’monic, Desi,
Silvi, Mira, Cendani, Tata, Ayu, Tyas, Ita, Yemi, Dewi, Uut, dan Dian serta Yeyen sebagai teman komsel atas canda tawa, dan kehebohan yang menyenangkan.
10.Teman-teman kelas C angkatan 2003 yang disebut Chemistry’03. Semoga persahabatan dan kebersamaan yang telah kita jalin bertahan selamanya. 11.Pihak-pihak yang turut membantu penulis dalam penyusunan skripsi ini yang
tidak dapat disebutkan satu-persatu.
Penulis menyadari dengan rendah hati bahwa skripsi ini jauh dari sempurna, oleh sebab itu penulis mengharapkan kritik dan saran demi kemajuan di masa yang akan datang. Akhir kata, penulis berharap semoga skripsi ini dapat
bermanfaat bagi masyarakat dan perkembangan ilmu pengetahuan. Penulis
INTISARI
Inflamasi merupakan respon biologik pada jaringan tubuh yang cedera atau mati. Akar krokot belanda (Talinum triangulare (Jacq) Willd) merupakan salah satu obat tradisional yang diduga berefek sebagai anti inflamasi. Oleh karena itu, penelitian ini bertujuan untuk membuktikan kebenaran efek anti inflamasi dan mengetahui besarnya persentase efek anti inflamasi ekstrak etanol akar krokot belanda dalam menghambat terjadinya udema pada mencit putih betina.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah. Metode yang digunakan adalah metode Langford dkk. yang telah dimodifikasi pelaksanaannya, yaitu induksi udema pada kaki kiri belakang hewan uji secara subplantar menggunakan suspensi karagenin 1%. Hewan uji yang digunakan adalah mencit betina galur Swiss, berumur 2-3 bulan dengan berat badan 20-30 gram. Enam puluh tiga ekor mencit dikelompokkan menjadi 9 kelompok secara acak. Kelompok I adalah kontrol negatif karagenin 1%, kelompok II adalah kontrol negatif CMC Na 1%, kelompok III, IV, dan V adalah kontrol positif natrium diklofenak dengan dosis 9,75 mg/kgBB; 10,795 mg/kgBB; dan 11,95 mg/kgBB, sedangkan kelompok VI, VII, VIII, dan IX adalah perlakuan ekstrak etanol akar krokot belanda dengan dosis 1674,49 mg/kgBB; 2411,26 mg/kgBB; 3472,22 mg/kgBB; dan 5000 mg/kgBB. Lima belas menit kemudian kaki kiri mencit bagian belakang diinjeksi dengan karagenin 1%, setelah 3 jam mencit dikorbankan dan kedua kakinya dipotong pada sendi torsocrural, kemudian ditimbang. Data bobot udema yang diperoleh selanjutnya digunakan untuk mencari persentase efek anti inflamasi. Distribusi data dianalisis dengan uji Kolmogorov-Smirnov, dilanjutkan dengan Anova satu arah dan uji Scheffe dengan taraf kepercayaan 95%.
Hasil penelitian menunjukkan bahwa ekstrak etanol akar krokot belanda memiliki efek anti inflamasi. Efek anti inflamasi ekstrak etanol akar krokot belanda dosis 1674,49 mg/kgBB; 2411,26 mg/kgBB; 3472,22 mg/kgBB; dan 5000 mg/kgBB berturut-turut sebesar 13,37%; 20,53%; 27,47%; dan 51,18%. Kata kunci : anti inflamasi, ekstrak etanol akar krokot belanda, modifikasi
pelaksanaan metode Langford
ABSTRACT
Inflammation is a biological response that occured in injury area. Krokot belanda root is one of the traditional medicine which is assuming to have effects in anti inflammation. Because of that, the purpose of this research is to prove the truth of anti inflammation effect and to know the amount of potency anti inflammation effect of ethanolic extract of krokot belanda root on preventing oedema.
This research is pure experimental research by one way complete random design. The experiment method which used was Langford method which the implementation had been modified. Implementation of Langford et al. method was oedema inductional method to the left underside of the experiment animals foot-sole with 1% carrageenan. The subject of this experiment were Swiss strain white female mice, whose age 2-3 months, and its weight were 20-30 grams. Sixty three mice were divided into 9 groups by random. Group I was carageenaan 1% negative control, group II was aquadest negative control, group III until group V were natrium diclofenac positive control with dose of 9,75 mg/kgBB; 10,795 mg/kgBB; dan 11,95 mg/kgBB, and group VI until group IX were ethanol extract of krokot belanda root with dose of 1674,49 mg/kgBB; 2411,26 mg/kgBB; 3472,22 mg/kgBB; dan 5000 mg/kgBB. Fifteen minutes later, those mice’s left legs were injected with carrageenan 1%. After three hours those mice were killed and its two legs were cut at torsocrural joint. Data obtained were data of weight of mice paws that used to calculate the percentage of anti inflammation effect. Distribution data were analyzed statistically with Kolmogorov-Smirnov. After that, the analysis were continued with one way ANOVA with 95% significance level and were continued with Scheffe test.
The results shows that ethanol extract of krokot belanda root has anti inflammation effect. Anti inflammation effect of ethanol extract of krokot belanda root on the dose of 1674,49 mg/kgBB; 2411,26 mg/kgBB; 3472,22 mg/kgBB; dan 5000 mg/kgBB were 13,37%; 20,53%; 27,47%; dan 51,18%.
Key words : anti inflammation, ethanolic extract of krokot belanda root, modified implementation of Langford method
DAFTAR ISI
Halaman
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
PERNYATAAN KEASLIAN KARYA ... vi
PRAKATA... vii
INTISARI ... ix
ABSTRACT... x
DAFTAR ISI... xi
DAFTAR TABEL... xv
DAFTAR GAMBAR ... xvii
DAFTAR LAMPIRAN... xix
BAB I. PENGANTAR... 1
A. Latar Belakang ... 1
B. Permasalahan ... 3
C. Keaslian Penelitian... 3
D. Manfaat Penelitian ... 4
1. Manfaat teoritis ... 4
2. Manfaat praktis ... 4
E. Tujuan Penelitian ... 5
1. Tujuan umum ... 5
2. Tujuan khusus ... 5
BAB II. PENELAAHAN PUSTAKA ... 6
A. Tanaman Krokot Belanda ... 6
1. Sistematika ... 6
2. Sinonim ... 6
3. Nama lain ... 6
4. Uraian tanaman ... 7
5. Kandungan kimia ... 8
6. Khasiat dan kegunaan ... 13
B. Perkolasi... 13
C. Inflamasi ... 15
1. Patogenesis... 15
2. Gejala ... 16
3. Mekanisme ... 18
D. Obat Anti Inflamasi... 25
E. Natrium Diklofenak ... 27
F. Metode Pengujian Aktivitas Anti Inflamasi... 28
G. Landasan Teori... 34
H. Hipotesis ... 35
BAB III. METODOLOGI PENELITIAN ... 36
A. Jenis dan Rancangan Penelitian ... 36
B. Metode Penelitian ... 36
C. Variabel Penelitian dan Definisi Operasional... 37
1. Variabel Penelitian... 37
2. Definisi Operasional ... 37
D. Subjek dan Bahan Penelitian... 38
1. Subjek Penelitian ... 38
2. Bahan Penelitian ... 38
E. Alat atau Instrumen Penelitian ... 39
F. Tata Cara Penelitian ... 40
1. Determinasi tanaman... 40
2. Pengumpulan bahan ... 40
3. Pembuatan ekstrak etanol akar krokot belanda... 40
4. Penyiapan hewan uji ... 41
5. Pembuatan suspensi karagenin 1% ... 41
6. Pembuatan CMC-Na 1%... 41
7. Pembuatan larutan natrium diklofenak ... 41
8. Pembuatan suspensi ekstrak etanol akar krokot belanda ... 42
9. Penetapan dosis ... 42
10.Uji pendahuluan rentang waktu pemotongan kaki setelah injeksi suspensi karagenin 1% ... 44
11.Uji pendahuluan rentang waktu pemberian ekstrak etanol
akar krokot belanda ... 45
12.Perlakuan Hewan Uji ... 45
13.Perhitungan Respon Daya Anti Inflamasi... 46
G. Analisis Hasil ... 47
BAB IV. HASIL DAN PEMBAHASAN PENELITIAN... 48
A. Determinasi Tanaman ... 48
B. Pembuatan Ekstrak Etanol Akar Krokot Belanda... 48
C. Uji Pendahuluan... 49
1. Uji pendahuluan rentang waktu pemotongan kaki setelah injeksi suspensi karagenin 1% ... 50
2. Uji pendahuluan rentang waktu pemberian ekstrak etanol akar krokot belanda... 53
D. Pengujian Efek Anti Inflamasi Ekstrak Etanol Akar Krokot Belanda... 56
BAB V. KESIMPULAN DAN SARAN ... 69
A. Kesimpulan ... 69
B. Saran ... 69
DAFTAR PUSTAKA ... 70
LAMPIRAN... 74
BIOGRAFI PENULIS ... 104
DAFTAR TABEL
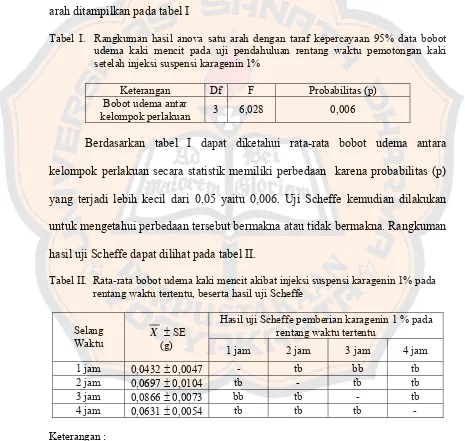
Halaman Tabel I. Rangkuman hasil anova satu arah dengan taraf kepercayaan
95% data bobot udema kaki mencit pada uji pendahuluan rentang waktu pemotongan kaki setelah injeksi suspensi karagenin 1% ... 51 Tabel II. Rata-rata bobot udema kaki mencit akibat injeksi suspensi
karagenin 1% pada rentang waktu tertentu, beserta hasil uji
Scheffe ... 51 Tabel III. Rangkuman hasil anova satu arah dengan taraf kepercayaan
95% data bobot udema kaki mencit pada uji pendahuluan rentang waktu pemberian ekstrak etanol akar krokot belanda ... 54 Tabel IV. Rata-rata bobot udema kaki mencit akibat injeksi suspensi
karagenin 1% pada uji pendahuluan rentang waktu pemberian ekstrak etanol akar krokot belanda... 54 Tabel V. Rata-rata bobot udema kaki mencit beserta persen (%) daya
anti inflamasi dari seluruh kelompok perlakuan ... 59 Tabel VI. Rangkuman hasil anova satu arah dengan taraf kepercayaan
95% persentase daya anti inflamasi ekstrak etanol akar krokot belanda dalam empat peringkat dosis beserta kontrolnya ... 62
Tabel VII. Hasil uji Scheffe daya anti inflamasi pada perlakuan ekstrak etanol akar krokot belanda dalam empat peringkat dosis beserta kontrolnya... 62
DAFTAR GAMBAR
Halaman
Gambar 1. Kerangka flavonoid... 9
Gambar 2. Struktur saponin ... 10
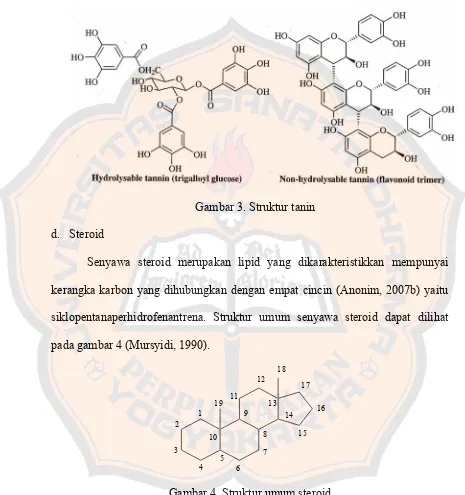
Gambar 3. Struktur tanin ... 11
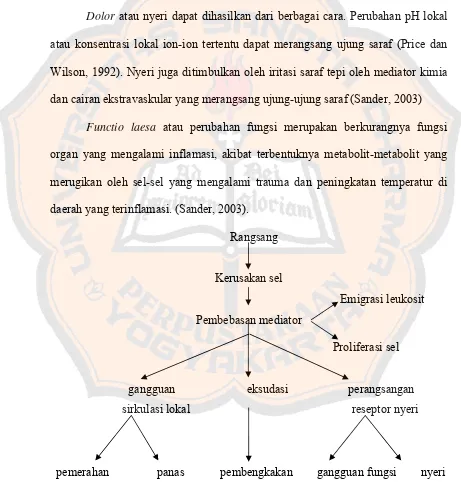
Gambar 4. Struktur umum steroid ... 11
Gambar 5. Patogenesis dan gejala inflamasi ... 17
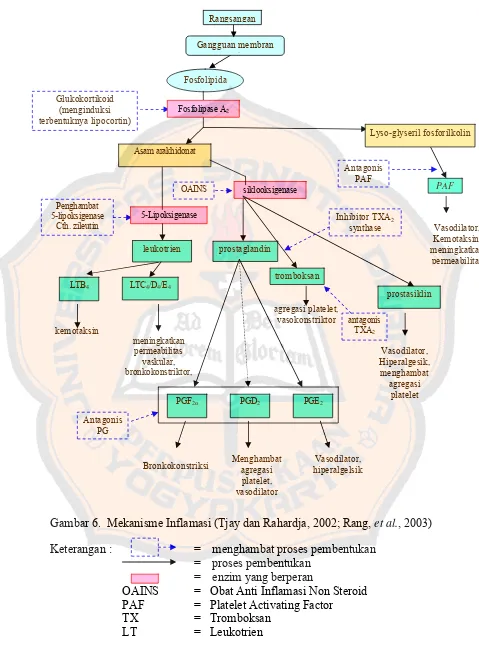
Gambar 6. Mekanisme inflamasi ... 24
Gambar 7. Struktur diklofenak ... 27
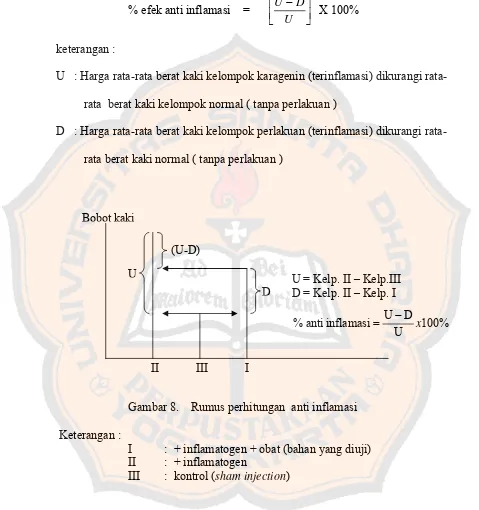
Gambar 8. Rumus perhitungan anti inflamasi ... 33
Gambar 9. Grafik rata-rata bobot udema kaki mencit hasil uji pendahuluan rentang waktu pemotongan kaki setelah injeksi suspensi karagenin 1% ... 53
Gambar 10. Grafik rata-rata bobot udema kaki mencit hasil uji pendahuluan rentang waktu pemberian ekstrak etanol akar krokot belanda... 56
Gambar 11. Diagram batang rata-rata bobot udema kaki mencit perlakuan ekstrak etanol akar krokot belanda dalam 4 peringkat dosis beserta kontrolnya... 60
Gambar 12. Diagram batang persentase efek anti inflamasi perlakuan ekstrak etanol akar krokot belanda beserta kontrolnya... 61
Gambar 13. Tanaman Krokot Belanda ... 77
Gambar 14. Akar Krokot Belanda ... 78
Gambar 15. Serbuk akar Krokot Belanda ... 78 Gambar 16. Ekstrak etanol kental akar Krokot Belanda ... 79 Gambar 17. Perbandingan persamaan garis antara log dosis natrium
diklofenak dan log dosis ekstrak etanol akar krokot belanda.. 101
DAFTAR LAMPIRAN
Lampiran 1. Surat pernyataan pengambilan dan determinasi dari BPTO . . 74 Lampiran 2. Sertifikat analisis natrium diklofenak ... 76 Lampiran 3. Foto tanaman Krokot Belanda ... 77 Lampiran 4. Foto akar Krokot Belanda dan serbuk akar Krokot Belanda 78 Lampiran 5. Foto ekstrak etanol akar Krokot Belanda... 79 Lampiran 6. Skema kerja uji pendahuluan rentang waktu pemotongan
kaki mencit setelah injeksi suspensi karagenin 1% ... 80 Lampiran 7. Hasil dan analisis hasil uji pendahuluan rentang waktu
pemotongan kaki mencit setelah injeksi suspensi karagenin
1% ... 81 Lampiran 8. Skema kerja uji pendahuluan rentang waktu pemberian
ekstrak etanol akar krokot belanda... 84 Lampiran 9. Hasil dan analisis hasil uji pendahuluan rentang waktu
pemberian ekstrak etanol akar krokot belanda... 85 Lampiran 10. Skema kerja perlakuan hewan uji ... 88 Lampiran 11. Hasil dan analisis hasil bobot udema kaki mencit akibat
pemberian ekstrak etanol akar krokot belanda dalam empat peringkat dosis dan kontrolnya ... 90 Lampiran 12. Hasil perhitungan dan analisis hasil persen (%) efek anti
inflamasi akibat pemberian ekstrak etanol akar krokot belanda dalam empat peringkat dosis dan kontrolnya ... 95
Lampiran 13. Perbandingan persamaan garis antara log dosis natrium diklofenak dan log dosis ekstrak etanol akar krokot belanda.. 101 Lampiran 14. Hasil Perhitungan Potensi Relatif Efek Anti inflamasi
Pemberian Ekstrak Etanol Akar Krokot BelandaDalam Empat Peringkat Dosis... 103
BAB I PENGANTAR
A. Latar Belakang
Inflamasi atau radang merupakan respon yang menyolok pada jaringan hidup yang mengalami cedera atau mati. Respon inflamasi yang terjadi berupa penginaktivasian atau perusakan organisme penyerang, penghilangan zat iritan, dan perbaikan jaringan (Harvey, Mycek, dan Champe, 2001).
Reaksi inflamasi diperlukan karena inflamasi ini merupakan respon biologik dari reaksi-reaksi kimia berurutan dan berfungsi melindungi tubuh dari infeksi dan memperbaiki jaringan yang rusak akibat trauma (Wilmana, 1995). Namun bila reaksi inflamasi tersebut berlebihan maka akan merugikan sehingga diperlukan obat-obat anti inflamasi untuk mengendalikan reaksi inflamasi sampai taraf yang tidak merugikan.
Obat tradisional merupakan salah satu alternatif yang digunakan sebagai sarana perawatan kesehatan dan untuk menanggulangi berbagai macam penyakit. Penggunaan obat tradisional sudah menjadi tradisi budaya dalam mengatasi masalah kesehatan oleh masyarakat di Indonesia. Salah satu alasan masyarakat untuk tetap menggunakan obat tradisional adalah karena masyarakat berasumsi bahwa obat tradisional dinilai memiliki efek samping yang lebih ringan daripada obat modern terutama untuk pengunaan jangka panjang.
Krokot belanda (Talinum triangulare (Jacq.)Willd) merupakan salah satu tanaman di Indonesia yang memiliki khasiat sebagai obat. Bagian tanaman yang
sering dimanfaatkan adalah akarnya. Akar krokot belanda secara tradisional umumnya digunakan sebagai tonikum atau penghilang keletihan. Menurut Perry (1980), akar krokot belanda juga berkhasiat untuk mengatasi inflamasi dan mengurangi bengkak.
Senyawa kimia yang terkandung di dalam akar krokot belanda adalah flavonoid, steroid, saponin dan tanin (Anonim, 1994; Dalimarta, 2003; Misra, 1992) yang dapat larut dalam etanol. Flavonoid, steroid dan tanin diduga dapat menimbulkan efek anti inflamasi. Penelitian ini menggunakan etanol dengan harapan kandungan kimia pada akar krokot belanda yang diduga berefek anti inflamasi dapat terekstraksi dengan baik. Hal tersebut di atas, yang mendorong dilakukannya penelitian tentang uji efek anti inflamasi ekstrak etanol akar krokot belanda pada mencit putih betina.
B. Permasalahan
Berdasarkan latar belakang yang telah dipaparkan di atas, masalah pada penelitian ini dibatasi sebagai berikut:
a. Apakah ekstrak etanol akar krokot belanda memiliki efek anti inflamasi terhadap mencit putih betina?
b. Berapa besar efek anti inflamasi ekstrak etanol akar krokot belanda terhadap mencit putih betina?
C. Keaslian Penelitian
Sejauh penelusuran penulis di Universitas Sanata Dharma, penelitian tentang Uji Efek Anti Inflamasi Ekstrak Etanol Akar Krokot Belanda pada Mencit Putih Betina belum pernah dilakukan. Adapun penelitian yang pernah dilakukan adalah sebagai berikut :
a. Evaluasi Efek Stimulan Susunan Syaraf Pusat Ekstrak Daun dan Batang
Talinum triangulare (Jacq) Willd (Rustam, 1991). Hasil penelitian menunjukkan bahwa ekstrak daun dan batang Krokot Belanda memberikan
efek stimulan dengan dosis oral terendah adalah 1,33 g/kg BB pada mencit dan 0.89 g/kg BB pada tikus jantan.
b. Pemeriksaan Pendahuluan Kandungan Kimia Tumbuhan Talinum triangulare
c. Khasiat dan Keamanan Som Jawa (Talinum paniculatum Gaertn) dan Kolesom (Talinum triangulare Willd) (Nugroho, 2000). Hasil penelitian menunjukkan bahwa uji toksisitas akut Som Jawa mempunyai LD50 sebesar
32,22 mg/10 g BB sedangkan Kolesom mempunyai LD50 sebesar 45,1 mg/10
g BB (rute i.p. pada mencit). Som Jawa dan Kolesom aman berdasarkan uji toksisitas akut.
d. Uji Efek Tonikum Infusa Akar Krokot Belanda (Talinum triangulare (Jacq) Willd) terhadap Fungsi Motorik pada Mencit Jantan dengan Metode Rotarod test (Astawa, 2005). Hasil penelitian menunjukkan bahwa infusa akar krokot belanda dosis 2 mg/g BB/hari, 3,5 mg/g BB/hari dan 5 mg/g BB/hari terbukti memiliki efek tonikum yang setara dengan Panax ginseng dosis 1,2 mg/g BB/hari
D. Manfaat Penelitian a. Manfaat teoritis
Penelitian ini diharapkan dapat memberikan sumbangan ilmiah bagi perkembangan ilmu pengetahuan khususnya bidang obat tradisional tentang khasiat akar krokot belanda sebagai obat anti inflamasi
b. Manfaat praktis
E. Tujuan Penelitian 1. Tujuan Umum
Penelitian ini bertujuan untuk menambah informasi kepada masyarakat tentang tanaman obat yang berkhasiat sebagai anti inflamasi.
2. Tujuan Khusus
BAB II
PENELAAHAN PUSTAKA
A. Tanaman Krokot Belanda 1. Sistematika
Sistematika tanaman Talinum triangulare (Jacq.) Willd adalah sebagai berikut:
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledonae Bangsa : Caryophyllales Suku : Portulacaceae Marga : Talinum
Jenis : Talinum triangulare (Jacq) Willd (Anonim, 1994) 2. Sinonim
Sinonim tanaman krokot belanda adalah Talinum racemosum Rohrbach (Anonim, 1994; Dalimarta, 2003).
3. Nama lain
Tanaman krokot belanda memiliki nama daerah dan nama asing sebagai berikut :
a. Nama daerah
Poslen, Gelang (Jawa), Krokot Belanda (Sunda), Talesom, Som Jawa (Jawa) (Pitojo, 2000).
b. Nama asing
Suriname postelein, Grand pourpier, Cia ren shen (Anonim, 1986a;
Pitojo, 2000).
4. Uraian Tanaman
Krokot Belanda merupakan tanaman yang hidup menahun di dataran
rendah hingga dataran tinggi pada ketinggian 1000 meter di atas permukaan laut
(Dalimarta, 2003). Tumbuh mengerombol, memiliki banyak percabangan dan
sejumlah anakan yang letaknya berdekatan dengan induknya (Pitojo, 2000).
Akarnya tunggang bila berasal dari biji, sedangkan tanaman yang berasal
dari stek tidak membentuk akar tunggang. Akar berwarna keputihan saat muda,
setelah tua berwarna coklat. Akar serabut intensif di lapisan atas tanah. Pada
bagian pangkal, tumbuh akar-akar kecil memanjang. Batang muda berwarna hijau
bulat, relatif lunak dan mudah dipatahkan. Batang tua berwarna kemerahan, agak
keras. Daunnya hijau, bertangkai pendek, panjang daun antara 3 -13 cm dengan
lebar 1,5 - 5 cm. Letak daun tersebar, melekat pada batang dan cabang tanaman.
Bunganya majemuk, terdapat pada malai yang muncul dari ujung tangkai atau di
ketiak percabangan atas. Daun kelopak berupa selaput, dengan 1-3 tulang daun
hijau tua. Bunga memiliki 5 helai daun mahkota berbentuk solet dengan panjang
1-12 mm berwarna ungu kemerahan. Biji pada buah muda berwarna hijau,
berukuran kecil, berbentuk ujung korek api. Pada buah agak tua, berwarna
5. Kandungan Kimia
Akar dan daun krokot belanda mengandung saponin, dan flavonoid
(Anonim, 1994), di samping itu akarnya juga mengandung tanin dan steroid
(Misra, 1992; Dalimarta, 2003).
a. Flavonoid
Flavonoid merupakan senyawa metabolit sekunder yang banyak terdapat
pada tumbuh-tumbuhan. Kandungan senyawa flavonoid di dalam tumbuhan
sangat rendah, yaitu sekitar 0,25% dan secara umum terikat atau terkonjugasi
dengan senyawa gula membentuk glikosida (Robinson, 1995). Khusus pada divisi
Angiospermae yang lazim dijumpai adalah flavon dan flavonol, C-glikosida dan
O-glikosida, di samping isoflavon dan flavanon(Markham, 1988).
Flavonoid merupakan senyawa polar, maka umumnya flavonoid cukup
larut dalam pelarut polar seperti etanol (EtOH), metanol (MeOH), butanol
(BuOH) dan aseton. Adanya gula yang terikat pada flavonoid cenderung
menyebabkan flavonoid lebih mudah larut dalam air dan dengan demikian
campuran pelarut di atas dengan air merupakan pelarut yang lebih baik untuk
glikosida (Markham, 1988).
Flavonoid menghambat banyak reaksi oksidasi, baik secara enzim maupun
non enzim. Efek flavonoid terhadap organisme sangat banyak macamnya
sehingga tumbuhan yang mengandung flavonoid dapat dipakai dalam pengobatan
(Robinson, 1995). Flavonoid menunjukkan aktivitasnya sebagai anti alergi, anti
inflamasi, anti mikrobial, dan anti kanker. Pada kenyataannya, flavonoid bekerja
(Anonim, 2007a). Di antara senyawa flavonoid yang telah lama dikenal dan
merupakan suatu kelompok antioksidan yakni, kelompok polifenol memiliki
kemampuan sebagai penangkal superoksida, oksigen singlet, dan radikal peroksi
lipid (Sitompul, 2003). Flavonoid dapat bekerja sebagai inhibitor lipoksigenase
yang berperan dalam produksi mediator inflamasi yaitu leukotrien (Robinson,
1995) sehingga proses peradangan dapat terhambat. Kerangka flavonoid dapat
dilihat pada gambar 1 (Robinson, 1995).
O
Gambar 1. Kerangka flavonoid
b. Saponin
Saponin adalah glikosida triterpena dan sterol dan telah terdeteksi dalam
lebih dari 90 suku tumbuhan. Saponin merupakan senyawa aktif permukaan dan
bersifat seperti sabun, serta dapat dideteksi berdasarkan kemampuannya
membentuk busa dan menghemolisis sel darah. Pencarian saponin dalam
tumbuhan telah dipicu oleh kebutuhan akan sumber sapogenin yang mudah
diperoleh dan dapat diubah di laboratorium menjadi sterol hewan yang berkhasiat
penting (misalnya, kortison, estrogen kontraseptik, dll) (Harborne, 1987).
Berdasarkan aglikonnya, saponin dibagi menjadi dua yaitu saponin steroid
Saponin steroid Saponin triterpenoid
Gambar 2. Struktur saponin
Senyawa glikosida seperti saponin dan glikosida jantung tidak larut dalam
pelarut non polar. Senyawa ini paling cocok diekstraksi dari tumbuhan memakai
etanol atau metanol panas 70-95% (Robinson, 1995).
c. Tanin
Tanin merupakan substrat kompleks yang biasanya terjadi sebagai
campuran polifenol yang sulit diseparasi karena tidak dapat dikristalkan. Tanin
terdapat luas dalam tumbuhan berpembuluh dalam angiospermae khususnya
jaringan kayu. Tanin dapat dibedakan menjadi tanin terhidrolisis dan tanin tidak
terhidrolisis (tanin terkondensasi) (Heinrich, Barnes, Gibbons danWilliamson,
2004). Dalam industri, tanin merupakan senyawa yang berasal dari tumbuhan
yang mampu mengubah kulit hewan mentah menjadi kulit siap pakai. Sedangkan
dalam dunia kesehatan tanin bermanfaat untuk mengurangi bengkak (edema),
radang, dan sekresi pada gastrointestinal (Harborne, 1987). Tanin dapat
mempengaruhi respon inflamasi dengan aktivitasnya sebagai penangkal radikal
Tanin terhidrolisiskan dan glikosida dapat diekstraksi dengan air panas atau
campuran etanol-air (Robinson, 1995).
Gambar 3. Struktur tanin
d. Steroid
Senyawa steroid merupakan lipid yang dikarakteristikkan mempunyai
kerangka karbon yang dihubungkan dengan empat cincin (Anonim, 2007b) yaitu
siklopentanaperhidrofenantrena. Struktur umum senyawa steroid dapat dilihat
pada gambar 4 (Mursyidi, 1990).
2
3
4 5
6 7 8 9
10 11
12
13 14
15 16 17 18
19 1
Gambar 4. Struktur umum steroid
Steroid dapat berupa senyawa alkohol, aldehid dan keton atau asam
dalam fraksi lipid. Menurut fungsi fisiologis dan terdapatnya steroid secara garis
besar dibagi menjadi : golongan sterol, golongan asam empedu, golongan hormon,
golongan saponin dan sapogenin dan golongan glikosida jantung (Mursyidi,
1990). Secara umum sterol dapat diisolasi dengan pelarut organik seperti metanol,
etanol, eter, kloroform, dan campuran dari pelarut-pelarut tersebut (Mursyidi,
1990).
Steroid dapat menghambat pelepasan prostaglandin dari sel-sel sumbernya
(Anonim, 1991) sehingga pembentukan histamin, prostaglandin, dan
mediator-mediator kimia lainnya yang mengakibatkan peradangan dapat terhambat pula
(Greene, Harris, dan Goodyer, 2000).
Nama sterol dipakai khusus untuk steroid alkohol, tetapi karena praktis
semua steroid tumbuhan berupa alkohol dengan gugus hidroksil pada C-3 sering
kali semuanya disebut sterol (Robinson, 1995). Golongan fitosterol (sterol
tumbuhan) yang termasuk golongan ini adalah sitosterol yang merupakan sterol
tumbuhan terbanyak dan terdiri dari α, β, dan γ sitosterol, stigmasterol,
kampesterol, dan spinasterol (Mursyidi, 1990). Tiga senyawa ‘fitosterol’ yang
mungkin terdapat dalam tiap tumbuhan tinggi tersebut yaitu sitosterol (dahulu
dikenal sebagai ß-sitosterol), stigmasterol, dan kampestrol. Fitosterol dilaporkan
dapat menurunkan kolesterol, anti-inflamasi, antibakteri, antijamur, dan
6. Khasiat dan kegunaan
Akar tanaman krokot belanda berkhasiat untuk mengatasi inflamasi dan
mengurangi bengkak (Perry, 1980) serta untuk mengatasi bisul (Dalimartha,
2003). Akar krokot belanda juga berkhasiat sebagai obat lemah syahwat, penyegar
atau tonikum terhadap fungsi motorik pada keadaan keletihan (Anonim, 1994;
Wahjoedi, 2003).
B. Perkolasi
Perkolasi adalah proses penyarian dengan pelarut yang selalu baru
sampai sempurna yang umumnya dilakukan pada temperatur ruangan. Proses
terdiri atas tahapan pengembangan bahan, tahap maserasi antara, tahap perkolasi
sebenarnya (penetesan dan penampungan ekstrak), terus-menerus sampai
diperoleh ekstrak atau perkolat (Anonim, 1986b).
Perkolasi merupakan cara penyarian yang dilakukan dengan mengalirkan
melalui serbuk simplisia yang telah dibasahi. Prinsip perkolasi adalah sebagai
berikut: serbuk simplisia ditempatkan dalam suatu bejana silinder yang bagian
bawahnya diberi sekat berpori. Cairan penyari dialirkan dari atas ke bawah
melalui serbuk tersebut, cairan penyari akan melarutkan zat aktif sel-sel yang
dilalui sampai mencapai keadaan jenuh. Gerak ke bawah disebabkan oleh
kekuatan gaya beratnya sendiri dan cairan di atasnya, dikurangi dengan daya
kapiler yang cenderung untuk menahan (Anonim,1986b).
Alat yang digunakan untuk perkolasi disebut perkolator, cairan yang
yang keluar dari perkolator disebut perkolat atau sari, sedang sisa setelah
penyarian disebut ampas atau sisa perkolasi (Anonim,1986b).
Kekuatan yang berperan pada perkolasi antara lain : gaya berat,
kekentalan, daya larut, tegangan permukaan, difusi, osmosa, adhesi, daya kapiler
dan daya geseran (friksi). Cara perkolasi lebih baik daripada dengan cara maserasi
karena:
1. Aliran cairan penyari menyebabkan adanya pergantian larutan yang terjadi
dengan larutan yang konsentrasinya lebih rendah, sehingga meningkatkan
derajat perbedaan konsentrasi.
2. Ruangan di antara butir-butir serbuk simplisia membentuk saluran tempat
mengalir cairan penyari. Karena kecilnya saluran kapiler tersebut maka
kecepatan pelarut cukup untuk mengurangi lapisan batas sehingga dapat
meningkatkan perbedaan konsentrasi (Anonim,1986b).
Sebagian besar ekstrak dibuat dengan mengekstraksi bahan baku obat
secara perkolasi. Seluruh perkolat biasanya dipekatkan dengan cara destilasi
dengan pengurangan tekanan, agar bahan utama obat sesedikit mungkin terkena
panas (Anonim, 1995).
Etanol digunakan sebagai penyari karena lebih selektif, kapang dan kuman
sulit tumbuh dalam etanol 20% ke atas, tidak beracun, netral, absorpsinya baik,
dapat bercampur dengan air pada segala perbandingan dan panas yang diperlukan
C. Inflamasi 1. Patogenesis
Peradangan yang merupakan respon menyolok yang terjadi pada
jaringan-jaringan hidup di sekitar sel atau jaringan tubuh yang cedera atau mati
adalah suatu reaksi vaskular yang hasilnya merupakan pengiriman cairan, zat-zat
terlarut, dan sel-sel dari darah yang bersirkulasi ke dalam jaringan-jaringan
interstisial pada daerah cedera atau nekrosis (Price dan Wilson, 1992). Inflamasi
disebabkan oleh pengaruh-pengaruh yang sifatnya merusak sel (noksi). Noksi
dapat berupa noksi kimia (obat-obatan), noksi fisika (panas atau dingin yang
berlebihan, radiasi, benturan), serta infeksi dengan mikroorganisme atau parasit
(Muschler, 1986).
Adanya jaringan yang rusak menyebabkan terjadinya pelepasan mediator
kimia dan reaksi imun yang meliputi : histamin, eicosanoid (prostaglandin,
tromboksan, leukotrien), PAF (platelet activating factor), bradikinin, nitrit oksida,
neuropeptida, dan cytokine (seperti interleukin, intereferon, dll) (Rang, Dale,
Ritter, and Moore, 2003)
Menurut waktu terjadinya, inflamasi dibagi menjadi 2 yaitu inflamasi akut
dan inflamasi kronis. Inflamasi akut disebabkan oleh rangsangan sesaat atau
mendadak (akut). Inflamasi kronis disebabkan oleh luka yang berlangsung
beberapa minggu, bulan, atau bersifat menetap dan merupakan kelanjutan dari
2. Gejala
Pada level makroskopik gejala reaksi radang yang dapat diamati adalah
kemerahan (rubor), panas meningkat (calor), pembengkakan (tumor), nyeri
(dolor), dan gangguan fungsi (functio laesa). (Mutschler, 1986; Rang, et al, 2003).
Rubor biasanya merupakan hal pertama yang terlihat di daerah yang
mengalami proses peradangan. Waktu reaksi peradangan dimulai maka arteriol
yang mensuplai daerah itu melebar, sehingga darah yang mengalir ke
mikrosirkulasi lokal bertambah. Kapiler yang semula kosong atau sebagian saja
meregang dengan cepat terisi darah. Keadaan ini dinamakan hiperemia atau
kongesti yang menyebabkan warna merah lokal karena peradangan akut.
Timbulnya hiperemia pada awal reaksi peradangan diatur oleh tubuh, baik secara
neurogenik maupun secara kimia, melalui pengeluaran zat seperti histamin (Price
dan Wilson, 1992).
Calor terjadi bersamaan dengan rubor pada reaksi peradangan akut.
Sebenarnya calor atau panas hanya terjadi pada permukaan tubuh, yang dalam
keadaan normal lebih dingin dari 37oC yaitu panas tubuh. Daerah peradangan
pada kulit lebih panas dari sekelilingnya sebab darah yang disalurkan ke
permukaan daerah yang terkena infeksi lebih banyak daripada daerah yang
normal. Fenomena panas lokal ini tidak terlihat pada daerah radang yang jauh di
dalam tubuh karena jaringan-jaringan tersebut sudah memiliki suhu inti 37oC, dan
hiperemia lokal tidak menimbulkan perubahan (Price dan Wilson, 1992).
Tumor atau pembengkakan merupakan segi paling mencolok dari
dari sirkulasi darah ke jaringan interstisial. Cairan dan sel yang tertimbun dalam
daerah peradangan disebut eksudat. Pada keadaan dini reaksi peradangan sebagian
besar eksudat adalah cair, seperti yang terjadi pada lepuhan akibat luka bakar
ringan. Kemudian sel-sel darah putih atau leukosit meninggalkan aliran darah dan
tertimbun sebagai bagian dari eksudat (Price dan Wilson, 1992).
Dolor atau nyeri dapat dihasilkan dari berbagai cara. Perubahan pH lokal
atau konsentrasi lokal ion-ion tertentu dapat merangsang ujung saraf (Price dan
Wilson, 1992). Nyeri juga ditimbulkan oleh iritasi saraf tepi oleh mediator kimia
dan cairan ekstravaskular yang merangsang ujung-ujung saraf (Sander, 2003)
Functio laesa atau perubahan fungsi merupakan berkurangnya fungsi
organ yang mengalami inflamasi, akibat terbentuknya metabolit-metabolit yang
merugikan oleh sel-sel yang mengalami trauma dan peningkatan temperatur di
daerah yang terinflamasi. (Sander, 2003).
Rangsang
Kerusakan sel
Emigrasi leukosit
Pembebasan mediator
Proliferasi sel
gangguan eksudasi perangsangan
sirkulasi lokal reseptor nyeri
pemerahan panas pembengkakan gangguan fungsi nyeri
3. Mekanisme
Proses peradangan akut memiliki tiga komponen penting: (1) perubahan
penampang pembuluh darah dengan akibat meningkatnya aliran darah
(vasodilatasi), (2) perubahan struktural pembuluh darah yang memungkinkan
protein plasma dan leukosit meninggalkan sirkulasi darah (peningkatan
permeabilitas vaskular), dan (3) migrasi leukosit ke daerah jejas (Robbins dan
Kumar, 1995).
Bila agen penyebab jejas menyerang, maka fenomena vaskular akan
terjadi. Fenomena vaskular memiliki ciri khas yaitu bertambahnya aliran darah
pada daerah terjejas, terutama disebabkan oleh dilatasi arteriol dan pembukaan
anyaman kapiler. Hal ini terjadi akibat perangsangan pada membran sel yang
melepaskan mediator kimia seperti histamin, bradikinin dan zat-zat prostaglandin
(PGE2, PGI2, dan PGD2). Pada manusia, histamin dan bradikinin utamanya dapat
bertindak pada sel-sel endotel dengan meningkatkan celah antar sel sehingga
terjadi peningkatan permeabilitas vaskular.
Peningkatan permeabilitas vaskular mengakibatkan protein plasma disertai
leukosit bergerak menuju benda asing, mikroorganisme atau jaringan yang rusak
(proses eksudasi). Sel-sel darah putih atau leukosit pada proses peradangan akut
mengalami marginasi. Massa sel darah merah akan menggumpal dan berada di
bagian tengah dalam aliran darah aksial, dan sel-sel darah putih pindah ke bagian
tepi (marginasi). Leukosit akan mengadakan hubungan dengan permukaan
endotel, melekat, dan melapisi permukaan endotel. Protein plasma meninggalkan
neutrofil juga meninggalkan pembuluh darah melalui pertemuan antar endotel
menuju daerah jejas (emigrasi). Setelah meninggalkan pembuluh darah, leukosit
bergerak menuju ke arah utama lokasi jejas. Migrasi sel darah putih yang terarah,
disebabkan oleh pengaruh-pengaruh kimia yang dapat berdifusi disebut
kemotaksis. Agen kemotaksis yang penting untuk neutrofil adalah (1) C5a,
komponen system komplemen, (2) leukotrin B4, hasil metabolisme asam
arakidonat dan (3) produk-produk kuman. Setelah leukosit bermigrasi ke lokasi
jejas, maka leukosit akan menggerombol pada pusat radang atau mengelilingi
pusat radang dengan tujuan melokalisir daerah radang. Pada akhirnya leukosit
akan memfagosit agen yang menyerang dengan akibat penghancuran dan
pemusnahan semua bentuk jejas.
Neutrofil merupakan sel pertama yang muncul dalam jumlah besar di
dalam eksudat pada jam-jam pertama peradangan (Price dan Wilson, 1992).
Stimulasi membran neutrofil menghasilkan radikal bebas yang berasal dari
oksigen. Anion superoksida dibentuk oleh reduksi oksigen molekuler yang dapat
memacu produksi molekul lain yang reaktif, seperti hidrogen peroksida (H2O2)
dan radikal hidroksil (OH·). Interaksi bahan-bahan ini dengan asam arakidonat menghasilkan pembentukan substansi substansi kemotaksis, selanjutnya secara
berkesinambungan meneruskan inflamasi (Furst dan Munster, 2002)
Pada proses peradangan terjadi pembentukan atau pengeluaran zat-zat
kimia di dalam tubuh yang dinamakan mediator. Mediator yang dikenal dalam
peradangan dapat dikelompokkan, yaitu dalam kelompok amina vaso aktif,
produk leukosit dan berbagai macam produk sel lainnya (Price dan Wilson, 1992;
Robins dan Kumar, 1995). Metabolit asam arakhidonat merupakan mediator
peradangan yang paling penting.
Asam arakhidonat ialah suatu asam lemah poli-tidak jenuh yang terdapat
dalam jumlah banyak sebagai fosfolipid selaput sel. Bila terdapat kerusakan pada
sel, maka enzim fosfolipase A2 diaktifkan untuk membebaskan asam arakhidonat
yang ada dari fosfolipid. Asam arakhidonat dapat juga dilepaskan oleh suatu
kombinasi fosfolipase C dan diasilgliserol lipase (DAG) lipase. Turunan asam
arakhidonat adalah eicosanoids (prostanoids dan leukotrienes). Prostanoids terdiri
dari zat-zat prostaglandin (PG) dan tromboksan (TX). Leukotrienes terdiri dari
zat-zat leukotrien (Rang, et al, 2003).
Asam arakhidonat dimetabolisme untuk diubah baik oleh enzim
siklooksigenase-1 (COX-1) maupun enzim siklooksigenase-2 (COX-2) menjadi
endoperoksida siklik (PGG2, PGH2) dan seterusnya menjadi zat-zat prostaglandin
dan tromboksan. Bagian lain dari arakhidonat diubah oleh enzim 5-lipoksigenase
menjadi zat-zat leukotrien, lipoksinin dan komponen lainnya (Rang, et al, 2003).
Prostaglandin dan leukotrien bertanggung jawab bagi sebagian besar dari gejala
peradangan. Selain itu radikal bebas oksigen yang dihasilkan peroksida juga
berperan dalam menimbulkan nyeri yang merupakan salah satu gejala peradangan
(Tjay dan Rahardja, 2002).
Enzim siklooksigenase bekerja ganda, memiliki dua aktivitas yang cukup
berbeda : aksi utama, membentuk PGG2, dan aksi peroksidase mengubah PGG2
dua isoenzim, yaitu siklooksigenase-1 (COX-1) dan siklooksigenase-2 (COX-2).
Enzim COX-1 terdapat di kebanyakan jaringan antara lain di ginjal dan saluran
cerna (Tjay dan Rahardja, 2002). Enzim COX-1 bersifat konstitutif (bersifat
pokok, selalu ada) dan diperkirakan prostanoids terlibat fungsi homeostatis
normal.. Enzim COX-2 dalam keadaan normal tidak terdapat di jaringan tetapi
dibentuk selama proses peradangan oleh stimulus inflamasi (Rang, et al, 2003).
Melalui jalur siklooksigenase-2 (COX-2), prostaglandin terpenting yang
terbentuk adalah prostaglandin-E2 (PgE2) dan prostaglandin-F2 (PgF2), zat ini
berdaya vasodilatasi dan meningkatkan permeabilitas dinding pembuluh dan
membran sinovial sehingga terjadi radang dan nyeri. Prostaglandin-E2 (PgE2) dan
prostasiklin dalam jumlah nanogram bisa menimbulkan eritema, vasodilatasi dan
peningkatan aliran darah lokal. Prostasiklin (PgI2) dibentuk terutama di dinding
pembuluh, berperan dalam vasodilatasi, anti trombosis, dan memiliki efek
protektif terhadap mukosa lambung. Mediator ketiga yang dibentuk pada jalur
siklooksigenase adalah tromboxan (TXA2, TXB2), zat ini berdaya vasokonstriksi
dan menstimulasi agregasi pelat darah (trombosit) (Tjay dan Rahardja, 2002).
Aksi prostanoid :
1. PGD2 : vasodilatasi, inhibisi agregasi platelet, relaksasi otot pencernaan,
relaksasi uterine, modifikasi pembebasan hormon hipotalamus.
2. PGF2α : kontraksi otot rahim pada manusia, luteolisis pada makhluk hidup
tertentu (hewan ternak), bronkonstriksi pada spesies lain (kucing dan
3. PGI2 : vasodilatasi, inhibisi agregasi platelet, pelepasan renin dan natriuresis
melalui efek reabsorbsi Na+ tubular.
4. Tromboksan A2 : vasokonstriksi, agregasi platelet dan bronkokonstriksi,
5. PGE2 memiliki aksi kerja antara lain sebagai berikut : a). pada reseptor EP1
menimbulkan kontraksi bronkial dan otot halus pencernaan b). pada reseptor
EP2 menimbulkan bronkodilatasi, vasodilatasi, stimulus sekresi cairan usus
dan relaksasi otot halus pencernaan c). pada reseptor EP3 menimbulkan
kontraksi otot halus usus, inhibisi sekresi asam lambung, meningkatkan
sekresi mukus lambung, inhibisi lipolisis, inhibisi pembebasan
neurotransmiter otonomik, dan stimulus kontraksi uterus pada wanita hamil
(Rang, et al, 2003)
PGE2, PGI2, dan PGD2 pada dasarnya adalah vasodilator yang sangat kuat
dan bersinergi dengan vasodilator inflamasi lain seperti histamin dan bradikinin.
Aksi kombinasi vasodilator tersebut berperan pada timbulnya kemerahan dan
peningkatan aliran darah pada daerah inflamasi akut. Zat-zat prostanoids ini tidak
secara langsung meningkatkan permeabilitas post capillary venules, tetapi
memperkuat efek dari histamine dan bradikinin (Rang, et al, 2003). Bahan-bahan
yang dihasilkan oleh jaringan yang menimbulkan reaksi ini meliputi histamin,
bradikinin, serotonin, prostaglandin (Guyton, 1993).
Melalui jalur lipoksigenase terbentuklah leukotrien yang juga merupakan
mediator radang dan nyeri. Leukotrien (LT) ini terdiri dari LTB4, LTC4, LTD4,
dan LTE4. LTC4, LTD4, dan LTE4 terutama dibentuk di granulosit eusinofil yang
khusus disintesis di makrofag dan neutrofil alveolar dan bekerja kemotaktis yaitu
menstimulus migrasi lekosit dengan jalan meningkatkan mobilitas dan fungsinya.
Dengan adanya leukotrien ini sejumlah besar lekosit akan menginvasi daerah
peradangan dan mengakibatkan gejala radang juga (Tjay dan Rahardja, 2002).
Leukotrien-B4 (LTB4) adalah kemotraktan kuat bagi eosinofil. Leukotrien tersebut
juga meningkatkan perlekatan eusinofil, degranulasi, dan pembentukan oksigen
radikal bebas (Furst dan Munster, 2002)
Fosfolipida selain diubah menjadi arakhidonat oleh enzim fosfolipase A2
juga diubah menjadi lyso-glyseril fosforilkolin yang diubah lagi menjadi Platelet
Activating Factor (PAF). Platelet Activating Factor menyebabkan agregasi dan
pelepasan trombosit, vasodilatasi, peningkatan permeabilitas vaskuler,
Bronkokonstriksi Menghambat agregasi
platelet,
Gambar 6. Mekanisme Inflamasi (Tjay dan Rahardja, 2002; Rang, et al., 2003)
Keterangan : = menghambat proses pembentukan
= proses pembentukan
= enzim yang berperan
OAINS = Obat Anti Inflamasi Non Steroid PAF = Platelet Activating Factor
D. Obat Anti Inflamasi
Pengobatan inflamasi meliputi dua sasaran yaitu pertama, mengurangi
nyeri sebagai gejala yang paling sering tampak, dan kedua dengan menghambat
atau mencegah proses pengrusakan jaringan. Pengobatan inflamasi dengan obat
anti inflamasi akan mengurangi nyeri selama waktu tertentu (Furst dan Munster,
2002).
Dua golongan senyawa yang banyak digunakan untuk menghambat
prostaglandin yaitu kortikosteroid dan anti inflamasi non steroid (AINS) (Greene,
et al, 2000).
1. Kortikosteroid
Kortikosteroid dibedakan menjadi dua golongan besar yaitu
glukokortikoid dan mineralokortikoid. Efek utama glukokortikoid ialah pada
penyimpanan glikogen hati dan efek anti-inflamasinya sedangkan
mineralokortikoid efek utamanya terhadap keseimbangan air dan elektrolit.
Pengaruh mineralokortikoid pada penyimpanan glikogen hati sangat kecil
(Wilmana, 1995)
Umumnya golongan mineralkortikoid tidak mempunyai khasiat
anti-inflamasi yang berarti, kecuali 9α-fluorokortisol, namun demikian sediaan ini
tidak pernah digunakan sebagai obat anti-inflamasi karena efeknya terhadap
keseimbangan air sangat besar (Wilmana, 1995).
Glukokortikoid dikenal dapat menghambat fosfolipase A2, enzim yang
bertanggung jawab atas pembebasan asam arakhidonat dari fosfolipid (Furst dan
menginduksi terbentuknya lipokortin. Lipokortin tersebut yang dapat menghambat
aktivasi enzim fosfolipase A2 (Rang, et al., 2003).
Kortikosteroid bekerja dengan menghambat enzim fosfolipase yang
berperan dalam pembentukan fosfolipid menjadi asam arakhidonat. Hal ini
mengakibatkan pembentukan histamin, prostaglandin, dan mediator-mediator
kimia lainnya dapat terhambat pula (Greene, et al., 2000). Berkurangnya
komponen vaskular inflamasi dan penghambatan pelepasan mediator kimia yang
berhubungan dengan kenaikan permeabilitas pembuluh darah dapat mengurangi
pembentukan udema. Efeknya terhadap gejala rematik lebih baik daripada AINS.
Keberatannya adalah efek sampingnya yang lebih berbahaya pada dosis tinggi dan
penggunaan lama (Tjay dan Rahardja, 2002). Termasuk dalam golongan ini
adalah kortison asetat, hidrokortison, prednison, prednisolon, deksametason, dan
lain-lain (Bowman dan Rand, 1980).
2. Anti Inflamasi Non Steroid (AINS)
Mekanisme kerja AINS adalah menghambat enzim siklooksigenase
sehingga konversi asam arakhidonat menjadi prostaglandin akan terganggu.
Idealnya AINS hanya menghambat COX-2 yang hanya timbul pada saat ada
peradangan dan tidak COX-1. Hal ini disebabkan karena penghambatan pada
COX-1 akan memberikan efek samping terhadap mukosa lambung-usus dan ginjal
(Tjay dan Rahardja, 2002).
Berbagai AINS mungkin memiliki mekanisme kerja tambahan termasuk
hambatan kemotaksis, regulasi rendah (down-regulation) produksi interleukin-1,
E. Natrium Diklofenak
CH2 COOH
NH
Cl Cl
Gambar 7. Struktur diklofenak
Natrium Diklofenak termasuk turunan fenilasetat yang terkuat daya anti
radangnya dan efek samping yang kurang keras dibandingkan dengan obat anti
inflamasi lainnya (indometasin, piroxicam) (Tjay dan Rahardja, 2002). Obat ini
adalah penghambat siklooksigenase yang relatif nonselektif dan kuat, juga
mengurangi bioavailabilitas asam arakhidonat (Furst dan Munster, 2002). Struktur
diklofenak dapat dilihat pada gambar 7 (Budavari, 1989).
Absorbsi obat ini melalui saluran cerna berlangsung cepat dan lengkap.
Obat ini terikat 99% pada protein plasma dan mengalami efek lintas awal sebesar
40-50%. Walaupun waktu paruhnya singkat yaitu 1-3 jam, diklofenak diakumulasi
di cairan sinovial yang menjelaskan efek terapi di sendi lebih lama dari waktu
paruh obat tersebut (Wilmana, 1995). Metabolismenya mengalami metabolisme
lintasan pertama dalam hati dan dimetabolisme hampir sempurna. Ekskresinya
berlangsung sebagian melalui kandung kemih sebagai glukoronida dan sisanya
melalui ginjal kurang dari 1 % (Tjay dan Rahardja, 2002).
Efek samping yang lazim adalah mual, gastritis, eritema kulit, dan sakit
penderita tukak lambung (Wilmana, 1995). Obat ini banyak digunakan sebagai
obat rematik, gangguan otot skelet lanilla, gout akut, dan nyeri paska bedah. Dosis
oral yang dianjurkan adalah 75-150 mg/hari dalam 2-3 dosis (Anonim, 2000).
F. Metode Pengujian Aktivitas Anti-Inflamasi
Metode pengujian aktivitas anti-inflamasi dapat dilakukan dengan cara :
1. In Vitro
In vitro adalah metode pengujian yang dilakukan di luar tubuh makhluk
hidup. Percobaan in vitro berguna untuk mengetahui peran dan pengaruh
substansi-substansi fisiologis seperti histamin, bradikinin, prostaglandin, dan
lain-lain dalam terjadinya inflamasi. Contoh percobaan in vitro antara lain-lain : pengikatan
reseptor 3H-bradikinin, pengikatan reseptor neurokinin, dan uji kemotaksis
leukosit polimorfonuklear (Vogel, 2002).
Daya anti inflamasi uji pengikatan reseptor 3H-bradikinin, ditunjukkan
dengan persen penghambatan pengikatan 3H-bradikinin terhadap reseptor pada
preparat membran. Daya anti inflamasi uji pengikatan neurokinin, juga
ditunjukkan dengan persen penghambatan pengikatan neurokinin terhadap
reseptor pada preparat membran. Sedangkan pada uji kemotaksis leukosit
polimorfonuklear, daya anti inflamasi ditunjukkan dengan persentase jumlah
leukosit polimorfonuklear yang bergerak ke arah kemoatraktan (contohnya
2. In Vivo
In vivo adalah metode pengujian yang dilakukan di dalam tubuh makhluk
hidup. Metode pengujian aktivitas anti inflamasi yang dapat dilakukan secara in
vivo dibedakan menjadi dua sesuai dengan jenis inflamasi yaitu inflamasi akut dan
inflamasi kronis. Inflamasi akut dapat dibuat dengan beberapa cara, yaitu dengan
induksi edema kaki tikus, pembentukan eritema (respon kemerahan) dan
pembentukan eksudatif inlamasi. Inflamasi kronik dibuat dengan cara
pembentukan granuloma dan induksi arthritis (Gryglewski, 1977).
1. Uji Eritema
Tanda paling awal dari reaksi inflamasi di kulit adalah kemerahan
(eritema) yang berhubungan dengan vasodilatasi, dimana belum disertai eksudasi
plasma dan udema. Pada marmot albino reaksi eritema terlihat dua jam setelah
penyinaran UV pada kulit yang telah dicukur. Uji eritema yang disebabkan UV
dapat digunakan untuk mengukur fase vasodilatasi pada reaksi inflamasi.
Mekanisme dari reaksi ini tidak diketahui, tapi pelepasan prostaglandin
kelihatannya berperan pada fenomena ini (Gryglewski, 1977). Keuntungan dari uji
ini adalah sederhana tapi membutuhkan latihan bagi penggunanya untuk
menggunakan fotometer refleksi dengan tujuan untuk menghilangkan penilaian
subjektif (Vogel, 2002)
2. Radang telapak kaki belakang
Diantara banyak metode yang digunakan untuk skrining obat
anti-inflamasi, satu dari teknik yang paling umum digunakan didasarkan pada
uji setelah injeksi bahan pembuat radang. Banyak zat pembuat radang (iritan)
yang telah digunakan seperti formaldehid, dextran, albumin telur, karagenin, dll
(Vogel, 2002). Iritan yang paling banyak digunakan adalah karagenin. Karagenin
adalah fosfolipida tersulfatasi yang diekstrak dari lumut irlandia Chondrus cripus
(Glyglewski, 1977). Reaksi inflamasi yang diinduksi karagenin mempunyai dua
fase: fase awal dan akhir. Fase awal berakhir setelah 60 menit dan dihubungkan
dengan pelepasan histamin, serotonin, dan bradikinin. Fase akhir terjadi antara 60
menit setelah injeksi dan berakhir setelah tiga jam. Fase ini dihubungkan dengan
pelepasan prostaglandin dan neutrofil yang menghasilkan radikal bebas, seperti
hidrogen peroksida, superoksida, dan radikal hidroksil (Suleyman, dkk, 2004).
Efeknya dapat diukur dengan memotong kaki belakang pada sendi torsocrural
dan ditimbang (Vogel, 2002).
3. Tes radang selaput dada
Radang selaput dada dikenal sebagai fenomena inflamasi eksudatif pada
manusia (Vogel, 2002). Radang selaput dada pada tikus dapat disebabkan injeksi
intrapleural dari turpentine, evans blue, gum arab, glikogen, dekstran, atau
karagenin. Pada waktu tertentu setelah injeksi iritan hewan uji dibunuh dan
eksudat dipindahkan, lebih baik dengan mencuci rongga dada dengan sejumlah
larutan Hank’s yang diketahui volumenya untuk memastikan didapatnya eksudat
dan sel utuh yang lengkap (Gryglewski, 1977). Radang selaput dada yang
disebabkan karagenin dipertimbangkan sebagai model inflamasi akut yang paling
yang ada dalam respon inflamasi dapat diukur dengan mudah dari eksudat (Vogel,
2002)
4. Radang Sendi
Hewan uji diinjeksi subplantar suspensi yang mengandung 0,5% mycobacterium
tuberculosis mati (0,05 ml untuk tikus dan 0,025 ml untuk mencit). Pemberian
obat untuk anti inflamasinya sudah diberikan satu hari sebelum injeksi dan
dilanjutkan maksimal sampai 28 hari. Untuk mengetahui adanya radang dilihat
saat benjolan sudah muncul (biasanya pada hari ke-13), kemudian diukur
volumenya (Williamson, 1996).
5. Tes kantung granuloma
Metode ini dapat digunakan untuk memperkirakan potensi anti-inflamasi
kortikosteroid (Vogel, 2002). Setelah kantung dibuat di punggung tikus dengan
injeksi subkutan 10 – 25 ml udara steril, berbagai iritan (minyak croton yang
dicairkan, turpentine, microbacterial, fosfolipase A2 atau karagenin) dimasukkan
pada lubang (Gryglewski, 1977). Empat puluh delapan jam sesudahnya udara
diambil dan hewan diinjeksi larutan uji atau larutan standar (Vogel, 2002). Empat
dampai empat belas hari setelahnya respon inflamasi dievaluasi dengan dasar
volume cairan yang diambil dari kantung sama seperti berat dan tebal dinding
kantung. Model kantung granuloma ini lebih sensitif terhadap obat anti-inflamasi
steroid daripada non steroid (Gryglewski, 1977).
Metode aktivitas anti inflamasi yang digunakan pada penelitian ini adalah
metode secara in vivo karena faktor keterbatasan alat, dan lebih aman
in vivo yang digunakan adalah metode Langford dkk (1972) yang telah
dimodifikasi pelaksanaannya. Bila dibanding metode in vivo lainnya, metode ini
dipilih karena dapat digunakan sebagai langkah pengujian awal untuk mengetahui
apakah bahan uji memiliki efek anti inflamasi atau tidak. Selain itu karena metode
ini mudah dilaksanakan, pengukuran dapat dilakukan secara obyektif serta dapat
diandalkan untuk pengujian efek anti inflamasi dalam waktu yang singkat.
Dasar metode Langford dkk (1972) ini adalah induksi udema pada telapak
kaki belakang mencit. Metode ini dimodifikasi pelaksanaannya dengan mengganti
zat penginduksi udem (karagenin 1% meggantikan ragi) serta rumus efek anti
inflamasinya. Menurut Langford dkk (1972) persentase efek anti inflamasi dapat
dihitung dari perubahan bobot kaki hewan uji dengan rumus sebagai berikut :
% efek anti inflamasi = ⎢⎣⎡ − ⎥⎦⎤ D
D U
X 100%
keterangan :
U : Harga rata berat kaki kelompok karagenin (terinflamasi) dikurangi
rata-rata berat kaki kelompok normal ( tanpa perlakuan )
D : Harga rata berat kaki kelompok perlakuan (terinflamasi) dikurangi rata-rata berat kaki normal ( tanpa perlakuan )
Setelah dianalisis lebih lanjut, rumus di atas ternyata menunjukkan
peningkatan udema. Karena persentase efek anti inflamasi dihitung dari
% efek anti inflamasi = ⎢⎣⎡ − ⎥⎦⎤ U
D U
X 100%
keterangan :
U : Harga rata berat kaki kelompok karagenin (terinflamasi) dikurangi
rata-rata berat kaki kelompok normal ( tanpa perlakuan )
D : Harga rata berat kaki kelompok perlakuan (terinflamasi) dikurangi rata-rata berat kaki normal ( tanpa perlakuan )
D U
II III I
(U-D) Bobot kaki
U = Kelp. II – Kelp.III D = Kelp. II – Kelp. I
% 100 U
D U inflamasi anti
% = − x
Gambar 8. Rumus perhitungan anti inflamasi
Keterangan :
I : + inflamatogen + obat (bahan yang diuji) II : + inflamatogen
G. Landasan Teori
Inflamasi terjadi karena adanya reaksi antara jaringan ikat pembuluh
dengan pengaruh-pengaruh yang merusak (noksi) baik kimia, fisika, maupun
infeksi organisme. Rangsangan tersebut membuat adanya pembebasan
mediator-mediator inflamasi yang meliputi : histamin, eicosanoid (prostaglandin,
tromboksan, leukotrien), PAF (platelet activating factor), bradikinin, nitrit oksida,
neuropeptida, dan cytokine (seperti interleukin, intereferon, dll) (Rang, et al,
2003)
Akar dan daun krokot belanda mengandung saponin, dan flavonoid
(Anonim, 1994), di samping itu akarnya juga mengandung tanin dan steroid
(Misra, 1992; Dalimarta, 2003).
Efek flavonoid terhadap organisme sangat banyak macamnya sehingga
tumbuhan yang mengandung flavonoid dapat dipakai dalam pengobatan.
Flavonoid menunjukkan aktivitasnya sebagai anti alergi, anti inflamasi, anti
mikrobial, dan anti kanker. Flavonoid mampu menghambat enzim lipoksigenase
sehingga pembentukan leukotrien (Robinson, 1995) yang dapat menyebabkan
peradangan menjadi terhambat. Flavonoid juga dikenal dengan aktivitasnya
sebagai antioksidan (Anonim, 2007a)
Steroid juga bermanfaat sebagai anti inflamasi dengan menghambat
pelepasan prostaglandin dari sel-sel sumbernya (Anonim, 1991). Selain itu, di
dalam dunia kesehatan tanin juga bermanfaat mengurangi bengkak (edema)
aktivitasnya sebagai penangkal radikal bebas, karena radikal bebas dapat
merangsang terjadinya proses inflamasi (Diane, 2006).
Etanol dapat melarutkan flavonoid, steroid, saponin, dan tanin. Pada
penelitian ini digunakan etanol 70% dengan harapan senyawa aktif yang
terkandung dalam akar krokot belanda dapat terekstraksi dengan baik. Adanya
senyawa kimia akar krokot belanda yang dapat terekstrak oleh etanol 70%,
diharapkan memiliki aktivitas sebagai anti inflamasi.
H. Hipotesis
Ekstrak etanol akar krokot belanda memiliki efek anti inflamasi terhadap
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian tentang uji efek anti inflamasi ekstrak etanol akar krokot belanda pada mencit putih betina ini merupakan jenis penelitian eksperimental murni dengan menggunakan rancangan acak lengkap pola searah.
B. Metode Penelitian
Pada penelitian ini digunakan metode pembentukan radang telapak kaki belakang dengan menggunakan hewan uji mencit betina. Metode ini merupakan metode yang telah dikembangkan oleh Langford dkk. (1972). Dasar metode yang pelaksanaannya telah dimodifikasi ini adalah dengan membuat udema pada telapak kaki belakang mencit menggunakan karagenin 1%, kemudian kaki dipotong pada sendi torsocrural dan ditimbang. Persentase efek anti inflamasi dapat dihitung dari perubahan bobot kaki mencit dengan rumus sebagai berikut :
% efek anti inflamasi = ⎢⎣⎡ − ⎥⎦⎤ U
D U
X 100%
keterangan :
U : Harga rata berat kaki kelompok karagenin (terinflamasi) dikurangi rata-rata berat kaki kelompok normal ( tanpa perlakuan )
D : Harga rata berat kaki kelompok perlakuan (terinflamasi) dikurangi rata-rata berat kaki normal ( tanpa perlakuan )
C. Variabel dan Definisi Operasional 1. Variabel Penelitian
Variabel penelitian ini meliputi: a. Variabel utama
1). Variabel bebas : dosis ekstrak etanol akar krokot belanda 2). Variabel tergantung : persentase efek anti inflamasi b. Variabel pengacau terkendali
umur mencit 2-3 bulan, berat badan mencit 20-30 gram, jenis kelamin betina, galur Swiss, umur tanaman, tempat tumbuh tanaman, dan waktu pemanenan.
c Variabel pengacau tak terkendali Kondisi patologis hewan uji 2. Definisi operasional
Definisi operasional penelitian ini adalah : a. Dosis ekstrak etanol akar krokot belanda
Dosis ekstrak etanol akar krokot belanda adalah sejumlah miligram (mg) ekstrak etanol kental akar krokot belanda hasil perkolasi, yang disuspensikan dalam sejumlah CMC-Na 1% dan diberikan secara peroral tiap kg berat badan mencit
b. Persentase efek anti inflamasi
efek anti inflamasi dapat dihitung dari perubahan berat kaki hewan uji (berat kaki terinflamasi (kontrol negatif) dikurangi berat kaki terinflamasi yang telah diobati dengan ekstrak etanol akar krokot belanda).
c. Ekstrak etanol akar krokot belanda
Ekstrak etanol akar krokot belanda adalah ekstrak kental yang diperoleh dengan mengekstraksi 150 gram serbuk kering akar krokot belanda secara perkolasi dengan menggunakan pelarut etanol 70% sejumlah 4000 ml selama 2 minggu.
D. Subyek dan Bahan Penelitian 1. Subjek uji
Subjek uji yang digunakan adalah mencit betina galur Swiss dengan berat badan 20-30 gram dengan umur 2-3 bulan, yang diperoleh dari laboratorium Farmakologi Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Bahan penelitian a. Bahan uji
Bahan uji yang digunakan berupa ekstrak etanol akar krokot belanda. Akar krokot belanda diperoleh dari Balai Penelitian Tanaman Obat (BPTO) Tawangmangu, Kabupaten Karang Anyar, Jawa Tengah.
b. Bahan kimia
1) Natrium Diklofenak sebagai kontrol positif berupa bantuan yang diperoleh dari PT. Fahrenheit, Tangerang.
2) Karagenin tipe I (Sigma Chemical Co) sebagai zat penginduksi radang yang diperoleh dari Laboratorium Farmakologi-Toksikologi Universitas Sanata Dharma Yogyakarta
3) NaCl 0,9% sebagai pensuspensi karagenin yang diperoleh dari Laboratorium Farmakologi-Toksikologi Universitas Sanata Dharma Yogyakarta
4) CMC-Na produksi Merck, Jerman sebagai pensuspensi natrium diklofenak dan ekstrak etanol yang diperoleh dari Laboratorium Farmakologi-Toksikologi Universitas Sanata Dharma Yogyakarta 5) Aquadest sebagai pengencer konsentrasi etanol yang diperoleh dari
Laboratorium Farmakologi-Toksikologi Universitas Sanata Dharma Yogyakarta
6) Etanol kualitas p.a. (pro analisa) produksi Merck, Jerman, sebagai pelarut dalam perkolasi, yang diperoleh dari Laboratorium Farmakognosi Fitokimia, Universitas Sanata Dharma, Yogyakarta.
E. Alat atau Instrumen Penelitian
Ika Combimag Net spuit injeksi subplantar 1 ml merek Terumo; spuit injeksi per oral 1 ml merek Terumo; stopwatch; seperangkat alat bedah.
F. Tata Cara Penelitian 1. Determinasi tanaman
Determinasi tanaman krokot belanda dilakukan oleh Balai Penelitian Tanaman Obat (BPTO) Tawangmangu, kabupaten Karang Anyar, Jawa Tengah. 2. Pengumpulan bahan
Akar tanaman krokot belanda diperoleh dari Balai Penelitian Tanaman Obat (BPTO) Tawangmangu, kabupaten Karang Anyar, Jawa Tengah. Akar krokot belanda yang diperoleh berupa serbuk kering.
3. Pembuatan ekstrak etanol akar krokot belanda
4. Penyiapan hewan uji
Hewan uji yang digunakan dalam penelitian adalah mencit betina, galur Swiss, usia 2-3 bulan, dengan berat badan 20-30 gram. Hewan uji dibagi secara acak menjadi 2 kelompok. Kelompok untuk orientasi sebanyak 40 ekor dan kelompok perlakuan sebanyak 63 ekor. Sebelum digunakan, mencit dipuasakan 18-24 jam dan tetap diberi minum. Kelompok perlakuan terdiri dari 9 kelompok yaitu kontrol negatif karagenin 1 %, kontrol negatif CMC-Na 1%, kontrol positif natrium diklofenak dalam 3 peringkat dosis (9,75; 10,795; dan 11,95 mg/kg BB) dan kelompok perlakuan ekstrak etanol akar krokot belanda dalam 4 peringkat dosis (1674,49; 2411,26; 3472,22; dan 5000 mg/kgBB).
5. Pembuatan suspensi karagenin 1%
Timbang 100 mg karagenin, larutkan dengan larutan NaCl fisiologis 0,9% dalam labu takar 10 ml.
6. Pembuatan CMC-Na 1%
Larutan CMC-Na 1% dibuat dengan cara menimbang secara seksama CMC-Na sebanyak 1 gram kemudian dilarutkan ke dalam sejumlah air panas sambil terus diaduk-aduk sampai semuanya terlarut dan menjadi jernih. Larutan dituang ke dalam labu ukur 100 ml dan tambahkan air panas sampai diperoleh volume 100 ml.
7. Pembuatan larutan natrium diklofenak
8. Pembuatan suspensi ekstrak etanol akar krokot belanda
Timbang ekstrak etanol akar krokot belanda dan suspensikan ke dalam larutan CMC-Na sampai diperoleh konsentrasi tertentu berdasarkan orientasi 9. Penetapan dosis
a. karagenin 1 %
Dosis karagenin ditetapkan berdasarkan penelitian Williamson, Okpako, dan Evans (1996) dengan konsentrasi karagenin yang digunakan adalah 1% dengan volume 0,05 ml. 0,05 ml karagenin 1% adalah volume pemberian untuk mencit dengan berat 20 gram sehingga dosis bisa dicari dengan cara :
Dosis karagenin =
b. Natrium Diklofenak
Dosis natrium diklofenak yang digunakan sebagai dosis orientasi adalah 9,75 mg/kg BB; 10,795 mg/kg BB; 11, 95 mg/kg BB. Dosis ini diperoleh berdasarkan penelitian sebelumnya yang dilakukan oleh Novita (2003).
konversi ke mencit 20 gBB = 91,923 mg/70kgBB x 0,0026 = 0,239 mg/20 gBB
= 11,95 mg/kgBB c. CMC 1%
Sebagai kontrol negatif CMC 1% diberikan secara per oral, dan volume pemberian maksimal pada mencit adalah 1 ml, diketahui berat mencit maksimal dalam penelitian ini adalah 30 g sehingga bisa dihitung dengan rumus: d. ekstrak etanol akar krokot belanda
Dosis tertinggi ekstrak etanol akar krokot belanda ditetapkan berdasarkan konsentrasi maksimal yang diperoleh saat orientasi sebesar 15%.
Penetapan dosis tertinggi ekstrak etanol akar krokot belanda sesuai rumus : V (ml)x C (mg/ml) = BB (kg) x D (mg/kg)
Volume pemberian x Konsentrasi = Berat badan x Dosis 1 ml x 150 mg/ml = 0,03 kgBB x Dosis
kemudian dicari peningkatannya untuk menentukan dosis tengah melalui rumus :
Peningkatan = 1
terendah tertinggi
−
n
dosis dosis
Peningkatan = 4 1
kgBB 1666,67mg/
B 5000mg/kgB
− = 1,44
Keterangan :
n = jumlah peringkat dosis
Tiga dosis dibawah dosis tertinggi diperoleh dengan membagi dosis 1,44 kali dari dosis tertinggi sesuai deret ukur. Dari hasil perhitungan diperoleh dosis ekstrak etanol akar krokot belanda sebesar 1674,49 mg/kgBB; 2411,26 mg/kgBB; 3472,22 mg/kgBB; 5000 mg/kgBB.
10. Uji pendahuluan rentang waktu pemotongan kaki setelah injeksi suspensi karagenin 1%