BAB II
TINJAUAN PUSTAKA 2.1 Minyak Sawit dan Minyak Inti Sawit
Kelapa sawit (Elaeis guineensis Jacq.) pada bagian buahnya terdiri dari eksokarp (kulit paling luar), mesokarp (serabut, mirip serabut kelapa), endokarp (tempurung), dan kernel (inti sawit). Pengolahan bagian serabutnya (mesokarp) dengan cara ekstraksi dapat menghasilkan minyak sawit (crude palm oil), sedangkan pengolahan bagian kernel (inti) dapat menghasilkan minyak inti sawit (palm kernel oil) (Haryati, 1999). Minyak sawit dan minyak inti sawit memiliki perbedaan dalam hal karakteristiknya walaupun keduanya berasal dari pohon yang sama. Minyak sawit kaya akan asam lemak berupa C16 dan C18, sedangkan minyak inti sawit kaya akan asam lemak C12 (O’Brien, 2009).
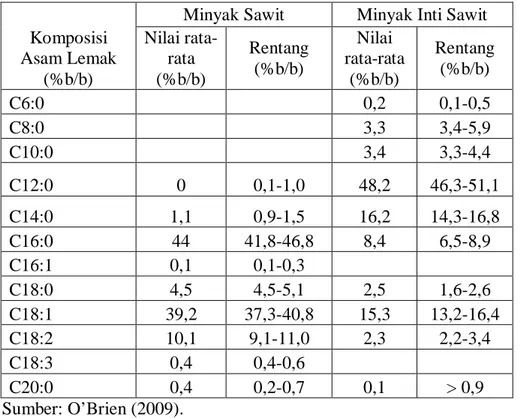
Minyak sawit dan minyak inti sawit dapat dipergunakan untuk bahan makanan melalui proses penyulingan, penjernihan dan penghilangan bau. Disamping itu minyak sawit dan minyak inti sawit dapat difraksinasi sehingga menghasilkan produk Stearin dan Olein. Fraksinasi minyak sawit menghasilkan fraksi stearin (palm stearin) dan fraksi olein (palm olein) sedangkan minyak inti sawit difraksinasi menghasilkan fraksi stearin (palm kernel stearin) dan fraksi olein (palm kernel olein). Karakteristik komposisi asam lemak dari minyak sawit dan minyak inti sawit dapat dilihat pada Tabel 1. Fraksi stearin dari minyak inti sawit (palm kernel stearin, PKS) dapat digunakan sebagai cocoa butter substituted (CBS) setelah mengalami hidrogenasi penuh ( De Greyt, 2003). Selain CBS, CBR yang merupakan CBS non laurat dapat dihasilkan dengan cara hidrogenasi sebagian dan fraksinasi dari minyak sawit dan minyak inti sawit (Hasibuan, 2009).
Tabel 1. Karakteristik komposisi asam lemak dari minyak sawit dan minyak inti sawit
Komposisi Asam Lemak
(%b/b)
Minyak Sawit Minyak Inti Sawit Nilai rata-rata (%b/b) Rentang (%b/b) Nilai rata-rata (%b/b) Rentang (%b/b) C6:0 0,2 0,1-0,5 C8:0 3,3 3,4-5,9 C10:0 3,4 3,3-4,4 C12:0 0 0,1-1,0 48,2 46,3-51,1 C14:0 1,1 0,9-1,5 16,2 14,3-16,8 C16:0 44 41,8-46,8 8,4 6,5-8,9 C16:1 0,1 0,1-0,3 C18:0 4,5 4,5-5,1 2,5 1,6-2,6 C18:1 39,2 37,3-40,8 15,3 13,2-16,4 C18:2 10,1 9,1-11,0 2,3 2,2-3,4 C18:3 0,4 0,4-0,6 C20:0 0,4 0,2-0,7 0,1 > 0,9 Sumber: O’Brien (2009).
Lemak dan minyak nabati merupakan komponen penting dalam formulasi bahan pangan tertentu seperti margarin, minyak goreng, minyak salad, coklat, konfeksioneri, coffee creamer, topping, dan icings (dua terakhir digunakan dalam industri kue). Minyak dan lemak mempengaruhi karakteristik bahan pangan tersebut, seperti sifat fungsional, citarasa (tekstur, rasa, kelezatan) dan nilai gizi (sumber energi, penyedia asam lemak esensial dan sebagai pelarut vitamin A, D, E, dan K) (Siahaan, 1996).
2.2 Proses Produksi Modifikasi Minyak Sawit dan Minyak Inti Sawit Menjadi Cocoa Butter Substitute (CBS), Cocoa Butter Replacer (CBR), dan Cocoa Butter Equivalent (CBE)
Modifikasi minyak sawit dan minyak inti sawit menjadi hard butter dilakukan dengan cara hidrogenasi, interesterifikasi, dan fraksinasi. Modifikasi ini dilakukan dengan menggunakan satu atau beberapa proses seperti yang tersebut di
atas. Sedangkan pendekatan formulasi hard butter dapat dilakukan dengan dua cara. Pertama dengan cara replikasi komposisi trigliserida, cara ini digunakan terutama dalam pembuatan CBE. Kedua, dengan pendekatan sifat fungsional yang diharapkan dapat diperoleh dalam formulasi yang dihasilkan. Cara ini dilakukan dalam pembuatan CBS (Siahaan, 1996).
Hidrogenasi minyak atau lemak merupakan proses penambahan molekul hidrogen pada rantai asam lemak tidak jenuh sehingga menyebabkannya menjadi jenuh dengan menambahkan satu molekul hidrogen pada masing-masing ikatan rangkap. Proses hidrogenasi dikembangkan oleh Norman 1902, dengan mengkonversikan minyak cair menjadi bentuk semi padat yang digunakan untuk produk shortening atau margarin (Silalahi, 1999). Tujuan utama dari hidrogenasi ini yaitu untuk meningkatkan stabilitas oksidatifnya dan untuk meningkatkan kandungan lemak padatnya sehingga titik lelehnya meningkat dan dapat memperbaiki tekstur makanan (Kodali, 2005). Hidrogenasi sebagian adalah proses yang merubah sebagian asam lemak tak jenuh menjadi asam lemak jenuh dan berpotensi menghasilkan asam lemak trans. Sedangkan hidrogenasi total adalah proses yang merubah seluruh asam lemak tidak jenuh menjadi asam lemak jenuh (Basiron, 2000).
Proses fraksinasi dapat memisahkan minyak atau lemak menjadi fraksi-fraksi yang mempunyai sifat fisika yang berbeda dari bentuk aslinya. Pemisahan fraksi minyak atau lemak didasarkan pada kelarutannya dalam komponen trigliserida. Perbedaan kelarutan secara langsung berhubungan dengan tipe trigliserida didalam sistem lemak. Tipe trigliserida ditentukan oleh komposisi asam lemaknya dan distribusi asam lemak dalam masing-masing molekul trigliserida. Komponen minyak atau lemak yang berbeda titik lelehnya dapat
dipisahkan dengan cara kristalisasi dan filtrasi untuk memisahkan minyak atau lemak didasarkan pada jenis produknya. Ada dua tujuan utama dari aplikasi fraksinasi: (i) menghilangkan bentuk fraksi dari minyak dan lemak yang tidak diinginkan dan (ii) menghasilkan fraksi yang bermanfaat dan memiliki sifat yang unik. Ada tiga proses fraksinasi yang umum digunakan yaitu dry fractionation, detergent fractionation, dan solvent fractionation. Pada dry fractionations, prosesnya didasarkan pada pendinginan dibawah kondisi yang dikontrol untuk kristalisasi yang lambat dengan tidak adanya pelarut. Solvent fractionation didasarkan pada perbedaan kelarutan dari gliserida pada suhu yang diberikan. (Silalahi, 1999).
Istilah interesterifikasi berhubungan dengan rekasi antara minyak atau lemak yang mana ester asam lemak yang satu bereaksi dengan ester asam lemak lainya untuk menghasilkan senyawa ester yang baru dengan mengubah kelompok asam lemaknya (O’Brien, 2009).
2.2.1 Cocoa Butter Substitutes (CBS)
CBS mempunyai sifat kimia yang berbeda sama sekali dengan CB, tetapi beberapa sifat fisiknya mirip, sehingga hanya sebagai pensubstitusi CB. Cocoa butter substitutes dapat dikelompokkan menjadi dua bagian yaitu CBS laurat dan CBS non laurat (Minifie, 1989).
CBS Laurat
CBS laurat ini merupakan lemak dengan sifat kimia yang berbeda dan tidak kompatibel dengan cocoa butter. Umumnya terdiri atas asam lemak dengan rantai pendek. Lemak ini kebanyakan berasal dari minyak inti sawit yaitu dari fraksi stearin yang mempunyai karakteristik yang hampir sama dengan cocoa butter dan dari minyak inti sawit yang dihidrogenasi. CBS laurat memiliki sifat stabilitas
yang baik dan teksturnya juga sangat baik. Lemak ini harganya lebih murah dibanding cocoa butter (Minifie, 1989).
CBS Non Laurat
Lemak ini terdiri dari fraksi yang diperoleh dari proses hidrogenasi minyak. Minyak ini dihidrogenasi secara selektif dan menyebabkan terbentuknya asam lemak trans (Minifie, 1989). CBS nonlaurat ini umumnya disebut sebagai cocoa butter replacer (CBR) yang mempunyai sifat diantara CBS laurat dan CBE. CBR mempunyai distribusi asam lemak yang mirip dengan CB, tetapi struktur triasilgliserolnya berbeda, sehingga hanya dalam rasio kecil kompatibel dengan CB. CBE mempunyai fungsionalitas yang paling tinggi diantara ketiga jenis cocoa butter alternative (CBA), oleh karena itu harga CBE relatif paling mahal dan CBS relatif paling murah (Sokopitojo, 2008).
2.2.2 Cocoa Butter Equivalents (CBE)
CBE mempunyai sifat fisikokimia mirip dengan CB dan sepenuhnya kompatibel dengan CB. CBE didesain untuk menggantikan CB atau dapat dicampur dengan CB pada proporsi berapapun tanpa mengakibatkan perubahan yang berarti pada kualitas akhir produk-produk coklat, baik sifat pelelehan, kristalisasi maupun reologinya. Salah satu teknik produksi CBE yang banyak dilakukan selama ini adalah dengan cara blending (pencampuran) antara lemak yang kaya triasilgliserol POP dengan lemak yang kaya triasilgliserol POS dan SOS. Formulasi yang proporsional akan menghasilkan lemak dengan sifat pelelehan dan kristalisasi yang sangat mirip dengan CB (Sokopitojo, 2008).
Pada awalnya produk CBE dikembangkan dengan pertimbangan ekonomi untuk menurunkan biaya produksi. Seiring dengan kemajuan teknologi dan kebutuhan industri, maka perkembangan selanjutnya bergeser ke arah peningkatan
fungsionalitas dari produk CBE tersebut antara lain untuk memperbaiki toleransi terhadap lemak susu, meningkatkan daya tahan terhadap panas (pada iklim panas), memperbaiki daya tahan terhadap blooming (gloss retentiton), memperbaiki kemudahan tempering dan sebagainya. Oleh karena itu, aplikasi CBE menjadi semakin luas, tidak hanya terbatas untuk produk coklat konfeksioneri tetapi juga untuk produk-produk snack lainnya yang menggunakan coklat dalam variasi produknya (Sokopitojo, 2008).
2.3 Asam Lemak Trans
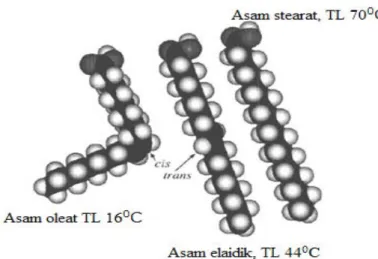
Asam lemak trans merupakan asam lemak tidak jenuh yang terdiri dari sedikitnya memiliki satu ikatan rangkap berada pada konfigurasi trans sebagai hasil dari konfigurasi geometrik. Di alam kebanyakan asam lemak memiliki atom hidrogen yang atom karbonnya terikat pada sisi yang sama dari suatu molekul atau disebut juga bentuk cis. Atom hidrogen yang terikat pada atom karbon yang ikatan rangkapnya berada pada posisi berseberangan dari suatu molekul disebut dengan isomer trans. Asam lemak trans selalu mempunyai titik leleh yang lebih tinggi dan stabillitas oksidasi yang lebih baik dibanding bentuk cis-nya (O’Brien,
2009).
Gambar 1. Sruktur molekul asam oleat (cis-9, titik leleh 160C), asam elaidik (trans-9, titik leleh 440C), dan asam stearat (titik leleh 700C).
2.3.1 Proses Terbentuknya Asam Lemak Trans
Mayoritas asam lemak trans terbentuk dari proses pengolahan minyak, yaitu proses hidrogenasi dan juga sedikitnya karena proses deodorisasi, penggorengan, dan pemanggangan. Jumlah asam lemak trans bisa mencapai 50% karena pengaruh proses hidrogenasi parsial (persen dari lemak total). Isomerisasi selama deodorisasi, pemanasan, dan pemanggangan merupakan fungsi waktu dan temperatur. Tergantung pada kondisi prosesnya, 3-24% asam lemak linolenat dan maksimum 2% asam lemak linoleat akan dikonversikan menjadi bentuk isomer trans. Kondisi deodorisasi selama 60 menit pada suhu 2500C (4820F) menghasilkan 1,8% asam lemak trans pada proses minyak canola (O’Brien, 2009).
2.3.2 Pengaruh Asam Lemak Trans
Berdasarkan hasil penelitian selama dekade terakhir ini menunjukkan bahwa keberadaan asam lemak trans (trans fatty acid, TFA) dalam makanan dapat menimbulkan dampak negatif terhadap kesehatan yakni sebagai pemicu penyakit jantung koroner (PJK). Konsumsi TFA bisa menaikkan kadar low density lipoprotein (LDL), sama seperti pengaruh dari asam lemak jenuh. Akan tetapi disamping meningkatkan LDL, TFA juga akan menurunkan high density lipoprotein (HDL), sedangkan asam lemak jenuh tidak akan mempengaruhi kadar HDL. Tambahan lagi, TFA cenderung menaikkan lipoprotein aterogenik. Jadi efek negatif TFA adalah lebih besar daripada asam lemak jenuh dan kolesterol. TFA juga dapat mengurangi kemampuan tubuh mengendalikan gula darah karena dapat mengurangi respon terhadap hormon insulin (Silalahi dan Tampubolon, 2002).
Karena efek negatif asam lemak trans ini maka pada 11 Juli 2003, Food and Drug Administration’s (FDA) mengeluarkan aturan yang memerintahkan agar sejumlah produsen melabelin sejumlah asam lemak trans yang ada dalam produk makanan termasuk juga dalam suplemen. Hal ini akan membantu konsumen mengerti bahwa asam lemak trans berbeda secara kimia dengan asam lemak jenuh dan akan membantu konsumen mengatur diet kesehatan (Moss, 2005).
2.3.3 Analisis Asam Lemak Trans
Asam lemak trans yang terdapat di dalam makanan dapat dianalisa menggunakan kromatografi gas cair dengan menggunakan kolom kapiler, dalam hal ini dapat dipisahkan isomer cis dan isomer trans-nya. Jumlah asam lemak trans yang terdapat di dalam makanan yang mengandung minyak terhidrogenasi berkisar antara 0-34,9%. Kandungan asam lemak trans pada makanan ini bervariasi tergantung pada perbedaan minyak atau lemak yang digunakan pada proses pembuatan (Semma, 2002).
Beberapa penelitian yang telah dilakukan terhadap berbagai jenis makanan untuk mengetahui jumlah asam lemak trans antara lain yaitu, Satchithanandam, et al (2004) menganalisis 117 produk makanan berupa margarin, kue dan crakers, produk kentang goreng, minyak nabati dan shorthening, cereals, dan mayonnaise yang ada di Amerika secara kromatografi gas dan diperoleh hasil 30% produk makanan berupa roti dan kue yang dianalisa kandungan asam lemak transnya melewati 25 g/100 g lemak, pada produk margarin diperoleh hasil jumlah ALT + asam lemak jenuh berkisar antara 33-42 g/100 g lemak, crakers 8-35 g ALT/100 g lemak, produk kentang goreng 25-38 g ALT/ 100 g lemak, dan untuk
produk-produk seperti minyak nabati, shorthening, mayonnaise, dan cereal memiliki jumlah asam lemak trans yang sangat rendah.
Kromatografi gas telah luas digunakan dalam metode analisa metil ester asam lemak (fatty acid methyl ester/FAME). Kesuksesan pemisahan komposisis asam lemak trans dalam bentuk FAME dengan kromatografi gas bergantung pada kondisi percobaan dari metode yang digunakan. Kebanyakan metode kromatografi gas untuk mendeteksi trans menggunakan kolom kapiler yang panjang dengan fase diam berupa senyawa yang kepolarannya tinggi. Dibawah kondisi ini, pemisahan berdasarkan pada panjang rantai dari asam lemak, derajat ketidakjenuhan, dan geometri serta posisi ikatan rangkapnya. Deretan elusi yang diharapkan untuk asam lemak yang spesifik dengan panjang rantai yang sama pada kolom yang kepolarannya tinggi yaitu sebagai berikut: bentuk jenuh (saturated), bentuk tidak jenuh dengan satu ikatan rangkap (monounsaturated), bentuk tidak jenuh dengan dua ikatan rangkap (diunsaturated), dll (Mossoba, 2005).
Berdasarkan AOCS Ce If-96 (AOCS, 1999), penentuan kualitatif dan kuantitatif untuk isomer asam lemak trans, saturated fatty acid (SFA), monounsaturated fatty acid (MUFA), dan polyunsaturated acid (PUFA) secara kromatografi gas dapat menggunakan kolom kapiler. AOCS Ce If-96 juga menetapkan bahwa kolom yang dapat digunakan bisa pendek (50-60 m) atau panjang (100-120 m) dengan fase diam yang kepolarannnya tinggi. Selain itu, detektor yang dapat digunakan yaitu flame ionization detector (FID) dengan suhu pengoperasian 2500C. Gas pembawa yang dapat digunakan yaitu helium, nitrogen, atau hidrogen. Metode boron triflorida merupakan metode yang dapat digunakan
untuk menghasilkan asam lemak metil ester dari trigliserol minyak atau lemak. kloroform (Mossoba, 2005)
Metil ester asam lemak dari minyak sawit dan minyak inti sawit dibuat terlebih dahulu dengan mereaksikan minyak dengan NaOH yang akan membentuk garam natrium asam lemak, reaksi akan terus berlangsung hingga seluruh asam lemak lepas dari lemak. Kemudian ke dalam garam natrium asam lemak ditambahkan BF3 14% dalam metanol maka akan terbentuk metil ester asam
lemak dengan reaksi sebagai berikut:
O O O C O R C O R C O R Na O O O C O R C O R OH C O R OH + O O O C O R C O R + R C O OH + Na
O O O C O R C O R + R C O O H + Na O O OH C O R C O R + R C O ONa Garam Natrium CH3 O H + BF3 CH3 H O BF3 R CO O Na + H3C O BF3 H R C O OCH3 + H O BF3 + Na R C O OCH3 + BF3 + NaOH
Metil Ester Asam Lemak
Pembuatan metil ester asam lemak menggunakan NaOH gunanya untuk membentuk metoksida yang bersifat basa kuat sehingga pembentukan metil ester menjadi lebih baik. BF3 adalah asam Lewis sebagai katalisator yang dapat
menerima sepasang elektron sehingga pembentukan metanoat lebih cepat dan sempurna (Solomons, 1994). NaCl jenuh berguna untuk memisahkan koloid
berwarna putih yang tersebar dalam larutan akibat dari komponen asam lemak yang tidak tersabunkan. Sedangkan isooktan digunakan sebagai pelarut untuk mengekstraksi metil ester asam lemak (Haryati, 1994).
Pembuatan metil ester untuk sampel coklat dilakukan setelah coklat diekstraksi menggunakan n-heksan secara sokletasi sehingga didapat ekstrak berupa minyak. Lalu minyak yang diperoleh ini dapat direaksikan dengan Na metanolik menggunakan katalisator BF3 sehingga didapat bentuk asam lemak
metil esternya.
2.4 Kromatografi Gas
Dasar pemisahan secara kromatografi gas ialah penyebaran cuplikan diantara dua fase, yaitu fase diam yang permukaannya luas dan fase lain berupa gas yang melewati fase diam. Kromatografi gas ialah suatu cara untuk memisahkan senyawa atsiri dengan mengalirkan arus gas melalui fase diam berupa zat padat (Kromatografi gas padat). Jika fase diam berupa zat cair, cara tadi disebut Kromatografi gas cair. Fase cair diselaputkan berupa lapisan tipis pada zat padat yang lembam dan pemisahan didasarkan pada partisi cuplikan yang masuk dan keluar dari lapisan zat cair ini (Bonelli, 1988).
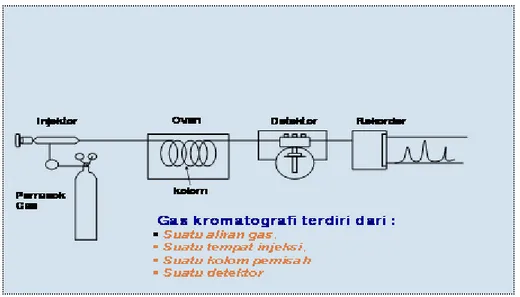
Alat kromatografi gas terdiri atas 7 bagian, yaitu:
1. Silinder tempat gas pembawa/pengangkut 2. Pengatur aliran dan pengatur tekanan 3. Tempat injeksi cuplikan
4. Kolom 5. Detektor 6. Pencatat
Gambar 2. Diagram blok perangkat kromatografi gas Bagian-bagian dari kromatografi gas :
1. Gas pembawa
Gas pembawa merupakan fase gerak yang tujuan utamanya adalah membawa sampel melewati kolom. Gas pembawa harus memenuhi persyaratan :
• Harus inert, tidak bereaksi dengan cuplikan, cuplikan-pelarut, dan material dalam kolom.
• Murni dan mudah diperoleh, serta murah. • Sesuai/cocok untuk detektor (McNair, 1933).
Gas-gas yang sering dipakai adalah Helium, Argon, Nitrogen, Karbon Dioksida dan Hidrogen. Gas Helium dan Argon sangat baik, tidak mudah terbakar, tetapi sangat mahal. H2 mudah terbakar, sehingga harus berhati-hati
dalam pemakaiannya. Kadang-kadang digunakan juga CO2 (Madbardo, 2010).
Pemilihan gas pengangkut atau pembawa ditentukan oleh detektor yang digunakan. Tabung gas pembawa dilengkapi dengan pengatur tekanan keluaran dan pengukur tekanan. Sebelum masuk ke kromatografi, ada pengukur
kecepatan aliran gas serta sistem penapis molekuler untuk memisahkan air dan pengotor gas lainnya (Madbardo, 2010).
2. Pengatur aliran dan pengatur tekanan
Pengatur aliran gas pembawa merupakan bagian yang utama dalam efisiensi kolom dan untuk analisis kualitatif. Efisiensi kolom bergantung pada kecepatan gas yang mengalir. Untuk analisis kualitatif, kecepatan aliran gas haruslah konstan dan dapat direproduksi agar waktu retensi dapat dihasilkan kembali. Membandingkan waktu retensi merupakan teknik tercepat dan termudah dalam identifikasi senyawa karena tidak ada senyawa yang bisa mempunyai dua waktu retensi yang berbeda. Oleh karena itu, waktu retensi merupakan karakteristik dari suatu analit (McNair, 1933).
3. Tempat injeksi (The injection port)
Dalam pemisahan dengan kromatografi gas cuplikan harus dalam bentuk fase uap. Gas dan uap dapat dimasukkan secara langsung. Tetapi kebanyakan senyawa organik berbentuk cairan dan padatan. Hingga dengan demikian senyawa yang berbentuk cairan dan padatan pertama-tama harus diuapkan. Ini membutuhkan pemanasan sebelum masuk dalam kolom (Madbardo, 2010).
Tempat injeksi dari alat kromatografi gas selalu dipanaskan. Dalam kebanyakan alat, suhu dari tempat injeksi dapat diatur. Aturan pertama untuk pengaturan suhu ini adalah suhu tempat injeksi sekitar 50 °C lebih tinggi dari titik didih campuran dari cuplikan yang mempunyai titik didih yang paling tinggi. Bila kita tidak mengetahui titik didih komponen dari cuplikan maka kita harus mencoba-coba. Namun demikian suhu tempat injeksi tidak boleh terlalu tinggi, sebab kemungkinan akan terjadi perubahan karena panas atau penguraian dari senyawa yang akan dianalisis (Madbardo, 2010).
Cuplikan dimasukkan ke dalam kolom dengan cara menginjeksikan melalui tempat injeksi. Hal ini dapat dilakukan dengan pertolongan jarum injeksi yang sering disebut "a gas tight syringe" (Madbardo, 2010).
Perlu diperhatikan bahwa kita tidak boleh menginjeksikan cuplikan terlalu banyak, karena kromatografi gas sangat sensitif. Biasanya jumlah cuplikan yang diinjeksikan pada waktu kita mengadakan analisis 0,5-50 ml gas dan 0,2-20 ml untuk cairan (Madbardo, 2010).
4. Kolom
Kolom adalah jantung kromatografi. Pemisahan sesungguhnya komponen cuplikan dicapai dalam kolom. Karena itu, keberhasilan atau kegagalan suatu pemisahan sebagian besar bergantung pada pemilihan kolom. Pada kromatografi gas cair, ada kolom kapiler dan kolom kemas. Kolom kapiler adalah tabung terbuka bergaris tengah sangat kecil yang pada dindingnya terdapat lapisan cairan tipis. Kolom kemas terdiri atas bahan padat lembam yang menyangga lapisan tipis cairan tak atsiri. Tabung dapat berupa kaca, logam, atau plastik, dilingkarkan agar sesuai dalam tanur kromatografi. Penyangga padat, jenis, dan jumlah fase cair, cara mengemas dan panjang serta suhu kolom merupakan faktor penting untuk mencapai daya pisah yang diinginkan. Ukuran kolom menentukan jumlah total gas dan cairan yang dapat terwadahi (Bonelli, 1988).
5. Detektor
Detektor kromatografi merupakan suatu gawang yang menunjukkan dan mengukur banyaknya komponen yang terpisah dalam gas pembawa. Detektor dapat dikelompokkan kedalam golongan detektor yang mengintegrasi atau detektor yang mendifrensiasi. Detektor mengintegrasi memberikan tanggapan
yang berbanding lurus dengan massa total komponen dalam daerah yang dielusi. Jika gas pembawa murni melewati detektor, daftar carik menunjukkan garis lurus. Jika daerah komponen melewati detektor, pena perekam bergerak melintasi gaftar-carik yang jaraknya berbanding lurus dengan massa total komponen dalam daerah. Jika komponen lain dielusi, pena bergerak lebih jauh melintasi gaftar (Bonelli, 1988)
Detektor difrensiasi menghasilkan tanggapan yang berbanding lurus dengan konsentrasi atau laju aliran massa kmponen yang dielusi. Contoh detektor yang memberikan tanggapan terhadap konsentrasi yang paling dikenal ialah detektor hantar bahang (DHB = TCD = Thermal conductivity detector) atau katarometer. Contoh detektor yang memberikan tanggapan terhadap laju aliran massa ialah detektor pengionan nyala (DPN = FID = Flame ionization detector). Kromatogram yang dihasilkan oleh detektor yang mendifrensiasi terdiri atas sederet puncak, masing-masing puncak menyatakan komponen yang berlainan. Luas puncak berbanding lurus dengan massa keeluruhan komponen tersebut (Bonelli, 1988).
6. Pencatat
Pencatat (rekorder) berfungsi sebagai pengubah sinyal dari detektor yang diperkuat melalui elektrometer menjadi bentuk kromatogram. Dari kromatogram yang diperoleh dapat dilakukan analisis kualitatif dan kuantitatif. Analisis kualitatif dengan cara membandingkan waktu retensi sampel dengan standar. Analisis kuantitatif dengan menghitung luas area maupun tinggi dari kromatogram. Sinyal analitik yang dihasilkan detektor dikuatkan oleh rangkaian elektronik agar bisa diolah oleh rekorder atau sistem data. Sebuah
rekorder bekerja dengan menggerakkan kertas dengan kecepatan tertentu. Di atas kertas tersebut dipasangkan pena yang digerakkan oleh sinyal keluaran detektor sehingga posisinya akan berubah-ubah sesuai dengan dinamika keluaran penguat sinyal detektor. Hasil rekorder adalah sebuah kromatogram berbentuk pik-pik dengan pola yang sesuai dengan kondisi sampel dan jenis detektor yang digunakan. Rekorder biasanya dihubungkan dengan sebuah elektrometer yang dihubungkan dengan sirkuit pengintregrasi yang bekerja dengan menghitung jumlah muatan atau jumlah energi listrik yang dihasilkan oleh detektor. Elektrometer akan melengkapi puncak-puncak kromatogram dengan data luas puncak atau tinggi puncak lengkap dengan biasnya (Madbardo, 2010).