KAJIAN AKTIVITAS ANTIBAKTERI PRODUK ETANOLISIS DARI CAMPURAN MINYAK INTI SAWIT (Elaeis quineensis Jacq.) DAN
MINYAK BIJI MENGKUDU (Morinda citrifolia L.)
[Antibacterial Activities of Crude Ethanolysis Product from Mixture of Palm Kernel Oil and Morinda Seeds Oil]
Murhadi1) dan Suharyono AS1)
1)
Staf Pengajar Jurusan Teknologi Industri Pertanian Fakultas Pertanian Universitas Lampung Jl. Prof. Soemantri Brojonegoro No. 1 Bandar Lampung, Lampung 35145
Telp. 0721-781823; e-mail: murhadi_thp@unila.ac.id
ABSTRACT
The objective of this research was to measure antibacterial activities of ethanolysis products that produced through ethanolysis reaction of mixture of palm kernel oil (PKO) and Morinda seeds oil (25:1 and 50:1, w/w) in ethanol solution contained 1% NaOH (v/w based on oil weight) at ratio of 5 : 6 (b/v) and shaken on a shaker (300 rpm, room temp.) for 3, 6, 9 and 12 minutes. Fractionation of ethanolysis products using absolute ethanol (1:3; v/v) and centrifuged at 4.000 rpm for 30 min, yielding Fraction 1 (upper layer) and Fraction 2 (lower layer). Generally, all ethanolysis products showed antibacterial activities against four test bacteria (E. coli, S. aureus, B. cereus and S. enteritidis) at range of d values (mm) from 0,93 (B. cereus; 3 min) up to 3,87 (E. coli; 9 min). Fraction 1 showed the highest antibacterial activity with d values (mm) from 1,20 (B. cereus; 9 min) up to 5,63 (E. coli; 9 min), while Fraction 2 for all treatments had no antibacterial activity, relativelly. Ethanolysis products and its fraction (Fraction 1) were resulted from ethanolysis reaction for 6 and 9 min showed higher antibacterial activities than those for 3 and 12 min.
Keywords: Antibacterial activities, ethanolysis product, Morinda seeds oil, PKO
PENDAHULUAN
Salah satu produk samping industri pengolahan buah sawit menjadi minyak sawit kasar (CPO) adalah minyak inti sawit atau PKO (palm kernel oil) yang banyak digunakan sebagai bahan baku pada berbagai industri pangan dan non pangan.
Minyak inti sawit berwarna kuning,
dihasilkan dari ekstraksi terhadap daging buah biji (inti) sawit. Komposisi asam lemak PKO berbeda dengan CPO, karena asam lemaknya didominasi oleh asam laurat (12:0) dan asam miristat (14:0), masing-masing 45% dan 18% (Gurr, 1992).
Mengkudu dengan nama spesiesnya
Morinda citrifolia L. atau juga dikenal
dengan nama buah “noni”, merupakan salah satu jenis tanaman yang banyak tumbuh di Indonesia terutama tumbuh liar di halaman rumah dan sekitarnya. Sejak sekitar tahun 2000, buah mengkudu telah diketahui
banyak manfaatnya terutama untuk
kesehatan manusia dan telah banyak diusahakan untuk pembudidayaan tanaman mengkudu. Mengkudu termasuk famili
Rubiaceae, tumbuh sedikit membengkok
dengan ketinggian antara 3-8 meter disertai cabang yang banyak serta ranting segi empat. Tanaman ini tumbuh di dataran rendah sampai dataran relatif tinggi dengan ketinggian antara 500-1500 meter dari atas
permukaan laut (Wijayakusuma dan
Sebagai limbah dari pengolahan daging buah mengkudu, di antaranya menjadi produk sari buah mengkudu, serbuk (tepung) mengkudu, selai buah mengkudu, dan untuk keperluan pengobatan dalam bentuk kapsul serta untuk kosmetik, adalah biji buah mengkudu yang belum banyak dimanfaatkan. Biji mengkudu mengandung minyak dengan berbagai komponen asam lemaknya, terutama didominasi oleh asam lemak esensial yaitu asam lemak omega 6 (linoleat; 18:2, n6) yang dapat mencapai 66.8% dan sejumlah kecil asam lemak omega 3 (linolenat; 18:3, n3) serta vitamin E kira-kira 11-25 IU/100 g (John dan Wadsworth, 2002).
Produk etanolisis campuran dari PKO dengan minyak biji mengkudu (MBM) diharapkan cukup potensial sebagai bahan pengawet sekaligus dapat meningkatkan nutrisi asam lemak esensial omega 6 dan 3 pada bahan/produk pangan. Hal ini
terutama diharapkan dari kontribusi
aktivitas antibakteri dari senyawa
monogliserida (MG) terutama dalam bentuk monolaurin (asam laurat; 12:0) yang
bersumber dari PKO dan tingginya
kandungan asam lemak omega 6 (asam linoleat; 18:2) yang berasal dari MBM. Kombinasi tingginya kandungan asam laurat (12:0; sebagai antimikroba) dan asam linoleat (18:2; asam lemak esensial) dalam produk etanolisis tersebut, diharapkan merupakan kombinasi potensial sebagai pengawet pangan pada produk pangan yang bersesuaian.
Hasil penelitian menunjukkan bahwa produk-produk MG dalam bentuk mono-laurin dan monomiristin (asam miristat; 14:0) terbukti mempunyai aktivitas anti bakteri (Gram + dan Gram -), kamir, dan kapang dengan spektrum luas (Wang et al., 1993; Bautista et al., 1993; Oh dan
Marshall, 1994; Cotton dan Marshall, 1997; Mappiratu, 1999; Mappiratu et al., 2003; dan Rangga et al., 2005), bahkan juga terbukti sebagai anti sel-sel tumor dan HIV-1 (Kovacs et al., HIV-1999). Produk-produk MG tersebut umumnya dihasilkan dari suatu reaksi gliserolisis minyak nabati baik dari reaksi secara kimia (katalis kimia) pada
suhu tinggi (> 210oC) ataupun secara
enzimatis baik komersial atau dari sumber alami.
Kelemahan dengan metode-metode tersebut di antaranya adalah: rusaknya sebagian struktur kimia asam lemak akibat suhu tinggi (pirolisis), waktu yang lama, relatif mahal (enzim komersial), dan rendemen yang masih rendah (enzim dari sumber nabati). Salah satu metode produksi MG dan digliserida (DG) yang cukup potensial adalah dengan reaksi etanolisis
minyak nabati pada suhu ruang.
Hasanuddin et al. (2003), melaporkan bahwa produksi MG dan DG dengan reaksi etanolisis terhadap minyak sawit mentah (CPO) selama 6 menit pada suhu ruang
(30oC) dengan nisbah etanol dan CPO
adalah 1 : 1 (v/b) dapat menghasilkan fraksi massa MG sejumlah 9.36% (b/b) dari berat sampel.
Penelitian bertujuan untuk mengukur aktivitas antibakteri produk etanolisis dan fraksinya dari campuran PKO dengan MBM (25:1 dan 50:1; b/b) yang direaksikan dengan larutan etanol teknis 96% yang telah mengandung NaOH 1% (b/b campuran minyak) di atas shaker (300 rpm) selama 3, 6, 9 dan 12 menit. Nisbah larutan etanol-NaOH 1% terhadap campuran PKO dengan MBM yang digunakan adalah 1,2 atau 6 : 5 (v/b).
BAHAN DAN METODE Bahan dan Alat
Bahan utama adalah PKO dan buah mengkudu yang sudah masak/tua. Bahan kimia: heksana p.a., etanol p.a., etanol 96%, NaOH, HCl, sodium sulfat anhidrat, dan akuades. Kultur bakteri: Escherichia coli (ATCC 25922), Staphylococcus aureus (ATCC 25923), Bacillus cereus (ATCC 11778), dan Samonella enteritidis (ATCC 13076). Media: NA (Nutrient Agar) dan NB (Nutrient Broth). Peralatan terdiri dari:
soxhlet, shaker, separating funnel,
timbangan analitik, rotavapor, pompa
vakum, sentrifuge, penangas air, corong Buchner, otoklaf, vial, jangka sorong. dan alat-alat penunjang penelitian untuk uji antibakteri.
Tahapan Penelitian
Tahapan penelitian meliputi tahap persiapan bahan, ekstraksi minyak biji mengkudu, produksi produk etanolisis dan fraksinasi produk etanolisis dari campuran PKO dengan MBM.
Persiapan Bahan
PKO diperoleh dari PTPN VII Bekeri, Lampung Tengah, lalu disaring mengguna-kan kertas saring (Whatman No. 42) dengan bantuan corong Buchner dan pompa vakum sehingga dihasilkan PKO yang bebas dari kotoran. Buah mengkudu dipilih yang sudah tua/masak, lalu dilakukan pemisahan biji mengkudu dengan mencucinya pada air mengalir, pengeringan biji mengkudu dalam
oven 60oC sampai kadar air 8-10%,
penggilingan biji mengkudu kering hingga dihasilkan bubuk (serbuk) biji mengkudu kering yang siap diekstraksi minyaknya dengan pelarut heksana.
Ekstraksi Minyak
Ekstraksi bubuk biji mengkudu kering dilakukan terlebih dahulu dengan ekstraksi maserasi dalam pelarut heksana dengan penggoyangan (shaker; 275 rpm, 24 jam), disaring sehingga dihasilkan Filtrat 1 dan residu bubuk biji mengkudu. Selanjutnya residu tersebut diekstrak lagi dengan heksana pada alat soxhlet (24 jam) sehingga dihasilkan Filtrat 2. Filtrat 1 dan Filtrat 2
dicampur lalu dihilangkan pelarutnya
(heksana) menggunakan rotary evaporator, disaring (Whatman No. 42) sehingga dihasilkan MBM bebas kotoran.
Produksi Produk Etanolisis
Produksi produk etanolisis dilakukan dengan dua perlakuan, yaitu: (1) Komposisi campuran PKO dengan MBM, terdiri dari 2 taraf, 25:1 dan 50:1 (b/b); dan (2) Waktu reaksi etanolisis terdiri dari 4 taraf, 3, 6, 9 dan 12 menit. Reaksi etanolisis dilakukan dengan penambahan etanol 96% yang telah mengandung NaOH 1% (b/b campuran minyak) dengan nisbah terhadap campuran PKO dengan MBM adalah 1,2 (v/b) atau 6 : 5 (v/b). Penelitian ini dilakukan secara deskriptif (3 kali ulangan) dan data yang
diperoleh disajikan dalam bentuk
histogram/grafik, lalu dianalisis secara deskriptif.
Prosedur percobaan mengikuti
prosedur yang telah dikembangkan oleh Hasanuddin et al. (2003) dengan modifikasi. Sejumlah (mL) etanol 96% yang telah mengandung NaOH 1% ditambah sejumlah (g) campuran PKO dengan MBM (sesuai
perlakuan) dengan nisbah 1,2 (v/b),
direaksikan di dalam Erlenmayer 250 mL (tertutup), lalu digoyang di atas shaker (kecepatan 300 rpm) selama 3, 6, 9 atau 12 menit (sesuai perlakuan) pada suhu ruang
(28 ± 1oC) dengan volume reaksi kurang
labu pemisah, dicuci dengan akuades hingga lapisan bawah relatif jernih. Lapisan atas
(produk etanolisis) dibebaskan dari
kandungan airnya dengan menambahkan
Na2SO4 anhidrat, lalu disaring. Terhadap
masing-masing produk etanolisis tersebut, dihitung rendemen dan diuji aktivitas antibakterinya.
F
FrraakkssiinnaassiiPPrroodduukkEEttaannoolliissiiss
Fraksinasi produk etanolisis
menggunakan metode pemusingan
(sentrifuge; Mappiratu, 1999; Rangga et al., 2005) dalam pelarut etanol p.a dengan perbandingan produk etanolisis dan pelarut = 1 : 3 (v/v). Sebelum pemusingan, produk
etanolisis didinginkan dalam lemari
pendingin (2-4oC) selama 1 jam.
Pemusingan berlangsung selama 30 menit pada kecepatan putar 4.000 rpm sehingga menghasilkan dua fraksi terpisah (Fraksi 1 dan Fraksi 2). Terhadap masing-masing fraksi, diuji aktivitas antibakterinya. Pengujian Aktivitas Antibakteri
Pengujian aktivitas antibakteri
dilakukan terhadap produk etanolisis dan fraksinya menggunakan metode difusi agar/sumur (Gariga et al., 1983; Murhadi, 2002; Rangga et al., 2005). Pengujian aktivitas antibakteri produk etanolisis PKO-MBM dan fraksinya dilakukan terhadap enam jenis sampel, yaitu: (1) Sampel A =
produk etanolisis PKO-MBM tanpa
pengenceran; (2) Sampel B = produk etanolisis PKO-MBM dengan pengenceran menggunakan etanol (1:3, v/v); (3)Sampel C = Fraksi 1 yaitu lapisan atas; (4) Sampel D = pengenceran Fraksi 1 dengan etanol (1:3, v/v); (5) Sampel E = Fraksi 2 yaitu lapisan bawah; dan (6) Sampel F = pengenceran Fraksi 2 dengan etanol (1:3, v/v).
Masing-masing kultur bakteri murni disegarkan di dalam medium NB steril
selama 24 jam pada 37oC, dihomogenkan
(vorteks), diinokulasikan sebanyak 20 µL ke
dalam Erlenmeyer yang berisi 20 mL
medium agar cair (NA, 44-45oC) steril,
dikocok merata, kemudian dituang ke dalam cawan petri (100 x 15 mm) steril dan dibiarkan sampai membeku. Selanjutnya dibuat 5 lubang (sumur) secara aseptis dengan diameter sumur 6.0 mm (seragam). Ke dalam tiap lubang, diinokulasi dengan
60 µL produk etanolisis atau fraksinya
(dengan dan tanpa pengenceran). Sebagai
kontrol, diinokulasi sebanyak 60 µL etanol
96%. Zona penghambatan yang diukur adalah radius (r, mm) penghambatan berupa areal bening di sekeliling sumur uji, setelah
diinkubasi selama 24 jam pada 37oC.
Pengukuran jari-jari (r, mm) zona hambat di sekeliling sumur uji dilakukan dengan cara mengukur jarak dari tepi sumur uji ke batas lingkaran zona hambat menggunakan jangka sorong (ketelitian 0.01 mm) pada beberapa
sisi sumur uji, lalu dirata-ratakan.
Selanjutnya nilai d (mm) dapat dihitung dengan rumus: 2 x r.
HASIL DAN PEMBAHASAN Warna PKO yang telah disaring adalah kuning cerah, relatif sama dengan warna MBM hasil ekstraksi dari biji mengkudu. Berat jenis PKO dengan MBM juga relatif sama, masing-masing adalah 0,9198 dan 0,9177, sehingga mudah dicampurkan.
Rendemen Produk Etanolisis
Histogram rendemen produk
etanolisis kasar dari reaksi etanolisis campuran PKO dengan MBM,
masing-masing untuk perlakuan dengan
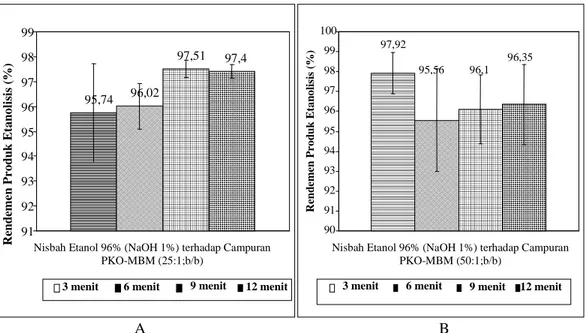
perbandingan 25:1 (b/b) dan 50:1 (b/b) serta perbedaan waktu etanolisis selama 3, 6, 9 dan 12 menit, disajikan pada Gambar 1.
A B
Gambar 1. Histogram rendemen produk etanolisis campuran dan minyak biji mengkudu dengan perbandingan 1:25 (b/b; A) dan 1:50 (b/b; B)
Pola rendemen produk etanolisis kasar pada perlakuan PKO : MBM baik untuk perbandingan 25:1 (b/b) maupun 50:1 (b/b) relatif sama dengan semakin lama waktu reaksi etanolisis pada selang waktu 3 sampai 12 menit, yaitu dengan rendemen berkisar antara 95,56 – 97,92%.
Aktivitas Antibakteri
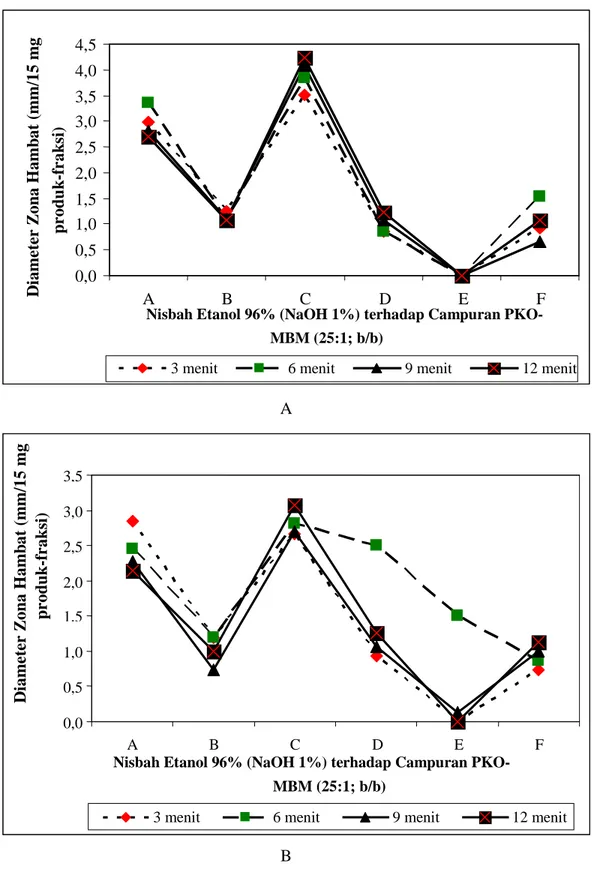
Grafik aktivitas antibakteri produk etanolisis kasar dari campuran PKO dengan MBM serta fraksinya terhadap E. coli, S.
aureus, B. cereus dan S. enteritidis dengan
perlakuan lama reaksi etanolisis (3, 6, 9, dan 12 menit), masing-masing dapat dilihat pada Gambar 2, 3, 4, dan Gambar 5.
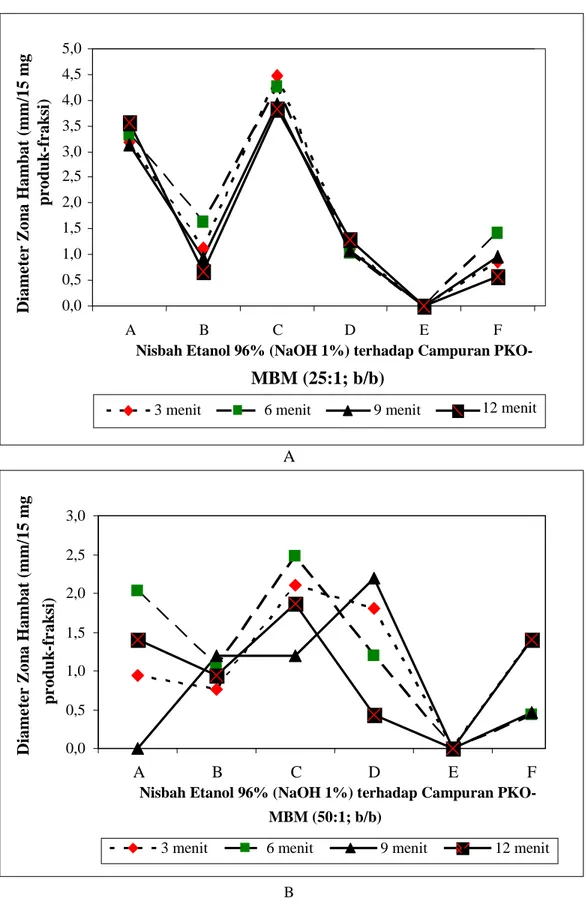
Produk etanolisis kasar dari campuran PKO dengan MBM memiliki aktivitas antibakteri terhadap empat bakteri penguji dengan kisaran nilai diameter (mm) zona penghambatan antara 2,27 (B. cereus; 9 menit) hingga 3,87 (E. coli; 9 menit) untuk campuran PKO dengan MBM = 25: 1 (b/b), sedangkan untuk perbandingan 50 : 1 (b/b)
adalah 0,93 (B. cereus; 3 menit) sampai 3,12 (S. aureus; 6 menit).
Fraksinasi dengan cara sentrifusi 4000 rpm 30 menit terhadap produk etanolisis kasar dari campuran PKO dengan MBM menghasilkan 2 fraksi, yaitu Fraksi 1 sebagai lapisan atas (Sampel C) dan Fraksi 2 sebagai lapisan bawah/endapan (Sampel E). Aktivitas antibakteri Fraksi 1 lebih
tinggi dibandingkan dengan produk
etanolisis kasarnya dengan kisaran nilai diameter (mm) penghambatan antara 2,91 (B. cereus; 12 menit) hingga 5,63 (E. coli; 9 menit) untuk campuran PKO dengan MBM = 25 : 1 (b/b), sedangkan untuk perbanding-an 50 : 1 (b/b) adalah 1,20 (B. cereus; 9 menit) sampai 3,75 (S. aureus; 12 menit). Sementara Fraksi 2 relatif tidak memiliki aktivitas antibakteri untuk semua perlakuan. Pengenceran terhadap produk etanolisis
kasar atau fraksinya, masing-masing
menggunakan etanol (1:3, b/v), rata-rata menurunkan daya aktivitas antibakterinya. 95,74 96,02 97,51 97,4 91 92 93 94 95 96 97 98 99
Nisbah Etanol 96% (NaOH 1%) terhadap Campuran PKO-MBM (25:1;b/b) R en d em e n P r o d u k E ta n o li si s (% )
3 menit 6 menit 9 menit 12 menit
97,92 95,56 96,1 96,35 90 91 92 93 94 95 96 97 98 99 100
Nisbah Etanol 96% (NaOH 1%) terhadap Campuran PKO-MBM (50:1;b/b)
3 menit 6 menit 9 menit 12 menit
R en d em en P ro d u k E ta n o li si s (% )
A
B
Gambar 2. Grafik diameter zona hambat produk etanolisis PKO-MBM (A = 25:1; B = 50:1) dan fraksinya terhadap E. coli
0,0 1,0 2,0 3,0 4,0 5,0 6,0 A B C D E F
Nisbah Etanol 96% (NaOH 1%) terhadap Campuran PKO- MBM (25:1; b/b) D ia m e te r Z o n a H a m b a t (m m /1 5 m g p ro d u k -f r a k si )
3 menit 6 menit 9 menit 12 menit
0,0
0,5
1,0
1,5
2,0
2,5
3,0
3,5
A B C D E FNisbah Etanol 96% (NaOH 1%) terhadap Campuran PKO- MBM (50:1; b/b) D ia m et er Z o n a H a m b a t (m m /1 5 m g p r o d u k -f ra k si )
A
B
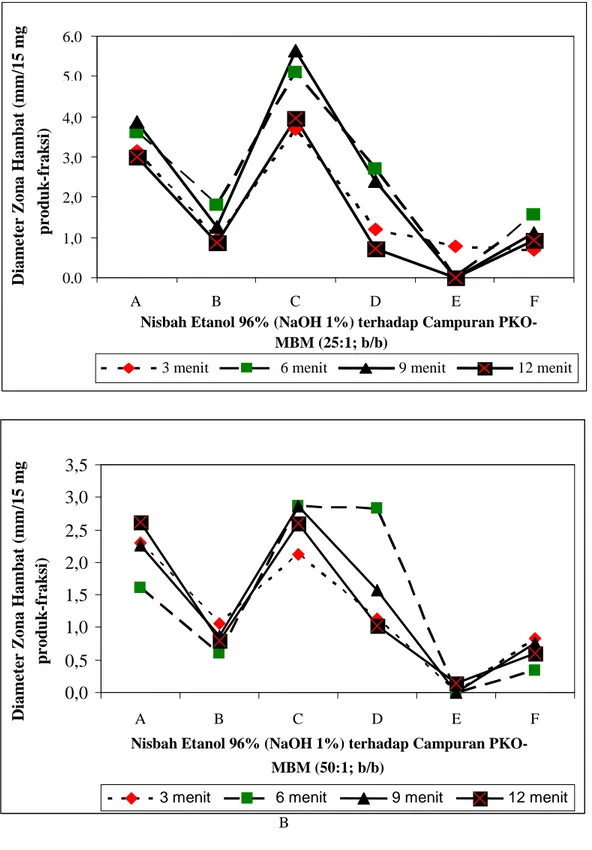
Gambar 3. Grafik dimaeter zona hambat produk etanolisis PKO-MBM (A = 25:1; B = 50:1) dan fraksinya terhadap S. aureus
0,0 1,0 2,0 3,0 4,0 5,0 6,0 A B C D E F
Nisbah Etanol 96% (NaOH 1%) terhadap Campuran PKO-MBM (25:1; b/b) D ia m et er Z o n a H a m b a t (m m /1 5 m g p ro d u k -f r a k si )
3 menit 6 menit 9 menit 12 menit
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 A B C D E F
Nisbah Etanol 96% (NaOH 1%) terhadap Campuran PKO- MBM (50:1; b/b) D ia m et er Z o n a H a m b a t (m m /1 5 m g p ro d u k -f r a k si )
A
B
Gambar 4. Grafik dimaeter zona hambat produk etanolisis PKO-MBM (A = 25:1; B = 50:1) dan fraksinya terhadap B. cereus
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 4,5 5,0 A B C D E F
Nisbah Etanol 96% (NaOH 1%) terhadap Campuran
PKO-MBM (25:1; b/b)
D ia m et er Z o n a H a m b a t (m m /1 5 m g p ro d u k -f r a k si )3 menit 6 menit 9 menit 12 menit
0,0 0,5 1,0 1,5 2,0 2,5 3,0 A B C D E F
Nisbah Etanol 96% (NaOH 1%) terhadap Campuran PKO-MBM (50:1; b/b) D ia m e te r Z o n a H a m b a t (m m /1 5 m g p ro d u k -f r a k si )
A
B
Gambar 5. Grafik dimaeter zona hambat produk etanolisis PKO-MBM (A = 25:1; B = 50:1) dan fraksinya terhadap S. enteritidis
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 4,5 A B C D E F MBM (25:1; b/b) D ia m et er Z o n a H a m b a t (m m /1 5 m g p ro d u k -f r a k si )
3 menit 6 menit 9 menit 12 menit
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 A B C D E F
Nisbah Etanol 96% (NaOH 1%) terhadap Campuran PKO- MBM (25:1; b/b) D ia m et er Z o n a H a m b a t (m m /1 5 m g p ro d u k -f ra k si )
3 menit 6 menit 9 menit 12 menit
Fraksi 1 diduga merupakan campuran monogliserida (MG) dan digliserida (DG) dari proses etanolisis campuran PKO dengan MBM yang memiliki aktivitas antibakteri dan bersifat semipolar menuju polar, sehingga sangat larut dalam etanol. Diketahui bahwa etanol bersifat polar
dengan karakteristik nilai ∈ = 0,68 (Moyler
dalam Ashurst; 1995) dan konstanta
dielektrik (25oC) = 24,30 (Pomerans dan
Meloan, 1994) yang dapat melarutkan substansi polar (Houghton dan Raman, 1998) termasuk MG dan DG. Ester asam lemak dengan gliserol dalam bentuk MG dengan komposisi asam lemaknya adalah asam laurat (12:0) misalnya yang berasal dari minyak kelapa (Wang et al., 1993; Mappiratu, 1999; Mappiratu et al., 2003) atau dari PKO (Rangga et al., 2005) telah terbukti memiliki aktivitas antimikroba dengan spektrum luas.
Fraksi 2 merupakan lapisan bawah (kurang larut dalam etanol/mengendap) dari hasil fraksinasi produk etanolisis campuran PKO dengan MBM relatif tidak memiliki
aktivitas antibakteri, yang diduga
merupakan sisa trigliserida (TG) dari proses etanolisis tersebut. Hal ini mengindikasikan
bahwa produk etanolisis kasar dari
campuran PKO dengan MBM masih merupakan gabungan antara MG, DG dan sisa TG dari campuran PKO dengan MBM. Sehubungan dengan aktivitas antimikroba asam-asam lemak dari sumber minyak atau lemak tanaman, diketahui bahwa lemak (dalam bentuk TG) tidak memiliki efek penghambatan terhadap mikroba, kecuali
yang mengandung asam-asam lemak
berantai karbon rendah-sedang khususnya dalam bentuk MG atau asam lemak bebas (Kabara dalam Branen dan Davidson, 1983).
Aktivitas antibakteri produk etanolisis campuran PKO dengan MBM (25:1 dan 50:1, b/b) dan fraksi-fraksinya tertinggi adalah pada perlakuan reaksi etanolisis selama 6 dan 9 menit untuk Fraksi 1, khususnya terhadap bakteri uji E. coli dan
B. cereus (Gambar 3 dan 5), sedangkan
terhadap bakteri S. aureus dan S. enteritidis untuk reaksi etanolisis selama 12 menit, juga untuk Fraksi 1 (Gambar 4 dan 6). Reaksi etanolisis terhadap minyak sawit kasar (CPO) pada selang waktu reaksi 5 sampai 8 menit lebih optimal menghasilkan MG dan etil ester ketiga, lebih tinggi dari pada etanolisis CPO untuk menghasilkan DG dan etil ester pertama (Hasanuddin et
al., 2003).
KESIMPULAN
Produk etanolisis kasar dari campuran PKO dengan MBM memiliki aktivitas antibakteri terhadap empat bakteri penguji (E. coli, S. aureus, B. cereus dan S.
enteritidis) dengan kisaran nilai diameter
(mm) zona penghambatan antara 2,27 (B.
cereus; 9 menit) sampai 3,87 (E. coli; 9
menit) untuk campuran PKO dengan MBM
= 25: 1 (b/b), sedangkan untuk
perbandingan 50 : 1 (b/b) adalah 0,93 (B.
cereus; 3 menit) sampai 3,12 (S. aureus; 6
menit).
Aktivitas antibakteri Fraksi 1 lebih
tinggi dibandingkan dengan aktivitas
antibakteri produk etanolisis kasarnya, dengan kisaran nilai diameter (mm) zona penghambatan Fraksi 1 antara 2,91 (B.
cereus; 12 menit) hingga 5,63 (E. coli; 9
menit) untuk campuran PKO dengan MBM = 25 : 1 (b/b), sedangkan untuk perbandingan 50 : 1 (b/b) adalah 1,20 (B.
cereus; 9 menit) sampai 3,75 (S. aureus; 12
memiliki aktivitas antibakteri untuk semua perlakuan.
Secara keseluruhan, diameter zona penghambatan baik pada produk etanolisis kasar dari campuran PKO dengan MBM maupun pada fraksi-fraksinya terhadap 4 bakteri penguji (E. coli, S. aureus, B. cereus dan S. enteritidis) relatif masih rendah, yaitu di bawah 6,00 mm. Untuk itu masih perlu
dilakukan penelitian lanjutan untuk
memodifikasi proses etanolisis campuran PKO dengan MBM dan mengoptimalkan proses fraksinasinya.
UCAPAN TERIMA KASIH Peneliti mengucapkan terima kasih
kepada Direktorat Penelitian dan
Pengabdian kepada Masyarakat (DP2M), Direktorat Jenderal Pendidikan Tinggi Departemen Pendidikan Nasional Republik Indonesia, yang telah membiayai penelitian ini yaitu pada Program Penelitian Hibah Bersaing Tahun Anggaran 2007 berdasarkan Surat Perjanjian Kontrak antara Lembaga Penelitian Unila dengan Direktorat Jenderal Pendidikan Tinggi Nomor: 028/SP2H/PP/ DP2M/ III/2007 tanggal 29 Maret 2007.
D
DAAFFTTAARRPPUUSSTTAAKKAA Bautista, D. A., A. R. Hill, and M.W.
Griffiths. 1993. An all natural approach to preserve cottage cheese. Modern Dairy. 72(1):12-13.
Cotton, L.N. and D.L. Marshall. 1997. Monolaurin preparation methods effects activity against vegetative cell of Bacillus cereus. J. Food Sci. Technol. 30(8):830-832.
Gariga, M., M. Hugas, T. Aymerich, and J.M. Monfort. 1983. Bacteriogenic
activity of lactobacilli from fermented sausage. App. Bacteriol. 75:142-148.
Gurr, M.I. 1992. Role of Fats in Food and Nutrition. Elsevier Appl. Sci. New York.
Hasanuddin, A., Mappiratu, dan G.S. Hutomo. 2003. Pola Perubahan Mono dan Diasilgliserol dalam Reaksi Etanolisis Minyak Sawit Mentah. J. Teknol. dan Industri Pangan. XIV(3): 241-246.
Houghton, P.J. and A. Raman. 1998. Laboratory Handbook for The Fractionation of Natural Extracts. Chapman & Hall. London. John, J. and Wadsworth. 2002. Morinda
Citrifolia Oil. United States Patent. Di
dalam http://www.Patft.Uspto.Gov/
Netacgi/Nph-Parser. Diakses Tanggal 10 Juni 2008.
Kabara, J.J. Medium-chain fatty acids and esters. In Branen, A. L. and P.M. Davidson. 1983. Antimicrobials in Foods. Marcel Dekker, Inc. New york.
Kovacs, A., M. Schluchter, and K. Easley. 1999. Cytomegalovirus infection and HIV-1 disease progressionin infant born to HIV-1-infected women. New England J.Medicine. 341: 77-84. Mappiratu. 1999. Penggunaan Biokatalis
Dedak Padi dalam Biosintesis Antimikroba Monoasilgliserol dari Minyak Kelapa. Disertasi S3. PPs IPB. Bogor.
Mappiratu, D. Fardiaz, dan A. Hasanuddin. 2003. Produksi dan Aplikasi Produk Monoasilgliserol dari Minyak Kelapa dalam Pengolahan Santan Awet. J.
Teknologi & Industri Pangan. XIV(3): 233-240.
Moyler, D.A. Oleoresins, tinctures, and extracts. In Ashurst, P.R. (Ed.). 1995. Food Flavorings. Blackie Academic & Profesional. New York. Murhadi. 2002. Isolasi dan Karakterisasi
Komponen Antibakteri dari Biji Atung (Parinarium glaberrimum Hassk). Disertasi. Program Pascasarjana IPB. Bogor. Oh, D.H. and D.L. Marshall. 1994.
Enhanced inhibition of Listeria
monocytogenes by glycerol
monolaurat with organic acids. J. Food Sci. 59(6): 1258-1261. Rangga, A., Murhadi, F. Nuraeni, dan
Pitutur. 2005. Produksi dan Kajian Aktivitas Antibakteri Produk Gliserolisis dari Minyak Inti Sawit (PKO). Bahan Seminar Nasional Research and Studies TPSDP Dikti Depdiknas. Yogyakarta, Mei 2005. Wang, L.L., B.K. Yang, K.L. Parkin, and
E.A. Johnson. 1993. Inhibition of
Listeria monocytogenes by
monoacylglyceros synthesized from coconut oil and milk fat by lipase-catalyzed glycerolysis. J. Agric. Food Chem. 41: 1000-1005.