i
EFEK KOMBINASI EKSTRAK METANOL-AIR DAUN Macaranga tanarius L. DENGAN GLIBENKLAMID TERHADAP PENURUNAN GLUKOSA DARAH PADA TIKUS PUTIH JANTAN GALUR WISTAR
TERBEBANI GLUKOSA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
Oleh
Stephanie Irena Nugrahesti
NIM : 088114107
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Jalan yang mulus dan lurus tidak akan pernah menghasilkan pengemudi yang hebat.
Laut yang tenang tidak akan menghasilkan pelaut yang tangguh. Langit yang cerah tidak akan menghasilkan pilot yang handal.
Hidup yang tidak ada masalah, tidak akan membuat orang menjadi kuat
Aku berkata kepadamu apa saja yang kamu minta dan doakan percayalah
bahwa kamu telah menerimanya, maka hal itu akan diberikan kepadamu
( Markus 11:24)
Kupersembahkan karyaku ini untuk……. Bapa ku di surga Tuhan Yesus Kristus dan Bunda Maria
yang selalu menjaga dan memberikan kekuatan kepadaku
Untuk Papa, Mamaku dan Cicikku Vina yang telah memberikan dukungan dan doa
vii PRAKATA
Puji syukur kepada Tuhan Yang Maha Kasih atas berkatnya yang
melimpah, sehingga penulis dapat menyelesaikan skripsi berjudul “Efek
Kombinasi Ekstrak Metanol-Air Daun Macaranga tanarius L. dengan
Glibenklamid terhadap Penurunan Glukosa Darah Pada Tikus Putih Jantan Galur
Wistar Terbebani Glukosa” dengan baik.
Skripsi ini dibuat untuk memenuhi salah satu syarat memperoleh gelar
Sarjana Farmasi (S.Farm.) program studi Farmasi Universitas Sanata Dharma.
Penulis menyadari sepenuhnya bahwa dalam pelaksanaan dan penyusunan skripsi,
tidak terlepas dari bantuan dan campur tangan dari berbagai pihak. Oleh karena
itu, pada kesempatan ini penulis mengucapkan terima kasih kepada :
1. Tuhan Yang Maha Kasih atas berkat, rahmat dan penyertaan-Nya selama
ini.
2. Bapak Ipang Djunarko, M.Sc., Apt. sebagai Dekan Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta.
3. Ibu Phebe Hendra, M.Si., Ph.D. Apt. sebagai Dosen Pembimbing Utama
skripsi ini atas segala kesabarannya telah memberikan bimbingan,
pengarahan, tuntunan, dukungan dan motivasi selama penelitian dan
penyusunan skripsi.
4. Bapak Prof. Dr. C.J. Soegihardjo, Apt. sebagai Dosen Penguji skripsi atas
bantuan masukkan dan saran serta perhatian kepada penulis demi
viii
5. Ibu dr. Fenty, M.Kes, Sp.PK. sebagai Dosen Penguji skripsi bantuan
masukkan dan saran serta perhatian kepada penulis demi kemajuan skripsi
ini.
6. Ibu Rini Dwiastuti, M.Si., Apt selaku Pimpinan Laboratorium Farmasi
yang telah memberikan ijin penggunaan semua fasilitas laboratorium guna
penelitian skripsi ini.
7. Bapak Yohanes Dwiatmaka, M.Si., yang telah membimbing dalam
determinasi tanaman Macaranga tanarius L.
8. Bapak Heru, Bapak Parjiman, Bapak Kayat, Drh. Ari N, Mas Yuwono,
Mas Yohanes R dan Pak Timbul yang telah banyak membantu
menyediakan fasilitas yang dibutuhkan untuk melakukan penelitian ini.
9. Teman-teman “Tim Macaranga 2” Martina Tri Handayani, Triana Oktavia,
Rio Bagus Permadi, Ivan Pradipta, Ana Puspita Dewi, Viviane Theresia,
atas kerja sama, bantuan, suka duka, dan perjuangan dalam menyelesaikan
penelitian ini sampai akhir.
10.Teman-teman “Tim Macaranga 1” Elisa Eka Andrianto, Aryanti Prima
Andini, Ari Widya Nugraha, Andreas Arry Mahendra, Aloysia Yossy
Kurniawaty, dan Dina Wulandari atas kerja sama, dan telah banyak
memberikan informasi dan masukan dalam menyelesaikan penelitian ini
sampai akhir.
11.Seluruh warga FKK angkatan 2008 kelas B dan semua teman farmasi USD
atas kebersamaannya selama kuliah S1 di Fakultas Farmasi Universitas
x INTISARI
Tujuan penelitian ini adalah untuk mengetahui bahwa kombinasi ekstrak metanol-air daun M. tanarius (EMMT) dan glibenklmida mempunyai aktivitas penurunan glukosa darah pada tikus terbebani glukosa. Penelitian ini bersifat eksperimantal murni dengan rancangan acak lengkap pola searah. Penelitian ini menggunakan tikus jantan galur Wistar, umur 2-3 bulan. Tiga puluh lima ekor tikus dibagi secara acak dalam tujuh kelompok perlakuan. Kelompok I (kontrol negatif) diberi CMC 1%. Kelompok II (kontrol positif) diberikan Glibenklamid 0,45 mg/kg BB. Kelompok III diberikan kontrol EMMT dosis 0,43 g/kg BB. Kelompok IV diberikan glibenklamid 0,45 mg/kg BB dan EMMT 0,43g/kg BB; kelompok V diberikan glibenklamid 0,23 mg/kg BB dan EMMT 0,43g/kg BB; kelompok VI diberikan glibenklamid 0,45 mg/kg BB dan EMMT 0,22g/kg BB; kelompok VII diberikan glibenklamid 0,23 mg/kg BB dan EMMT 0,22g/kg BB.
Semua pemberian dilakukan secara per-oral. Efek hipoglikemik dari kombinasi diuji menggunakan metode uji toleransi glukosa oral (UTGO). Kadar glukosa darah ditetapkan pada menit ke-0 sebelum UTGO dan menit ke-15, 30, 45, 60, 90, 180 dan 240 setelah UTGO dari hewan uji yang sebelumnya telah mendapatkan pra-perlakuan kontrol negatif, positif, EMMT dan kombinasi EMMT dengan glibenklamid. LDDK 0-240 diuji dengan one way ANOVA dan dilanjutkan dengan uji Scheffe bertaraf kepercayaan 95%.
Kombinasi EMMT dan Glibenklamida memberikan efek penurunan kadar glukosa darah tikus terbebani glukosa.
xi ABSTRCT
The purpose of this research was to find out that the combination of
M.tanarius L. leaf methanol-water extract (MTME) and glibenklmida has effect to decrease blood glucose levels on burdened glucose rats. The research was pure experimental with direct sampling design. The research used Wistar male rats, age 2-3 months.Thirty five rats can be divided into seven treatment groups. First group (negative control) given CMC 1%. Second group (positive control) given glibenclamide 0.45 mg/kg BW. Third group given MEMT 0.43 g/kg BW. Fourth group given glibenclamide 0.45 mg/kg BW and MTME 0.43g/kg BW; fifth group given glibenclamide 0.23 mg/kg BW and MTME 0.43g/kg BW; sixth group given glibenclamide 0.45 mg/kg BW and MTME 0.22g/kg BW; seventh group given glibenclamide 0.23 mg/kg BW and MTME 0.22g/kg BW.
All of the processes were given through the oral method. The hypoglycemic effect of combination was tested by following the Oral Glucose Tolerance Test (OGTT) method. The blood-glucose contents were taken, at the 0 minutes before the OGTT and also taken at minutes of 15, 30, 45, 60, 90, 180 and 240 after the OGTT, from the tested animal that had been gotten the pre-treatment of the negative control, positive, MTME control and combination of MTME with glibenclmide. The AUC 0-240 was statistically analyzed using the one way ANOVA test and then continued by using Scheffe test with 95 % level of confidence.
The combination of MTME and Glibenklamida giving effect to decresase blood glucose levels on burdened glucose rats.
xii
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ... vi
PRAKATA ... vii
DAFTAR SINGKATAN, ARTI LAMBANG DAN ISTILAH ... xviii
xiii
5. Diagnosis penyakit ... 8
6. Terapi farmakologi ... 10
B. Transport Glukosa ... 11
C. Glibenklamida ... 14
D. Penghambat Enzim -glukosidase ... 16
E. Interaksi Antar Obat ... 17
F. Tanaman Macaranga tanarius L. ... 19
1. Keterangan botani... 19
2. Morfologi ... 20
3. Kandungan kimia ... 20
4. Khasiat ... 22
5. Ekologi penyebaran dan budaya ... 23
G. Metode Penyarian... 23
H. Teknik Uji Diabetik dan Metode Penetapan Kadar Glukosa Darah ... 24
1. Teknik uji diabetik ... 24
2. Metode penetapan kadar glukosa darah ... 26
I. Landasan Teori ... 28
J. Hipotesis ... 28
BAB III METODOLOGI PENELITIAN ... 29
A. Jenis dan Rancangan Penelitian ... 29
B. Variabel dan Definisi Operasional ... 29
1. Variabel ... 29
2. Definisi operasional ... 30
C. Bahan Penelitian ... 31
D. Alat dan Instrumen Penelitian ... 32
E. Tata Cara Penelitian ... 33
1. Determinasi tanaman M. tanarius ... 33
2. Pengumpulan bahan... 33
3. Pembuatan serbuk... 33
xiv
5. Penetapan konsentrasi pekat ekstrak ... 34
6. Penetapan dosis efektif ekstrak daun M. tanarius ... 34
7. Preparasi bahan ... 34
8. Percobaan pendahuluan ... 36
9. Pengelompokan dan perlakuan hewan uji ... 38
10. Penetapan kadar glukosa darah ... 39
F. Tata Cara Analisis Data ... 40
BAB IV HASIL DAN PEMBAHASAN... 41
A. Determinasi Tanaman... 41
B. Hasil Maserasi Daun M. tanarius L. ... 41
C. Percobaan pendahuluan ... 43
1. Penetapan waktu pemberian larutan glibenklamid ... 43
2. Penetapan waktu pemberian larutan ekstrak metanol-air M. tanarius 45 D. Efek kombinasi Ekstrak Metanol-Air M. tanarius dan Glibenklamida ... 47
BAB V KESIMPULAN DAN SARAN ... 58
A. Kesimpulan ... 58
B. Saran ... 58
DAFTAR PUSTAKA ... 59
LAMPIRAN ... 62
xv
DAFTAR TABEL
Tabel I. Nilai Normal Kadar Gula Darah ... 9
Tabel II. Isi pereaksi enzim Glucose GOD-PAP ... 31
Tabel III. Keseragaman bobot tablet ... 35
Tabel IV. Volume pengukuran kadar glukosa darah ... 39
Tabel V. Nilai LDDK0-240 larutan glibenklamida sebelum UTGO ... 44
Tabel VI. Hasil uji Scheffe LDDK0-240 glukosa darah tikus putih jantan terbebani glukosa pada waktu pemberian 15, 30, 45 menit sebelum UTGO ... 45
Tabel VII. LDDK0-240 ekstrak metanol-air M. tanarius ... 45
Tabel VIII. Rerata kadar glukosa darah rata-rata dan LDDK 0-240 setiap kelompok perlakuan ... 48
Tabel IX. Hasil uji Scheffe LDDK0-240 glukosa darah tikus putih jantan terbebani glukosa ... 53
xvi
DAFTAR GAMBAR
Gambar 1. Sekresi insulin akibat peningkatan glukosa dalam darah ... 12
Gambar 2. Insulin memperantarai transport glukosa ke dalam sel... 13
Gambar 3. Struktur glibenklamida ... 14
Gambar 4. Penggolongan antaraksi obat berdasarkan perubahan efek... 18
Gambar 5. Struktur kandungan senyawa daun M.tanarius ... 21
Gambar 6. Ellagitannins diisolasi dari daun M.tanarius asam mailotinik(1), corilagin(2), macatannins A (3), asam chebulagic (4) dan macatannins B(5) ... 22
Gambar 7. Struktur aloksan ... 25
Gambar 8. Struktur streptozotosin ... 26
Gambar 9. Diagram penentuan selang waktu pemberian glibenklamida terhadap % selisih LDDK ... 44
Gambar 10. Diagram penentuan selang waktu pemberian ekstrak metanol-air M. tanarius terhadap LDDK... 46
Gambar 11. Reaksi enzimatik antara glukosa dan reagen GOD-PAP ... 47
Gambar 12. Kurva hubungan antara waktu sampling dan kadar rata-rata glukosa darah akibat pemberian CMC, glibenklamida, dan ekstrak metanol-air M.tanarius ... 49
Gambar 13. Hasil analisis normalitas variansi menggunakan uji Kolmogorov Smirnov ... 52
Gambar 14. Test mean LDDK0 240 ketujuh kelompok perlakuan dengan uji Anova one way... 52
xvii
DAFTAR LAMPIRAN
Lampiran 1. Determinasi daun M.tanarius ... 62
Lampiran 2. Tanaman M. tanarius ... 63
Lampiran 3. Foto ekstrak metanol air M. tanarius ... 63
Lampiran 4. Foto hewan uji ( tikus putih jantan galur Wistar) ... 63
Lampiran 5. Alat penelitian ... 64
Lampiran 6. Preparasi bahan ... 66
Lampiran 7. Perhitungan volume pemberian ... 68
Lampiran 8. Uji normalitas orientasi waktu pemberian glibenklamid ... 69
Lampiran 9. Uji scheffe orientasi waktu pemberian glibenklamid ... 69
Lampran 10. Uji normalitas waktu pemberianEMMT ... 70
Lampiran 11. Uji normalitas Kolmogorov- Smirnov ... 70
Lampiran 12. Uji one way Anova dan uji deskripsi ... 71
Lampiran 13. Uji scheffe kelompok kontrol negatif, positif dan kombinasi ... 72
Lampiran 14. Rendemen ekstrak ... 73
xviii
DAFTAR SINGKATAN, ARTI LAMBANG, DAN ISTILAH
CMC : Carboxy Methyl Cellulosa
GOD–PAP : Glucose Oxydase - Phenol Antipirin
Hipoglikemi(k): penurunan kadar glukosa dalam darah secara abnormal
LDDK : Luas Daerah di Bawah Kurva, kadar glukosa dalam darah vs
waktu
LDDK0-240 : Luas Daerah di Bawah Kurva dari menit 0 sampai menit
ke-240
1 BAB I PENGANTAR
A.Latar Belakang
Dewasa ini semakin banyak masyarakat yang menderita penyakit
degeneratif. Penyakit degeneratif merupakan penyakit yang tidak menular akan
tetapi struktur dari jaringan atau organ akan mengalami penurunan fungsinya dari
waktu ke waktu (Subroto, 2006). Diabetes merupakan contoh dari penyakit
degeneratif. Indonesia adalah negara yang menduduki peringkat empat teratas
pada 2010 yang penduduknya mengidap diabetes. Menurut “Diabetes Health
Center” pada tahun 2030 kemungkinan pengidap diabetes akan bertambah dua
kali lipatnya atau seratus persen. Pada tahun 2010 ada sekitar 8,4 juta jiwa
penderita diabetes dan kemungkinan di tahun 2030 bisa mencapai 21,3 juta jiwa
(Setiwan, 2010). Diabetes mellitus merupakan gangguan metabolisme pada karbohidrat, protein dan lemak yang ditunjukan dengan hiperglikemia (kadar gula
dalam darah tinggi), hal ini disebabkan karena penurunan sekresi insulin ataupun
sensitivitas dari reseptor insulin (Sukandar, Andrajati, Sigit, Adya, Setiadi,
Kusnandar, 2009).
Sampai saat ini pengobatan untuk penyakit diabetes mellitus adalah
dengan menggunakan obat hipoglikemik oral (OHO), suntikan insulin maupun
dengan diet. Glibenklamida merupakan obat hipoglikemik oral yang sering
digunakan. Penggunaan obat-obat oral maupun suntikan insulin jelas memakan
dilakukan seumur hidup penderitanya. Penggunaan tanaman obat merupakan salah
satu solusi dari permasalahan tersebut.
Tanaman Macaranga tanarius L. merupakan tanaman tropis yang banyak
ditemukan di Asia Selatan hingga Australia bagian utara (Lim, Lim, dan Yule,
2009). Kulit kayunya diketahui memiliki banyak kandungan tanin sehingga dapat
digunakan sebagai antidiare dan antiseptik (Lim, dkk., 2009). Di Thailand
biasanya digunakan sebagai antipiretik dan antitusif (Phommart, Sutthivaiyakit,
Chimnoi, Ruchirawat, dan Sutthivaiyakit, 2005).
Daun M. tanarius diketahui memiliki aktivitas daya antioksidan pada uji
DPPH oleh penelitian Lim dkk. (2009). Hasil penelitian Puteri dan Kawabata
(2010) menunjukkan bahwa isolasi ekstrak metanol dari M. tanarius (EMMT)
memiliki daya hambat α-glikosidase. Penelitian in vivo pada EMMT juga penah
dilakukan diantaranya yaitu sebagai analgesik (Andini dan Hendra, 2011)
antiinflamasi dan sebagai hepatoprotektif (Kurniawaty, Andrianto, dan Hendra,
2011). Bentuk sediaan yang digunakan pada penelitian ini menggunakan ekstrak
metanol-air. Hal ini berdasarkan hasil penelitian Puteri dan Kawabata (2010)
bahwa senyawa hasil isolasi EMMT menghasilkan senyawa inhibitor α
-glikosidase. Handayani (2011) melaporkan bahwa EMMT 0,43 g/kg BB dapat
menurunkan glukosa darah tikus jantan.
Di seluruh dunia, termasuk di Indonesia, penggunaan pengobatan
komplementer dan alternatif (complementary and alternative medicine, CAM)
dalam 20 tahun terakhir semakin meningkat tajam. Pada dasarnya obat herbal dan
herbal digunakan untuk melengkapi atau komplementer dari obat konvensional.
Akan tetapi pada kenyataanya, masyarakat seringkali bereksperimen dalam
penggunaan herbal dan konvensional untuk mengobati penyakitnya. Mereka
beranggapan bahwa alami berarti aman. Namun faktanya adalah walaupun herbal
bersifat alami, namun banyak jenis herbal yang dalam penggunaannya perlu
pengawasan ketat dari tenaga medis profesional karena cukup berbahaya. Selain
itu, penggunaan herbal seringkali memiliki interaksi negatif bila dikonsumsi
bersamaan dengan obat konvensional (Harmanto dan Subroto, 2006)
Oleh sebab itu peneliti melakukan penelitian apakah kombinasi ekstrak
metanol-air daun M. tanarius dan glibenklamida mempunyai efek menurunkan
kadar glukosa darah pada tikus jantan galur Wistar yang terbebani glukosa oral.
1. Permasalahan
Apakah kombiansi EMMT dan Glibenklamida mempunyai aktivitas
penurunan kadar glukosa darah pada tikus putih jantan galur Wistar ?
2. Keaslian penelitian
Beberapa penelitian mengenai daun M. tanarius yang pernah dilakukan
adalah uji efektivitas antioksidan melalui uji DPPH oleh Phommart, dkk (2005).
Penelitian Puteri dan Kawabata (2010) menunjukkan bahwa isolasi EMMT
memiliki daya hambat α-glikosidase. Penelitian in vivo pada EMMT juga penah
dilakukan diantaranya, yaitu penelitian efek analgesik oleh Andini dan Hendra
(2011), penelitian efek antiinflamsi dan efek hepatoprotektif oleh Kurniawaty, dkk
(2011), dan penelitian efek penurunan kadar glukosa darah pada tikus terbebani
potensiasi efek menurunkan kadar glukosa darah dari EMMT dengan
Glibenklamid pada tikus jantan galur Wistar terbebani glukosa belum pernah
dilakukan.
3. Manfaat penelitian
a) Manfaat teoritis
Penelitian ini diharapkan dapat memberikan informasi yang bermanfaat
tentang penggunaan tanaman alternatif yang digunakan secara bersamaan
dengan obat dokter sebagai penurun kadar glukosa darah.
b) Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi kepada masyarakat
tentang kegunaan daun M. tanarius yang digunakan bersama
Glibenklamida sebagai penurun kadar glukosa darah.
B. Tujuan
Untuk mengetahui bahwa kombinasi EMMT dan glibenklamida
mempunyai aktivitas penurunan kadar glukosa darah pada tikus putih jantan galur
5 BAB II
PENELAHAN PUSTAKA
A.Diabetes Mellitus
1. Definisi
Diabetes mellitus adalah gangguan metabolisme yang ditandai dengan
hiperglikemia yang berhubungan dengan abnormalitas metabolisme karbohidrat,
lemak dan protein yang disebabkan karena penurunan sekresi insulin atau
penurunan sensitifitas insulin, atau keduanya menyebabkan komplikasi kronis
mikrovaskular, makrovaskular dan neuropati (Sukandar, dkk., 2009). Diabetes
ditandai dengan poliuria, polidipsi, polifagia dan peningkatan kadar gula dara atau
hiperglikemia, yaitu glukosa puasa ≥ 126 ml/dL atau postprandial ≥ 200mg/dL
atau glukosa sewaktu ≥ 200mg/dL (Suherman, 2008).
2. Gejala
Gejala klasik penyakit diabetes mellitus, dikenal dengan istilah trio-P,
yaitu poliuria (banyak kencing), polidipsi (banyak minum), dan polifagia (banyak
makan). Dengan kadar glukosa darah 180 mg/dl, ginjal sudah tidak bisa
mereabsorpsi glukosa dari filtrat glomerulus sehingga timbul glikosuria. Karena
glukosa menarik air, osmotik diuretik akan terjadi yang mengakibatkan poliuria.
Poliuria akan mengakibatkan hilangnya banyak air dan elektrolit lewat urine,
mengakibatkan sering merasa haus dan peningkatan asupan air (polidipsia).
Karena sel tubuh juga mengalami kekurangan bahan bakar (cell starvation),
pasien merasa sering lapar dan ada peningkatan asupan makanan (polifagia). Pada
IDDM, lingkaran setan dengan hilangya banyak glukosa (lewat urine) dan glukosa
yang tidak dapat dipakai (dalam darah) akan mengakibatkan banyak kalori yang
hilang dan berat badan pasien menurun walaupun ia banyak makan (Baradero,
Dayrit, Siswadi, 2005).
Gejala lain yang mungkin dikeluhkan pasien adalah kesemutan, gatal,
mata kabur, dan impotensi pada pria, serta pruritus vulva pada wanita (Mansjoer,
Triyanti, Savitri, Wardhani, Setiowulan, 2001)
3. Klasifikasi
Diabetes mellitus dibedakan menjadi 2 yaitu:
a. Diabetes mellitus tipe 1. Terjadi karena adanya gangguan produksi
insulin akibat autoimun atau idiopatik. Tipe ini sering disebut juga insulin
dependent diabetes mellitus atau IDDM karena pasien mutlak membutuhkan
insulin (Suherman, 2008). IDDM umumnya muncul sebelum usia dewasa,
walaupun seringkali juga terjadi pada orang-orang dewasa non-obese dan pasien
yang sudah lanjut usia pada waktu diabetes mulai muncul. Diabetes tipe ini
disebabkan oleh gangguan katabolisme, dimana insulin tidak ada sama sekali
dalam sirkulasi, glukagon plasma meningkat dan sel-sel B pankreas tidak
responsif terhadap semua stimuli insulinogen. Oleh sebab itu, pasien-pasien ini
mutlak memerlukan pengobatan insulin eksogen untuk memperbaiki katabolisme,
dalam darat dapat turun (Insulin dependent) (Direktoral Jendral Pengawasan Obat
dan Makanan, 1991).
b. Diabetes mellitus tipe 2. Terjadi akibat resistensi insulin atau
gangguan sekresi insulin. Pada tipe ini tidak selalu dibutuhkan insulin,
kadang-kadang cukup dengan diet atau antidiabetik oral. Karena tipe ini sering disebut
juga nondependent insulin diabetes mellitus atau NIDDM (Suherman, 2008).
NIDDM biasanya muncul pada usia dewasa, walaupun dapat muncul pada
anak-anak. Pada diabetes tipe ini, insulin endogen dalam sirkulasi sebenarnya masih
cukup tinggi untuk mencegah ketoasidosis, tetapi sering kali sub-normal atau
relatif tidak cukup karena kebutuhan yang meningkat yang disebabkan oleh tidak
sensitifnya jaringan. Dengan demikian, pasien-pasien diabetes tipe ini tidak
mutlak memerlukan insulin untuk mempertahankan hidup. NIDDM dibagi
menjadi dua yaitu berhubungan dengan kegemukan dan tidak berhubungan
dengan kegemukan (obesitas). NIDDM yang berhubungan dengan kegemukan
inilah yang paling sering dijumpai (Direktoral Jendral Pengawasan Obat dan
Makanan, 1991).
c. Diabetes mellitus tipe lain. Tipe ini disebabkan oleh berbagai kelainan
genetik spesifik (kerusakan genetik sel ß pankreas dan kerja insulin), penyakit
pada pankreas, obat-obatan, bahan kimia, infeksi, dan lain- lain (Wijayakusuma,
2006).
d. Diabetes mellitus saat kehamilan. Diabetes mellitus saat kehamilan
merupakan istilah yang digunakan untuk wanita yang menderita diabetes selama
diabetes kehamilan kembali normal saat postpartum (setelah kelahiran), tetapi
pada beberapa wanita tidak demikian (Wijayakusuma, 2006).
4. Prevalensi
Di Indonesia berdasarkan penelitian epidemiologis didapatkan
prevalensi. Diabetes mellitus sebesar 1,5 – 2,3% pada penduduk yang usia lebih
15 tahun, bahkan di daerah urban prevalensi DM sebesar 14,7% dan daerah rural
sebesar 7,2%. Prevalensi tersebut meningkat 2-3 kali dibandingkan dengan negara
maju, sehingga diabetes mellitus merupakan masalah kesehatan masyarakat yang
serius. Berdasarkan data Badan Pusat Statistik Indonesia tahun 2003 penduduk
Indonesia yang berusia di atas 20 tahun sebesar 133 juta jiwa, maka pada tahun
2003 diperkirakan terdapat penderita DM di daerah urban sejumlah 8,2 juta dan di
daerah rural sejumlah 5,5 juta. Selanjutnya, berdasarkan pola pertambahan
penduduk diperkirakan pada tahun 2030 akan terdapat 194 juta penduduk yang
berusia di atas 20 tahun maka diperkirakan terdapat penderita sejumlah 12 juta di
daerah urban dan 8,1 juta di daerah rural (Perkeni, 2006).
5. Diagnosis penyakit
a. Pemeriksaan Gula Darah. Pemeriksaan terhadap kadar gula dalam
darah vena pada saat pasien puasa 12 jam sebelum pemeriksaan atau 2 jam setelah
Tabel I. Nilai Normal Kadar Gula Darah (Sutedjo, 2006)
No Jenis pemeriksaan Nilai Normal Keterangan
1 Kadar Glukosa
Hasil pemeriksaan berulang diatas nilai normal kemungkinan menderita
diabetes Mellitus. Pemeriksaan glukosa darah toleransi adalah pemeriksaan kadar
gula dalam darah puasa (sebelum diberi glukosa 75 gram oral), 1 jam setelah
diberi glukosa dan 2 jam setelah diberi glukosa. Pemeriksaan ini bertujuan untuk
melihat toleransi tubuh terutama insulin terhadap pemberian glukosa dari waktu
ke waktu (Sutedjo, 2006).
b. Hb A1C. Pemeriksaan dengan menggunakan bahan darah, untuk
memperoleh informasi kadar gula darah yang sesungguhnya, karena pasien tidak
dapat mengkontrol hasil tes dalam waktu 2-3 bulan. Glikosiliasi adalah masuknya
gula ke dalam sel darah merah dan terikat. Maka tes ini berguna untuk mengukur
tingkat ikatan gula pada hemoglobin A (AIC) sepanjang umur sel darah merah
(120 hari). AIC menunjukkan kadar hemoglobin terglikosilasi yang pada orang
normal antara 4-6%. Semakin tinggi nilai AIC pada penderita DM semakin
potensial beresiko terkena komplikasi (Sutedjo, 2006).
c. Glukosa Sewaktu. Pemeriksaan glukosa darah tanpa persiapan
bertujuan untuk melihat kadar gula darah sesaat tanpa puasa dan tanpa
penderita yang diduga DM sebelum dilalukan pemeriksaan yang sesungguhnya
dipersiapkan misalnya puasa, setelah makan dan toleransi (Sutedjo, 2006).
d. Fruktosamin. Peningkatan kadar fruktosamin menggambarkan
adanya defisensi enzim yang juga berpengaruh pada berkurangnya kemampuan
tubuh mensintesis glukosa dari jenis lain sehingga terjadi hipoglikemi.
Pemeriksaan fruktosamin menggunakan metode enzimatik seperti pada
pemeriksaan glukosa (Sutedjo, 2006).
6. Terapi farmakologi
a. Insulin. Digunakan untuk menurunkan kadar guka darah dengan
menstimulasi pengambilan glukosa perifer dan menghambat produksi glukosa
hepatik.
b. Sulfonilurea. Bekerja dengan cara merangsang sekresi insulin pada
pankreas sehingga hanya efektif bila sel beta masih dapat berproduksi. Golongan
ini tidak boleh diberikan pasien dengan gangguan hepar dan ginjal.
c. Biguanid. Digunakan untuk NIDDM yang gagal dikendalikan
dengan diet dan sulfonilurea terutama untuk pasien yang gemuk. Golongan ini
tidak menyebabkan hipoglikemik. Mekanismenya dengan cara menurunkan
produksi gula dihepar dan meningkatkan sensitivitas jaringan otot dan adipose
dalam insulin.
d. Meglitinid. Mekanisme kerjanya sama seperti sulfonilurea yaitu
cara merangsang sekresi insulin pada pankreas. Pasien dengan gangguan fungsi
hepar dan ginjal harus diberikan hati-hati. Golongan ini dapat menyebabkan
e. Tiazolidindion. Digunakan untuk meningkatkan sensitivitas insulin
pada otot dan jaringan adiposa dan menghambat glukogenesis hepatik.
f. Penghambat α-glukosidase. Obat golongan penghambat enzim α
-glikosidase ini dapat memperlambat absorbsi polisakarida, dektrin, dan disakarida
di intestin. Dengan menghambat kerja enzim α-glikosidase di intestin, dapat
mencegah peningkatan glukosa plasma pada orang normal dan diabetes. Karena
tidak mempengaruhi sekresi insulin, maka tidak akan menyebabkan hipoglikemia
(Sukandar, dkk.2009 dan Suherman, 2008).
B. Transport Glukosa
Glukosa merupakan karbohidrat yang paling penting. Glukosa
merupakan karbohidrat dalam makanan yang diserap dalam jumlah besar kedalam
darah (Mayes, Murray, dan Granner, 2000). Glukosa merupakan bahan bakar
utama jaringan tubuh yang pada akhirnya digunakan oleh sel tubuh untuk
membentuk ATP. Glukosa merupakan jenis monosakarida yang paling banyak
diabsorbsi oleh usus biasanya mencakup 80% dari kalori karbohidrat yang
diabsobsi. Alasanya adalah bahwa glukosa merupakan produk cerna terakhir dari
makanan (Guyton dan Hall 2006). Glukosa diserap usus melalui dua tahap, yaitu
masuknya glukosa melewati membran apikal usus dan kemudian dari sel masuk
melewati membrane basal. Absobsi glukosa melewati membrane apikal difasilitasi
oleh Sodium-dependent glucose transporter (SGLT1), sedangkan pada membran
basalis difasilitasi oleh transporter glukosa (GLUT2) (Boron dan Boulpaep, 2005).
tranpost aktif, sebab masuknya glukosa ke dalam sel epitel usus, terjadi melawan
gradient kadar konsentrasi glukosa. Glukosa masuk melewati membran basalis
diberi energi oleh gradient elektrokimia Na+, yang mana pada gilirannya dijaga
oleh tekanan Na+ yang melewati membran basolateral dengan pompa Na-K.
Sistem transport glukosa dengan Na+ ini adalah salah satu contoh proses transport
aktif sekunder, sedangkan masuknya melewati membran basalis terjadi secara
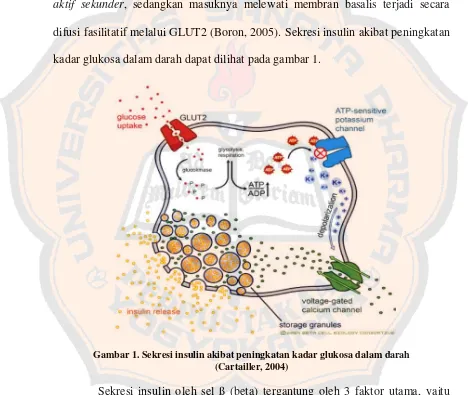
difusi fasilitatif melalui GLUT2 (Boron, 2005). Sekresi insulin akibat peningkatan
kadar glukosa dalam darah dapat dilihat pada gambar 1.
Gambar 1. Sekresi insulin akibat peningkatan kadar glukosa dalam darah (Cartailler, 2004)
Sekresi insulin oleh sel ß (beta) tergantung oleh 3 faktor utama, yaitu
kadar glukosa darah, ATP-sensitive K+ channels dan Voltage-sensitive Calsium
Channels sel ß pankreas. Mekanisme kerja faktor- faktor tersebut adalah sebagai
channels pada membran sel ß akan terbuka sehingga ion kalium akan
meninggalkan sel ß, dan Ca-channels tertutup, akibatnya kalsium tidak dapat
masuk ke dalam sel ß, dan perangsangan sel ß untuk mensekresi insulin menurun
(Merentek, 2006).
Pada saat keadaan setelah makan, kadar glukosa darah akan meningkat
dan akan ditangkap oleh sel ß melalui glucose transporter 2 (GLUT2) dan dibawa
ke dalam sel ß. Di dalam sel, glukosa akan mengalami fosforilase menjadi
glukosa-6-fosfat (G6P) dengan bantuan enzim glukokinase. Glukosa-6-fosfat akan
mengalami glikolisis menjadi asam piruvat. Proses glikolisis juga menghasilkan
produk 6-8 ATP. Penambahan ATP ini akan meningkatkan rasio ATP/ADP dan
menutup kanal kalium. Penumpukan kalium dalam sel mengakibatkan
depolarisasi membran sel sehingga membuka kanal kalsium dan kalsium akan
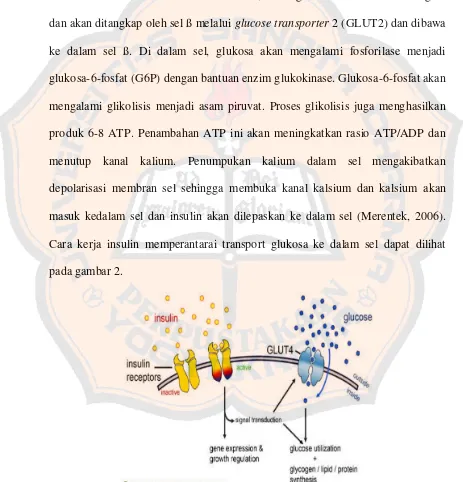
masuk kedalam sel dan insulin akan dilepaskan ke dalam sel (Merentek, 2006).
Cara kerja insulin memperantarai transport glukosa ke dalam sel dapat dilihat
pada gambar 2.
Sekresi insulin pada orang non diabetes meliputi 2 fase, yaitu early peak
(fase 1) yang terjadi dalam 3–10 menit pertama setelah makan. Insulin yang
disekresi pada fase ini adalah insulin yang disimpan dalam sel beta (siap pakai).
Fase 2 atau disebut juga fase lanjut adalah sekresi insulin yang dimulai 20 menit
setelah stimulasi glukosa. Pada fase 1 pemberian glukosa meningkatkan sekresi
insulin untuk mencegah kenaikan kadar glukosa darah, dan kenaikan glukosa
darah selanjutnya akan merangsang fase 2 untuk meningkatkan produksi insulin.
Pada diabetes mellitus tipe-2, sekresi insulin pada fase 1 tidak mampu
menurunkan glukosa darah sehingga merangsang fase 2 untuk menghasilkan
insulin lebih banyak, tetapi sudah tidak mampu meningkatkan sekresi insulin
sebagaimana pada orang non diabetes (Merentek, 2006).
C. Glibenklamida
Glibenklamida (gambar 3.) merupakan obat hipoglikemik oral yang
digunakan secara luas di dalam pengobatan diabetes mellitus tidak tergantung
insulin (tipe-2). Glibenklamida merupakan sulfonilurea paling poten dan dikenal
sebagai sulfonilurea ”generasi kedua” (Dollery, 1999). Mekanisme kerjanya
sering disebut insulin secretagogues, yaitu merangsang sekresi insulin dari
Aksi farmakologi glibenklamida adalah mentimulasi pelepasan insulin
dengan meningkatkan fungsi sel-sel pankreas. Pada terapi jangka pendek, hal
ini signifikan dengan peningkatan sirkulasi konsentrasi insulin, tetapi dengan
penggunaan berkelanjutan biasanya terjadi penurunan kadar insulin tanpa
merusak kontrol glikemik. Sulfonilurea menunjukkan peningkatan sintesis
glikogen dan penghambatan glikogenolisisi dan glukoneogenesis pada hati. Pada
subyek normal puasa, peningkatan konsentrasi insulin dalam plasma dan
penurunan glukosa plasma terjadi 15-60 menit setelah pemberian glibenklamida
oral dan mencapai maksimum setelah 1-2 jam sebelum kembali ke nilai dasar
setelah 3 jam (Dollery, 1999).
Glibenklamida dimetabolisme dalam hati menjadi produk dengan
aktivitas hipoglikemik yang sangat rendah. Meskipun analisis spesifik untuk
senyawa yang tidak dimetabolisme menimbulkan dugaan terdapatnya suatu
waktu-paruh plasma yang singkat, tetapi efek biologis glibenklamida jelas
bertahan selama 24 jam setelah pemberian satu dosis tunggal yang diberikan
pada pagi hari pada pasien diabetes. Awal dosis pemberian yang biasa adalah 2,5
mg/hari atau kurang, dan rata-rata dosis pemeliharaan adalah 5-10 mg/hari yang
diberikan sebagai dosis tunggal pada pagi hari. Tidak dianjurkan untuk
memberikan dosis pemeliharaan lebih dari 20 mg/hari (Nolte dan Karam, 2002).
Obat golongan tiazid dan beta bloker dapat menurunkan efektifitas
glibenklamida, sedangkan penggunaan yang bersamaan dengan golongan obat
meningkatkan risiko terjadinya hipoglikemia (Lacy, Armstrong, Goldman,
Lance, 2006).
D. Penghambat Enzim -Glikosidase
Obat golongan penghambat enzim α-glukosidase ini dapat
memperlambat absorpsi polisakarida (starch), dektrin, dan disakarida di intestin.
Dengan menghambat kerja enzim α-glukosidase di brush border intestin, dapat
mencegah peningkatan glukosa plasma pada orang normal dan pasien DM
(Suherman, 2008).
Karena kerjanya tidak mempengaruhi sekresi insulin, maka tidak
menyebabkan efek samping hipoglikmia. Akarbose dapat digunakan sebagai
monoterapi pada DM usia lanjut atau DM yang glukosa postprandialnya sangat
tinggi. Diklinik sering digunakan bersamaan antidiabetik oral lain dan atau insulin
(Suherman, 2008).
Obat golongan ini diberikan pada waktu mulai makan. Akarbose,
merupakan oligosakarida yang berasal dari mikroba, dan miglitol, yang secara
kompetitif juga menghambat glukoamilase dan sukrase, tetapi efeknya pada α
-amilase pankreas lemah. Kedua preparat dapat menurunkan glukosa plasma
postprandial pada DM tipe 1 dan 2, dan pada DM tipe 2 dengan hiperglikemia
yang hebat dapat menurunkan HbA1C secara bermakna. Pada pasien DM dengan
hiperglikemia ringan sampai sedang, hanya dapat mengatasi hiperglikemia sekitar
30%-50% dibandingkan antidiabetik oral lainnya (dinilai dengan pemeriksaan
Efek samping yang bersifat dose-dependent antara lain malabsorpsi,
flatulen, diare, dan abdominal bloating. Untuk mengurangi efek samping
sebaiknya dosis dititrasi, mulai dosis awal 25 mg pada saat mulai makan untuk
selama 4-8 minggu sampai dosis maksimal 75 mg setiap tepat sebelum makan.
Dosis yang lebih kecil dapat diberikan dengan makanan kesil (snack) (Suherman,
2008).
Penghambat enzim α-glukosidase paling efektif bila diberikan bersama
makanan yang berserat, mengandung polisakarida, dengan sedikit kandungan
glukosa dan sukrosa. Bila akarbose diberikan bersama insulin atau golongan
sulfonilurea, dan menimbulkan hipoglikemia, pemberian glukosa akan lebih baik
daripada pemberian sukrose, polisakarida atau maltosa (Suherman, 2008).
E. Interaksi Antar Obat
Antaraksi obat didefinisikan sebagai peristiwa manakala efek obat
tertentu (obat-obyek) diubah oleh obat lain (antaraktan) yang diberikan sebelum
atau bersama-sama dengannya. Kedua berdasarkan perantara (mekanisme kerja),
antaraksi obat didefinisikan sebagai peristiwa yang terjadi manakala dua obat
diberikan bersama-sama, saling mempengaruhi proses farmakokinetika dan / atau
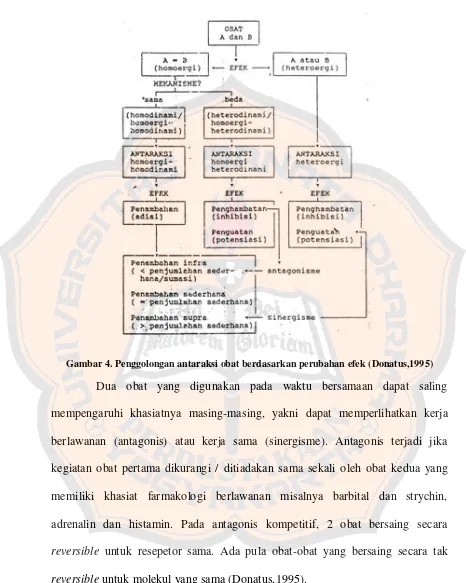
farmakodinamika masing-masing obat (Donatus, 1995). Rangkuman
penggolongan antaraksi obat berdasarkan perubahan efek dapat dilihat pada
Gambar 4. Penggolongan antaraksi obat berdasarkan perubahan efek (Donatus,1995)
Dua obat yang digunakan pada waktu bersamaan dapat saling
mempengaruhi khasiatnya masing-masing, yakni dapat memperlihatkan kerja
berlawanan (antagonis) atau kerja sama (sinergisme). Antagonis terjadi jika
kegiatan obat pertama dikurangi / ditiadakan sama sekali oleh obat kedua yang
memiliki khasiat farmakologi berlawanan misalnya barbital dan strychin,
adrenalin dan histamin. Pada antagonis kompetitif, 2 obat bersaing secara
reversible untuk resepetor sama. Ada pula obat-obat yang bersaing secara tak
Sinergisme adalah kerja sama antar dua obat dan dikenal dalam 2 jenis :
1. Adisi (penambahan)
Efek kombinasi adalah sama dengan jumlah kegiatan dari masing-masing
obat misalnya kombinasi asetosal dan paracetamol juga trisulfa
2. Potensiasi (peningkatan potensi)
Kedua obat saling memperkuat khasiatnya, sehingga terjadi efek yang
melebihi jumlah matematis dari a+b. Kedua obat kombinasi dapat memiliki
kekuatan yang sama seperti esterogen dan progesteron, sulfametoksazol dan
trimetroprim, asetosal dan kodein atau satu obat dari kombinasi memiliki efek
berlainan misalnya analgetika dan klorporamazin, benzodiazepin dan
meprobamat/ alkohol, perintang MAO dan amfetamin, juga tiamin/piridoksi dan
diklofenak (NSAIDs) (Tjay dan Raharja, 2007).
F. Tanaman Macaranga tanarius L. 1. Keterangan botani
Kingdom : Plantae (tumbuhan)
Subkingdom : Tracheobionta (tumbuhan berpembuluh)
Super Divisi : Spermatophyta (menghasilkan biji)
Divisi : Magnoliphyta (tumbuhan berbunga)
Kelas : Magnoliopsida (berkeping dua/dikotil)
Sub Kelas : Rosidae
Ordo : Euphorbiales
Genus : Macaranga
Spesies : Macaranga tanarius L. (Plantamor, 2008)
Tanaman M. tanarius termasuk dalam famili euphorbiaceae. Tanaman ini
dikenal di beberapa daerah dengan nama Tutup ancur (Jawa), Mapu (Batak) dan
Mara (Sunda) (Prosea, 2010).
2. Morfologi
M. tanarius merupakan pohon kecil sampai sedang, dengan dahan agak
besar. Daun berseling, agak membundar, dengan stipula besar yang luruh.
Perbungaan malai di ketiak, bunga ditutupi oleh daun gagang. Buah kapsul
berkokus 2, ada kelenjar kekuningan di luarnya. Biji membulat dan
menggelembur. Jenis ini juga mengandung tanin yang cukup untuk menyamak
jala dan kulit (Prosea, 2010).
3. Kandungan kimia
Hasil penelitian Lim dkk. (2009) ditemukan bahwa ekstrak aseton daun
M. tanarius mengandung tujuh hidrolyzable tanin baru yang sebelumnya telah
ditemukan sebanyak 21 komponen didalamnya.pada penelitian Phommart dkk.
(2005) diketahui bahwa ekstrak n-heksana dan kloroform dari daun M. tanarius
mempunyai aktivitas daya antioksidan pada uji 2,2-diphenyl-1 picryhydrazyl
(DPPH) serta diketemukannya tiga komponen baru, yaitu flavononol, tanari
flavonon C, tanari flavonon D bersama tujuh komponen sebelumnya, yaitu
Nymphaeol A,B,C ,tanari flavononeB, Blumenol A,B ,annuionone E. Hasil
penelitian selanjutnya oleh Matsunami dkk. (2006) dari ekstrak daun M. tanarius
Macarangloside B, Macarangloside C, mallophenol B bersamaan dengan lima
komponen sebelunya yang pernah diketemukan yaitu mallophenol B, Lauroside E,
methyl brevitolin carboxylate, Hyperin dan isoquercitrin. Sedangkan pada tahun
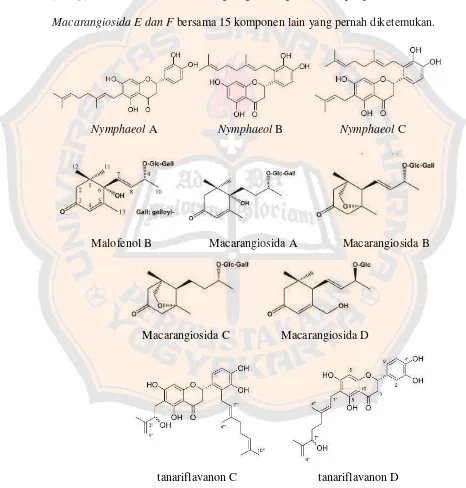
2009 diketemukan glikosida, (+)-pinoresinol 4-O-[6”-O-galloly]-β -D-glucopyranosida dan dua megastigman glukosida yang diberi nama
Macarangiosida E dan F bersama 15 komponen lain yang pernah diketemukan.
Nymphaeol A Nymphaeol B Nymphaeol C
Malofenol B Macarangiosida A Macarangiosida B
Macarangiosida C Macarangiosida D
tanariflavanon C tanariflavanon D
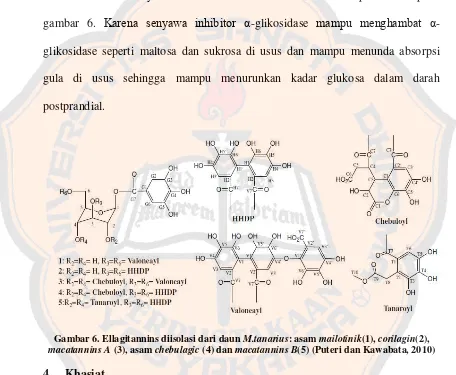
Hasil penelitian Puteri dan Kawabata (2010) menunjukkan bahwa isolasi
EMMT terdiri dari asam mailotinik, corilagin, asam chebulagic dan dua
komponen baru macatannins A dan macatannins B memiliki daya hambat α
-glikosidase sehingga bisa dimanfaatkan sebagai obat diabetes dan obesitas.
Gambar struktur senyawa hasil isolasi ekstrak metanol air dapat dilihat pada
gambar 6. Karena senyawa inhibitor α-glikosidase mampu menghambat α
-glikosidase seperti maltosa dan sukrosa di usus dan mampu menunda absorpsi
gula di usus sehingga mampu menurunkan kadar glukosa dalam darah
postprandial.
Gambar 6. Ellagitannins diisolasi dari daun M.tanarius: asam mailotinik(1), corilagin(2), macatannins A (3), asam chebulagic (4) dan macatannins B(5)(Puteri dan Kawabata, 2010)
4. Khasiat
Kulit kayu dan daun dari M. tanarius diketahui mengandung banyak
tanin sehingga dimanfaatkan sebagai obat diare, luka dan juga antiseptik (Lin,
dkk., 1990), sedangkan di Thailand dimafaatkan sebagai obat tradisional untuk
antipiretik dan antitusif, sementara akar dan daun segarnya dimanfaatkan sebagai
tanarius digunakan sebagai pakan ternak ataupun sebagai pembungkus tempe
(Puteri dan Kawabata, 2010).
5. Ekologi penyebaran dan budaya
M. tanarius tersebar luas, dari Kepulauan Andaman dan Nicobar,
Indo-Cina, Cina Selatan, Taiwan dan Kepulauan Ryukyu, seluruh Malesia, sampai ke
Australia Utara dan Timur dan Melanesia. Jenis ini umum dijumpai di daratan
Asia Tenggara (Thailand Selatan, Semenanjung Malaya), dan pada banyak pulau
di Malesia (yaitu Sumatra, Borneo, Kepulauan Sunda Kecil, Sulawesi, Nugini,
seluruh Kepulauan Filipina) (Prosea, 2010). Tumbuhan ini dapat ditemukan
disepanjang Asia Timur dan Selatan, khususnya Cina Selatan, Korea dan Jepang
(Matsunami, dkk., 2006).
G. Metode Penyarian
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat
aktif dari simplisia nabati ataupun simplisia hewani menggunakan pelarut yang
sesuai, kemudian semua atau hampir semua pelaut diuapkan dan massa atau
serbuk yang tersisa diperlakukan sedemikian hingga memenuhi baku yang telah
ditetapkan (Direktoral Jendral Pengawasan Obat dan Makanan, 1995).
Maserasi merupakan cara penyarian yang sederhana. Maserasi dilakukan
dengan merendam serbuk simplisia dalam cairan penyari. Cairan penyari akan
menembus dinding sel dan masuk ke rongga sel yang mengandung zat aktif, zat
aktif akan larut dan karena adanya perbedaan konsentrasi antara larutan zat aktif
tersebut berulang sehingga terjadi keseimbangan konsentrasi antara larutan di
luar dan di dalam sel (Direktoral Jendral Pengawasan Obat dan Makanan, 1986).
H. Teknik Uji Diabetik dan Metode Penetapan Kadar Glukosa Darah 1. Teknik uji diabetik
a. Uji Toleransi Glukosa Oral. Kemampuan tubuh untuk mentolelir
gula yang dikonsumsi diukur dengan uji toleransi glukosa sesuai pedoman WHO
(WHO, 1985), yang dilakukan sebelum dan sesudah menjalani pengobatan.
Semalam sebelum dilakukan GTT, hewan uji dipuasakan terlebih dahulu (10-16
jam). Kemudian di pagi hari, hewan uji diberi larutan gula. Sampel darah diambil
sesaat sebelum meminum glukosa, dan 2 jam setelah pemberiaan. Bila perlu
sampel-sampel darah juga bisa diambil tiap 0,5 jam stelah pembebanan glukosa
(jam ke 0; 0,5 ; 1; 1,5; dan 2 jam). Kemudian sampel –sampel tersebut segera
dianalisis untuk menentukan kadar glukosa. Apabila analisis tidak dapat segera
dilakukan, maka sampel dapat disimpan dalam bentuk plasmanya (Direktoral
Jendral Pengawasan Obat dan Makanan, 1991).
b. Induksi Aloksan. Aloksan (2,4,5,6-tetraoksipirimidin;
5,6-dioksiurasil) merupakan senyawa hidrofilik dan tidak stabil (gambar 7). Waktu
paro pada suhu 37°C dan pH netral adalah 1,5 menit dan bisa lebih lama pada
Gambar 7. Struktur aloksan
Sebagai diabetogenik, aloksan dapat digunakan secara intravena,
intraperitoneal dan subkutan. Dosis intravena yang digunakan biasanya 65 mg/kg
BB, sedangkan intraperitoneal dan subkutan adalah 2-3 kalinya. Aloksan secara
cepat dapat mencapai pankreas. Pembentukan oksigen reaktif merupakan faktor
utama pada kerusakan sel β Langerhans. Salah satu target dari oksigen reaktif
adalah DNA pulau Langerhans pankreas. Pada kondisi tersebut, konsentrasi
insulin meningkat sangat cepat, dan secara signifikan mengakibatkan gangguan
pada sensitivitas insulin perifer dalam waktu singkat. Selain itu aloksan juga
diduga berperan dalam penghambatan glukokinase dalam proses metabolisme
energi (Nugroho, 2006).
c. Streptozotosin. Streptozotosin (STZ) atau
2-deoksi-2-[3-(metil-3-nitrosoureido)-D-gluko piranose] diperoleh dari Streptomyces achromogenes
dapat digunakan untuk menginduksi baik DM tipe 1 maupun tipe 2 pada hewan
Gambar 8. Struktur streptozotosin
Dosis yang digunakan untuk menginduksi DM tipe 1 untuk intravena
adalah 40-60 mg/kg, sedangkan dosis intraperitoneal adalah lebih dari 40 mg/kg
BB. STZ juga dapat diberikan secara berulang, untuk menginduksi DM tipe 1
yang diperantarai aktivasi sistem imun. Untuk menginduksi DM tipe 2, STZ
diberikan intravena atau intraperitoneal dengan dosis 100 mg/kg BB pada tikus
yang berumur 2 hari kelahiran, pada 8-10 minggu tikus tersebut mengalami
gangguan respon terhadap glukosa dan sensitivitas sel β terhadap glukosa.
Patofisiologis tersebut identik pada DM tipe II. Selain itu, STZ juga mampu
membangkitkan oksigen reaktif yang mempunyai peran tinggi dalam kerusakan
sel β pankreas (Nugroho, 2006).
2. Metode penetapan kadar glukosa darah
Secara umum metode penentuan glukosa darah menurut Widowati,
Dzulkarnain, dan Sa’roni (1997) dapat ditentukan dengan beberapa cara :
a. Metode kondensasi gugus amin. Prinsip :aldosa dikondensasi
dengan orto toludin dalam suasana asam dan menghasilkan larutan berwarna hijau
setelah dipanaskan. Kadar glukosa darah dapat ditentungkan sesuai dengan
b. Metode enzimatik. Glukosa dapat ditentukaan secara enzimatik,
misalnya dengan penambahan enzim glukosa oksidase (GOD). Dengan adanya
oksigen atau udara , glukosa dioksidasi oleh enzim menjadi asam glukoronat
disertai pembentukan H2O2 akan membebaskan O2 yang mengoksidasi akseptor
kromogen yang sesuai serta memberikan warna yang sesuai pula. Kadar glukosa
darah ditentukan berdasarkan intensitas warna yang terjadi, diukur secara
spektrofotometri.
c. Metode reduksi. Prinsip : kadar glukosa darah ditentukan secara
reduksi dengan menggunakan suatu oksidan ferisianida yang direduksi menjadi
ferosianida oleh glukosa dalam suasana basa dengan pemanasan. Kemudian
kelebihan garam feri dititrasi secara iodometri.
d. Metode pemisahan glukosa. Glukosa dipisahkan dalam keadaan
panas dengan antron atau timol dalam suasana asam sulfat pekat. Glukosa juga
dapat dipisahkan secara kromatografi, tetapi pemisahan glukosa ini jarang
I. Landasan Teori
Diabetes merupakan gangguan metabolisme yang ditandai dengan
hiperglikemia yang berhubungan dengan abnormalitas metabolisme karbohidrat,
lemak dan protein yang disebabkan karena penurunan sekresi insulin atau
penurunan sensitifitas insulin (Sukandar,dkk., 2009). Dari hasil penelitian Puteri
dan Kawabata (2010) yang menyatakan bahwa senyawa hasil isolasi EMMT
menghasilkan senyawa inhibitor α-glikosidase. Hasil penelitian Handayani (2011)
menyatakan bahwa EMMT dosis 0,43g/kgBB mempunyai efek menurunkan
kadar glukosa darah pada tikus jantan terbebani glukosa.
Tjay dan Raharja (2007) melaporkan bahwa pada dasarnya kedua obat
yang dikombinasi dapat saling memperkuat khasiatnya, sehingga terjadi efek yang
melebihi kemampuan sebelumnya. Kedua obat kombinasi dapat memiliki
kekuatan yang sama efeknya maupun berlainan efek. Oleh karena itu uji
pontensiasi juga perlu dilakukan untuk perkembangan obat baru.
Glibenklamida merupakan obat hipoglikemik oral yang digunakan secara
luas di dalam pengobatan diabetes mellitus tidak tergantung insulin (tipe-2).
Mekanisme kerja glibenklamida adalah mentimulasi pelepasan insulin dengan
meningkatkan fungsi sel-sel pankreas. Pada penelitian ini akan melihat efek
kombinasi dari glibenklamid dosis 0,45 mg/kg BB dan EMMT dosis 0,43g/kg BB.
J. Hipotesis
Kombinasi EMMT dan Glibenklamida memiliki efek menurunkan kadar
29 BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Jenis dan rancangan penelitian ini adalah eksperimental murni dengan
penelitian rancangan acak lengkap pola searah.
B. Variabel dan Definisi Operasional
1. Variabel
a. Variabel bebas
Variabel bebas penelitian ini adalah kombinasi dosis EMMT dengan
Glibenklamida.
b. Variabel tergantung
Variabel tergantung penelitian ini adalah kadar glukosa darah
c. Variabel pengacau terkendali
i)Galur hewan uji adalah tikus dengan galur Wistar
ii) Jenis kelamin hewan uji adalah tikus jantan
iii)Umur hewan uji adalah 2-3 bulan
iv)Berat hewan uji adalah 200-300 gram
v) Waktu pengamatan antara 08.00-15.00
d. Variabel pengacau tak terkendali
i) Kemampun absorbsi, distribusi dan eleminasi dari tikus terhadap
kombinasi EMMT dan glibenklamida
ii) Kondisi patologis dari tikus
2. Definisi operasional
a. Daun M. tanarius adalah daun yang diambil dari tanaman M. tanarius,
memiliki daun yang berwarna hijau, tidak berlubang, segar, tidak terlalu tua dan
muda (diambil daun yang berada tidak dipangkal dan diujung batang).
b. Ekstrak metanol-air daun M. tanarius berupa ekstrak kental yang
diperoleh dengan mengekstraksi serbuk kering daun M. tanarius seberat 10,0
gram yang dilarutkan dalam 100 ml pelarut metanol 50% secara maserasi selama
72 jam, dengan putaran 140 rpm. Kemudian disaring dengan kertas saring dan
diuapkan di oven pada suhu 50oC, hingga diperoleh bobot ekstrak tetap dengan
susut pengeringan sebesar 0%.
c. Dosis ekstrak metanol-air daun M. tanarius adalah sejumlah berat
ekstrak metanol-air daun M. tanarius tiap satuan berat badan hewan uji dengan
satuan g/KgBB.
d. Daya antidiabetik adalah penurunan kadar glukosa dalam darah yang
C. Bahan Penelitian
1. Hewan uji tikus jantan galur Wistar dengan berat 200-300 gram dengan
umur 2-3 bulan yang diperoleh dari Laboratorium Hayati Imono Fakultas
Farmasi Universitas Sanata Drama Yogyakarta.
2. Bahan uji daun M. Tanarius diperoleh dari kebun obat Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta yang dipanen pada bulan April
3. Senyawa pembanding adalah kaplet Glibenklamida yang diproduksi oleh
PT. IndoFarma.
4. Pereaksi untuk pengukuran kadar glukosa darah
Pereaksi yang digunakan adalah enzim Glukose GOD FS * (DiaSys,
Germany) yang terdiri atas
Tabel II. Isi perekasi enzim Glucose GOD-PAP
Reagen
Buffer fosfat pH 7,5 250 mmol/l
Fenol 5 mmol/l
4-aminoantipyrine 0,5 mmol/l
Glukosa oksidase GOD ≥10 kU/I
Phenol Aminoantipirin Peroksidase PAP ≤1 kU/I
Glukosa standart 100 mg/dl 5,5 mmol/dl
5. Glukosa monohidrat p.a (Merck) dengan dosis 1,75 g/kg BB sebagai
larutan untuk pembuatan kurva baku dan untuk uji toleransi glukosa oral
yang diperoleh dari Laboratorium Farmakologi Toksikologi Fakultas
6. Paraffin cair sebagai pelancar aliran darah dalam pengambilan sampel
darah dari hewan uji yang didapat dari Laboratorium Biofarmasetika dan
Bioanalisis Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
7. Metanol yang diperoleh dari Laboratorium Farmakognosi Fitokimia
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
8. Aquadest diperoleh dari Laboratorium Farmakologi dan Toksikologi
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
D. Alat atau Instrumen Penelitian
1. Seperangkat alat gelas (beaker glass, labu takar, gelas pengaduk, gelas
ukur) merk Pyrex
2. Mortir dan stamper
3. Jarum suntik (injeksi peroral) yaitu jarum suntik yang ujungnya diberi
bulatan kecil dengan lubang ditengahnya agar tidak melukai hawan uji.
4. Mikropipet, yellow tipe, blue tipe
5. Sentrifuge (Centurion Scientific C2 Series) dan microtube
6. Surgical blade no 10 dan 11
7. Vitalab mikro (Microlab 200, Merck)
8. Alat timbang elektrik (Mettler Tolendo AB 204, Switzerland)
9. Vortex
10.Holder
11.Tabung Efendrof
E. Tata Cara Penelitian 1. Determinasi tanaman M.tanarius
Determinasi tanaman M. tanarius dilakukan dengan mencocokan kunci
determinasi tanaman M. tanarius dengan buku acuan (Backer dan Van Den
Brink, 1963). Determinasi dilakukan oleh Bapak Yohanes Dwiatmaka, M.Si.,
dosen Fakultas Farmasi, Universitas Sanata Dharma Yogyakarta.
2. Pengumpulan bahan
Bahan uji yang digunakan adalah daun M. tanarius yang masih segar dan
berwarna hijau, dipetik dari Kebun Obat Fakultas Farmasi Universitas Sanata
Dharma Yogyakarta
3. Pembuatan serbuk
Daun M. tanarius dicuci bersih di bawah air mengalir. Setelah bersih
daun diangin-anginkan hingga daun tidak tampak basah lagi kemudian untuk
mengoptimalkan pengeringan, pengeringan dilakukan dengan menggunakan oven
pada suhu 50°C selama 24 jam. Setelah kering daun dibuat serbuk dan diayak
dengan ayakan nomor 50.
4. Pembuatan ekstrak metanol air daun M.tanarius
Sebelum pembuatan ekstrak, daun M. tanarius dibuat serbuk terlebih
dahulu supaya kandungan fitokimia yang terkandung dalam daun M. tanarius
lebih mudah terekstrak karena luas permukaan serbuk yang kontak dengan pelarut
makin besar. Sebanyak 10 g serbuk kering daun M. tanarius diekstraksi secara
maserasi dengan melarutkan serbuk dalam 100 ml pelarut metanol 50% pada suhu
pelarut metanol adalah agar senyawa kimia yang terkandung dalam daun M.
tanarius dapat larut dalam pelarut. Setelah dilakukan perendaman, hasil maserasi
disaring dengan kertas saring. Larutan hasil saringan dipindahkan dalam cawan
porselen yang telah ditimbang sebelumnya, agar mempermudah perhitungan
randemen ekstrak yang akan diperoleh. Selanjutnya, beaker glass yang berisi
larutan hasil maserasi tersebut dimasukkan dalam oven untuk diuapkan dengan
suhu 50°C agar mendapatkan ekstrak metanol-air daun M. tanarius yang kental
dengan bobot pengeringan ekstrak yang tetap.
5. Penetapan konsentrasi pekat ekstrak
Menghitung rata-rata randemen ke-5 replikasi ekstrak metanol-air daun
M. tanarius kental yang telah dibuat.
Randemen ekstrak = Berat cawan ekstrak kental – berat cawan kosong
Konsentrasi ekstrak didapat dari hasil rata-rata randemen ekstrak. Konsentrasi
yang dapat digunakan adalah konsentrasi pekat yang dapat dibuat dimana pada
konsentrasi tersebut ekstrak dapat dimasukkan serta dikeluarkan dari spuit oral.
6. Penetapan dosis efektif ekstrak daun M.tanarius
Dosis efektif didapatkan dari hasil penelitian Handayani (2011).
7. Preparasi bahan
a. Pembuatan larutan stok glukosa p.a. 15% b/v. Glukosa monohidrat
p.a. ditimbang sebanyak 3,75 gram dan dilarutkan dengan aquades dalam labu
b. Pembuatan CMC 1 % b/v. Timbang CMC sebanyak 0,25 gram
kemudian diencerkan dengan menggunakan air panas dengan menggunakan labu
takar 25 mL hingga tanda.
c. Pembuatan larutan ekstrak 38,4 % b/v. Ekstrak ditimbang sebanyak
1,92 gram dan dilarutkan dengan CMC 1% dalam labu takar 5 mL sampai tanda.
d. Penentuan keseragaman bobot kaplet Glibenklamida. Penentuan
keseragaman bobot kaplet glibenklamida mengacu pada Direktoral Jendral
Pengawasan Obat dan Makanan 1979. Timbang 20 tablet, hitung bobot tablet. Jika
ditimbang satu satu, tidak boleh lebih dari 2 tablet yang masing-masing bobotnya
menyimpang dari bobot rata-ratanya lebih besar dari harga yang ditetapkan kolom
A, dan tidak satu tabletpun menyimpang dari bobot rata-ratanya lebih dari harga
yang ditetapkan kolom B. Nilai penyimpangan bobot rata-rata kolom A dan B
dapat dilihat pada tabel III.
Tabel III. Keseragaman bobot tablet
Bobot rata-rata Penyimpangan bobot dalam %
A B
25 mg atau kurang 15 % 30%
26 mg samapi dengan 150 mg 10 % 20%
151 mg sampai dengan 300 mg 7,5 % 15 %
Lebih dari 300 mg 5 % 10%
e. Penentuan dosis Glibenklamida. Dosis glibenklamida yaitu 5 mg
pada manusia dengan berat badan 70 kg dikonversikan ke tikus 200 mg dengan
faktor konversi 0,018.
5 mg Glibenklamida x 0,018 = 0,09 mg Glibenklamida / 200 mg
Berdasarkan perhitungan maka besarnya dosis Glibenklamida pada hewan uji
tikus yaitu 0,45 mg/kg BB
f. Pembuatan larutan Glibenklamida 0,1125 mg/ml. Timbang serbuk
glibenklamida setara dengan 25 mg glibenklamida murni, larutkan dengan CMC
1% dalam labu takar 10 ml sampai tanda sebagai larutan induk glibenklamida.
Buat dengan konsentrasi 0,1125 mg/ml dalam labu ukur 10 ml dari larutan induk
glibenklamida tersebut. Caranya dengan mengambil 0,45 ml larutan baku induk
Glibenklamida kemudian diencerkan dalam labu takar 10 ml.
8. Percobaan pendahuluan
a. Penetapan pemberian glibenklamida. Tujuan dari penetapan
pemberian glibenklamida adalah untuk melihat pengaruh waktu pemberian
terhadap efek hipoglikemik glibenklamida, agar pada saat uji toleransi glikosa oral
(UTGO) glibenklamida sudah memberikan efek penurunan kadar glukosa darah.
Orientasi ini menggunakan 12 ekor tikus yang terbagi dalam 4 kelompok dimana
masing-masing kelompok diberi perlakuan kontrol positif dan kontrol negatif.
Perlakuan tersebut dilakukan terhadap masing-masing kelompok yaitu pada menit
ke-15 sebelum UTGO untuk kelompok kesatu, menit ke-30 sebelum UTGO untuk
kelompok kedua, dan menit ke-45 sebelum UTGO untuk kelompok ketiga dan
pada kelompok keempat sebagai kontrol negatifnya yaitu dengan diberikan larutan
CMC 1%. Semua pemberian dilakukan secara peroral, selanjutnya dilakukan
UTGO dengan diberikan larutan glukosa monohidrat 15% b/v; 1,75 g/kgBB.
Pengambilan cuplikan darah dilakukan sesaat sebelum perlakuan sebagai menit
Pengukuran kadar glukosa darah dilakukan dengan menggunakan metode
GOD-PAP. Selanjutnya dibuat kurva UTGO dan perhitungan harga LDKK0-240.
Penentuan waktu pemberian Glibenklamida didasarkan pada harga selisih
LDKK0-240 kontrol positif dan negatif tertinggi.
b. Penetapan pemberian ekstrak metanol-air M.tanarius. Tujuan dari
penetapan pemberian ekstrak metanol-air M.tanarius adalah untuk melihat
pengaruh waktu pemberian terhadap efek hipoglikemik ekstrak metanol-air
M.tanarius, agar pada saat uji toleransi glikosa oral (UTGO) ekstrak sudah
memberikan efek penurunan kadar glukosa darah. Orientasi ini menggunakan 6
ekor tikus yang terbagi dalam 2 kelompok dimana masing-masing kelompok
diberi perlakuan ekstrak metanol-air M.tanarius. Perlakuan tersebut dilakukan
terhadap masing-masing kelompok yaitu pada menit bersamaan dengan UTGO
untuk kelompok kesatu, dan menit ke-15 sebelum UTGO untuk kelompok kedua.
Semua pemberian dilakukan secara peroral, selanjutnya dilakukan UTGO dengan
diberikan larutan glukosa monohidrat 15% b/v; 1,75 g/kgBB. Pengambilan
cuplikan darah dilakukan sesaat sebelum perlakuan sebagai menit ke-0 dan pada
menit ke-15, 30, 45, 60, 90, 180, dan 240 setelah UTGO. Pengukuran kadar
glukosa darah dilakukan dengan menggunakan metode GOD-PAP. Selanjutnya
dibuat kurva UTGO dan perhitungan harga LDKK0-240. Penentuan waktu
pemberian ekstrak metanol-air M.tanarius didasarkan pada harga LDKK0-240
9. Pengelompokan dan perlakuan hewan uji
Penelitian ini mengikuti rancangan acak lengkap pola searah, sehingga
nantinya 35 ekor tikus dibagi acak menjadi 7 kelompok yang tiap ekornya
terdiri dari 5 ekor. Tiap hewan uji diadaptasi dengan kondisi yang sama, jauh
dari kebisingan dan dihindarkan dari stress. Sebelum mendapatkan perlakuan,
masing-masing kelompok dipuasakan selama 18 jam dengan diberi minum, dan
kemudian diberi perlakuan sebagai berikut.
Kelompok I adalah aquades 5 ml/ kg BB (kontrol negatif untuk perlakuan
EMMT).
Kelompok II adalah larutan glibenklamida 0,45 mg/kgBB (kontrol positif).
Kelompok III adalah EMMT 0,43 g/kg BB.
Kelompok IV adalah kombinasi Glibenklamida 0,45 mg/kg BB dan EMMT
0,43 g/kg BB.
Kelompok V adalah kombinasi Glibenklamida 0,23 mg/kg BB dan EMMT
0,43 g/kg BB.
Kelompok VI adalah kombinasi Glibenklamida 0,45 mg/kg BB dan EMMT
0,22 g/kg BB.
Kelompok VII adalah kombinasi Glibenklamida 0,23 mg/kg BB dan EMMT
0,22 g/kg BB.
Semua pemberian dilakukan secara peroral, selanjutnya dilakukan UTGO
10. Penetapan kadar glukosa darah
Kadar glukosa darah ditetapkan dengan metode GOD-PAP. Pada
tiap kelompok dilakukan pengambilan cuplikan darah sebanyak 0,5 ml melalui
vena lateralis ekor dan ditampung dalam efendrof. Pengambilan cuplikan
darah dilakukan sesaat sebelum perlakuan sebagai menit ke-0 dan pada menit
ke-15, 30, 45, 60, 90, 180, dan 240 setelah UTGO. Kemudian darah
dipusingkan 3000 rpm selama 10 menit. Selanjutnya diambil 10 l serum
darah, kemudian dilakukan pengukuran seperti dalam tabel IV.
Tabel IV. Volume pengukuran kadar glukosa darah
Bahan Sampel Standart Blangko
Supernatan 10 l - -
Larutan baku glukosa - 10 l -
Aquabidest - - 10 l
Pereaksi GOD-PAP 1000 l 1000 l 1000 l
Bahan-bahan tersebut dicampur dan diinkubasi selama operating time yaitu
selama 20 menit. Kemudian divorteks. Lalu kadar glukosa darah ditetapkan
dengan menggunakan alat Micro VitaLab.
Selanjutnya dibuat kurva dengan mem-plot-kan nilai kadar glukosa darah
lawan waktu ke-0 sampai menit ke 240 dengan metode trapezoid (LDDK0-240)
dan rumus yang digunakan adalah sebagai berikut:
LDDKto-tn = x (Co+C1) + x (C2+C1) + x (C3+C2) +
x (Cn+Cn-1)
Keterangan:
t = waktu (jam-1/menit-1)
C = konsentrasi zat dalam darah (mg/ml)
F. Tata Cara Analisis Data
Dari harga LDDK0-240 glukosa darah dilakukan uji distribusi
menggunakan uji Kolmogorov Smirnov kemudian jika distribusinya normal
dilanjutkan dengan analisis Anova One Way dan post hoc tests Scheffe dengan
tingkat kepercayaan 95%. Jika nilai LDDK0-240 glukosa darah mempunyai variansi
yang berbeda maka dilakukan uji Kruskal Wallis dan dilanjutkan uji Mann
Whitney dengan tingkat kepercayaan 95% untuk mengetahui perbedaan
41 BAB IV
HASIL DAN PEMBAHASAN
A. Determinasi Tanaman
Determinasi tanaman dilakukan untuk memastikan bahwa tanaman yang
digunakan telah sesuai dan tidak terjadi kesalahan dalam pengambilan sampel.
Determinasi tanaman dilakukan di laboratorium Farmakognosi–Fitokimia fakultas
Farmasi Universitas Sanata Dharma Yogyakarta dengan menggunakan pustaka
acuan (Backer dan Van Den Brink, 1963).
Hasil determinasi sebagai berikut:
1b, 2b, 3b, 4b, 12b, 13b, 14b, 17b, 18b, 19b, 20b, 21b, 22b, 23b, 24b, 25a famili:
Euphorbiaceae.
1b, 3b, 4b, 6a, 7b, 8b, 10b, 13a, 14b Genus: Macaranga.
1a, 2a, 3b, 5b Species : Macaranga tanarius (L.) M. A.
Hasil determinasi menyatakan bahwa tanaman yang dipergunakan dalam
penelitian ini adalah benar tanaman Macaranga tanarius L..
B. Hasil Maserasi Daun M. tanarius L.
Daun M. tanarius L. yang diambil merupakan daun yang masih segar dan
berwarna hijau kemudian dicuci dengan air mengalir lalu dikeringkan untuk
menghilangkan air. Simplisia kering kemudian diserbuk/ diblender untuk
memperluas permukaan, sehingga zat-zat yang terkandung di dalam daun lebih