OPTIMASI RANCANGAN ASSAY KIT TRIIODOTYRONINE (T
3)
METODE COATED TUBE
Sutari, Veronika Yulianti S, Gina Mondrida,Triningsih, Agus Arianto, Puji Widayati
Pusat Radioisotop dan Radiofarmaka – BATAN,PUSPIPTEK Serpong, Tangerang 15310 E-mail : [email protected]
ABSTRAK
OPTIMASI RANCANGAN ASSAY KIT TRIIODOTHYRONINE (T3) METODE
COATED TUBE. Triiodothyronine (T3) adalah salah satu hormon yang diekskresikan
oleh kelenjar tiroid. Sernyawa T3 dianggap sebagai molekul biologis paling aktif yang
diproduksi hingga sekitar 80% melalui deiodinasi tetraiodothironin (T4) di dalam
jaringan pheripheral.Teknik Untuik mendeteksi adanya hormon pada kelenjar tiroid ini, diperlukan suatu yang dapat mengukur jumlah hormon dengan konsentrasi yang sangat kecil dalam darah. Teknik radioimmunoassay (RIA) mempunyai kesensitifan dan kespesifikan yang tinggi, sangat sesuai untuk kebutuhan ini. Pusat Radioisotop dan Radiofarmaka (PRR) Badan Tenaga Nuklir Nasional sejak tahun 1995 telah mengembangkan kit RIA-T3 dengan metode Coated tube. Pada penelitian ini dilakukan optimasi kondisi assay kit RIA-T3 PRR. Tujuan dari penelitian ini untuk mendapatkan kit RIA-T3 yang handal dengan rancangan dan kondisi assay yang
optimum. Optimasi dilakukan dengan mencari nilai ikatan maksimum dari variasi berbagai komponen kit meliputi volume standar,Cacahan perunut, volume perunut dan volume assay buffer. Hasil yang optimum diperoleh pada volume standar 50 µl dengan cacahan perunut sekitar 20000 cpm, volume perunut 50 µl dan volume assay buffer 250 µl. Kondisi assay yang optimum dicapai dengan inkubasi pada suhu ruang sambil diaduk dengan memakai shaker selama 2 jam. Pada assay dengan kondisi optimum tersebut di atas, diperoleh ikatan maksimum (maximum binding) sebesar 71,50 % ± 3,00 dan non spesifik binding (NSB) 1,43%.
Kata kunci : Optimasi,Triiodothyronine, Radioimmunoassay. Coated Tube
ABSTRACT
OPTIMATION ASSAY DESIGN OF TRIIODOTHYRONINE (T3) RIA KIT COATED
TUBE METHOD..Triodothyronine (T3) is one of hormones that is secreted by thyroid
gland. The T3 is a biologicaly active molecule that is produced up to 80% by
deiodination tetraiodothironine (T4) in pheriperal tissue. In order the measure the
existeence of this hormone, a method is needed to detect this sustance at a very low concentration in blood. Radioimmunoassay (RIA) offers a highly sensitive and spesific method is suitable for this demand. Therefore, since 1995 the Centre Radioisotope and Radiopharmaceuticals - National Nuclear Energy Agency has developed T3 RIA kit
coated tube method. The aim of this research is optainednan reliable T3 RIA kit - with
optimum design and condition of assay. Data obtained from optimation of kit component, optimum condition was obtained using 50 µl of standard solution , 50 µl tracer at ± 20000 cpm and 250 µl assay buffer. This optimum assay condition was performed by incubating the assay sistem in room temperatur while shaking for two hours, giving maximum binding valued 71,50 % ± 3,00 and non spesific binding 1.43 %. Keywords: Optimation, Triiodothyronine, Radioimmunoassay,Coated Tube
PENDAHULUAN
riiodothyronine (T3) adalah salah satu
hormon yang diekskresi oleh kelenjar tiroid. T dianggap sebagai molekul biologis yang paling
aktif yang diproduksi hingga sekitar 80% melalui deiodinasi tetraiodothironin (T4) di dalam
jaringan pheripheral[1]. Tiroid adalah salah satu kelenjar endokrin dengan berat kurang lebih 2-3 gram pada anak dan 18-20 gram pada orang
dewasa. Kelenjar ini ditemukan pada leher berbentuk seperti kupu-kupu. Hormon T3 dalam
serum normal berkisar antara 1,4 - 3,3 nmol/L untuk wanita dan 1,0 – 2,6 nmol/L untuk pria. Jika fungsi kelenjar tiroid terganggu maka sirkulasi hormon tiroid (T3 dan T4) dalam darah
akan tidak normal, sehingga akan menyebabkan beberapa penyakit tiroid seperti: gangguan pada janin,abortus cacat bawaan, retardadasi mental , bisu tuli kelumpuhan dan kerdil. Ketidaknormalan tersebut pada anak-sekolah dapat ditunjukkan dengan prestasi dan IQ anak yang kurang, sedangkan pada orang dewasa dapat menyebabkan gangguan pada gondok dan segala jenis komplikasinya bahkan sampai terjadi kanker kelenjar tiroid.[1,2]
Keberadaan T3 secara signifikan
diketahui pada daerah euthyroid, dan total kadar T3 dapat digunakan untuk skrining terhadap
gangguan tiroid setelah dilakukan dengan beberapa tes pengujian. Untuk menentukan kadar hormon T3 pada kelenjar tiroid diperlukan suatu
metode yang dapat mengukur jumlah hormon dalam konsentrasi yang sangat kecil, salah satunya adalah dengan menggunakan teknik
radioimmunoassay (RIA). [1,8]
Teknik RIA merupakan teknik pengukuran yang didasarkan pada reaksi immunologi yaitu reaksi antigen dan antibodi dengan menggunakan radioisotop sebagai perunut, sehingga mudah dideteksi. Teknik RIA dikembangkan oleh Yalow & Berson didasarkan pada reaksi kompetisi antara antigen bertanda radioaktif (Ag*) dan antigen tak bertanda (Ag) yang terdapat dalam cuplikan/standar terhadap antibodi yang jumlahnya
terbatas. Dalam analisis kuantitatif jumlah antigen bertanda dan antibodi adalah tetap, maka jumlah antigen tak bertanda yang ada dalam standar bervariasi. Makin banyak antigen tak bertanda (Ag) yang ada dalam cupplikan/standar, makin sedikit kompleks Ag*-Ag yang terbentuk. Banyaknya Ag*-Ab yang terbentuk diukur dengan pencacah gamma.[3,4,5]
Pada teknik RIA, setelah kesetimbangan reaksi dicapai, maka perlu dilakukan tahap pemisahan dimana ligan yang terikat dan yang bebas harus dipisahkan. Ada dua sitem pemisahan pada teknik RIA yaitu pereaksi pemisah fasa cair yaitu dengan menambahkan pereaksi pengendap, misalnya larutan polyetilenglikol (PEG), tetapi metode ini sudah ditinggalkan karena pengerjaannya kurang effisien. Sedang pereksi pemisah fasa padat dengan mengimobilisasi antibodi ke fasa padat, misalnya magnetig, polystiren bead ( coated bead) atau tabung polystiren (coated tube).
Teknik RIA sangat cocok untuk mendeteksi adalanya hormon T3 pada kelenjar tiroid dalam
tubuh pasien secara invitro dengan mudah, sederhana, sensitif dan mempunyai ketelitian tinggi serta spesifik karena menggunakan antigen yang ditandai dengan radioaktif. Pada teknik ini menggunakan sistem pemisah fasa padat yaitu dengan menempelkan antibodi kedalam tabung reaksi polystiren berdasar bintang (coated tube), karena dengan metode ini pengerjaan mudah, cepat , sederhana dan effisien. Konsentrasi T3 yang
terdapat dalam sampel dapat dihitung dengan rumus: [5,6]
Cacahan fase terikat-BG
% ikatan dari masing-masing standar (B/T) = ────────────── X 100% (1)
Cacahan Total -BG
Cacahan fase terikat-BG
% ikatan Non Spesifik Bounding (B/T) = ────────────── X 100% (2)
Cacahan Total % Pusat Radioisotop dan Radifarmaka BATAN mempunyai fungsi dan tugas pokok untuk mengembangkan Radioisotop dan Radiofarmaka termasuk Teknik
Radioimmunoassay (RIA) salah satunya kit
RIA-125
I-T3. Beberapa Rumah sakit di Indonesia dalam
pekerjaannya menggunakan kit RIA-125I-T3 untuk
menentukan kadar T3, namun kit tersebut masih
diimpor dari luar negeri sehingga harganya menjadi mahal. Untuk menanggulangi hal tersebut maka dilakukan penelitian tentang produksi kit RIA-125I-T3. Setiap kit yang
diproduksi perlu dilakukan optimasi dan rancangan assay dari kit tersebut agar diperoleh
kit yang berkualitas baik dan dapat digunakan untuk penentuan T3. Optimasi rancangan assay
komponen kit dilakukan dari mengoptimasikan volume standar, cacahan perunut , volume perunut dan volume assay buffer. Sedang optimasi kondisi assay yaitu dengan mengoptimasikan kondisi inkubasi pada suhu ruang sambil diaduk menggunakan shaker selama waktu tertentu. [5,6,7]
Dalam makalah ini akan dilaporkan tentang hasil-hasil yang diperoleh dari setiap tahap yang telah dilakukan sampai dengan hasil optimasi yang diperoleh dalam penelitian ini.
TATA KERJA Bahan dan Peralatan
Tabung coated tube T3 PRR , Standar T3
PRR, perunut (T3-125 I) PRR, assay buffer
(dengan melarutkan 1,82 gram Trizma Base dari Sigma dalam 100 ml aquades dan diatur pHnya menjadi 8,25).
Peralatan yang digunakan antara lain: Pipet mikro berbagai ukuran (Eppendorf) beserta tipnya. Rak tabung (lokal), Vortex buatan (Fisher Scientific), Shaker (Fisher Scientific), Neraca analitik (Mettler AE 160), Gamma Managemen System buatan DPC, Inkubator (EYELA)
Cara Kerja
Optimasi Assay Volume Larutan Standar Diambil Coated tube (tabung bersalut antibodi T3) yang telah diberi nomor 1 sampai
dengan 6 dan 1 tabung NSB ( tabung bukan
coated tube ) dibuat 4 set. Dipipet standar nol
dengan variasi volume untuk tabung NSB, kemudian dipipet ke tabung coated tube yang sudah diberi nomor masing-masing secara berurutan dimasukkan standar 0 nmol/L, 1 nmol/L, 2 nmol/L,3 nmol/L, 5 nmol/L dan 10 nmol/L dengan variasi volume : 25 µl, 50 µl, 100 µldan 150 µl. Ke dalam semua tabung ditambah 50 µl perunut (T3-125 I) dengan cacahan kira-kira
40.000 cpm dan 500 µl assay buffer. Campuran dihomogenkan dengan vorteks kemudian diaduk dengan shaker selama 2 jam pada suhu ruang. Tabung didekantasi dan biarkan sampai kering kemudian diukur radioaktivitasnya memggunakan pencacah gamma selama satu menit. Persentase ikatan dari masing-masing standar (B/T) dihitung menggunakan persamaan (1) kemudian dibuat kurva konsentrasi standar VS %B/T yang hasilnya terlihat pada gambar 1. Sedang %NSB dihitung menggunakan persamaan (2)
Optimasi Assay Cacahan Tracer
Diambil Coated tube (tabung bersalut antibodi T3) yang telah diberi nomor 1 sampai
dengan 6 dan 1 tabung NSB ( tabung bukan
coated tube ) dibuat 4 set. Dipipet 50 µl standar 0
nmol/L ke semua tabung NSB , kemudian kedalam masing-masing tabung coated tube yang sudah diberi nomor secara berurutan dipipet 50 µl standar 0 nmol/L, 1 nmol/L, 2 nmol/L,3 nmol/L, 5 nmol/L dan 10 nmol/L. Ke dalam masing-masing tabung ditambah 50 µl perunut (T3-125 I) dengan Variasi cacahan kira-kira
10.000, 20.000 40.000 dan 80.000 cpm dan 500 µl assay buffer ke semua tabung. Campuran dihomogenkan dengan vortek kemudian diaduk dengan shaker selama 2 jam pada suhu ruang.
Tabung didekantasi dan biarkan sampai kering kemudian diukur radioaktivitasnya memggunakan pencacah gamma selama satu menit. Persentase ikatan dari masing-masing standar (B/T) dihitung menggunakan persamaan (1) kemudian dibuat kurva konsentrasi standar VS %B/T yang hasilnya terlihat pada gambar 2. Sedang %NSB dihitung menggunakan persamaan (2).
Optimasi Assay Volume Tracer
Diambil Coated tube (tabung bersalut antibodi T3) yang telah diberi nomor 1 sampai
dengan 6 dan 1 tabung NSB ( tabung bukan
coated tube ) dibuat 4 set. Dipipet 50 µl standar 0
nmol/L ke semua tabung NSB, kemudian kedalam masing-masing tabung coated tube yang sudah diberi nomor secara berurutan dipipet 50 µl standar 0 nmol/L, 1 nmol/L, 2 nmol/L, 3 nmol/L, 5 nmol/L dan 10 nmol/L. Ke dalam masing-masing tabung ditambah perunut (T3-125I)
dengan cacahan kira-kira 20.000 cpm dengan variasi volume: 25 , 50 , 100 dan 150 µl dan 500 µl assay buffer ke semua Tabung. Campuran dihomogenkan dengan vortek kemudian diaduk dengan shaker selama 2 jam pada suhu ruang. Tabung didekantasi dan biarkan sampai kering kemudian diukur radioaktivitasnya memggunakan pencacah gamma selama satu menit. Persentase ikatan dari masing-masing standar (B/T) dihitung menggunakan persamaan (1) kemudian dibuat kurva konsentrasi standar VS %B/T yang hasilnya terlihat pada gambar 3. Sedang % NSB dihitung menggunakan persamaan (2).
Optimasi Assay Volume Assay Buffer
Diambil Coated tube (tabung bersalut antibodi T3) yang telah diberi nomor 1 sampai
dengan 6 dan 1 tabung NSB ( tabung bukan
coated tube ) dibuat 4 set. Dipipet 50 µl standar 0
nmol/L ke semua tabung NSB , kemudian kedalam masing-masing tabung coated tube yang sudah diberi nomor secara berurutan dipipet 50 µl standar 0 nmol/L, 1 nmol/L, 2 nmol/L, 3 nmol/L, 5 nmol/L dan 10 nmol/L. Ke dalam semua tabung ditambah 50 µl perunut (T3-125 I)
dengan cacahan kira-kira 20.000 cpm dan
assay buffer dengan variasi volume : 250, 500 dan
1000 µl.. Campuran dihomogenkan dengan vortek kemudian diaduk dengan shaker selama 2 jam pada suhu ruang. Tabung didekantasi dan biarkan sampai kering kemudian diukur radioaktivitasnya memggunakan pencacah gamma selama satu menit. Persentase ikatan dari masing-masing standar (B/T) dihitung menggunakan persamaan (1) kemudian dibuat kurva konsentrasi standar VS
%B/T yang hasilnya terlihat pada gambar 4. Sedang %NSB dihitung menggunakan persamaan (2).
Optimasi Kondisi Inkubasi
Diambil Coated tube (tabung bersalut antibodi T3) yang telah diberi nomor 1 sampai
dengan 6 dan 1 tabung NSB ( tabung bukan
coated tube ) dibuat 4 set. Dipipet 50 µl standar 0
nmol/L ke semua tabung NSB, kemudian kedalam masing-masing tabung coated tube yang sudah diberi nomor secara berurutan dipipet 50 µl standar 0 nmol/L, 1 nmol/L, 2 nmol/L, 3 nmol/L, 5 nmol/L dan 10 nmol/L. Ke dalam semua tabung ditambah 50 µl tracer (T3-125 I)
dengan cacahan kira-kira 20.000 cpm dan 500 µl assay buffer . Campuran dihomogenkan dengan vortek kemudian dinkubasi 2 jam pada suhu 37°C, diaduk dengan shaker selama 2 jam pada suhu ruang dan inkubasi 2 jam pada suhu ruang tanpa diaduk dengan shaker Tabung didekantasi dan biarkan sampai kering kemudian diukur radioaktivitasnya memggunakan pencacah gamma selama satu menit. Persentase ikatan dari masing-masing standar (B/T) dihitung menggunakan persamaan (1) kemudian dibuat kurva konsentrasi standar VS %B/T yang hasilnya terlihat pada gambar 5. Sedang %NSB dihitung menggunakan persamaan (2).
.
Optimasi Waktu Pengadukkan
Diambil Coated tube (tabung bersalut antibodi T3) yang telah diberi nomor 1 sampai
dengan 6 dan 1 tabung NSB ( tabung bukan
coated tube ) dibuat 4 set. Dipipet 50 µl standar 0
nmol/L ke semua tabung NSB , kemudian kedalam masing-masing tabung coated tube yang sudah diberi nomor secara berurutan dipipet 50 µl standar 0 nmol/L, 1 nmol/L, 2 nmol/L, 3 nmol/L, 5 nmol/L dan 10 nmol/L. Ke dalam semua tabung ditambah 50 µl perunut (T3-125 I)
dengan cacahan kira-kira 20.000 cpm dan 500 µl assay buffer . Campuran dihomogenkan dengan vortek kemudian dinkubasi sambil diaduk dengan shaker dengan variasi waktu 1, 2, 3 dan 4 jam pada suhu ruang. Tabung didekantasi dan biarkan sampai kering kemudian diukur radioaktivitasnya memggunakan pencacah gamma selama satu menit. Persentase ikatan dari masing-masing standar (B/T) dihitung menggunakan persamaan (1) kemudian dibuat kurva konsentrasi standar VS %B/T yang hasilnya terlihat pada gambar 6. Sedang % NSB dihitung menggunakan persamaan (2).
HASIL DAN PEMBAHASAN
Optimasi dilakukan dengan tujnuan untuk mencari kondisi yang optimum, dalam arti yang menguntungkan. Dalam pembuatan kit RIA, optimasi assay sangat diperlukan karena berpengaruh dalam karakterisasi assay.[5]
Beberapa hal yang perlu diperhatikan dalam optimasi assay (Wayan Rediating,2004) yaitu limit deteksi harus sesuai dengan konsentrasi yang diukur sehingga mampu menganalisis cuplikan pada batas konsentrasi yang dikehendaki dengan ketelitian tinggi, persen B/T diatas 30%, NSB (Non spesific binding) diusahakan sekecil mungkin,ketelitian maksimal terletak di daerah kurva standar, pengerjaan mudah dan cepat, biaya murah. Dalam penelitian ini telah dilakuakn optimasi assay komponen dan kondisi assay Kit RIA-125I-T3.
Hasil dari optimasi yang dilakukan tercanrum sebagai berikut:
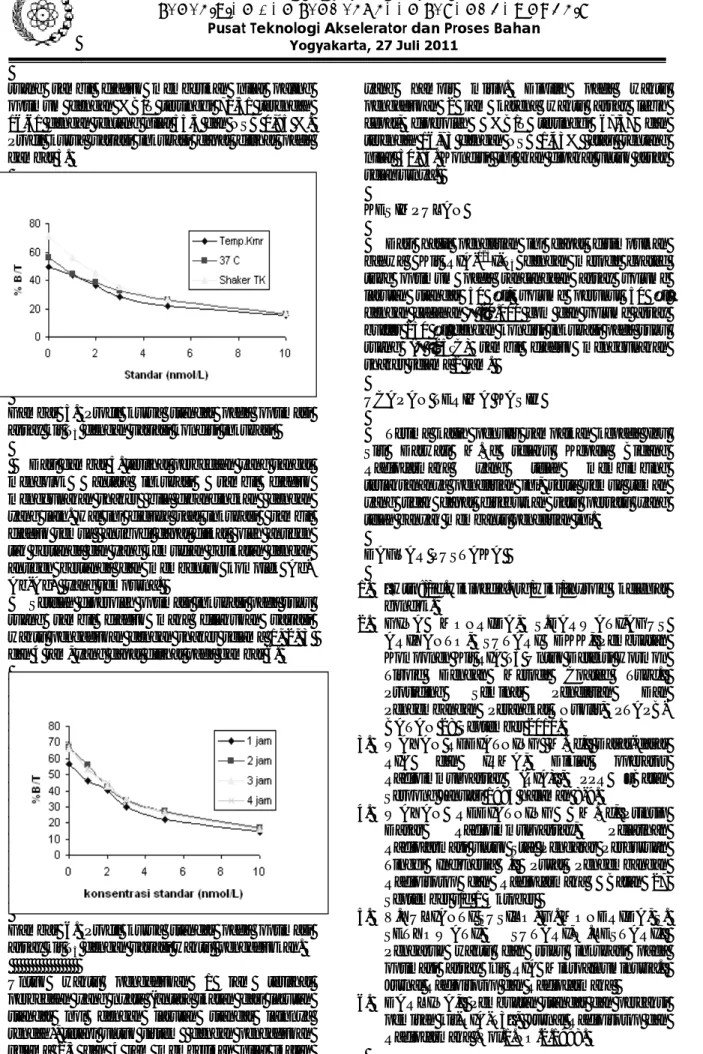
Optimasi volume larutan standar menggunakan variasi volume (25 µl, 50 µl, 100 µl dan 150 µl) serta menggunakan 50 µl perunut dengan cacahan ± 40.000 cpm dan 500 µl assay
buffer dengan hasil dapat dilihat pada gambar 1.
Gambar 1. Profil kurva standar pada optimasi
assay kit T3 dengan variasi volume standar.
Terlihat bahwa volume larutan standar 50 µl memberikan ikatan maksimum (B/T) tertinggi 70,51 % ± 4,55 (std 0 nmol/L) dan terendah 16,99% ± 3,36 (std 10 nmol/L ) dengan NSB 1,42 %. Profil kurva volume standar 50 µl terlihat paling baik bila dibanding dengan lainnya, sehingga kurva ini dipilih karena mempunyai rentang nilai paling lebar. Untuk volume standar 25 µl memberikan nilai ikatan maksimum (B/T) lebih tinggi dari pada volume standar 50 µl, tetapi profil kurvanya tidak curam. Sedangkan volume 100 dan 150 ul hampir sama dengan kurva volume 50 uL, tetapi tidak dipakai sebagai standar yang optimum karena memerlukan volume larutan standar yang lebih banyak., atau dengan kata lain tidak ekonomis.
Optimasi penggunaan cacahan tracer
dilakukan dengan variasi cacahan perunut
kira-kira 10.000 cpm, 20.000 cpm , 40.000 cpm dan 80.000 cpm dengan volume perunut 50 µl menggunakan standar 50 µl dan 500 µl assay
buffer. Disini tidak memberi pengaruh terhadap
nilai ikatan maksimum (B/T) yang dihasilkan, dapat dilihat pada gambar 2.
Gambar 2. Profil kurva standar pada optimasi
assay kit T3 dengan variasi cacahan perunut.
Pada gambar 2, terlihat pada cacahan perunut kira-kira 20.000 cpm dengan rata-rata %B/T tertinggi 74,66 ± 1,98 sedangkan % B/T terendah 16,44 ± 1.24 dan NSB 1,43%. Dari keduanya diperoleh rentang nilai paling besar yaitu 58,22 ( selisih angka % B/T tertinggi dikurangi % B/T terendah) , yang merupakan daerah kerja optimum. Sedangkan untuk perunut dengan cacahan kira-kira 10.000 cpm, 40.000 cpm dan 80.000 cpm daerah kerjanya lebih pendek sehingga kurang sensitif.
Pada optimasi volume perunut yang dilakukan dengan variasi volume 25 µl, 50 µl , 100 µl dan 150 µl dengan cacahan kira-kira 20.000 cpm menggunakan volume larutan standar 50 µl dan 500 µl assay buffer, volume tracer 50µl menghasilkan nilai ikatan maksimum (B/T) tertinggi dibanding dengan lainnya dan diperoleh rata-rata % B/T tertinggi 71,42 ± 2,45, terendah 18,49 ±1,97 dan NSB 1,35 %. Dari kedua nilai tersebut diperoleh rentang nilai 52,93 atau daerah kerja paling lebar. Profil kurva volume tracer 50µl lebih curam dibanding kurva lainnya seperti terlihat pada gambar 3.
Gambar 3. Profil kurva standar pada optimasi
assay kit T3 dengan variasi volume tracer dengan
cacahan tetap.
Optimasi pemakain assay buffer dilakukan dengan variasi volume 250 µl, 500 µl dan 1000 ul mengunakan larutan standar 50µl dan perunut 50 µl dengan cacahan kira-kira 20.000 cpm. Dapat dilihat pada gambar 4.
Gambar 4. Profil kurva standar pada optimasi
assay kit T3 dengan variasi volume assay buffer.
Dari gambar.4 optimasi assay buffer optimum pada volume assay buffer 250 µl, dengan rata-rata % B/T tertinggi 73,49 ± 1,55 dan terendah 18,96 ± 0,06 dengan NSB 1,29 %. Dari profil kurva optimasi assay buffer pada penggunaan volume 250 µl bila dibandingkan dengan 500 µl memberikan profil kurva yang sangat mirip, tetapi untuk menghemat penggunaan pereaksi tersebut maka dipilih volume 250 µl.
Selain optimasi komponen kit yang juga dilakukan optimasi perlakuan atau langkah-langkah yang berpengaruh terhadap kit T3 yaitu
variasi inkubasi dan variasi waktu pengadukan. Variasi yang dilakukan meliputi inkubasi pada suhu ruang (± 25ºC tanpa pengadukan), suhu ruang sambil diaduk menggunakan shaker, dan pada suhu 37ºC. Ketiga kondisi dilakukan dengan waktu 2 jam. Dari percobaan diperoleh pada suhu
ruang sambil diaduk memberikan nilai paling optimum dengan %B/T tertinggi 71,51 terendah 16,61 dengan rentang nilai 55,5 dan NSB 0,95 %. Profil kurva variasi inkubasi dapat dilihat pada gambar 5.
Gambar 5. Profil kurva standar pada optimasi
assay kit T3 dengan variasi kondisi inkubasi
Dari gambar 5. terlihat perbedaan yang sangat mencolok antara inkubasi sambil diaduk menggunakan shaker bila dibandingkan dengan yang lain. Hal ini diduga saat inkubasi sambil diaduk semua antibodi dapat diikat oleh antigen tak bertanda dan yang kemudian berikatan dengan antigen bertanda dan membentuk komplek Ag-Ab-Ag* yang sempurna.
Setelah diperoleh optimasi inkubasi pada suhu ruang sambil diaduk maka dilakukan variasi waktu pengadukan dengan shaker selama 1, 2, 3 dan 4 jam, yang dapat dilihat pada gambar 6.
Gambar 6. Profil kurva standar pada optimasi
assay kit T3 dengan variasi waktu pengadukkan.
Untuk waktu pengadukan 1 jam terlihat perbedaan yang nyata (antara ikatan dari larutan standar nol dengan larutan standar lainnya rendah), tetapi untuk sistem dengan pengadukan selama 2,3 dan 4 jam memberikan nilai ikatan
yang hampir mirip. Dipilih pada waktu pengadukan 2 jam karena waktu assay lebih cepat, diperoleh %B/T tertinggi 67,57 dan terendah 16,73 dengan NSB 1,43% atau rentang nilai 50,84. Kondisi ini akan dipakai untuk assay selanjutnya.
KESIMPULAN
Dari hasil penelitian ini dapat disimpulkan bahwa Kit RIA-125I-T3 dengan metode coated
tube optimum pada rancangaan assay volume
larutan standar 50 µl, volume perunut 50 µl dengan cacahan ± 20.000 cpm dan volume assay
buffer 250 µl dengan kondisi inkubasi pada suhu
ruang (± 25ºC) sambil diaduk menggunakan
shaker selama 2 jam.
UCAPAN TERIMA KASIH
Terima kasih penulis sampaikan kepada Ibu Siti Darwati M.Sc selaku Kepala Bidang Radiofarmaka yang telah membimbing terlaksananya penelitian ini, serta semua teman yang tidak dapat disebutkan satu persatu yang telah banyak membantu penelitian ini.
DAFTAR PUSTAKA
1. ”Http://id.wikipedia.org/wiki/thyroid kelenjar gondok.
2. GINA MONRIDA, S.DARWATI,AGUS ARIYANTO, SUTARI DKK,”Pembuatan
Komponen Kit RIA T3 Untuk Deteksi Hormon Tiroid Dengan Metode Coated Tube.”
Prosiding Seminar Penelitian Dan Pengembangan Perangkat Nuklir, PTAPB-BATAN 28 September 2010.
3. WAYAN REDIATNING M.Sc,” Dasar-dasar RIA dan IRMA, Diklat operator
Radioimmunoassay (RIA)”, PPR –Batan
Serpong Januari 1993 halaman 8-9.
4. WAYAN REDIATNING M.Sc,”Prinsip
Dasar Radioimmunoassay, Pelatihan Radiofarmasi untuk Staf Pengajar Perguruan Tinggi Indonesia .” Pusat Pengembangan
Radioisotop dan Radiofarmaka Batan 27 September s/d 1 Oktober
5. V.YULIANTI SUSILO, G. MONDRIDA, S. SETYOWATI, SUTARI,W.LESTARI,”
Pengaruh waktu dan suhu inkubasi pada optimasi assay kit RIA Mikroalbuminuria.”
Jurnal Radioisotop dan Radiofarmaka
6. DARLINA,” Pembuatan standar dan pereaksi pemisah kit-RIA-T3”, Jurnal Radioisotop dan Radiofarmaka .Vol.1.NO.2.1998.
7. PUJI WIDAYATI;TR NGSIH; SRISETYOWATI; FITRIYUNITA .”
OPTIMASI ASSAY KIT IRMA CA15.3 UNTUK DETEKSI KANKER PAYUDARA.”
Prosiding Seminar Nasional XII.”Kimia Dalam Pembangunan” Hotel Santika Yogyakarta,06 Agustus 2009.
8. Institute Of Isotopes Co., Ltd 1535 Budapest, Pf,:851,”Protokol Assay Kit RIA T3, Produksi
tahun 2009 Lot No. 90527C “.