UJI LETHAL DOSE 50% (LD50) POLIHERBAL (Curcuma xanthorriza,
Kleinhovia hospita, Nigella sativa, Arcangelisia flava dan Ophiocephalus
striatus) PADA HEPARMIN
®TERHADAP MENCIT (Mus Musculus)
Lethal Dose 50% (LD50) Tests of Poliherbal (Curcuma Xanthorriza, Kleinhovia hospita,
Nigella sativa, Arcangelisia flava and Ophiocephalus striatus) on Heparmin® in Mice (Mus musculus)
Mansur Ibrahim, Akhyar Anwar, Nur Ihsani Yusuf
RESEARCH & DEVELOPMENT PT ROYAL MEDICALINK PHARMALAB
1 Abstrak
Telah dilakukan penelitian Uji Lethal Dose 50% (LD50) Poliherbal (Curcuma xanthorriza,
Kleinhovia hospita, Nigella sativa, Arcangelisia flava dan Ophiocephalus striatus) pada Sedian
Kapsul Heparmin® terhadap mencit (Mus musculus). Penelitian dilakukan dengan menggunakan
mencit (Mus musculus). Mencit dibagi secara acak menjadi 5 kelompok. Tiap kelompok terdiri dari 5 ekor jantan dan 5 ekor betina. Kelompok I – IV diberikan sediaan Heparmin® yang telah dilarutkan dengan air suling secara oral kepada mencit, dengan dosis yang bervariasi yaitu 2,5g/kgBB, 5g/kgBB, 10g/kgBB dan 20g/kgBB, sedangkan kelompok V adalah kelompok kontrol hanya diberikan air suling. Berdasarkan penelitian menunjukkan Heparmin® praktis tidak toksik dengan LD50 semu > 20g/kgBB.
Kata kunci: Heparmin, LD50
Abstract
Test studies have been conducted Lethal Dose 50% (LD50) of Poliherbal (Curcuma Xanthorriza,
Kleinhovia hospita, Nigella sativa, Arcangelisia flava and Ophiocephalus striatus) on
Heparmin® in mice (Mus musculus). The study was conducted using mice (Mus musculus). Mice
were divided randomly into 5 groups. Each group consisted of 5 males and 5 females. Group I - IV given Heparmin ® that has been diluted with distilled water orally to mice, with varying doses of 2.5 g / kg, 5g/kgBB, 10g/kgBB and 20g/kgBB, while the V group was a control group given only distilled water. Based on research showing Heparmin® practically non-toxic with LD50> 20g/kgBB.
2 BAB I PENDAHULUAN I.1 Latar Belakang
Heparmin® merupakan sediaan jamu dalam bentuk kapsul yang mengandung ekstrak rimpang temulawak (Curcuma xanthorriza), daun paliasa (Kleinhovia hospita), jintan hitam (Nigella sativa), kayu kuning (Arcangelisia flava) dan ikan gabus (Ophiocephalus striatus). Kelebihan Heparmin® yaitu dari kandungannya yang terdiri dari 100% bahan alam, aman dan efektif menurunkan SGOT dan SGPT, sebagai hepatoprotektor, antiinflamasi, antioksidan dan antivirus. Pengamatan hasil laboratorium terhadap pasien yang diberi sediaan heparmin menunjukkan penurunan kadar SGOT dan SGPT pada pasien hepatitis (Mansur: 2009).
Untuk mengetahui keamanan penggunaan heparmin, maka diperlukan uji toksisitas. Uji toksisitas dibedakan menjadi uji toksisitas akut, subkronik, dan kronik. Uji toksisitas akut dimaksudkan untuk mendapatkan informasi tentang gejala keracunan, penyebab kematian, urutan proses kematian dan rentang dosis yang mematikan hewan uji (Lethal dose 50% atau disingkat LD50) suatu bahan (Ngatidjan,1997). Parameter toksisitas akut yang digunakan untuk
melihat keamanan Heparmin dalam pengobatan adalah nilai LD50.
Uji toksisitas akut sangat penting untuk mengukur dan mengevaluasi karakteristik toksik dari suatu bahan kimia. Uji ini dapat menyediakan informasi tentang bahaya kesehatan manusia yang berasal dari bahan kimia yang terpapar dalam tubuh pada waktu pendek melalui jalur oral. Data uji akut juga dapat menjadi dasar klasifikasi dan pelabelan suatu bahan kimia.
Dalam penelitian ini dilakukan uji LD50. Penelitian ini bertujuan untuk mendeteksi efek
toksik akut sehingga dapat diperoleh gambaran keamanan sediaan Heparmin®
I.2 Tujuan Penelitian
Tujuan dari penelitian ini adalah mengetahui nilai LD50 dari sediaan Heparmin® pada
3 BAB II
TINJAUAN PUSTAKA
II.1 Heparmin®
Heparmin® merupakan produk yang dibuat dari ekstrak bahan alam yang mengandung ekstrak rimpang temulawak (Curcuma xanthorriza), daun paliasa (Kleinhovia hospita), jintan hitam (Nigella sativa), kayu kuning (Arcangelisia flava) dan ikan gabus (Ophiocephalus
striatus). Kurcuminoid yang terdapat pada Curcuma xanthorriza mempunyai efek biologis
sebagai hepatoprotektor, anti bakteri dan antiinflamasi. Nigella sativa yang kandungan utamanya tymoquinon mempunyai efek sebagai hepatoprotektor, antioksidan, antimikroba dan antivirus.
Ophiocephalus striatus dengan kandungan utama protein, asam amino, vitamin dan Ig yang
sangat dibutuhkan oleh tubuh sebagai sumber energy, proses metabolism, regenerasi sel-sel tubuh yang rusak dan meningkatkan system pertahanan tubuh. Kandungan flavonoid dan saponin yang terdapat pada Kleinhovia hospital dan Arcangelisia flava telah terbukti sebagai antioksidan, hepatoprotektor, dan antimikroba.
Penelitian LD50 infus daun kayu paliasa (Kleinhovia hospita Linn.) yang diberikan secara oral pada binatang percobaan dengan menggunakan 80 ekor binatang percobaan yang dibagi dalam 8 kelompok terdiri dari 10 ekor mencit yaitu 5 ekor jantan dan 5 ekor betina. Tiap binatang percobaan diberi infius daun kayu paliasa 1 mL/25 g bb. Untuk kelompok 1 dengan dosis 8 g/kg bb., kelompok 2 dengan dosis 14g/kg bb, kelompok 3 dengan dosis 16 g/kg bb, kelompok 4 dengan dosis 20 g/kg bb, kelornpok 5 dengan dosis 24 g/kg bb, kelompok 6 dengan dosis 28 g/kg bb.. kelompok 7 dengan dosis 32 g/kg bb dan untuk kelompok 8 diberi air suling sebagai kontrol. Berdasarkan hasil perhitungan dengan metode analisis probil dan uji ketelilian secara stalistik diperoleh nilai LD50 infus daun paliasa sebesar 18,5 ± 1.70 g/kg BB (Tahir:
1993).
Studi pada beberapa hewan coba, dosis kurkumin 100 – 200 mg/kg BB menunjukkan adanya aktifitas antiinflamasi. Pada dosis yang sama tidak menimbulkan efek samping yang nyata pada system organ manusia. LD50 pada mencit lebih dari 2,0 g/kg BB (Itokawa, dkk:
2008). Dari data potensi ketoksikan akut (LD50) temu lawak terlihat bahwa sampai dengan hari
4
tidak ditemukan adanya tikus jantan maupun betina yang mati (% respons = 0). Berdasarkan atas data kualitatif dan kuantitatif yang dikumpulkan, serta analisis dan evaluasi hasil yang diterapkan maka potensi ketoksikan akutoral suspensi ekstrak kurkuminoid rimpang kunyit dan minyak atsiri rimpang temulawak pada tikus jantan maupun betina, termasuk kategori minimal praktis tidak toksik yaitu antara 5 – 15 g/kg BB (Loomis, 1978) ; LD50 semu > 6400 mg/kg BB (Kertia
dkk: 2005).
Dari hasi uji toksisitas atau tingkat keracunan akut terhadap mencit atau tikus putih
Arcangelisia flava diketahui bahwa ekstrak air menunjukkan pada dosis 1.122 mg/100g mampu
mematikan 50% dari jumlah mencit yang ada (LD50 1.122 mg/100g) dengan kisaran 638-1.972
mg/100 g, sedangkan toksisitas ekstrak etanol hanya setengahnya (Indonesian Biotecnology Information Centre:2004). Ekstrak methanol 70% dari Arcangelisia flava ini memiliki LD50
36680 mg/kg berat badan tikus percobaan (Sa’roni:1996) yang dapat diartikan bahwa ekstrak ini tidak bersifat toksik (Gleason: 1969). Hasil penelitian lain menunjukkan bahwa dengan pemberian rebusan kayu kuning konsentrasi 1% b/v tidak ada binatang percobaan mencit yang mati sedang pada konsentrasi 70 % dan 80 % b/v semua binatang percobaan mencit mati.Dengan menggunakan perhitungan metoda grafik, diperoleh kesimpulan bahwa LD50 rebusan kayu kuning sebesar 31,82% b/v/25 g BB. atau 12,65 g/kgBB (Wahab:1986).
Penelusuran toksisitas dengan menentuan LD50 pada komponen biji Nigella sativa
(yaitu ekstrak air, minyak lemak, minyak atsiri) dan komponen utama dari minyak atsiri (yaitu
thymoquinon, α-pinene) menunjukkan nilai LD50 dari semua komponen Nigella sativa dianggap
memiliki toksisitas sedang ( jarak LD50 adalah 616,6 – 3317 mg/kg) kecuali thymoquinon yang sangat toksik (LD50 =90,3 mg/kg) (El-Hadiyah dkk:2003).
II.2 Lethal Dose 50% (LD50)
Toksisitas akut didefinisikan sebagai kejadian keracunan akibat pemaparan bahan toksik dalam waktu singkat, yang biasanya dihitung dengan menggunakan nilai LC50 atau LD50.
Nilai ini didapatkan melalui proses statistik dan berfungsi mengukur angka relatif toksisitas akut bahan kimia. Toksisitas akut dari bahan kimia lingkungan dapat ditetapkan secara eksperimen menggunakan spesies tertentu seperti mamalia, bangsa unggas, ikan, hewan invertebrata,
5
tumbuhan vaskuler dan alga. Uji toksisitas akut dapat menggunakan beberapa hewan mamalia, namun yang dianjurkan untuk uji LD50 diantaranya tikus, mencit dan kelinci.
Uji LD50 adalah suatu pengujian untuk menetapkan potensi toksisitas akut LD50,
menilai berbagai gejala toksik, spektrum efek toksik, dan mekanisme kematian. Tujuan Uji LD50 adalah untuk mendeteksi adanya toksisitas suatu zat, menentukan organ sasaran dan kepekaannya, memperoleh data bahayanya setelah pemberian suatu senyawa secara akut dan untuk memperoleh informasi awal yang dapat digunakan untuk menetapkan tingkat dosis yang diperlukan.
Uji toksisitas akut dapat dipengaruhi oleh respon biologik hewan uji seperti jenis kelamin. Contoh respon tubuh akibat jenis kelamin yaitu nilai LD50 digoxin yang diuji pada tikus
jantan diperoleh angka 56 mg/kg bb, sementara untuk tikus betina 94 mg/kg bb (Buck, dkk. 1976). Penggunaaan jenis kelamin hewan dalam penelitian uji toksisitas bervariasi. Anonimus (1998) merekomendasikan hewan sejenis, namun beberapa menganjurkan penggunaan hewan jantan dan betina. Hewan uji (mencit dan tikus) yang digunakan dalam uji toksisitas direkomendasikan umur 8-12 minggu sementara untuk kelinci 12 minggu. Pada prinsipnya, penelitian uji toksisitas akut bertujuan untuk mengetahui dosis relatif toksisitas akut terhadap produk obat herbal.
Materi hewan coba yang digunakan dalam penelitian umumnya cukup 14 ekor mencit galur Swiss, jenis kelamin jantan dan betina, umur 3 bulan dengan berat rata-rata 25-30 gram. Mencit bisa diperoleh dari unit layanan penjualan hewan coba seperti di Biofarma, Unit pra klinik LPPT, dll. Mencit dikandangkan menggunakan fasilitas kandang yang memenuhi syarat dengan suhu pemeliharaan 26 ± 1 0C, dan kelembaban 65 ± 5 %. Mencit sebelum diberi perlakuan diadaptasikan dahulu terhadap kondisi penelitian selama 1 minggu. Pakan mencit diharapkan standar berbentuk pellet misalnya jenis Extra Fortuna (Produksi PT. Multiphala Agrinusa) serta air minum diberikan pada mencit uji secara ad libitum.
Selanjutnya, membuat rancangan percobaan LD50 berdasarkan metode Weil (1952).
Maksud dari LD50 adalah dalam dosis dimana 50% dari populasi spesies tertentu mati. Untuk
menentukan LD50, terlebih dahulu dilakukan penelitian dengan menggunakan 2 ekor mencit pada
tiap kelompok (Al Sultan and Husein, 2006). Uji ini dimaksudkan untuk mendapatkan dosis antara di mana kedua mencit tidak mengalami kematian dan dosis yang mengakibatkan kedua
6
mencit mengalami kematian (Miya et al., 1976). Tahapan yang sesungguhnya, mencit dipuasakan makan sebelum diperlakukan namun tetap diberi minum selama 4 jam sebelum perlakuan dan 2 jam sesudah perlakuan. Selanjutnya sediaan produk bahan herbal diberikan secara oral dengan dosis tertentu misalnya 312,5; 625; 1250; 2500; 5000; dan 10000 mg/Kg BB. Untuk contoh pemberian dosis seperti diatas, hewan uji dibagi ke dalam 7 kelompok perlakuan sebagai berikut:
kelompok A: kontrol, diberi makan dan minum standar; oral;kelompok B sampai dengan G secara berturut-turut diberi dosis : 312,50 mg, 625 mg, 1250 mg, 2500 mg, 5000 mg dan 10000 mg/Kg BB/per oral.
Penentuan LD50 dilakukan dengan melihat data kematian mencit pada setiap kelompok
perlakuan mulai dosis 312,5 – 10000 mg/Kg BB selama 48 jam. Data kematian dari setiap kelompok diolah menjadi data kumulatif yang kemudian dijadikan persentase kematian. Hasil persentase kematian kemudian diolah menurut metode Reed-Muench dengan interpolasi linier untuk mendapat LD50 dan standar error (SE) (Miya et al: 1976). Sedangkan metode penetapan
sifat toksik dilakukan setelah perlakuan dengan bahan uji pada dosis tunggal, jumlah kematian hewan uji yang mati diamati selama 24 jam. Apabila diperlukan, pengamatan kematian hewan uji dapat diikuti sampai hari ke-15.
Untuk metode penetapan gejala klinis pada umumnya menimbulkan beberapa gejala klinis, di antaranya peningkatan aktifitas, peningkatan laju bernafas, mencit tampak meregangkan badan dan beristirahat di sudut kandang. Hal ini disebabkan karena kandungan bahan kimia dari produk herbal yang memiliki sifat toksik berat. Pada akhirnya mencit mulai menutup mata dan terlihat tenang, dan akhirnya mengalami kematian setelah periode kritis (3 jam).
Selain itu metode teknik etanasi yang digunakan adalah teknik dislokasi serviks (Inglis: 1980). Awalnya mencit dibiarkan dalam posisi lordosis, maksudnya dada membusung ke depan atau punggung berbentuk cekung, kemudian gunting diletakkan pada leher, ekor mencit ditarik ke atas, sehingga os serviks terlepas dari lokasinya. Sebelum dilakukan pembedahan, dilakukan pengamatan kembali terhadap denyut jantung dan nafas untuk memastikan hewan telah benar-benar mati.
7
Uji toksisitas akut dirancang untuk menentukan atau menunjukkan secara kasar median
lethal dose (LD50) dari toksikan. LD50 ditetapkan sebagai tanda statistik pada pemberian suatu
bahan sebagai dosis tunggal yang dapat menyebabkan kematian 50% hewan uji (Frank:1996). Jumlah kematian hewan uji dipakai sebagai ukuran untuk efek toksik suatu bahan (kimia) pada seke lompok hewan uji. Jika dalam hal ini hewan uji dipandang sebagai subjek, respon berupa kematian tersebut merupakan suatu respon diskretik. Ini berarti hanya ada dua macam respon yaitu ada atau tidak ada kematian (Ngatidjan:1997).
Quantal respon , yaitu jumlah respon pada sekelompok hewan uji terhadap dosis
tertentu suatu obat atau bahan. Pengamatan terhadap efek ini dilakukan untuk menentukan jumlah respon dari suatu respon diskretik (all or none response) pada suatu kelompok hewan uji. Jumlah respon tersebut dapat 100%, 99%, 50%, 20%, 10%, atau 1%. Respon yang bersifat diskret itu dapat berupa kematian, aksi potensial, dan sebagainya (Ngatidjan, 1997). Uji toksisitas akut ini biasanya menggunakan hewan uji mencit dari kedua jenis kelamin. Hewan uji harus sehat dan berasal dari satu galur yang jelas. Menurut Weil penelitian uji toksisitas akut ini paling tidak menggunakan 4 peringkat dosis yang masing-masing peringkat dosis menggunakan paling sedikit 4 hewan uji. Dosis dibuat sebagai suatu peringkat dengan kelipatan logaritmik yang tetap. Dosis terendah merupakan dosis yang tidak menyebabkan timbulnya efek atau gejala keracunan, dan dosis tertinggi merupakan dosis yang menyebabkan kematian semua (100%) hewan uji. Cara pemberian obat atau bahan yang diteliti harus disesuaikan pada pemberiannya pada manusia, sehingga dapat mempermudah dalam melakukan ekstrapolasi dari hewan ke manusia (Ngatidjan, 1997). Dalam uji toksisitas akut, penentuan LD50 dilakukan dengan cara
menghitung jumlah kematian hewan uji yang terjadi dalam 24 jam pertama sesudah pemberian dosis tunggal bahan yang diteliti menurut cara yang ditunjukkan oleh para ahli. Namun demikian, kematian dapat terjadi sesudah 24 jam pertama karena proses keracunan dapat berjalan lambat. Gejala keracunan yang muncul sesudah 24 jam menunjukkan bahwa bahan obat atau bahan itu mempunyai titik tangkap kerja pada tingkat yang lebih bawah sehingga gejala keracunan dan kematian seolah-olah tertunda (delayed toxicity). Oleh karena itu banyak ahli berpendapat bahwa gejala keracunan perlu diamati sampai 7 hari (Ngatidjan: 1997), bahkan juga sampai 2 minggu (Paget: 1970). Sediaan yang akan diuji dipersiapkan menurut cara yang sesuai dengan karakteristik bahan kimia tersebut, dan tidak diperbolehkan adanya perubahan selama
8
waktu pemberian. Untuk pemberian per oral ditentukan standar volume yang sesuai dengan hewan uji (Paget: 1970).
Metode Uji Toksisitas Akut
1. Cara aritmatik Reed dan Muench (1983)
Cara ini menggunakan harga kumulatif sebagai dasarnya. Harga kumulatif diperoleh dari asumsi bahwa hewan uji yang mati pada suatu dosis, tentu akan mati oleh dosis yang lebih besar, dan hewan uji yang tidak mati atau tetap hidup pada suatu dosis, tentu juga tidak akan mati oleh karena dosis yang lebih kecil. Angka kumulatif diperoleh dari menjumlahkan kematian hewan uji pada dosis terbesar yang menyebabkan kematian 100% hewan uji dengan jumlah hewan uji yang mati pada dosis dosis yang lebih kecil. Angka kumulatif survivor (hidup) diperoleh dari menjumlahkan hewan uji yang tetap hidup pada dosis terkecil yang tidak menyebabkan kematian (100% hewan uji tetap hidup) dengan jumlah hewan uji yang tetap hidup pada dosis-dosis diatasnya. Persentase survival pada dosis di bawah LD50 dengan LD50,
kemudian dibagi dengan selisih persentase survival pada dosis di atas dan di bawah LD50.
Proporsi jarak ini jika kemudian dikalikan dengan dengan Logaritme rasio di atas terhadap dosis di bawah LD50, didapat harga antilog LD50 (Ngatidjan:1997).
2. Cara aritmatik dari Karber (1931)
Pada cara ini interval rata-rata jumlah kematian pada tiap kelompok digunakan dalam perhitungan sebagaimana pada perbedaan dosis dari interval yang sama. LD50 diperoleh dari
selisih dosis terkecil yang menyebabkan seluruh kematian hewan uji dengan angka yang diperoleh dari pembagian hasil dengan jumlah hewan uji tiap kelompok (Ngatidjan:1997).
3. Cara C.S Weil (1952)
Dalam mencari harga LD50 diperlukan ketepatan atau jika dilihat dari taraf kepercayaan
tertentu, harga tersebut hanya sedikit sekali bergeser dari harga sebenarnya, atau berada pada rentang atau interval yang sempit. Untuk mencapai tujuan itu, Weil memanfaatkan tabel yang dibuat oleh Thompson dan Weil (1952). Pada penggunaan tabel itu, percobaan harus memenuhi beberapa syarat berikut:
1) Jumlah hewan uji tiap kelompok peringkat dosis sama.
9
3) Jumlah kelompok paling tidak 4 peringkat dosis. Jika umumnya digunakan K=3 maka jumlah kelompok harus paling tidak (K+1) peringkat dosis.
LD50 dapat dihitung dengan rumus : Log (LD50) = log Da + d.(f+1)
Da adalah dosis terendah, f adalah faktor yang diperoleh dari table Thompson dan Weil, dan d adalah logaritma kelipatan dosis (Ngatidjan:1997).
4. Cara Farmakope Indonesia
Menurut Farmakope Indonesia III penelitian toksisitas akut harus memenuhi syarat sebagai berikut:
1) Menggunakan seri dosis dengan pengenceran berkelipatan tetap.
2) Jumlah hewan percobaan atau jumlah biakan jaringan tiap kelompok harus sama. 3) Dosis diatur sedemikikan rupa, sehingga memberikan efek dari 0% sampai 100%. Nilai LD 50 dapat dihitung dengan rumus:
m = a – b (∑pi – 0,5 ) m = log LD50
a = logaritma dosis terendah yang masih menyebabkan kematian 100% tiap kelompok.
b = beda logaritma dosis yang berurutan.
pi = jumlah hewan yang mati yang menerima dosis i dibagi dengan jumlah hewan seluruhnya
yang menerima dosis i
Klasifikasi Zat Kimia Sesuai dengan Toksisitas Relatifnya (Frank: 1996)
Kategori LD50 (mg/kgBB)
Super toksik < 5
Amat sangat toksik 5-50
sangat toksik 50-500
Toksik sedang 500-5000
Toksik ringan 5000-15000
10 BAB III
METODE PENELITIAN
III.1Hewan Uji
Hewan yang digunakan berupa mencit (Mus musculus) jantan dan betina dewasa dengan bobot 20-30g. Hewan dipuasakan 4 jam sebelum perlakuan.
III.2 Bahan Uji
Bahan yang digunakan adalah sediaan heparmin® dan air suling III.3 Alat Uji
Alat yang digunakan adalah spoit 1 ml, jarum oral, timbangan analitik, botol 60 ml dan labu ukur 10 ml.
III.4 Prosedur Penelitian
Isi Kapsul heparmin® dikeluarkan dari cangkang kemudian ditimbang sesuai
perhitungan dosis kemudian dilarutkan dengan air suling. Bahan uji diberikan secara oral terhadap mencit yang dibagi menjadi 5 kelompok dosis, 4 kelompok uji dan 1 kelompok kontrol. Tiap kolompok terdiri dari 10 ekor mencit, masing-masing 5 ekor mencit jantan dan betina.
Sedian heparmin diberikan dengan dosis 2,5g/kgBB, 5g/kgBB, 10 g/kgBB, dan 20 g/kgBB, sedangkan kelompok kontrol hanya diberi larutan pembawa air suling. Semua diberikan dengan volume 1 ml per 30 g bobot badan. Sebelum diberikan bahan uji, mencit diamati perilakunya. Setelah pemberian, efek diamati pada menit ke-30, 60, dan 120. Efek yang diamati meliputi aktivitas motorik, fenomena straub, piloereksi, ptosis, midriasis, grooming, urinasi, defekasi dan salivasi. Data mencit yang mati diambil hingga 24 jam setelah pemberian sediaan. Mencit yang bertahan hidup diamati sampai hari ke-14.
11 BAB IV
HASIL DAN PEMBAHASAN
IV.1 Hasil Pengamatan A. Gejala Klinis
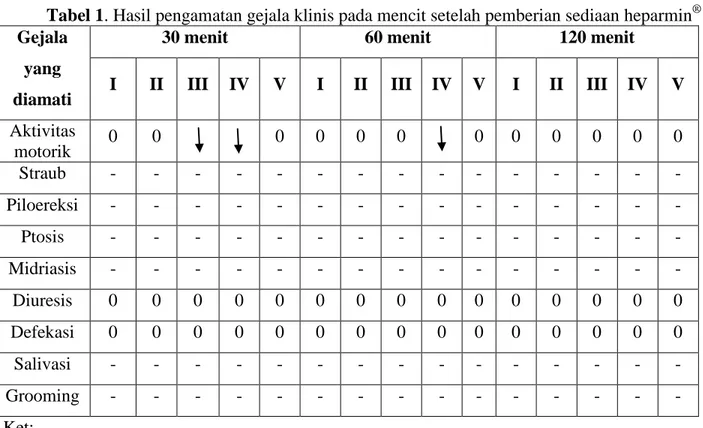
Tabel 1. Hasil pengamatan gejala klinis pada mencit setelah pemberian sediaan heparmin® Gejala
yang diamati
30 menit 60 menit 120 menit
I II III IV V I II III IV V I II III IV V Aktivitas motorik 0 0 0 0 0 0 0 0 0 0 0 0 Straub - - - - Piloereksi - - - - Ptosis - - - - Midriasis - - - - Diuresis 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 Defekasi 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 Salivasi - - - - Grooming - - - - Ket:
+ : ada aktivitas = meningkat
- : Tidak ada aktivitas = menurun
12 B. Mortalitas
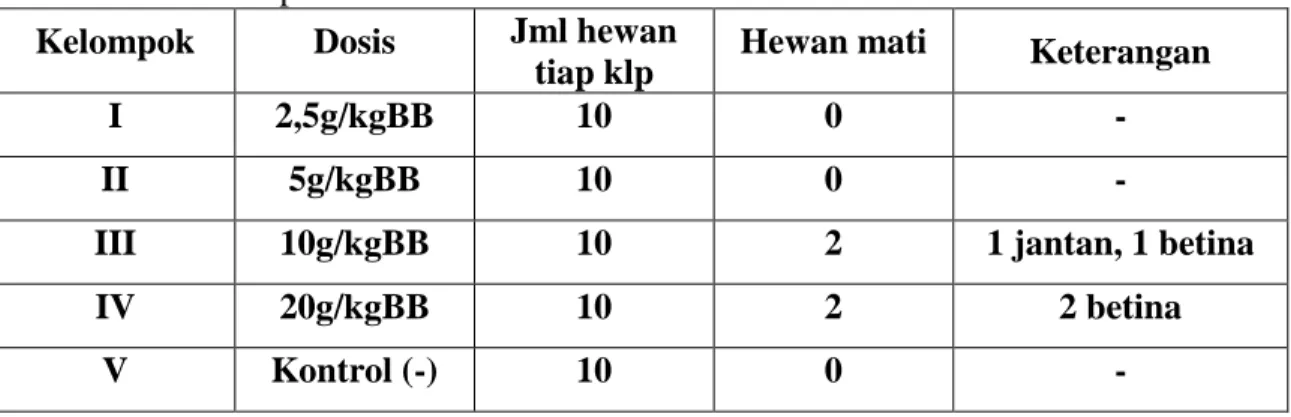
Tabel 2. Hasil pengamatan jumlah mencit yang mati setelah 24 jam pemberian sediaan heparmin®
Kelompok Dosis Jml hewan
tiap klp Hewan mati Keterangan
I 2,5g/kgBB 10 0 -
II 5g/kgBB 10 0 -
III 10g/kgBB 10 2 1 jantan, 1 betina
IV 20g/kgBB 10 2 2 betina
V Kontrol (-) 10 0 -
IV.2 Pembahasan
Uji LD50 terhadap sediaan heparmin dilakukan untuk mengetahui pada dosis berapa sediaan heparmin® dapat memberikan efek toksik. Efek tersebut ditandai dengan adanya kematian pada mencit yang telah diberikan sediaan heparmin®.
Pada pengamatan hewan coba setelah perlakuan didapatkan hasil bahwa tidak terdapat gejala-gejala toksik yang timbul setelah pemberian sediaan heparmin. Adanya penurunan aktivitas motorik pada kelompok III hanya terjadi 30 menit setelah perlakuan, sedangkan pada kelompok IV hingga 1 jam setelah serlakuan. Setelah itu aktivitas motorik semua mencit kembali normal (tabel 1).
Hasil pengamatan selama 24 jam perlakuan tidak menunjukkan adanya hewan coba yang mati melebihi 50% dari jumlah hewan pada tiap kelompok (10 ekor) baik pada kelompok kontrol maupun kelompok perlakuan (tabel 2). Hal ini menunjukkan bahwa pemberian dosis secara oral sediaan heparmin sampai dengan dosis maksimum yang masih dapat diberikan secara teknis pada hewan uji (20g/kgBB) atau sekitar 179 kali dosis yang lazim dipakai pada manusia, tidak menimbulkan kematian pada hewan coba. Dosis tertinggi tersebut dinyatakan sebagai LD50
semu. Berdasarkan kriteria Frank (1996), hasil tersebut mempunyai makna toksikologi bahwa potensi ketoksikan akut sediaan heparmin® termasuk dalam kategori praktis tidak toksik (>15000mg).
Hasil pada kelompok III dan IV dapat diabaikan karena hanya terjadi pada dua ekor mencit (tidak mencapai 50%), yang mungkin disebabkan oleh faktor lain diluar efek yang
13
disebabkan oleh sediaan heparmin. Kematian tersebut dapat disebabkan adanya kesalahan pada saat pemberian sediaan.
Berdasarkan hasil tersebut dapat diketahui bahwa pemberiaan kombinasi (poliherbal)
Curcuma xanthorriza, Kleinhovia hospita, Nigella sativa, Arcangelisia flava dan Ophiocephalus striatus tidak menyebabkan peningkatkan toksisitas (LD50) dari masing-masing komposisi
14 BAB V PENUTUP V.1 Kesimpulan
Berdasarkan hasil penelitian diperoleh kesimpulan bahwa Sediaan heparmin® adalah sediaan yang praktis tidak toksik karena memiliki LD50 diatas 15g/kgBB (LD50 semu >
20g/kgBB).
V.2 Saran
Saran untuk penelitian selanjutnya adalah dilakukan penelitian tentang uji efektifitas sediaan heparmin® sebagai hepatoterapi dan hepatoprotektor.
15
DAFTAR PUSTAKA
Mansur. Studi Kasus Penggunaan Multi Herbal Terhadap Penurunan SGPT dan SGOT. Royal Medicalink Pharmalab. Makassar. 2009
Angelina M, dkk. Penentuan LD50 Daun Cinco (Cyclea barbata Miers.) pada Mencit. Makara,
Sains, Volume 12, No. 1, April 2008: 23-26
Soemardji A, dkk. Toksisitas Akut dan Penentuan DL50 Oral Ekstrak Air Daun Gandarusa (Justicia gendarussa Burm. F.) pada Mencit Swiss Webster. Jurnal Matematika dan Sains
Vol. 7 No. 2, Oktober 2002, hal 57 – 62
Tahir M. Penentuan LD50 infus daun kayu paliasa (Kleinhovia hospita Linn.) pada binatang
percobaan mencit. FMIPA Unhas. 1993
Itokawa H.,dkk. Recent advances in the investigation of curcuminoids. Natural Products Research Laboratories, School of Pharmacy, University of North Carolina . 2008
Agusta A., dkk. Komponen Kimia Fraksi Nonpolar Arcangelisia flava. Majalah Farmasi Indonesia. 1996
El-Hadiyah dkk. Evaluation of Nigella sativa seed constituents for their invivo Toxicity in Mice. Department of Pharmacology, College of Pharmacy King Saud Uviversity. 2003
Haramain W. Penentuan LD,0 rebusan kayu kuning (Arcangelisia flava (L.) Merr. pada binatang percobaan mencit. Jurusan Farmasi Unhas. 1986
16 LAMPIRAN
Perhitungan dosis hewan coba
Bobot standar mencit = 20 g
Mencit terberat = 30 g
Dosis mencit (Klp I) = 2,5 g/kgBB = 75 mg/30 g
Untuk 10 ekor = 750 mg ad 10 ml air suling ambil 1 ml (diberikan pada tiap mencit klp I)
Dosis mencit Klp II = 5 g/kgBB = 150 mg/30 g
Untuk 10 ekor = 1500 mg ad 10 ml air suling ambil 1 ml (diberikan pada tiap mencit Klp II)
Dosis mencit Klp III = 10 g/kgBB = 300 mg/30 g
Untuk 10 ekor = 3000 mg ad 10 ml air suling ambil 1 ml (diberikan pada tiap mencit Klp III)
Dosis mencit Klp IV = 20 g/kgBB = 600 mg/30 g
Untuk 10 ekor = 6000 mg ad 10 ml air suling ambil 1 ml (diberikan pada tiap mencit Klp IV)
17 Volume Pemberian
Volume pemberian = bobot mencit perlakuan/bobot mencit terberat x 1 ml
Untuk mencit 20 g = 20g/30g x 1ml = 0,66 ml Untuk mencit 21 g = 21g/30g x 1ml = 0,7 ml Untuk mencit 22 g = 22g/30g x 1ml = 0,73 ml Untuk mencit 23 g = 23g/30g x 1ml = 0,76 ml Untuk mencit 24 g = 24g/30g x 1ml = 0,8 ml Untuk mencit 25 g = 25g/30g x 1ml = 0,83 ml Untuk mencit 26 g = 26g/30g x 1ml = 0,86 ml Untuk mencit 27 g = 27g/30g x 1ml = 0,9 ml Untuk mencit 28 g = 28g/30g x 1ml = 0,93 ml Untuk mencit 29 g = 29g/30g x 1ml = 0,96 ml Untuk mencit 30 g = 30g/30g x 1ml = 1,0 ml
18 Skema Kerja
Sedian Heparmin® Kapsul
Larutkan dengan air suling hingga 10 ml
Mencit 10 ekor tiap kelompok
Keluarkan isi kapsul, Timbang Timbang, Puasakan 4 jam 2,5g/kgBB 5g/kgBB 10g/kgBB 20g/kgBB Kontrol (-) KLP I KLP II KLP III KLP IV KLP V Data Gejala klinis (30’,60’120’) Kematian (24 jam) LD50 Kesimpulan
19 Komposisi Heparmin®
Tiap kapsul mengandung ekstrak:
Kleinhovia hospital 100 mg
Curcuma xanthoriza 75 mg
Nigella sativa 100 mg
Arcangelisia flava 50 mg
Ophiocephalus striatus 100 mg
Bahan tambahan hingga 650 mg
LD50 Komposisi Heparmin®
Kleinhovia hospital 18,5 g/kgBB (Tahir:1993)
Curcuma xanthoriza 2 g/kgBB (Itokawa:1998)
Nigella sativa 616,6 mg/kgBB (El-Hadiyah dkk:2003)
Arcangelisia flava 12,65 g/kgBB (Haramain:1986)