UJI TOKSISITAS SUBKRONIK EKSTRAK ETANOL
BUNGA PEPAYA JANTAN (
Carica papaya
L
.)
PADA MENCIT JANTAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
AGUNG SETIAWAN
NIM 091501051
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI TOKSISITAS SUBKRONIK EKSTRAK ETANOL
BUNGA PEPAYA JANTAN (
Carica papaya
L
.)
PADA MENCIT JANTAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
AGUNG SETIAWAN
NIM 091501051
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI TOKSISITAS SUBKRONIK EKSTRAK ETANOL
BUNGA PEPAYA JANTAN (
Carica papaya
L
.)
PADA MENCIT JANTAN
OLEH:AGUNG SETIAWAN NIM 091501051
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 15 Juli 2014
Pembimbing I, Panitia Penguji,
Dr. Edy Suwarso, S.U., Apt. Prof. Dr. Urip Harahap, Apt.
NIP 130953857 NIP 195301011983031004
Pembimbing II, Dr. Edy Suwarso, S.U., Apt. NIP 130953857
Dr. Marline Nainggolan, M.S., Apt. Dr. Poppy Anjelisa Z. Hsb, S.Si., M.Si., Apt. NIP 195709091985112001 NIP 197506102005012003
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan
karunia kepada penulis sehingga dapat menyelesaikan penyusunan skripsi yang
berjudul Uji Toksisitas Subkronik Ekstrak Etanol Bunga Pepaya Jantan (Carica
papaya L.) Pada Mencit Jantan. Skripsi ini diajukan untuk melengkapi salah satu
syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas
Sumatera Utara.
Pada kesempatan ini, dengan segala kerendahan hati penulis mengucapkan
terima kasih kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan
Fakultas Farmasi yang telah menyediakan fasilitas kepada penulis selama
perkuliahan di Fakultas Farmasi. Penulis juga mengucapkan terima kasih kepada
Bapak Dr. Edy Suwarso, S.U., Apt., dan Ibu Dr. Marline Nainggolan, M.S., Apt.,
yang telah membimbing penulis dengan penuh kesabaran, memberikan petunjuk
dan saran-saran selama penelitian hingga selesainya skripsi ini. Ucapan terima
kasih juga penulis sampaikan kepada Bapak Prof. Dr. Urip Harahap, Apt., selaku
ketua penguji juga kepada Ibu Dr
telah memberikan saran untuk menyempurnakan skripsi ini, dan I
membimbing penulis selama masa perkuliahan hingga selesai.
Penulis mengucapkan terima kasih yang tak terhingga kepada keluarga
tercinta, Ayahanda Alm. Muhammad Rusli dan Ibunda Tukarni, serta kakanda
dan abangda tercinta Teti Irawati, Dewi Utari, Dedi Ahmad Fauzi, Sri Ayu Rizky
kasih sayang yang tak ternilai dengan apapun. Penulis juga mengucapkan terima
kasih kepada Geje, Sulek, Makmor, Halem, Nurol, Iwen, Panjang, Sus, Ceripel,
dan semua teman-teman masinis 2009 yang telah mendoakan, membantu dan
memberi semangat.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum
sempurna. Oleh karena itu, penulis mengharapkan saran dan kritik yang
membangun demi kesempurnaan skripsi ini. Semoga Allah membalas segala budi
baik dan penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan
khususnya di bidang farmasi.
Medan, 15 Juli 2014 Penulis,
Uji Toksisitas Subkronik Ekstrak Etanol Bunga Pepaya Jantan (Carica papaya L.) Pada Mencit Jantan
Abstrak
Uji toksisitas subkronik merupakan suatu pengujian untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji dengan dosis berulang yang diberikan secara oral pada hewan uji selama 28 atau 90 hari. Bunga pepaya jantan (Carica papaya L.) termasuk famili Caricaceae, ekstrak etanolnya berkhasiat sebagai antimutagenik, antioksidan, antibakteri dan antikanker payudara. Tujuan dari penelitian ini adalah mengetahui efek toksik dan mengetahui batas keamanan dosis ekstrak etanol bunga pepaya jantan (EEBPJ).
Serbuk simplisia dimaserasi dengan pelarut etanol 80% kemudian diuapkan dengan rotary evaporator ± 40oC dandi freeze dryer ± -40oC selanjutnya ekstrak yang diperoleh diuji toksisitas subkroniknya menggunakan mencit sebanyak 25 ekor dibagi dalam 5 kelompok yaitu kontrol diberi akuades, perlakuan diberi EEBPJ dosis 1000, 2000, 4000 dan 8000 mg/kg bb yang diberi secara oral setiap hari selama 28 hari. Pengamatan dilakukan setiap hari meliputi gejala toksik, berat badan, kematian, pengukuran kadar ALT, makropatologi dan histopatologi organ hati, kemudian dianalisis statistik dengan ANOVA menggunakan Statistical Program Service Solution (SPSS) versi 19.
Hasil pengamatan tidak ditemukan gejala toksik pada kelompok kontrol, EEBPJ dosis 1000 dan 2000 mg/kg bb sedang dosis 4000 dan 8000 mg/kg bb ditemukan gejala toksik. Hasil uji statistik tidak ada perbedaan yang signifikan antara kenaikan berat badan dengan pemberian EEBPJ (p > 0,05). Mencit yang mati pada kelompok kontrol, dosis 1000 dan 2000 mg/kg bb tidak ada dijumpai sedang dosis 4000 dan 8000 mg/kg bb dijumpai. Hasil rata-rata kadar ALT terdapat perbedaan yang signifikan antara kelompok perlakuan (p < 0,05) yaitu kontrol (35,20 IU/L), EEBPJ dosis 1000 mg/kg bb (56,40 IU/L), dosis 2000 mg/kg bb (70,80 IU/L), rata-rata kadar ALT ketiga kelompok tersebut masih dalam batas normal, sedang dosis 4000 mg/kg bb (88,50 IU/L), dosis 8000 mg/kg bb (97,00 IU/L) sudah di atas batas normal. Hasil makropatologi dan histopatologi organ hati pada kelompok kontrol, EEBPJ dosis 1000 dan 2000 mg/kg bb tidak dijumpai perubahan sedang dosis 4000 dan 8000 mg/kg bb dijumpai perubahan organ, yang berarti EEBPJ toksik pada dosis 4000 dan 8000 mg/kg bb.
Subchronic Toxicity Test Ethanol Extract Of Male Papaya Flowers (Carica papaya L.) On Male Mice
Abstract
Subchronic toxicity test is a test to detect the toxic effects that appear after administration of the test preparation with repeated doses which are given orally to test animals for 28 or 90 days. Male papaya flowers (Carica papaya L.) is included in Caricaceae family which its ethanol extract can be used as antimutagenic, antioxidant, antibacterial and breast anticancer. The purpose of this study is to determine the toxic effects and safety range dose ethanol extract of male papaya flowers (EEBPJ).
Simplex powder was macerated by ethanol 80% and evaporated by using rotary evaporator ± 40oC and freeze dried ± -40oC then obtained extract was tested for its subchronic toxicity using 25 mice which were divided into 5 groups: control group was given distilled water, the treatment groups which were given with EEBPJ dose 1000, 2000, 4000 and 8000 mg/kg bw which were administered orally everyday for 28 days. Observations were conducted everyday including toxic symptoms, weight loss, death, measurement of ALT level, macropathology and histopathology of liver then data were analyzed by ANOVA using the Statistical Program Service Solution (SPSS) version 19.
The results showed that there were no toxic symptoms in the control group, EEBPJ dose 1000 and 2000 mg/kg bw, while EEBPJ dose 4000 and 8000 mg/kg bw showed toxic symptoms. Result of statistic showed no significant difference in weight gain within treatment groups given with EEBPJ (p > 0.05). Death mice in the control group, EEBPJ dose 1000 and 2000 mg/kg bw didnt show, while EEBPJ dose 4000 and 8000 mg/kg bw showed. Result of ALT level showed significant differences within all groups (p < 0.05), which were control group (35.20 IU/L), EEBPJ dose 1000 mg/kg bw (56.40 IU/L), EEBPJ dose 2000 mg/kg bw (70.80 IU/L), ALT level of these three groups were still in the normal state, whereas ALT level in treatment groups given EEBPJ dose 4000 mg/kg bw (88.50 IU/L) and EEBPJ dose 8000 mg/kg bw (97.00 IU/L) exceeds the upper limit of normal state. Macropathology and histopathology of liver result in the control group and treatment groups given with EEBPJ dose 1000 and 2000 mg/kg bw showed no changed while EEBPJ dose 4000 and 8000 mg/kg bw showed changed organ, which mean EEBPJ were toxic at dose 4000 and 8000 mg/kg bw.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
1.6 Kerangka Pikir Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Sistematika tumbuhan ... 5
2.1.2 Morfologi tumbuhan ... 5
2.1.3 Nama daerah ... 6
2.1.4 Kandungan kimia ... 7
2.2 Ekstraksi ... 7
2.3 Toksisitas ... 9
2.3.1 Toksisitas umum ... 10
2.3.1.1 Toksisitas akut ... 10
2.3.1.2 Toksisitas subkronik ... 10
2.3.1.3 Toksisitas kronik ... 11
2.3.2 Toksisitas khusus ... 11
2.3.2.1 Uji teratogenik ... 11
2.3.2.2 Uji mutagenik ... 12
2.3.2.3 Uji karsinogenik ... 12
2.4 Hati ... 12
2.4.1 Anatomi hati ... 13
2.4.2 Fisiologi hati ... 13
2.4.3 Histologi hati ... 14
2.4.4 Intoksikasi hati ... 15
2.5 ALT (Alanin Aminotransferase) ... 16
BAB III METODE PENELITIAN ... 18
3.1 Alat dan Bahan ... 18
3.1.1 Alat ... 18
3.1.2 Bahan ... 18
3.2 Hewan Percobaan ... 18
3.3 Penyiapan Sampel ... 19
3.3.1 Pengumpulan tumbuhan ... 19
3.3.2 Identifikasi tumbuhan ... 19
3.4 Pembuatan Ekstrak Etanol Bunga Pepaya Jantan ... 19
3.5 Pengujian Efek Toksistas ... 20
3.5.1 Pembuatan sediaan uji ekstrak etanol bunga pepaya jantan ... 20
3.5.2 Uji pendahuluan ... 20
3.5.3 Pengujian toksisitas subkronik ... 20
3.5.4 Pengamatan ... 21
3.5.4.1 Gejala toksik ... 21
3.5.4.2 Berat badan ... 21
3.5.4.3 Kematian hewan ... 21
3.5.4.4 Pengukuran kadar ALT ... 22
3.5.4.5 Makropatologi ... 22
3.5.4.6 Histopatologi organ hati ... 22
3.5.5 Analisis statistik ... 22
BAB IV HASIL DAN PEMBAHASAN ... 23
4.1 Hasil Identifikasi Tumbuhan ... 23
4.2 Hasil Ekstraksi Serbuk Bunga Pepaya Jantan ... 23
4.3 Hasil Uji Pendahuluan ... 23
4.4 Hasil Pengujian Toksisitas Subkronik ... 23
4.4.1 Hasil pengamatan gejala toksik ... 24
4.4.2 Hasil pengamatan berat badan ... 25
4.4.3 Hasil pengamatan kematian ... 26
4.4.4 Hasil pengukuran kadar ALT ... 27
4.4.5 Hasil pengamatan makropatologi ... 28
BAB V KESIMPULAN DAN SARAN ... 37
5.1 Kesimpulan ... 37
5.2 Saran ... 37
DAFTAR PUSTAKA ... 38
DAFTAR TABEL
Tabel Halaman
4.1 Hasil pengamatan gejala toksik ... 24
4.2 Hasil rata-rata berat badan ... 25
4.3 Hasil pengamatan kematian ... 26
4.4 Hasil pengamatan makropatologi ... 28
DAFTAR GAMBAR
Gambar Halaman
1.1 Kerangka pikir penelitian ... 4
2.1 Anatomi hati ... 13
2.2 Histologi hati ... 14
4.1 Grafik rata-rata hasil pengukuran kadar ALT ... 27
DAFTAR LAMPIRAN
Lampiran Halaman
1 Hasil identifikasi tumbuhan ... 43
2 Gambar tumbuhan bunga pepaya jantan ... 44
3 Simplisia dan serbuk bunga pepaya jantan ... 45
4 Bagan pembuatan ekstrak ….. ... 46
5 Bagan alur penelitian uji toksisitas subkronik ... 47
6 Contoh perhitungan dosis ... 48
7 Hasil uji pendahuluan ... 49
8 Hasil pengukuran kadar ALT ... 50
9 Hasil rata-rata kadar ALT ... 51
10 Hasil gambar makropatologi organ hati ... 52
11 Gambar alat, bahan dan objek yang digunakan ... 54
12 Gambar hewan percobaan yang digunakan ... 56
13 Hasil analisis spss berat badan ... 57
Uji Toksisitas Subkronik Ekstrak Etanol Bunga Pepaya Jantan (Carica papaya L.) Pada Mencit Jantan
Abstrak
Uji toksisitas subkronik merupakan suatu pengujian untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji dengan dosis berulang yang diberikan secara oral pada hewan uji selama 28 atau 90 hari. Bunga pepaya jantan (Carica papaya L.) termasuk famili Caricaceae, ekstrak etanolnya berkhasiat sebagai antimutagenik, antioksidan, antibakteri dan antikanker payudara. Tujuan dari penelitian ini adalah mengetahui efek toksik dan mengetahui batas keamanan dosis ekstrak etanol bunga pepaya jantan (EEBPJ).
Serbuk simplisia dimaserasi dengan pelarut etanol 80% kemudian diuapkan dengan rotary evaporator ± 40oC dandi freeze dryer ± -40oC selanjutnya ekstrak yang diperoleh diuji toksisitas subkroniknya menggunakan mencit sebanyak 25 ekor dibagi dalam 5 kelompok yaitu kontrol diberi akuades, perlakuan diberi EEBPJ dosis 1000, 2000, 4000 dan 8000 mg/kg bb yang diberi secara oral setiap hari selama 28 hari. Pengamatan dilakukan setiap hari meliputi gejala toksik, berat badan, kematian, pengukuran kadar ALT, makropatologi dan histopatologi organ hati, kemudian dianalisis statistik dengan ANOVA menggunakan Statistical Program Service Solution (SPSS) versi 19.
Hasil pengamatan tidak ditemukan gejala toksik pada kelompok kontrol, EEBPJ dosis 1000 dan 2000 mg/kg bb sedang dosis 4000 dan 8000 mg/kg bb ditemukan gejala toksik. Hasil uji statistik tidak ada perbedaan yang signifikan antara kenaikan berat badan dengan pemberian EEBPJ (p > 0,05). Mencit yang mati pada kelompok kontrol, dosis 1000 dan 2000 mg/kg bb tidak ada dijumpai sedang dosis 4000 dan 8000 mg/kg bb dijumpai. Hasil rata-rata kadar ALT terdapat perbedaan yang signifikan antara kelompok perlakuan (p < 0,05) yaitu kontrol (35,20 IU/L), EEBPJ dosis 1000 mg/kg bb (56,40 IU/L), dosis 2000 mg/kg bb (70,80 IU/L), rata-rata kadar ALT ketiga kelompok tersebut masih dalam batas normal, sedang dosis 4000 mg/kg bb (88,50 IU/L), dosis 8000 mg/kg bb (97,00 IU/L) sudah di atas batas normal. Hasil makropatologi dan histopatologi organ hati pada kelompok kontrol, EEBPJ dosis 1000 dan 2000 mg/kg bb tidak dijumpai perubahan sedang dosis 4000 dan 8000 mg/kg bb dijumpai perubahan organ, yang berarti EEBPJ toksik pada dosis 4000 dan 8000 mg/kg bb.
Subchronic Toxicity Test Ethanol Extract Of Male Papaya Flowers (Carica papaya L.) On Male Mice
Abstract
Subchronic toxicity test is a test to detect the toxic effects that appear after administration of the test preparation with repeated doses which are given orally to test animals for 28 or 90 days. Male papaya flowers (Carica papaya L.) is included in Caricaceae family which its ethanol extract can be used as antimutagenic, antioxidant, antibacterial and breast anticancer. The purpose of this study is to determine the toxic effects and safety range dose ethanol extract of male papaya flowers (EEBPJ).
Simplex powder was macerated by ethanol 80% and evaporated by using rotary evaporator ± 40oC and freeze dried ± -40oC then obtained extract was tested for its subchronic toxicity using 25 mice which were divided into 5 groups: control group was given distilled water, the treatment groups which were given with EEBPJ dose 1000, 2000, 4000 and 8000 mg/kg bw which were administered orally everyday for 28 days. Observations were conducted everyday including toxic symptoms, weight loss, death, measurement of ALT level, macropathology and histopathology of liver then data were analyzed by ANOVA using the Statistical Program Service Solution (SPSS) version 19.
The results showed that there were no toxic symptoms in the control group, EEBPJ dose 1000 and 2000 mg/kg bw, while EEBPJ dose 4000 and 8000 mg/kg bw showed toxic symptoms. Result of statistic showed no significant difference in weight gain within treatment groups given with EEBPJ (p > 0.05). Death mice in the control group, EEBPJ dose 1000 and 2000 mg/kg bw didnt show, while EEBPJ dose 4000 and 8000 mg/kg bw showed. Result of ALT level showed significant differences within all groups (p < 0.05), which were control group (35.20 IU/L), EEBPJ dose 1000 mg/kg bw (56.40 IU/L), EEBPJ dose 2000 mg/kg bw (70.80 IU/L), ALT level of these three groups were still in the normal state, whereas ALT level in treatment groups given EEBPJ dose 4000 mg/kg bw (88.50 IU/L) and EEBPJ dose 8000 mg/kg bw (97.00 IU/L) exceeds the upper limit of normal state. Macropathology and histopathology of liver result in the control group and treatment groups given with EEBPJ dose 1000 and 2000 mg/kg bw showed no changed while EEBPJ dose 4000 and 8000 mg/kg bw showed changed organ, which mean EEBPJ were toxic at dose 4000 and 8000 mg/kg bw.
BAB I PENDAHULUAN 1.1Latar Belakang
Toksisitas adalah kemampuan suatu zat kimia dalam menimbulkan
kerusakan pada organisme baik saat digunakan atau saat berada dalam
lingkungan. Secara umum toksisitas dibedakan menjadi toksisitas akut, sub kronik
dan kronik (Priyanto, 2009). Uji toksisitas subkronik merupakan suatu pengujian
untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji dengan
dosis berulang yang diberikan secara oral pada hewan uji selama 28 atau 90 hari
(OECD, 2008).
Hati merupakan organ dalam tubuh yang terlibat dalam metabolisme suatu
zat (Lu, 1995). Hati sering menjadi organ sasaran karena zat makanan, sebagian
besar obat-obatan serta toksikan memasuki tubuh melalui sistem gastrointestinal
dan setelah diserap toksikan dibawa oleh vena porta ke hati. Oleh sebab itu, hati
menjadi organ yang sangat potensial menderita keracunan lebih dahulu sebelum
organ lain (Santoso dan Nurlaini, 2006). Pemeriksaan enzim seringkali menjadi
satu-satunya petunjuk adanya kerusakan pada sel hati. Gangguan hati ditandai
dengan peningkatan aktivitas serum aminotransferase berupa ALT (Alanin
Aminotransferase) (Widmann, 1995).
Masyarakat selama ini beranggapan bahwa obat tradisional tidak bisa
menyebabkan keracunan tetapi karena mengandung zat kimia dan digunakan
dalam waktu yang panjang maka efek toksik bisa saja terjadi. Oleh karena itu
perlu terlebih dahulu dilakukan uji keamanan sebagai dasar untuk menjadikan
Obat tradisional agar dapat diterima di masyarakat maupun pelayanan
kesehatan, maka harus didukung secara ilmiah adanya khasiat dan keamanan
penggunaannya pada manusia (Dewoto, 2007).
Salah satu tumbuhan berkhasiat yang dapat dimanfaatkan sebagai obat dan
makanan adalah bunga pepaya jantan (Carica papaya L.), famili Caricaceae
daunnya hal ini disebabkan oleh kandungan alkaloid carpein (C14H25NO2) (Kalie,
1996; Anonim, 2013). Alkaloid banyak digunakan dalam pengobatan (Sumardjo,
2008). Golongan alkaloid dikenal dengan toksisitasnya, namun tidak semua
senyawa alkaloid bersifat toksik (Simbala, 2009).
Hasil skrining bunga pepaya jantan ditemukan adanya alkaloid,
flavonoida, tannin dan steroida-triterpenoida (Henova, 2012). Hasil karakterisasi
simplisia bunga pepaya jantan diperoleh kadar air 7,32%, kadar sari larut dalam
air 19,25%, kadar sari larut dalam etanol 10,61%, kadar abu total 2,25% dan kadar
abu tidak larut asam 0,22% (Sitorus, 2012). Hasil penelitian yang telah dilakukan
terhadap khasiat bunga pepaya jantan antara lain, ekstrak etanol sebagai
antimutagenik (Sitorus, 2012), fraksi etil asetat sebagai antimutagenik (Fransisca,
2012), ekstrak etanol sebagai antioksidan (Henova, 2012), ekstrak metanol
sebagai antibakteri (Iman, 2009) dan ekstrak etanol, fraksi n-heksan, fraksi
etilasetat sebagai antioksidan dan antikanker payudara (Suwarso, dkk., 2013).
Berdasarkan uraian di atas peneliti tertarik untuk melakukan pengujian
toksisitas subkronik ekstrak etanol bunga pepaya jantan (EEBPJ) pada mencit
jantan, mengingat pemanfaatannya yang beragam dan belum ditemukan informasi
1.2Perumusan Masalah
Berdasarkan latar belakang di atas, maka perumusan masalah pada
penelitian ini adalah:
a. apakah EEBPJ berpengaruh terhadap gejala toksik mencit jantan?
b. apakah EEBPJ berpengaruh terhadap berat badan mencit jantan?
c. apakah EEBPJ memberikan efek toksik pada organ hati mencit jantan?
d. berapakah batas keamanan dosis EEBPJ terhadap mencit jantan?
1.3Hipotesis
Berdasarkan perumusan masalah di atas, maka hipotesis pada penelitian
ini diduga:
a. EEBPJ berpengaruh terhadap gejala toksik mencit jantan.
b. EEBPJ tidak berpengaruh terhadap berat badan mencit jantan.
c. EEBPJ memberikan efek toksik pada organ hati mencit jantan.
d. EEBPJ aman digunakan pada dosis 1000 dan 2000 mg/kg bb.
1.4Tujuan Penelitian
Adapun tujuan penelitian ini untuk mengetahui:
a. pengaruh EEBPJ terhadap gejala toksik mencit jantan.
b. pengaruh EEBPJ terhadap berat badan mencit jantan.
c. pengaruh EEBPJ terhadap organ hati mencit jantan.
1.5Manfaat Penelitian
Adapun manfaat penelitian ini adalah dapat memberikan informasi
mengenai efek toksik yang ditimbulkan dari EEBPJ dan memberikan informasi
mengenai batas keamanan dosis dari EEBPJ serta sebagai acuan uji klinik untuk
dijadikan sebagai obat.
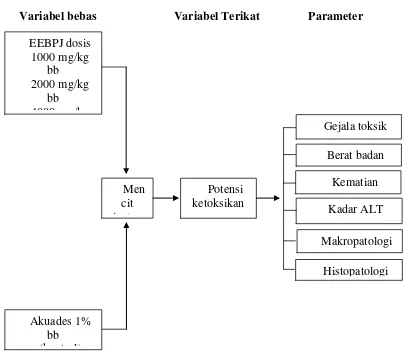
1.6Kerangka Pikir Penelitian
Penelitian dilakukan terhadap mencit jantan yang diberikan EEBPJ selama
28 hari. Tardapat 5 variabel bebas yaitu kelompok kontrol (akuades), perlakuan
EEBPJ dosis 1000, 2000, 4000 dan 8000 mg/kg bb. Variabel terikat potensi
ketoksikan seperti yang ditunjukan pada Gambar 1.1.
Variabel bebas Variabel Terikat Parameter
BAB II
TINJAUAN PUSTAKA 2.1Uraian Tumbuhan
Pepaya (Carica papaya L.) termasuk famili Caricaceae yang merupakan tanaman berasal dari Amerika tropis dimana pusat penyebarannya berada di
daerah Meksiko bagian selatan dan Nikaragua (Kalie, 1996). Di Indonesia pepaya
tersebar hampir di seluruh kepulauan yang dapat tumbuh di daerah basah hingga
kering, dataran maupun pegunungan dan pada ketinggian 1-1000 meter dari
permukaan air laut (BPOM, 2010).
2.1.1Sistematika tumbuhan
Tumbuhan pepaya memilki sistematika sebagai berikut (BPOM, 2008):
Kingdom : Plantae
Divisi : Spermatophyta
Sub divisi : Angiospermae
Class : Dicotyledoneae
Ordo : Cistales
Famili : Caricaceae
Genus : Carica
Spesies : Carica papaya L.
2.1.2Morfologi tumbuhan
Pepaya (Carica papaya L.) merupakan tanaman herba dengan batang
berongga, biasanya tidak bercabang dan tingginya dapat mencapai 10 meter.
Daunnya termasuk daun tunggal, berukuran besar dan bercangap menjari dengan
tangkai daun panjang (BPOM, 2008). Bunga pepaya terdiri dari bunga jantan,
Secara morfologis, bunga pepaya jantan termasuk bunga majemuk yang
memiliki bentuk serupa terompet kecil warnanya kuning pucat cenderung putih
dan dilengkapi dengan tangkai yang memanjang (Anonim, 2013). Bunga pepaya
jantan adalah bunga yang hanya memiliki benang sari saja dengan panjang
kira-kira 2,5 cm. Mahkota terdiri dari lima helai dan berukuran kecil-kecil. Benang sari
berjumlah 10 yang tersusun menjadi dua lapis (Kalie, 1996).
2.1.3Nama daerah
Tanaman pepaya (Carica papaya L.) di Indonesia memiliki berbagai
macam nama daerah, seperti di Sumatera, Jawa, Kalimantan, Nusa Tenggara,
Sulawesi, Maluku dan Papua (BPOM, 2010).
Sumatera : kabaelo, peute, pastelo, embetik, botik, bala, sikailo, kates,
kepaya, kustela, papaya, pepaya, singsile, batiek, kalikih,
pancene, pisang, katuka, pisang patuka, pisang pelo, gedang,
punti kayu.
Jawa : gedang, ketela gantung, kates, gedhang.
Kalimantan : bua medung, pisang malaka, buah dong, majan, pisang
mentela, gadang, bandas.
Nusa Tenggara : gedang, kates, kampaja, kalu jawa, padu, kaut panja, kalailu,
paja, kapala, hango, muu jawa, muku jawa, kasi.
Sulawesi : kapalay, papaya, pepaya, keliki, sumoyori, unti jawa,
tangan-tangan nikare, kaliki, rianre.
Maluku : tele, palaki, papae, papaino, papau, papaen, papai, papaya,
sempain, tapaya, kapaya.
2.1.4 Kandungan kimia
Berdasarkan penelitian yang telah dilakukan, hasil skrining bunga pepaya
jantan menunjukkan adanya golongan senyawa alkaloid, flavonoid, tanin,
steroid-triterpenoid (Henova, 2012).
2.1.5 Khasiat tumbuhan
Tumbuhan pepaya hampir seluruh bagiannya memiliki khasiat (Kalie,
1996). Daunnya berkhasiat sebagai antibakteri (Kalie, 1996; Setyowati, dkk.,
2011), antimalaria (Kalie, 1996; Rehena, 2010), antijerawat (Budiman, dkk.,
2010), analgesik (Lasarus, dkk., 2013), antikanker (Sukardiman, dkk., 2006),
penambah nafsu makan (Heyne, 1987; Kalie 1996).
Bunganya berkasiat sebagai antimutagenik (Sitorus, 2012; Fransisca,
2012), antioksidan (Henova, 2012; Suwarso, dkk., 2013), antibakteri (Iman,
2009), antikanker payudara (Suwarso, dkk., 2013). Bijinya berkhasiat sebagai
antibakteri (Martiasih, dkk., 2011), mengobati cacing kremi (Kalie, 1996).
Akarnya juga berkhasiat sebagai antiinflamasi (Adjirni dan saruni, 2006),
gangguan saluran kencing (Kalie, 1996), antidiuretik (BPOM, 2010).
2.2 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan suatu
pelarut cair. Senyawa aktif yang terdapat dalam berbagai simplisia dapat
digolongkan kedalam golongan minyak atsiri, alkaloida, flavonoida dan lain-lain.
Dengan diketahuinya senyawa aktif yang dikandung simplisia akan
mempermudah pemilihan pelarut dengan cara ekstraksi yang tepat (Ditjen POM,
Ekstrak adalah sediaan kering, kental atau cair dibuat dengan menyari
simplisia nabati atau hewani menurut cara yang cocok, di luar pengaruh cahaya
matahari langsung (Depkes, 1979). Metode ekstraksi yang umum digunakan
dalam berbagai penelitian antara lain (Ditjen POM, 2000) yaitu:
1. Maserasi
Maserasi adalah proses penyarian simplisia menggunakan pelarut dengan
beberapa kali pengocokan atau pengadukan pada temperatur ruangan, sedangkan
remaserasi merupakan pengulangan penambahan pelarut setelah dilakukan
penyaringan maserat pertama, dan seterusnya.
2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu
baru sampai sempurna yang umumnya dilakukan pada temperatur ruangan.
Serbuk simplisia yang akan diperkolasi tidak langsung dimasukkan kedalam
bejana perkolator, tetapi dibasahi atau dimaserasi terlebih dahulu dengan cairan
penyari sekurang-kurangnya selama 3 jam.
3. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada
temperatur titik didihnya dalam waktu tertentu dimana pelarut akan terkondensasi
menuju pendingin dan kembali ke labu.
4. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang
selalu baru, dilakukan dengan menggunakan alat soklet dimana pelarut akan
5. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada
temperatur lebih tinggi dari temperatur kamar, yaitu secara umum dilakukan pada
temperatur 40-50°C.
6. Infundasi
Infundasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 90°C selama 15 menit.
7. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 90°C selama 30 menit.
2.3 Toksisitas
Toksisitas adalah kemampuan suatu zat kimia dalam menimbulkan
kerusakan pada organisme baik saat digunakan atau saat berada dalam lingkungan
(Priyanto, 2009). Uji toksisitas adalah suatu uji untuk mendeteksi efek toksik
suatu zat pada sistem biologi dan untuk memperoleh data dosis-respon yang khas
dari sediaan uji. Data yang diperoleh dapat digunakan untuk memberi informasi
mengenai derajat bahaya sediaan uji tersebut bila terjadi pemaparan pada
manusia, sehingga dapat ditentukan dosis penggunaannya demi keamanan
manusia (OECD, 2008).
Obat sebelum dipasarkan atau digunakan harus menjalani serangkaian uji
untuk memastikan efektivitas dan keamanannya (Priyanto, 2009). Umumnya uji
toksisitas terdiri atas dua jenis, yaitu toksisitas umum (akut, subkronik dan kronik)
dan toksisitas khusus (teratogenik, mutagenik dan karsinogenik) (Dewoto, 2007;
2.3.1Toksisitas umum 2.3.1.1Toksisitas akut
Uji toksisitas akut adalah suatu pengujian untuk mendeteksi efek toksik
yang muncul dalam waktu singkat setelah pemberian sediaan uji secara oral dalam
dosis tunggal yang diberikan dalam waktu 24 jam (Lu, 1995). Tujuan
dilakukannya uji toksisitas akut adalah untuk menentukan LD50 (potensi
ketoksikan) akut dari suatu senyawa (Priyanto, 2009). Semakin kecil harga LD50
maka semakin besar potensi ketoksikannya (OECD, 2001).
Prinsip uji toksisitas akut oral yaitu, sediaan uji dalam beberapa tingkat
dosis yang diberikan pada beberapa kelompok hewan uji dengan satu dosis per
kelompok, kemudian dilakukan pengamatan terhadap adanya efek toksik dan
kematian (OECD, 2001).
2.3.1.2Toksisitas subkronik
Uji toksisitas subkronik merupakan suatu pengujian untuk mendeteksi efek
toksik yang muncul setelah pemberian sediaan uji dengan dosis berulang yang
diberikan secara oral pada hewan uji (OECD, 2008).
Tujuan toksisitas subkronik oral adalah untuk memperoleh informasi
adanya efek toksik zat yang tidak terdeteksi pada uji toksisitas akut, informasi
kemungkinan adanya efek toksik setelah pemaparan sediaan uji secara berulang
dalam jangka waktu tertentu, informasi dosis yang tidak menimbulkan efek toksik
dan mempelajari adanya efek kumulatif dan efek reversibilitas zat tersebut
(OECD, 2008). Serta bertujuan untuk menentukan organ sasaran (organ yang
rentan) (Priyanto, 2009).
Prinsip uji toksisitas subkronik oral adalah sediaan uji dalam beberapa
dosis per kelompok selama 28 atau 90 hari. Selama pemberian sediaan uji, hewan
harus diamati setiap hari untuk menentukan adanya toksisitas. Selama waktu dan
pada akhir periode pemberian sediaan uji, hewan yang mati dan masih hidup
diotopsi selanjutnya dilakukan pengamatan secara makropatologi pada setiap
organ dan jaringan. Selain itu juga dilakukan pemeriksaan hematologi, biokimia
klinis dan histopatologi (OECD, 2008).
2.3.1.3Toksisitas kronik
Uji toksisitas kronis dilakukan dengan memberikan senyawa uji
berulang-ulang selama masa hidup hewan uji atau sebagian besar masa hidupnya (Priyanto,
2009). Prinsip toksisitas kronik oral pada umumnya sama dengan uji toksisitas
subkronik, hanya sediaan uji yang diberikan lebih lama tidak kurang dari 12
bulan. Pengamatan juga dilakukan secara lengkap seperti gejala toksik,
monitoring berat badan dan konsumsi makanan, pemeriksaan hematologi,
biokimia klinis, makropatologi, penimbangan organ dan histopatologi (OECD,
2008).
2.3.2Toksisitas khusus 2.3.2.1Uji teratogenik
Uji teratogenik adalah suatu pengujian untuk memperoleh informasi
adanya abnormalitas fetus yang terjadi karena pemberian suatu zat dalam masa
perkembangan embrio (Priyanto, 2009).
Prinsip pengujian ini senyawa uji dalam beberapa tingkat dosis diberikan
kepada beberapa kelompok hewan hamil selama paling sedikit masa
organogenesis dari kehamilan, satu dosis untuk satu kelompok. Sesaat sebelum
waktu melahirkan, uterus diambil dan dilakukan evaluasi terhadap fetus (OECD,
2.3.2.2Uji mutagenik
Uji mutagenik adalah uji yang dilakukan untuk memperoleh informasi
mengenai kemungkinan terjadinya efek mutagenik suatu senyawa. Efek
mutagenik merupakan efek yang menyebabkan terjadinya perubahan pada sifat
genetika sel tubuh makhluk hidup (Loomis, 1978).
2.3.2.3Uji karsinogenik
Uji karsinogenik adalah uji yang dilakukan untuk memperoleh informasi
mengenai efek korsinogenik suatu senyawa pada hewan percobaan (Lu, 1995) dan
untuk mengetahui apakah zat jika dipakai dalam jangka panjang akan dapat
menimbulkan kanker . Uji ini dilakukan jika nantinya obat akan digunakan dalam
jangka panjang selama 2 tahun (Priyanto, 2009).
2.4Hati
Salah satu organ yang sering menderita karena adanya zat-zat toksik adalah
hati. Bahan kimia kebanyakan mengalami metabolisme dalam hati oleh karenanya
berpotensi merusak sel-sel hati. Bahan kimia yang dapat mempengaruhi hati
disebut hepatotoksik (Wisaksono, 2002).
2.4.1Anatomi hati
Hati merupakan organ tubuh terbesar kedua di dalam tubuh, dengan berat
rata-rata sekitar 1,5 kg. Organ ini terletak dalam rongga perut sebelah kanan di
bawah diafragma (Junqueira and Carneiro, 2007). Hati terbagi dalam dua belahan
utama kanan dan kiri yang dipisahkan oleh fisura longitudinal (Irianto, 2004).
Warnanya dalam keadaan segar merah kecoklatan, warna tersebut
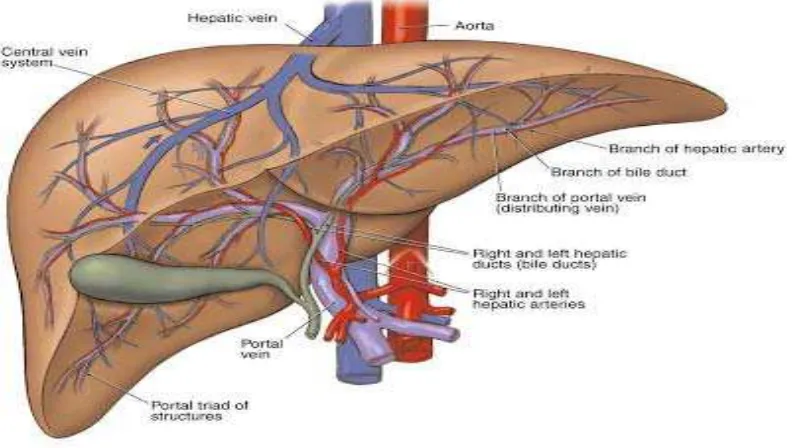
terutama disebabkan oleh adanya darah yang amat banyak (Lee, et al., 1997).
Gambar 2.1 Anatomi hati
Secara anatomi hati terdiri dari beberapa lobus tergantung pada
spesiesnya, untuk mencit terdapat empat lobus (lobus medial, kaudal, lateral kiri
dan lateral kanan) (Harada, et al., 1999). Setiap lobus hati terdiri dari beberapa
lobulus yang terdiri dari berbagai komponen, yaitu sel-sel hati (hepatosit), vena
sentralis, sinusoid, cabang-cabang vena porta, cabang-cabang arteri hepatika, sel
kupffer dan kanalikuli biliaris (Junqueira and Carneiro, 2007).
2.4.2Fisiologi hati
Organ hati terlibat dalam metabolisme zat makanan serta sebagian besar
obat dan toksikan (Lu, 1994). Hati mempunyai fungsi yang sangat banyak dan
kompleks yang penting untuk mempertahankan hidup (Husadha, 1996) yaitu :
a. Fungsi pembentukan dan ekskresi empedu
Hal ini merupakan fungsi utama hati yaitu mengekskresikan sekitar satu
liter empedu setiap hari. Garam empedu penting untuk pencernaan dan absorbsi
b. Fungsi metabolik
Hati berperaan penting dalam metabolisme karbohidrat, lemak, protein,
vitamin dan juga memproduksi energi. Hati mengubah ammonia menjadi urea,
untuk dikeluarkan melalui ginjal dan usus.
c. Fungsi pertahanan tubuh
Hati mempunyai fungsi detoksifikasi dan perlindungan yang dilakukan
oleh enzim-enzim hati untuk melakukan oksidasi, reduksi, hidrolisis, atau
konjugasi zat yang kemungkinan membahayakan dan mengubahnya menjadi zat
yang secara fisiologis tidak aktif. Fungsi perlindungan dilakukan oleh sel kupffer
yang terdapat di dinding sinusoid hati.
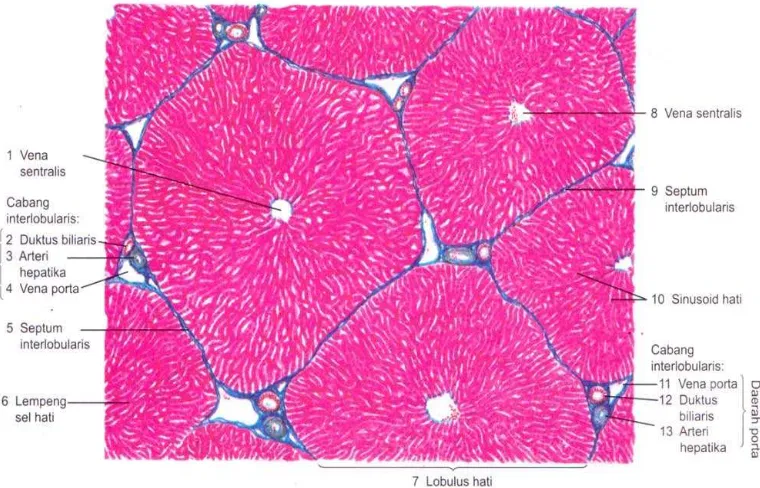
2.4.3Histologi hati
Hati terdiri atas unit-unit heksagonal yaitu lobulus hati. Di bagian tengah
setiap lobulus hati terdapat sebuah vena sentralis yang dikelilingi secara radial
oleh sel-sel hati (hepatosit) (Junqueira dan Corneiro, 2007). Gambar histologi hati
dapat dilihat pada Gambar 2.2 berikut (Eroschenko, 2010).
Sel hati bebentuk polihedral dengan inti bulat yang terletak di tengah dan
kadang tampak lebih dari satu inti akibat pembelahan sitoplasma yang tidak
sempurna (Dellman and Brown 1992). Sel tersebut terletak di antara sinusoid
yang berisi darah dan saluran empedu (Lu, 1995). Darah yang mengandung toksin
dibawa dari usus kemudian masuk ke hati melalui vena porta kemudian melewati
sinusoid menuju vena sentralis (Macfarlane, et al., 2000).
Hati menerima darah dari dua sumber yaitu darah arteri dari arteri hepatika
kiri dan kanan, dan darah vena dari vena porta hepatika yang mengalir dari
saluran pencernaan dan limpa (Underwood, 1994). Sebanyak 80% dari aliran
darahnya berasal dari vena porta yang mengangkut darah rendah oksigen. Sisanya
(20%) berasal dari arteri hepatika yang memasok darah kaya oksigen. Darah
meninggalkan hati melalui vena hepatika yang mengalir menuju vena kava
inferior (Underwood, 1994).
2.4.4Intoksikasi hati
Metabolisme umumnya berlangsung di hati karena di hati banyak terdapat
enzim pemetabolisme. Tujuannya adalah membuat senyawa menjadi lebih polar
sehingga mudah dieksresikan dan menjadi kurang toksik, namun ada senyawa
tertentu yang setelah mengalami metabolisme menjadi lebih toksik (Priyanto,
2009).
Kerusakan pada hati dapat terjadi oleh beberapa faktor yaitu onset
pemaparan yang terlalu lama, durasi pemaparan, dosis dan sel inang yang rentan
(Jubb, 1993). Kerusakan yang terjadi pada sel hati dapat bersifat sementara
(reversible) dan tetap (irreversible) (Wisaksono, 2002). Sel akan mengalami
perubahan untuk beradaptasi mempertahankan hidupnya, perubahan ini biasa
disebabkan oleh iskemia, anemia, metabolisme abnormal dan zat kimia yang
bersifat toksik (Cheville, 1999).
Degenerasi hidropik merupakan peristiwa meningkatnya kadar air di
intraseluler yang menyebabkan sitoplasma dan organel-organel membengkak dan
membentuk vakuola-vakuola. Rusaknya permeabilitas membran sel menyebabkan
terhambatnya aliran Na+ keluar dari sel sehingga menyebabkan ion-ion dan air
masuk secara berlebihan kedalam sel. Degenerasi hidropik merupakan respon
awal sel terhadap bahan-bahan yang bersifat toksik, serta merupakan proses awal
dari kematian sel (Jones, et al., 1997; Cheville, 1999). Kadar Na+ intrasel diatur
oleh pompa Na+ yang memerlukan ATP, jika ATP berkurang maka akan
mengakibatkan masuknya Na+ ke intrasel melebihi jumlah normalnya (Priyanto,
2009).
Kerusakan sel secara terus-menerus akan mencapai suatu titik sehingga
terjadi kematian sel (Lu, 1995). Paparan zat toksik pada sel apabila cukup hebat
atau berlangsung cukup lama, maka sel tidak dapat lagi mengkompensasi dan
tidak dapat melanjutkan metabolisme (Priyanto, 2009). Inti sel yang mati dapat
terlihat lebih kecil dan menjadi lebih padat (kariopiknosis), hancur
bersegmen-segmen (karioreksis) dan kemudian inti sel menghilang (kariolisis) (Underwood,
1994). Nekrosis hati adalah kematian hepatosit yang umumnya merupakan
kerusakan akut (Lu, 1995).
2.5ALT (Alanine Aminotransferase)
Tes fungsi hati yang umum untuk mengetahui adanya gangguan dalam
organ hati adalah dengan mengukur serum aminotransferase yaitu ALT (Alanine
dkk., 2005). ALT memindahkan satu gugus amino antara alanin dan asam alfa
keto-glutamat, fungsi ini penting untuk pembentukan asam-asam amino yang
dibutuhkan untuk menyusun protein di hati (Sacher dan Richard, 2004).
ALT merupakan enzim aminotransferase yang dibuat dalam sel hati
(hepatosit), jadi lebih spesifik untuk penyakit hati dibandingkan dengan enzim
lain. ALT sering dijumpai dalam hati, sedangkan AST terdapat lebih banyak di
jantung, otot rangka, otak dan ginjal dibandingkan di hati (Sagita, dkk., 2012).
ALT memberikan hasil yang lebih spesifik dari pada AST (Sherlock, 1981; Bauer,
1982; Murray, et al., 1995). Kadarnya dalam serum meningkat terutama pada
kerusakan dalam hati dibandingkan dengan AST (Hadi, 1995).
Hepatosit apabila mengalami cedera enzim yang secara normal tersebut
berada di dalam sel yaitu sitoplasma akan masuk ke dalam aliran darah (Sacher
dan Richard, 2004). Kerusakan pada sel hati yang sedang berlangsung dapat
diketahui dengan mengukur parameter fungsi hati berupa zat dalam peredaran
darah yang dibentuk oleh sel hati yang rusak atau mengalami nekrosis.
Pemeriksaan enzim seringkali menjadi satu-satunya petunjuk adanya penyakit hati
yang dini atau setempat (Widman, 1995). ALT darah mencit normal adalah 17–77
BAB III
METODE PENELITIAN
Penelitian ini menggunakan metode eksperimental dengan tahapan
penelitian yaitu pengumpulan tumbuhan, identifikasi tumbuhan, pembuatan
simplisia, pembuatan ekstrak, pengamatan meliputi gejala toksik, berat badan,
kematian, pengukuran kadar ALT, makropatologi dan histopatologi organ hati
kemudian dilakukan analisis statistik.
3.1Alat dan Bahan 3.1.1Alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas
laboratorium, alat bedah (Wells spencer), alat destilasi, blender (Miyako), freeze
dryer (Edward), kamera digital, lemari pengering, neraca digital (Vibra), neraca
hewan (Presica Geniweigher GW-1500), neraca kasar (ohaus), oral sonde, rotary
evaporator (heidolph VV-300) dan spuit 1 ml (Terumo).
3.1.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini meliputi bahan
tumbuhan dan bahan kimia. Bahan tumbuhan yang digunakan yaitu bunga pepaya
jantan (Carica papaya L.). Bahan kimia yang digunakan yaitu akuades, etanol
80%, formalin 10%, kloroform dan natrium klorida 0,9%.
3.2 Hewan Percobaan
Hewan percobaan yang digunakan adalah mencit jantan dengan berat
badan 25-35 gram, berumur 2-3 bulan. Sebelum pengujian, mencit diaklimatisasi
terlebih dahulu selama 7-14 hari. Sebanyak 25 ekor mencit dibagi dalam 5
3.3 Penyiapan Sampel
3.3.1 Pengumpulan tumbuhan
Pengumpulan tumbuhan dilakukan secara purposif yaitu tanpa
membandingkan dengan tumbuhan yang sama dari daerah lain. Tumbuhan yang
digunakan adalah bunga pepaya jantan (Carica papaya L.) yang diperoleh dari
desa Gunung Berkat, Kecamatan Bandar Pulau, Kabupaten Asahan, Provinsi
Sumatera Utara.
3.3.2 Identifikasi tumbuhan
Identifikasi bunga pepaya jantan (Carica papaya L.) dilakukan di
Herbarium Medanense (MEDA), Universitas Sumatera Utara.
3.3.3 Pembuatan simplisia
Bunga pepaya jantan (Carica papaya L.) yang masih segar dipisahkan dari
tangkainya, dicuci kemudian ditiriskan dan ditimbang beratnya sebagai berat
basah (6200 g). Selanjutnya dikeringkan dalam lemari pengering hingga kering
yang ditandai dengan sampel mudah dipatahkan, kemudian ditimbang kembali
sebagai berat kering selanjutnya diblender dan ditimbang sebagai berat serbuk
simplisia (1200 g). Serbuk simplisia dimasukkan ke dalam kantong plastik, diberi
etiket dan disimpan di tempat yang sesuai.
3.4 Pembuatan Ekstrak Etanol Bunga Pepaya Jantan
Pembuatan EEBPJ dilakukan secara maserasi menggunakan etanol 80%.
Cara kerja:
Sebanyak 1200 g serbuk simplisia bunga pepaya jantan dimasukkan ke
dalam bejana, kemudian dituangi dengan 9 liter etanol 80%. Ditutup dan
diperas. Ampas dicuci kembali dengan 3 liter etanol 80%, dipindahkan ke dalam
bejana tertutup, dibiarkan di tempat sejuk, terlindung dari cahaya selama 2 hari,
selanjutnya disaring (Depkes RI, 1979). Maserat etanol yang diperoleh diuapkan
dengan menggunakan rotary evaporator ± 40oC sampai diperoleh ekstrak kental
kemudian dipekatkan dengan freeze dryer ± -40oC.
3.5 Pengujian Efek Toksisitas
Pengujian efek toksisitas meliputi pembuatan sediaan uji EEBPJ, uji
pendahuluan, pengujian toksisitas subkronik meliputi gejala toksik, perubahan
berat badan, kematian hewan, pengukuran kadar ALT, makropatologi dan
histopatologi organ hati.
3.5.1 Pembuatan sediaan uji ekstrak etanol bunga pepaya jantan
Sediaan uji dibuat dengan konsentrasi 25%, ditimbang ekstrak kemudian
dimasukkan ke dalam lumpang, dan ditambahkan akuades digerus hingga merata.
Sediaan uji EEBPJ dimasukkan ke dalam labu ukur, cukupkan dengan akuades
hingga dicapai batas volume.
3.5.2 Uji pendahuluan
Sebanyak 10 ekor mencit dibagi dalam 5 kelompok, setiap kelompok
terdiri dari 2 ekor. Kelompok kontrol diberi akuades 1% bb, kelompok perlakuan
diberi EEBPJ dosis 100, 200, 400 dan 800 mg/kg bb secara oral selama 28 hari
dan dilakukan pengamatan (Hasti, dkk., 2012).
3.5.3Pengujian toksisitas subkronik
Berdasarkan hasil uji pendahuluan maka didapatkan dosis untuk dilakukan
masing-masing terdiri dari 5 ekor mencit yaitu: kelompok kontrol (1) dan
kelompok perlakuan (2-5).
- Kelompok 1: kontrol, diberi akuades 1% bb - Kelompok 2: diberi EEBPJ dosis 1000 mg/kg bb - Kelompok 3: diberi EEBPJ dosis 2000 mg/kg bb - Kelompok 4: diberi EEBPJ dosis 4000 mg/kg bb - Kelompok 5: diberi EEBPJ dosis 8000 mg/kg bb 3.5.4Pengamatan
Penimbangan mencit dilakukan pada hari ke-0 kemudian pada hari ke-1
diberi sediaan uji secara oral setiap hari selama 28 hari dan dilakukan pengamatan
(OECD, 2008; Krysanti dan Widjanarko, 2014; Murtini, dkk., 2010; Prasetyawati,
dkk., 2004).
3.5.4.1Gejala toksik
Pengamatan dilakukan 3 jam pertama setelah pemberian sediaan uji
(Prasetyawati, dkk., 2004). Pengamatan untuk gejala toksik diamati adanya
kejang, salivasi, diare, lemas, perubahan bulu, gerak-gerik mencit seperti berjalan
mundur dan berjalan dengan perut (OECD, 2008).
3.5.4.2Berat badan
Mencit ditimbang setiap hari selama 28 hari untuk menentukan volume
sediaan uji yang akan diberikan. Perubahan berat badan dianalisis seminggu
sekali. Pada akhir penelitian, hewan yang masih hidup ditimbang dan diotopsi
(OECD, 2008).
3.5.4.3Kematian hewan
Kematian mencit diamati dari hari pertama sampai hari terakhir dan
mencit yang mati selama waktu pemberian sediaan uji segera diotopsi (Hendriani,
3.5.4.4Pengukuran kadar ALT
Pada akhir periode pemberian sediaan uji semua mencit yang masih hidup
diotopsi. Hewan dianestesi dengan kloroform kemudian darah diambil melalui
jantung (intra cardiac) secara perlahan-lahan menggunakan alat suntik steril
sebanyak 1-3 ml. Sebanyak 1 ml darah dimasukkan ke dalam tabung
mikrosentrifuge dan didiamkan pada suhu kamar selama 10 menit, kemudian
dipindahkan ke dalam tangas es dan segera disentrifuge selama 10 menit dengan
kecepatan 3000 rpm. Serum dipisahkan dan disimpan dalam lemari beku (OECD,
2008; Sagita, dkk., 2012). Kadar ALT selanjutnya diperiksa di Balai
Laboratorium Kesehatan, Dinas Kesehatan Propinsi Sumatera Utara.
3.5.4.5Makropatologi
Mencit yang mati segera diotopsi dan dilakukan pengamatan (OECD,
2008). Pengamatan meliputi warna, permukaan dan konsistensi organ hati secara
visual (Anggraini, 2008).
3.5.4.6Histopatologi organ hati
Pada akhir periode pemberian sediaan uji semua mencit yang masih hidup
dianestesi dengan kloroform kemudian diotopsi, selanjutnya diambil organ hati
dan dicuci dengan larutan fisiologis 0,9% kemudian dimasukkan dalam larutan
dapar formaldehida 10% dan hasilnya dilihat di bawah mikroskop (OECD, 2008;
Hendriani, 2007). Pembuatan preparat histopatologi dilakukan di Laboratorium
Patologi Anatomi Fakultas Kedokteran USU.
3.5.5Analisis statistik
Pengamatan berat badan, pengukuran ALT dianalisis dengan
menggunakan one-way analysis of variance (ANOVA) dan dilanjutkan dengan uji
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Medanense (MEDA),
Universitas Sumatera Utara Medan, disebutkan sampel yang digunakan adalah
tumbuhan bunga pepaya jantan (Carica papaya L.) suku Caricaceae. Hasil
identifikasi dapat dilihat pada Lampiran 1 dan gambar tumbuhan pada Lampiran
2.
4.2 Hasil Ekstraksi Serbuk Bunga Pepaya Jantan
Pembuatan ekstrak dilakukan dengan metode maserasi menggunakan
pelarut etanol 80%. Hasil maserasi dari 1200 g serbuk simplisia diperoleh ekstrak
kental 97,38 g (randemen 8,115%).
4.3 Hasil Uji Pendahuluan
Hasil uji pendahuluan selama 28 hari tidak ditemukan adanya gejala toksik
dan kematian serta tidak ada perbedaan yang signifikan antara kenaikan berat
badan dengan pemberian EEBPJ (p > 0,05) pada kelompok kontrol maupun
kelompok perlakuan dosis 100, 200, 400 dan 800 mg/kg bb. Hasil uji pendahuluan
dapat dilihat pada Lampiran 7.
4.4 Hasil Pengujian Toksisitas Subkronik
Berdasarkan hasil uji pendahuluan dari EEBPJ maka didapatkan dosis
untuk pengujian toksisitas subkronik yaitu dosis 1000, 2000, 4000 dan 8000
mg/kg bb. Pengamatan dilakukan selama 28 hari meliputi gejala toksik, berat
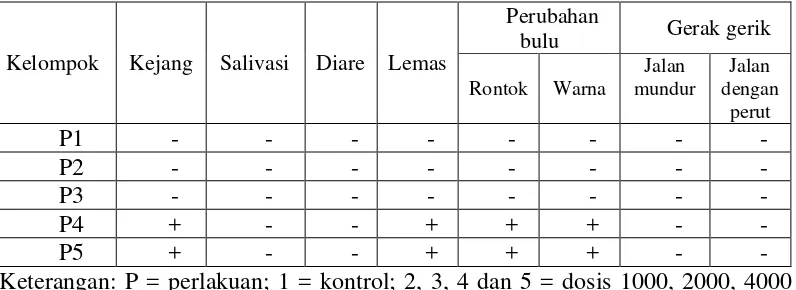
4.4.1 Hasil pengamatan gejala toksik
Hasil pengamatan yang dilakukan setiap hari selama 28 hari terhadap
adanya kejang, salivasi, diare, lemas, perubahan bulu, gerak-gerik hewan seperti
berjalan mundur dan berjalan dengan perut dapat dilihat pada Tabel 4.1.
Tabel 4.1 Hasil pengamatan gejala toksik
Kelompok Kejang Salivasi Diare Lemas
Perubahan dan 8000 mg/kg bb; bb = berat badan; (-) = tidak menunjukkan gejala; (+) = menunjukkan adanya gejala
Pada Tabel 4.1 terlihat bahwa pemberian EEBPJ tidak ditemukan adanya
gejala toksik pada kelompok kontrol dan perlakuan pada dosis 1000 dan 2000
mg/kg bb. Pada dosis 4000 dan 8000 mg/kg bb ditemukan gejala toksik yaitu
terjadi kejang, lemas dan perubahan bulu pada mencit. Hal tersebut menunjukkan
adanya hubungan antara dosis dan efek toksik, dimana makin besar dosis yang
diberikan makin besar efek toksik yang timbul (Lu, 1995). Zat dapat
menimbulkan efek yang tidak diinginkan berkaitan dengan dosis yang diberikan
yaitu efek samping, efek merugikan dan efek toksik (Priyanto, 2009).
Setiap zat bila diberikan dengan dosis yang cukup besar akan
menimbulkan gejala-gejala toksik (Ganiswara, 1995). Hewan percobaan yang
bereaksi terhadap toksisitas suatu senyawa tertentu, akan disertai tanda-tanda
seperti bulu berdiri, diare, serta pembengkakan atau pembentukan warna merah
4.4.2 Hasil pengamatan berat badan
Penimbangan berat badan dilakukan setiap hari dari hari 0 sampai hari ke
28 untuk menentukan volume sediaan yang diberikan, sedangkan yang dianalisis
secara statistik dilakukan seminggu sekali. Rata-rata berat badan dapat dilihat
pada Tabel 4.2.
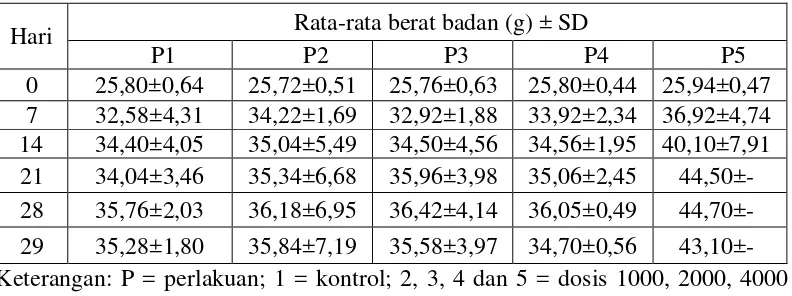
Tabel 4.2 Hasil rata-rata berat badan
Hari Rata-rata berat badan (g) ± SD
P1 P2 P3 P4 P5
0 25,80±0,64 25,72±0,51 25,76±0,63 25,80±0,44 25,94±0,47 7 32,58±4,31 34,22±1,69 32,92±1,88 33,92±2,34 36,92±4,74 14 34,40±4,05 35,04±5,49 34,50±4,56 34,56±1,95 40,10±7,91 21 34,04±3,46 35,34±6,68 35,96±3,98 35,06±2,45 44,50±- 28 35,76±2,03 36,18±6,95 36,42±4,14 36,05±0,49 44,70±- 29 35,28±1,80 35,84±7,19 35,58±3,97 34,70±0,56 43,10±- Keterangan: P = perlakuan; 1 = kontrol; 2, 3, 4 dan 5 = dosis 1000, 2000, 4000
dan 8000 mg/kg bb; bb = berat badan
Pada Tabel 4.2 hasil uji statistik menunjukkan tidak ada perbedaan yang
signifikan antara kenaikan berat badan dengan pemberian EEBPJ (p > 0,05). Hal
ini dapat dinyatakan bahwa pemberian EEBPJ selama 28 hari tidak berpengaruh
terhadap perkembangan berat badan mencit.
Parameter yang merupakan indikator sensitif untuk mengetahui toksisitas
yaitu gejala toksik dan berat badan. Hewan uji diamati setiap hari untuk gejala
toksik dan berat badan diukur secara berkala (Gupta dan Bhardwaj, 2012).
Berkurangnya pertambahan berat badan merupakan indeks efek toksik
yang sederhana namun sensitif (Lu, 1995). Kekurangan protein dalam ransum
dapat mengakibatkan terhambatnya pertumbuhan. Secara umum penambahan
berat badan akan dipengaruhi oleh jumlah konsumsi pakan yang dimakan dan
4.4.3 Hasil pengamatan kematian
Mencit yang mati selama waktu pemberian sediaan uji dapat dilihat pada
Tabel 4.3.
Tabel 4.3 Hasil pengamatan kematian
Keterangan: P = perlakuan; 1 = kontrol; 2, 3, 4 dan 5 = dosis 1000, 2000, 4000 dan 8000 mg/kg bb; bb = berat badan
Pada Tabel 4.3 terlihat pada kelompok kontrol, dosis 1000 dan 2000
mg/kg bb tidak ada mencit yang mati selama waktu pemberian sediaan uji, sedang
pada dosis 4000 mg/kg bb jumlah mencit yang mati 3 ekor dan dosis 8000 mg/kg
bb 4 ekor. Hal tersebut dikarenakan pemberian EEBPJ setiap hari selama 28 hari
sehingga terjadi kerusakan organ yang dapat menyebabkan kematian pada mencit.
Kandungan senyawa metabolit sekunder dalam EEBPJ juga merupakan penyebab
kematian mencit. Alkaloid cukup toksik sehingga pemberian dalam jumlah yang
besar dapat menyebabkan kematian (Elya, dkk., 2010).
Suatu zat pada dasarnya bersifat racun dan terjadinya keracunan
ditentukan oleh dosis dan cara pemberian, namun dosis merupakan faktor utama
yang terpenting (Ganiswara, 1995).
Efek toksik merupakan efek yang sangat berbahaya dan dapat
menyebabkan kematian. Efek toksik suatu zat dipengaruhi oleh zatnya, target
organ, besar dosis dan kondisi fisiologi membran biologi yang terpapar (Priyanto,
2009).
Kelompok Jumlah mencit Jumlah
35,2 4.4.4 Hasil pengukuran kadar ALT
Pengukuran kadar ALT dilakukan pada hari ke 29, hasil rata-rata kadar
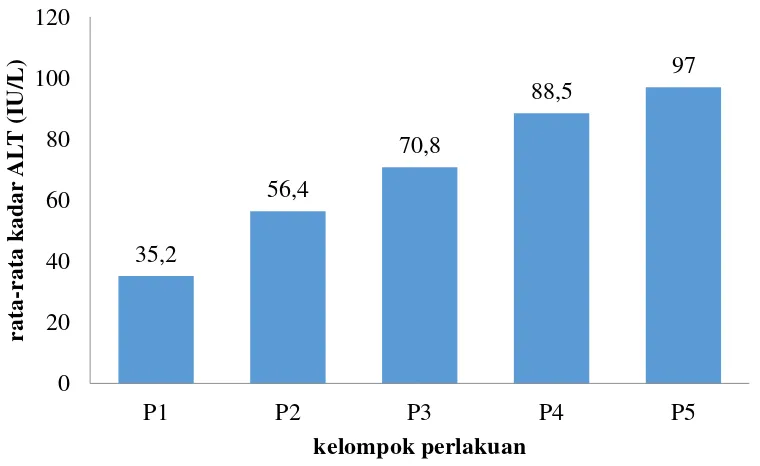
ALT dapat dilihat pada Lampiran 9. Grafik rata-rata dapat dilihat pada Gambar
4.1.
Gambar 4.1 Grafik rata-rata hasil pengukuran kadar ALT
Keterangan: P = perlakuan; 1 = kontrol; 2, 3, 4 dan 5 = dosis 1000, 2000, 4000 dan 8000 mg/kg bb; bb = berat badan
Pada Gambar 4.1 terlihat bahwa terdapat adanya perbedaan yang
signifikan antara kelompok perlakuan (p < 0,05). Pada kelompok kontrol rata-rata
kadar ALT (35,20 IU/L), dosis 1000 mg/kg bb (56,40 IU/L) dan 2000 mg/kg bb
(70,80 IU/L), terlihat hasil rata-rata kadar ALT dari ketiga kelompok tersebut
masih dalam batas normal. Pada dosis 4000 mg/kg bb (88,50 IU/L) dan dosis
8000 mg/kg bb (97,00 IU/L), rata-rata kadar ALT kelompok tersebut di atas batas
normal. Kadar ALT darah mencit normal adalah 17–77 IU/L (Anonymous,
2009).
Indikator yang spesifik untuk kerusakan hati adalah besarnya kandungan
(Sherlock, 1981; Bauer, 1982; Murray, et al., 1995). Enzim ALT adalah enzim
yang dibuat dalam sel hati (hepatosit), jadi lebih spesifik untuk penyakit hati
dibandingkan dengan enzim lain. ALT sering dijumpai dalam hati, sedangkan
dalam jantung, ginjal, otak dan otot rangka kurang jika dibandingkan dengan
SGOT (Hadi, 1995).
Hepatosit apabila mengalami cedera enzim yang secara normal tersebut
berada di dalam sel yaitu sitoplasma akan masuk ke dalam aliran darah (Sacher
dan Richard, 2004).
4.4.5 Hasil pengamatan makropatologi
Hasil gambar makropatologi organ hati dapat dilihat pada Lampiran 10.
Hasil pengamatan makropatologi meliputi pengamatan warna, permukaan dan
konsistensi organ hati dapat dilihat pada tabel 4.4.
Tabel 4.4 Hasil pengamatan makropatologi
Kelompok Pengamatan
Warna Permukaan Konsistensi
P1 Merah kecoklatan Licin Kenyal
P2 Merah kecoklatan Licin Kenyal
P3 Merah kecoklatan Licin Kenyal
P4 Merah kehitaman Licin Kenyal
P5 Pucat Tidak licin Tidak kenyal
Keterangan: P = perlakuan; 1 = kontrol; 2, 3, 4 dan 5 = dosis 1000, 2000, 4000 dan 8000 mg/kg bb; bb = berat badan
Pada Tabel 4.4 terlihat pada kelompok kontrol, dosis 1000 dan 2000
mg/kg bb organ hati masih dalam keadaan normal yang berwarna merah
kecoklatan, permukaannya licin dan konsistensinya kenyal. Kriteria normal pada
organ hati bila tidak ditemukan perubahan warna, perubahan struktur permukaan
dan perubahan konsistensi (Anggraini, 2008). Pada dosis 4000 dan 8000 mg/kg bb
sudah terjadi perubahan warna menjadi merah kehitaman dan pucat. Perubahan
mendapatkan informasi mengenai toksisitas zat uji yang berkaitan dengan organ
sasaran dan efek terhadap organ tersebut (Lu, 1995).
4.4.6 Hasil histopatologi organ hati
Organ hati pada mencit yang mati segera diambil dan pada akhir periode
pemberian sediaan uji, semua mencit yang masih hidup diotopsi. Organ hati
diambil kemudian dibuat menjadi preparat histopatologi selanjutnya dilihat
kerusakan jaringan di bawah mikroskop, hasil kerusakan dapat dilihat pada Tabel
4.5.
Tabel 4.5 Hasil histopatologi berdasarkan kerusakan hepatosit
Keterangan: P = perlakuan; 1 = kontrol; 2, 3, 4 dan 5 = dosis 1000, 2000, 4000 dan 8000 mg/kg bb; bb = berat badan; (-) = normal; (+) = ringan; (++) = sedang; (+++) = parah
Pada Tabel 4.5 terlihat pada kelompok kontrol, dosis 1000 dan 2000
mg/kg bb tidak terjadi kerusakan hepatosit, sedang pada dosis 4000 dan 8000
mg/kg bb terjadi kerusakan hepatosit yaitu degenerasi hidropik dan nekrosis
dengan tingkat keparahan ringan sampai parah.
Penggunaan bahan obat yang sama dalam jangka waktu panjang dapat
menyebabkan penumpukan metabolit dalam hati yang bersifat toksik terhadap
hepatosit (Donatus, 2001). Organ-organ tubuh akan bekerja keras untuk
menyaring dan membuang senyawa-senyawa yang tidak dibutuhkan oleh tubuh
(Nisa, dkk., 2012). Hasil gambar histopatologi dari organ hati dapat dilihat pada
Gambar 4.2.
Kelompok Jenis kerusakan hepatosit
Degenerasi hidropik Nekrosis
P1 - -
P2 - -
P3 - -
P4 ++ +
Gambar 4.2 Gambar histopatologi organ hati dengan perbesaran (10x40)
Keterangan: kelompok kontrol
1 = hepatosit; 2 = vena sentral; 3 = sinusoid
3 2
1 3
2
Keterangan: perlakuan dosis 1000 mg/kg bb
1 = hepatosit; 2 = vena sentral; 3 = sinusoid
3 2
1 3
2
Keterangan: perlakuan dosis 2000 mg/kg bb
1 = hepatosit; 2 = vena sentral; 3 = sinusoid
3 2
1 1
3 2
Keterangan: perlakuan dosis 4000 mg/kg bb
1 = degenerasi hidropik; 2 = kariopiknosis; 3 = karioreksis; 4 = kariolisis; 5 = vena sentral; 6 = sinusoid
6 5
4 3 2 1 6
5
Keterangan: perlakuan dosis 8000 mg/kg bb
1 = degenerasi hidropik; 2 = kariopiknosis; 3 = karioreksis; 4 = kariolisis; 5 = vena sentral; 6 = sinusoid
6 5
4 3 2 1 6
5
Berdasarkan gambar di atas dapat dilihat bahwa kelompok kontrol, dosis
1000 dan 2000 mg/kg bb menunjukkan gambaran histopatologi masih dalam
keadaan normal yaitu dengan menunjukkan hepatosit tersusun secara radial dalam
lobulus hati. Celah antara lempeng-lempeng ini mengandung sinusoid-sinusoid
kapiler yang dinamakan sinusoid hati. Sinusoid merupakan pembuluh yang
melebar tidak teratur dan hanya terdiri atas satu lapisan endotel yang tidak
kontinyu (Junqueira dan Corneiro, 2007). Pada dosis 4000 dosis 8000 mg/kg bb
hepatosit sudah mengalami kerusakan yaitu sebagian dari hepatosit sudah
mengalami degenerasi hidropik hal ini terjadi karena adanya gangguan membran
sel sehingga cairan masuk ke dalam sitoplasma dan sebagian juga terjadi nekrosis.
Kerusakan pada hati dapat terjadi oleh beberapa faktor yaitu onset pemaparan
yang terlalu lama, durasi pemaparan, dosis dan sel inang yang rentan (Jubb, dkk.,
1993).
Hasil histopatologi tersebut sesuai dengan pengukuran kadar ALT dimana
pada kelompok kontrol, dosis 1000 dan 2000 mg/kg bb rata-rata kadar ALT masih
dalam batas normal, sedangkan pada kelompok dosis 4000 dan 8000 mg/kg bb
rata-rata kadar ALT sudah di atas batas normal. Jika sel hati mengalami nekrosis
dapat segera dideteksi melalui peningkatan aktivitas enzim. Salah satu enzim yang
dihasilkan oleh hati dan peka terhadap kelainan fungsi hati adalah enzim ALT
(Elisma, dkk., 2009).
Hepatosit merupakan sebagian besar dari organ hati yang bertanggung
jawab terhadap metabolisme. Sel-sel ini terletak di antara sinusoid yang berisi
darah dan saluran empedu (Lu, 1995). Darah yang mengandung toksin dibawa
dari usus, masuk ke hati melalui vena porta kemudian melewati sinusoid menuju
Degenerasi hidropik merupakan peristiwa meningkatnya kadar air di
intraseluler yang menyebabkan sitoplasma dan organel-organel membengkak dan
membentuk vakuola-vakuola. Rusaknya permeabilitas membran sel menyebabkan
terhambatnya aliran Na+ keluar dari sel sehingga menyebabkan ion-ion dan air
masuk secara berlebihan kedalam sel. Degenerasi hidropik merupakan respon
awal sel terhadap bahan-bahan yang bersifat toksik, serta merupakan proses awal
dari kematian sel (Jones, et al., 1997; Cheville, 1999). Kadar Na+ intrasel diatur
oleh pompa Na+ yang memerlukan ATP, jika ATP berkurang maka akan
mengakibatkan masuknya Na+ ke intrasel melebihi jumlah normalnya (Priyanto,
2009).
Kerusakan sel secara terus-menerus akan mencapai suatu titik sehingga
terjadi kematian sel (Lu, 1995). Paparan zat toksik pada sel apabila cukup hebat
atau berlangsung cukup lama, maka sel tidak dapat lagi mengkompensasi dan
tidak dapat melanjutkan metabolisme (Priyanto, 2009). Inti sel yang mati dapat
terlihat lebih kecil dan menjadi lebih padat (kariopiknosis), hancur
bersegmen-segmen (karioreksis) dan kemudian inti sel menghilang (kariolisis) (Underwood,
1994). Nekrosis hati adalah kematian hepatosit yang umumnya merupakan
BAB V
KESIMPULAN DAN SARAN 5.1Kesimpulan
Berdasarkan penelitian yang telah dilakukan, maka kesimpulan dari
penelitian ini adalah:
a. EEBPJ pada kelompok kontrol, dosis 1000 dan 2000 mg/kg bb tidak
berpengaruh terhadap gejala toksik sedang dosis 4000 dan 8000 mg/kg bb
berpengaruh pada mencit jantan.
b. EEBPJ sampai dengan dosis 8000 mg/kg bb tidak berpengaruh terhadap berat
badan mencit jantan.
c. EEBPJ pada kelompok kontrol, dosis 1000 dan 2000 mg/kg bb tidak
memberikan efek toksik sedang dosis 4000 dan 8000 mg/kg bb memberikan
efek toksik pada organ hati mencit.
d. EEBPJ pada dosis 4000 mg/kg bb mulai toksik terhadap mencit jantan.
5.2Saran
Berdasarkan penelitian yang telah dilakukan, maka disarankan kepada
peneliti selanjutnya untuk menguji toksisitas kronik EEBPJ pada organ hati,
ginjal, jantung dan lain sebagainya dan menguji toksisitas khusus EEBPJ seperti
DAFTAR PUSTAKA
Adjirni dan saruni (2006). Penelitian Antiinflamasi dan Toksisitas Akut Ekstrak Akar Pepaya (Carica papaya L.) Pada Tikus Putih. Jurnal Cermin Dunia Kedokteran. 129(3): 42-44.
Anderson, J.W., Nicolosi R.J., and Borzelleca J.F. (2005). Glucosamine Effects In Humans: A Review Of Effects On Glucose Metabolism, Side Effects, Safety Considerations And Efficacy. Food and Chem Toxicol. 43(18): 675-687.
Anggraini, D.R. (2008). Gambaran Makroskopik dan Mikroskopik Hati dan Ginjal Mencit Akibat Pemberian Plumbum Asetat. Tesis. Medan: Sekolah Pascasarjana Universitas Sumatera Utara. Halaman 52.
Anonim. (2013). Pepaya. Diakses tanggal 20 September 2013.
Anonymous. (2009). Reference Values for Laboratory Animals, Normal Hematology Values. ReseachAnimal Resources. University of Minnesota. Page 275.
Arifin, H., Leny, S., dan Netty, M. (2006). Kajian Toksisitas Akut Ekstrak Etanol Daun Capo (Blumea Balsamifera L.) Dan Pengaruhnya Terhadap Gambaran Histologi Ginjal Mencit Putih Jantan. Jurnal Media farmasi. 14(2): 120-124.
Bauer, J.D. (1982). Clinical Laboratory Methods. 9th edition. The C.V. Mosby Company, London. page 578.
Budiman, A., Wulandari, R.S., dan Darma, E. (2010). Uji Aktivitas Antijerawat Sediaan Krim Ekstrak Daun Pepaya (Carica papaya L.) dan Madu Terhadap Bakteri Propionibacterium acne. Jurnal Farmaka. 8(2): 211-217.
BPOM. (2010). Acuan Sediaan Herbal. Volume Kelima Edisi Pertama. Jakarta: Badan Pengawas Obat dan Makanan RI Deputi Bidang Obat Tradisional, Kosmetik dan Produk Komplemen. Halaman 74.
BPOM. (2008). Taksonomi Koleksi Tanaman Obat Kebun Tanaman Obat Citeureup. Jakarta: Badan Pengawas Obat dan Makanan RI Deputi Bidang Obat Tradisional, Kosmetik dan Produk Komplemen. Halaman 20.
Cheville, N.F. (1999). Introduction to Veterinary Pathology. Ed ke-2. Iowa: Iowa State University Press. Page 214.
Dellmann, H.D., dan Brown, E. (1992). Buku Teks Histologi Veteriner I dan II. Penerjemah: Hartono. Jakarta: Universitas Indonesia. Halaman 376.
Dewoto, H.R. (2007). Pengembangan Obat Tradisional Indonesia Menjadi Fitofarmaka. Jurnal Maj Kedokt Indon. 57(7): 205-211.
Ditjen POM. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Cetakan Pertama. Jakarta: Departemen Kesehatan RI. Halaman 3-5, 10-11.
Donatus, A.I. (2001). Toksikologi Dasar. Yogyakarta: Fakultas Biofarmasi Universitas Gajahmada. Halaman 67-79.
Elisma, Arifin, H., dan Handayani, D. (2009) Pengaruh Fraksi Daun Sidaguri (Sida Rhombifolia L.) Terhadap Kadar Asam Urat Dan Uji Toksisitas Sub Akutnya pada Mencit Putih Jantan. Jurnal Cermin Dunia Kedokteran. 32(1): 15-19.
Elya, B., Amin, J., dan Emiyanah. (2010). Toksisitas Akut Daun Justicia gendarussa Burm. Jurnal Makara Sains. 14(2): 129-134.
Eroschenko, V.P. (2010). Atlas Histologi diFiro: dengan Korelasi Fungsional Edisi 11. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 325-334. Francisca, N. (2012). Uji Antimutagenik Fraksi Etilasetat Bunga Pepaya Jantan
(Carica papaya L.) Pada Mencit Yang Diinduksi Dengan Siklofosfamid. Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara.
Ganiswara, S.G. (1995). Farmakologi Dan Terapi. Edisi 4. Jakarta: Bagian Farmakologi Fakultas Kedokteran Universitas Indonesia. Halaman 763-764.
Gupta, D., and Bhardwaj, S. (2012). Study of Acute, Subacute and Chronic Toxicity Test. International Journal of Advanced Research in Pharmaceutical and Bio Sciences (IJARPB). 1(2): 103-114.
Hadi, S. (1995). Gastroenterologi. Edisi 6. Bandung: Alumni, pp: 400-12 ; 644-50.
Harada, T., Enotomo, A., Boorman, G., and Maronpot, R.R. (1999). Liver and Gallbladder. In: Maronpot RR. Pathology of The Mouse. Reference and Atlas. 1st ed. Cache River Press. Pages 120-141.
Hasti, S., Novita, G., dan Ramadhani, G.W. (2012). Toksisitas Sub Kronis Ekstrak Etanol Daun Beringin (Ficus benjamina L.) Terhadap Fungsi Ginjal Mencit Putih Betina. Jurnal Scientia. 2(1): 2087-5045.
Hendriani, R. (2007). Uji Toksisitas Subkronis Kombinasi Ekstrak Etanol Buah Mengkudu (Morinda citrifolia Linn.) Dan Rimpang Jahe Gajah (Zingiber officinale rosc.) Pada Tikus Wistar. Karya Ilmiah. 11(4): 312-316.