INTISARI
Tanaman pegagan adalah salah satu contoh tanaman yang digunakan dalam produk kosmetik tradisional berupa masker wajah. Penelitian ini bertujuan untuk mengetahui golongan senyawa yang memiliki aktivitas penangkap radikal bebas, UV protection, dan antibakteri pada ekstrak etanolik daun pegagan (Centella asiatica (L.) Urban.).
Ekstrak daun pegagan dibuat menggunakan pelarut etanol 90% v/v dengan metode maserasi. Kromatografi Lapis Tipis (KLT) dilakukan untuk mengetahui bercak senyawa aktif yang terkandung dalam ekstrak etanolik. Uji aktivitas penangkap radikal bebas dilakukan menggunakan metode DPPH, UV
protection menggunakan metode inhibition of bleaching of �- caroten, dan antibakteri menggunakan metode bioautografi kontak. Senyawa aktif diisolasi menggunakan kromatografi kolom sehingga didapatkan 2 isolat aktif yang kemudian diuji kembali aktivitas penangkap radikal bebas dengan metode DPPH, UV protection dengan metode inhibition of bleaching of �- karoten , dan antibakteri menggunakan metode disc diffusion.
Hasil penelitian yang diperoleh menunjukkan bahwa ekstrak etanolik daun pegagan memiliki aktivitas penangkap radikal bebas pada senyawa dengan Rf 0,14; 0,36; 0,46; 0,75; 0,88; 0,92. Senyawa yang memiliki aktivitas UV proteksi terdapat pada Rf 0,14-0,20 dan 0,73-0,74. Senyawa yang memiliki aktivitas antibakteri terhadap bakteri S. aureus terdapat pada Rf 0,16-0,17; 0,21-0,23; 0,29-0,34; 0,51-0,53. Isolat 1 dan isolat 2 yang didapat memiliki aktivitas penangkap radikal bebas dan isolat kedua memiliki aktivitas antibakteri, tetapi kedua isolat tidak memiliki aktivitas UV protection. Hasil identifikasi menunjukkan bahwa kedua isolat merupakan golongan senyawa terpenoid.
ABSTRACT
Pegagan is one example of a plant used in the traditional cosmetics product of a face masker. This research aims to identification of active principle that have activity free radical scavenger , UV protection , and antibacterial in ethanolic pegagan (Centella asiatica (L.) Urban.) leaf extract.
C. asiatica leaf extract prepared using ethanol 90% v/v with maceration
method. Thin Layer Chromatography (TLC) was conducted to determine spott of active compound contained in the ethanolic extracts. Activity of free radical scavenger was tested by DPPH method, UV protection using a method of inhibition of bleaching of β-carotene , and antibacterial using bioautografi contact method. The active compound were isolated using column chromatography to obtain 2 isolates active then tested again activity of free radical scavenger with DPPH method , UV protection by inhibition of bleaching of β-carotene method, and antibacterial use disc diffusion method.
The research results showed that ethanolic pegagan leaves extract have antioxidant activity in a compound with Rf 0,14; 0.36; 0,46; 0.75; 0,88; 0.92. Compounds that have UV protection activities Rf 0.14-0.20 and Rf 0.73-0.74. Compounds that have antibacterial activity against S. aureus bacteria Rf 0.16-0.17; 0.21-0.23; 0.29-0.34; 0.51-0.53. Isolate 1 and isolate 2 presented activity as free radical scavenger and the second isolate have antibacterial activity, but both of isolates did not have UV protection activities. Isolates identified as terpenoid compound.
ISOLASI DAN IDENTIFIKASI GOLONGAN SENYAWA AKTIF PENANGKAP RADIKAL BEBAS, ULTRAVIOLET PROTECTION, DAN
ANTIBAKTERI PADA EKSTRAK ETANOLIK DAUN PEGAGAN (Centella asiatica (L.) Urban.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh : Setio Agustin NIM : 118114181
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ISOLASI DAN IDENTIFIKASI GOLONGAN SENYAWA AKTIF PENANGKAP RADIKAL BEBAS, ULTRAVIOLET PROTECTION, DAN
ANTIBAKTERI PADA EKSTRAK ETANOLIK DAUN PEGAGAN (Centella asiatica (L.) Urban.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh : Setio Agustin NIM : 118114181
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
Persetujuan Pembimbing
ISOLASI DAN IDENTIFIKASI GOLONGAN SENYAWA AKTIF PENANGKAP RADIKAL BEBAS, ULTRAVIOLET PROTECTION, DAN
ANTIBAKTERI PADA EKSTRAK ETANOLIK DAUN PEGAGAN (Centella asiatica (L.) Urban.)
Skripsi yang diajukan oleh :
Setio Agustin
NIM : 118114181
telah disetujui oleh :
Pembimbing Utama
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma: Nama : Setio Agustin
Nomor mahasiswa : 118114181
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
ISOLASI DAN IDENTIFIKASI GOLONGAN SENYAWA AKTIF PENANGKAP RADIKAL BEBAS, ULTRAVIOLET PROTECTION, DAN
ANTIBAKTERI PADA EKSTRAK ETANOLIK DAUN PEGAGAN (Centella asiatica (L.) Urban.)
Beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama saya tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta Pada tanggal 19 Juni 2015 Yang menyatakan
Halaman Persembahan
Aku persembahkan karyaku ini untuk:
Tuhan Yesus dan Bunda Maria,
Keluargaku dan Aditya Tri Saputra tersayang
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka saya bersedia menanggung segala sanksi peraturan perundang-undangan yang berlaku.
Yogyakarta, 19 Juni 2015 Penulis
PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala berkat anugerah dan perlindungan, kasih dan sayang, serta tuntunan yang
diberikan sehingga skripsi berjudul “ISOLASI DAN IDENTIFIKASI GOLONGAN SENYAWA AKTIF PENANGKAP RADIKAL BEBAS, ULTRAVIOLET PROTECTION, DAN ANTIBAKTERI PADA EKSTRAK ETANOLIK DAUN PEGAGAN (Centella asiatica (L.) Urban.)” dapat terselesaikan dengan baik dan lancar.
Penulis menyadari bahwa penulisan skripsi ini tidak terlepas dari berbagai pihak. Kesempatan ini, penulis pergunakan untuk mengungkapkan rasa terima kasih kepada:
1. Ibu Aris Widayati, M. Si., Ph.D., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Bapak Dr. rer. nat. Yosi Bayu Murti, Apt. selaku Dosen Pembimbing Skripsi yang telah membimbing, mendampingi dan memberikan arahan, evaluasi serta kritik dan saran mulai dari pembuatan proposal penelitian hingga penulisan skripsi ini selesai.
3. Bapak Prof. Dr. C.J. Soegihardjo, Apt. selaku Dosen Penguji yang telah meluangkan waktu untuk memberikan kritik dan saran selama penulisan skripsi.
5. Bapak Yohanes Dwiatmaka, M. Si. selaku Dosen Pembimbing Akademik yang selalu memberikan motivasi dan bimbingan selama mengikuti perkuliahan.
6. Ibu Agustina Setiawati, M. Sc., Apt. selaku Kepala Penanggungjawab Laboratorium Fakultas Farmasi yang telah memberikan ijin dalam penggunaan semua fasilitas laboratorium untuk kepentingan penelitian skripsi.
7. Bapak Wagiran, Bapak Mukminin, Bapak Bimo, Bapak Parlan, serta semua laboran yang telah membantu selama proses penelitian di laboratorium. 8. Elyn Prameswari, Agustine Kurniawaty, Surya Adhi Nugraha, dan Skolastika
Feranda atas bantuannya baik tenaga maupun ide-ide cemerlangnya serta motivasi dalam suka dan duka selama penelitian di laboratorium.
9. Teman-teman FST dan FKK 2011 atas doa dan dukungan.
10. Semua pihak yang tidak dapat penulis sebutkan satu per satu sehingga penulis dapat menyelesaikan tugas akhir ini dengan baik.
Penulis menyadari bahwa naskah skripsi ini masih banyak kekurangan dengan keterbatasan yang ada sehingga penulis membuka diri terhadap semua kritik dan saran dari semua pihak yang membangun untuk kemajuan diri dan ilmu pengetahuan. Akhir kata, penulis berharap semoga naskah skripsi ini dapat bermanfaat bagi semua pihak terutama di Bidang Farmasi.
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... iv
HALAMAN PERSEMBAHAN... v
PERNYATAAN KEASLIAN KARYA ... vi
PRAKATA ... vii
B. Tujuan Penelitian ... 6
1. Tujuan umum ... 6
2. Tujuan khusus ... 6
BAB II PENELAAHAN PUSTAKA... 7
A. Pegagan (Centella asiatica (L.) Urban) ... 7
1. Klasifikasi tanaman ... 7
2. Uraian tanaman ... 7
3. Kandungan kimia ... 8
B. Polifenolik ... 9
D. Triterpenoid ... 10
E. Ekstraksi ... 10
1. Maserasi ... 10
2. Triturasi ... 11
F. Kromatografi ... 11
1. Kromatografi lapis tipis ... 12
2. Kromatografi kolom... 13
G. Antioksidan dan Uji Aktivitas Penangkap Radikal Bebas ... 13
1. Radikal bebas ... 13
2. Antioksidan ... 14
H. UV Protection dan Uji Aktivitas UV Protection ... 15
I. Antibakteri ... 17
1. Bioautografi ... 18
2. Disc Diffusion ... 19
J. Landasan Teori ... 19
K. Hipotesis ... 20
BAB III METODE PENELITIAN... 21
A. Jenis dan Rancangan Penelitian ... 21
B.Bahan dan Alat Penelitian ... 21
1. Bahan ... 21
2. Alat ... 22
C.Tata Cara Penelitian ... 22
1. Alur pengerjaan penelitian ... 22
2. Penyiapan simplisia ... 23
3. Perhitungan susut pengeringan simplisia ... 23
4. Ekstraksi ... 23
5. Susut pengeringan ekstrak ... 24
6. Uji kualitatif golongan senyawa ... 24
7. Uji kualitatif aktivitas penangkap radikal bebas ekstrak dan isolat ... 25
10.Uji kualitatif aktivitas antibakteri ... 27
11.Isolasi senyawa aktif ... 29
12.Alur pengerjaan isolasi senyawa aktif ... 30
BAB IV HASIL DAN PEMBAHASAN ... 31
A. Penyiapan Bahan, Penyerbukan dan Susut Pengeringan Serbuk Simplisia Daun Pegagan ... 31
B. Pembuatan Ekstrak Etanolik Daun Pegagan... 33
C. Optimasi Fase Gerak ... 36
D. Uji Kualitatif Aktivitas Penangkapan Radikal Bebas Ekstrak Etanolik ... 37
E. Uji Kualitatif Aktivitas UV Protection Ekstrak Etanolik ... 40
F. Uji Kualitatif Aktivitas Antibakteri Ekstrak Etanolik Menggunakan Metode Bioautografi ... 45
G. Isolasi Senyawa Aktif Pada Ekstrak Etanolik Daun Pegagan ... 50
1. Uji kualitatif aktivitas penangkap radikal bebas isolat ... 53
2. Uji kualitatif aktivitas UV protection isolat... 55
3. Uji kualitatif aktivitas antibakteri isolat menggunakan Metode Disc Diffusion ... 58
4. Uji kualitatif identifikasi senyawa aktif pada ekstrak etanolik dan isolat menggunakan reagen semprot... 63
BAB V KESIMPULAN DAN SARAN ... 71
A. Kesimpulan ... 71
B. Saran ... 71
DAFTAR PUSTAKA ... 72
LAMPIRAN ... 75
DAFTAR TABEL
Tabel 1. Uji Kualitatif Aktivitas Penangkap Radikal Bebas Ekstrak
Etanolik ... 40
Tabel 2. Uji Kualitatif Aktivitas UV Protection Ekstrak Etanolik ... 44
Tabel 3. Simpangan deviasi (SD) pengukuran uji kualitatif UV Protection pada ekstrak etanolik ... 45
Tabel 4. Uji kualitatif aktivitas antibakteri ekstrak terhadap bakteri E. coli menggunakan Metode Bioautografi ... 48
Tabel 5. Uji kualitatif aktivitas antibakteri ekstrak terhadap bakteri S. aureus menggunakan Metode Bioautografi ... 50
Tabel 6. Uji Kualitatif Aktivitas Penangkap Radikal Bebas Isolat 1 ... 54
Tabel 7. Uji Kualitatif Aktivitas Penangkap Radikal Bebas Isolat 2 ... 55
Tabel 8. Uji Kualitatif Aktivitas UV Protection Isolat 1 ... 57
Tabel 9. Uji Kualitatif Aktivitas UV Protection Isolat 2 ... 58
Tabel 10. Uji kualitatif aktivitas antibakteri isolat 1 terhadap bakteri S. aureus ... 60
Tabel 11. Uji kualitatif aktivitas antibakteri isolat 2 terhadap bakteri S. aureus ... 61
Tabel 12. Klasifikasi kekuatan aktivitas antibakteri ... 61
Tabel 13. Uji kualitatif aktivitas antibakteri Amoxicillin terhadap bakteri S. aureus ... 63
DAFTAR GAMBAR
Gambar 1. Senyawa radikal bebas DPPH dan Senyawa DPPH non radikal ... 15
Gambar 2. Bagan alur pengerjaan penelitian ... 22
Gambar 3. Bagan alur pengerjaan isolasi senyawa aktif ... 30
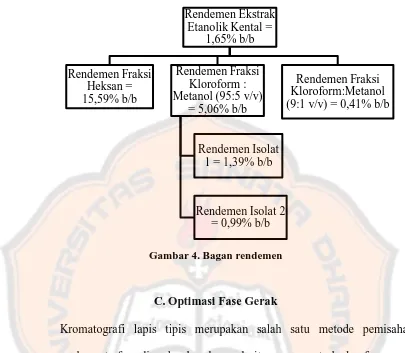
Gambar 4. Bagan rendemen ... 36
Gambar 5. Reaksi penangkapan radikal bebas DPPH oleh senyawa antioksidan ... 38
Gambar 6. Uji kualitatif aktivitas antioksidan menggunakan DPPH semprot ... 39
Gambar 7. Grafik hasil optimasi ketinggian lampu UV dalam pengujian aktivitas UV protection ... 42
Gambar 8. Uji kualitatif UV protection pada ekstrak etanolik ... 43
Gambar 9. Uji kualitatif aktivitas antibakteri ekstrak etanolik terhadap bakteri E. coli ... 48
Gambar 10. Uji kualitatif aktivitas antibakteri ekstrak etanolik terhadap bakteri S. aureus menggunakan metode bioautografi ... 49
Gambar 11. Uji Kualitatif Aktivitas Antioksidan Isolat 1 dan Isolat 2 ... 53
Gambar 12. Uji Kualitatif Aktivitas UV Protection Isolat 1 dan Isolat 2 ... 56
Gambar 13. Uji kualitatif aktivitas antibakteri Isolat 1 terhadap bakteri S. aureus ... 59
Gambar 14. Uji kualitatif aktivitas antibakteri Isolat 2 terhadap bakteri S. aureus ... 60
Gambar 15. Uji kualitatif aktivitas antibakteri Amoxicillin terhadap bakteri S. aureus ... 62
Gambar 16. Identifikasi golongan senyawa menggunakkan reagen semprot ... 64
Gambar 17. Identifikasi golongan senyawa isolat 1 menggunakan reagen semprot ... 68
DAFTAR LAMPIRAN
Lampiran 1. Formula kosmetik tradisional ... 76
Lampiran 2. Simplisia kering herba Pegagan (Centella asiatica (L.) Urban.) ... 77
Lampiran 3. Surat keterangan pembelian dan determinasi tanaman Pegagan (Centella asiatica (L.) Urban.) ... 78
Lampiran 4. Perhitungan susut pengeringan serbuk simplisia kering ... 80
Lampiran 5. Perhitungan berat serbuk simplisia untuk ekstraksi ... 81
Lampiran 7. Sertifikat hasil uji bakteri Staphylococcus aureus ATCC25923 ... 84
Lampiran 8. Sertifikat hasil uji bakteri Eschericia coli ATCC 25922 ... 85
Lampiran 9. Rangkaian alat lampu UV pada pengujian aktivitas UV protection ... 86
Lampiran 10. Alat pengukur intensitas cahaya lampu UV ... 87
Lampiran 11. Indikator warna untuk pembanding warna pada uji aktivitas UV protection ... 88
Lampiran 12. Optimasi intensitas cahaya lampu UV ... 89
Lampiran 13. Hasil pengujian aktivitas antibakteri ekstrak etanolik daun pegagan terhadap bakteri Eschericia coli metode bioautografi ... 90
Lampiran 14. Hasil pengujian antibakteri ekstrak etanolik daun pegagan terhadap bakteri Staphyloccocus aureus metode bioautografi ... 91
Lampiran 15. Hasil fraksinasi yang didapat dengan cara triturasi ... 92
Lampiran 16. Hasil pemisahan fraksi dengan kromatografi lapis tipis ... 93
Lampiran 17. Proses dan Hasil kromatografi kolom Lampiran 18. Hasil KLT isolat ... 94
Lampiran 18. Hasil KLT isolat ... 95
Lampiran 19. Hasil pengujian antibakteri isolat 1 terhadap bakteri S. aureus ... 96
Lampiran 20. Hasil pengujian antibakteri isolat 2 terhadap bakteri S. aureus ... 97
Lampiran 21. Hasil pengujian aktivitas UV protection isolat 1 ... 98
Lampiran 22. Hasil pengujian aktivitas UV protection isolat 2 ... 99
INTISARI
Tanaman pegagan adalah salah satu contoh tanaman yang digunakan dalam produk kosmetik tradisional berupa masker wajah. Penelitian ini bertujuan untuk mengetahui golongan senyawa yang memiliki aktivitas penangkap radikal bebas, UV protection, dan antibakteri pada ekstrak etanolik daun pegagan (Centella asiatica (L.) Urban.).
Ekstrak daun pegagan dibuat menggunakan pelarut etanol 90% v/v dengan metode maserasi. Kromatografi Lapis Tipis (KLT) dilakukan untuk mengetahui bercak senyawa aktif yang terkandung dalam ekstrak etanolik. Uji aktivitas penangkap radikal bebas dilakukan menggunakan metode DPPH, UV
protection menggunakan metode inhibition of bleaching of �- caroten, dan antibakteri menggunakan metode bioautografi kontak. Senyawa aktif diisolasi menggunakan kromatografi kolom sehingga didapatkan 2 isolat aktif yang kemudian diuji kembali aktivitas penangkap radikal bebas dengan metode DPPH, UV protection dengan metode inhibition of bleaching of �- karoten , dan antibakteri menggunakan metode disc diffusion.
Hasil penelitian yang diperoleh menunjukkan bahwa ekstrak etanolik daun pegagan memiliki aktivitas penangkap radikal bebas pada senyawa dengan Rf 0,14; 0,36; 0,46; 0,75; 0,88; 0,92. Senyawa yang memiliki aktivitas UV proteksi terdapat pada Rf 0,14-0,20 dan 0,73-0,74. Senyawa yang memiliki aktivitas antibakteri terhadap bakteri S. aureus terdapat pada Rf 0,16-0,17; 0,21-0,23; 0,29-0,34; 0,51-0,53. Isolat 1 dan isolat 2 yang didapat memiliki aktivitas penangkap radikal bebas dan isolat kedua memiliki aktivitas antibakteri, tetapi kedua isolat tidak memiliki aktivitas UV protection. Hasil identifikasi menunjukkan bahwa kedua isolat merupakan golongan senyawa terpenoid.
ABSTRACT
Pegagan is one example of a plant used in the traditional cosmetics product of a face masker. This research aims to identification of active principle that have activity free radical scavenger , UV protection , and antibacterial in ethanolic pegagan (Centella asiatica (L.) Urban.) leaf extract.
C. asiatica leaf extract prepared using ethanol 90% v/v with maceration
method. Thin Layer Chromatography (TLC) was conducted to determine spott of active compound contained in the ethanolic extracts. Activity of free radical scavenger was tested by DPPH method, UV protection using a method of inhibition of bleaching of β-carotene , and antibacterial using bioautografi contact method. The active compound were isolated using column chromatography to obtain 2 isolates active then tested again activity of free radical scavenger with DPPH method , UV protection by inhibition of bleaching of β-carotene method, and antibacterial use disc diffusion method.
The research results showed that ethanolic pegagan leaves extract have antioxidant activity in a compound with Rf 0,14; 0.36; 0,46; 0.75; 0,88; 0.92. Compounds that have UV protection activities Rf 0.14-0.20 and Rf 0.73-0.74. Compounds that have antibacterial activity against S. aureus bacteria Rf 0.16-0.17; 0.21-0.23; 0.29-0.34; 0.51-0.53. Isolate 1 and isolate 2 presented activity as free radical scavenger and the second isolate have antibacterial activity, but both of isolates did not have UV protection activities. Isolates identified as terpenoid compound.
BAB I PENGANTAR A.Latar Belakang
Kosmetik adalah setiap bahan yang dibutuhkan untuk digunakan dengan cara mengoleskan, menaburkan, maupun cara mengaplikasikan pada tubuh manusia lainnya untuk membersihkan, mempercantik, meningkatkan daya tarik, mengubah penampilan tubuh manusia, dan yang terpenting adalah untuk kesehatan kulit dan rambut di mana saat diaplikasikan pada tubuh akan memberikan sensasi segar (Mitsui, 1997).
Dalam kehidupan sehari-hari, masyarakat tidak dapat terlepas dengan penggunaan kosmetik. Kosmetik digunakan tidak hanya untuk menunjang penampilan seseorang, tetapi juga dipergunakan untuk melindungi tubuh bagian luar dari bahaya polusi, debu, dan sinar UV yang semakin meningkat. Polusi dan sinar UV dapat membentuk radikal bebas yang berbahaya bagi tubuh terutama pada bagian kulit sehingga dapat mengakibatkan terjadinya penuaan dini. Debu yang menempel pada kulit, jika tidak dibersihkan maka dapat mengakibatkan timbulnya jerawat dan akan diperparah dengan adanya infeksi bakteri.
Meningkatnya permintaan pasar terhadap produk kosmetik, memicu industri kosmetik berlomba–lomba untuk memproduksi produk kosmetik yang harganya dapat dijangkau oleh masyarakat. Kondisi inilah yang sering kali
dimanfaatkan oleh produsen “nakal” untuk memproduksi produk kosmetik
Produk kosmetik berbahaya ini sangat memberikan dampak negatif bagi penggunanya baik yang terlihat langsung dari penggunaan jangka pendek maupun efeknya yang timbul dalam penggunaan jangka panjang. Menurut Pusat Informasi Kosmetik Berbahaya di Indonesia (2013), penggunaan kosmetik berbahaya dapat menyebabkan gangguan pernapasan, kerusakan bagian tubuh, kanker, tumor, dan kerusakan sel otak. Menurut Ratnadita (2012), kasus efek samping penyakit kulit yang ditemui di Yogyakarta, 40% dikarenakan penggunaan produk kosmetik berbahaya.
Akibat produk kosmetik yang berbahaya inilah, penggunaan herbal dan jamu di masyarakat mulai kembali populer tidak hanya untuk pengobatan dan pencegahan tetapi berkembang sebagai bahan kosmetik yang berfungsi untuk mempertahankan atau meningkatkan kecantikan khususnya bagi kaum wanita (Yuliarti, 2010). Masyarakat pun mulai kembali menggunakan kosmetik yang terbuat dari bahan alam di mana resiko bahaya yang timbul minimum dan relatif aman.
Brzezińska, 2013). Pegagan juga banyak digunakan sebagai bahan kosmetik karena memiliki aktivitas antibakterial yang terdapat pada kulit (Kedzia, Kozlowska, Furnamowa, Mikolajczak, Kedzia, dan Kozaryn, 2007). Besarnya manfaat dari tanaman pegagan ini maka penelitian ini dilakukan untuk mengetahui adanya aktivitas penangkap radikal bebas
1,1-diphenyl-2-picrylhydrazyl (DPPH), UV protection, dan antibakteri serta dapat mengetahui
golongan senyawa aktif yang bertanggungjawab terhadap adanya aktivitas penangkap radikal bebas, UV protection, dan antibakteri pada ekstrak etanolik daun pegagan.
1. Rumusan masalah
a. Apakah ekstrak etanolik daun pegagan memiliki aktivitas penangkap radikal bebas DPPH, UV protection, dan antibakteri?
b. Golongan senyawa apa saja yang bertanggungjawab terhadap aktivitas penangkap radikal bebas DPPH, UV protection, dan antibakteri pada ekstrak etanolik daun pegagan?
2. Keaslian penelitian
metode DPPH scavenging activity juga pernah dilakukan oleh Kedzia et al. (2013) menggunakan ekstrak etanolik 30% dan 60%.
Tidak hanya aktivitas antioksidan yang mendukung daun pegagan dapat dijadikan sebagai bahan kosmetik tetapi juga potensi ekstrak pegagan yang telah diteliti oleh Zaidan (2005) yang menunjukkan aktivitas antibakteri terhadap S.
aureus dan Methycillin Resistant S. aureus (MRSA) menggunakan metode difusi.
Aktivitas antibakteri juga pernah diteliti menggunakan metode dilusi oleh Kedzia
et al. (2013) yang menunjukkan bahwa ekstrak etanolik 30% dapat menghambat
bakteri S. aureus.
Penelitian terhadap analisis kualitatif kandungan kimia yang terdapat pada bagian akar dan daun dari pegagan menggunakan kromatografi lapis tipis juga pernah dilakukan oleh Biradar dan Rachetti (2013) di mana bagian akar dan daun pegagan diekstraksi menggunakan metode maserasi dengan pelarut etanol absolut selama 72 jam. Ekstrak dianalisis menggunakan kromatografi lapis tipis dengan berbagai sistem fase gerak yaitu metanol : amonium hidroksida (17:3 v/v), kloroform : metanol (18:2 v/v), kloroform : asam asetat glasial : metanol : air (6:2:2:1 v/v), benzena : etil asetat (1:1 v/v).
penelitian menggunakan kromatografi lapis tipis dengan fase gerak kloroform : metanol (95:5 v/v) untuk melakukan skrining senyawa aktif antioksidan, UV proteksi dan antibakteri. Pada daun pegagan juga belum pernah ada yang melakukan menggunakan metode metode penghambat pemutihan (inhibition of
bleaching of �-caroten) untuk menguji aktivitas UV protection. Selain itu, belum
pernah dilakukan skrining senyawa aktif antibakteri ekstrak etanolik daun pegagan menggunakan metode bioautografi. Isolasi senyawa aktif pada ekstrak etanol 90% menggunakan kromatografi kolom dengan cara step gradient
chromatography dan menguji aktivitas penangkap radikal bebas menggunakan
metode DPPH, UV protection menggunakan metode inhibition of bleaching of � -caroten, antibakteri menggunakan metode disc diffusion, dan menguji golongan
senyawa isolat aktif yang didapat secara kualitatif belum pernah dilakukan.
3. Manfaat penelitian
a. Manfaat teoritis
b. Manfaat praktis
Hasil penelitian ini diharapkan mampu membuktikan keefektifitasan tanaman pegagan sehingga dapat meningkatkan pemanfaatannya sebagai bahan kosmetik tradisional yang berkualitas.
B. Tujuan Penelitian
1. Tujuan umum
Tujuan umum dari penelitian ini adalah mengetahui aktivitas dan golongan senyawa aktif penangkap radikal bebas, UV protection, dan antibakteri yang terdapat pada ekstrak etanolik daun pegagan sehingga dapat dibuktikan khasiatnya sebagai bahan kosmetik.
2. Tujuan khusus
Tujuan khusus dari penelitian ini adalah sebagai berikut.
a. Mengetahui golongan senyawa isolat aktif dari ekstrak etanolik daun pegagan dalam menghambat aktivitas radikal bebas DPPH.
b. Mengetahui golongan senyawa isolat aktif dari ekstrak etanolik daun pegagan yang dapat melindungi β-karoten dan menghambat efek paparan sinar UV.
BAB II
PENELAAHAN PUSTAKA A. Pegagan (Centella asiatica (L.) Urban)
1. Klasifikasi tanaman menurut United States Departement of Agriculture : Kingdom : Plantae
Subkingdom : Tracheobionta
Superdivision : Spermatophyta
Division : Mangnoliophyta
Class : Dicotyledoneae
Subclass : Rosidae
Ordo : Apiales
Family : Apiaceae
Genus : Centella
Species : Centella asiatica (L.). Urb.
Nama Indonesia : Pegagan
2. Uraian tanaman
berambut. Panjang tangkai daun mencapai 50 mm, helai daun berbentuk ginjal, lebar dan bundar dengan garis tengah 1-7 cm, dan tepi daun beringgit (Depkes RI, 2009).
Pegagan banyak hidup di daerah tropis, sub-tropis, dan dapat berkembang subur di daerah lembab seperti daerah berawa di India, Sri Lanka, Madagaskar, Afrika, Australia, China, Indonesia, Malaysia, Australia, Afrika Selatan dan Tengah (James dan Dubery, 2009).
3. Kandungan kimia
Ekstrak tanaman pegagan memiliki aktivitas biologis, khususnya penyembuhan luka yang berhubungan dengan antimikroba, antiinflamasi, antioksidan, dan imunostimulan. Aktivitas tersebut ditimbulkan dengan adanya respon dari derivat triterpenoid yaitu asam asiatat dan asiatikosida, fenolik, flavonoid, dan minyak atsiri (Kedzia, et. al., 2007). Ekstrak etanolik 50% tanaman pegagan mengandung polifenolik 45 μg/mg ekstrak, flavonoid 14,6 μg/mg ekstrak, β-karoten 0,7 μg/mg ekstrak, tanin 59,7 μg/mg ekstrak, Vitamin C 9,5
μg/mg ekstrak (Rahman, 2013).
dalam bentuk glikosidanya yaitu brahminosida, madasiatikosida dan centellosida (Bylka, et. al., 2013).
Aktivitas antibakteri dalam tanaman pegagan karena adanya kandungan saponin triterpenoid pentasiklik, terutama asam asiatat dan asam madekasat (James dan Dubery, 2009). Dari hasil penelitian yang dilakukan oleh Kedzia (2013), pada ekstrak etanolik 30% memiliki aktivitas antibakterial yang paling baik jika dibandingkan dengan ekstrak etanolik 60% dengan menunjukkan hasil MIC dari ekstrak etanolik 30%, yaitu 1000μg/mL dan MIC dari ekstrak etanolik 60%, yaitu >1000 μg/mL.
B.Polifenolik
Polifenolik adalah suatu metabolit sekunder yang ada pada tanaman. Karakteristik struktur dari polifenolik sendiri adalah memiliki satu atau lebih dari enam karbon dengan cincin aromatik dan terdapat dua atau lebih gugus fenolik yaitu gugus hidroksil yang langsung berikatan dengan cincin aromatik. Polifenolik yang terdapat pada tanaman memiliki fungsi yang berbeda – beda yaitu sebagai pemberi warna pada bagian bunga, daun, dan buah, juga berfungsi sebagai antimikrobial, anti jamur, melindungi dari kerusakan akibat radiasi UV, dan sebagai antioksidan (Stevenson dan Hurst, 2007).
C.Flavonoid
berdasarkan skeleton yang menyusunnya yaitu flavon, flavonol, antisianidin, dan katekin. Flavonoid sangat bermanfaat untuk antioksidan di mana dengan adanya gugus fenolik aktivitas antioksidan dapat merusak radikal bebas (Dewick, 2002).
D. Triterpenoid
Terpen merupakan metabolit sekunder yang jumlahnya pada tanaman paling besar. Terpen dapat dibiosintesis dari unit isoprene yang memiliki struktur siklik dan diklasifikasikan berdasarkan jumlah unit isoprene C5 penyusunnya,
yaitu monoterpen (C10), sesquiterpen (C15), diterpen (C20), sesterpen (C25),
triterpen (C30), karotenoid (C40), dan politerpen yang memiliki unit isopren yang
sangat panjang. Pada tanaman pegagan terdapat banyak saponin triterpen pentasiklik yang disintesis melalui jalur isoprenoid. Saponin triterpenoid yang terkandung dalam pegagan memiliki kontribusi terhadap aktivitas biologis dari tanaman tersebut sebagai antibakterial (James dan Dubery, 2009).
E. Ekstraksi
Ekstraksi merupakan salah satu teknik pemisahan suatu senyawa berdasarkan distribusi zat dalam pelarut yang digunakan. Ekstraksi secara umum dilakukan menggunakan dua pelarut yang berbeda di mana kelarutan zat pada pelarut kedua lebih besar daripada pelarut pertama (Dirjen POM, 1996).
1. Maserasi
sel melewati dinding sel. Isi sel akan larut karena adanya perbedaan konsentrasi antara larutan di dalam sel dengan di luar sel. Larutan yang konsentrasinya tinggi akan terdesak keluar dan digantikan oleh cairan penyari dengan konsentrasi rendah melalui proses difusi. Peristiwa tersebut berulang sampai terjadi keseimbangan konsentrasi antara larutan di luar sel dan di dalam sel. Selama proses maserasi berlangsung dilakukan pengadukan dan penggantian cairan penyari setiap hari. Endapan yang diperoleh dipisahkan dan filtratnya dipekatkan (Sudjadi, 1986).
2. Triturasi
Triturasi merupakan salah satu teknik pemurnian yang digunakan pada sampel dengan berat kurang dari 500 mg bertujuan untuk menghilangkan sampel dari keadaan bergetah dan pengotor bersifat non polar. Untuk menghilangkan getah maka dapat dilakukan dengan cara ditumbuk. Untuk menghilangkan pengotor yang bersifat non polar maka dapat dilakukan dengan melarutkannya menggunakan pelarut non polar, seperti ; n-heksana, n-pentana, dietil eter (Zala, et
al., 2012).
F. Kromatografi
1. Kromatografi lapis tipis
Kromatografi Lapis Tipis (KLT) merupakan bentuk kromatografi planar di mana fase diamnya berupa lapisan yang seragam pada permukaan bidang datar yang didukung oleh lempeng kaca, pelat aluminium, atau pelat plastik. Fase diam yang digunakan dalam KLT merupakan penjerap berukuran kecil dengan diameter partikel antara 10-30 μm. Semakin kecil ukuran rata–rata partikel fase diam dan semakin sempit kisaran ukuran fase diam, maka semakin baik kinerja KLT dalam hal efisiensi dan resolusinya. Fase gerak pada KLT yang disebut sebagai pelarut pengembang akan bergerak sepanjang fase diam karena pengaruh kapiler pada pengembangan secara menaik (ascending), atau karena pengaruh gravitasi pada pengembangan secara menurun (descending). Sistem yang paling sederhana ialah campuran dua pelarut organik, karena daya elusi campuran kedua pelarut dapat mudah diatur sedemikian rupa sehingga didapatkan pemisahan yang optimal (Gandjar dan Rohman, 2007).
KLT pada umumnya digunakan untuk analisis kualitatif dengan cara membandingkan nilai Rf solut dengan nilai Rf senyawa baku. Nilai retardasi
factor (Rf) dapat menggambarkan pemisahan yang terjadi pada kromatografi
planar. Nilai Rf dapat dihitung menggunakan perbandingan melalui persamaan : Nilai Rf = �� � �
�� � � � �
2. Kromatografi kolom
Kromatografi kolom secara umum digunakan sebagai salah satu teknik pemurnian dengan tujuan untuk dapat mengisolasi suatu komponen dari suatu campuran. Step gradient elution merupakan perubahan komposisi fase gerak pada umumnya digunakan dalam analisis kromatografi cair untuk mempersingkat durasi analisis. Perubahan ini memungkinkan untuk beralih langsung dari fase gerak pertama menjadi fase gerak kedua dengan perbedaan kekuatan elusi atau polaritas secara bertahap (Wu, Liang, dan Berthod, 2013).
G. Antioksidan dan Uji Aktivitas Penangkap Radikal Bebas
1. Radikal bebas
2. Antioksidan
Antioksidan dapat terkandung dalam vitamin, mineral, dan bioflavonoida alamiah yang dapat berguna dalam menetralkan radikal bebas. Antioksidan ini bekerja dengan cara mendonorkan atom hidrogen pada radikal hidroksi membentuk molekul air yang tidak berbahaya (Youngson, 2003).
Pada tubuh manusia, memliki suatu jaringan pelindung yang terdiri dari antioksidan alamiah yang mudah dioksidasi (menyerahkan elektron) sehingga dapat menetralkan adanya radikal bebas. Antioksidan yang terpenting adalah vitamin A, C, dan E, serta enzim-enzim alamiah glutathionperoxydase (GPx),
superoxide-dismutase (SOD) dan katalase. Adanya kandungan antioksidan pada
senyawa bioflavon terbukti dapat berkhasiat sebagai antitumor, antilipidermia, anti-arterosklerosis (Tjay, 2007).
Berbagai macam model in vitro kimia telah dikembangkan untuk menilai kemampuan untuk mencegah kerusakan oksidatif, di antaranya tes kimia mengukur kapasitas radikal menggunakan metode DPPH. Menurut Molyneux (2004), dasar dari metode DPPH adalah adanya pereduksian warna. DPPH adalah suatu radikal bebas yang bila dicampurkan dengan suatu senyawa yang dapat mendonorkan atom hidrogren sehingga membentuk senyawa tereduksi dan kehilangan warna violet. Reaksi yang terjadi, radikal bebas DPPH disimbolkan sebagai Z* dan senyawa pendonor atom hidrogen disimbolkan sebagai AH :
Gambar 1. Senyawa radikal bebas DPPH (1) dan Senyawa DPPH non radikal (2)
H. UV Protection dan Uji Aktivitas UV Protection
Fotoproteksi dapat dicapai dengan menghindari sinar matahari, berpakaian dan penggunaan tabir surya yang mengandung organik dan anorganik UV filter. Penggunaan tabir surya secara teratur dapat mengurangi efek berbahaya yang disebabkan oleh paparan jangka panjang terhadap radiasi UVB dan UVA (Osterwalder, Jung, Seifert, dan Herrling, 2009).
Zat yang aktif sebagai sunscreen dimaksudkan dapat menyerap setidaknya 85% dari radiasi sinar UV-B pada panjang gelombang 290-320 nm dan sinar UV-A pada panjang gelombang 320-400 nm. Zat aktif sunscreen yang banyak digunakan merupakan bahan anargonik yaitu titan dioksida dan zinc oksida dengan mekanisme kerja merefleksikan sinar ultraviolet (Farage, 2010).
Aktivitas UV Protection dapat diuji menggunkan metode inhibition of
bleaching of �-caroten di mana KLT ekstrak uji yang sudah kering disemprot
menggunakan larutan 0,05% β-karoten dalam kloroform kemudian dipaparkan pada sinar UV 366 nm. Senyawa aktif berwarna kuning-orange dengan
background pelat berwarna putih, menunjukkan bahwa senyawa tersebut dapat
melindungi β-karoten yang sensitif terhadap cahaya (Marston,2011).
I. Antibakteri
Bakteri merupakan sumber penyebab penyakit yang banyak terjadi. Bakteri secara global dibagi menjadi dua kelompok besar, yaitu bakteri Gram positif dan bakteri Gram negatif. Bakteri Gram positif memiliki dinding sel yang lebih sederhana. Staphylococcus aureus merupakan salah satu bakteri Gram positif yang termasuk dalam family Micrococcaceae. Bakteri S. aureus dapat menyebabkan infeksi pada manusia terutama infeksi yang terjadi pada kulit.
Escherichia coli yang termasuk dalam family Enterobacteriaceae merupakan salah
satu bakteri Gram negatif. Bakteri Gram negatif memiliki membran luar yang tersusun dari liposakarida-endotoksi yang menyebabkan toksisitas. Bakteri E. coli dapat menyebabkan infeksi pada manusia terutama menyerang sistem pencernaan (Campbell, Reece, dan Mitchell, 2003).
1. Zat bakterisida, merupakan suatu senyawa di mana pada dosis kecil dapat mematikan mikroba.
2. Zat bakteriostatis, merupakan suatu senyawa di mana pada dosis kecil dapat menghentikan pertumbuhan dan menghambat perbanyakan mikroba (Tjay,2007).
Aktivitas antibakteri dibuktikan melalui pengujian untuk mengatahui kemampuan suatu senyawa dalam mengahambat atau membunuh bakteri. Metode yang dapat digunakan dalam pengujian aktivitas antibakteri dibedakan menjadi dua, yaitu metode difusi dan metode dilusi. Metode difusi digunakan untuk mengukur potensi antibakteri berdasarkan luas zona jernih yang terbentuk disekitar tempat penginokulasian obat karena terdifusinya obat (Jawetz, Melnick, Brooks, dan Adelberg, 2005).
Metode difusi dapat dilakukan dengan berbagai cara.
1. Bioautografi
Uji bioautografi sering dilakukan untuk skrining senyawa yang aktif sebagai antibakteri. Bioautografi merupakan suatu metode kromatografi lapis tipis di mana komponen aktif dipisahkan menggunakan pelat kromatografi yang kemudian pelat tersebut diinkubasi pada media agar yang sudah berisi bakteri uji. Hasil yang dapat memberikan zona jernih dari media agar mengekspresikan aktivitas suatu senyawa yang sudah terpisah pada pelat KLT (Purkayastha dan Dahiya, 2012).
metode bioutografi kontak, pelat KLT diletakkan pada media agar yang sudah diinolukasikan bakteri uji selama beberapa menit atau jam untuk senyawa dapat berdifusi. Kemudian, pelat KLT diambil dan media agar diinkubasi. Hasil positif ditunjukkan dengan adanya zona hambat pada tempat senyawa aktif antibakteri sesuai dengan kontak pelat KLT pada media agar (Choma dan Gerzelak, 2011).
2. Disc Diffusion
Metode cakram kertas (Disc diffusion) merupakan salah satu metode difusi lainnya yang dapat menggambarkan potensi antibakteri karena adanya difusi obat sehingga dapat menghambat pertumbuhan bakteri. Hasil uji menggunakan disc diffusion terlihat dengan terbentuknya zona jernih dan pengukuran dilakukan dengan menghitung rata–rata dari zona jernih yang dihasilkan (Hermawan, Eliyani, dan Tyasningsih, 2007).
J. Landasan Teori
Kosmetik merupakan suatu kebutuhan yang wajib digunakan oleh manusia dengan tujuan mempercantik, merawat, maupun melindungi kulit dari debu, polusi, dan paparan sinar matahari. Sekarang ini, masyarakat mulai kembali menggunakan kosmetik tradisional karena penggunaannya yang relatif lebih aman daripada kosmetik bahan kimia.
polifenolik, flavonoid yang dapat memberikan aktivitas farmakologis. Seiring dengan berkembangnya kosmetik tradisional, semakin banyak pula kosmetik yang beredar di pasaran dengan komposisi bahan herbal salah saatunya adalah masker wajah ekstrak daun pegagan yang diklaim dapat memperhalus kulit wajah dan sebagai masker merawat kulit wajah yang berjerawat.
Aktivitas antioksidan, UV protection, dan antibakteri dilakukan untuk menguji kandungan senyawa apa yang berperan aktif dalam memberikan aktivitas tersebut dalam ektstrak etanolik daun pegagan, dengan demikian untuk mengetahui kandungan senyawa dilakukan pengecekan menggunakan kromatografi lapis tipis sehingga senyawa bioaktif dapat terpisah menjadi beberapa komponen berdasarkan sifat polaritasnya.
Penelitian yang dilakukan ini diharapkan dapat memberikan informasi kepada masyarakat tentang manfaat tanaman pegagan terutama bagian daunnya terkait aktivitasnya sebagai penangkap radikal bebas, UV protection, dan antibakteri.
K. Hipotesis
Daun pegagan mengandung senyawa kimia terpenoid, flavonoid, fenolik, dan minyak atsiri yang dapat memberikan aktivitas penangkap radikal bebas, UV
BAB III
METODE PENELITIAN A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksploratif. Penelitian dilakukan di Laboratorium Farmakognogsi-Fitokimia dan Laboratorium Mikrobiologi Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
B. Bahan dan Alat Penelitian 1. Bahan
Bahan yang digunakan pada penelitian ini adalah simplisia kering daun pegagan sebanyak 1 kg yang didapatkan dari Balai Besar Penelitian dan Pengembangan Tanaman Obat dan Obat Tradisional (B2P2TOOT) Tawangmangu, Karanganyar, Jawa Tengah. Bahan kimia yang digunakan berupa bahan kualitas pro analitik Sigma hem. Co., USA yaitu DPPH dan β-karoten. Pelarut kualitias pro analitik dari Merck, yaitu kloroform, etanol, metanol, n-heksana, etil asetat, asam formiat, dan asam asetat glasial. TLC silica gel 60 F254
dan silica gel 60 (0,040-0,063) dari Merck. Bahan kualitas teknis dari Brataco Chemica yaitu ethanol 96% v/v ethanol 96% v/v antiseptik, dan aquadest. Kultur bakteri uji S. aureus, E. coli, media pertumbuhan bakteri berupa Mueller Hinton
Agar (MHA) dari Merck didapat dari Laboratorium Balai Kesehatan Yogyakarta.
2. Alat
Alat yang digunakan pada penelitian ini adalah vortex (Junke & Kunkel),
rotary vacuum evaporator (Buchi Labortechnik AG CH-9230), waterbath
(Memmert), mikropipet 10-1000 μL; 1-10 mL (Acura 825, Socorex), timbangan analitik digital (Scaltec SBC 22, BP 160P), autoclave (YX – 400Z), oven (WTE binder), cawan petri, cawan porselin, sendok, bunsen, jarum ose, tabung kaca, mikrotube, pipa kapiler (Brand), corong, kain mori, kertas saring no. 41 (Whatman), tabung reaksi bertutup dan alat-alat gelas yang lazim digunakan di laboratorium analisis (Pyrex-Germany dan Iwaki).
C. Tata Cara Penelitian 1. Alur pengerjaan penelitian
Pembelian bahan
Maserasi menggunakan etanol 90% v/v evaporasi
Uji kualitatif aktivitas
Uji kualitatif aktivitas pada isolat
2. Penyiapan simplisia
Bahan penelitian yang digunakan yaitu bagian daun pegagan yang sudah kering sebanyak 1 kg yang didapatkan dari B2P2TOOT dan sudah dideterminasi. Simplisia kering disortasi kering untuk menghilangkan pengotor yang ada, kemudian dihaluskan kasar menggunakan blender.
3. Perhitungan susut pengeringan simplisia
Serbuk simplisia ditimbang sebanyak 1 g menggunakan cawan petri. cawan petri yang berisi serbuk simplisia ditimbang sebagai berat pada waktu 0 menit. Panaskan menggunakan oven dengan suhu 105℃ tiap 30 menit kemudian didiamkan pada desikator selama 10 menit dilakukan sampai memperoleh bobot tetap. Replikasi dilakukan sebanyak tiga kali.
4. Ekstraksi
5. Susut pengeringan ekstrak
Ekstrak kental ditimbang sebanyak 1 g menggunakan cawan petri yang sudah ditimbang berat kosongnya. Cawan petri yang berisi ekstrak kental ditimbang sebagai berat pada waktu 0 menit. Panaskan menggunakan oven dengan suhu 105℃ tiap 30 menit kemudian didiamkan pada desikator selama 10 menit dilakukan sampai memperoleh bobot tetap. Replikasi dilakukan sebanyak tiga kali.
6. Uji kualitatif golongan senyawa
a. Optimasi fase gerak
Berbagai macam fase gerak dibuat dengan perbandingan : 1) n-heksana : etil asetat (2:3 v/v)
2) kloroform : metanol (7:3 v/v) 3) kloroform : metanol (9:1 v/v) 4) kloroform : metanol (95:5 v/v)
5) etil asetat : asam formiat : asam asetat glasial : air (100:11:11:20 v/v)
b. Uji kualitatif golongan senyawa
Enam buah pelat KLT yang sudah dielusi dibiarkan beberapa saat untuk menghilangkan pelarut fase gerak yang masih tersisa pada pelat KLT. Satu buah pelat KLT dilihat dibawah lampu UV 254 nm dan 360 nm beri tanda pada spot pemisahan yang meredam atau berpendar. Lima buah pelat disemprotkan pelat KLT tersebut dengan reagen semprot :
1) AlCl3
2) FeCl3
3) Dragendroff
4) Vanilin-asam sulfat 5) Sitroborat
Nilai Rf tiap spot senyawa yang muncul dihitung.
7. Uji kualitatif aktivitas penangkap radikal bebas ekstrak dan isolat
Pelat KLT disiapkan untuk pengujian, totolkan larutan ekstrak konsentrasi 5 mg/mL dan isolat konsentrasi 1 mg/mL (ditotolkan hingga mendapatkan mass loading 10 μg, 20 μg, dan 30 μg), kemudian dielusikan pada fase gerak yang sudah dipilih paling optimal. Satu buah pelat untuk kontrol dan satu buah untuk disemprotkan menggunakan larutan DPPH 0,25mg/10mL metanol. Hitung nilai Rf pada spot pemisahan yang dapat menghambat DPPH dengan memberikan warna ungu yang memudar hingga kekuningan.
8. Optimasi ketinggian lampu UV dan waktu perlakuan
dasar, 50 cm dari dasar, dan 35 cm dari dasar. Ditiap perbedaan ketinggian diukur intensitas cahaya lampu UV dengan alat lightmeter. Ditiap perbedaan ketinggian, pelat KLT yang sudah dicelupkan ke dalam larutan �-karoten dan dimasukkan ke dalam rangkaian alat dengan lampu UV yang menyala. Diukur perubahan warnanya menggunakan indikator warna tiap menit hingga 15 menit. Perubahan warna setiap diamati tiap 0, 1, 3, 6, 9, 12, dan 15 menit.
9. Uji kualitatif aktivitas UV protection ekstrak dan isolat
10. Uji kualitatif aktivitas antibakteri
Seluruh pekerjaan dilakukan secara aseptis menggunakan bunsen dan alkohol antiseptik.
a. Pembuatan media pertumbuhan 1) Media padat
Triptic Soy Broth (TSB) ditimbang sebanyak 6 g dan agar sebanyak 2,4 g. TSB dilarutkan kedalam aquadest 300 mL sambil dipanaskan. Tambahakan agar sedikit demi sedikit hingga homogen dan campuran menjadi bening. Autoklaf selama 15 menit. Selagi masih panas, tuangkan media pada cawan petri yang sudah disterilisasi.
2) Media cair
TSB ditimbang sebanyak 3 g dan larutkan kedalam erlenmeyer berisi aquadest 100 mL sambil dipanaskan. Aduk hingga homogen kemudian autoklaf selama 15 menit. Selagi panas pindahkan ke dalam tabung reaksi bertutup.
b. Pengawetan bakteri
gliserol 50μL, lakukan hingga habis kemudian ditutup rapat. Kultur bakteri diinkubasi dalam inkubator selama 1 jam kemudian disimpan di freezer.
c. Pembuatan kultur bakteri uji
Satu tabung eppendrof berisi bakteri S. aureus dan satu tabung berisi bakteri E. coli disiapkan. Pada tabung reaksi yang berisi cairan fisiologis 0,9% sebanyak 10 mL ditambahkan koloni bakteri yang sudah siap tetes demi tetes hingga sama dengan MacFarland 0,5 yang setara dengan jumlah bakteri (1,5x108 CFU).
d. Perlakuan uji kualitatif aktivitas antibakteri ekstrak menggunakan metode bioautografi
Pada cawan petri yang berisi media padat, digoreskan menggunakan cottonbud steril yang sudah dimasukkan dalam larutan bakteri uji yang sudah disiapkan secara merata keseluruh bagian.
Tiga buah pelat KLT disiapkan dengan lebar 1 cm. dengan larutan ekstrak 5mg/mL ditotolkan sebanyak 15μL, 20μL, 30μL. Kemudian elusi menggunakan fase gerak yang optimal. Tunggu 30 menit untuk menghilangkan sisa pelarut fase gerak yang digunakan.
e. Uji kualitatif aktivitas antibakteri isolat menggunakan metode disc diffusion
Larutan isolat disiapkan dengan konsentrasi 1mg/mL. Diambil
larutan isolat sebanyak 50 μL, 75 μL, dan 100 μL kemudian kering uapkan
larutan tersebut pada paper disc blank. Media Muller Hilton yang sudah memadat diinokulasikan bakteri S. aureus dengan teknik streak hingga merata, kemudian diinkubasi pada suhu ruang selama 30 menit. Paper disc isolat yang sudah siap diinokulasikan pada media yang sudah ditumbuhi bakteri dan diinkubasi selama 24 jam. Amati zona jernih yang terbentuk dan diukur besar diameternya.
11. Isolasi senyawa aktif
a. Triturasi
Ekstrak kental dan seasand ditimbang sebanyak 5 g. Keduanya dicampurkan dengan cara digerus sambil ditetesi menggunakan metanol secukupnya untuk mempermudahkan homogenisasi dan diibiarkan satu malam untuk menghilangkan metanol yang ditambahkan. Campuran ekstrak dipindahkan ke dalam tube sentrifuge hingga tanda volume 1 kemudian ditambahkan pelarut n-heksana hingga tanda volume 3. Tube divortex hingga homogen kemudian disentrifuge selama 10 menit.
Supernatant yang terbentuk diambil dan disaring, lalu diuapkan. Endapan
b. Kromatografi kolom
Fraksi ekstrak dari hasil triturasi menggunakan pelarut kloroform : metanol (95:5 v/v) dicampurkan dengan serbuk silika gel masing-masing sebanyak 300 mg kemudian digerus hingga homogen. Packing kolom yang digunakan dengan urutan susunan : kapas, silika gel setinggi 2 cm, ekstrak setinggi 0,5 cm, silika gel setinggi 1 cm, dan tutup dengan kapas. Masukkan eluen secara bergradien menggunakan pelarut yang sesuai yaitu 10 mL n-heksana : kloroform (20:80 v/v), 10 mL n-heksana : kloroform (10:90 v/v), dan 20 mL kloroform, kemudian ditampung setiap 2 mL ke dalam tabung kaca. Isolat dipastikan kemurniannya menggunakan kromatografi lapis tipis. Isolat yang memiliki pola pemisahan yang sama digabungkan menjadi satu isolat, diuapkan, dan dihitung rendemen yang didapat. Isolat yang sudah kering, dipindahkan kedalam eppendrof sehingga terdapat 1 mg tiap eppendrof.
12. Alur pengerjaan isolasi senyawa aktif
BAB IV
HASIL DAN PEMBAHASAN
Penelitian yang telah dilakukan ini secara umum bertujuan untuk mengetahui aktivitas penangkap radikal bebas DPPH, UV protection, dan antibakteri pada ekstrak etanolik daun pegagan (C. asiatica). Selain itu, untuk mempertegas aktivitas yang dimiliki maka penelitian ini bertujuan untuk melakukan isolasi senyawa aktif dan mengetahui golongan senyawa aktif yang bertanggungjawab terhadap aktivitas yang diberikan dalam ekstrak etanolik daun pegagan.
A.Penyiapan Bahan, Penyerbukan dan Susut Pengeringan Serbuk Simplisia Daun Pegagan
Simplisia kering herba pegagan (C. asiatica) sebanyak 1 kg didapatkan dari B2P2TOOT, Tawangmangu, Jawa Tengah.
Simplisia kering herba pegagan diperoleh dari B2P2TOOT, Tawangmangu, Jawa Tengah dijadikan sebagai bahan penelitian dan sudah didukung kebenaran dari tanaman dengan adanya determinasi seperti yang dilampirkan pada Lampiran 3. Simplisia kering yang didapat masih dalam campuran herba sehingga perlu dilakukan sortasi kering yang bertujuan untuk menghilangkan bagian-bagian tanaman yang tidak diinginkan seperti akar dan tangkai daun, sehingga yang didapatkan hanya bagian daunnya saja.
Penyerbukan dilakukan untuk memperkecil permukaan simplisia sehingga dapat memperbesar luas permukaan dan dapat mempermudah penyarian. Simplisia diserbuk kasar menggunakan blender dengan tujuan mengurangi tumbukan pada blender supaya memperkecil kemungkinan kerusakan senyawa kimia yang terkandung pada daun pegagan.
yang dipanaskan pada suhu 105℃ hingga memperoleh bobot tetap. Pada kondisi ini, diasumsikan bahwa air yang terkandung dalam simplisia sudah menguap secara keseluruhan sehingga dapat menggambarkan kandungan air yang ada. Pada penelitian dilakukan tiga kali replikasi pengukuran sehingga didapatkan rata-rata susut pengerinngan pada simplisia kering daun pegagan sebesar 9,46% b/b. Dari hasil susut pengeringan yang diperoleh serbuk simplisia daun pegagan masih memenuhi persyaratan kadar air yang sudah ditetapkan.
B.Pembuatan Ekstrak Etanolik Daun Pegagan
Bahan penelitian yang digunakan selanjutnya adalah ekstrak etanolik daun pegagan. Ekstrak etanolik daun pegagan dibuat melalui proses ekstraksi dengan metode maserasi dan menggunakan etanol 90% v/v sebagai pelarut. Metode maserasi dipilih untuk preoses ekstraksi dengan tujuan menghindari adanya perubahan senyawa kimia yang mungkin terjadi karena adanya pemanasan dapat menyebabkan kerusakan senyawa kimia. Maserasi sendiri merupakan salah satu cara penyarian dingin yang mudah dilakukan dengan alat dan pengerjaannya yang sederhana.
homogen. Penggojogan dilakukan untuk mempercepat proses ekstraksi dibandingkan dengan cara ekstraksi yang hanya direndam saja. Adanya penggojogan yang berasal dari alat bantu, yaitu shaker akan membuat kontak serbuk simplisia dengan pelarut diperbesar sehingga memudahkan penarikan senyawa kimia dari serbuk simplisia.
Maserasi dilakukan selama 24 jam dan dilakukan penyaringan untuk memisahkan hasil ekstraksi dengan serbuk simplisia. Penyaringan dilakukan sebanyak dua kali, yang pertama menggunakan kain mori dan yang kedua menggunakan kertas saring Whatman no 41. Penyaringan menggunakan kain mori bertujuan untuk mendapatkan hasil ekstrak secara keseluruhan dan membantu mempercepat proses penyaringan karena serbuk simplisia selanjutnya dilakukan remaserasi. Penyaringan menggunakan kertas saring Whatman no 41 bertujuan untuk memisahkan hasil ekstraksi dengan partikel serbuk simplisia yang mungkin dapat melewati pori-pori pada kain mori.
Remaserasi adalah proses maserasi kembali dari serbuk simplisia yang sudah dilakukan maserasi sebelumnya. Remaserasi dilakukan selama 24 jam dan kembali dilakukan penyaringan menggunakan kain mori. Proses remaserasi dilakukan dengan tujuan untuk memperoleh ekstrak yang lebih banyak karena pelarut yang sudah jenuh dapat diperbaharui sehingga senyawa kimia yang tertarik keluar oleh pelarut semakin banyak dan rendemen yang didapatkan diharapkan akan semakin banyak pula.
rotary vaccuum evaporator adalah destilasi untuk menghilangkan kandungan
pelarut dengan bantuan pemanasan dan pompa vakum. Pemanasan dilakukan untuk menguapkan pelarut etanol sehingga dapat memisahkan pelarut dengan ekstrak kental. Pelarut etanol yang menguap tersebut akan ditarik oleh pompa vakum sehingga dapat memasuki kondesator sehingga uap tersebut kembali menjadi titik-titik cairan pelarut.
Gambar 4. Bagan rendemen
C.Optimasi Fase Gerak
Kromatografi lapis tipis merupakan salah satu metode pemisahan senyawa pada suatu fase diam berdasarkan polaritas senyawa terhadap fase gerak pembawa. KLT ini bertujuan untuk membantu skrining fitokimia dalam mengetahui komponen bioaktif apa saja yang terdapat dalam ekstrak etanolik daun pegagan.
Pada penelitian, pemisahan senyawa bioaktif dilakukan menggunakan fase diam yaitu pelat aluminium TLC Silica gel 60 F254 karena partikel silika pada
pelat KLT dapat dikontrol keseragamannya sehingga pemisahan yang akan terbentuk semakin optimal dan efisien. Pemisahan yang optimal pada KLT ditunjukkan dengan nilai Rf 0,2-0,8, untuk mendapat pemisahan yang baik maka
mencoba menggunakan 5 macam fase gerak, yaitu n-heksana : etil asetat (2:3 v/v) ; kloroform : metanol (7:3 v/v) ; kloroform : metanol (9:1 v/v) ; kloroform : metanol (95:5 v/v) ; etil asetat:asam formiat:asam asetat glasial:air (100:11:11:20 v/v). Pada Tabel 1, dapat dilihat hasil KLT yang menunjukkan bahwa pada fase gerak etil asetat:asam formiat:asam asetat glasial:air (100:11:11:20 v/v) dapat memisahkan senyawa dengan sempurna menjadi 11 spot pemisahan. Akan tetapi, fase gerak yang dipilih untuk penelitian selanjutnya adalah kloroform : metanol (95:5 v/v). Pemilihan fase gerak ini karena fase gerak dapat memisahkan senyawa aktif dengan optimal setelah fase gerak etil asetat:asam formiat:asam asetat glasial:air (100:11:11:20 v/v) yaitu didapatkan 6 spot pemisahan dengan bercak yang lebih jelas. Pada fase gerak etil asetat:asam formiat:asam asetat glasial:air (100:11:11:20 v/v) tidak dipilih dengan pertimbangan pada saat uji aktivitas selanjutnya akan sangat sulit menghilangkan pelarut karena fase gerak tersebut mengandung komponen pelarut yang susah menguap.
D.Uji Kualitatif Aktivitas Penangkapan Radikal Bebas Ekstrak Etanolik
Optimasi fase gerak yang telah dilakukan ini sekaligus untuk uji kualitatif aktivitas penangkap radikal bebas menggunakan DPPH sebagai sumber radikal bebas.
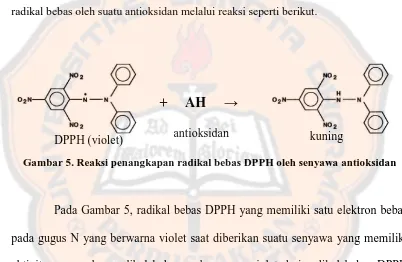
Radikal bebas merupakan sumber masalah terutama bagi kulit yang merupakan perlindungan pertama tubuh manusia dari segala paparan lingkungan yang dapat membentuk radikal bebas, seperti ; polusi dan sinar UV. Radikal bebas ini dapat merusak jaringan kulit sehingga mengakibatkan penuaan dini yang ditunjukkan dengan adanya pembentukan keriput pada kulit wajah. Aktivitas antioksidan suatu senyawa aktif ditunjukkan melalui perubahan warna DPPH yaitu violet yang mengalami pemudaran menjadi warna kuning akibat adanya aktivitas penangkapan radikal bebas oleh suatu antioksidan melalui reaksi seperti berikut.
Gambar 5. Reaksi penangkapan radikal bebas DPPH oleh senyawa antioksidan
Pada Gambar 5, radikal bebas DPPH yang memiliki satu elektron bebas pada gugus N yang berwarna violet saat diberikan suatu senyawa yang memiliki aktivitas penangkap radikal bebas maka warna violet dari radikal bebas DPPH akan memudar. Pemudaran ini terjadi karena suatu senyawa antioksidan dapat mendonorkan satu elektronnya kepada radikal bebas DPPH sehingga DPPH menjadi suatu senyawa non radikal yang berwarna kuning.
+ AH
→
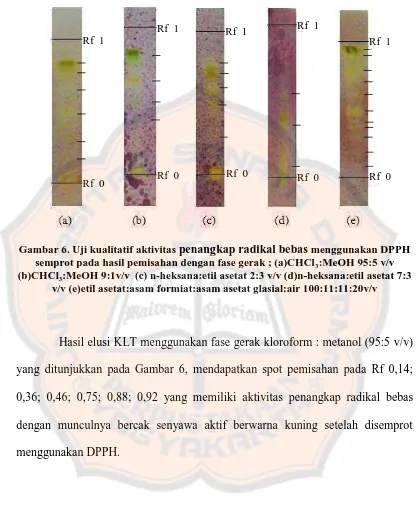
Gambar 6. Uji kualitatif aktivitas penangkap radikal bebas menggunakan DPPH semprot pada hasil pemisahan dengan fase gerak ; (a)CHCl3:MeOH 95:5 v/v
(b)CHCl3:MeOH 9:1v/v (c) n-heksana:etil asetat 2:3 v/v (d)n-heksana:etil asetat 7:3
v/v (e)etil asetat:asam formiat:asam asetat glasial:air 100:11:11:20v/v
Hasil elusi KLT menggunakan fase gerak kloroform : metanol (95:5 v/v) yang ditunjukkan pada Gambar 6, mendapatkan spot pemisahan pada Rf 0,14; 0,36; 0,46; 0,75; 0,88; 0,92 yang memiliki aktivitas penangkap radikal bebas dengan munculnya bercak senyawa aktif berwarna kuning setelah disemprot menggunakan DPPH.
Rf 1
Rf 1 Rf 1
Rf 1 Rf 1
Tabel 1. Uji Kualitatif Aktivitas Penangkap Radikal Bebas Ekstrak Etanolik
Fase Gerak Retention factor (Rf)
kloroform : metanol (95 : 5 v/v)
etil asetat : asam formiat : asam asetat glasial : air (100 :11 : 11 :20 v/v)
E.Uji Kualitatif Aktivitas UV Protection Ekstrak Etanolik
bleaching of �-caroten dengan cara melapisi pelat KLT kering hasil pemisahan
senyawa ekstrak menggunakan �-karoten.
�-karoten dipilih karena sifatnya yang fotosensitif terhadap sinar UV. � -karoten akan memudar akibat adanya oksidasi oleh sinar UV sehingga memutuskan ikatan rantai penyusun �-karoten. Hal ini yang dimanfaatkan dalam penelitian uji kualitatif aktivitas UV protection dengan cara mengamati perubahan warna �-karoten yang terjadi akibat adanya paparan ultraviolet dari warna kuning menjadi memudar. Senyawa aktif yang memiliki aktivitas UV protection dapat mempertahankan warna kuning �-karoten pada spot pemisahannya.
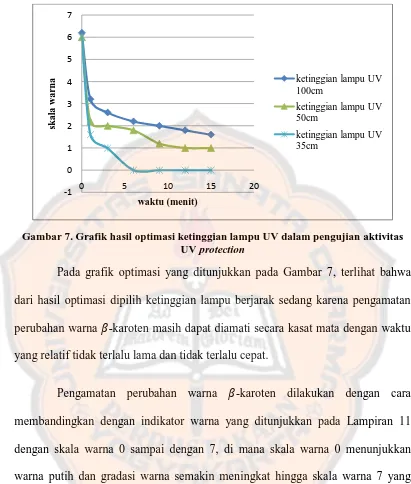
Gambar 7. Grafik hasil optimasi ketinggian lampu UV dalam pengujian aktivitas UV protection
Pada grafik optimasi yang ditunjukkan pada Gambar 7, terlihat bahwa dari hasil optimasi dipilih ketinggian lampu berjarak sedang karena pengamatan perubahan warna �-karoten masih dapat diamati secara kasat mata dengan waktu yang relatif tidak terlalu lama dan tidak terlalu cepat.
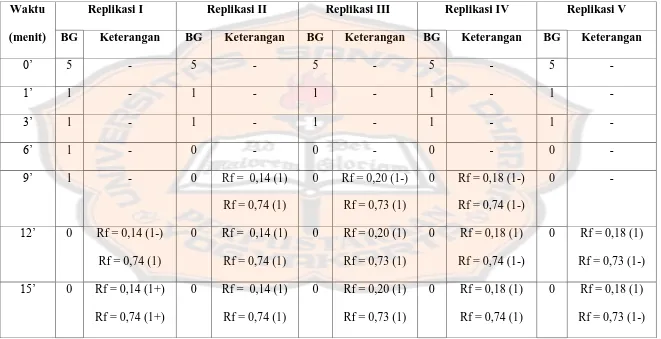
karoten mengalami pemudaran pada menit pertama setelah paparan lampu UV dari skala warna 5 menjadi 1. Pada saat menit ke-9 warna �-karoten pada pelat KLT kembali mengalami pemudaran dari skala warna 1 hingga skala warna 0 yang menunjukkan warna putih, dan terlihat spot pemisahan senyawa yang berwarna lebih kuning daripada warna pelat KLT yang ditunjukkan melalui skala warna 1 dengan warna putih kekuningan. Hasil yang dapat dilihat pada Gambar 8, menunjukkan bahwa dalam ekstrak etanolik daun pegagan terdapat senyawa aktif UV protection dengan spot pemisahan pada Rf 0,14-0,20 dan 0,73-0,74.
Gambar 8. Uji kualitatif UV protection pada ekstrak etanolik (A : kontrol ; B-D : Replikasi I – Replikasi III)
Mekanisme reaksi senyawa aktif pada ekstrak etanolik daun pegagan yang memiliki aktivitas UV protection belum dapat diketahui dengan pasti, namun aktivitas ini dapat dikaitkan dengan adanya aktivitas antioksidan yang terdapat pada spot pemisahan senyawa pada Rf 0,14 dan 0,75. Aktivitas antioksidan ini dapat menghambat terjadinya pemutusan rantai akibat oksidasi paparan sinar UV sehingga warna dari β-karoten dapat dipertahankan.
A B C D
Rf 1 Rf 1 Rf 1 Rf 1
Rf 0 Rf 0
Tabel 2. Uji Kualitatif Aktivitas UV Protection Ekstrak Etanolik
Pengukuran uji aktivitas UV Protection menggunakan lampu dengan ketinggian 50 cm dan intensitas cahaya 15,81 Waktu
(menit)
Replikasi I Replikasi II Replikasi III Replikasi IV Replikasi V
BG Keterangan BG Keterangan BG Keterangan BG Keterangan BG Keterangan
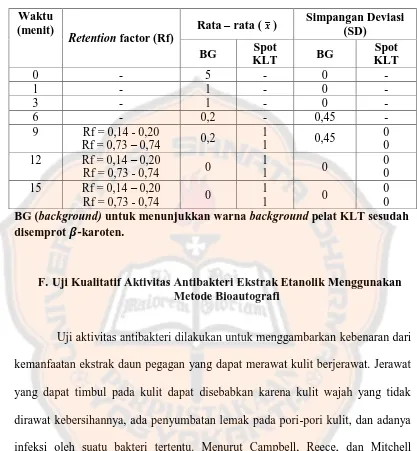
Tabel 3. Simpangan deviasi (SD) pengukuran uji kualitatif UV Protection BG (background) untuk menunjukkan warna background pelat KLT sesudah disemprot �-karoten.
F. Uji Kualitatif Aktivitas Antibakteri Ekstrak Etanolik Menggunakan Metode Bioautografi
Uji aktivitas antibakteri dilakukan untuk menggambarkan kebenaran dari kemanfaatan ekstrak daun pegagan yang dapat merawat kulit berjerawat. Jerawat yang dapat timbul pada kulit dapat disebabkan karena kulit wajah yang tidak dirawat kebersihannya, ada penyumbatan lemak pada pori-pori kulit, dan adanya infeksi oleh suatu bakteri tertentu. Menurut Campbell, Reece, dan Mitchell (2003), salah satu bakteri yang dapat menginfeksi kulit adalah bakteri S. aureus.
menyebabkan terjadinya sumbatan aliran minyak dari folikel rambut ke pori-pori dan bakteri akan berkumpul dalam pori kulit. Bakteri yang tumbuh pada bagian tersumbat ini akan menguraikan lemak dari minyak sehingga menyebabkan iritasi kulit berupa bintil putih berisi nanah atau yang sering disebut jerawat. Penelitian uji kualitatif aktivitas antibakteri ekstrak etanolik daun pegagan dilakukan terhadap bakteri S. aureus yang merupakan bakteri pada kulit dan merupakan kelompok bakteri Gram positif serta pengujian terhadap bakteri E.coli yang merupakan bakteri kelompok bakteri Gram negatif. Kebenaran bakteri uji yang digunakan dalam penelitian dapat dilihat pada Lampiran 7 dan 8.
Uji kualitatif aktivitas antibakteri ekstrak etanolik daun pegagan dilakukan menggunakan metode bioautografi. Bioautografi merupakan teknik pengujian antibakteri terhadap pemisahan senyawa bioaktif pada suatu pelat KLT. Prinsip dari metode bioautografi adalah adanya kontak senyawa aktif dengan media agar yang menyebabkan senyawa aktif tersebut dapat berdifusi dari hasil pemisahan pada pelat KLT menuju media agar yang telah diinokulasikan bakteri uji sehingga dapat menghambat pertumbuhan bakteri dengan adanya zona jernih pada tiap spot pemisahan senyawa bioaktif sebagai tanda positif aktif antibakteri.
aktivitas antibakteri yang terdapat pada ekstrak etanolik dengan suatu aktivitas senyawa pembanding yaitu amoxicillin. Amoxicillin dipilih sebagai pembanding karena amoxicillin merupakan antibiotik turunan penisilin yang mempunyai spektrum kerja yang luas yaitu dapat menghambat pertumbuhan bakteri Gram positif dan bakteri Gram negatif.
Konsentrasi ekstrak etanolik daun pegagan yang digunakan untuk penotolan pada pelat KLT adalah 5 mg/mL dengan adanya variasi volume penotolan membuat variasi mass loading pula, yaitu 75 μg, 100 μg, dan 150 μg. Pelat KLT yang sudah dielusi, dikeringuapkan terlebih dahulu secara aseptis untuk menghindari adanya hasil positif palsu akibat masih adanya pelarut fase gerak kloroform:metanol (95:5 v/v) di mana kedua pelarut ini memiliki daya antibakteri pula.
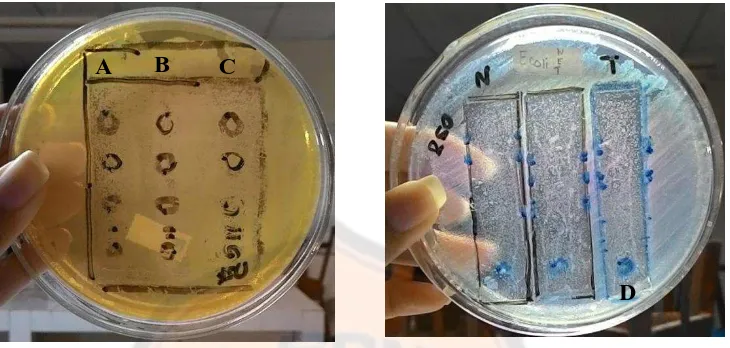
Gambar 9. Uji kualitatif aktivitas antibakteri ekstrak etanolik terhadap bakteri E. coli menggunakan metode bioautografi (A: mass loading 75μg; B: mass loading
100 μg; C: mass loading 150 μg; D : mass loading 250 μg)
Berbeda dengan hasil pengujian ekstrak etanolik terhadap bakteri S.
aureus memiliki aktivitas antibakteri dengan terbentuknya zona hambat sesuai
dengan spot pemisahan yang ditunjukkan pada Gambar 10. Spot pemisahan senyawa bioaktif yang memiliki aktivitas antibakteri ditunjukkan pada Rf 0,16-0,17; 0,21-0,23; 0,29-0,34; 0,51-0,53. Zona hambat yang terbentuk tidak dapat dihitung secara pasti karena zona jernih yang terbentuk tidak rata dan saling berhimpit namun dapat terlihat secara kasat mata bahwa seiring dengan adanya peningkatan mass loading besar zona hambat yang terbentuk juga semakin besar. Walaupun, jika dibandingkan dengan amoxicillin efek antibakteri yang ditunjukkan efek antibakteri ekstrak etanol tidak sebaik amoxicillin, tapi dengan dilakukannya metode bioatugrafi dapat memberikan informasi bahwa pada mass
loading 75μg ekstrak etanolik sudah dapat menhambat pertumbuhan bakteri.