1
SINTESIS DAN KARAKTERISASI Fe
3O
4/SiO
2DENGAN METODE KOPRESIPITASI
SKRIPSI
YOSALIHA BR TUMORANG 170801054
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN
2021
2
SINTESIS DAN KARAKTERISASI Fe
3O
4/SiO
2DENGAN METODE KOPRESIPITASI
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
YOSALIHA BR TUMORANG 170801054
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN
2021
i
PERNYATAAN ORISINALITAS
SINTESIS DAN KARAKTERISASI Fe
3O
4/SiO
2DENGAN METODE KOPRESIPITASI
SKRIPSI
Saya menyatakan bahwa skripsi ini adalah hasil karya saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juli 2021
Yosaliha Br Tumorang 170801054
iii
SINTESIS DAN KARAKTERISASI Fe
3O
4/SiO
2DENGAN METODE KOPRESIPITASI
ABSTRAK
Telah dilakukan sinesis Fe3O4/SiO2 dengan metode kopresipitasi. Proses preparasi sampel Fe3O4 3 g didispersikan ke dalam 40 ml larutan etanol. tambahkan 1 g SiO2 dan 4,5 ml NH4OH pekat ditambahkan secara cepat menggunakan T = 30°C. Larutan yang disterilkan diaduk dengan proses stiring t = 10 jam untuk menyelesaikan reaksi. Kemudian endapan dicuci menggunakan air dan etanol. Kalsinasi pada 100°C. Hasil Analisa X-Ray Diffraction (XRD) Fe3O4/SO2 menunjukkan puncak difraksi pada puncak 32,6° dan puncak bidang (111),(220),(311), (400), dan (511). Berdasarkan hasil mikrostruktur permukaan sampel menggunakann Scanning Electron Microscopy (SEM) menunjukan bahwa sampel tidak homogen, hal ini disebabkan oleh waktu penggerusan sampel yang terlalu singkat yang mengakibatkan adanya jarak antar partikel, sehingga persebaran partikel sampel tidak merata dan permukaan sampel tidak homogen.
Kata Kunci : Fe3O4/SiO2, Kopresipitas, Na4OH, SEM, Sintesis
iv
SYNTHESIS AND CHARACTERIZATION OF Fe
3O
4/SiO
2WITH METHOD COOPRECIPITATION
ABSTRACT
Synthesis of Fe3O4/SiO2 has been carried out by coprecipitation method. Sample preparation process Fe3O4 3 g was dispersed into 40 ml of ethanol solution. add 1 g of SiO2 and 4.5 ml of concentrated Na4OH is added rapidly using T = 30°C. The sterilized solution was stirred with a stirring process t = 10 hours to complete the reaction. Then the precipitate was washed with water and ethanol. Calcination at 100°C. The results of the X-Ray Diffraction (XRD) analysis of Fe3O4/SiO2 showed the diffraction peaks at 32.6°
peaks and plane peaks (111), (220), (311), (400), and (511). Based on the results of the sample surface microstructure using Scanning Electron Microscopy (SEM) shows that the sample is not homogeneous, this is caused by the sample grinding time is too short which results in the distance between the particles, so that the distribution of sample particles is uneven and the sample surface is not homogeneous.
Keywords : Fe3O4/SiO2, Na4OH, coprecipitation, SEM, Syntesis.
v
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan yang Maha Esa yang senantiasa menjadi penopang dan teman terbaik sehingga penulis dapat menyelesaikan Tugas Akhir ini yang berjudul “Sintesis dan karakterisasi Fe3O4/SiO2 dengan metode kopresipitasi”.
Selama di bangku kuliah ini, penulis banyak mendapatkan dukungan-dukungan secara moril, material, serta bimbingan dari berbagai pihak sehingga kesulitan-kesulitan dapat terlewati dengan baik. Dengan segenap hati penulis mengucapkan terima kasih kepada :
1. Ibu Dr. Nursahara Pasaribu M,sc Sebagai Dekan MIPA USU, Bapak Dr. Perdinan Sinuhaji, MS, sebagai Ketua Departemen Fisika FMIPA USU, seluruh dosen, staff dan pegawai Departemen Fisika FMIPA USU yang telah membantu dan menyelesaikan skripsi ini.
2. Bapak Prof. Dr. Timbangen Sembiring, M.sc selaku dosen pembimbing yang telah memberikan bimbingan dan arahan serta bantuan selama penyusunan Skripsi ini.
3. Ibu Prof. Dr. Zuriah Sitorus, Ms, Bapak Dr. Syahrul humaidi, M.Sc selaku dosen penguji yang telah memberikan kritik saran kepada penulis dalam menyelesikan skripisi ini.
4. Orang tua tercinta, Ayah Rebensius Situmorang, dan Ibu Lasmi Br Hutabalian, yang telah memberikan doa, dukungan, semangat serta seluruh jiwa dan raga nya dari saya dilahirkan sampai terselesaikannya study saya, Kakak Nia Fransiska Situmorang, Ekaristi Br, Adik Putra Pranata Situmorang dan Maria Fiani Br Tumorang abang Samuel panjaitan yang telah memberikan dukungan dan semangat sehingga saya dapat menyelesaikan Skripsi ini.
5. Ibu Hariyati lubis, M.si, Bapak Ridwan Yusuf Lubis, M.si yang selalu memberikan kritik dan saran serta dukungan dalam mengerjakan skripsi ini.
vi 6. Sahabat seperjuangan yang telah membantu, dan memberi semangat saya dalam mengerjakan skirpisi ini Adila Ningsih Br Sinulingga dan Eliza Fadilah Nainggolan.
7. Ebenezer Sinulingga yang selalu memberikan semangat, dukungan, doa dan selalu menemani saya dalam mengerjakan Skripsi ini.
8. Sahabat Seperdopingan yang telah memberikan semangat, doa dan dukungan nya dalam menyelesaikan skripisi ini Seperdopingan ( Jeprin Tua Sihite, Monika Klarizca saragih dan David A Hutajulu).
9. Esmosi Monja (Mitra, Maria Sihombing),( Melva, shara santy Violin, gift dan Ega Malau, yosia ) teman seperjuangan yang telah memberikan doa dan bantuan dalam menyelesaikan skripisi ini.
10. Best Paok ( Surya, feby, Ramot, Santo, wita) teman seperjuangan dari maba yang telah memberikan doa dan dukungan dalam menyelesaikan skripsi ini.
11. Seluruh teman-teman Fisika USU Angkatan 2017 yang telah mewarnai cerita perjalanan perkulihan penulis.
Penulis menyadari sepenuhnya bahwa dalam penyelesaian skripsi ini masih jauh dari sempurna, untuk itu kritik dan saran yang bersifat membangun sangat diharapkan dari para pembaca.
Medan, Juli 2021
Yosaliha Br Tumorang
vii
DAFTAR ISI
PENGESAHAN SKRIPSI ... i
ABSTRAK ... ii
ABSTRACT ... iii
PENGHARGAAN ... iv
DAFTAR ISI ... vi
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xi
DAFTAR SINGKATAN ... xii
BAB 1 PENDAHULUAN 1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 3
1.3 Tujuan Penelitian ... 3
1.4 Batasan Masalah... 3
1.5 Manfaat Penelitian... 4
BAB 2 TINJAUAN PUSTAKA 2.1 Besi (II,III) Oksida (Fe3O4) ... 5
2.2 Silika dioksida (SiO2) ... 6
2.3 Metode Kopresipitasi ... 8
2.4 Tetraethyl Orthosilicate (TEOS) ... 9
2.5 Amonium Hidroksida (NH4OH) ... 9
2.6 Karakterisasi Pengujian ... 10
2.6.1 Karakterisasi XRD (X-Ray Difraction) ... 10
2.6.2 Karakterisasi SEM (Scanning Electron Microscope) ... 12
BAB 3 METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian ... 15
3.2 Alat dan Bahan Penelitian ... 15
3.2.1 Alat Penelitian ... 15
3.2.2 Bahan Penelitian ... 16
3.3 Prosedur Penelitian ... 17
3.3.1 Sintesis Fe3O4 dengan metode kopresipitasi dengan suhu 100º C 17 3.3.2 Sintesis Fe3O4 menggunakan precursor TEOS... 17
3.3.3 Sintesis Fe3O4/ SiO2 dengan metode kopresipitasi ... 17
3.4 Diagram Alir ... 18
3.4.1 Diagram Sintesis Fe3O4 dengan metode kopresipitasi dengan suhu 100º C ... 18
viii 3.4.2 Diagram Sintesis Fe3O4 menggunakan precursor TEOS ... 19 3.4.3 Diagram Sintesis Fe3O4/ SiO2 dengan metode kopresipitasi ... 20 BAB 4 HASIL DAN PEMBAHASAN
4.1 Hasil Karakterisasi XRD (X-ray Diffraction) ... 21 4.2 Hasil Karakterisasi SEM (Scanning Electron Microscope) ... 22 BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan ... 29 5.2 Saran ... 29 DAFTAR PUSTAKA
LAMPIRAN
ix
DAFTAR TABEL
Nomor Tabel
Judul Halaman
2.1 Sifat-sifat Magnetit Fe3O4 5
2.2 Sifat-sifat Silika (SiO2) 7
2.3 Sifat Fisik TEOS 9
2.4 4.1
4.2
Amonium Hidroksida (NH4OH)
Data Sampel Fe3O4/SiO2 dan Sampel Fe3O4/ SiO2 5% Hasil XRD
Data Sampel Fe3O4/TEOS dan Sampel Fe3O4/ TEOS5% hasil XRD
10 22
24
x
x
xi
DAFTAR GAMBAR
Nomor Gambar
Judul Halaman
2.1 Struktur ikatan kimia Fe3O4 6
2.2 Struktur ikatan kimia SiO2 8
2.5 Difraksi bidang atom 11
2.6 2.7 2.8 3.1
Hasil karakterisasi XRD Prinsip kerja SEM Hasil karakterisasi SEM Diagram Sintesis Fe3O4
12 13 14
xii
DAFTAR LAMPIRAN
Nomor
Lampiran Judul Halaman
1 2 3
Alat dan Bahan Penelitian Perhitungan NH4OH 3,2 Molar Hasil Macth XRD
32 36 38
xiii
DAFTAR SINGKATAN
Fe3O4 Besi (II,III) Oksida (Fe3O4)NH4OH Amonium hidroksida
SEM Scanning Electron Microscope
SiO2 Silika dioksida
TEOS Tetraethyl Orthosilicate
XRD X-Ray Diffraction
1
BAB I
PENDAHULUAN
1.1 Latar Belakang Masalah
Aplikasi penggunaan Fe3O4 saat ini berkembang pesat di bidang industri. Partikel Fe3O4 merupakan material yang mempunyai sifat magnetik yang banyak dipelajari karena memiliki bermacam-macam sifat kimia dan sifat fisik. Sintesis partikel Fe3O4, pada dasarnya menggunakan metode kimia basa dengan cara yang sangat efektif (Merdekani, 2013). Proses pelapisan dengan penambahan bahan kimia lain seperti SiO2 untuk mengatur ukuran dan struktur pori Fe3O4. Setelah sintesis Fe3O4 kemudian difungsionalisasi dengan SiO2 yang di dasarkan pada sifat biokompatibel, bersifat inner dan area permukaan yang luas (Suryani, 2015).
Magnetit (Fe3O4), merupakan material yang menarik dan memiliki aplikasi yang sangat luas. Pada ukuran bulk-nya, material ini merupakan kelompok bahan ferrimagnetik.
Pada ukuran nanometer, Fe3O4 ini menjadi bahan superparamagnetik, dan memiliki sifat- sifat yang lebih baik seperti magnetisasi saturasi yang tinggi, biological compatibility, dan environmental stability. (Wei Y et al., 2012).
Dalam beberapa tahun terakhir, pemanfaatan material magnet dalam berbagai aspek kehidupan masyarakat mengalami peningkatan yang sangat berarti. Salah satu nya adalah pemanfatan degradasi dan penanganan air limbah methylene blue (Cucun, 2019).
Silika adalah kristal silikat alami walaupun dapat juga berasal dari sintesis, salah satu kristal yang terdiri dari ikatan tetrahedral (pasangan atom silikon dengan atom oksigen). Pada umumnya, struktur dari asam silikat terdiri dari lapisan silikat yang terpisahkan oleh kation natrium terhidrasi. Silika merupakan senyawa logam oksida yang banyak terdapat di alam, namun keberadaannya tidak dalam kondisi bebas melainkan terikat dengan senyawa lain baik secara fisik maupun secara kimia (Merdekani, 2013).
Salah satu metode kimia basa adalah kopresipitasi (Sajidah, 2017). Metode kopresipitasi merupakan proses kimia yang membawa suatu zat terlarut ke bawah sehingga terbentuk endapan yang di kehendaki. Teknik ini sering di pakai untuk
2
memisahkan analitik dari pengotornya. Dengan prinsip melepas ikatan kontiniu yang dimiliki oleh suatu senyawa logam dalam bentuk cairan tanpa mempertimbangkan mekanisme spesifik yang terjadi. Metode kopresipitasi yang paling sederhana karena prosedurnya lebih mudah dilakukan dan memerlukan temperatur reaksi yang rendah (<100°C) (B. Parman, 2017). Keunggulan lain dari metode kopresipitasi dapat mengunakan suhu ruang dan membutuhkan waktu yang singkat dalam percobaan (Hefdea, et al., 2020).
Material Fe3O4 divariasikan terhadap SiO2 yang berbeda-beda, prekursor yang di pakai untuk silika yaitu Tetraethyl Orthosilicate (TEOS) (Suryani, 2015). Pengaruh penambahan SiO2 terhadap karakteristik dan kinerja fotokatalitik Fe3O4 pada degradasi methylene blue telah dilakukan penambahan SiO2 pada bahan nanokatalis bermagnet Fe3O4 menggunakan larutan Tetraethyl Orthosilicate (TEOS) membentuk Fe3O4/SiO2 dengan tujuan untuk meningkatkan efektivitas katalitik bahan.
Penggabungan bahan katalis dengan superparamagnetik Fe3O4 ini akan membentuk komposit Fe3O4. Material komposit merupakan kombinasi antara dua bahan atau lebih yang memiliki sejumlah sifat berbeda yang dimiliki oleh masing-masing komponen (Wei Y et al., 2012). Karakterisasi silika menggunakan XRD menunjukkan bahwa silika memiliki puncak yang melebur pada kisaran 2θ = 22ᵒ, dan berfasa amorf. Puncak SiO2
ditemukan pada 2θ = 45.82ᵒ; 66.69ᵒ dan 74ᵒ, yang memiliki puncak yang melebar pada 2θ
= 20ᵒ - 30ᵒ. Spektra tersebut memiliki korespodensi dengan SiO2 berkeadaan amorf (Yudia, 2018).
Tetraethyl Orthosilicate (TEOS) adalah sistem heterogen yaitu larutan tidak dapat bercampur dengan baik antara TEOS dengan air. Adapun sistem heterogen terdiri dari TEOS dan air tanpa adanya penambahan etanol sedangkan sistem homogen terdiri dari TEOS dan air serta adanya etanol. Sintesis dilakukan dengan menggunakan TEOS sebagai sumber silika, larutan ammonia (katalis basa), aquadest, etanol (Siti et al., 2016).
Pada penelitian ini dilakukan dengan pembuatan material magnetit bahan komposit Fe3O4 - SiO2 dan melakukan uji degradasi dan penanganan air limbah methylene blue. Pada penelitian ini dapat menghasilkan katalis berwarna hitam dan memiliki sifat
3
magnetik Uji Karakterisasi Fe3O4 - SiO2 di lakukan dengan menggunakan, X-Ray Diffraction (XRD), Scanning Electron Microscope (SEM) (Didin, 2012).
1.2 Rumusan Masalah
Dalam penelitian ini di paparkan perumusan masalah yang di selesaikan yaitu :
• Bagaimana cara mesintesis Fe3O4/SiO2 dengan metode kopresipitasi?
• Bagaimana hasil pengujian mikrostruktur menggunakan XRD dan SEM dari sintesis dan karakterisasi Fe3O4/SiO2 dengan metode kopresipitasi?
1.3 Tujuan Penelitian
Berdasarkan rumusan masalah diatas dapat ditentukan tujuan dari penelitian ini, yaitu:
• Mengetahui Langkah-langkah dalam mensintesis Fe3O4/SiO2 dengan metode kopresipitasi.
• Mengetahui hasil pengujian mikrostruktur menggunakan XRD, SEM dari sintesis dan karakterisasi Fe3O4/SiO2 dengan metode kopresipitasi.
1.4 Batasan masalah
Adapun batasan masalah dalam penelitian ini adalah:
• Suhu yang di gunakan dalam proses sintering 100oC.
• Suhu yang di gunakan dalam proses pengadukan magnetic stirrer 300C.
• Waktu yang di gunakan untuk proses pengadukan sampel 10 jam.
• Prekursor yang digunakan adalah Tetraethyl Orthosilicate (TEOS).
4
• Asam yang digunakan untuk sintesis Fe3O4/SiO2 adalah Amonium Hidroksida (NH4OH) pekat dan NH4OH 3,2 Molar
• Karakterisasi Fe3O4/SiO2 menggunakan XRD, SEM.
1.5 Manfaat Penelitian
Manfaat penelitian ini adalah sebagai bahan untuk degradasi dan penanganan air limbah methylene blue. Serta, memberikan informasi yang bermanfaat untuk usaha penanganan limbah melalui metode kopresipitasi sehingga pada saat proses pengolahan limbah yang ramah lingkungan.
5
BAB II
TINJAUAN PUSTAKA
2.1 Besi (II,III) Oksida (Fe3O4)
Material Fe3O4 memiiki sifat super paramagnetik, yaitu bahan yang bersifat magnet apabila diberikan medan magnet dan bahan tersebut akan hilang sifat magnetnya apabila medan magnet dihilangkan. Bahan tersebut tidak mempunyai momen magnet spontan, sehingga terdispersi secara baik di dalam air dan mudah dikumpulkan kembali dengan bantuan medan magnet dari luar. Penggabungan bahan katalis dengan super paramagnetik Fe3O4 ini akan membentuk komposit Fe3O4 (Wei Y et al., 2012 ; Siti et al., 2016).
Karakterisasi Fe3O4 dengan XRD dapat dilihat dalam material magnet karena disintesis mempunyai kesesuaian puncak difraksi dengan Fe3O4 sudut difraksi 2θ yaitu 30,3°; 35,5°; 57,1° dan 62,5°. Adapun hasil karakterisasi Fe3O4 yang bergerombol diperkuat data analisis SEM yang terlihat penumpukan nanopartikel Fe3O4 pada beberapa tempat (Cucun et al., 2018).
Tabel 2.1 Sifat-Sifat Magnetit Fe3O4
Sifat-Sifat Fe3O4
Kategori Mineral Oksida
Rumus Kimia Besi (II, III) Oksida
Warna Hitam
Sistim Kristal Isometrik, Heksoktahedral
Sifat Dalam Rapuh
Kelarutan Larut perlahan pada asam klorida
Kekerasan 5.5 – 6.5 kg/mm2 [Cucun et al., 2018]
Magnetit Fe3O4 merupakan oksida besi yang paling banyak ditemukan dan memiliki sifat kemagnetan yang paling kuat dibandingkan oksida-oksida besi lainnya (Cucun et al., 2018).
6
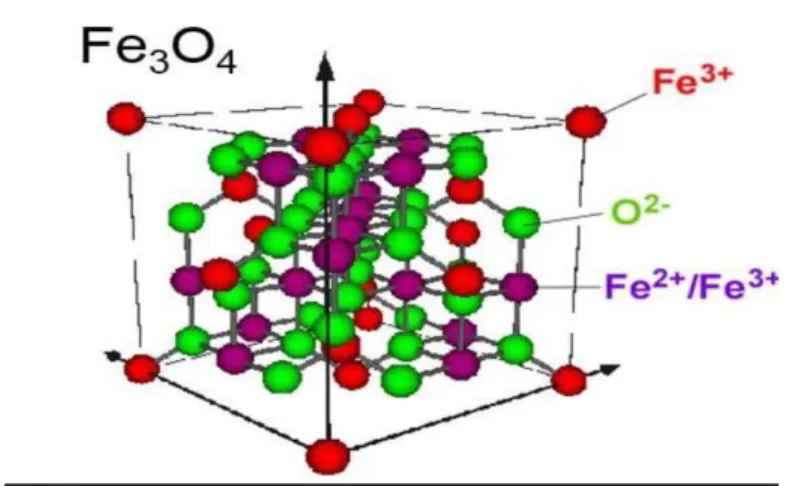
Secara struktur, Fe3O4 memiliki struktur kristal kubik invers spinel (Gambar 2.1).
Rumus molekul Fe3O4 dapat dituliskan sebagai (Fe2+)( Fe3+)2O4. Berdasarkan Gambar 2.1, maka terdapat 8 kation divalen Fe2+ menempati site oktahedral, 8 kation trivalen Fe3+
menempati site tetrahedral, dan 8 kation Fe3+ juga menempati site oktahedral. Kation Fe3+
yang menempati tetrahedral site dan octahedral memiliki resultan momen magnetik yang sama besar, namun orientasi berlawanan (Indra
yana, 2019).
Gambar 2.1 Struktur ikatan kimia Fe3O4
Untuk menghaikan magnetit Fe3O4 yang efisien digunakan untuk menyerap logam maka dalam beberapa penelitian sering diteliti tentang karakterisasi kemudian dilanjutkan dengan aplikasi magnetit Fe3O4 secara elektrokimia. Magnetit Fe3O4 yang dihasikan selanjutnya dikarakterisasi dengan menggunakan X-Ray Diffraction (XRD), Scanning Electron Microscope (SEM) sehingga dapat diketahui serta mampu didefenisikan fasanya (Marlisa, 2017).
2.2 Silika dioksida (SiO2)
Silika (SiO2)merupakan kristal silikat alami maupun proses sintesis. SiO2 terdiri dari ikatan tetrahedral pasangan atom silikon dengan atom oksigen. Pada umumnya, struktur dari asam SiO2 terdiri dari lapisan silikat yang terpisahkan oleh kation natrium terhidrasi. SiO2 merupakan senyawa logam oksida yang banyak terdapat di alam, namun keberadaannya tidak dalam kondisi bebas melainkan terikat dengan senyawa lain. Sifat fisik maupun secara kimia SiO2 juga bisa digunakan untuk mengontrol senyawa. SiO2
7
dapat di fungsionalkan sebagai biokompatibel, ikatan nya juga bersifat ionic dan inner di area permukaan yang cukup luas (Merdekani, 2013 ; Siti, 2018).
Karakterisasi XRD SiO2 menunjukkan bahwa silika memiliki puncak yang melebur pada kisaran 2θ = 22ᵒ, dan berfasa amorf. Puncak SiO2 ditemukan pada 2θ = 45.82ᵒ; 66.69ᵒ dan 74ᵒ, yang memiliki puncak yang melebar pada 2θ = 20ᵒ - 30ᵒ. Spektra tersebut memiliki korespodensi dengan SiO2 berbentuk amorf (Yudia, 2018).
Tabel 2.2 Sifat-Sifat Silika (SiO2)
Sifat-Sifat SiO2
Rumus Molekul SiO2
Penampilan Kristal Transparan
Kepadatan 2,648 g/cm
Massa Molar 60,08 g/mol
Titik Lebur 1600 – 1752ᵒC
Titik Didih 2230ᵒC
Reaksi Kimia Reaksi Asam, Reaksi Basa [Retnosari et al., 2013]
Kristal silika juga memiliki sifat sebagai berikut, setiap atom silikon berada pada pusat suatu tetrahedron yang terdiri dari empat atom oksigen, setiap atom oksigen berada ditengah-tengah antara dua atom silikon. Adapun sebagian besar logam pada suhu 25ᵒC atau pada suhu yang lebih tinggi, tetapi dapat diserap oleh F2, HF aqua, hidroksida alkali dan leburan-leburan karbonat (Wei et al., 2012).
Gambar 2.2 merupakan struktur ikatan kimia dari silikon dioksida (SiO2) yang terdiri dari tiga molekul atom, dimana atom silikon melekat pada dua atom oksigen dengan ikatan kovalen. Adapun reaksi kimia dari silikon dioksida ini adalah sebagai berikut :
SiO2 → Si + O2...(2.2)
8
Gambar 2.2 Struktur ikatan kimia SiO2
2.3 Metode Kopresipitasi
Metode kopresipitasi merupakan proses kimia yang membawa suatu zat terlarut ke bawah sehingga terbentuk endapan yang di kehendaki, teknik ini sering di pakai untuk memisahkan analitik dari pengotornya. Metode sintesis bottom up pada kopresipitasi digunakan untuk mendapatkan ukuran partikel kecil berukuran nanometer. Dengan prinsip yaitu melepas ikatan kontiniu yang dimiliki oleh suatu senyawa logam dalam bentuk cairan tanpa mempertimbangkan mekanisme spesifik yang terjadi. Di antara sekian metode sintesis tersebut, metode kopresipitasi yang paling sederhana karena prosedurnya lebih mudah dilakukan dan memerlukan temperatur reaksi yang rendah (<100°C), adapun keuntungan metode kopresipitasi menggunakan suhu ruang dan membutuhkan waktu yang sangat singkat dalam percobaan (Trianasari, 2017).
Metode kopresipitasi digunakan pada pembuatan Fe3O4, memperoleh Fe3O4
dengan ukuran partikel yang relatif kecil, lebih aman dan sederhana karena dilakukan pada suhu yang rendah (Siti et al., 2016).
Kopresipitasi merupakan salah satu metode yang digunakan untuk membuat preparasi material nanopartikel yang paling efektif karena metode ini dapat dilakukan pada kondisi lingkungan yang normal. Dalam proses sintesisnya digunakan pasangan asam basa, dimana asam berfungsi sebagai pelarut dan basa berfungsi untuk membawa zat terlarut kebawah sehingga terbentuk endapan yang di inginkan. Prinsip kerja metode
9
ini adalah mengubah suatu garam logam menjadi endapan dan kemudian diubah ke bentuk oksidanya dengan cara pemanasan (Marlisa, 2017).
2.4 Tetraethyl Orthosilicate (TEOS)
Tetraethyl Orthosilicate (TEOS) digunakan sebagai prekursor atau sumber silika dalam pembuatan material mesopori, TEOS termasuk jenis senyawa silikon alkoksi yang terdiri dari atom Si yang berikatan dengan gugus organik (OR) dengan rumus kimia Si (OC-Hs)4. TEOS memiliki sifat tidak dapat larut (incompatible) dalam zat seperti air, alkali asam-asam mineral dan agen pengoksidasi yang kuat. Berikut ini merupakan sifat fisik dari TEOS (Salim, 2012).
Tabel 2.3 Sifat Fisik TEOS
Sifat-Sifat TEOS
Berat moleku 208,33
Berat jenis 0.94 gr/cc3
Titik didih 169oF (336oF)
Titik lebur -86oC (-123oF) [Salim et al., 2012]
Senyawa yang banyak digunakan dalam sintesis material mesopori adalah Tetramethyl Orthosilicate (TMOS, Si (OCH3)4) dan Tetraethyl Orthosilicate (TEOS, Si (OCH2CH3)4).
Pada penelitian ini, prekursor yang digunakan adalah TEOS (Salim, 2012).
2.5 Amonium hidroksida (NH4OH)
Amonium hidroksida adalah larutan amonia didalam air dengan NH4OH. Amonium hidroksida merupakan senyawa yang tidak berwarna dan memiliki bau yang sangat tajam.
Larutan ini juga termasuk cairan yang sangat larut dalam air, dengan berat molekul 35,04 g/mol, titik didih 37,7ᵒC, dan titik lebur – 57,5ᵒC. (Kusma,2011).
10
Tabel 2.4 Sifat-Sifat NH4OH
Sifat-Sifat NH4OH
Massa jenis dan fase ( g/L ) 0,6942 Kelarutan dalam air ( gr/100 ml pada 0C) 89,9 Titik lebur ( 0C ) -77,73 Titik didih ( 0C ) -33,34 Keasaman ( PKa ) 9,25
Kebasaan (PKb) 4,75
[ Hari et al., 2015]
Pada proses pemisahan NH4OH, ion amonium harus merubah wujud menjadi molekulamonia (NH3) terlebih dahulu karena itu proses penyisihan dapat terjadi, kenaikan pH (semakin banyak ion OH-) dipengaruhi oleh penambahan NaOH ke sampel tersebut.
Gas ammonia juga merupakan gas yang tidak berwarna dengan baou yang sangat menyengat (Rahmat, 2017).
2.6 Karakterisasi pengujian 2.6.1 X-Ray Diffraction
X-Ray Diffraction (XRD) merupakan salah satu metode karakteristik material
yang digunakan dari dulu hingga sekarang. Teknik ini digunakan untuk mengidentifikasi fasa kristalin dalam material dengan cara menentukan parameter struktur kisi serta untuk mendapatkan ukuran partikel. Bahan yang dianalisis tanah halus, homogen dan rata-rata komposisi massal ditentukan (Marlisa, 2017). Arah berkas yang di pantulkan semata- mata ditentukan oleh geometri kisi, yang bergantung pada orientasi dan jarak bidang kristal. Apabila kristal memiliki simetri hexagonal ( a = b = 90º, c = 120º ) dengan ukuran parameter kisi a, maka sudut difraksi bekas bidang kristal (hkl) dapat dihitug dengan hukum Bragg.
11
Prinsip kerja XRD adalah difraksi sinar-x. Ketika sinar-x datang mengenai bidang kristal suatu bahan dengan sudut datang θ dan terjadi pemantulan dengan sudut θ, maka akan terjadi difraksi sinar-x pada bidang kristal tersebut sesuai dengan hukum Bragg ditunjukkan pada Gambar 2.5
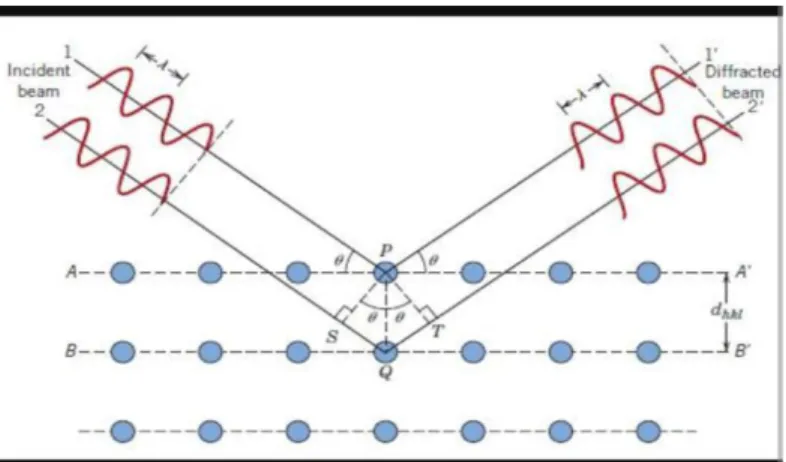
Gambar 2.5 Difraksi bidang atom (Callister,2009)
Gambar 2.5, menunjukkan suatu berkas sinar-x dengan panjang gelombang λ, jatuh pada sudut θ pada sekumpulan bidang atom berjarak d, sinar yang dipantulkan dengan sudut θ hanya dapat terlihat jika berkas dari setiap bidang yang berdekatan saling menguatkan. Oleh sebab itu, jarak tambahan satu berkas dihamburkan dari setiap bidang yang berdekatan, dan menempuh jarak sesuai dengan perbedaan kisi yaitu sama dengan panjang gelombang n λ. Syarat pemantulan dan saling menguatkan dinyatakan oleh :
nλ = PO + OQ
nλ = 2d sin θ ; n = 1, 2, 3,……… (2.3) Dengan:
λ : panjang gelombang sinar-x yang digunakaan, d : jarak antar bidang (hkl) yang sama, dan θ : sudut difraksi
12
Tahap pertama yang dilakukan dalam analisa sinar-x adalah melakukan analisa pemeriksaan terhadap sampel x yang belum diketahui struktur nya. Sampel ditempatkan pada titik fokus haburan sinar-x yang tepat ditengah-tengah plat yang digunakan sebagai tempat yaitu sebuah plat tipis yang berlubang ditengah berukuran sesuai dengan sampel dengan perekat pada sisi baliknya (Afza,2011).
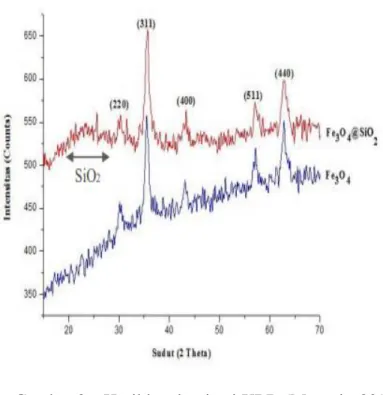
Gambar 2.6 Hasil karakterisasi XRD (Munasir, 2018)
Hasil uji XRD menunjukkan bahwa pola difraksi komposit Fe3O4 / SiO2 menunjukkan pola difraksi SiO2 pada posisi 2θ = 21-28 dengan struktur amorf dan pola difraksi Fe3O4
sesuai dengan masing-masing bidang kristal [6, 8]. Puncak difraksi komposit Fe3O4 / SiO2
yang terjadi pada sudut 2θ = 30,3 °, 35,5 °, 43,2 °, 57,0 °, 62,8 ° dengan masing-masing bidang kristal (220), (311), (400), (511), (440 ) yang juga menunjukkan puncak Fe3O4
yang tidak berubah [6,8,10]. Dari hasil puncak, sampel memiliki kemiripan dengan penelitian sebelumnya yang dilakukan oleh [8,10,11]. Berdasarkan hasil yang diperoleh
13
menunjukkan bahwa komposit telah berhasil terbentuk yang ditandai dengan munculnya puncak-puncak karakteristik Fe3O4 dan SiO2 (Munasir, 2018)
2.6.3 Scanning Electron Microscope (SEM)
Mikroskop pemindai elektron digunakan dalam situasi yang membutuhkan
pengamatan permukaan kasar dengan perbesaran berkisar antara 20-500.000 kali.
Sebelum melalui lensa elektromagnetik terakhir scanning raster mendefleksikan berkas elektron untuk men-scan permukaan sampel. Hasil scan ini tersinkronisasi dengan tabung sinar katoda dan gambar sampel akan tampak pada area yang di-scan. Tingkat kontras yang tampak pada tabung sinar katoda timbul karena hasil refleksi yang berbeda-beda dari sampel (Marlisa, 2017).
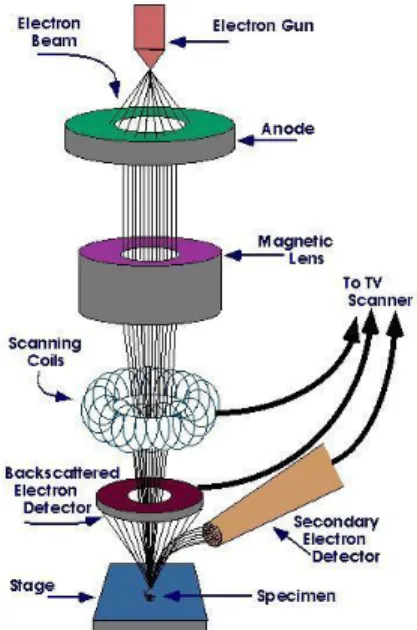
Gambar 2.7 Prinsip kerja SEM
Prinsip kerja SEM adalah dengan menggambarkan permukaan benda atau material dengan berkas elektron yang dipantulkan dengan energi tinggi. Permukaan materi yang disinari atau terkena berkas elektron yang memantulkan kembali berkas elektron atau dinamakan berkas elektron sekunder ke segala arah. Tetapi dari semua berkas elektron
14
yang dipantulkan dengan intensitas tertinggi. Detektor yang terdapat di dalam SEM akan mendeteksi berkas elektron berintensitas tertinggi yang dipantulkan oleh benda atau material yang dianalisis. Selain itu juga dapat menentukan lokasi berkas elektron yang berisintensitas tertinggi itu (Marlisa, 2017).
Gambar 2.8 Hasil Karakterisasi SEM (Weiyan, 2012)
Gambar menunjukkan bahwa partikel Fe3O4 berstruktur tetragonal. Ukuran partikelnya sekitar 400nn dan terdistribusi merata, dapat dilihat dengan jelas menunjukkan bahwa permukaan Fe3O4 menjadi halus; Tepi dan sudut tidak lagi jelas, pada saat yang sama ukuran partikel meningkat, menunjukkan bahwa SiO2
telah berhasil dibungkus pada permukaan Fe3O4 dan menunjukkan bahwa permukaan menjadi kasar dengan zat granular (Weiyan, 2012).
15
BAB III
METODOLOGI PENELITIAN
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan pada Bulan Januari 2021 sampai dengan Bulan Juli 2021 di : 1. Laboratorium Ilmu Dasar dan Umum Fakultas Matematika Ilmu Pengetahuan
Alam Universitas Sumatera Utara.
2. Pengujian karakterisasi X- Ray Diffraction (XRD) di Pusat Survei Geologi Bandung.
3. Pengujian karakterisasi Scanning Electron Microscope (SEM) di Laboratorium Terpadu Universitas Sumatera Utara.
3.2 Alat dan Bahan Penelitian 3.2.1 Alat
1. Beaker Glass
Fungsi : Sebagai wadah untuk menampung dan membuat larutan.
2. Tabung Ukur
Fungsi : Sebagai alat mengukur volume cairan.
3. Neraca Analitik
Fungsi : Untuk menimbang bahan yang akan digunakan.
4. Magnetic stirrer
Fungsi : Untuk mengaduk, memanaskan, dan menghomogenkan suatu larutan.
5. Oven
Fungsi : Sebagai alat mengeringkan sample.
6. Spatula
16
Fungsi : Sebagai alat untuk mengambil sampel.
7.Cawan porselin
Fungsi : Sebagai wadah untuk menguapkan larutan atau zat padat yang basah.
8.Pipet Tetes
Fungsi : untuk memindahkan larutan dari sebuah wadah ke wadah yang lain.
9.Lemari asam
Fungsi : Sebagai tempat reaksi kimia yang menggunakan bahan-bahan yang mudah menguap atau gas yang berbahaya.
3.2.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah
• Silikon Dioksida (SiO2) ( ID Merck : 1.13126.0500)
• Prekursor FeCl2.4H2O (ID Merck: 1.03861.0250)
• Prekursor FeCl3.6H2O (ID Merck: 1.00731.1000)
• Prekursor TEOS (ID Merck: 1.00808.1000)
• NH4OH
• Etanol
• Aquabidest
17
3.3 Prosedur Percobaan
3.3.1 Sintesis Fe3O4 dengan metode kopresipitasi dengan suhu 100ᵒC
Ditimbang FeCl3.6H2O (5,2001 gr) dan FeCl2.6H2O (2,0002 gr) kemudian ditambahkan 80 ml aquabides dan diaduk t = 1 jam lalu ditambahkan larutan V = 20 ml NH4OH (3,2 M). Kemudian larutan diaduk dengan t = 1 jam untuk menyempurnakan reaksi. Endapan dicuci menggunakan 10 ml etanol sebanyak 5 kali t = 20 menit dan V = 10 ml aquabides t = 20 menit. Dilakukan proses kalsinasi dengan T = 100ᵒC dengan t = 10 jam dan penggerusan menggunakan mortar t = 1 jam.
3.3.2 Sintesis Fe3O4 menggunakan Prekursor TEOS
Preparasi bahan Fe3O4 dengan prekursor TEOS. Sintesis Fe3O4 sebanyak3 gram didispersikan ke dalam 40 ml larutan etanol. Ditambahkan larutan 0.8 ml TEOS dan 4.5 ml NH4OH pekat secara cepat dengan menggunakan T = 30oC. Proses sintering t = 10 jam untuk menyempurnakan reaksi. Kemudian endapan dicuci menggunakan aquabidest dan etanol. Kalsinasi dengan suhu 100oC dengan t = 5 jam. Uji karakterisasi X-Ray Diffraction (XRD), Scanning Electron Microscope (SEM).
3.3.3 Sintesis Fe3O4/SiO2 dengan metode kopresipitasi
Preparasi bahan Fe3O4/SiO2 dengan metode kopresipitasi. Sintesis Fe3O4 sebanyak 3 gram didispersikan ke dalam V = 40 ml larutan etanol. Ditambahkan larutan 1 gram SiO2 dan 4.5 ml NH4OH pekat secara cepat dengan menggunakan T = 30oC. Proses sintering larutan diaduk dengan t = 10 jam untuk menyempurnakan reaksi. Kemudian endapan dicuci menggunakan air dan etanol. Kalsinasi dengan suhu 100oC dengan t = 5 jam. Uji karakterisasi X-Ray Diffraction (XRD), Scanning Electron Microscope (SEM).
18
3.4 Diagram Alir
3.4.1 Sintesis Fe3O4 dengan metode kopresipitasi dengan suhu 100ᵒC
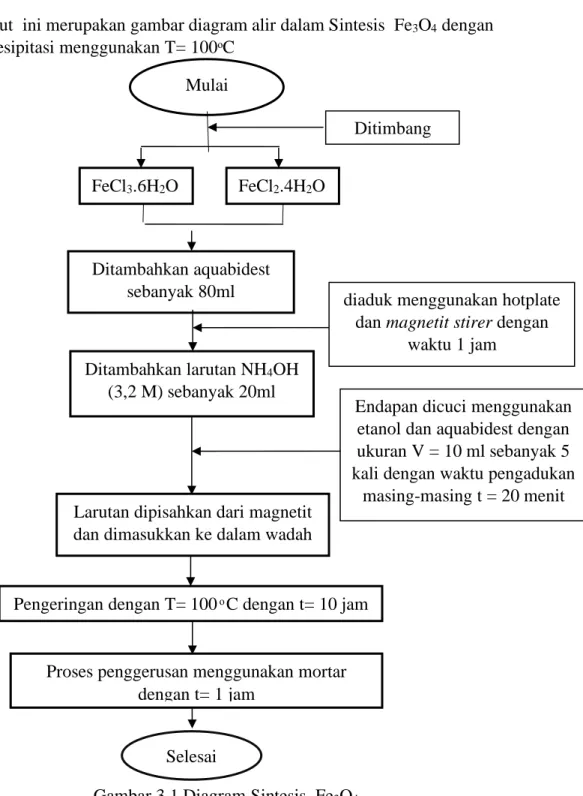
Berikut ini merupakan gambar diagram alir dalam Sintesis Fe3O4 dengan metode kopresipitasi menggunakan T= 100ᵒC
Gambar 3.1 Diagram Sintesis Fe3O4
Mulai
Proses penggerusan menggunakan mortar dengan t= 1 jam
Ditambahkan larutan NH4OH (3,2 M) sebanyak 20ml Ditambahkan aquabidest
sebanyak 80ml
FeCl2.4H2O FeCl3.6H2O
Larutan dipisahkan dari magnetit dan dimasukkan ke dalam wadah
Selesai
Pengeringan dengan T= 100 ͦ C dengan t= 10 jam
diaduk menggunakan hotplate dan magnetit stirer dengan
waktu 1 jam Ditimbang
Endapan dicuci menggunakan etanol dan aquabidest dengan ukuran V = 10 ml sebanyak 5 kali dengan waktu pengadukan
masing-masing t = 20 menit
19
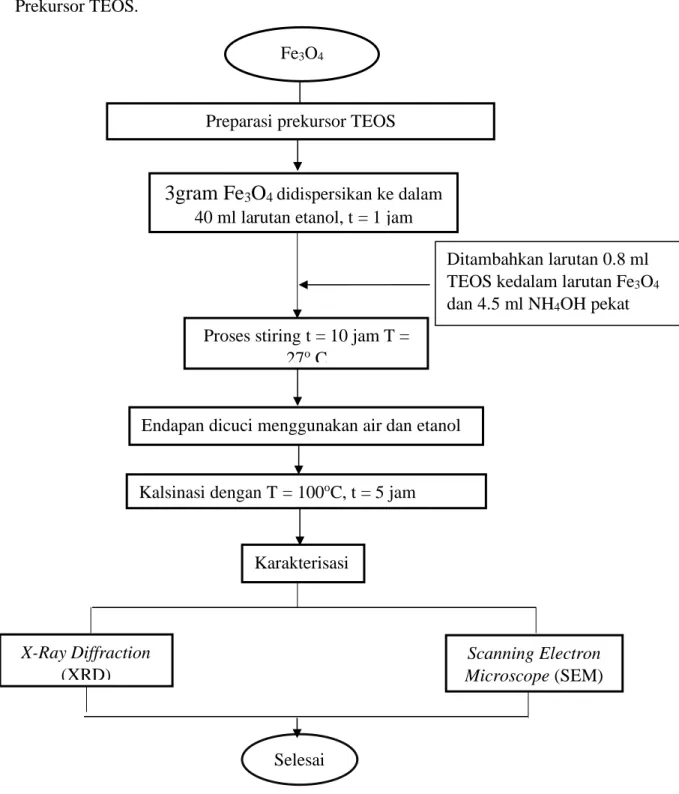
3.4.2 Sintesis Fe3O4 menggunakan Prekursor TEOS
Berikut ini merupakan gambar diagram alir Sintesis Fe3O4 menggunakan Prekursor TEOS.
Gambar 3.2 Sintesis Fe3O4 menggunakan Prekursor TEOS Fe3O4
Proses stiring t = 10 jam T = 27o C
3gram Fe3O4 didispersikan ke dalam 40 ml larutan etanol, t = 1 jam
Preparasi prekursor TEOS
Endapan dicuci menggunakan air dan etanol
Ditambahkan larutan 0.8 ml TEOS kedalam larutan Fe3O4
dan 4.5 ml NH4OH pekat
Kalsinasi dengan T = 100oC, t = 5 jam
Karakterisasi
X-Ray Diffraction (XRD)
Scanning Electron Microscope (SEM)
Selesai
20
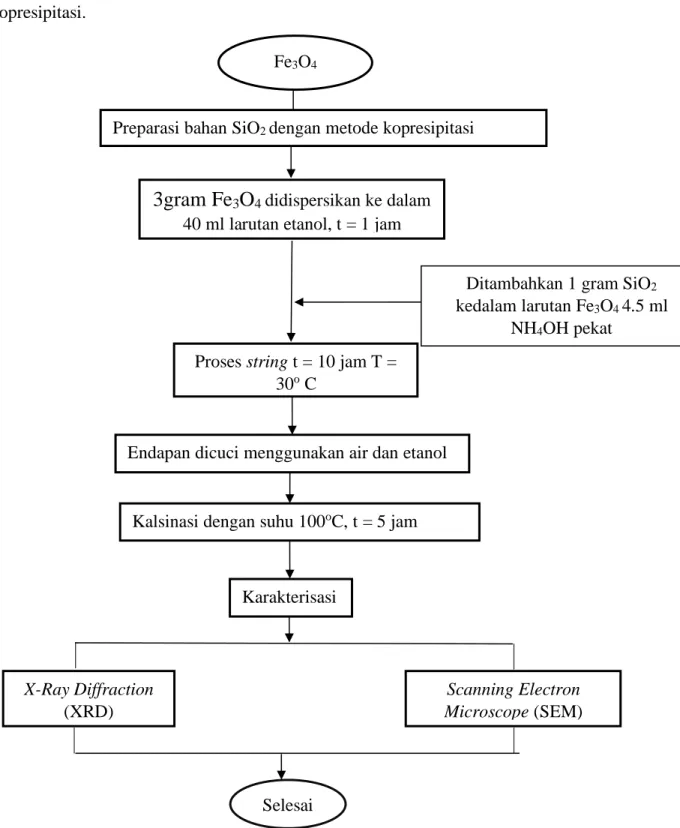
3.3.3 Sintesis Fe3O4/SiO2 dengan metode kopresipitasi
Dibawah ini merupakan gambar diagram alir Sintesis Fe3O4/SiO2 dengan metode kopresipitasi.
Gambar 3.3 Sintesis Fe3O4/SiO2 dengan metode kopresipitasi Fe3O4
Proses string t = 10 jam T = 30o C
3gram Fe3O4 didispersikan ke dalam 40 ml larutan etanol, t = 1 jam
Preparasi bahan SiO2 dengan metode kopresipitasi
Endapan dicuci menggunakan air dan etanol
Ditambahkan 1 gram SiO2
kedalam larutan Fe3O4 4.5 ml NH4OH pekat
Kalsinasi dengan suhu 100oC, t = 5 jam
Karakterisasi
X-Ray Diffraction (XRD)
Scanning Electron Microscope (SEM)
Selesai
21
BAB IV
HASIL DAN PEMBAHASAN
4.1 Analisis Hasil Karakterisasi Sintesis Fe3O4/SiO2 melalui metode Kopresipitasi
4.1.1 Hasil pola XRD pada Fe3O4/SiO2 dan Fe3O4/ SiO2 5%
Untuk dapat mengetahui fasa-fasa yang terbentuk pada sampel dilakukan pengujian menggunakan X- Ray Diffraction (XRD). Pengujian XRD dilakukan untuk mengetahui fasa yang terbentuk, puncak (peak) tertinggi dan struktur Kristal sampel Fe3O4/SiO2 dan Fe3O4/ SiO2 5% pada Gambar 4.1
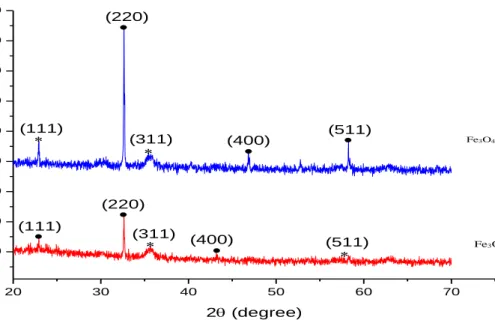
Gambar 4.1 (a) Hasil Pola XRD sampel Fe3O4/SiO2 (b) Hasil pola XRD sampel Fe3O4/ SiO2 5%
Hasil karakterisasi XRD pada gambar 4.1 (a) menunjukkan bahwa Fe3O4/SiO2 memiliki puncak utama pada daerah 2θ yaitu 32,6° yang merupakan puncak bidang (220) Berdasarkan PDF number 04-002-3668, International Center of Diffraction Data (ICDD)
20 30 40 50 60 70
200 400 600 800 1000 1200 1400 1600 1800
•
•
•
•
•
Insensity (cps)
2 (degree)
Fe3O4/SiO2 5%
Fe3O4/SiO2
• (111)
(111)
(220)
(220) (311)
(311) (400)
(400) (511)
(511)
22
puncak teridentifikasi dalam sampel Fe3O4/SiO2 murni secara berturut turut (111), (220), (311), (400), dan (511).
Gambar 4.1 b menunjukan pola difraksi untuk sampel Fe3O4/ SiO2 5%
penambahan 5% SiO2. Pada gambar dapat dilihat bahwa terjadi pergeseran di 2θ yaitu 32,68° yang merupakan puncak bidang (220), melainkan terjadinya intesitasnya yang naik dikarenakan penambahan SiO2 yang bersifat amorf. Fasa-fasa yang terbentuk oleh pola difraksi pada gambar 4.1 untuk sampel Fe3O4/SiO2 dan Fe3O4/ SiO2 5% adalah fasa tunggal.
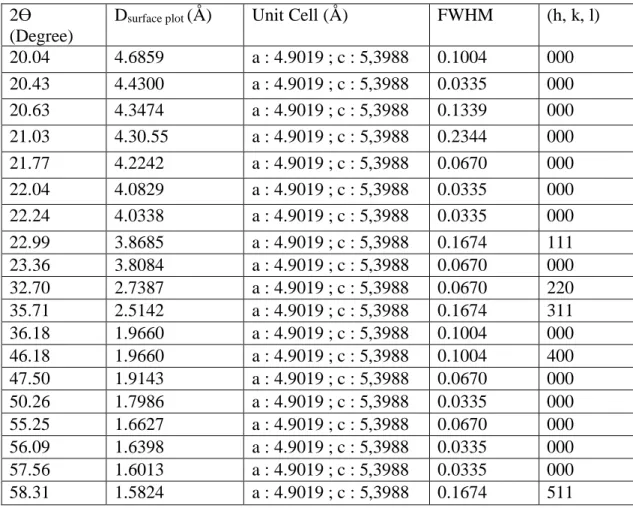
Tabel 4.1 Data Sampel Fe3O4/SiO2 dan Sampel Fe3O4/ SiO2 5% Hasil XRD 2Ө
(Degree)
Dsurface plot (Å) Unit Cell (Å) FWHM (h, k, l)
20.04 4.6859 a : 4.9019 ; c : 5,3988 0.1004 000 20.43 4.4300 a : 4.9019 ; c : 5,3988 0.0335 000 20.63 4.3474 a : 4.9019 ; c : 5,3988 0.1339 000 21.03 4.30.55 a : 4.9019 ; c : 5,3988 0.2344 000 21.77 4.2242 a : 4.9019 ; c : 5,3988 0.0670 000 22.04 4.0829 a : 4.9019 ; c : 5,3988 0.0335 000 22.24 4.0338 a : 4.9019 ; c : 5,3988 0.0335 000 22.99 3.8685 a : 4.9019 ; c : 5,3988 0.1674 111 23.36 3.8084 a : 4.9019 ; c : 5,3988 0.0670 000 32.70 2.7387 a : 4.9019 ; c : 5,3988 0.0670 220 35.71 2.5142 a : 4.9019 ; c : 5,3988 0.1674 311 36.18 1.9660 a : 4.9019 ; c : 5,3988 0.1004 000 46.18 1.9660 a : 4.9019 ; c : 5,3988 0.1004 400 47.50 1.9143 a : 4.9019 ; c : 5,3988 0.0670 000 50.26 1.7986 a : 4.9019 ; c : 5,3988 0.0335 000 55.25 1.6627 a : 4.9019 ; c : 5,3988 0.0670 000 56.09 1.6398 a : 4.9019 ; c : 5,3988 0.0335 000 57.56 1.6013 a : 4.9019 ; c : 5,3988 0.0335 000 58.31 1.5824 a : 4.9019 ; c : 5,3988 0.1674 511
23
4.1.2 Hasil pola XRD pada sampel Fe3O4/TEOS dan Fe3O4/TEOS 5%
Untuk dapat mengetahui fasa-fasa yang terbentuk pada sampel dilakukan pengujian menggunakan X- Ray Diffraction (XRD). Pengujian XRD dilakukan untuk mengetahui fasa yang terbentuk, puncak (peak) tertinggi dan struktur Kristal sampel Fe3O4/TEOS
dan Fe3O4/ TEOS5% pada Gambar 4.2
Gambar 4.2 (a) Hasil Pola XRD sampel Fe3O4/ TEOS (b) Hasil pola XRD sampel Fe3O4/
TEOS 5%
Hasil karakterisasi XRD pada gambar 4.2 (a) menunjukkan bahwa Fe3O4/TEOSmemiliki puncak utama pada daerah 2θ yaitu 32,6° yang merupakan puncak bidang (220) Berdasarkan PDF number 04-002-3668, International Center of Diffraction Data (ICDD)
20 30 40 50 60 70
200 400 600 800 1000 1200 1400 1600 1800 2000 2200 2400 2600 2800
•
•
•
•
insensity (cps)
2 (degree)
Fe3O4/TEOS 5%
Fe3O4/TEOS
•
(111)
(111)
(220) (220)
(311) (311)
(400) (400)
(511) (511)
24
puncak teridentifikasi dalam sampel Fe3O4/TEOSmurni secara berturut turut (111), (220), (311), (400), dan (511).
Gambar 4.1 b menunjukan pola difraksi untuk sampel Fe3O4/ TEOS 5%
penambahan 5% TEOS. Pada gambar dapat dilihat bahwa tidak terjadi pergeseran tetap di 2θ yaitu 32,68° yang merupakan puncak bidang (220), melainkan terjadinya intesitasnya yang naik dikarenakan penambahan TEOSyang bersifat amorf. Fasa-fasa yang terbentuk oleh pola difraksi pada gambar 4.1 untuk sampel Fe3O4/TEOS dan Fe3O4/ TEOS5% adalah fasa tunggal.
Tabel 4.2 Data Sampel Fe3O4/TEOS dan Sampel Fe3O4/ TEOS5% hasil XRD 2Ө
(Degree)
Dsurface plot (Å) Unit Cell (Å) FWHM (h, k, l)
20.83 4.44550.670 a : 4.7650 ; c : 5,2960 0.0670 000 21.85 4.0681 a : 4.7650 ; c : 5,2960 0.0335 000 22.07 4.0284 a : 4.7650 ; c : 5,2960 0.0670 000 22.64 3.9866 a : 4.7650 ; c : 5,2960 0.0670 000 23.02 3.8636 a : 4.7650 ; c : 5,2960 0.1004 111 23.89 3.7637 a : 4.7650 ; c : 5,2960 0.0335 000 24.04 3.7017 a : 4.7650 ; c : 5,2960 0.2009 000 25.10 3.5649 a : 4.7650 ; c : 5,2960 0.0335 000 26.42 3.3738 a : 4.7650 ; c : 5,2960 0.0670 000 27.51 3.2428 a : 4.7650 ; c : 5,2960 0.1004 000 28.73 3.1075 a : 4.7650 ; c : 5,2960 0.1004 000 29.18 3.0604 a : 4.7650 ; c : 5,2960 0.0670 000 30.37 2.9433 a : 4.7650 ; c : 5,2960 0.1004 000 31.19 2.8678 a : 4.7650 ; c : 5,2960 0,0335 000 32.75 2.7349 a : 4.7650 ; c : 5,2960 0.1004 220 35.56 2.5248 a : 4.7650 ; c : 5,2960 0.1674 311 40.38 2.2338 a : 4.7650 ; c : 5,2960 0.0670 000 43.24 2.0923 a : 4.7650 ; c : 5,2960 0.0335 000 46.96 1.9350 a : 4.7650 ; c : 5,2960 0.1004 400 58.38 1.5809 a : 4.7650 ; c : 5,2960 0.0670 511
25
4.2 Analisis Struktur menggunakan SEM (Scanning Electron Microscope)
terhadap Sintesis Fe3O4/SiO2 melalui metode kopresipitasi
4.2.1 Hasil SEM (Scanning Electron Microscope) sampel Fe3O4/SiO2
Analisis menggunakan alat Scanning Electron Microscopy (SEM) dilakukan untuk mengetahui mikrostruktur Fe3O4/SiO2. Dari gambar 4.3 dibawah ini dapat diamati
mikrostruktur sampel Fe3O4/SiO2 kristalit yang terbentuk tidak homogen.
(a) (b)
Gambar 4.3 (a) Hasil SEM Sampel Fe3O4/ SiO2 perbesaran 500 kali (b) Hasil SEM Sampel Fe3O4/ SiO2 perbesaran 5000 kali.
Dari Gambar di atas dapat dilihat bahwa sampel Fe3O4/ SiO2 dianalisis menggunakan SEM dengan perbesaran 500 kali dan 5000 kali, masing-masing ditunjukkan pada gambar 4.3 (a) dan (b). Dari hasil analisis menunjukkan bahwa sampel Fe3O4/ SiO2 tidak homogen yang ditunjukkan oleh adanya celah pada permukaan sampel. Hal ini disebabkan oleh waktu penggerusan sampel yang terlalu singkat yang mengakibatkan adanya jarak antar partikel, sehingga persebaran partikel sampel tidak merata dan permukaan sampel tidak homogen.
26
4.2.2 Hasil SEM (Scanning Electron Microscope) sampel Fe3O4/ SiO2 5%
Analisis menggunakan alat Scanning Electron Microscopy (SEM) dilakukan untuk mengetahui mikrostruktur Fe3O4/SiO2 5%. Dari gambar 4.3 dibawah ini dapat diamati
mikrostruktur sampel Fe3O4/SiO2 5% kristalit yang terbentuk tidak homogen.
(a) (b)
Gambar 4.4 (a) Hasil SEM Sampel Fe3O4/ SiO2 5% perbesaran 500 kali (b) Hasil SEM Sampel Fe3O4/ SiO2 5% perbesaran 5000 kali.
Dari Gambar di atas dapat dilihat bahwa sampel Fe3O4/ SiO2 5% dianalisis menggunakan SEM dengan perbesaran 500 kali dan 5000 kali, masing-masing ditunjukkan pada gambar 4.3 (a) dan (b). Dari hasil analisis menunjukkan bahwa sampel Fe3O4/ SiO2 5% tidak homogen yang ditunjukkan oleh adanya celah pada permukaan sampel. Hal ini disebabkan oleh waktu penggerusan sampel yang terlalu singkat yang mengakibatkan adanya jarak antar partikel, sehingga persebaran partikel sampel tidak merata dan permukaan sampel tidak homogen.
4.2.3 Hasil SEM (Scanning Electron Microscope) sampel Fe3O4/ TEOS
Analisis menggunakan alat Scanning Electron Microscopy (SEM) dilakukan untuk mengetahui mikrostruktur Fe3O4/TEOS. Dari gambar 4.3 dibawah ini dapat diamati
mikrostruktur sampel Fe3O4/TEOS kristalit yang terbentuk tidak homogen.
27
(a) (b)
Gambar 4.5 (a) Hasil SEM Sampel Fe3O4/ TEOS perbesaran 500 kali (b) Hasil SEM Sampel Fe3O4/ TEOS perbesaran 5000 kali.
Dari Gambar di atas dapat dilihat bahwa sampel Fe3O4/ TEOS dianalisis menggunakan SEM dengan perbesaran 500 kali dan 5000 kali, masing-masing ditunjukkan pada gambar 4.3 (a) dan (b). Dari hasil analisis menunjukkan bahwa sampel Fe3O4/ TEOS tidak homogen yang ditunjukkan oleh adanya celah pada permukaan sampel. Hal ini disebabkan oleh waktu penggerusan sampel yang terlalu singkat yang mengakibatkan adanya jarak antar partikel, sehingga persebaran partikel sampel tidak merata dan permukaan sampel tidak homogen.
4.2.4 Hasil SEM (Scanning Electron Microscope) sampel Fe3O4/ TEOS 5%
Analisis menggunakan alat Scanning Electron Microscopy (SEM) dilakukan untuk mengetahui mikrostruktur Fe3O4/TEOS 5% Dari gambar 4.3 dibawah ini dapat diamati
mikrostruktur sampel Fe3O4/TEOS 5% kristalit yang terbentuk tidak homogen.
28
(a) (b)
Gambar 4.5 (a) Hasil SEM Sampel Fe3O4/ TEOS 5% perbesaran 500 kali (b) Hasil SEM Sampel Fe3O4/ TEOS 5% perbesaran 5000 kali.
Dari Gambar di atas dapat dilihat bahwa sampel Fe3O4/ TEOS 5% dianalisis menggunakan SEM dengan perbesaran 500 kali dan 5000 kali, masing-masing ditunjukkan pada gambar 4.3 (a) dan (b). Dari hasil analisis menunjukkan bahwa sampel Fe3O4/ TEOS 5% tidak homogen yang ditunjukkan oleh adanya celah pada permukaan sampel. Hal ini disebabkan oleh waktu penggerusan sampel yang terlalu singkat yang mengakibatkan adanya jarak antar partikel, sehingga persebaran partikel sampel tidak merata dan permukaan sampel tidak homogen.
29
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Berdasarkan hasil penelitian dan pembahasan yang telah dilakukan, dapat di peroleh kesimpulan sebagai berikut:
1.Sintesis Fe3O4/ SiO2 telah berhasil di lakukan dengan Metode Kopresipitasi.
2. Hasil pengujian XRD dan SEM
a. Hasil karakterisasi XRD menunjjukan semua sampel mengkristal baik dengan puncak 32,6º dan 32,68 puncak bidang (111),(220),(311), (400), dan (511).
b. Hasil karakterisasi sampel menggunakan Scanning Electron Microscopy (SEM) menunjukan bahwa sampel tidak homogen, hal ini disebabkan oleh waktu penggerusan sampel yang terlalu singkat yang mengakibatkan adanya jarak antar partikel, sehingga persebaran partikel sampel tidak merata dan permukaan sampel tidak homogen.
5.2 Saran
1. Untuk menghasikan permukaan sampel yang homogen di perlukan ketelitian dan waktu yang cukup untuk penggerusan sampel.
2. Untuk penelitian selanjutnya diharapkan untuk mengkaji lebih banyak sumber maupun refrensi yang terkait dengan penelitian.
3. Untuk penelitian selanjutnya diharapkan agar lebih memperhatikan tempat pembuatan sampel, lengkap atau tidaknya alat alat yang di perlukan untuk penelitian agar tidak terlalu lama mendiamkan sampel.
30
DAFTAR PUSTAKA
Afza E, 2011. Pembuatan Magnet Permanent Ba-Hexa Ferrite (Bao.6Fe2O3) Dengan Metode Koopresipitasi Dan Karakterisasinya. Medan: Universitas Sumatera Utara, Program Studi S-1.
Agus Salim, 2012. Sintesis dan Karakterisasi Silica Gel dari Tetraetilortosilikat (TEOS) Menggunakan Surfaktan Polyethylene Glycol (PEG) 6000 dalam Kondisi Basa.
Universitas Deponegoro. Semarang.
Amalia P.L., Rahadian Z. 2011. Interaksi molekular ammonium hidroksida.
Universitas padang. Padang. Asadina Kusma Cahyaninggalih.
B. Permana, 2017. Sintesis nanopartikel gan metode kopresipitasi. Universitas Padjadjaran. Bandung.
Cucun A. R., Nur A.W. 2018. Characterization of Fe3O4 nanoparticles and their application for Ni (II) and Co (II) adsorption. uksw.edu. Jawa tengah.
Cucun A. R., Nur A.W. 2019. Karakterisasi Nanopartikel Fe3O4 Dan Aplikasi nya dalam Adsorpsi Ni(II) dan Co(II). Universitas Kristen Satya Wacana. Jawa Tengah.
Hefdea A, 2020. Sintesis Fe3O4 dari pasir mineral tulungagung menggunakan metode kopresipitasi. Universitas Negeri Surabaya. Surabaya.
Indrayana tedy, 2019 Sintesis karakterisasi dan fungsionalisasi hingga aplikasi dalam bidang nanoteknologi maju. Universitas Halmahera. Maluku Utara.
Lisa Marlisa, 2017. Uji Karakterisasi Nanopartikel Magnetit Fe3O4
Menggunakan X-RAY Diffraction dan Scaning Elctron.Microscopy.
Univesits Islam Alauddin. Makassar.
Rahmat, 2017. Pembuatan dan karakterisasi magnetic elastomer.Uin Alauddin Makassar. Makassar.
31
Retnosari Agustin. 2013. Ekstraksi dan penentuan kadar silika (SiO2) hasil
ekstraksi dari abu terbang (fly ash) batubara. Universitas jember. Jember Sahidin.A.2012. Sintesis Komposit Fe3O4 - SiO2 – TiO2 dan aplikasinya untuk
mendegradasi limbah zat warna methylene blue. BATAN.Tangerang Selatan.
Sari Mayang, 2011. Identifikasi protein menggunakan FTIR. Teknik kimia Universitas Indonesia Depok, Jakarta.
Sera Merdekani, 2013. Sintesis Partikel Nanokomposit Fe3O4/SiO2 Dengan Metode Korpresipitasi.kimia UNPAD jatunangor. Bandung.
Siti Nurjanah. 2018. Sintesis dan karakterisasi nanopartikel magnetik Fe3O4 pasir besi glagah kulon progo dengan metode kopresipitasi. Universitas negeri yogyakarta.
Yogyakarta.
Siti, W., W. Ari, S. Winatapura. 2016. The SiO2 addition effect to Fe3O4/TiO2
photocatalytic characteristic and performance on methylene blue
degradation. Pusat sains dan teknologi bahan maju, BATAN. Gedung 42, puspiptek Serpong, Tangerang Selatan.
Suryani, 2015. Sintesis Nanopartikel Magnetite (Fe3O4) dengan Template Silika (SiO2) dan Karakterisasi Sifat Kemagnetannya. Universitas Gadjah Mada. Yogjakarta.
Trianasari, 2017. Analisis dan Karakterisasi kandungan Silika (SiO2) sebagai Hasil Ektraksi Batu apung (pumice).
Wei Y., Han B., Xiaoyang H., Lin Y., Wang X., Deng X. 2012. Syntesis of
Fe3O4 nanoparticles and their magnetic properties. Chinese materials conference. China.
Yudia, P. N. 2018. Sintesis dan karakterik nanopartikel silika dari limbah geothermal sebagai fluorescent fingerprint powder. UINSYAH. Jakarta.
32
LAMPIRAN 1
GAMBAR PERALATAN DAN BAHAN
Tabung Ukur Magnetit Stirer
33
Pipet Tetes Gelas Ukur
Neraca Analitik Cawan Porselin
Spatula Mortar
34
Oven Lemari Asam
PrekursorFeCl3.6H2O NH4OH
35
Etanol Aquabidest
Prekursor FeCl2.4H2O
36
LAMPIRAN 2
HASIL PERHITUNGAN NH
4OH PEKAT MENJADI NH
4OH 3,2 MOLAR
Perhitunga NH4OH pekat menjadi NH4OH 3,2 Molar Proses pencampuran NH4OH pekat dengan Aquabides
NH4OH = 7+4+16+1 = 28 M = 𝑔𝑟
𝑀𝑟 × 1000
𝑉
3.2 = 𝑔𝑟
28 × 1000
100
89.6 = 10 gr gr = 89.6
10
= 8.96 gram
Massa NH4OH = 8.96 gram = 8.96 mililiter 1 gram = 1 milimeter
Proses pencampuran NH4OH pekat dengan Etanol
M1V1 = M2V2
3,2 . V1 (ml) = 98% . 1000 (ml) 3,2 . V1 = 1,73 . 1000 ml
V1 =1,73
3,2
V1 = 5,4 ml
37
Etanol = mol = 0,173 ml
M = mol × 100
𝑃
M = 0,173 × 1000
100
M = 1,73
Maka, V NH4OH = 5,4 mililiter
38
LAMPIRAN 3
Match Report
Sample: 0284 XRD
Diffraction Pattern Graphics
Match! Copyright © 2003-2021 CRYSTAL IMPACT, Bonn, Germany
39
Sample: 0285 XRD
Diffraction Pattern Graphics
Match! Copyright © 2003-2021 CRYSTAL IMPACT, Bonn, Germany
40
Sample: 02846 XRD
Diffraction Pattern Graphics
Match! Copyright © 2003-2021 CRYSTAL IMPACT, Bonn, Germany
41
Sample: 0287 XRD
Diffraction Pattern Graphics
Match! Copyright © 2003-2021 CRYSTAL IMPACT, Bonn, Germany
42