APLIKASI SELULOSA-g-POLIAKRILAMIDA SEBAGAI
FASE DIAM KROMATOGRAFI KOLOM DAN SINTESISNYA
MELALUI REAKSI KOPOLIMERISASI CANGKOK DAN
TAUT-SILANG
TATI ROHAYATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
BOGOR 2014
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Aplikasi Selulosa-g-Poliakrilamida sebagai Fase Diam Kromatografi Kolom dan Sintesisnya Melalui Reaksi Kopolimerisasi Cangkok dan Taut-Silang adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Desember 2013
Tati Rohayati
ABSTRAK
TATI ROHAYATI. Aplikasi Selulosa-g-Poliakrilamida sebagai Fase Diam Kromatografi Kolom dan Sintesisnya Melalui Reaksi Kopolimerisasi Cangkok dan Taut-Silang. Dibimbing oleh TUN TEDJA IRAWADI dan NOVRIYANDI HANIF.
Kopolimerisasi cangkok dan taut-silang akrilamida pada isolat selulosa serabut ampas sagu telah dilakukan dengan N,N’-metilena-bis-akrilamida (MBA) sebagai penaut-silang dan amonium peroksidisulfat sebagai inisiator. Jumlah MBA yang ditambahkan sebanyak 1.0, 1.5, dan 2.0 g. Nisbah dan efisiensi pencangkokan dengan 2.0 g MBA adalah paling tinggi, sedangkan kapasitas penyerapan airnya adalah paling rendah. Spektrum inframerah menunjukkan adanya gugus amida, hidroksil, dan eter. Distribusi ukuran pori produk tergolong mesopori (diameter 3.6 nm). Mikrograf elektron pemayaran memperlihatkan morfologi permukaan yang lebih rapat pada selulosa-g-poliakrilamida dengan penambahan 2.0 g MBA. Kinerja produk dievaluasi menggunakan kromatografi cair kinerja tinggi menggunakan ekstrak temu lawak (Curcuma xanthorrizha). Nilai selektivitas dan resolusi pemisahan xantorizol dengan fase diam hasil penambahan 2.0 g MBA berturut-turut sebesar 1.276 dan 1.870. Spektrum resonans magnet inti dan nilai rotasi spesifik xantorizol hasil pemisahan membuktikan bahwa fase diam yang digunakan tidak mengubah struktur dan konfigurasi tiga dimensi xantorizol, sehingga dapat diajukan sebagai material bernilai guna tinggi dalam pengembangan komersial.
Kata kunci: kopolimerisasi cangkok, kromatografi, penaut-silang, selulosa
ABSTRACT
TATI ROHAYATI. Application of Cellulose-g-Polyacrylamide as a Stationary Phase Column Chromatography and Its Synthesis through Grafting and Crosslinking Copolymerization Reaction. Supervised by TUN TEDJA IRAWADI and NOVRIYANDI HANIF.
The graft and crosslink copolymerization of acrylamide to cellulose isolate have been carried out using N,N’-methylene-bis-acrylamide (MBA) as crosslinker and ammonium peroxydisulfate as initiator. The amount of MBA added were 1.0, 1.5, and 2.0 g. Grafting ratio and efficiency of cellulose-g-polyacrylamide using MBA 2.0 g were the highest, while water absorption capacity was the lowest. Infrared spectrum showed the presence of amide and hydroxyl as well as ether functional groups. Pore size distribution of the product was classified as mesoporous (3.6 nm in diameter). Scanning electron micrograph showed a more tight surface morphology on cellulose-g-polyacrylamide with addition of 2.0 g MBA. Performances of the product were evaluated by high performance liquid chromatography using Curcuma xanthorrhiza extract. The selectivity and resolution value of xanthorrhizol separation in the stationary phase synthesized from 2.0 g MBA addition were 1.276 and 1.870, respectively. Nuclear magnetic resonance spectrum and specific rotation value of the isolated xanthorrhizol proved that the stationary phase did not change the structure and the three-dimensional configuration of the xanthorrhizol, so that it can be proposed as a highly useful value in commercial development.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
APLIKASI SELULOSA-g-POLIAKRILAMIDA SEBAGAI
FASE DIAM KROMATOGRAFI KOLOM DAN SINTESISNYA
MELALUI REAKSI KOPOLIMERISASI CANGKOK DAN
TAUT-SILANG
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
BOGOR 2014
Judul Skripsi : Aplikasi Selulosa-g-Poliakrilamida sebagai Fase Diam Kromatografi Kolom dan Sintesisnya Melalui Reaksi Kopolimerisasi Cangkok dan Taut-Silang
Nama : Tati Rohayati
NIM : G44090041
Disetujui oleh
Prof Dr Ir Tun Tedja Irawadi, MS Pembimbing I
Novriyandi Hanif, DSc Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
Judul Skripsi : Aplikasi Selulosa-g-Poliakrilamida sebagai Fase Diam
Kromatografi Kolom dan Sintesisnya Melalui Realesi
Kopolimerisasi Cangkok dan Taut-Silang
Nama : Tati Rohayati
NIM : G44090041
Disetujui oleh
Prof Dr Ir Tun Tedja Irawadi, MS
Pembimbing I
Diketahui oleh
Prof Dr MS
PRAKATA
Assalamualaikum Wr. Wb.
Puji dan syukur penulis panjatkan ke hadirat Yang Maha Kuasa Allah SWT karena atas rahmat dan karunia-Nya penulis dapat menyelesaikan karya ilmiah ini yang dilaksanakan sejak bulan Februari sampai Oktober 2013. Tema yang dipilih adalah Aplikasi Selulosa-g-Poliakrilamida sebagai Fase Diam Kromatografi Kolom dan Sintesisnya Melalui Reaksi Kopolimerisasi Cangkok dan Taut-Silang sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada Departemen Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Penulis mengucapkan terima kasih atas semua bimbingan, dukungan, dan kerja sama yang telah diberikan oleh Ibu Tun Tedja Irawadi dan Bapak Novriyandi Hanif selaku pembimbing. Selain itu, penghargaan penulis sampaikan kepada Ibu Henny Purwaningsih, Bapak Muhammad Farid, dan Bapak Mohammad Khotib atas segala diskusi dan saran berkaitan dengan penelitian, serta kepada Kepala Laboratorium Kimia Terpadu (LT IPB) atas fasilitas yang diberikan selama penulis melakukan penelitian dan staf LT yang turut memberikan motivasi dalam pembuatan karya ilmiah ini. Ungkapan terima kasih juga disampaikan kepada Ayah, Ibu, serta seluruh keluarga, atas doa dan kasih sayangnya.
Semoga karya ilmiah ini dapat bermanfaat. Terima kasih.
Wassalamualaikum Wr. Wb.
Bogor, Desember 2013
DAFTAR ISI
DAFTAR TABEL vii
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN vii
PENDAHULUAN 1
METODE 2
Alat dan Bahan 2
Preparasi Sampel dan Isolasi Selulosa Serabut Ampas Sagu 2
Pencirian Selulosa 2
Sintesis Fase Diam 2
Pencirian Fase Diam Selulosa-g-poliakrilamida 3
Kromatografi Kolom 4
Analisis Fraksi dengan Hasil Pemisahan Terbaik 5
HASIL DAN PEMBAHASAN 5
Kopolimer Cangkok dan Taut-Silang 5
Selulosa-g-poliakrilamida 6
Ciri-ciri Selulosa-g-Poliakrilamida 8
Hasil Aplikasi Selulosa-g-poliakrilamida sebagai Fase Diam 10
SIMPULAN DAN SARAN 13
Simpulan 13
Saran 13
DAFTAR PUSTAKA 13
LAMPIRAN 16
DAFTAR TABEL
1 Komponen kimia isolat selulosa serabut ampas sagu 5
2 Hasil analisis ukuran pori 9
DAFTAR GAMBAR
1 Nilai NP dan EP hasil sintesis selulosa-g-poliakrilamida dengan
berbagai bobot MBA 7
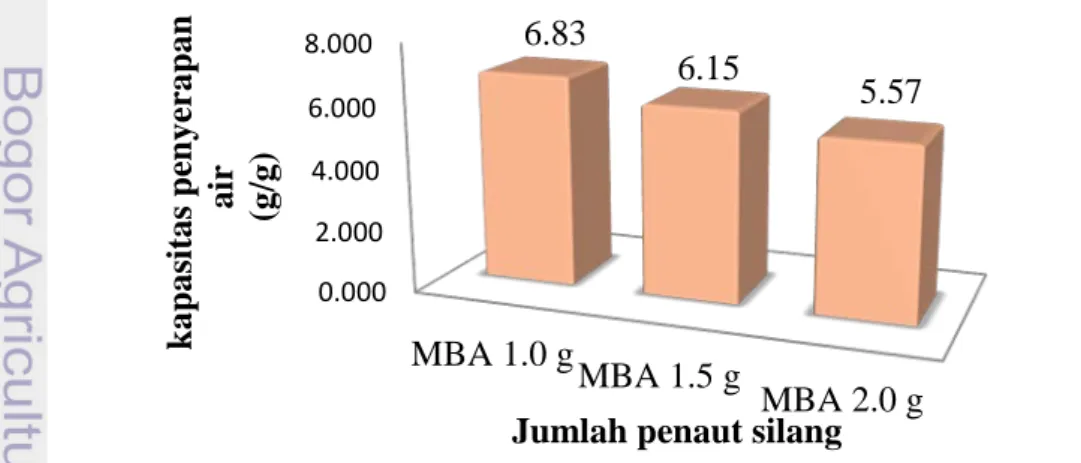
2 Nilai kapasitas penyerapan air hasil sintesis selulosa-g-poliakrilamida
dengan berbagai bobot MBA 7
3 Spektrum IR isolat selulosa dan selulosa-g-poliakrilamida dengan penaut-silang MBA sebanyak 1.0 g, 1.5 g, dan 2.0 g 8 4 Mikrograf isolat selulosa dengan perbesaran 750× dan 1500× 9 5 Mikrograf hasil sintesis dengan 1.0 g MBA pada perbesaran 750× dan
1500× 10
6 Mikrograf hasil sintesis dengan 1.5 g MBA pada perbesaran 750× dan
1500× 10
7 Mikrograf hasil sintesis dengan 2.0 g MBA pada perbesaran 750× dan
1500× 10
8 Struktur R*-(‒)-xantorizol 12
DAFTAR LAMPIRAN
1 Bagan alir penelitian 16
2 Reaksi kopolimerisasi 17
3 Hasil pembuatan kopolimer selulosa-g-poliakrilamida 19 4 Analisis kadar N kopolimer selulosa-g-poliakrilamida 20 5 Hasil perhitungan kapasitas penyerapan air 21
6 Pencirian pita FTIR 21
7 Hasil analisis distribusi ukuran pori silika gel komersial 21
8 Hasil analisis KCKT 22
9 Hasil analisis 1H-NMR 29
17
PENDAHULUAN
Indonesia merupakan salah satu negara penghasil tanaman sagu terbesar di dunia. Sagu telah lama dibudidayakan secara luas di beberapa wilayah nusantara, seperti Riau, Sulawesi Selatan, Maluku, dan Papua. Di Maluku dan Papua, tanaman ini menjadi sumber karbohidrat yang penting bagi penduduknya sehingga dapat menjadi pangan alternatif yang meringankan atau bahkan mengatasi masalah ketahanan pangan nasional (Jong dan Widjono 2007). Jumlah industri pengolahan sagu semakin meningkat berdasarkan data ekspor tepung sagu pada tahun 2010, 2011, dan 2012 (BPS 2012). Meningkatnya industri pengolahan sagu diiringi dengan meningkatnya limbah yang dihasilkan. Industri pengolahan sagu menghasilkan limbah berupa ampas sagu (ela dan serabut), air buangan, dan kulit batang. Air buangan biasanya dialirkan ke sungai, sedangkan ampas sagu digunakan untuk pakan ternak, sumber zat hara bagi tanah, dan herbisida (Kumoro et al. 2008).
Serabut ampas sagu mengandung selulosa yang lebih tinggi dibandingkan dengan ela ampas sagu. Setyorini (2011) menyatakan bahwa serabut ampas sagu mengandung 41.47% α-selulosa, sedangkan Segara (2011) menyatakan bahwa ela ampas sagu mengandung 14.23% α-selulosa. Oleh karena itu, dalam penelitian ini digunakan isolat selulosa dari serabut ampas sagu. Berbagai penelitian telah dilakukan untuk meningkatkan nilai ekonomis ampas sagu. Kumaran et al. (1997) melaporkan bahwa serabut ampas sagu berpotensi sebagai solid substrate
fermentation. Kandungan utama serabut ampas sagu adalah selulosa dan lignin
yang berpotensi sebagai absorben ramah lingkungan (Vickineswary et al. 1994). Selulosa telah lama dipelajari karena kelimpahannya, harganya murah, tidak berbahaya, mudah terdegradasi, dan dapat diperbaharui (Lin et al. 2009). Selain itu, selulosa dapat dimodifikasi dengan teknik kopolimerisasi. Selulosa dikopolimerisasi melalui cangkok dan taut-silang dengan berbagai paduan sebagai fase diam, superabsorben, dan berbagai keperluan industri lainnya (Israel et al. 2008).
Setyorini (2011) telah memodifikasi isolat selulosa yang berasal dari serabut ampas sagu melalui kopolimerisasi cangkok dan taut-silang dengan nisbah
selulosa-akrilamida (AAm) 1:1 dengan penambahan N,N’-metilena-bis-akrilamida
(MBA) sebanyak 0.1, 0.5, dan 1.0 g sebagai penaut-silang. Produk yang dihasilkan dapat memisahkan xantorizol dari ekstrak kasar temu lawak.
Penelitian ini menggunakan AAm yang dicangkokkan pada isolat selulosa dari serabut ampas sagu dengan nisbah 3:1 dengan penaut-silang MBA sebanyak 1.0, 1.5, dan 2.0 g. Penggunaan komposisi selulosa yang lebih besar bertujuan memanfaatkan lebih banyak limbah serabut ampas sagu agar dapat mengatasi masalah lingkungan. Variasi MBA yang ditambahkan diharapkan dapat meningkatkan kinerja kopolimer cangkok dan taut-silang selulosa-g-poliakrilamida sebagai fase diam dalam memisahkan xantorizol dari ekstrak kasar temu lawak. Produk juga dicirikan dengan menggunakan spektrofotometer inframerah transformasi Fourier (FTIR), analisis distribusi ukuran pori, dan mikroskop elektron pemayaran (SEM).
2
METODE
Alat dan Bahan
Alat yang digunakan pada penelitian ini adalah radas sintesis, motor
pengaduk, alat-alat kaca, shaker, mantel pemanas, kromatografi kolom, radas Kjeldahl, radas refluks, mesin penggiling, neraca analitik, spektrofotometer FTIR IRPrestige–21 Shimadzu, SEM Carl Zeiss EVO 50-50-87, NOVA-1000 American Quantachrome, polarimeter Kruss Optronic Germany, kromatografi cair kinerja tinggi (KCKT) LC-10AD VP Shimadzu, dan spektrofotometer resonans magnet inti (1H NMR) JEOL Delta ECA 500.
Bahan-bahan yang digunakan adalah isolat selulosa; akrilamida (AAm), amonium peroksidisulfat (APS), dan N,N-metilena-bis-akrilamida (MBA) p.a. (Merck); N2 (BOC); metanol, etanol, aseton, dan n-heksana p.a. (Smart); serta bahan kimia untuk analisis kadar nitrogen.
Preparasi Sampel dan Isolasi Selulosa Serabut Ampas Sagu
Ampas sagu yang digunakan berasal dari Tanah Baru, Bogor. Serabut ampas sagu diseleksi. Serabut yang masih dalam kondisi baik dikeringkan di bawah sinar matahari hingga kering, kemudian digiling hingga berukuran 40 mesh. Selulosa diisolasi dari serabut ampas sagu (modifikasi Sun et al. 2005; modifikasi SNI 3729-2008) dan diperoleh isolat selulosa. Bagan alir selengkapnya diberikan pada Lampiran 1.
Pencirian Selulosa
Pencirian selulosa meliputi penetapan kadar holoselulosa (ASTM 1104-56 1981), hemiselulosa, α-selulosa (ASTM 1103-60 1981), lignin (TAPPI T 13 m-451961), analisis gugus fungsi dari spektrum FTIR, dan analisis morfologi permukaan dari mikrograf SEM.
Sintesis Fase Diam Sintesis Selulosa-g-Poliakrilamida (Maesaroh 2013)
Sintesis g-poliakrilamida dilakukan dengan komposisi selulosa-AAm 75:25 dalam skala 30 g. Isolat selulosa dimasukkan ke dalam labu leher tiga sejumlah 22.5 g kemudian ditambahkan 150 mL akuades. Setelah itu, larutan dipanaskan hingga mencapai suhu 90 °C sambil diaduk dengan kecepatan 200 rpm. Apabila telah mencapai suhu 90 °C, gas nitrogen dialirkan ke dalam labu reaksi dan suhu dibiarkan konstan selama 30 menit. Setelah 30 menit, suhu diturunkan sampai kira-kira 60–65 °C. Ke dalam labu reaksi ditambahkan larutan APS (0.25 g APS dalam 12.5 mL akuades) dan suhu dijaga konstan pada 60–65 °C sampai 15 menit. Sejumlah 7.5 g AAm yang dilarutkan dalam 100 mL akuades selanjutnya ditambahkan. Setelah 5 menit, MBA dimasukkan ke dalam radas
3
dengan kecepatan 2–3 tetes/detik. Jumlah MBA divariasikan dari 1.0, 1.5, dan 2.0 g yang dilarutkan dalam 100 mL akuades. Setelah semua pereaksi dimasukkan, suhu pemanasan dinaikkan menjadi 70 °C dan dijaga konstan selama 3 jam hingga terbentuk gel kopolimer.
Pencucian Gel (Liang et al. 2009)
Gel selulosa-g-poliakrilamida hasil cangkok dan taut-silang yang telah didinginkan ditambahkan 150 mL metanol dan diaduk dengan kecepatan 200 rpm. Setelah 30 menit, gel ditambahkan 150 mL etanol dan diaduk cepat dengan kecepatan 300–400 rpm selama 5 menit, kemudian didiamkan selama 30 menit. Gel dan cairan alkohol dipisahkan, lalu gel dipotong kecil-kecil dan direfluks dengan 200 mL aseton pada suhu 70 °C selama 1 jam. Kemudian gel dipisahkan dari aseton, dikeringkan dalam oven bersuhu 60 °C hingga mencapai bobot konstan, dan dihaluskan dengan mesin penggiling.
Pencirian Fase Diam Selulosa-g-poliakrilamida
Kopolimer selulosa-g-poliakrilamida hasil sintesis dicirikan untuk mengetahui perubahan sifat fisik dan kimianya. Pencirian yang dilakukan meliputi analisis kadar nitrogen, uji kapasitas penyerapan air, penentuan gugus fungsi dari spektrum FTIR, analisis luas permukaan, volume pori, dan diameter pori dari analisis distribusi ukuran pori, serta morfologi permukaan menggunakan SEM.
Analisis Kadar N (Metode Kjeldahl)
Sejumlah 0.1 g sampel selulosa-g-poliakrilamida, 2 g selen, dan 10 mL H2SO4 pekat ditambahkan ke dalam labu Kjeldahl. Setelah itu, sampel didestruksi
dengan cara dipanaskan di atas pembakar bunsen sampai berwarna hijau bening kekuningan dan tidak ada lagi asap putih yang terbentuk, lalu didinginkan. Radas distilasi dirangkai dan sebagai penampung gas NH3 disiapkan 20 mL asam borat
2% yang ditambah indikator hijau bromkresol dan merah metil. Larutan hasil destruksi dipindahkan ke dalam labu kjeldahl 500 mL, dibilas dengan 150 mL akuades, lalu ditambahkan batu didih dan 50 mL NaOH 40%. Selanjutnya larutan didistilasi dengan cara dipanaskan di atas pembakar bunsen. Apabila distilasi selesai, distilat dititrasi dengan HCl 0.1 N hingga terbentuk warna merah. Kadar nitrogen dihitung menggunakan persamaan
Nitrogen (%) = (𝑉1− 𝑉0 ) × 𝑁 HCl × BE N 𝑊 × 100% Keterangan
W = bobot sampel (mg)
V1 = volume titrasi sampel (mL)
V0 = volume titrasi blangko (mL)
N HCl = normalitas HCl (N)
4
Nisbah serta efisiensi cangkok dan taut-silang (NP dan EP) ditentukan dari kadar nitrogen yang didapat. Berikut ini adalah persamaan yang digunakan (modifikasi Lanthong et al. 2006):
NP (%) = 100% [N(%) × (BM AAm/BA N)] 100% – [N(%) × (BM AAm/BA N)] EP (%) = % N percobaan
% N teoretis × 100%
Uji Kapasitas Penyerapan Air (Modifikasi Liu et al. 2007)
Sejumlah 0.1 g sampel selulosa-g-poliakrilamida dimasukkan ke dalam wadah bertutup yang berisi 200 mL akuades. Campuran didiamkan selama 24 jam pada suhu ruang. Setelah 24 jam, sampel yang telah mengembang disaring menggunakan saringan 400 mesh hingga tidak ada lagi air yang menetes. Kapasitas penyerapan air dihitung dengan menggunakan persamaan berikut:
Kapasitas penyerapan =𝑊1𝑊− 𝑊0
0 × 100%
Keterangan
W0 = Bobot polimer awal (g)
W1 = Bobot polimer akhir (g)
Analisis Spektrum FTIR
Sejumlah 0.005 g produk selulosa-g-poliakrilamida dicampur dengan 0.1 g KBr. Campuran digerus sampai halus dan homogen kemudian dipanaskan dalam oven 40 °C selama 24 jam. Campuran dianalisis dengan spektrofotometer FTIR IR Prestige-21 Shimadzu.
Analisis Distribusi Ukuran Pori
Sejumlah 2 g sampel dimasukkan ke dalam alat NOVA-1000 American Quantachrome. Analisis dilakukan dengan metode Brunauer-Emmett-Teller (BET) dan Barrett-Joyner-Halenda (BJH) di Pusat Teknologi Akselerator dan Proses Bahan, BATAN, Yogyakarta.
Analisis Morfologi Permukaan dari Fotograf SEM
Analisis morfologi permukaan dilakukan menggunakan SEM JEOL T330A di Pusat Penelitian Fisika, LIPI, Bandung. Sebelum dianalisis, sampel terlebih dahulu dilapisi dengan emas.
Kromatografi Kolom
Preparasi Ekstrak Temu Lawak (Modifikasi Segara 2011)
Serbuk kering rimpang temu lawak sejumlah 20 g ditambahkan ke dalam labu erlenmeyer 250 mL, kemudian direndam dengan 200 mL n-heksana p.a selama 3×24 jam sambil sesekali diaduk. Maserat dipisahkan dan dikumpulkan
6
Reaksi kopolimerisasi berlangsung melalui reaksi radikal bebas (Liu et al. 2007). APS digunakan sebagai inisiator dan MBA digunakan sebagai penaut-silang. Inisiator lain yang lazim digunakan pada reaksi kopolimerisasi cangkok ialah dibenzoil peroksida, azabisisobutironitril, atau bahan pengoksidasi seperti garam serium (Lanthong et al. 2006). Selama reaksi ini berlangsung, gas nitrogen terus dialirkan untuk mencegah adanya oksigen dan meminimumkan pembentukan radikal peroksida yang dapat menghambat reaksi kopolimerisasi.
Mekanisme reaksi kopolimerisasi cangkok dan taut-silang melalui 3 tahap, yaitu inisiasi, propagasi, dan terminasi (Lampiran 2). Pada tahap inisiasi, APS menyerang atom H pada gugus OH di posisi C6 dari selulosa. Selanjutnya, makroradikal tersebut akan berikatan dengan monomer AAm (Lampiran 2). Tahap propagasi sering disebut tahap pemanjangan rantai: makroradikal polimer tersebut terus berikatan dengan akrilamida lainnya. Pada tahap terminasi, di antara makroradikal yang telah mengalami pemanjangan satu sama lain ditaut-silangkan oleh MBA membentuk kopolimer selulosa-g-poliakrilamida. Data hasil sintesis dapat dilihat pada Lampiran 3.
Selulosa-g-poliakrilamida
Faktor yang dapat memengaruhi reaksi kopolimerisasi cangkok adalah rantai utama, monomer, pelarut, inisiator, zat tambahan, dan suhu (Bhattacharyaa dan Misra 2004). Reaksi kopolimerisasi ini menggunakan pelarut air. Menurut Bhattacharyaa dan Misra (2004), air adalah media yang tepat untuk pencangkokan.
Analisis kadar N digunakan untuk menentukan nilai NP dan EP dari sintesis selulosa-g-poliakrilamida yang telah dilakukan. NP menunjukkan persen pencangkokan AAm terhadap jumlah selulosa awal, sedangkan EP menunjukkan persentase jumlah monomer AAm yang tercangkok terhadap jumlah AAm yang ditambahkan di awal reaksi (Lanthong et al. 2006). Pada penelitian ini, nilai NP dan EP naik seiring dengan meningkatnya jumlah MBA yang ditambahkan (Lampiran 4). Hal tersebut terjadi karena MBA mengandung atom N pada gugus amida.
Hasil sintesis menunjukkan nilai NP berturut-turut 35.28, 38.27, dan 41.09%, serta nilai EP berturut-turut 92.89, 93.47, dan 93.51% untuk penambahan 1.0, 1.5, dan 2.0 g MBA. Nilai NP dan EP merupakan salah satu indikator keberhasilan sintesis selulosa-g-poliakrilamida. Gambar 1 menunjukkan bahwa nilai NP dan EP paling besar dihasilkan oleh sintesis dengan penambahan MBA sebanyak 2.0 g.
5
dalam satu labu bulat, kemudian dipekatkan dengan penguap putar pada suhu 40 °C hingga diperoleh ekstrak pekat.
Kromatografi Kolom
Kolom kromatografi diisi dengan 6–7 g produk fase diam hasil sintesis. Tinggi fase diam di dalam setiap kolom dibuat seragam (20 cm) dan ekstrak yang digunakan berjumlah 0.5 mL. Ekstrak dielusi dengan mengalirkan fase gerak sampai semua fraksi keluar dari kolom. Fraksi yang keluar dari kolom ditampung setiap 3 mL di dalam tabung gelap dan diuji dengan KCKT.
Analisis Fraksi dengan Hasil Pemisahan Terbaik
Fraksi terbaik yang diperoleh dari hasil analisis dengan menggunakan KCKT kemudian dianalisis strukturnya menggunakan 1H-NMR dan diukur rotasi spesifiknya menggunakan polarimeter.
Analisis 1H-NMR dilakukan menggunakan spektrofotometer JEOL Delta ECA 500 di Pusat Penelitian Kimia, LIPI, Serpong. Sebelum dianalisis, fraksi dilarutkan terlebih dahulu dalam CDCl3.
Untuk analisis rotasi spesifik, fraksi tersebut dilarutkan terlebih dahulu dalam 10 mL methanol, kemudian dimasukkan ke dalam tabung polarimeter dengan panjang 10 cm. Larutan dianalisis menggunakan polarimeter Kruss Optronic Germany.
HASIL DAN PEMBAHASAN
Kopolimer Cangkok dan Taut-Silang
Kopolimerisasi cangkok dan taut-silang dilakukan dengan cara mencangkokkan AAm pada tulang punggung selulosa yang selanjutnya akan ditaut-silangkan oleh MBA. Selulosa yang digunakan diisolasi dari serabut ampas sagu. Kemurnian selulosa dapat dilihat dari kadar α-selulosa yang dihasilkan (Tabel 1). Kadar α-selulosa dan lignin berturut-turut sebesar 78.61% dan 0.03% menandakan bahwa mutu dari isolat serabut ampas sagu cukup baik. Kadar α-selulosa dan kadar lignin tersebut dapat memengaruhi proses sintesis. Reaksi kopolimerisasi cangkok dan taut-silang akan mendapatkan produk yang baik jika isolat selulosa mengandung α-selulosa yang cukup tinggi dan kadar ligninnya rendah.
Tabel 1 Komponen kimia isolat selulosa serabut ampas sagu
Analisis Kadar (%)
Lignin 0.03
Holoselulosa 93.96
α-Selulosa 78.61
7
Gambar 1 Nilai NP dan EP hasil sintesis selulosa-g-poliakrilamida dengan berbagai bobot MBA
Selain dari kadar N, uji kapasitas penyerapan air pada selulosa-g-poliakrilamida juga perlu dilakukan karena dapat berpengaruh pada proses pemisahan. Nilai kapasitas penyerapan air hasil sintesis menurun seiring dengan meningkatnya jumlah MBA yang direaksikan (Gambar 2). Hal serupa juga terjadi pada NaAlg-g-PAA/SH, kapasitas penyerapan air menurun seiring dengan meningkatnya jumlah penaut-silang yang digunakan (Hua dan Wang 2009). Penaut-silang berfungsi menghubungkan kopolimer satu dengan kopolimer lainnya membentuk rongga 3 dimensi. Semakin tinggi konsentrasi penaut-silang, rongga tersebut akan semakin rapat sehingga kemampuan dalam menyerap air akan semakin menurun (Chauhan dan Lal 2003; Liu et al. 2007).
Hasil sintesis dengan penambahan 2.0 g MBA menunjukkan nilai kapasitas penyerapan air paling kecil jika dibandingkan dengan penambahan 1.0 dan 1.5 g MBA. Hal tersebut dapat mengindikasikan bahwa kopolimer yang dihasilkan dengan penambahan 2.0 g MBA baik untuk diaplikasikan sebagai fase diam karena jika kapasitas penyerapan air yang besar akan mengganggu proses pemisahan. Fase diam tersebut akan mengembang sehingga kinerjanya tidak optimal. Data nilai kapasitas penyerapan air selengkapnya dapat dilihat pada Lampiran 5.
Gambar 2 Nilai kapasitas penyerapan air hasil sintesis selulosa-g-poliakrilamida dengan berbagai bobot MBA
0 20 40 60 80 100
MBA 1.0 g MBA 1.5 g MBA 2.0 g 35.28 38.27 41.09
92.89 93.47 93.51
(%
)
Jumlah penaut silang
NP EP 0.000 2.000 4.000 6.000 8.000 MBA 1.0 g MBA 1.5 g MBA 2.0 g 6.83 6.15 5.57 k ap as it as p en ye rap an ai r (g/ g)
8
Ciri-ciri Selulosa-g-Poliakrilamida Spektrum FTIR
Spektrum FTIR selulosa-g-poliakrilamida menunjukkan adanya serapan baru pada daerah bilangan gelombang sekitar 1663 cm-1 (Lampiran 6). Menurut Lanthong et al. (2006), tambahan serapan di daerah 3400, 1650, dan 1600 cm-1 berturut-turut mengindikasikan ulur –N-H, ulur –C=O, dan tekuk –N-H yang merupakan penanda dari gugus amida yang berasal dari akrilamida. Serapan baru juga ditunjukkan pada daerah bilangan gelombang sekitar 1531 cm-1 karena adanya vibrasi tekuk –N-H.
Keberhasilan sintesis selulosa-g-poliakrilamida juga ditandai dengan adanya pergeseran bilangan gelombang 3000 cm-1 ke arah bilangan gelombang yang lebih kecil. Hal tersebut disebabkan oleh adanya serapan tumpang-tindih antara –O-H dan –N-H (Purwaningsih et al. 2012). Bilangan gelombang antara 3100 dan 3500 cm-1 merupakan daerah serapan untuk –O-H dan –N-H (Gambar 3). Selulosa-g-poliakrilamida hasil sintesis juga menunjukkan spektrum dengan serapan yang lebih tajam daripada isolat selulosa.
Gambar 3 Spektrum IR isolat selulosa ( ) dan selulosa-g-poliakrilamida dengan penaut-silang MBA sebanyak 1.0 g ( ), 1.5 g ( ), dan 2.0 g ( )
Distribusi Ukuran Pori
Ukuran pori yang diperoleh dari hasil analisis meliputi luas muka spesifik, volume pori total, dan jejari pori rerata (Tabel 2). Hasil analisis menunjukkan penurunan luas muka spesifik seiring dengan bertambahnya jumlah MBA. Luas muka spesifik paling besar ditunjukkan oleh hasil sintesis dengan penambahan 1.0 g MBA, yaitu 4.041 m2/g. Volume pori total dan jejari pori rerata terbesar ditunjukkan oleh hasil sintesis dengan penambahan 1.5 g MBA, yaitu berturut-turut 3.622 × 10-3 cm3/g dan 19.865 Å. Walaupun nilai luas muka spesifik, volume pori total, dan jejari pori rerata hasil sintesis dengan penambahan MBA sebesar 2.0 g bukan yang paling besar, namun perbedaan nilai dari masing-masing parameter tersebut tidak signifikan.
Jejari pori rerata dari semua hasil sintesis menunjukkan ukuran mesopori, karena diameter pori sebesar 2–50 nm (Bell dan Dietz 2009). Mesopori merupakan bentuk yang saat ini sedang dikembangkan. Menurut Jungbauer
9
(2005), mesopori baik digunakan untuk bioseparator. Monolit jenis mesopori juga akan memberikan pilihan fase diam untuk persiapan contoh dan aplikasi kromatografi (Wu et al. 2008). Luas muka spesifik yang dihasilkan berbeda nyata dengan silika gel komersial (Lampiran 7). Perbedaan luas muka spesifik yang terjadi dapat disebabkan oleh perbedaan ukuran partikel antara silika gel komersial dan hasil sintesis.
Tabel 2 Hasil analisis ukuran pori Sampel
Hasil uji Luas muka spesifik
(m2/g)
Volume pori total (cm3/g)
Jari-jari pori rerata (Å)
MBA 1.0 g 4.041 3.108 × 10-3 15.384
MBA 1.5 g 3.647 3.622 × 10-3 19.865
MBA 2.0 g 3.507 3.255 × 10-3 18.627
Mikrograf SEM
Gambar 4–7 memperlihatkan mikrograf isolat selulosa dan selulosa-g-poliakrilamida. Morfologi permukaan pada isolat selulosa (Gambar 4) berbentuk fibril. Bentuk yang serupa juga teramati pada selulosa yang berasal dari permukaan bahan katun, dengan perbesaran 100× (Zhao et al. 2007).
Keberhasilan sintesis juga dapat ditunjukkan dengan cara membandingkan morfologi permukaan isolat selulosa dengan selulosa-g-poliakrilamida. Kopolimer hasil sintesis sudah tidak berbentuk fibril lagi seperti pada selulosa, tetapi berbentuk monolit mesopori.
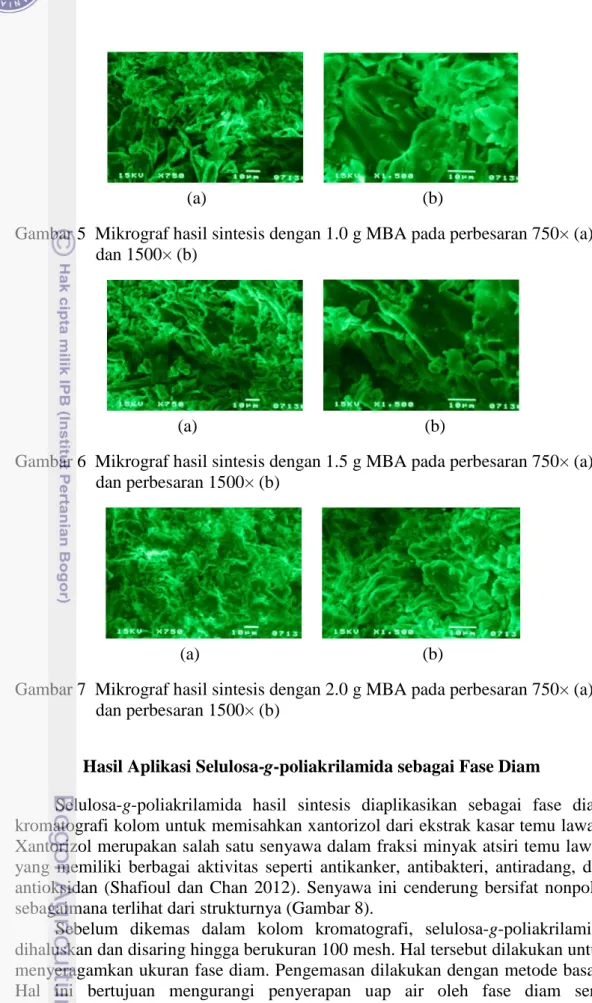
Perbedaan jumlah MBA yang ditambahkan juga menghasilkan perbedaan morfologi permukaan hasil sintesis. Pada penambahan 2.0 g MBA (Gambar 7), permukaan yang dihasilkan lebih rapat dibandingkan dengan penambahan MBA sejumlah 1.0 g (Gambar 5) dan 1.5 g (Gambar 6). Hal ini sesuai dengan nilai kapasitas penyerapan air yang paling rendah pada penambahan MBA sejumlah 2.0 g.
(a) (b)
Gambar 4 Mikrograf isolat selulosa dengan perbesaran 750× (a) dan 1500× (b)
10
(a) (b)
Gambar 5 Mikrograf hasil sintesis dengan 1.0 g MBA pada perbesaran 750× (a) dan 1500× (b)
(a) (b)
Gambar 6 Mikrograf hasil sintesis dengan 1.5 g MBA pada perbesaran 750× (a) dan perbesaran 1500× (b)
(a) (b)
Gambar 7 Mikrograf hasil sintesis dengan 2.0 g MBA pada perbesaran 750× (a) dan perbesaran 1500× (b)
Hasil Aplikasi Selulosa-g-poliakrilamida sebagai Fase Diam
Selulosa-g-poliakrilamida hasil sintesis diaplikasikan sebagai fase diam kromatografi kolom untuk memisahkan xantorizol dari ekstrak kasar temu lawak. Xantorizol merupakan salah satu senyawa dalam fraksi minyak atsiri temu lawak yang memiliki berbagai aktivitas seperti antikanker, antibakteri, antiradang, dan antioksidan (Shafioul dan Chan 2012). Senyawa ini cenderung bersifat nonpolar sebagaimana terlihat dari strukturnya (Gambar 8).
Sebelum dikemas dalam kolom kromatografi, selulosa-g-poliakrilamida dihaluskan dan disaring hingga berukuran 100 mesh. Hal tersebut dilakukan untuk menyeragamkan ukuran fase diam. Pengemasan dilakukan dengan metode basah. Hal ini bertujuan mengurangi penyerapan uap air oleh fase diam serta meminimumkan terbentuknya gelembung dalam kolom. Fase diam terlebih
11
dahulu dialiri dengan metanol dan n-heksana untuk mengeluarkan kotoran yang dapat mengganggu proses pemisahan.
Pemisahan campuran xantorizol dilakukan dengan menggunakan selulosa-g-poliakrilamida hasil sintesis yang bersifat polar sebagai fase diam dan n-heksana yang bersifat nonpolar sebagai fase gerak. Metode ini paling umum digunakan untuk pemisahan senyawa yang relatif nonpolar dengan kromatografi kolom, dengan menyerupai pemisahan dengan fase diam silika gel yang polar dan pelarut dari nonpolar ke polar. Selulosa-g-poliakrilamida, seperti halnya silika gel juga bersifat cenderung polar karena adanya gugus –N-H yang berasal dari akrilamida dan MBA serta gugus –OH dari selulosa. Pelarut n-heksana, n-pentana, dan sikloheksana telah dilaporkan tidak mengalami interaksi dengan fase diam hasil sintesis ini berdasarkan pengukuran indeks bias pelarut sebelum dan sesudah digunakan untuk elusi (Maesaroh 2013).
Analisis KCKT
Fraksi-fraksi hasil pemisahan dengan kromatografi kolom ditampung setiap 3 mL kemudian dianalisis dengan KCKT. Analisis KCKT ini menggunakan kolom C18 dengan fase gerak asetonitril dan asam fosfat. Metode kromatografi fase terbalik seperti ini, yaitu fase gerak yang digunakan lebih polar dibandingkan dengan fase diamnya lazim digunakan pada KCKT. Detektor ultraviolet-tampak (UV-Vis) dengan panjang gelombang 210–366 nm digunakan karena senyawa yang ingin diidentifikasi, yaitu xantorizol memiliki λmaks sekitar 220 nm yang
berada dalam daerah UV dekat (200–380 nm) (Creswell et al. 2005).
Kromatogram yang berbeda ditunjukkan oleh hasil sintesis dengan penambahan MBA sebesar 1.0, 1.5, dan 2.0 g (Lampiran 8). Menggunakan fase diam hasil sintesis dengan penambahan 1.0 g MBA, puncak-puncak hasil pemisahan ekstrak kasar temu lawak baru terlihat pada fraksi 2. Pada fraksi ke-4, puncak xantorizol sudah mulai terpisah dari puncak lainnya dan terpisah secara optimum pada fraksi ke-5 dengan nilai resolusi 1.750 dan selektivitas 1.209. Pemisahan yang lebih cepat teramati menggunakan fase diam hasil sintesis dengan penambahan 1.5 dan 2.0 g MBA. Puncak-puncak hasil pemisahan ekstrak kasar temu lawak sudah terlihat pada fraksi ke-1. Puncak xantorizol mulai terpisah pada fraksi ke-2 untuk hasil sintesis dengan penambahan 2.0 g MBA, sedangkan pada hasil sintesis dengan penambahan 1.5 g MBA, puncak tersebut baru terpisah pada fraksi ke-3. Hasil sintesis dengan penambahan 1.5 maupun 2.0 g MBA menunjukkan puncak xantorizol yang terpisah secara optimum pada fraksi ke-3, dengan nilai resolusi berturut-turut sebesar 1.577 dan 1.870 dan selektivitas berturut-turut sebesar 1.243 dan 1.276.
Hasil analisis KCKT menunjukkan bahwa pemisahan terbaik diperoleh dari selulosa-g-poliakrilamida hasil sintesis dengan penambahan 2.0 g MBA. Pemilihan ini berdasarkan nilai resolusi dan selektivitas yang paling besar. Nilai resolusi menunjukkan keterpisahan atau jarak antarpuncak. Nilai resolusi dikatakan baik apabila >1.5, sedangkan kolom dikatakan selektif jika selektivitasnya >1 (Gritter et al. 1991).
Analisis NMR dan Rotasi Spesifik
Analisis NMR dilakukan pada fraksi 3 hasil pemisahan dengan selulosa-g-poliakrilamida terbaik untuk membuktikan bahwa senyawa yang dipisahkan
12
merupakan (–)-xanthorrhizol berkonfigurasi relatif R* (Gambar 8) serta untuk membuktikan bahwa fase diam dapat memisahkan xantorizol tanpa mengubah strukturnya.
Analisis spektrum 1H-NMR (Lampiran 9) memperlihatkan sinyal-sinyal sebagai berikut: δH 1.66 menunjukkan 3 proton pada C13, sinyal δH 1.53
menunjukkan 3 proton pada C12. Kedua nilai geseran kimia ini mungkin dipertukarkan karena posisinya yang identik dalam struktur. Sinyal δH 5.08
menunjukkan 1 proton pada C10dengan nilai tetapan kopling (J) 6.8 Hz. Sinyal δH 1.87 menunjukkan 2 proton pada C9, sinyal δH 1.56 menunjukkan 2 proton
pada C8. Geseran kimia pada C9lebih besar dibandingkan dengan C8karena C9 lebih dekat dengan ikatan rangkap, sehingga mengalami efek anisotropi. Sinyal δH
2.61 menunjukkan 1 proton pada C7. Sinyal δH 1.20 menunjukkan 3 proton pada
C16 dengan nilai J 7.1 Hz. Hal yang mendekati juga diungkapkan oleh Hong dan Sirat (2004) yang menyatakan bahwa nilai J pada posisi C16 berturut-turut sebesar 6.8 dan 6.9 Hz. Oleh karena itu, konfigurasi relatif gugus metil C16 pada C7 adalah R*. Sinyal δH 6.67 menunjukkan 1 proton pada C6dengan nilai J 1.6
akibat kopling meta dengan C2, dan 7.6 akibat kopling orto dengan C5. Sinyal δH
7.8 menunjukkan 1 proton pada C5 dengan nilai J 7.8 Hz. Sinyal δH 2.21
menunjukkan 3 proton pada C14, sinyal δH 4.60 menunjukkan proton pada gugus
hidroksil, sinyal δH 6.61 menunjukkan 1 proton pada C2. Nilai perbedaan δH
antara isolat xantorizol dalam fraksi dengan literatur sebesar –0.09 hingga –0.02. Hasil analisis 1H-NMR ini menunjukkan bahwa fraksi murni yang terpisahkan oleh fase diam hasil sintesis merupakan (–)-xantorizol berkonfigurasi relatif R*.
1 2 3 4 5 6 7 8 9 10 11 12 13 14 16 OH 15 R*
Gambar 8 Struktur R*-(‒)-xantorizol (Hwang et al. 2000)
Selain analisis struktur menggunakan NMR, nilai rotasi spesifik juga ditentukan untuk membuktikan bahwa senyawa yang dipisahkan adalah xantorizol alami tanpa menimbulkan epimerisasi. Menurut Mayers dan Diana (1997) serta Pyo et al. (2013), xantorizol memiliki 1 pusat kiral, sehingga memiliki isomer R-(‒) dan S-(+). R-(‒)-xantorizol merupakan seskuiterpena alami yang banyak terdapat pada temu lawak. Hasil analisis nilai [∝]𝐷27yang diperoleh sebesar –55.6° (Lampiran 10), tidak berbeda jauh dengan nilai [∝]𝐷 yang dinyatakan oleh Hong dan Sirat (2004) serta Hwang et al. (2000), yaitu berturut-turut sebesar –49.4° dan –50.2°. Nilai [∝]𝐷 S-(+)-xantorizol adalah +52.8° (Mayers dan Diana 1997). Berdasarkan hasil ini, fase diam dapat digunakan untuk memisahkan tanpa mengubah struktur R-(‒)-xanthorrhizol.
13
SIMPULAN DAN SARAN
Simpulan
Selulosa-g-poliakrilamida hasil kopolimerisasi cangkok dan taut-silang telah berhasil digunakan sebagai fase diam untuk memisahkan R-(‒)-xantorizol tanpa mengubah struktur tiga dimensinya. Hal ini sesuai dengan nilai NP dan EP yang tinggi serta nilai kapasitas penyerapan air yang rendah. Spektrum FTIR, distribusi ukuran pori, dan morfologi permukaan dengan SEM juga mendukung bahwa hasil sintesis ini dapat digunakan sebagai fase diam. Variasi penambahan jumlah silang berpengaruh pada kinerja fase diam. Penambahan jumlah peanut-silang sebesar 2.0 g menunjukkan hasil terbaik pada pemisahan xantorizol dengan nilai resolusi 1.870 dan nilai selektivitas 1.276 yang ditunjang dengan analisis 1 H-NMR dan rotasi spesifik.
Saran
Perlu dilakukan aplikasi fase diam dengan menggunakan senyawa lain untuk mengetahui ketahanan dan kinerjanya pada pemisahan senyawa berdasarkan kiralitasnya.
DAFTAR PUSTAKA
[ASTM] American Society for Testing and Materials. 1981. Annual Book of
ASTM Standards. Wood: Adhesives 22. Philadelphia (US): ASTM.
[BPS] Badan Pusat Statistik. 2012. Data Ekspor Impor. [internet]. [diunduh 2012 April 20]. Tersedia pada: www.bps.go.id.
[BSN] Badan Standardisasi Nasional. 2008. Tepung Sagu. SNI 3729:2008. Jakarta (ID): BSN.
Baggiani C, Patrizia B, Cristina G, Laura A, Cinzia P, Gianfranco G. 2011. Binding behaviour of molecularly imprinted polymers prepared by a hierarchical approach in mesoporous silica beads of varying porosity. J
Chromatogr. 1218:1828-1834. doi:10.1016/j.chroma.2011.02.003.
Bell W, Dietz S, penemu; TDA Research’ Inc. 2001 Okt 2. Mesoporous carbons and polymers. US Patent US 6,297,293 B1.
Bhattacharya A, Misra BN. 2004. Grafting: a versatile means to modify polymers techniques, factors and applications. Prog Polym Sci. 29:767-814.
Chauhan GS, Lal L. 2003. Novel grafted cellulose-based hydrogels for water technologies. Desalination. 159:131-138.
Chen X, Chiyo Y, Yoshio O. 2007. Polysaccharide derivatives as useful chiral stationary phases in high-performance liquid chromatography. Pure Appl
Chem. 79(9):1561-1573. doi:10.1351/pac200779091561.
Creswell CJ, Runquist OA, Campbell MM. 2005. Analisis Spektrum Senyawa
14
dari: Spectrum Analysis of Organic Compound. An Introductory
Programmed Text.
Gritter RJ, Bobbitt JM, Schwarting AE. 1991. Pengantar Kromatografi. Padmawinata K, penerjemah. Bandung: Penerbit ITB. Terjemahan dari:
Introduction to Chromatography.
Hong NM, Sirat H. 2004. Synthesis of several bisabolanesesquiterpenoids from xanthorrhizol isolated from C. xanthorrhiza and their bioactivities. Di dalam: The 4th Annual Seminar of National Science Fellowship; 2004; Johor Bahru, Malaysia. Johor Bahru (MY): Universiti Teknologi Malaysia. hlm 181-186.
Hua S, Wang A. 2009. Synthesis, characterization and swelling behaviors of sodium alginate-g-poly(acrylic acid)/sodium humate superabsorbent.
Carbohydr Polym. 75:79-84. doi:10.1016/j.carbpol.2008.06.013.
Hwang JK, Shim JS, Baek NI, Pyun YR. 2000. Xanthorrhizol: a potential antibacterial agent from Curcuma xanthorrhiza against Streptococcus
mutans. Planta Med. 66:196-197.
Israel AU, Obot IB, Umoren SA, Mkpenie V, Asuquo JB. 2008. Production of cellulosic polymers from agricultural wastes. E-J Chem. 5(1):81-85.
Jong FS, Widjono A. 2007. Sagu: potensi besar pertanian indonesia. Iptek
Tanaman Pangan. 2(1):54-65.
Jungbauer A. 2005. Chromatographic media for bioseparation. J Chromatogr. 1035:3-12. doi: 10.1016/j.chroma.2004.08.162.
Kumaran S, Sastry CA, Vickineswary S. 1997. Laccase, cellulose and xylanase activities during growth of Pleurotus sajor-caju on sago hampas. World J
Microbiol Biotech. 13:43-49.
Kumoro AC, Ngoh GC, Hasan M, Ong CH, Teoh EC. 2008. Conversion of fibrous sago (Metroxylon sagu) waste into fermentable sugar via acid and enzymatic hydrolysis. Asian J Scientific Res. 1(4):412-420.
Lanthong P, Nuisin R, Kiatkamjornwong S. 2006. Graft copolymerization, characterization, and degradation of cassava starch-g-acrylamide/itaconic acid superabsorbents. Carbohydr Polym. 66:229-245. doi: 10.1016/j.carbpol.2006.03.006.
Liang R, Yuan H, Xi G, Zhou Q. 2009. Synthesis of wheat straw-g-poly (acrylic acid) superabsorbent composites and release of urea from it. Carbohydr
Polym. 77:181-187. doi:10.1016/j.carbpol.2008.12.018.
Lin C, Zhan H, Liu M, Fu S, Zhang J. 2009. Preparation of cellulose graft poly(methyl methacrylate) copolymers by atom transfer radical polymerization in an ionic liquid. Carbohydr Polym. 78:432-438. doi:10.1016/j.carbpol.2009.04.032.
Liu J, Wang Q, Wang A. 2007. Synthesis and characterization of chitosan-g-poly(acrylic acid)/sodium humate superabsorbent. Carbohydr Polym. 70:166-173. doi:10.1016/j.carbpol.2007.03.015.
Maesaroh M. 2013. Modifikasi sintesis dan pencirian fase diam kromatografi kolom selulosa berbasis serabut ampas sagu [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Mayers AI, Diana S. 1997. Short asymmetric synthesis of (+)-α-curcumene and (+)-xanthorrhizol. J Org Chem. 62:5219-5221.
15
Purwaningsih H, Irawadi TT, Mas’ud ZA, Fauzi AM. 2012. Rekayasa biopolimer jerami dengan teknik kopolimerisasi cangkok dan taut silang. Valensi. 2(4):489-500.
Pyo JI, Kim RW, Azam SMS, Song C, Cheong CS, Kim KS. 2013. Two-step biocatalytic resolution of rac-primary alcohol for obtaining each isomeric intermediate of xanthorrhizol. Bull Korean Chem Soc. 34(1):252-254. Segara B. 2011. Modifikasi kopolimerisasi cangkok taut silang selulosa ampas
sagu sebagai media pemisahan xantorizol [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Setyorini A. 2011. Sintesis dan aplikasi selulosa-g-poliakrilamida sebagai fase diam kromatografi kolom dari serabut ampas sagu [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Shafioul ASM, Chan SC. 2012. Lipase catalyzed kinetic resolution of rac-2-(3-methoxy-4-methylphenyl) propan-1-ol and
rac-2-(3-hydroxy-4-methylphenyl)propyl propanoate for S-(+)-xanthorrhizol. Bull Korean Chem
Soc. 33(2):409-414.
Sun JX, Xu F, Sun XF, Xiao B, Sun RC. 2005. Physico-chemical and thermal characterization of cellulose from barley straw. Polym Degrad & Stability. 88:521-531.
[TAPPI] Technical Association of The Pulp and Paper Industry. 1961. TAPPI
Standards and Suggested Methods. New York (US): TAPPI.
Vickineswary S, Shim YL, Thambirajah JJ, Blakebrough N. 1994. Possible microbial utilization of sago processing wastes. Resource Conserv Recycl. 11:289-296.
Wu R, Lianghai H, Fangjun W, Mingliang Y, Hanfa Z. 2008. Recent development of monolithic stationary phases with emphasis on microscale chromatographic separation. J Chromatogr. 1184:369-392. doi:10. 1016/j.chroma.2007.09.022.
Zhao H, Ja HK, Conrad Z, Heather MB, Bruce WA, Johnathan EH. 2007. Studying cellulose fiber structure by SEM, XRD, NMR and acid hydrolysis.
17
Lampiran 1 Bagan alir penelitian
Kopolimerisasi pencangkokan dan penatautan-silang
Isolat selulosa serabut ampas
sagu Pengujian kadar lignin,
α-selulosa, hemiselulosa, dan holoselulosa Pencirian dengan FTIR dan SEM Polimer selulosa-g-poliakrilamida Pengujian kadar nitrogen (metode Kjeldahl) dan kapasitas
penyerapan air
Aplikasi kromatografi kolom dan analisis
dengan KCKT
Pencirian dengan FTIR
dan SEM
Analisis 1H NMR dan rotasi spesifik dari
senyawa yang dipisahkan
17
Lampiran 2 Reaksi kopolimerisasi Inisiasi NH4 O S O O O O CH2 OH H O H OH OH H H O CH2 O O H O H OH OH H H O NH4 O S O O OH H H APS selulosa O CH2 O H O H OH OH H H O H2C CH NH2 O O H2C H O H OH H H O CH2 HC NH2 O O H H akrilamida Propagasi O H2C H O H OH OH H H O H2C HC NH2 O O H2C CH NH2 O O H2C H O H OH OH H H O H2C C NH2 O O H2C HC NH2 O H H H2C CH NH2 O O H2C H O H OH OH H H O CH2 HC NH2 O O H2C HC NH2 O CH2 HC NH2 O n O H2C H O H OH OH H H O H2C C NH2 O O H2C HC NH2 O H H n
18 lanjutan Lampiran 2 Terminasi O CH2 H O H OH OH H H O H2C HC NH2 O O CH2 HC NH2 O H2C HC NH2 O n O CH2 H O H OH OH H H O H2C HC NH2 O O CH2 HC NH2 O H2C H2C NH2 O n O H2C H O H OH OH H H O O H H H O H2C H O H OH OH H H OH O H O H2C H O H OH OH H H O CH2 HC NH2 O O H2C HC NH2 O CH2 HC NH2 O n O H2C H O H OH OH H H O CH2 HC NH2 O O H2C HC NH2 O CH2 HC NH2 O n O CH2 H O H OH OH H H O O H H H O CH2 H O H OH OH H H HO O H H2C C H C N H H2 C N H C C H CH2 O O MBA
19 lanjutan Lampiran 2 O H2C H O H OH HO H H O H2C CH H2N O O O H2C H O H OH HO H H O O H O CH2 H O H OH OH H H O O O H2C H O H OH HO H H O H2C CH H2N O O H H 2 C C H 2 C N H H 2 C N H C C H 2 H 2 C O O H 2 C C H 2 C N H H 2 C N H C C H 2 H 2 C O O n n O H2C H O H OH HO H H O H2C CH H2N O O O CH2 H O H OH HO H H O O H O H2C H O H OH OH H H O O O H2C H O H OH HO H H O H2C CH H2N O O H n n O H2C H O H OH HO H H O H2C CH H2N O O H H 2 C C H 2 C N H H 2 C N H C C H 2 H 2 C O O n O H2C H O H OH HO H H O H2C CH H2N O O H n O H2C H O H OH HO H H O O O CH2 H O H OH HO H H O O H H H H
Lampiran 3 Hasil pembuatan kopolimer selulosa-g-poliakrilamida MBA (g) Ulangan Selulosa (g) AAm (g) MBA (g) APS (g) Polimer (g) 1.00 1 22.5003 7.5000 1.0001 0.2500 27.7499 2 22.5003 7.5000 1.0003 0.2501 29.7640 1.50 1 22.5000 7.5004 1.5004 0.2501 30.5107 2 22.5000 7.5006 1.5003 0.2500 29.3922 2.00 1 22.5007 7.5005 2.0000 0.2503 30.4650 2 22.5007 7.5000 2.0002 0.2500 30.0046
20
Lampiran 4 Analisis kadar N kopolimer selulosa-g-poliakrilamida MBA (g) Ulangan Bobot sampel (mg) Volume HCl (mL) N Teori (%) N Percobaan (%) NP (%) EP (%) 1.00 1 100.0 3.70 5.54 5.16 35.45 93.23 2 101.3 3.72 5.54 5.12 35.10 92.54 Rerata 5.14 35.28 92.89 1.50 1 100.1 3.95 5.84 5.51 38.77 94.35 2 100.7 3.90 5.84 5.41 37.77 92.58 Rerata 5.46 38.27 93.47 2.00 1 101.6 4.17 6.14 5.71 40.77 92.99 2 100.0 4.15 6.14 5.77 41.41 94.02 Rerata 5.74 41.09 93.51 Contoh perhitungan
• Kadar nitrogen percobaan N (%) = (V1 – V2) × NHCl × BEN
W × 100%
= (3.70 –0.05 ) mL ×0.1010mek mL� ×14 mg/mek
100.00 mg × 100% = 5.16%
• Kadar nitrogen teoretis (modifikasi Lanthong et al. 2006) N (%) = N AAm (%) + N MBA (%)
= ( W AAm × BA N
W total sampel × BM AAm× 100%) + (2 ×
W MBA × BA N
W total sampel × BM MBA× 100%)
=�7.5002 g × 14 g mol 27.7499 g × 71molg ×100%� +(2× 1.0001g × 14 g/mol 27.7499 g × 154 g/mol×100%)= 55.4 = 5.54% • Nisbah pencangkokan-penautan-silang (NP) NP = 100% [N (%) × (BM AAm/BA N)] 100% – [N (%) × (BM AAm/BA N)] = 100% [5.16% × (71 g/mol/14 g/mol)] 100% – [5.16% × (71 g/mol/14 g/mol)]= 35.45% • Efisiensi pencangkokan-penautan-silang (EP)
EP = % N percobaan
% N teoretis × 100%
= 4.96 %
21
Lampiran 5 Hasil perhitungan kapasitas penyerapan air MBA (g) Ulangan Bobot polimer awal (g) Bobot polimer mengembang (g) Penyerapan air Rerata 1.00 1 0.1000 0.7985 6.9850 6.8310 2 0.1000 0.7677 6.6770 1.50 1 0.1002 0.7323 6.2866 6.1538 2 0.1005 0.7035 6.0210 2.00 1 0.1001 0.6545 5.5450 5.5662 2 0.1000 0.6594 5.5874 Contoh perhitungan
Kapasitas penyerapan air = Bobot polimer akhir – Bobot polimer awal Bobot polimer awal
= 0.7985 – 0.1000
0.1000 = 6.9850 g/g
Lampiran 6 Pencirian pita FTIR
Selulosa Selulosa-g-poliakrilamida
Bilangan gelombang (cm-1) Gugus fungsi Bilangan gelombang (cm-1) Gugus fungsi
3306 Ulur O-H 3487 Ulur N-H
2893 Ulur C-H 3198 Ulur O-H
1420 Ulur C-O-C 2901 Ulur C-H
1531 Tekuk N-H
1420 Ulur C-O-C
895 Ikatan β
Lampiran 7 Hasil analisis distribusi ukuran pori silika gel komersial
Sampel Luas muka
spesifik (m2/g)
Volume pori total (cm3/g)
Diameter pori rerata (Å)
Fluka cat. num. 95021 300 0.85 100
Fluka cat. num. 86981 210 0.80 200
Fluka cat. num. 89752 100 0.80 300
Baggiani et al. (2011) Keterangan:
22
Lampiran 8 Hasil analisis KCKT
MBA (g) Waktu retensi (tm) Waktu retensi (tr1) Waktu retensi (tr2) Fraksi Selektivitas (α) Resolusi 1.0 2.184 4.037 5.164 1 1.608 1.504 2.475 4.522 5.074 2 1.270 0.930 0.814 4.533 5.059 3 1.141 0.864 1.961 4.518 5.151 4 1.248 1.725 1.492 4.532 5.168 5 1.209 1.750 0.797 4.045 5.158 6 1.343 0.945 0.798 4.492 5.165 7 1.182 0.263 1.5 1.958 4.429 4.997 1 1.230 1.048 2.473 4.554 5.068 2 1.247 0.593 1.965 4.532 5.156 3 1.243 1.577 0.805 4.046 5.143 4 1.338 0.922 1.960 4.496 5.139 5 1.253 1.561 1.467 4.507 5.146 6 1.210 1.585 1.792 4.516 5.152 7 1.102 1.582 2.0 0.795 4.459 5.021 1 1.153 0.953 1.019 4.442 5.105 2 1.194 2.181 2.282 4.609 5.251 3 1.276 1.870 1.956 4.549 5.151 4 1.232 0.949 1.955 4.582 5.174 5 1.225 1.552 1.464 3.779 5.159 6 1.596 2.366
Contoh perhitungan selektivitas (α) α =𝑘𝑘2 1 = 𝑡𝑟2− 𝑡𝑚 𝑡𝑟1− 𝑡𝑚 Keterangan α = selektivitas
k2 = koefisien partisi senyawa 2
k1 = koefisien partisi senyawa 1
tr2 = waktu retensi senyawa 2
tr1 = waktu retensi senyawa 1
tm = waktu retensi yang tidak tertahan (fase gerak)
25
lanjutan Lampiran 8
Kromatogram hasil sintesis dengan penambahan 1.0 g MBA
fraksi 1 fraksi 2
fraksi 3 fraksi 4
25 lanjutan Lampiran 8 fraksi 5 fraksi 6 fraksi 7 24
25
lanjutan Lampiran 8
Kromatogram hasil sintesis dengan penambahan 1.5 g MBA
fraksi 1 fraksi 2
28 lanjutan Lampiran 8 fraksi 5 fraksi 6 Fraksi 7 26
29
lanjutan Lampiran 8
Kromatogram hasil sintesis dengan penambahan 2.0 g MBA
fraksi 1 fraksi 2
Fraksi 3 fraksi 4
29
lanjutan Lampiran 8
Kromatogram hasil sintesis dengan penambahan MBA 2.0 g
fraksi 5 fraksi 6
29
Lampiran 9 Hasil analisis 1H-NMR
32 lanjutan Lampiran 9 No Gugus awal Multiplisitas δ (ppm) Tetapan kopling (Hz) *δ (ppm) *Tetapan kopling (Hz) Selisih nilai δ (ppm) 1 -C- - - - 2 -CH doblet 6.61 1.9 6.63 1.8 -0.02 3 -C- - - - 4 -C- - - - 5 -CH doblet 7.02 7.8 7.05 7.8 -0.03
6 -CH doblet,doblet 6.67 1.6 dan 7.6 6.70 1.8 dan 7.8 -0.03
7 -CH- sekstet 2.61 - 2.63 - -0.02 8 -CH2- multiplet 1.56 - 1.62 - -0.06 9 -CH2- multiplet 1.87 - 1.89 - -0.02 10 -CH=C- triplet 5.08 6.8 5.11 4.6 -0.03 11 =C- - - - 12 -CH3 singlet 1.53 - 1.55 - -0.02 13 -CH3 singlet 1.66 - 1.69 - -0.03 14 -CH3 singlet 2.21 - 2.24 - -0.03 15 -OH singlet 4.60 - 4.69 - -0.09 16 -CH3 doblet 1.20 7.1 1.22 6.9 -0.02
*Hong dan Sirat (2004)
Selisih nilai tertinggi = -0.02 ppm Selisih nilai terendah = -0.09 ppm
Lampiran 10 Hasil penentuan nilai rotasi spesifik (R)*-xantorizol Perhitungan rotasi spesifik
[∝]𝐷27= 𝑙 × 𝑐 =∝ −0.20
1 dm × 0.03610g mL= −55.600 Keterangan
[∝]𝐷27= rotasi spesifik
∝ = sudut rotasi yang terbaca 𝑙 = panjang tabung (dm) 𝑐 = konsentrasi (mL)g 30
31
RIWAYAT HIDUP
Penulis dilahirkan di Ciamis pada tanggal 1 Juni 1991 dari Bapak Akim Saputra dan Ibu Ponirah. Penulis merupakan putri pertama dari 2 bersaudara. Tahun 2009 penulis lulus dari SMA Negeri 1 Babelan dan pada tahun yang sama penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB dan diterima di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis menjadi asisten praktikum Kimia Dasar pada tahun ajaran 2012/2013. Penulis juga pernah menjadi staf Departemen Komunikasi dan Informasi, Koperasi Mahasiswa Institut Pertanian Bogor. Bulan Juli−September 2012 penulis melaksanakan praktik lapangan di PT Bridgestone Tire Indonesia, Bekasi dengan judul Analisis Perubahan Kualitas Air pada WTP PT Bridgestone.