EKOLOGI TERNATE
EDITOR
Ibnu Maryanto
Hari Sutrisno
PUSAT PENELITIAN BIOLOGI-LIPI
2011
© 2011 Lembaga Ilmu Pengetahuan Indonesia (LIPI) Pusat Penelitian Biologi*
Katalog dalam Terbitan
Ekologi Ternate/Ibnu Maryanto dan Hari Sutrisno (Editor). – Jakarta: LIPI Press, 2011.
xiii + 371 hlm.; 14,8 x 21 cm
ISBN 978-979-799-609-3
1. Ekologi 2. Ternate
577
Editor Bahasa : Risma Wahyu Hartiningsih Penata Letak : Ibnu Maryanto
Penata Sampul : Fahmi Penerbit : LIPI Press
*Pusat Penelitian Biologi-LIPI
Gedung Widyasatwaloka, Cibinong Science Center Jln. Raya Bogor Km. 46, Cibinong 169111
Telp.: 021-8765056, 8765057
DAFTAR ISI
Ucapan Terimakasih iii
Kata Sambutan v
Kata Pengantar vii
DAFTAR ISI xi
GEOLOGI DAN IKLIM
Gunung Gamalama, Ternate, Maluku Utara: Dinamika Erupsi dan Potensi
Ancaman Bahayanya 1
Indyo Pratomo, Cecep Sulaeman, Estu Kriswati & Yasa Suparman Karakteristik Erupsi G Kie Besi dan Potensi Ancaman Bencananya Terhadap Lingkungan Kota Ternate: (Representasi dari karakter
gunungapi aktif di Busur Gunungapi Halmahera) 15
Estu Kriswati & Indyo Pratomo
Analisa Anomali Curah Hujan dan Parameter Laut-Atmosfer Periode
Januari - Agustus 2010 di Provinsi Maluku Utara 27
Dodo Gunawan FAUNA
Kelimpahan dan Keragaman Kelelawar (Chiroptera) dan Mamalia Kecil
di Pulau Ternate 43
Sigit Wiantoro & Anang S Achmadi
Keanekaragaman Mamalia Kecil di Pulau Moti 55
Anang Setiawan Achmadi & Sigit Wiantoro
Kajian Ekologi Burung di Hutan Gunung Gamalama, Ternate, Maluku
Utara 69 Wahyu Widodo
Komunitas Burung Pulau Moti Ternate Maluku Utara 83
Eko Sulistyadi
Keanekaragaman Herpetofauna di Pulau Ternate dan Moti, Maluku Utara 105 Mumpuni
Komunitas Keong Darat di Pulau Moti, Maluku Utara 121 Heryanto
Kajian keanekaragaman Ngengat (Insekta: Lepidoptera) di Gunung
Gamalama, Ternate 133
Hari Sutrisno
Tinjauan Keanekaragaman dan Sebaran Kupu Ternate 145
Djunijanti Peggie
Efektifitas Trap Warna Terhadap Keberadaan Serangga Pada Pertanaman
Budidaya Cabai di Kelurahan Sulamadaha Kecamatan P Ternate Ternate 159 Abdu Mas’ud
Eksplorasi Keragaman Serangga Coleoptera dan Lepidoptera di Pulau
Moti, Ternate, Maluku Utara 167
Warsito Tantowijoyo & Giyanto FLORA
Analisis Tutupan Lahan Kawasan Pulau Moti, Ternate, Maluku Utara 187 Hetty IP Utaminingrum & Roemantyo
Hutan mangrove di Pulau Moti 199
Suhardjono & Ujang Hapid
Keanekaragaman Anggrek di G Gamalama, Ternate 219
Izu Andry Fijridiyanto & Sri Hartini
Vegetasi Hutan Pulau Moti, Ternate, Maluku Utara 227
Edi Mirmanto
Keanekaragaman Jenis Pohon di Hutan Sekunder Pulau Moti,
Ternate-Maluku Utara 237
Razali Yusuf
Keanekaragaman Tumbuhan Berkhasiat Obat di Pulau Moti, Ternate,
Maluku Utara 251
Siti Sunarti
Eksplorasi Tumbuhan di Pulau Moti, Ternate, Maluku Utara 267 Deden Girmansyah & Siti Sunarti
MIKROBIOLOGI
Drug Discovery Antibiotik Berbasis Biodiversitas Aktinomisetes Lokal
Asal Ternate 283
Arif Nurkanto
Isolasi dan Identifikasi Kapang-Kapang Kontaminan Dari Biji Kenari
Kering (Canarium ovatum) 295
Nurhasanah &Sundari
Mikroba Laut Penghidrolisis Senyawa Nitril di Sekitar Pulau Moti,
Ternate 301
Nunik Sulistinah & Rini Riffiani
Isolasi dan Penapisan Bakteri Pendegradasi Dibenzothiophene,
Phenanthrene dan Fluoranthene Asal Perairan Laut Sekitar Pulau
Moti-Ternate 309 Rini Riffiani & Nunik Sulistinah
Penapisan dan Isolasi Bacillus Penghasil Amilase Dari Limbah Sagu
(Metroxylon sagu Rottb) 317
Deasy Liestianty1, Nurhasanah2 SOSIAL BUDAYA
Membangun Ternate Bermodal Kekayaan Sosio-Historis 329
Dhurorudin Mashad
Analisis Struktural Terhadap Mitos “Tujuh Putri” Pada Kebudayaan
Ternate, Maluku Utara 343
Safrudin Amin
Ekologi Ternate 283-293 (2011)
Drug Discovery Antibiotik Berbasis Biodiversitas Aktinomisetes Lokal
Asal Ternate
Arif Nurkanto
Mikrobiologi, Pusat Penelitian Biologi LIPI, Komplek Cibinong Science Center, Jl. Jakarta Bogor KM 46 Cibinong. E-mail : [email protected]
ABSTRACT
Research on antibiotic drug discovery based on biodiversity of Indonesian microbes has been conducted. Our research located at Ternate and Moti Island, North Maluku. Microbes target as antibiotic sources are bacterial group of actinomycetes. The steps have been performed in this study began with the collection of soil and litter samples. Advanced stages are isolation, identification using 16 S r DNA, antibiotic screening produced by actinomycetes, which include: cultivation, metabolite compounds extraction, antimicrobial activity testing, Minimum Inhibitor Concentration (MIC) determination, a leak test of nucleic acid, protein, Ca+ and K+ ions and
analyses of pathogen microbes cell damage using Scanning Electron Microscopy ( SEM) observation. The results showed that Ternate and Moti have high of Actinomycetes diversity. Most of them have antibiotic activity. We had selected one isolate with the highest activity for further analyses. The results showed that selected isolate capable of inhibiting some of microbial pathogens with MIC values varied (64 – 128 μg / ml). Mechanism of the active compounds from actinomycetes isolate was selected through the leakage of nucleic acid, protein, Ca+ and
K+ ions. We also detected several phatogenic cells damage through morphological observation
using SEM.
Key words: Antibiotic, aktinomisetes, Ternate PENDAHULUAN
Pencarian senyawa obat baru berbasis senyawa metabolit yang diproduksi oleh mikroba semakin mendapat perhatian yang tinggi. hal ini disebabkan beberapa faktor, diantaranya makin meningkatnya infeksi oleh mikroba pathogen yang bersifat resisten antibiotik dan juga pencarian senyawa obat baru yang menjanjikan keuntungan ekonomi yang tinggi dalam sektor industri. Mikroba merupakan sumber senyawa
obat yang sangat potensial karena belum banyak di eksplorasi, dapat memproduksi senyawa dengan waktu yang relative sangat cepat, mudah penanganannya dan mudah di manipulasi baik secara alami maupun genetik.
Salah satu kelompok mikroba yang paling potensial sebagai penghasil senyawa obat yang dicari saat ini adalah Actinomycetes. Mereka memproduksi lebih dari dua per tiga senyawa obat yang telah diproduksi secara komersial. Aktinomisetes merupakan kelompok
Arif Nurkanto
bakteri gram positip dan terdistribusi luas di alam. Mereka dikenal sebagai mikroba saprofitik pada tanah (Takisawa et al. 2003; Khamna et al. 2008). Kebanyakan aktinomisetes yang hidup pada habitat tanah masuk dalam genus Streptomyces (Goodfellow & Simpson 1987) dan 75% komponen bioaktif diproduksi oleh genus ini. Hal yang menarik dari aktinomisetes adalah kemampuannya dalam mempro-duksi komponen bioaktif yang penting dan memiliki nilai komersial yang tinggi dari sector medis (You et al. 2005; Moore et al. 2005). Senyawa aktif yang berguna tersebut diantaranya adalah antibiotik, anticancer, peningkat system imunitas dan juga agen verteriner yang potensial. Untuk menghasiilkan senyawa obat baru dari aktinomisetes, ada beberapa hal yang harus diperhatikan, yaitu pengembangan metode isolasi yang tepat untuk mempe-roleh isolate murni aktinomisetes dan penentuan relung ekologi yang baik seba-gai penentu diversitas dan penyebaran dalam habitat dan tipe ekosistemnya (Suzuki et al. 1994).
Kepulauan Indonesia merupakan aspek strategis dalam pencarian senyawa biokatif baru karena merupakan salah satu dari pusat keanekaragaman biota, termasuk mikroba di Dunia. Tipikal hutan hujan tropis di Indonesia yang khas dan kajian drug discovery berbasis mikroba yang belum banyak dilakukan sangat menjanjikan. Ternate dan pulau kecil di sekitarnya menjadi salah satu objek riset yang menarik untuk dipelajari. Wilayah yang secara biogeografi merupakan garis batas Wallacea, yang memberikan perbedaan zonasi distribusi dan keraga-man flora dan fauna, namun belum
dike-tahui komposisi biodiversitas mikroba di dalamnya. Studi keragaman dan drug discovery berbasis mikroba kawasan Ternate dan pulau di sekitarnya paling tidak akan memberikan informasi dan wacana baru karena belum pernah dilakukan riset sebelumnya.
Penelitian ini bertujuan untuk mengetahui biodiversitas aktinomisetes dan kemampuan antibiotik yang dihasilkan dalam melawan mikroba pathogen, sehingga diharapkan nantinya dapat dimanfaatkan sebagai sumber antibiotik indigenus yang potensial.
BAHAN DAN CARA KERJA Sampel yang diambil berupa tanah dan seresah dari berbagai tipe ekosistem di Ternate dan pulau Moti. Isolasi aktinomisetes dilakukan dengan menggu-nakan metode Rehidrasi Centrifugasi dan Sodium Dodesyl Sulfat – Yeast Ekstrak (SDS-YE) pada medium Humic Vitamin Agar (HVA) (Hayakawa & Nanomura, 1987; Hayakawa et al. 2004). Perhitu-ngan kelimpahan aktinomisetes berdasarkan metode Lee & Hwan (2002). Purifikasi isolat murni dilakukan pada medium Yeast Strach Agar (YSA). Identifikasi isolat terpilih dilakukan melalui pendekatan molekular 16S rDNA menggunakan metode Pitcher et al (1989). Tahapan yang dilakuan berupa ekstraksi DNA, amplifikasi menggu-nakan Polymerase Chain Reaction (PCR), visualisasi hasil PCR, purifikasi DNA hasil amplifikasi, cycle sequencing, sekuen dan analisis dengan ABI 3130 (Applied Biosystems Inc., Foster, California). Analisis DNA menggunakan
Drug Discovery Antibiotik Berbasis Biodiversitas
program BioEdit dan dilakukan blast pada Bank Gen NCBI dataLibrary. filogenetik analisis menggunakan program multiple aligment Clustal X versi 1.83. Konstruksi pohon filogenetik berdasarkan jarak kekerabatan genetik dengan metode Neighbor joining. Konstruksi jarak evolusi dalam derajat kepercayaan menggunakan bootstrap value pada program NJ plot.
Screening Aktinomisetes Penghasil Antibiotik
Masing-masing isolat aktinomisetes ditumbuhkan dengan 100 ml medium cair Actino Medium No. 1 (Daigo, Japan) dengan komposisi 5 g polipepton, 3 g ekstrak khamir, 1 L H2O, pH 7,2. Inku-basi dilakukan selama 7 hari dengan penggojogan pada rotary shaker dengan kecepatan 130 rpm pada suhu 28 oC.
Ekstraksi untuk mendapat produk metabolit dilakukan dengan menambah-kan 100 ml larutan etil asetat dan metanol (4:1) selama 3 kali, dan kemudian dikeringkan dengan rotary evaporator pada suhu 35 oC. Kristal metabolit yang
terbentuk ditimbang dan dilarutkan kembali dengan aseton. Ekstrak yang diperoleh dianalisis dengan teknik KLT (gel silika GF254) dengan larutan pengembang campuran CH2Cl2 dan methanol dengan perbandingan 15:1. Kromatogram KLT kemudian dimonitor dengan pemaparan sinar UV pada panjang gelombang 254 nm dan pereaksi penampak noda 1% CeSO4 dalam 10% H2SO4 pekat.
Mikroba uji yang digunakan berupa bakteri gram positip dan negatip ( Esche-richia coli NBRC 14237, Bacillus
subtilis NBRC 3134, Staphylococcus aureus NBRC 13276, Micrococcus luteus NBRC 1367) dan fungi/yeast (Candida albicans NBRC 1594, Saccharomyces cerevisiae NBRC 10217 dan Aspergilus niger). Uji antibiotik yang dilakukan adalah metode difusi media. Pengujian antibakteri dilakukan dengan menuangkan 4 mL top layer media Mueler Hinton (Difco) 0,5 resep yang mengandung 0,2 mL bakteri uji ke atas medium Mueller Hinton agar (ekstrak beef 2g/L, casein 17,5 g/L Strach 1,5 g/L dan agar 17 g/L) dalam petridish. Pengujian antifungi/yeast sama dengan pengujian antibakteri, tapi media yang digunakan adalah Saburoad (Difco, 10 g/L pepton, 40 g/L glukosa, 17 g/l agar). Uji antibiotik dilakukan dengan meletakkan paper disc steril yang dicelupkan dalam larutan hasil ekstraksi pada agar. Indikasi produk antibiotik dapat diamati dengan terbentuknya zona bening di sekitar paper disc.
Penentuan Minimum Inhibitor
Concentration (MIC)
Penentuan MIC dilakukan terhadap Mikroba uji, yaitu bakteri gram negatif, bakteri gram positip, yeast dan filamentous fungi berdasarkan metode Broth Microdilution Method (Schwalbe et al., 2007 ; Rahman et al., 2005).
Uji Kebocoran Sel
Uji kebocoran yang dilakukan berupa : analisis kebocoran protein, asam nukleat, kebocoran Ion Ca+ dan K+. Suspensi mikroba uji yang telah ditumbuhakan selama 24 jam dalam media NB (bakteri) dan YMB (kapang dan khamir) sebanyak
Arif Nurkanto
10 ml diambil, ditambahkan 0,5 mL tween 80. larutan bakteri uji disentrifuge dingin dengan kecepatan 3500 rpm selama 20 menit. Filtrat dibuang kemudian pelet dalam tabung dicuci dengan buffer fosfat pH 7,0 sebanyak dua kali. Larutan buffer fosfat dan sel mikroba di tambah dengan ekstrak isolat Aktino dengan konsentrasi 1 MIC dan 2 MIC serta kontrol (tanpa penambahan ekstrak), diinkubasi dalam inkubator goyang selama 24 jam. Suspensi di sentrigfuge 3500 rpm selama 15 menit, lalu dipisahkan supernatan dan peletnya. Cairan supernatan diambil dan diukur absorbansinya pada panjang gelombang 260 nm dan 280 nm dengan menggunakan spektrofotometri UV/VIS (Shimadzu, Japan) untuk mengetahui kebocoran asam nukleat dan protein. Untuk mengetahuii kebocoran ion K+ dan Ca+ digunakan analisis menggunakan AAS.
Analisis Kerusakan sel Mikroba Patogen
Analisis yang dilakuan adalah dengan menggunakan observasi morfo-logi sel setelah perlakuan. Prosedur perla-kuan seperti yang telah disebutkan, dimana supernatan sel dianalis keboco-rannya, sedangkan pelet sel dianalisis kerusakanya dengan pengamatan meng-gunakan Scaning Electro Microscope (SEM) seri JCM.
HASIL
Studi Biodiversitas dan Status Taksonomi
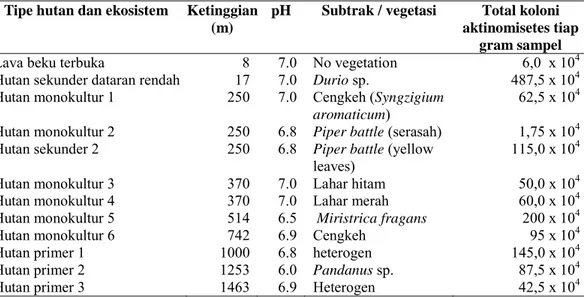
Ternate memiliki keragam aktinomi-setes yang cukup tinggi, walaupun tidak terdapat banyak tipe ekosistem didalam-nya. Daerah terestrial yang didominasi oleh pola pertanian monokultur sedikit banyak mempengaruhi keragaman mikroba tanah, terutama aktinomisetes. Tabel 1. Hasil enumerasi kelimpahan aktinomisetes berdasarkan random sampling dengan
variasi tipe hutan dan ekosistem.
Tipe hutan dan ekosistem Ketinggian
(m)
pH Subtrak / vegetasi Total koloni
aktinomisetes tiap gram sampel
Lava beku terbuka 8 7.0 No vegetation 6,0 x 104
Hutan sekunder dataran rendah 17 7.0 Durio sp. 487,5 x 104
Hutan monokultur 1 250 7.0 Cengkeh (Syngzigium
aromaticum)
62,5 x 104
Hutan monokultur 2 250 6.8 Piper battle (serasah) 1,75 x 104
Hutan sekunder 2 250 6.8 Piper battle (yellow
leaves) 115,0 x 10
4
Hutan monokultur 3 370 7.0 Lahar hitam 50,0 x 104
Hutan monokultur 4 370 7.0 Lahar merah 60,0 x 104
Hutan monokultur 5 514 6.5 Miristrica fragans 200 x 104
Hutan monokultur 6 742 6.9 Cengkeh 95 x 104
Hutan primer 1 1000 6.8 heterogen 145,0 x 104
Hutan primer 2 1253 6.0 Pandanus sp. 87,5 x 104
Hutan primer 3 1463 6.9 Heterogen 42,5 x 104
Drug Discovery Antibiotik Berbasis Biodiversitas
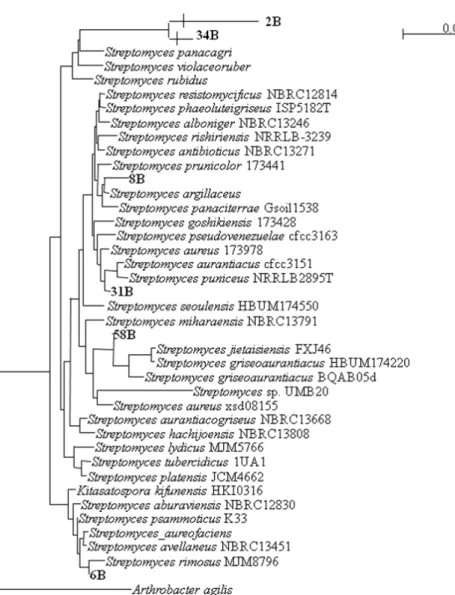
Aktinomisetes secara umum memiliki kecenderungan diversitas yang lebih rendah pada substrat pertanian dan minokultur. Dari berbagai lokasi pengambilan sampel, diperoleh kelimpa-han aktinomisetes seperti pada Tabel 1. Berdasarkan identifikasi molekuler 16S rDNA, beberapa jenis aktinomisetes Ternate merupakan kandidat jenis baru (Gambar 1 ). Walaupun demikian, masih memerlukan studi yang lebih lanjut untuk memastikan hal tersebut.
Studi antibiotik
Aktinomisetes yang telah diisolasi dan di purifikasi kemudian disimpan dalam bentuk kultur hidup pada agar miring suhu ruang dan gliserol 10% pada suhu -800C. Penapisan kemampuan
antibiotik oleh aktinomisetes telah dilakukan terhadap 120 isolat terseleksi. Kemampuan antibiotik dalam mengham-bat pertumbuhan mikroba patogen bervariasi dari aktinomisetes yang diisolasi dari sampel seresah maupun tanah (Gambar 2). Pembentukan zona bening oleh adanya aktivitas antibiotik seperti pada Gambar 3.
Satu aktinomisetes yang memiliki metabolit dengan aktivitas antibiotik tinggi diseleksi lagi untuk bioessay lebih lanjut. Pengujian yang dilakukan berupa perhitungan MIC, analisis kebocoran asam nukleat, kebocoran protein, pelepasaan ion serta aktivitasnya dalam nekrosis sel mikroba patogen.
Minimum Inhibitor Concentration (MIC), merupakan nilai konsentrasi minimum metabolit dalam menghambat atau membunuh mikroba. Berdasarkan hasil analisis menggunakan sistem Plate dilution (Rahman, et al. 2005), diperoleh hasil MIC seperti pada Tabel 2.
Kebocoran Sel bakteri patogen oleh Aktivitas Antibiotik Isolat Aktinomisetes
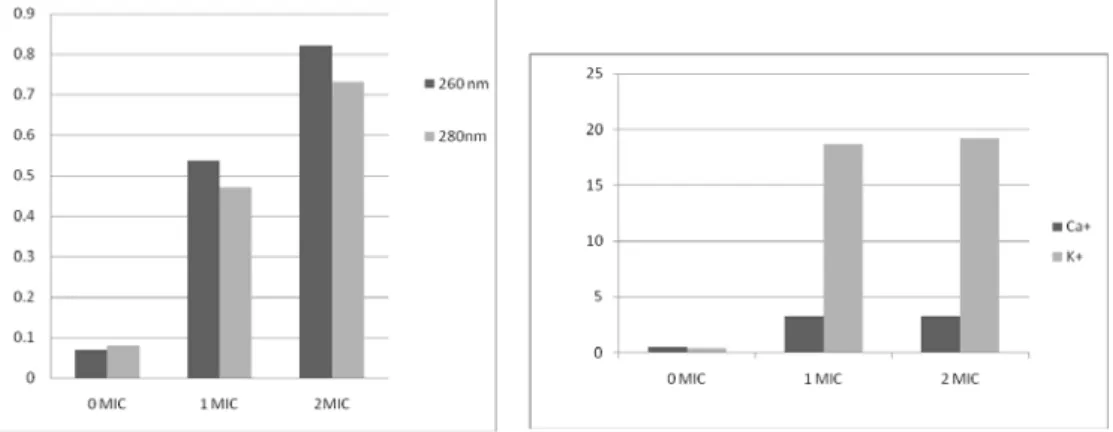
Analisis kebocoran sel yang dilakukan berupa kebocoran protein, asam nukleat, ion K dan ion Ca terhadap bakteri patogen Bacillus subtilis (Gambar 4) .
Hasil analisis menunjukkan bahwa pemberian senyawa metabolit menye-babkan kebocoran sel pada bakteri patogen. Uji konfirmasi untuk melihat
No Mikroba Uji Nilai MIC (µg/ ml)
1 Escherichia coli - 2 M. luteus 64 3 S. aureus 128 4 Bacillus subtilis 64 5 Candida albicans - 6 S. cerevisiae 128 7 Aspergillus niger - Tabel 2. Hasil analisis MIC menggunakan sistem Plate dilution
Drug Discovery Antibiotik Berbasis Biodiversitas
Gambar 1. Analisis Filigenetik beberapa Isolat aktinomisetes asal Ternate
bentuk sel bakteri patogen setelah perlakuan dengan senyawa metabolit yang diberikan dilakukan dengan
menggunakan Scaning Electro
Microscope (SEM) (Gambar 5). Semua isolat aktinomisetes yang telah diisolasi dan memiliki kemampuan
antibiotik disimpan dalam bentuk kultur murni di pusat Koleksi mikroba LIPI (LIPI Microbial Culture Collection-LIPIMC) Pusat Penelitian Biologi. Hal ini selain sebagai konservasi ex situ mikroba Indonesia, juga dengan tujuan untuk studi dan pemanfaatan lebih lanjut.
Arif Nurkanto
Gambar 2. Kemampaun antibiotik isolat aktinomisetes terseleksi dalam menghambat pertumbuhan mikroba patogen.
Gambar 3. Zona bening yang terbentuk oleh aktivitas antibiotik dari senyawa yang diproduksi oleh aktinomisetes.
Gambar 4. Tingkat kebocoran protein dan asam nukleat (a) dan antara ion (b) dengan berbagai dosis pemberian senyawa metabolit.
Drug Discovery Antibiotik Berbasis Biodiversitas
PEMBAHASAN
Berdasarkan teknik isolasi SDS-YE terhadap sampel, diperoleh bahwa lebih dari 75% aktinomisetes yang terisolasi dalam kelompok genus Streptomyces. Secara taksonomis, dari kajian aspek morfologi dan biokimia, genus ini memiliki ciri sebagai berikut: rantai spora pada hifa aerial dan memiliki miselium yang lengkap. Kelimpahan miselium yang tinggi dan rantai sporanya panjang. Spora tersusun dalam bentuk kumparan yang menggulung atau berpilin. Ada juga yang berbentuk untaian panjang melengkung. Rantai spora Streptomyces sangat jelas terlihat pada pengamatan mikroskopik, karena memiliki bentuk yang khas. Hifa vegetatif memproduksi miselium bercabang sangat banyak dan jarang yang berfragmen dengan diameter 0,5 – 2 um. Miselium aereal saat dewasa membentuk rantai spora berjumlah tiga atau lebih. Memiliki spora nonmotil. Kebanyakan memproduksi berbagai macam pigmen yang memberikan warna pada miselium aereal dan miselium vegetatif. Banyak jenis dari aktinomisetes mampu memproduksi antibiotik. Bersifat aerob kemoorganotrofik dan tipe metabolisme oksidatif. Mampu
menggu-nakan berbagai macam sumber karbon sebagai energi untuk pertumbuhannya. Temperatur optimum berkisar antara 25o
– 35o C. beberapa spesies tumbuh pada
temperatur rentang psikrofilik dan termofilik. Melimpah pada habitat tanah dan kompos dengan pH optimum 6,5 – 8,0. Beberapa spesies bersifat patogen dan fitopatogen dengan prosentase GC 69 – 75.
Sekitar 40% aktinomisetes yang diuji memiliki potensi sebagai antibiotik terhadap bakteri, jamur dan yeast yang bersifat patogen. Secara umum aktinomi-setes yang diisolasi dari serasah memiliki kemampuan antibiotik yang lebih tinggi, baik secara kuantitas maupun evektivitas-nya dibandingkan dengan isolat yang berasal dari substrak tanah. Kemapuan antibiotik dari aktinomisetes Ternate ini dapat dikatagorikan menjadi dua, yaitu spektrum luas dan spektrum sempit. Spektrum luas artinya bahwa satu aktinomisetes dapat menghambat beberapa mikroba patogen, sedangkan spektrum sempit artinya satu aktinomi-setes menghasilkan senyawa metabolit yang hanya menghambat satu atau mikroba tertentu saja. Kemampuan antibiotik tiap isolat sangat bervariasi, mulai dari yang lemah (diameter zona Gambar 5.. Morfologi sel setelah perlakuan 2 MIC (Dari kiri ke kanan: Kontrol, 1MC dan 2MC)
Arif Nurkanto
hambat kurang dari 10 mm) sampai kuat (diameter zona hambat lebih dari 30 mm).
Hasil penelitian dan analisis MIC yang telah dilakukan, menunjukkan bahwa antibiotik yang diproduksi oleh aktinomisetes terseleksi memiliki sifat spektrum luas, dimana dapat mengham-bat beberapa mikroba, baik bakteri maupun jamur, dengan nilai MIC yang berbeda.
Hasil analisis kebocoran sel protein, asam nukleat, ion Ca+ dan K+ yang telah
dilakukan dapat memberikan gambaran bahwa ekstrak isolat dapat menyebabkan terlepasnya protein dan asam nukleat dari sel. Terlepasnya metrial sel akibat kerusakan sel dapat dideteksi dengan spektrofotometi UV pada panjang gelombang 260 nm dan 280 nm. Senya-wa-senyawa yang memberikan serapan pada panjang gelombang 260 nm adalah RNA dan DNA sedangkan pada panjang gelombang 280 nm diidentifikasikan sebagai protein. Panjang gelombang 260 nm dapat mendeteksi purin, pirimidin, dan ribonukleotida, sedangkan panjang gelombang 280 nm dapat mendeteksi asam amino seperti tirosin dan triptofan. Profil analisis morfologi dengan menggunakan observasi SEM juga menunjukkan pola yang sama dengan kebocoran sel. Dengan pemberian senyawa metabolit, terlihat terjadi kerusakan sel yang berat. Dimana pada pemberian 1 MIC, sel mengalami penge-rutan dan memanjang. Terjadi beberapa tonjolan di sekujur sel. Menurut Gilbert (1984) dalam Miksusanti (2008), terbentuknya tonjolan tersebut disebabkan ketidakmampuan
peptidogli-kan manahan tepeptidogli-kanan intraseluler yang disebabkan oleh senyawa metabolit yang diberikan. Sitoplasma dan membran sitoplasma keluar. Biosintesis dinding sel juga tidak terbentuk atau terganggu oleh aktivitas senyawa metabolit yang diberikan. Pada dosis 2 MIC, sel telah benar-benar mengalami kerusakan parah, dimana terjadi nekrosis. Isi sel telah keluar. Hal ini menandakan kematian sel oleh pemberian metabolit. Ini didukung oleh data keluarnya material sel berupa ion, protein dan asam nukleat yang terdeteksi dari hasil penelitian.
KESIMPULAN DAN SARAN 1.Ternate meiliki keragaman aktinomi-setes yang cukup tinggi, dimana genus dominan yang terisolasi adalah Streptomyces.
2.Telah ditemukan aktinomisetes yang mampu memproduksi senyawa antibiotik dari Ternate dengan jumlah sekitar 40% dari aktinomisetes yang diuji. Antibiotik yang dihasilkan memiliki tipe spektrum luas dan spektrum sempit.
3.Mekanisme antibiotik oleh metabolit aktif yang dihasilkan oleh aktinomisetes terseleksi adalah kebocoran protein, asam nukleat, ion dan nekrosis pada bakteri patogen.
DAFTAR PUSTAKA
Goodfellow, M. & KE. Simson. 1987. Ecology of Streptomyces. Front Appl Microbiol 2 : 97 – 125. Hayakawa, M. & T. Nanomura. 1987.
Humic Acid Vitamin Agar, and a New Medium for the Selective
Drug Discovery Antibiotik Berbasis Biodiversitas
Isolation of Soil Actinomycetes. J. Ferment technology 65: 501 – 509.
Hayakawa, M., Y.Yoshida &Y. Iimura. 2004. Selective isolation of bioac-tive soil actinomycetes belonging to the Streptomyces violaceusniger phenotypic cluster. J. Appl. Microbiol. 96 : 973–981.
Khamna, S., A. Yokuta, L. Lumyong. 2008. Actinomycetes isolated from medical plant rhizosphere soil : Diversity and screening of Antifungal compound, indole-3-acetic acid siderophore production. World J. Microbial Biotechnol. Lee, YJ. & BK. Hwang. 2002. Diversity
of Antifungal Actinomycetes in Varios Vegetative soils of Korea. J. Microbiol 48: 407- 417. NRC Research Press.
Miksusanti, BSK. Jennie, B. Ponco & G. Trimulyadi. 2008. Cell wall Disruption of Escherchia coli K1.1 by Temu Kunnci (Kaempferia pandurata) Essential Oil. Berita Biologi. 9 (1) : 1 – 8.
Moore, Sb., JA. Kalaitzis and L. Xiang. 2005. Exploiting marine actinomy-cetes biosynthetic pathways for drug discovery. J Antonie van Leeuwenhock. 87 : 49 – 57.
Pitcher, DG., NA. Saunders and RJ. Owen. 1989. Rapid extraxtion of bacterial genomic DNA with Guanidium thiocyanate. Lett Appl Microbiol. 8: 108 – 114.
Rahman, A, MI Choudhary and WJ. Thomsen. 2005. Bioassay Techni-ques for Drug Development. Hardwood Academic Publishers. London.
Schwalbe,R, L. Stele-Moore & AC. Goodwin. 2007. Antimicrobial Susceptibility Testing Protocols. CRC Press. New York.
Suzuki, K., K. Nagai, Y. Shimizu & Y. Suzuki. ‘994. Search for actinomy-cetes in screening for new bioac-tive compound. J Actinomycetol. 8 : 122 – 127.
Takisawa,M.,RR. Colwel., & RT.Hill. 1993. Isolation and diversity of Actinomycetes in the Chesapheake bay. Appl Environ Microbial 59 : 997 – 1002.
You, JL., LX. Cou, GF. Liu, SN. Zhou, HM. Tan & YC. Lin. 2005. Isolation and Characterization of Actinomycetes antagonistic to phatogenic Vibrio spp. From nearshore marine sediment. World J. Micro. biotech.. 21 : 679 – 682.