II. TINJAUAN PUSTAKA
2.1. Bakteri Probiotik
Bakteri probiotik merupakan bakteri yang memiliki peranan penting bagi tubuh manusia. Menurut Matilla-Sandholm (1999), peranan probiotik yang besar pada tubuh karena peranan fisiologisnya yang penting dalam menjaga keseimbangan
mikroflora saluran pencernaan sehingga terbentuk suatu ekosistem yang unik, dimana terjadi interaksi yang kompleks yang bekerja secara sinergis dan antagonis tergantung
dari galur yang terlibat, jumlah, dan aktivitas metaboliknya. Menurut Reid (1999), suatu mikroba dikatakan probiotik bila memenuhi beberapa persyaratan, diantaranya: a) Stabil terhadap asam (terutama asam lambung), sehingga mampu bertahan dan
hidup selama melalui lambung dan usus.
b) Stabil terhadap garam empedu dan mampu bertahan hidup selama berada pada bagian atas usus kecil.
c) Memproduksi senyawa antimikroba seperti asam, hidrogen peroksida dan bakteriosin.
d) Mampu menempel dan mengkolonisasi sel usus manusia. Hal ini akan meningkatkan kompetisi dengan mikroba patogen dan penyebab karsinogen. e) Tumbuh baik dan berkembang dalam saluran pencernaan.
f) Koagregasi membentuk lingkungan mikroflora yang normal dan seimbang. g) Aman digunakan oleh manusia.
h) Tahan terhadap mikrobisida dan spermisida vaginal. Sifat ini diperlukan untuk probiotik yang ditujukan untuk mengobati infeksi saluran urinovaginal.
Mikroba yang digunakan sebagai probiotik dapat dilihat pada Tabel 1. Tabel 1. Mikroba yang Digunakan sebagai Probiotik
BAL
Selain spesies BAL Lactobacillus Bifidobacterium Species BAL yang
lain L. acidophilus L. casei L. amylovorus L. delbrueckii subsp bulgaricus L. gallinarum L. gasseri L. johnsonii L. paracasei L. plantarum L. reuteri L. rhamnosus B. adolescentis B. animalis B. bifidum B. breve B. infantis B. lactis B. longum Enterococcus faecalis E. faecium Lactococcus lactis Leuconostoc mesenteroides Pediococcus acidilactici Streptococcus thermophilus Sporolactobacillus inulis
Bacillus cereus var. toyoi Escherichia coli strain nissle Propionibacterium freudenreichii Saccharomyces cerevisiae S. boulardii
Sumber: Holzapfel, et al., 2001
Bakteri probiotik yang biasa digunakan umumnya berasal dari bakteri gram positif kelompok Bakteri Asam Laktat (BAL). Menurut Soeharsono (2010) dikutip Ramadhani (2015), mikroorganisme probiotik terutama terdiri dari strain
Lactobacillus, Bifidobacterium, dan Streptoccus. Lactobacillus merupakan strain
bakteri yang berasal dari mikroflora manusia, biasanya merupakan bagian dari ekosistem usus, namun jumlahnya bervariasi pada manusia. Bifidobacteria juga merupakan bagian dari mikroflora usus, namun spesiesnya berbeda berdasarkan usia; seperti contohnya bayi baru lahir sudah memiliki kolonisasi B. breve dan B. infantis, dan kolonisasi lebih banyak terjadi pada bayi yang mendapatkan ASI dibandingkan bayi yang mendapatkan susu formula.
Probiotik didefinisikan sebagai makanan suplemen berupa mikroba hidup yang memberi keuntungan pada manusia khususnya dalam keseimbangan mikroflora
usus (Fuller, 1999 dikutip Rizqiati, 2006). Menurut FAO/WHO (2006), mikroba probiotik yang digunakan untuk manusia harus memenuhi kualifikasi yaitu: isolat bakteri harus original dari manusia atau hewan, menunjukkan efek menguntungkan pada host, tidak bersifat patogen dan toksik, mengandung sel hidup mikroba yang cukup signifikan, dapat bertahan dan bersifat metabolik pada saluran pencernaan, tetap hidup selama penyimpanan dan penggunaannya, dan bersifat antagonis terhadap mikroba patogen. Viabilitas sel bakteri dalam produk pangan probiotik harus mengandung jumlah sel hidup minimal 107 CFU/g produk (Ouwehand dan Salminen, 1998 dikutip Krasaekoopt, Bhandari, dan Hilton, 2006).
Viabilitas merupakan parameter ketahanan suatu mikroba dalam hal ini terhadap penyimpanan dan terhadap kondisi tubuh, dimana mikroba probiotik dapat dikatakan bermanfaat saat mikroba tersebut telah sampai di usus. Menurut Dave dan Shah (1997), beberapa faktor yang mempengaruhi eksistensi bakteri probiotik dalam suatu produk di antaranya, pH, post-acidification (selama penyimpanan) dalam produk fermentasi, produksi hidrogen peroksida, toksisitas oksigen (permeabilitas kemasan terhadap oksigen), suhu penyimpanan, stabilitas dalam bentuk kering atau bekunya, keberadaan protease untuk memecah protein susu menjadi komponen yang lebih sederhana, dan kesesuaiannya dengan kultur yang secara alami terdapat pada produk (selama fermentasi). International Dairy Federation merekomendasikan bahwa bakteri probiotik harus aktif dan berlimpah dalam produk dan harus terdapat sekitar 107 cfu/g berat kering (Sultana, et al., 2000).
2.1.1. Bifidobacterium bifidum
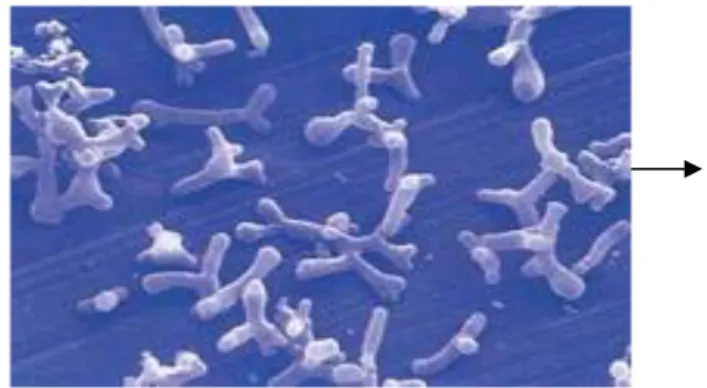
Bakteri Bifidobacterium bifidum termasuk golongan bakteri asam laktat dari filum Actinobacteria, kelas Actinobacteria, ordo Bifidobacteriales, famili Bifidobacteriaceae, dengan genus Bifidobacterium. Bakteri ini memiliki bentuk batang melengkung membentuk huruf V atau huruf Y tergantung pada kondisi kulturnya, memiliki panjang 2-8 µm, membentuk spora, dan non motil. Bakteri ini bersifat gram positif, katalase negatif, dan anaerobik dengan suhu pertumbuhan optimumnya 36-38 °C, bersifat heterofermentatif, memfermentasi laktosa untuk menghasilkan asam laktat dan asam asetat dengan rasio 2:3 tanpa menghasilkan CO2 (Chateris, Kelly, Morelli, dan Collins, 2002 dikutip Aritama, 2013). Bentuk koloni B.
bifidum dapat dilihat pada gambar 1.
Bentuk Sel
Gambar 1. Bentuk Sel Bifidobacterium (Anonima, 2009)
Menurut Soeharsono (2010), Bifidobacterium sp mempunyai bentuk koloni yang bulat, teratur, lembut putih berkilau, cembung, pertumbuhan seperti bentuk pohon dengan percabangan (arborescent), dan ada yang tepi luar koloni tegas dan rata (entire), transparan, cembung halus, ada yang non transparan, ada yang berwarna krem seperti benang tepi licin (filiform), koloni ada yang berukuran sangat kecil.
Bifidobacterium merupakan komponen mikroflora penting dalam usus
manusia dan hewan (Modler, 1994). Efek yang menguntungkan dari B. bifidum adalah kemampuannya untuk menghasilkan antibiotik bifidin yang stabil pada suhu 100 °C selama 30 menit. Selain itu, bakteri ini juga memiliki aktivitas antibakteri dan antagonis terhadap mikroba patogen, termasuk genus Salmonella, Escherichia,
Proteus, Shigella, dan Candida (Gagnon, et al., 2004).
2.1.2. Lactobacillus plantarum
Lactobacillus plantarum merupakan salah satu bakteri probiotik dari filum
Firmicutes, kelas Bacilli, ordo Lactobacillales, famili Lactobacilliceae, dan genus
Lactobacillus. Karakteristik dari L. plantarum adalah berbentuk batang (0,5-1,5 s/d
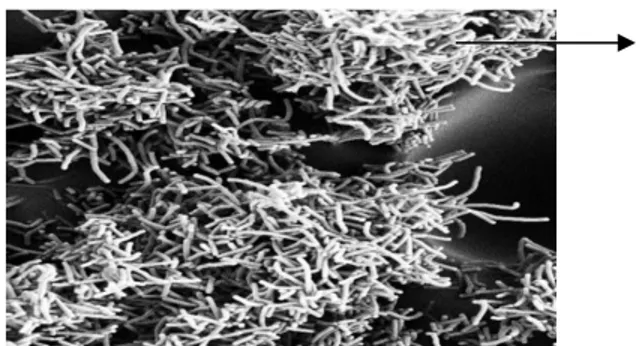
1,0-10 µm) dan tidak bergerak (non motil). Bakteri ini memiliki sifat katalase negatif, aerob atau fakultatif anaerob, mampu mencairkan gelatin, cepat mencerna protein, tidak mereduksi nitrat, toleran terhadap asam, dan mampu memproduksi asam laktat. Dalam media agar, L. plantarum membentuk koloni berukuran 2-3 mm, berwarna putih opaque, conveks, dan dikenal sebagai bakteri pembentuk asam laktat (Kuswanto dan Sudarmadji, 1988 dikutip Rostini, 2007). Menurut Frazier dan Westhoff (1998), L. plantarum adalah salah satu jenis BAL homofermentatif dengan temperatur optimal lebih rendah dari 37 °C. Bentuk sel L. plantarum dapat dilihat pada Gambar 2.
Menurut Delgado, et al. (2001), dalam keadaan asam, L. plantarum memiliki kemampuan untuk menghambat bakteri patogen dan bakteri pembusuk. Selain itu, L.
plantarum juga mempunyai kemampuan untuk menghasilkan bakteriosin yang
berfungsi sebagai zat antibiotik (Jenie dan Rini, 1995).
Gambar 2. Bentuk Sel Lactobacillus plantarum (Milton, 2010)
2.1.3. Lactobacillus acidophilus
Lactobacillus acidophilus merupakan nama spesies bakteri dari filum
Firmicutes, kelas Bacilli, ordo Lactobacillales, famili Lactobacilliceae, dan genus
Lactobacillus. Bakteri ini termasuk dalam golongan BAL homofermentatif. Menurut
Nakazawa dan Hosono (1992) dikutip Aritama (2013), L.acidophilus tidak dapat tumbuh pada suhu < 15 °C, memiliki suhu pertumbuhan optimum pada 35-38 °C dan pH optimum pada 5,5-6,0, dan memproduksi threonin adolase dan alkohol dehidrogenase yang akan mempengaruhi aroma.
L. acidophilus termasuk golongan bakteri gram positif, non motil, memiliki
bentuk batang dengan ukuran 0,6 – 0,9 hingga 1,0 – 6,0 µm, sel tunggal, berpasangan, ataupun membentuk rantai pendek (Breed, Murray, dan Smith, 1957).
L. acidophilus dapat ditemukan dalam gastro intestinal manusia, hewan, mulut, dan
vagina. Bakteri ini merupakan flora normal dalam saluran cerna yang sangat penting dalam memberikan pertahanan saluran cerna dengan cara menghambat kolonisasi
mikroba patogen (Subijanti dan Rahuh, 2005 dikutip Sulistijowati, 2012). Bentuk sel
L. acidophilus dapat dilihat pada Gambar 3.
Gambar 3. Bentuk Sel Lactobacillus acidophilus (Pyar dan Peh, 2014)
L.acidophilus merupakan bakteri probiotik karena mampu melewati
hambatan-hambatan hingga ke usus dalam keadaan hidup seperti asam lambung, enzim air liur, dan asam empedu (Aritama, 2013). L. acidophilus mempunyai ketahanan terhadap asam lambung buatan dengan pH 2,5 selama 3 jam dan bakteriosin yang dihasilkan tetap aktif pada pH 3 sampai pH 10 (Tamime A. dan R. K. Robinson, 1999 dikutip Senditya, dkk., 2014). Bakteri ini dapat memproduksi berbagai zat metabolit, seperti : asam organik, hidrogen peroksida, dan berbagai bakteriosin yang dapat menghambat perkembangan patogen (Kanbe, 1992). Bakteri ini mampu meningkatkan efisiensi penyerapan kalsium, besi, dan fosfor karena adanya asam laktat yang dihasilkan. Menurut Nakazawa dan Hosono (1992),
L.acidophilus diduga dapat menurunkan kadar kolesterol, mengendalikan
pertumbuhan kanker melalui aktivitas enzimnya yang mampu menurunkan produksi karsinogenik dan mencegah pengembangan kanker di dalam pencernaan.
Sel bakteri
2.2. Suspensi Bakteri Probiotik
Suspensi adalah sediaan cair yang mengandung partikel padat tidak larut yang terdispersi dalam fase cair. Salah satu masalah yang dihadapi dalam proses pembuatan suspensi adalah cara memperlambat pengendapan partikel serta menjaga homogenitas dari partikel. Menurut Lachman, Herbert, dan Joseph (1994), beberapa faktor yang mempengaruhi stabiltas suspensi, antara lain:
a) Ukuran partikel
Ukuran partikel erat hubungannya dengan luas penampang partikel tersebut serta daya tekan ke atas dari cairan suspensi. Hubungan antara ukuran partikel merupakan perbandingan terbalik dengan luas penampangnya, sedangkan antar luas penampang dengan daya tekan ke atas merupakan hubungan linier. Artinya semakin besar ukuran partikel maka semakin kecil luas penampangnya.
b) Kekentalan
Kekentalan suatu cairan mempengaruhi pula kecepatan aliran dari cairan tersebut, semakin kental suatu cairan kecepatan alirannya semakin turun (kecil). c) Jumlah partikel atau konsentrasi
Apabila di dalam suatu ruangan berisi partikel dalam jumlah besar, maka partikel tersebut akan susah melakukan gerakan yang bebas karena sering terjadi benturan antara partikel tersebut. Benturan akan menyebabkan terbentuknya endapan dari zat tersebut, oleh karena itu semakin besar konsentrasi partikel, semakin besar kemungkinan terjadinya endapan partikel dalam waktu yang singkat.
d) Sifat atau muatan partikel
Suatu suspensi kemungkinan besar terdiri dari beberapa macam campuran bahan yang sifatnya tidak sama, dengan demikian ada kemungkinan terjadi interaksi antar bahan yang menghasilkan bahan yang sukar larut dalam cairan tersebut.
Suspensi dengan partikel padat berupa sel bakteri probiotik disebut dengan suspensi bakteri probiotik. Pemilihan bahan pensuspensi yang digunakan harus sesuai dengan karakteristik partikel yang ingin dibuat suspensi dan tujuan pembuatan suspensi. Bahan pensuspensi untuk bakteri probiotik untuk tujuan preparasi enkapsulasi bakteri hendaknya berupa nutrisi (bahan makanan) yang diperlukan untuk pertumbuhan dan aktivitas bakteri. Hal ini bertujuan agar bakteri dapat berkembang biak dengan pesat sehingga didapat bakteri terenkapsulasi dalam jumlah banyak. Menurut Schiegel dan Karin (1994), secara garis besar nutrisi dibagi menjadi tujuh golongan yaitu:
a) Air
Air merupakan komponen utama sel mikroba dan medium. Fungsi air adalah sebagai sumber oksigen untuk bahan organik sel pada respirasi, sebagai pelarut, dan alat pengangkut dalam metabolisme.
b) Sumber energi
Ada beberapa sumber energi untuk mikroba yaitu senyawa organik atau anorganik yang dapat dioksidasi dan cahaya terutama cahaya matahari.
c) Sumber karbon
Sumber karbon untuk mikroba dapat berbentuk senyawa organik maupun anorganik. Senyawa organik meliputi karbohidrat, lemak, protein, asam amino, asam
organik, garam asam organik, polialkohol, dan sebagainya. Senyawa anorganik misalnya karbonat dan gas CO2 yang merupakan sumber karbon utama terutama untuk tumbuhan tingkat tinggi.
d) Sumber akseptor elektron
Proses oksidasi biologi merupakan proses pengambilan dan pemindahan elektron dari substrat, karena elektron dalam sel tidak berada dalam bentuk bebas, maka harus ada suatu zat yang dapat menangkap elektron tersebut. Penangkap elektron ini disebut akseptor elektron. Akseptor elektron ialah agensia pengoksidasi. Pada mikrobia yang dapat berfungsi sebagai akseptor elektron ialah O2, senyawa organik, NO3-, NO2-, N2O, SO4-, CO2, dan Fe3+.
e) Sumber mineral
Mineral merupakan bagian dari sel. Unsur penyusun utama sel ialah C, O, N, H, dan P. unsur mineral lainnya yang diperlukan sel ialah K, Ca, Mg, Na, S, Cl. Unsur mineral yang digunakan dalam jumlah sangat sedikit ialah Fe, Mn, Co, Cu, Bo, Zn, Mo, Al, Ni, Va, Sc, Si, Tu, dan sebagainya yang tidak diperlukan jasad. Unsur yang digunakan dalam jumlah besar disebut unsur makro, dalam jumlah sedang unsur oligo, dan dalam jumlah sangat sedikit unsur mikro. Selain berfungsi sebagai penyusun sel, unsur mineral juga berfungsi untuk mengatur tekanan osmose, kadar ion H+ (keasaman, pH), dan potensial oksidasi-reduksi (redox potential) medium. f) Faktor tumbuh
Faktor tumbuh ialah senyawa organik yang sangat diperlukan untuk pertumbuhan (sebagai precursor atau penyusun bahan sel) dan senyawa ini tidak
dapat disintesis dari sumber karbon yang sederhana. Faktor tumbuh sering juga disebut zat tumbuh dan hanya diperlukan dalam jumlah sangat sedikit.
g) Sumber nitrogen
Mikroba dapat menggunakan nitrogen dalam bentuk amonium, nitrat, asam amino, protein, dan sebagainya. Jenis senyawa nitrogen yang digunakan tergantung pada jenis jasadnya. Beberapa mikroba dapat menggunakan nitrogen dalam bentuk gas N2. Mikroba ini disebut mikrobia penambat nitrogen.
Susu skim mengandung nutrien yang relatif kaya, terutama kandungan gula. Gula susu, yaitu laktosa, yang terdapat pada susu skim berkisar antara 49,5%-52% (Sawitri, Manab, dan Huda, 2014). Keadaan ini baik untuk mendukung pertumbuhan strain Lactobacillus yang umumnya memiliki enzim laktase yang mampu mengubah laktosa menjadi glukosa, sehingga susu skim dapat dijadikan sebagai bahan pensuspensi bakteri probiotik.
2.3. Mikroenkapsulasi Probiotik
Enkapsulasi adalah sebuah proses penyalutan (coating) suatu bahan dengan menggunakan bahan lainnya. Bahan yang akan disalut biasanya disebut bahan inti atau bahan internal, sedangkan dinding pelapisnya biasanya adalah suatu lapisan polimer. Mikroenkapsulasi adalah suatu teknologi proses penggunaan penyalut yang relatif tipis pada partikel-partikel kecil zat padat atau tetesan cairan dan dispersi (Lachman, et al., 1994). Hasil dari proses mikroenkapsulasi disebut mikrokapsul. Mikrokapsul memiliki ukuran lebih dari 1 μm, biasanya antara 1 – 2000 μm dengan bentuk sferis (bentuk bola) atau tidak beraturan (Ghosh, 2006). Zat-zat yang
terkurung di dalam mikrokapsul dapat berwujud padat, cair atau gas dengan sifat permukaan hidrofilik (dapat mengikat air) atau hidrofobik (tidak dapat mengikat air). Struktur yang menyelimuti bahan mikrokapsul disebut dinding, kulit atau film pelindung yang berguna untuk melindungi inti dari kerusakan dan inti dapat terlepas pada saat kondisi yang memungkinkan.
Teknologi enkapsulasi dapat diterapkan pada bakteri probiotik untuk melindungi dari kondisi lingkungan yang ekstrim, sehingga dapat memperpanjang umur simpannya (Krasaekoop, Bhandari, dan Deeth, 2003). Enkapsulasi probiotik telah banyak dilakukan untuk meningkatkan ketahanan selama dalam jalur pencernaan (pH rendah dan cairan empedu) serta meningkatkan ketahanan atau viabilitas sel probiotik selama proses pembuatan produk dan penyimpanan (Sultana,
et al., 2000).
2.3.1 Tujuan Mikroenkapsulasi
Proses mikroenkaspsulasi memiliki beberapa tujuan, antara lain (Ghosh, 2006 dan Deasy, 1984 dikutip Pawestrisiwi, 2011):
a) Perlindungan bahan inti yang sensitif atau tidak stabil dari pengaruh lingkungan sebelum digunakan.
b) Memperbaiki kelarutan, kemampuan disperse, dan sifat alir bahan inti.
c) Peningkatan waktu simpan dengan mencegah reaksi degradasi (oksidasi dan dehidrasi)
d) Mengatur pelepasan bahan inti
f) Menutupi bau dan rasa yang tidak enak g) Mengubah bentuk cairan menjadi padatan
h) Mengurangi sifat iritasi bahan inti terhadap lambung dan saluran pencernaan i) Mencegah inkompatibilitas antara komposisi dalam sediaan
j) Mengurangi sifat higroskopis bahan inti
2.3.2 Morfologi Mikrokapsul
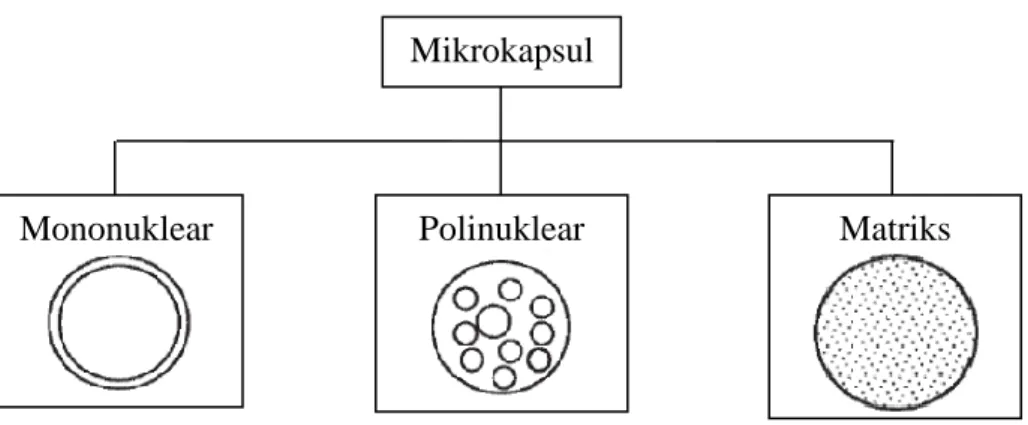
Morfologi mikrokapsul yang dihasilkan terutama tergantung pada bahan inti dan proses pembentukan dinding mikrokapsul. Berdasarkan morfologinya, mikrokapsul dapat diklasifikasikan menjadi tiga tipe, yaitu mononuklear, polinuklear, dan matrik. Morfologi mikrokapsul dapat dilihat pada Gambar 4.
Gambar 4. Morfologi Mikrokapsul (Ghosh, 2006)
Tipe mononuklear terdiri dari satu inti yang dikelilingi bahan penyalut (dinding mikrokapsul) sedangkan tipe polinuklear terdiri dari banyak inti dalam satu mikrokapsul. Pada tipe matriks, bahan inti terdistribusi secara homogen pada bahan penyalut (Ghosh, 2006).
Mikrokapsul
Morfologi mikrokapsul dengan bahan penyalut dan bakteri probiotik sebagai inti menggunakan metode freeze drying akan menghasilkan morfologi mikrokapsul matriks. Menurut penelitian Setyawati (2014) tentang penentuan proporsi enkapsulan kombinasi dan biomassa bakteri dalam pembuatan kultur mikroenkapsulasi, permukaan mikrokapsul yang dihasilkan ditemukan lekukan-lekukan (dents) dan tidak dijumpai retakan atau pecah-pecah, hal ini sebagai indikasi sifat perlindungan yang baik dari matriks mikrokapsul terhadap inti terutama yang sensitif antara lain terhadap oksigen. Selain itu, menurut Nicholaas dan Shimoni (2010) dikutip Adiyaman (2013), pemakaian metode freeze drying pada proses enkapsulasi akan menghasilkan morfologi matriks dengan ukuran partikel 20-5000 μm.
2.3.3 Komponen Mikroenkapsulasi
Pada prinsipnya, ada tiga bahan yang terlibat dalam proses mikroenkapsulasi, yaitu:
a) Bahan Inti
Bahan inti adalah bahan spesifik yang akan disalut, dapat berupa zat padat, cair, maupun gas. Inti zat padat dapat berupa campuran dari bagian-bagian yang aktif, stabilisator, pengencer, pengisi, dan penghambat atau pemacu pelepasan. Inti zat cair dapat terdiri dari senyawa polar atau non polar sebagai bahan aktif atau sebagai media bagi bahan aktif dalam bentuk larutan, suspensi atau emulsi (Lachman, et al., 1994).
Kompatibilitas dari bahan inti dengan bahan penyalut menjadi kriteria yang penting untuk meningkatkan efisiensi mikroenkapsulasi. Bahan inti sebaiknya tidak larut dan tidak bereaksi dengan bahan penyalut dan pelarut yang digunkaan. Ukuran
bahan inti juga memegang peranan penting untuk difusi, permeabilitas, dan pengendalian pelepasan bahan inti. Mikrokapsul dapat mengandung bahan inti sampai 99% dihitung terhadap berat mikrokapsul (Lachman, et al., 1994).
b) Penyalut
Bahan penyalut adalah bahan yang digunakan untuk melapisi inti dengan tujuan tertentu seperti menutupi rasa dan bau yang tidak enak, perlindungan terhadap pengaruh lingkungan, meningkatkan stabilitas, mencegah penguapan, kesesuaian dengan bahan inti maupun bahan lain yang berhubungan dengan proses penyalutan serta sesuai dengan metode mikroenkapsulasi yang digunakan. Bahan penyalut harus mampu memberikan suatu lapisan tipis yang kohesif dengan bahan inti, dapat bercampur secara kimia, tidak bereaksi dengan inti (bersifat inert), dan mempunyai sifat yang sesuai dengan tujuan penyalutan. Bahan penyalut yang digunakan dapat berupa polimer alam, semi sintetik, maupun sintetik. Jumlah penyalut yang digunakan antara 1-70% dan pada umumnya digunakan 3-30% dengan ketebalan dinding penyalut 0,1-6,0 μm (Istiyani, 2008).
c) Pelarut
Pelarut adalah bahan yang digunakan untuk melarutkan bahan penyalut dan mendispersikan bahan inti. Pemilihan pelarut biasanya berdasarkan sifat kelarutan dari bahan inti atau zat aktif dan bahan penyalut, dimana pelarut yang digunakan tersebut tidak atau hanya sedikit melarutkan bahan inti tetapi dapat melarutkan bahan penyalut. Pelarut polar akan melarutkan pelarut polar dan pelarut non polar akan melarutkan pelarut non polar (Istiyani, 2008).
2.4. Bahan Penyalut
Bahan penyalut adalah bahan yang berfungsi sebagai penyalut bahan inti (bahan aktif) dalam proses enkapsulasi. Penggunaan bahan enkapsulasi (coating) perlu diperhatikan, karena bahan-bahan tertentu belum tentu cocok dengan bahan jenis lainnya. Bahan penyalut harus mampu memberikan suatu lapisan tipis yang kohesif dengan bahan inti, dapat bercampur secara kimia, tidak bereaksi dengan bahan inti dan dapat memberikan sifat penyalutan yang diinginkan seperti kekuatan, fleksibilitas, impermeabilitas, sifat-sifat optic, dan stabilitas (Lachman, et al., 1994 dikutip Pawestrisiwi, 2011). Menurut Quellet, Taschi, dan Ubink (2001), bahan penyalut harus memiliki kriteria sebagai berikut:
a) Bersifat melindungi komponen aktif dari kerusakan seperti oksidasi dan cahaya.
b) Harus memiliki sifat kehilangan komponen aktif yang rendah selama proses berlangsung.
c) Komponen enkapsulat dapat terdispersi dalam larutan pengkapsul secara merata engan ukuran yang kecil.
d) Bahan pengkapsul harus memiliki sistem pengendalian pelepasan komponen aktif selama penyimpanan.
e) Bahan pengenkapsulasi harus aman.
f) Bahan pengenkapsulasi harus memiliki sifat fungsional spesifik seperti sifat emulsi, pembentukan film, dan dapat membentuk larutan konsentrasi tinggi. Menurut Fardiaz (1989), untuk mencegah kerusakan selama proses pengeringan maka digunakan komponen pelindung yang mempunyai sifat: 1) dapat
mencegah terjadinya pengeringan total, sehingga kerusakan DNA dan kematian sel dapat dicegah; 2) meminimalkan pembentukan kirstal es selama pembekuan cepat; 3) melindungi kultur kering dari kerusakan fisik. Beberapa bahan penyalut yang digunakan untuk mikroenkapsulasi dapat dilihat pada Tabel 2.
Tabel 2. Bahan Penyalut yang Digunakan untuk Mikroenkapsulasi
Kelompok Jenis
Gum Gum arab, agar, natrium alginat, karagenan
Karbohidrat Pati, dekstrin, sukrosa, sirup jagung, CMC, etil selulosa, metil selulosa, nitro selulosa, asetil selulosa, aetat fitat selulosa, asetat butilay fitat selulosa
Lemak Lilin, parafin, tristearin, asam stearat, monogliserida, digliserida, lilin tawon, minyak, lemak, minyak keras Bahan anorganik kalsium fosfat, silikat, tanah liat
Protein gluten, kasein, gelatin, albumin Sumber : Jackson dan Lee, 1991
Bahan penyalut yang umum digunakan dalam proses mikroenkapsulasi mikroorganisme adalah berbagai jenis polisakarida, seperti maltodekstrin, dan protein, seperti susu skim. Menurut Koswara (2009), maltodekstrin merupakan bahan penyalut yang harganya relatif murah, lebih komersil, mudah didapat, dan sering digunakan dalam indusrti pangan dibandingkan bahan penyalut lainnya. Menurut Young, Sarda, dan Rosenberg (1995), susu skim adalah salah satu bahan penyalut yang umum digunakan, terutama sebagai penyalut matriks yang diaplikasikan secara oral.
2.4.1 Susu Skim
Susu skim merupakan salah satu produk susu dengan kadar lemak yang rendah, yaitu 0,6-1,25% (Sawitri, et al., 2014). Menurut Iswahanik (2001), susu skim
merupakan sisa hasil pemisahan semua atau kebanyakan lemak susu dengan alat separator sentrifugal kontinyu. Susu skim yang banyak beredar di pasaran biasanya berbentuk bubuk dengan karakteristik berwarna putih, bersifat free flowing, dan bebas gumpalan, cita rasanya pada kondisi kering tidak berbau.
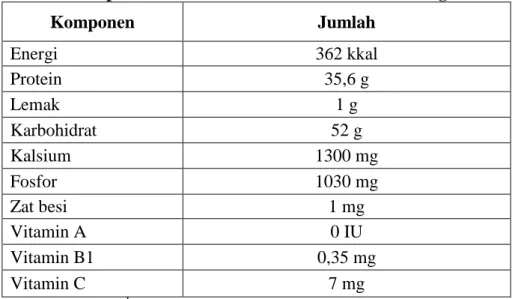
Protein merupakan kandungan terbesar pada susu skim. Komponen protein pada susu skim yang paling penting adalah kasein. Kasein merupakan fraksi utama protein yang mengendap saat susu segar diasamkan pada pH 4-6 pada suhu 20°C. Kasein menyusun 76-86% dari total protein susu skim. Protein nonkasein yang tertinggal setelah pengendapan kasein disebut protein whey atau serum protein. Whey menyusun 14-24% dari total protein susu skim (Thompson, et al., 1965). Protein whey bersifat labil terhadap panas dan terdenaturasi pada suhu 80°C. Hal ini berbeda dengan kasein yang stabil pada suhu 140°C. Komposisi nutrisi susu skim bubuk dalam 100 g bahan dapat dilihat pada Tabel 3.
Tabel 3. Komposisi Nutrisi Susu Skim Bubuk dalam 100 g bahan
Komponen Jumlah Energi 362 kkal Protein 35,6 g Lemak 1 g Karbohidrat 52 g Kalsium 1300 mg Fosfor 1030 mg Zat besi 1 mg Vitamin A 0 IU Vitamin B1 0,35 mg Vitamin C 7 mg Sumber: Anonimb (2001)
2.4.2 Maltodekstrin
Maltodekstrin merupakan salah satu bahan penyalut yang banyak digunakan pada industri pangan. Menurut Deman (1993), maltodekstrin merupakan produk hasil hidrolisis pati dengan menggunakan asam maupun enzim yang terdiri dari campuran glukosa, maltosa, oligosaokarida, dan dekstrin. Maltodekstrin pada dasarnya merupakan senyawa hasil hidrolisis pati yang tidak sempurna atau disebut hidrolisis parsial, yang terdiri dari campuran gula-gula dalam bentuk sederhana (mono dan disakarida) dalam jumlah kecil, oligosokarida dengan rantai pendek dalam jumlah relatif tinggi serta sejumlah kecil oligosakarida berantai panjang (Luthana, 2008 dikutip Lubis, 2011). Rumus umum maltodekstrin adalah [(C6H10O5)nH2O)].
Maltodekstrin didefinisikan sebagai produk hidrolisis pati yang mengandung unit α-D-glukosa yang sebagian besar terkait melalui ikatan 1,4 glikosidik dengan DE kurang dari 20 (Kearsley dan Dziedzic, 1995 dikutip Nurulhida, 2012 ) Menurut Chafid dan Kusumawardhani (2010), perbedaan nilai DE akan mempengaruhi karakteristik maltodekstrin. Jika nilai DE tinggi maka hygroscopicity, plasticity,
sweeteness, solubility, dan osmolality maltodekstrin pun akan meningkat. Namun jika
nilai DE rendah, yang akan meningkat adalah berat molekul, viscocity, cohesiveness, dan film-forming properties. Pernyataan ini didukung oleh Fennema (1996) dikutip Badarudin (2006) yang menjelaskan bahwa nilai DE berbanding terbalik dengan berat molekul, dimana maltodekstrin dengan nilai DE rendah biasanya bersifat non higroskopis sedangkan maltodekstrin dengan nilai DE tinggi bersifat higroskopis. Selain itu, maltodekstrin DE rendah cenderung mempunyai sifat yang mendekati sifat pati, sedangkan maltodekstrin DE tinggi cenderung bersifat seperti sirup jagung.
Penggunaan maltodekstrin terutama ditujukan untuk memberikan tekstur dan bentuk produk, mengontrol kristalisasi selama proses pembekuan (freezing), pengganti lemak, pembentuk film, dapat membentuk lapisan, tahan terhadap kekempalan, mampu mengikat flavor, dapat menjadi barrier oksigen, mempunyai dispersibilitas dan solubilitas yang baik (Frye & Setser, 1993 dikutip Iskandar, 2001). Maltodekstrin merupakan bahan pengental sekaligus dapat sebagai emulsifier, mudah melarut pada air dingin dan merupakan oligosakarida yang tergolong dalam prebiotik. Secara nyata dapat memperlancar saluran pencernaan dengan membantu berkembangnya bakteri probiotik (Triyono, 2010).
2.5. Freeze Drying
Freeze drying atau dehidrasi beku (pengeringan beku) merupakan suatu
sistem yang menggunakan vakum tinggi untuk memungkinkan terciptanya suatu keadaan suhu dan tekanan sehingga sifat fisik suatu substrat bahan pangan dapat diatur pada suatu titik kritis yang memungkinkan berhasilnya proses pengeringan dengan potensi rehidrasi yang dapat diperbaiki (Desrosier, 1988). Bahan aktif dan bahan penyalut terlarut dalam air dapat mengering beku untuk menghasilkan produk berpori dan tidak mengkerut (Zuidam, N.J dan Nedovic V.A, 2010).
Komponen alat freeze dryer terdiri dari: vacuum pump, ice condenser
chamber, ice condenser, glass lid, drying chamber, heatable shelf, vacuum sensor, drain valve, pressure control valve, aeration valve, rubber valve, thermal insulation, LDplus control and system main switch (Christ, 2006). Gambar alat freeze dryer
Gambar 5. Freeze dryer Christ alpha 1-4 LD-plus (Christ, 2006)
Menurut Haryani, Maulina, dan Haqioroh (2012), freeze drying dapat menyisakan kadar air hingga 1%, sehingga produk bahan alam yang dikeringkan menjadi stabil dan memenuhi syarat untuk pembuatan sediaan farmasi dari bahan alam yang kadar airnya harus kurang dari 10%. Berdasarkan hal tersebut, bahan pangan yang telah di freeze drying akan menjadi tahan lama karena metode freeze
drying menghilangkan kandungan air dalam bahan pangan sehingga dapat
meminimalisir terjadinya kerusakan bahan pangan oleh mikrooganisme dan enzim. Selain itu, freeze drying juga dapat mengurangi berat total bahan pangan sehingga akan memudahkan dalam proses transportasi. Hal yang perlu diperhatikan adalah semakin tipis bagian yang ingin di freeze drying, maka waktu yang diperlukan semakin singkat pula.
Proses pengeringan beku mengubah bentuk es dalam bahan yang beku langsung menjadi uap air tanpa mengalami proses pencairan terlebih dahulu. Sampel akan dibekukan terlebih dahulu, lalu setelah itu dimasukkan dalam alat freeze dryer
Tombol On/Off
Kontrol sistem LDplus Ruang kondensor
Rak
Penutup kaca
yang akan diset suhu dan tekanannya dibawah titik triple. Proses pengeringan beku (freeze dryer) suatu bahan didahului dengan proses pembekuan. Proses pembekuan pada prakteknya dilakukan dengan memasukkan dalam ruang pembeku dengan suhu -40°C, pada suhu ini produk akan membeku dengan cepat dan akan dihasilkan produk beku yang tidak merusak tekstur. Kualitas produk secara umum juga akan ditentukan oleh kualitas produk beku. Faktor utama proses pembekuan yang akan mempengaruhi mutu produk kering-beku yang dihasilkan adalah faktor kecepatan pembekuan (Hariyadi, 2013).
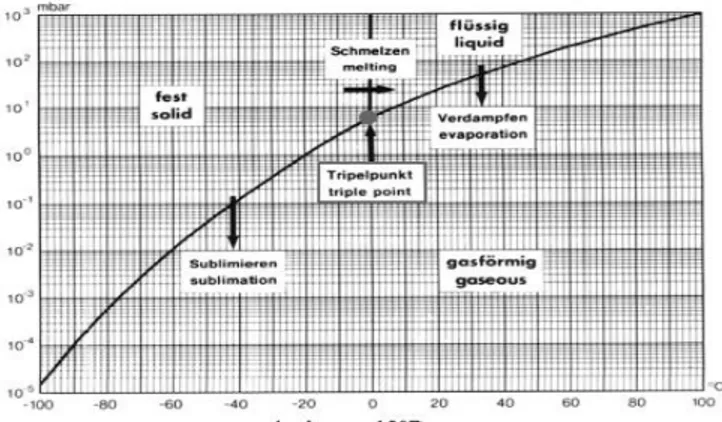
Proses pengeringan dilakukan dengan mengendalikan kondisi tekanan dan suhu. Pada kondisi tekanan 6.11 mbar dan suhu 0 °C, air akan berada pada kondisi kesetimbangan antara uap, air, dan es. Titik dimana terjadi kesetimbangan antar ketiga fase tersebut disebut sebagai titik triple (Christ, 2006). Kurva kesetimbangan antara uap, air, dan es dapat dilihat pada Gambar 6.
Gambar 6. Kurva Kesetimbangan Antara Uap, Air Dan Es (Christ, 2006)
Titik triple ini menunjukan hubungan antara suhu dan tekanan yang digunakan untuk dapat melakukan sublimasi pada proses freeze drying, dimana semakin rendah suhu yang digunakan maka semakin rendah pula tekanan yang
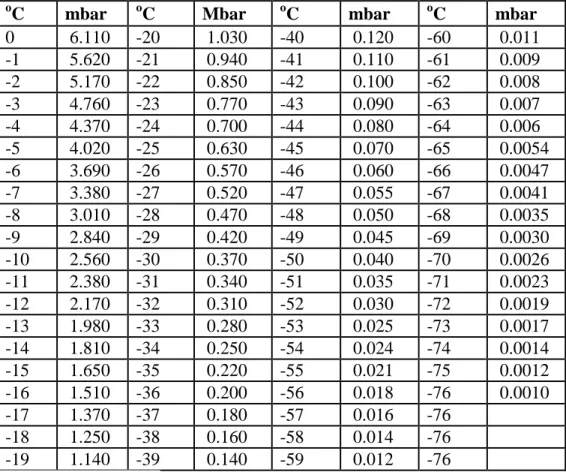
digunakan. Hubungan antara tekanan dan suhu pada saat proses sublimasi dapat dilihat pada Tabel 4.
Tabel 4. Hubungan Antara Tekanan dan Suhu pada saat Proses Sublimasi
o
C mbar oC Mbar oC mbar oC mbar
0 6.110 -20 1.030 -40 0.120 -60 0.011 -1 5.620 -21 0.940 -41 0.110 -61 0.009 -2 5.170 -22 0.850 -42 0.100 -62 0.008 -3 4.760 -23 0.770 -43 0.090 -63 0.007 -4 4.370 -24 0.700 -44 0.080 -64 0.006 -5 4.020 -25 0.630 -45 0.070 -65 0.0054 -6 3.690 -26 0.570 -46 0.060 -66 0.0047 -7 3.380 -27 0.520 -47 0.055 -67 0.0041 -8 3.010 -28 0.470 -48 0.050 -68 0.0035 -9 2.840 -29 0.420 -49 0.045 -69 0.0030 -10 2.560 -30 0.370 -50 0.040 -70 0.0026 -11 2.380 -31 0.340 -51 0.035 -71 0.0023 -12 2.170 -32 0.310 -52 0.030 -72 0.0019 -13 1.980 -33 0.280 -53 0.025 -73 0.0017 -14 1.810 -34 0.250 -54 0.024 -74 0.0014 -15 1.650 -35 0.220 -55 0.021 -75 0.0012 -16 1.510 -36 0.200 -56 0.018 -76 0.0010 -17 1.370 -37 0.180 -57 0.016 -76 -18 1.250 -38 0.160 -58 0.014 -76 -19 1.140 -39 0.140 -59 0.012 -76 Sumber: Christ (2006)
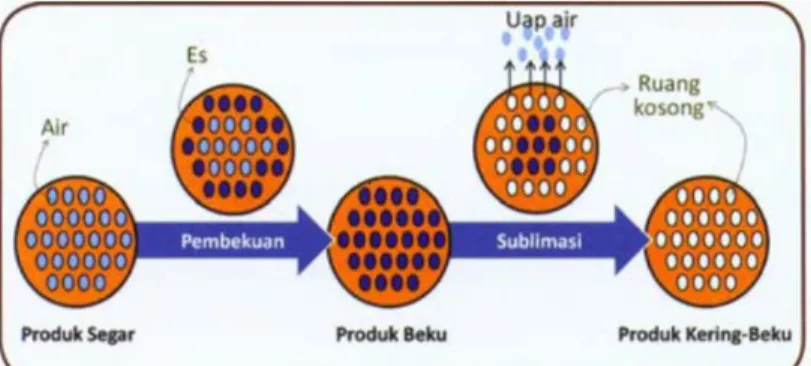
Mekanisme freeze drying menjadikan material bahan menjadi awet tanpa mengalami perubahan sifat biologi, kimia, dan struktur. Integritas produk tetap terjaga karena matriks es yang kaku menahan komponen padatan dalam bahan tetap pada tempatnya. Mekanisme proses pengeringan beku dapat dilihat pada Gambar 7.
Proses pengeringan (sublimasi) dilakukan dengan cara memasukkan produk beku ke dalam ruangan vakum. Harus dipertahankan bahwa kondisi proses tetap di bawah titik triple, sehingga bisa dijamin bahwa proses sublimasi bisa terjadi, dan tidak terjadi proses pelelehan. Kristal-kristal es yang berada pada struktur produk
pangan dipaksa untuk langsung mengalami sublimasi. Mekanisme alat freeze dryer yaitu uap air yang dihasilkan kemudian disedot dan dikondensasikan sehingga tidak membasahi produk yang sedang dikeringkan.
Gambar 7. Mekanisme Terjadinya Pengeringan Beku (Hariyadi, 2013)
2.6. Pengemasan
Pengemasan merupakan salah satu proses penting pada industri untuk menjaga mutu dan kualitas produk yang akan dipasarkan ke konsumen. Menurut Buckle, et al. (1987), pengemasan harus dilakukan dengan benar karena pengemasan yang salah dapat menyebabkan produk menjadi tidak memenuhi syarat mutunya. Pengemasan dilakukan untuk membantu untuk mencegah atau mengurangi kerusakan, melindungi produk yang ada di dalamnya, melindungi dari bahaya pencemaran serta gangguan fisik (gesekan, benturan, getaran). Selain itu, pengemasan juga mempermudah dalam proses penyimpanan, pengangkutan, dan pemasaran produk.
Dewasa ini, kemasan sudah memiliki bentuk dan bahan yang beragam jenisnya. Pemilihan bentuk dan jenis kemasan harus disesuaikan dengan produk yang akan dikemas, sehingga dapat memenuhi fungsi kemasan sebagai wadah produk,
pelindung produk, alat komunikasi, dan penambah daya tarik produk (Robertson, 1993 dikutip Ramadhani, 2015). Penggunaan kemasan dalam industri pangan harus dapat berfungsi dengan baik untuk mencegah penurunan mutu dan aman, serta tidak mengubah komposisi produk yang dikemas.
Menurut Buckle, et al., (1987) dikutip Ramadhani, 2015, kemasan yang dapat digunakan sebagai wadah penyimpanan harus memenuhi beberapa persyaratan, yakni dapat mempertahankan mutu produk supaya tetap bersih serta mampu memberi perlindungan terhadap produk dari kotoran, pencemaran, dan kerusakan fisik, serta dapat menahan perpindahan gas dan uap air. Pengemasan dapat mempengaruhi daya awet bahan pangan yang dikemasnya. Faktor-faktor utama yang mempengaruhi daya awet bahan pangan yang telah dikemas adalah :
1) Sifat alamiah dari bahan pangan dan mekanisme dimana bahan ini mengalami kerusakan, misalnya kepekaannya terhadap kelembaban dan oksigen, dan kemungkinan terjadinya perubahan-perubahan kimia dan fisik di dalam bahan pangan.
2) Ukuran bahan pengemas sehubungan dengan volumenya.
3) Kondisi atmosfer (terutama suhu dan kelembaban) di mana kemasan dibutuhkan untuk melindungi selama pengangkutan dan sebelum digunakan.
4) Ketahanan bahan pengemas secara keseluruhan terhadap gas atmosfer dan bau, termasuk ketahanan dari tutup, penutupan, dan lipatan.
Setiap bahan pangan masing-masing memiliki karakteristik yang berbeda-beda dalam sifatnya untuk menyerap atau mengeluarkan udara dan uap air. Hal ini
menyebabkan perlu adanya kemasan yang mempunyai daya tembus rendah sehingga menahan penyerapan air dan oksigen ke bahan pangan (Buckle, et al., 1987).
Produk kering yang memiliki sifat hidrofilik harus dilindungi dari penyerapan uap air karena dapat menurunkan kualitasnya. Umumnya produk-produk ini memiliki kelembaban relatif yang rendah oleh sebab itu harus dikemas dengan kemasan yang memiliki permeabilitas air yang rendah untuk mencegah produk yang berkadar gula tinggi merekat atau produk-produk tepung menjadi basah sehingga tidak lagi bersifat menggumpal (free flowing) (Syarief, Sassya, dan Isyana, 1989 dikutip Ramadhani, 2015). Salah satu kemasan yang dapat digunakan adalah kemasan metalized plastic.
2.6.1. Metalized Plastic
Plastik merupakan bahan dasar kemasan yang paling sering digunakan dalam pengemasan pangan. Kemasan plastik memiliki kelebihan dibandingkan kemasan lainnya, yaitu harga yang relatif murah, dapat dibentuk menjadi berbagai macam bentuk, dan dapat mengurangi biaya transportasi. Plastik juga memiliki sifat ringan, transparan, kuat, termoplastis, dan selektif dalam permeabilitasnya terhadap uap air, O2, dan CO2. Sifat permeabilitas plastik terhadap uap air dan udara menyebabkan plastik mampu berperan memodifikasi ruang kemas selama penyimpanan (Fitria, 2007).
Salah satu jenis kemasan plastik yang sering digunakan dalam industri pangan adalah metalized plastic. Metalized plastic merupakan kombinasi antara plastik dengan aluminium yang cocok digunakan sebagai pengemas makanan kering, keju, dan roti panggang (Fitria, 2007). Metallized plastic bersifat tidak meneruskan cahaya,
menghambat masuknya oksigen, menahan bau, memberikan efek mengkilap, dan mampu menahan gas (Brown, 1992). Kemasan metallized plastic dapat dilihat pada gambar 8.
Gambar 8. Kemasan metallized plastic (Dokumentasi Pribadi, 2015)
Metalizing merupakan proses pelapisan salah satu sisi film plastik transparan
dengan logam pada kondisi yang sangat vakum. Penggunaan logam yang dimaksud umumnya adalah aluminium. Kemurnian alumunium adalah 99,90 % dengan diameter wire sebesar 1,96 mm. Proses metalisasi dilakukan dengan cara menguapkan dan melelehkan aluminium pada suhu 1500 °C. Uap aluminium akan melapisi film plastik yang berputar pada sebuah rol pendingin bersuhu ± 15 °C (Febriyanti, 2002). Pengaturan rol pendingin pada suhu tersebut bertujuan agar film tidak meleleh ketika terkena uap alumunium yang panas (Febriyanti, 2002 dikutip Paramitha, 2011). Menurut Matsumoto (1999), walaupun lapisan penglogaman ini sangatlah tipis, sekitar 300-1000 Å (0,03-0,1 μm) tetapi dapat meningkatkan perlindungan, menahan bau, memberikan efek kilap dan menahan gas. Menurut Sumanti, Djali, dan Lanti (2009), metalized plastic memiliki permeabilitas sebesar 0.3205 g/m2.24h.
Menurut Brown (1992), plastik yang dilapisi logam (metalized plastic) dapat meningkatkan penampilan dan mengurangi transmisi. Plastik ini dapat melindungi produk dari cahaya. Penggunaan plastik ini antara lain untuk mengemas kopi, makanan kering, keju, dan roti panggang karena ketahanan terhadap uap air dan gas, tidak meneruskan cahaya, dan menghambat masuknya oksigen. Selain itu, metalized
plastic mudah disobek sehingga memudahkan konsumen saat membuka kemasan.
2.7. Pendugaan Umur Simpan
Menurut Institute of Food Technologist, umur simpan produk pangan adalah selang waktu antara saat produksi hingga saat konsumsi dimana produk berada dalam kondisi yang memuaskan pada sifat-sifat penampakan, rasa, aroma, tekstur, dan nilai gizi (Arpah, 2001). Terjadinya perubahan selama penyimpanan akan mempengaruhi mutu produk pangan tersebut.
Peraturan mengenai penentuan umur simpan bahan pangan di Indonesia terdapat dalam UU Pangan No. 7 tahun 1996 dan PP No. 69 tahun 1999. Umur simpan produk pangan biasa dituliskan sebagai best before date yang berarti produk masih dalam kondisi baik dan masih dapat dikonsumsi beberapa saat setelah tanggal yang tercantum terlewati. Istilah lain yang digunakan adalah use by date yang menyatakan produk tidak dapat lagi dikonsumsi, karena berbahaya bagi kesehatan manusia (produk yang sangat mudah rusak oleh mikroba) setelah tanggal yang tercantum terlewati (Ellis, 1994).
Menurut Syarief, et al. (1989), faktor-faktor yang mempengaruhi umur simpan bahan pangan yang dikemas adalah keadaan alamiah atau sifat makanan dan
mekanisme berlangsungnya perubahan, misalnya kepekaan terhadap air dan oksigen dan kemungkinan terjadinya perubahan kimia internal dan fisik, ukuran kemasan dalam hubungannya dengan volume, kondisi atmosfir (terutama suhu dan kelembaban) dimana kemasan dapat bertahan selama transit dan sebelum digunakan, kekuatan keseluruhan dari kemasan terhadap keluar masuknya gas, air, dan bau, termasuk perekatan, penutupan, dan bagian-bagian yang terlipat.
Penentuan umur simpan suatu produk pangan dilakukan dengan mengamati produk pangan selama penyimpanan sampai terjadi perubahan yang tidak dapat diterima lagi oleh konsumen (Ellis, 1994). Syarief dan Halid (1993) menyatakan bahwa perubahan mutu pangan terutama dapat diketahui dari perubahan faktor mutu tersebut. Oleh karena itu, dalam menentukan daya simpan suatu produk perlu dilakukan pengukuran terhadap atribut mutu produk tersebut. Jenis atribut mutu yang diuji tergantung pada jenis produk pangan. Suatu produk pangan, tidak semua parameter harus diuji, melainkan salah satu saja, yakni parameter yang paling cepat memengaruhi penerimaan konsumen.
Salah satu kendala yang sering dihadapi industri pangan dalam penentuan masa kadaluarsa produk adalah waktu. Menurut Syarief, et al. (1989), secara garis besar umur simpan produk pangan dapat diduga dan kemudian ditetapkan umur simpannya dengan menggunakan dua konsep yaitu dengan metode konvesional (Extended Storage Studies) dan metode percepatan (Accelerated Shelf Life Testing).
Metode konvensional adalah penentuan umur simpan dengan cara menyimpan suatu seri produk pada kondisi normal sehari-hari sambil dilakukan pengamatan terhadap penurunan mutunya hingga mencapai tingkat kadaluarsa. Metode ini akurat
dan tepat, namun membutuhkan waktu yang panjang dan analisis parameter mutu yang relatif banyak. Biasanya metode konvensional digunakan untuk produk yang mempunyai masa kadaluarsa kurang dari 3 bulan (Arpah, 2001). Metode Accelerated
Shelf Life Testing (ASLT) menggunakan suatu kondisi lingkungan yang dapat
mempercepat reaksi deteriorasi (penurunan mutu) produk pangan.
2.8. Accelerated Shelf Life Testing (ASLT)
Metode Accelerated Shelf Life Testing (ASLT) dilakukan dengan cara menyimpan produk pangan pada lingkungan ekstrim, sehingga menyebabkan produk pangan yang disimpan cepat rusak, baik pada suhu atau kelembaban ruang penyimpanan yang lebih tinggi. Salah satu keuntungan metode ASS (Accelerated
Storage Studies) atau metode akselerasi ini adalah waktu yang relatif singkat (3-4
bulan), namun memiliki ketepatan dan akurasi yang tinggi.
Pendekatan metode ASLT dapat dilakukan dengan model kadar air kritis. Menurut Kusnandar (2006) dikutip Nugroho (2007), model kadar air kritis biasanya digunakan untuk produk yang mudah rusak karena penyerapan air dari lingkungan selama penyimpanan. Selain model kadar air kritis, metode ASLT dapat dilakukan dengan model Arrhenius. Model Arrhenius banyak digunakan untuk pendugaan umur simpan bahan pangan yang mudah rusak oleh reaksi kimia, seperti oksidasi lemak, reaksi Maillard, denaturasi protein, serta yang sensitif terhadap suhu (Ristiani, 2014).
Model Arrhenius banyak digunakan oleh industri pangan karena dapat memberikan kerusakan produk pangan secara tepat dengan waktu yang relatif singkat. Model Arrhenius menggunakan teori kinetika yang pada umumnya
menggunakan ordo nol atau satu untuk produk pangan. Model persamaan matematika pada pendekatan kadar air diturunkan dari hukum difusi Fick unidireksional. Terdapat empat model matematika yang sering digunakan, yaitu model Heiss dan Eichner (1971), model Rudolf (1986), model Labuza (1982), dan model paruh waktu (Syarief dan Halid, 1993).
Menurut Syarief dan Halid (1993), dalam penentuan umur simpan, metode Arrhenius sangat baik untuk diterapkan dalam penyimpanan produk pada suhu penyimpanan yang relatif stabil dari waktu ke waktu. Selanjutnya laju penurunan mutu ditentukan dengan persamaan Arrhenius berdasarkan persamaan.
𝐾𝑇 = 𝐴0 . 𝑒−𝐸𝑎/𝑅𝑇 = 𝐴
0 . 𝑒−𝐵/𝑇 Keterangan:
KT = laju reaksi pada suhu T
A0 = konstanta laju kinetik pre-eksponensial Ea = energi aktivasi (Joule/g mol)
R = tetapan gas konstan (8.315 J/g moloK) T = temperature penyimpanan (oK)
B = konstanta eksponensial
Interpretasi Ea (energi aktivasi) dapat memberikan gambaran mengenai besarnya pengaruh temperatur terhadap reaksi. Nilai Ea diperoleh dari slope grafik garis lurus hubungan ln K dengan (1/T). Dengan demikian, energi aktivasi yang besar mempunyai arti bahwa nilai ln K berubah cukup besar dengan hanya perubahan beberapa derajat dari temperatur. Dengan demikian, nilai slope akan besar (Arpah,
2001). Lebih lanjut, besarnya nilai energi aktivasi dapat digolongkan menjadi tiga, yaitu :
1) Kecil (Ea 2-15 kkal/mol), kerusakan produk diakibatkan karena kerusakan karatenoid, klorofil, atau oksidasi asam lemak.
2) Sedang (Ea 15-30 kkal/mol), kerusakan produk diakibatkan karena kerusakan vitamin, kerusakan pigmen yang larut air, dan reaksi Mailard.
3) Besar (Ea 50-100 kkal/mol), kerusakan produk diakibatkan karena denaturasi enzim, inaktivasi mikroba dan sporanya.
Reaksi kimia pada umumnya dipengaruhi oleh suhu. Oleh sebab itu model Arrhenius mensimulasikan percepatan kerusakan produk pada kondisi penyimpanan suhu tinggi di atas suhu penyimpanan normal. Laju reaksi kimia yang dapat memicu kerusakan produk pangan umumnya mengikuti laju reaksi ordo 0 dan ordo 1 (Kusnandar, 2006 dikutip Wahyuningrum, 2010). Laju perubahan A menjadi B pada reaksi ordo 0 dinyatakan sebagai berikut:
𝑑𝐶 𝑑𝑇= 𝑘
dengan mengintegralkan kedua ruas persamaan diatas, diperoleh persamaan sebagai berikut:
𝐶𝑡 = 𝐶0 + 𝐾𝑡 Dimana:
C0 = nilai mutu awal
Ct = nilai mutu pada masa akhir shelf life K = konstanta laju reaksi
Menurut Labuza (1982) dan penelitian Hariyadi dan Andarwulan (2006), tipe kerusakan pangan yang mengikuti model reaksi ordo nol adalah perubahan kadar air; degradasi enzimatis (misalnya pada buah dan sayuran segar serta beberapa pangan beku); reaksi kecoklatan non-enzimatis (misalnya pada biji-bijian kering dan produk susu kering); dan reaksi oksidasi lemak (misalnya peningkatan ketengikan pada
snack, makanan kering dan pangan beku).
Jika pada reaksi ordo nol, persentase penurunan mutu bersifat konstan pada suhu tetap, maka pada reaksi ordo satu penurunan mutu terjadi secara eksponensial. Pada reaksi ordo satu, laju perubahan A menjadi B dinyatakan sebagai berikut:
𝑑𝐶
𝑑𝑇 = 𝐾 𝐶 𝑛
dengan integrasi, diperoleh persamaan sebagai berikut: 𝑙𝑛 𝐶𝑡= ln 𝐶0+ 𝐾𝑇 (𝑡) Dimana:
C0 = nilai mutu yang tersisa setelah waktu t Ct = nilai mutu pada akhir masa shelf life K = konstanta laju reaksi ordo-1 (first order)
Tipe kerusakan bahan pangan yang termasuk dalam rekasi ordo satu diantaranya (1) ketengikan (misalnya pada minyak salad dan sayuran kering); (2) pertumbuhan mikroorganisme (misal pada ikan dan daging, serta kematian mikoorganisme akibat perlakuan panas); (3) produksi off flavor oleh mikroba; (4) kerusakan vitamin dalam makanan kaleng dan makanan kering; dan (5) kehilangan mutu protein (makanan kering) (Labuza, 1982 dan Hariyadi dan Andrawulan, 2006).
Konstanta laju reaksi kimia (k), baik ordo nol maupun ordo satu dapat dipengaruhi oleh suhu. Secara umum reaksi kimia lebih cepat terjadi pada suhu tinggi. Oleh sebab itu konstanta laju reaksi kimia (k) akan semakin besar pada suhu yang lebih tinggi.
Penentuan umur simpan dengan pendekatan Arrhenius dilakukan dalam beberapa tahapan, yaitu penetapan parameter kriteria kadaluarsa, pemilihan jenis dan tipe pengemas, penentuan suhu untuk pengujian, prakiraan waktu dan frekuensi pengambilan contoh, plotting data sesuai ordo reaksi, analisis sesuai suhu penyimpanan, dan analisis pendugaan umur simpan sesuai batas akhir penurunan mutu yang dapat ditolerir (Kusnandar, 2004 dikutip Ristiani, 2014). Menurut Herawati, 2008 dikutip Ramadhani, 2015, penentuan umur simpan dengan AAS perlu mempertimbangkan faktor teknis dan ekonomis dalam distribusi produk yang di dalamnya mencakup keputusan manajemen yang bertanggung jawab.
Perubahan indikator mutu disebabkan adanya pengaruh dari faktor lingkungan, seperti suhu, kelembaban, dan tekanan udara atau karena faktor komposisi produk pangan tersebut. Suhu merupakan faktor yang sangat berpengaruh terhadap perubahan mutu makanan, semakin tinggi suhu penyimpanan maka laju reaksi berbagai senyawa kimia di dalam bahan pangan akan semakin cepat. Oleh karena itu faktor suhu harus selalu diperhitungkan dalam menduga kecepatan penurunan mutu,. Penggunaan suhu inkubasi untuk mengetahui umur simpan produk dapat dilihat pada Tabel 5.
Tabel 5. Suhu Percobaan Penyimpanan (°C) yang Dianjurkan untuk Menguji Masa Kadaluarsa Makanan
Jenis makanan beku Jenis makanan kering – semi basah
Makanan yang diolah secara termal
-40 (kontrol) 0 (kontrol) 5 (kontrol)
-15 Suhu kamar Suhu kamar
-10 30 30
-5 35 35
40 40
45 (jika diperlukan) Sumber : Syarief dan Halid, 1993
Model Q10 merupakan pemanfaatan lebih lanjut dari model Arrhenius. Model ini dipakai untuk menduga berapa besar perubahan laju reaksi oksidasi atau laju penurunan mutu produk makanan jika produk tersebut disimpan pada suhu-suhu tertentu (Ristiani, 2014). Model Q10 dapat digunakan untuk menduga masa kadaluarsa produk makanan tertentu yang disimpan pada berbagai suhu (Syarief dan Halid, 1993). Q10 disebut juga dengan istilah faktor percepatan reaksi yang dirumuskan sebagai berikut: 𝑄10= 𝐾35 𝐾25 = 𝐴0𝑒 −𝐸𝑎/𝑅(𝑇+10) 𝐴0𝑒−𝐸𝑎/𝑅(𝑇)
Model Arrhenius dilakukan dengan menyimpan produk pangan dengan kemasan pada suhu penyimpanan ekstrim. Percobaan dengan metode Arrhenius bertujuan untuk menentukan konstanta laju reaksi (k) pada beberapa suhu penyimpanan ekstrim, yang selanjutnya dilakukan ekstrapolasi untuk menghitung konstanta laju reaksi (k) pada suhu penyimpanan yang diinginkan melalui persamaan Arrhenius. Dari persamaan tersebut dapat ditentukan nilai k (konstanta penurunan
mutu) pada suhu penyimpanan umur simpan, kemudian dihitung umur simpan sesuai dengan ordo reaksinya (Wahyuningrum, 2010).