OPTIMASI KOMPOSISI TWEEN 80 DAN SPAN 80 SEBAGAI EMULSIFYING AGENT DALAM FORMULA EMULGEL ANTI-AGING
EKSTRAK TEH HIJAU (Camellia sinensis (L.) O.K) : APLIKASI DESAIN FAKTORIAL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh : Maria Oktavia NIM : 048114130
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
OPTIMASI KOMPOSISI TWEEN 80 DAN SPAN 80 SEBAGAI EMULSIFYING AGENT DALAM FORMULA EMULGEL ANTI-AGING
EKSTRAK TEH HIJAU (Camellia sinensis (L.) O.K) : APLIKASI DESAIN FAKTORIAL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh : Maria Oktavia NIM : 048114130
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
Skripsi Berjudul
OPTIMASI KOMPOSISI TWEEN 80 DAN SPAN 80 SEBAGAI EMULSIFYING AGENT DALAM FORMULA EMULGEL ANTI-AGING
EKSTRAK TEH HIJAU (Camellia sinensis (L.) O.K) : APLIKASI DESAIN FAKTORIAL
Yang diajukan oleh: Maria Oktavia NIM : 048114130
Telah disetujui oleh:
Pembimbing Utama
TN Saifullah Sulaiman, M.Si., Apt. Tanggal : 7 Agustus 2008
Berjudul
OPTIMASI KOMPOSISI TWEEN 80 DAI{ SPAI\I 80 SEBAGAI EMALSIYNNG AGENT DALAM FORMUL A EMULGEL ANTI.AGING
EKSTRAK TEH HIJATJ (Comellia sinensis (tJ O.K) : APLIKASI DESAIN FAKTORIAL
Oleh : Maria Oktavia NIM: 048114130
Dipertahankan dir hadapan Panitia Penguji Skripsi Fakultas Fprmasi
: Universitas Sanata Dharma pada tanggal : 5 Agustus 2fi18
Firmnri Dtlrma
M-Si,rfuil.
$uhinm,M*Sl,Afr.
Pinifir Fagtji:
l. Tlf. fffulhl Sukium, *I*fi"*F
L Sri Errafi Ynlirni, *I.sL AS
3. *gr$r Bsdi$srirs I.*rL ltil.si.n Apt
HALAMAN PERSEMBAHAN
Aku bersyukur...
Sungguh-sungguh bersyukur...
berterima kasih pada-Mu Tuhan, aku pernah melewati itu
semua
Menjadikan satu kenangan indah...
yang akan membawa ku menjadi lebih baik nantinya,
yang ajarkan aku, betapa sulit mewujudkan impian...
Dan memberi aku arti hidup tak semudah seperti apa
yang diinginkan
Kini...
Didetik bahagia ini, diakhir masa ku disini...
Dengan segala kedewasaan hati,
aku berjanji...
akan ku langkahkan kaki menantang jalan panjang ku nanti
didepan
Aku tak kuasa tuk tetap berdiri saja
karena ini bukan perhentian...
Karena aku adalah aku, yang tak ingin gagal
Karena aku adalah aku, yang memiliki banyak impian...
Tetap melangkah mewujudkan cita-cita...
Kupersembahkan karya kecilku ini untuk : Tuhan Yesus dan Bunda Maria
Keluargaku tercinta Almamaterku
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma : Nama : Maria Oktavia
Nomor Mahasiswa : 048114130
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
OPTIMASI KOMPOSISI TWEEN 80 DAN SPAN 80 SEBAGAI EMULSIFYING AGENT DALAM FORMULA EMULGEL ANTI-AGING
EKSTRAK TEH HIJAU (Camellia sinensis (L.) O.K) : APLIKASI DESAIN FAKTORIAL
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma, hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya. Dibuat di Yogyakarta
Pada tanggal : 12 Agustus 2008
Yang menyatakan,
KATA PENGANTAR
Pujian dan syukur senantiasa penulis haturkan kepada Tuhan Yesus Kristus karena hanya oleh berkat, anugerah, kasih dan pertolongan-Nya penulis dapat menyelesaikan laporan akhir ini guna memenuhi salah satu syarat untuk memperoleh gelar Sarjana Strata Satu Program Studi Ilmu Farmasi (S.Farm).
Selama perkuliahan, penelitian hingga proses penyusunan skripsi, penulis telah mendapat banyak bantuan dari berbagai pihak yang berupa dukungan, sarana, bimbingan, nasihat, kritik dan saran. Pada kesempatan ini, penulis ingin mengucapkan penghargaan dan ucapan terima kasih sebesar-besarnya kepada:
1. Rita Suhadi, M.Si., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. TN Saifullah Sulaiman, M.Si., Apt. selaku dosen pembimbing skripsi yang telah bersedia membimbing dan meluangkan waktunya untuk penulis selama penelitian dengan memberikan bimbingan, dukungan, kritik, dan nasihat. 3. Sri Hartati Yuliani, M.Si., Apt selaku dosen penguji yang telah bersedia
memberikan kritik dan saran selama penyusunan skripsi.
4. Agatha Budi Susiana Lestari, M.Si., Apt. selaku dosen penguji yang telah bersedia memberikan kritik dan saran selama penyusunan skripsi.
5. Bapak, Ibu dan adik-adikku yang selalu memberikan dukungan, motivasi dan doa.
6. Tri Dese Budi Prasetiyo yang selalu menemani, mendukung serta menyemangati penulis selama penelitian dan penulisan skripsi ini.
7. Mbak Ella yang selalu meluangkan waktunya untuk diskusi.
8. Pak Musrifin, Pak Agung, Pak Iswandi, Pak Ottok, Pak Wagiran, Pak Sigit, Pak Sarwanto, dan Pak Yuwono selaku laboran dan karyawan yang telah membantu selama penelitian.
9. Teman-teman 2004 FST & FKK semuanya atas kebersamaan, kenangan, dan persahabatan selama ini (semoga sampai selamanya). Semua teman, sahabat yang tak dapat penulis sebutkan satu persatu, yang telah membantu terselesaikannya skripsi ini.
Penulis menyadari bahwa skripsi ini masih banyak terdapat kesalahan dan kekurangan, oleh karena itu saran dan kritik yang sifatnya membangun sangat penulis harapkam demi kesempurnaan penulisan ini.
Akhirnya penulis berharap semuga skripsi ini bermenfaat bagi pengembangan ilmu farmasi khususnya dan kemajuan ilmu pengetahuan pada umumnya.
Yogyakarta, Juli 2008 Penulis,
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, Juli 2008 Penulis,
Maria Oktavia
INTISARI
Teh hijau mengandung senyawa antioksidan yang dapat menghambat efek penuaan dini. Tujuan dari penelitian ini adalah untuk mengetahui efek tween 80, span 80 dan interaksi keduanya yang dominan dalam menentukan sifat fisik dan kestabilan sediaan emulgel serta untuk mendapatkan area komposisi optimum tween 80 dan span 80 sebagai emulsifying agent dalam formula emulgel
anti-aging ekstrak teh hijau (Camellia sinensis (L.) O.K).
Penelitian ini menggunakan rancangan eksperimental murni dengan variabel eksperimental ganda (desain faktorial) dan teknik analisis statistik Yate’s
treatment dengan taraf kepercayaan 95 %. Optimasi formula emulgel dilakukan
dengan dua variasi level emulsifying agent dengan parameter sifat fisik (daya sebar, viskositas) dan stabilitas emulgel pada penyimpanan (perubahan viskositas, pemisahan fase emulgel). Formula tersebut diuji keamanannya dengan uji iritasi primer pada hewan percobaan kelinci.
Hasil penelitian menunjukkan bahwa span 80 dominan dalam menentukan respon daya sebar dan viskositas emulgel dan tween 80 dominan dalam menentukan respon perubahan viskositas emulgel. Tidak ada faktor yang dominan dalam menentukan pemisahan fase emulgel setelah penyimpanan 1 bulan. Hasil uji iritasi primer menunjukkan emulgel ekstrak teh hijau tidak mengiritasi. Dalam penelitian ini, ditemukan area komposisi optimum emulsifying
agent tween 80-span 80 dalam emulgel anti-aging ekstrak teh hijau.
ABSTRACT
Green tea have an antioxidant compounds which can inhibit the premature aging. The purpose of the research is to investigate the dominant effect among tween 80, span 80 and the interaction between tween 80 and span 80 on the emulgel physical properties and emulgel stability, and to obtain the optimum area of the composition tween 80 and span 80 as emulsifying agent from extract green tea (Camellia sinensis (L.) O.K) emulgel anti-aging formulas.
The research uses a pure experimental design with double experimental variables (factorial design) and Yate’s treatment as analytic statistic technique with 95 % degree of reliability. Optimizing emulgel formula was done by combine two various level of emulsifying agent with parameter on the physical characteristic of emulgel and emulgel stability. The formula safety is tested by primer irritation test to the experiment animal that are rabbits.
The result show that span 80 dominant in determining the spreadability and viscocity of emulgel and tween 80 dominant in determining viscocity moving. There is no dominant factor that influence in separation phase of emulgel after a month storage. The result of primer irritation test showed that emulgel from green tea extract does not irritate. In this research, the optimal compotition area of
emulsifying agent tween 80-span 80 in emulgel extract green tea has been figured
out.
DAFTAR ISI
HALAMAN SAMPUL ... i
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
KATA PENGANTAR ... vi
PERNYATAAN KEASLIAN KARYA ... viii
INTISARI ... ix
ABSTRACT ... x
DAFTAR ISI ... xi
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvii
BAB I. PENDAHULUAN ... 1 A. Latar Belakang ... 1 B. Perumusan Masalah ... 5 C. Keaslian Penelitian ... 5 D. Manfaat Penelitian ... 5 E. Tujuan Penelitian ... 6
BAB II. TINJAUAN PUSTAKA ... 7
B. Kulit ... 10 C. Penuaan dini ……... 13 D. Antioksidan ... 14 E. DPPH ... 15 F. Emulgel ... 16 G. Gelling Agent ... 17 H. Emulsifying Agent ... 18
I. Metode desain faktorial... 20
J. Uji iritasi primer... 22
K. Landasan Teori... 23
L. Hipotesis... 24
BAB III. METODOLOGI PENELITIAN ... 25
A. Jenis Rancangan Penelitian ... 25
B. Variabel dalam Penelitian ... 25
C. Definisi Operasional ... 26
D. Bahan dan Alat ... 28
E. Tata Cara Penelitian ... 29
1. Pemeriksaan ekstrak daun teh hijau …... 29
2. Pemeriksaan katekin.... ... 29
3. Uji aktivitas antioksidan... 30
4. Optimasi formula emulgel... ... 31
F. Analisis Hasil ... 37
BAB IV. HASIL DAN PEMBAHASAN ... 39
A. Identifikasi Ekstrak Teh Hijau... 39
B. Uji Aktivitas Antioksidan Ekstrak Teh Hijau... 42
C. Pembuatan Emulgel Ekstrak Teh Hijau... 46
D. Penentuan Tipe Emulsi Ekstrak Teh Hijau... 48
E. Sifat Fisik dan Stabilitas Emulgel... 50
F. Uji Mikromeritik Gel... 61
G. Uji Iritasi Primer . ... 63
H Optimasi Formula ... 64
BAB V. KESIMPULAN DAN SARAN ... 70
A. Kesimpulan ... 70
B. Saran ... 70
DAFTAR PUSTAKA ... 71
LAMPIRAN ... 74
DAFTAR TABEL
Tabel I. Level rendah dan level tinggi tween 80, level rendah dan level
tinggi span 80... 33
Tabel II. Formula emulgel anti-aging ekstrak teh hijau ... 34
Tabel III. Nilai hRx Ekstrak Teh Hijau... 40
Tabel IV. Hasil Pemeriksaan Ekstrak Teh Hijau... 41
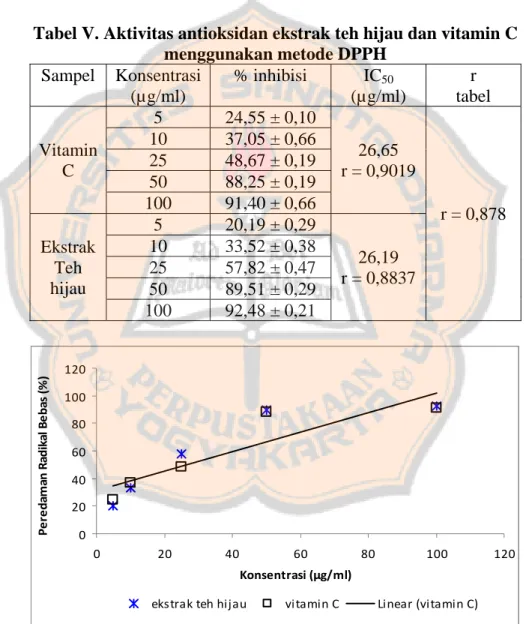
Tabel V. Aktivitas Antioksidan Ekstrak Teh Hijau dan Vitamin C menggunakan Metode DPPH...………… 43
Tabel VI. Nilai HLB Teoritis Emulgel... ... 46
Tabel VII. Hasil Uji pH Emulgel Anti-Aging Ekstrak Teh Hijau ... 47
Tabel VIII. Hasil Pengukuran Sifat Fisik dan Stabilitas Emulgel... 52
Tabel IX. Efek Tween 80, Span 80 dan Interaksi dalam Menentukan Sifat Fisik dan Stabilitas Emulgel... 53
Tabel X. Hasil perhitungan Yate’s treatment pada respon daya sebar emulgel... 55
Tabel XI. Hasil perhitungan Yate’s treatment pada respon viskositas emulgel... 57
Tabel XII. Hasil perhitungan Yate’s treatment pada respon perubahan viskositas emulgel... 59 Tabel XIII. Hasil perhitungan Yate’s treatment pada respon stabilitas fase emulgel... 61
Tabel XIV. Hasil Pengukuran Tetesan Minyak dalam Emulgel... 61
Tabel XV. Hasil Pengukuran Indeks Iritasi Primer dan Sifat Iritannya... 63
DAFTAR GAMBAR
Gambar 1. Struktur Kulit... ... 11 Gambar 2. Mekanisme Reaksi antara DPPH dengan antioksidan... 16 Gambar 3. Lempeng KLT diamati dengan sinar biasa dan sinar
UV... 39 Gambar 4. Spektrum perbandingan panjang gelombang antara ekstrak teh
hijau dengan katekin... ... 42 Gambar 5. Kurva hubungan antara konsentrasi (µg/ml) dengan peredaman
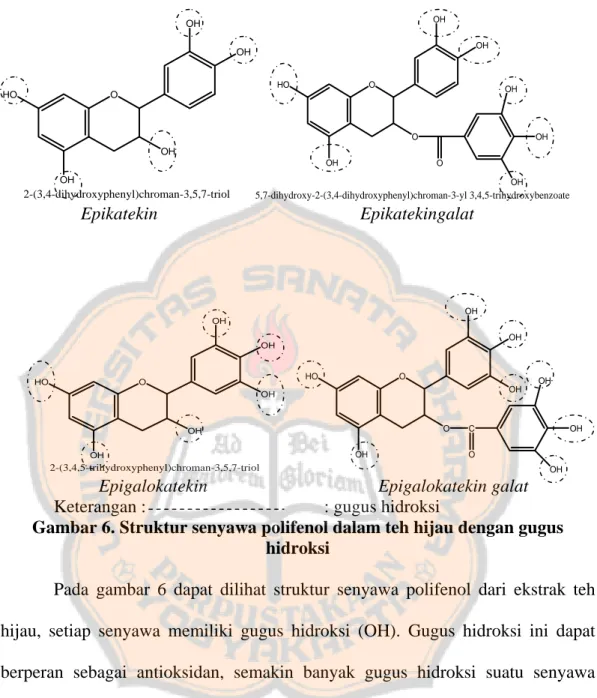
radikal bebas (%) pada vitamin C dan ekstrak teh hijau……... 43 Gambar 6. Struktur senyawa polifenol dalam teh hijau dengan gugus
hidroksi ... 45 Gambar 7. Gambar penampilan fisik emulgel setelah ditambah dengan fase
eksternal berlebih... 48 Gambar 8. Gambar emulgel setelah ditambah dengan zat warna methylene
blue………... 49
Gambar 9. Gambar emulgel dibawah mikroskop setelah ditambah dengan zat warna methylene blue ………... 50 Gambar 10. Grafik hubungan antara daya sebar-tween 80 dan grafik
hubungan antara daya sebar-span 80…... 54 Gambar 11. Grafik hubungan antara viskositas-tween 80 dan grafik hubungan
antara viskositas-span 80………... ... 56 Gambar 12. Grafik hubungan antara perubahan viskositas-tween 80 dan grafik
hubungan antara perubahan viskositas-span 80 ... 58 Gambar 13. Grafik hubungan antara pemisahan fase emulgel-tween 80 dan
grafik hubungan antara pemisahan fase emulgel-span 80... 60 Gambar 14. Grafik distribusi ukuran tetesan minyak dalam emulgel... 62
Gambar 15. Contour plot daya sebar emulgel... 65
Gambar 16. Contour plot viskositas emulgel... 66
Gambar 17. Contour plot perubahan viskositas emulgel... 67
Gambar 18. Contour plot pemisahan fase emulgel... 68
DAFTAR LAMPIRAN
Lampiran 1. Uji aktivitas antioksidan... 74
Lampiran 2. Data Sifat fisik dan stabilitas sediaan emulgel... 76
Lampiran 3. Perhitungan Perhitungan Yate’s treatment……... 89
Lampiran 4. Data uji mikromeritik... ... 99
Lampiran 5. Data uji iritasi primer... ... 101
Lampiran 6. Kuisioner subjective assessment... 102
Lampiran 7. Perhitungan subjective assessment... 103
Lampiran 8. Foto dokumentasi……… ...……... 107
BAB I
A. LATAR BELAKANG
Teh merupakan minuman yang paling populer di dunia. Posisinya berada pada urutan kedua setelah air mineral. Diperkirakan tidak kurang dari 120 ml setiap harinya, teh dikonsumsi setiap orang. Teh hijau memiliki khasiat yang lebih baik dibandingkan teh hitam untuk perawatan kesehatan dan kecantikan. Berbagai penelitian menunjukkan teh hijau bermanfaat untuk mencegah kanker, osteoporosis, kardiovaskular, aterosklerosis, menyembuhkan penyakit ginjal dan meningkatkan kekebalan tubuh. Sementara untuk perawatan kecantikan teh hijau berperan sebagai antioksidan untuk mencegah penuaan dini, menghilangkan bau mulut hingga sebagai obat pelangsing (Soraya, 2007). Berdasarkan hasil penelitian-penelitian tersebut, kini ekstrak teh hijau telah banyak digunakan dalam berbagai produk perawatan kecantikan, seperti facial foam, lotion, obat pelangsing dan lulur.
Teh hijau mengandung senyawa polifenol berupa katekin yang memberikan aktivitas antioksidan sehingga dapat mengurangi kerusakan sel dan proses penuaan dini menjadi lebih lambat (Syah, 2006). Kandungan polifenol dalam teh hijau antara lain adalah epikatekin, epikatekin galat, epigalokatekin dan
epigalokatekin galat. Menurut penelitian, kandungan zat antioksidan teh hijau 100
kali lebih efektif dari vitamin C dan 25 kali dari vitamin E yang juga merupakan antioksidan potensial sebagai penyegar kulit dan mengatur keseimbangan radikal bebas (Soraya, 2007).
Aktivitas antioksidan dari teh hijau dapat membantu mengontrol aktivitas radikal bebas, yakni zat berbahaya yang sangat reaktif dan bersifat merusak jaringan organ-organ tubuh hingga menimbulkan berbagai penyakit. Salah satu efek dari radikal bebas adalah penuaan dini. Manusia akan mengalami proses penuaan. Proses penuaan ini antara lain tampak dari kerutan dan keriput pada kulit atau kemunduran lainnya dibanding ketika masih muda. Sebagian besar garis-garis wajah dan kerut atau keriput disebabkan oleh pemaparan berlebihan terhadap sinar UV, baik UVA yang bertanggung jawab atas noda gelap, kerut atau keriput dan melanoma maupun UVB yang bertanggung jawab atas kulit terbakar serta karsinoma (Anonim, 2008a). Dalam tubuh sebenarnya ada enzim yang dapat menangkal radikal bebas, akan tetapi reaksi enzimatik ini tidak pernah mencapai 100%. Akibat dari kerusakan jaringan ini secara perlahan menyebabkan elastisitas kolagen merosot dan kulit menjadi keriput dan timbul bintik-bintik pigmen kecoklatan (Kumalaningsih, 2006).
Dengan adanya antioksidan proses penuaan dini serta kerusakan organ tubuh dan risiko terserang berbagai penyakit diusia tua dapat dicegah. Penuaan dini dapat dihambat dengan menggunakan 3 gram daun teh hijau yang diseduh dengan 150 ml air mendidih, didiamkan dalam keadaan tertutup sampai dingin dan disaring kemudian digunakan untuk membasuh wajah (Mursito, 2000). Cara-cara tersebut dirasakan kurang praktis, khususnya bagi masyarakat yang memiliki aktifitas cukup padat, karena itu dibuat suatu sediaan topikal yang dirancang untuk penggunaan lokal pada kulit secara lebih praktis dan lebih efektif yaitu
emulgel. Ekstrak teh hijau juga dapat digunakan sebagai anti penuaan dini dengan
konsentrasi 5-10% (Anonim, 2002).
Emulgel adalah sediaan yang dibuat dengan mencampurkan emulsi baik
berupa tipe minyak dalam air maupun berupa tipe air dalam minyak dan gelling
agent sebagai pembentuk gel dengan konsentrasi tertentu. Emulgel juga telah
digunakan sebagai penghantar obat ke dalam jaringan kulit (Magdy, 2004). Gel mempunyai kelebihan berupa kandungan air yang cukup tinggi sehingga memberikan kelembapan yang bersifat mendinginkan dan memberikan rasa nyaman pada kulit (Mitsui, 1997).
Emulsi mempunyai kelebihan berupa kemampuan penetrasi yang tinggi pada kulit. Emulsi minyak dalam air lebih banyak digunakan sebagai basis obat yang dapat tercuci dengan air untuk tujuan kosmetik. Emulsi air dalam minyak lebih dapat digunakan untuk perawatan kulit kering dan pemakaian sebagai emolien (Magdy, 2004). Atas dasar kelebihan dari emulsi dan gel tersebut maka dibuat sediaan emulgel dari ekstrak teh hijau yang dapat berfungsi sebagai pencegah proses penuaan dini.
Pada sediaan emulgel terdapat sistem gel dan sistem emulsi, dimana dalam penelitian ini digunakan hidroksipropilmetilselulosa (HPMC) sebagai
gelling agent, tween 80 dan span 80 sebagai emulsifying agent. Gelling agent
untuk kebutuhan farmasi dan sediaan kosmetik harus inert, aman dan tidak reaktif dengan komponen lain (Zath and Kushla, 1996). Tween 80 merupakan
emulsifying agent larut air yang digunakan dalam sediaan kosmetik, yang
merupakan emulsifying agent nonionik dengan HLB 4,3 karena gugus lipofilnya lebih dominan. Dalam interfacial film theory, adanya stable interfacial complex
condensed film yang terbentuk saat emulsifying agent yang bersifat larut air
dicampurkan dengan emulsifying agent yang bersifat larut lemak mampu membentuk dan mempertahankan emulsi dengan lebih efektif dibandingkan penggunaan emulsifying agent tunggal (Zats and Kushla, 1996). Emulsifying
agent akan mempengaruhi sifat fisik dan kestabilan sistem emulsi sehingga harus
diperhatikan sebelum sediaan dipasarkan kekonsumen. Suatu sediaan layak untuk digunakan oleh masyarakat apabila memenuhi syarat keamanan. Oleh karena itu selain optimasi, dalam penelitian ini juga dilakukan uji iritasi primer sebagai uji awal untuk mengetahui tingkat keamanannya.
Desain faktorial merupakan metode rasional untuk menyimpulkan dan mengevaluasi secara obyektif efek dari faktor-faktor yang berpengaruh terhadap kualitas produk. Dengan metode ini dapat diketahui efek yang dominan antara tween 80, span 80 dan interaksi keduanya dalam menentukan respon yang diharapkan. Selain untuk menentukan efek yang dominan, desain faktorial juga dapat digunakan untuk memperoleh sediaan dengan formula optimum. Komposisi tween 80 dan span 80 sebagai emulsifying agent dioptimasi dengan metode desain faktorial ini. Diharapkan dengan komposisi tween 80 dan span 80 yang optimum, diperoleh sediaan emulgel yang memenuhi kualitas fisik yang baik meliputi daya sebar, viskositas dan stabilitas fisik sehingga dapat diterima oleh masyarakat.
1. PERUMUSAN MASALAH
• Di antara tween 80, span 80 dan interaksi keduanya, mana yang lebih dominan dalam menentukan sifat fisik dan stabilitas emulgel anti-aging ekstrak teh hijau?
• Dapatkah ditemukan area komposisi optimum tween 80 dan span 80 pada
contour plot superimposed yang diprediksikan sebagai formula optimum emulgel anti- aging ekstrak teh hijau?
• Apakah formula emulgel anti-aging ekstrak teh hijau memberikan efek iritasi primer?
2. KEASLIAN KARYA
Sejauh penelusuran pustaka yang dilakukan oleh penulis, penelitian tentang optimasi komposisi tween 80 dan span 80 sebagai emulsifying agent dalam formula emulgel anti-aging ekstrak teh hijau (Camellia sinensis (L.) O.K) : aplikasi desain faktorial belum pernah dilakukan.
3. MANFAAT PENELITIAN a. Manfaat teoritis
Menambah pengetahuan tentang bentuk sediaan emulgel yang berasal dari bahan alam.
b. Manfaat metodologis
Menambah ilmu pengetahuan dalam bidang kefarmasian mengenai penggunaan metode desain faktorial.
c. Manfaat praktis
Manfaat praktis penelitian ini adalah dapat menghasilkan komposisi tween 80 dan span 80 yang optimal sehingga diperoleh sediaan yang berkhasiat, aman dan dapat diterima oleh masyarakat.
B. TUJUAN PENELITIAN
a. Tujuan umum
Penelitian ini secara umum bertujuan untuk mendapatkan formula dengan komposisi tween 80 dan span 80 yang optimum sebagai emulsifying agent dalam emulgel anti-aging ekstrak teh hijau (Camellia sinensis (L)), yang memenuhi persyaratan mutu yakni, berkhasiat, aman dan dapat diterima oleh masyarakat.
b. Tujuan khusus
Secara khusus tujuan penelitian ini adalah :
• Mengetahui manakah yang dominan antara tween 80, span 80 dan interaksi keduanya dalam menentukan sifat fisik dan stabilitas emulgel. • Menemukan area komposisi optimum tween 80 – span 80 pada contour
plot superimposed yang diprediksikan sebagai formula optimum emulgel anti-aging ekstrak teh hijau.
• Mengetahui apakah formula emulgel anti-aging ekstrak teh hijau memberikan efek iritasi primer atau sebaliknya, tidak memberikan efek iritasi primer.
BAB II
PENELAAHAN PUSTAKA A. Teh
Sinonim : Camellia bohea Griff, C. sinensis (L) O.K., C. theifera Dyer.,
Thea sinensis L,. T. asamica Mast, T. cochinchinensis Lour., T. cantoniensis Lour., T. chinensis Sims., T. viridis L.
Klasifikasi
Devisi : Spermathophyta (tumbuhan biji) Sub devisi : Angiospermae (tumbuhan biji terbuka) Kelas : Dicotyledoneae (tumbuhan biji belah) Sub kelas : Guttiferales (Clusiales)
Familia (suku) : Camelliaceae (Theaceae) Genus (marga) : Camellia
Spesies : Camellia sinensis
Varietas : Assamica (Tuminah, 2004).
1. Klasifikasi teh
Teh dapat dikelompokkan dalam tiga jenis berdasarkan pengolahannya, yaitu teh hijau (tidak difermentasi), teh oolong dan teh
pouchong (semifermentasi), dan teh hitam (fermentasi penuh) (Syah, 2006).
Teh hijau dibuat melalui inaktivasi enzim polifenol oksidasenya di dalam daun teh segar. Metode inaktivasi enzim polifenol oksidase teh hijau dapat dilakukan melalui pemanasan (udara panas) yaitu memanaskan daun
yang sudah kering dan penguapan (steam /uap air) dimana daun teh segar yang masih baru dipetik diuapkan sebentar kemudian dikeringkan. Kedua metode ini berguna untuk mencegah tejadinya oksidasi enzimatis katekin (Syah, 2006).
Teh hitam dibuat dengan cara memfermentasikan daun teh, yang sebelumnya sedikit dikeringkan dengan udara hangat, dilayukan dan digiling di bawah pengaruh panas yaitu melalui oksidase katekin dalam daun segar dengan katalis polifenol oksidase atau yang disebut dengan fermentasi. Proses fermentasi ini dihasilkan dalam oksidasi polifenol sederhana, yaitu katekin teh diubah menjadi molekul yang lebih kompleks dan pekat sehingga memberi ciri khas teh hitam, yaitu berwana kuat dan tajam (Syah, 2006).
Teh oolong diproses melalui pemanasan daun dalam waktu singkat setelah penggulungan, oksidasi terhenti dalam proses pemanasan, sehingga teh
oolong disebut dengan teh semifermentasi. Karakteristik teh oolong berada
diantara teh hitam dan teh hijau (Syah, 2006).
2. Kandungan kimia a. Substansi fenol
1) Katekin (polifenol)
Katekin merupakan senyawa dominan dari polifenol teh hijau yang merupakan senyawa larut dalam air, tidak berwarna dan memberikan rasa pahit, tidak bersifat menyamak dan tidak berpengaruh buruk terhadap pencernaan makanan, katekin teh bersifat antimikroba (bakteri, virus), antioksidan, antiradiasi, memperkuat pembuluh darah,
melancarkan sekresi air seni dan menghambat pertumbuhan sel kanker (Fulder, 2004).
Katekin dibagi menjadi dua kelompok utama yaitu proantocyanidin dan polyester. Katekin teh hijau tersusun sebagian besar atas senyawa-senyawa katekin, epikatekin, galokatekin, epigalokatekin, galokatekin galat dan epigalokatekin galat (Syah, 2006). Kandungan teh hijau bervariasi menurut cara pengolahannya. Kandungan katekin tertinggi ada pada teh hijau, disusul teh oolong, dan teh hitam. Teh hijau mengandung 16-30 % senyawa katekin.
2) Flavanol
Flavanol dalam teh meliputi quersetin, kaemferol, dan mirisetin. Flavanol merupakan antioksidan alami yang mampu mengikat logam.
b. Substansi bukan fenol
Substansi bukan fenol terdiri dari: 4 % karbohidrat, 6 % substansi pektin, 3-4 % alkaloid seperti teofilin (1,3-dimetil xantin), teobromin (3,7-dimetil xantin) dan kafein (1,3,7-trimetil xantin). Kafein dapat berfungsi sebagai stimulan pada sistem CNS (Central Nervous System) dalam sistem respiratori dan jantung). Kandungan teh hijau lainnya adalah klorofil dan zat warna lain, protein dan asam-asam amino, asam organik substansi resin, vitamin, substansi mineral.
c. Substansi penyebab aroma
Beberapa pendapat menyatakan bahwa aroma teh berasal dari glikosida yang terurai menjadi gula sederhana dan senyawa beraroma. Pendapat lain mengatakan aroma berasal dari oksidasi karotenoid yang menghasilkan senyawa mudah menguap (aldehid dan keton tidak jenuh) (Syah, 2006).
d. Enzim
Beberapa enzim terdapat dalam daun teh. Peranan penting enzim-enzim ini adalah sebagai biokatalisator pada setiap reaksi kimia dalam tanaman. Enzim yang dikandung dalam daun teh diantaranya invertase, amilase, β-glukosidase, oximetilase, protease dan peroksidase (Syah, 2006).
B. Kulit
Kulit merupakan organ terluas yang menutupi seluruh permukaan tubuh. Kulit berfungsi sebagai pelindung tubuh dari pengaruh luar baik secara fisik maupun imunologik. Kulit juga berperan penting dalam interaksi antar individu dengan lingkungan, karena merupakan indera yang sensitif terhadap sentuhan yang kadang membuat perasaan emosional (Rawling, 2002). Kulit memiliki kekakuan yang bervariasi di setiap bagian yang berbeda. Daerah yang paling kaku dan tebal adalah telapak kaki dan telapak tangan serta sela-sela jari. Kulit menjadi lebih tipis dan berkeriput pada usia tua dan kelihatan kekuningan bahkan
keabu-abuan, sering disebut penuaan kulit. Pada kulit wajah, sel-selnya sangat tipis, sehingga memungkinkan sediaan kosmetik dapat berpenetrasi (Young, 1972).
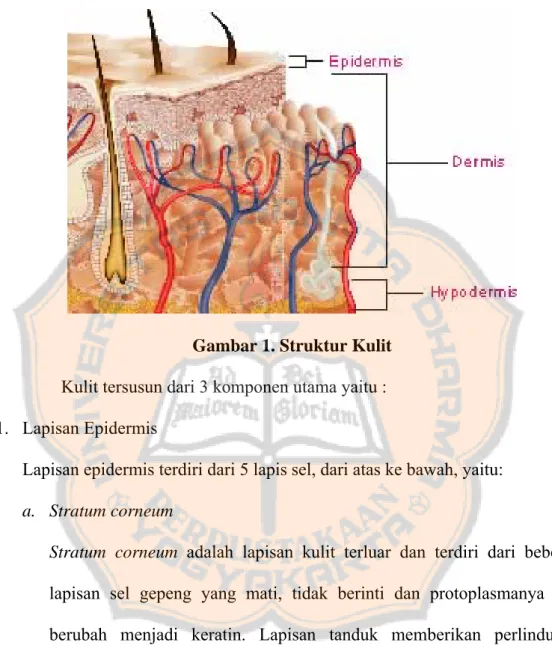
Gambar 1. Struktur Kulit Kulit tersusun dari 3 komponen utama yaitu : 1. Lapisan Epidermis
Lapisan epidermis terdiri dari 5 lapis sel, dari atas ke bawah, yaitu:
a. Stratum corneum
Stratum corneum adalah lapisan kulit terluar dan terdiri dari beberapa
lapisan sel gepeng yang mati, tidak berinti dan protoplasmanya telah berubah menjadi keratin. Lapisan tanduk memberikan perlindungan terhadap cahaya, panas bakteri dan berbagai bahan kimia.
b. Stratum lucidum
Lapisan ini merupakan sel gepeng, jernih dan sel mati yang berisi eleidin, eleidin dibentuk dari keratohialin dan akan berubah menjasi keratin.
c. Stratum granulosum
Lapisan ini terdiri dari 3-5 lapis sel gepeng yang berisi butiran berwarna gelap yang disebut keratohialin. Keratohialin ikut serta dalam langkah pembentukan keratin.
d. Stratum spinosum
Lapisan ini terdiri dari 8-10 lapis sel poligonal yang sangat rapat. Protoplasmanya jernih karena banyak mengandung glikogen dan inti sel terletak ditengah.
e. Stratum basale atau stratum germinativum
Stratum basale merupakan lapisan terdalam dalam epidermis. Lapisan ini
terdiri dari satu lapis sel kubus. Pada saat pembelahan sel, sel-sel ini akan bergerak maju kepermukaan menjadi lapisan-lapisan yang diatasnya. Inti selnya akan mengalami degenerasi dan selnya akan mati. Sel-sel ini akan menggantikan sel-sel yang ada pada bagian paling atas epidermis.
2. Lapisan Dermis
Dermis terdiri dari jaringan connective yang berisi serabut kolagen dan serabut
elastin. Ruang diantara serabut tersebut berisi jaringan adiposa, folikel rambut, saraf, kelenjar lemak dan kelenjar keringat.
Lapisan ini terdiri dari:
a. Pars papilaris terdiri dari jaringan connective yang berisi serabut elastis, ujung serabut saraf dan pembuluh darah.
b. Pars retikularis adalah bagian bawah dermis yang berhubungan dengan lapisan sub kutis. Bagian ini terdiri dari jaringan connective yang padat yang berisi serabut kolagen dan serabut elastis.
3. Lapisan Subkutis
Lapisan ini terdiri dari jaringan ikat longgar dengan isi sel lemak. Di lapisan ini terdapat ujung saraf tepi, pembuluh darah dan saluran getah bening (Tortora, 1990).
C. Penuaan dini
Kulit berubah mengikuti usia seseorang. Walaupun proses penuaan tidak dapat dihindari, pemahaman tentang proses penuaan yang terjadi di kulit sangat penting. Paparan sinar matahari dipercaya akan mempercepat proses perubahan kulit. Penuaan akan dapat dipercepat lagi oleh radikal bebas yang berada di sekitar kita. Proses penuaan kulit disebabkan oleh dua faktor, yaitu faktor instrinsik dan faktor ekstrinsik. Penuaan kulit karena faktor ekstrinsik terjadi akibat adanya faktor luar seperti sinar matahari, merokok, konsumsi alkohol yang berlebihan dan kekurangan nutrisi sedangkan faktor intrinsik dilatarbelakangi faktor genetik dari individu dan diakibatkan dari usia yang tidak dapat dihindari. Proses penuaan kulit yang disebabkan oleh faktor ekstrinsik dapat menyebabkan penuaan dini. Kelainan yang terjadi pada penuaan dini berupa kulit kering, kulit berkerut, muncul noda-noda hitam pada kulit, kulit kusam, dan tidak bercahaya. Hal ini terjadi karena adanya radikal bebas (Hermani, 2005).
Diantara tanda-tanda penuan kulit yang dapat terlihat, yaitu kulit terlihat kering, kasar, kendur dan kehilangan elastisitasnya, terdapat bercak atau noda coklat kehitaman, keriput, adanya regangan kulit, timbul lipatan pada leher, dan garis-garis ketuaan di wajah (Baumann, 2002).
D. Antioksidan
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya secara cuma-cuma kepada molekul radikal bebas tanpa terganggu sama sekali dan dapat merusak reaksi berantai dari radikal bebas (Hudson, 1990).
Atas dasar fungsinya, antioksidan dapat dibedakan menjadi lima seperti berikut :
1. Antioksidan primer yang bekerja dengan cara mencegah terbentuknya radikal bebas yang baru dan mengubah radikal bebas menjadi molekul yang tidak merugikan. Sebagian besar zat fenolik, tiokoferol, alkil galat, BHA, BHT dan glutation peroksidase.
2. Antioksidan sekunder yang berfungsi untuk menangkap radikal bebas dan menghalangi terjadinya reaksi berantai, misalnya vitamin C, Vitamin E, beta karoten.
3. Antioksidan tersier yang bermanfaat untuk memperbaiki kerusakan yang disebabkan oleh radikal bebas misalnya enzim metionin sulfoksidan reduktase yang dapat memperbaiki DNA dalam inti sel.
4. Oxygen scavenger, antioksidan yang dapat mengikat oksigen sehingga tidak mendukung reaksi oksidasi, misalnya vitamin C.
5. Chelators, kerjanya mengikat logam yang mampu mengkatalisis rekasi oksidasi, misalnya asam sitrat asam amino, ethylendiamin (Kumalaningsih, 2006).
E. DPPH ( 1,1-difenil-2-pikrilhidrasil )
Aktivitas antioksidan suatu senyawa dapat diukur dengan kemampuan meredam radikal bebas. Dalam penelitian ini radikal bebas yang digunakan adalah DPPH (1,1-difenil-2-pikrilhidrasil atau α,α-difenil-β-pikrilhidrasi). DPPH adalah merupakan suatu senyawa radikal bebas yang stabil. Prinsipnya adalah reaksi penangkapan hidrogen dari antioksidan oleh radikal bebas DPPH yang berwarna ungu dan berubah menjadi 1,1-difenil-2-pikrilhidrazin yang berwarna kuning stabil. Sebaliknya senyawa DPPH kehilangan H akan menjadi radikal baru yang reaktif. Suatu senyawa dapat digunakan sebagai radikal bebas yang bermanfaat, apabila setelah bereaksi dengan radikal bebas akan menghasilkan radikal baru yang stabil atau senyawa bukan radikal (Molyneux, 2004).
Antioksidan dinyatakan aktif bila menghambat radikal bebas lebih dari 80 %, dinyatakan sedang bila menghambat radikal bebas 50-80 % dan dinyatakan tidak aktif bila menghambat radikal bebas kurang dari 50 % (Yen, 1995).
Reaksi antara DPPH sebagai radikal bebas dengan antioksidan:
1,1-difenil-2-pikrilhidrazil antioksidan 1,1-difenil-2-pikrilhidrazin Gambar 2. Mekanisme reaksi antara DPPH dengan antioksidan
Nilai IC50 (Inhibiton Concentration 50) adalah konsentrasi antioksidan (μg/ml) yang mampu menghambat 50 % radikal bebas. Nilai IC50 diperoleh dari perpotongan garis antara 50 % daya hambatan dengan sumbu konsentrasi, kemudian dimasukkan ke persamaan Y = a + bx dimana Y = 50 dan nilai X menunjukkan IC50 (Yen, 1995).
F. Emulgel
Emulgel dibuat dengan mencampurkan emulsi dengan perbandingan
tertentu. Syarat sediaan emulgel sama seperti syarat untuk sediaan gel, yaitu untuk penggunaan dermatologi harus mempunyai syarat antara lain sebagai berikut : tiksotropik, mempunyai daya sebar yang mudah melembutkan, dapat bercampur dengan beberapa zat tambahan (Magdy, 2004).
Pembuatan emulgel dilakukan dengan cara mencampurkan emulsi dan gel dengan perbandingan tertentu. Bahan tambahan yang biasa digunakan dalam pembuatan emulgel adalah gelling agent yang dapat meningkatkan viskositas,
O2N NO2 N NO 2 N O2N + A • NO2 H N + AH NO2 N
emulsifying agent untuk menghasilkan emulsi yang stabil, humektan dan
pengawet.
Uji stabilitas merupakan proses evaluasi untuk menjamin bahwa sifat-sifat utama produk tidak berubah selama waktu yang dapat diterima oleh konsumen. Ketidakstabilan dapat dilihat dengan mengevaluasi karakteristik produk, baik dengan pengamatan secara subyektif maupun obyektif. Pengamatan secara subyektif misalnya dengan mengamati warna, bau dan penampilan produk, sedangkan pengamatan obyektif misalnya dengan mengukur pH, daya sebar, viskositas, ukuran partikel, dan lain-lain (Wilkinson, 1982).
G. Gelling Agent
Gel merupakan suatu sistem setengah padat yang terdiri dari suatu dispersi yang tersusun baik dari partikel anorganik yang kecil atau molekul organik yang besar dan saling diresapi cairan (Ansel, 1999). Gel pada umumnya memiliki sifat rheologi pseudoplastik (Nairn, 1997). Gel biasanya digunakan untuk diaplikasikan pada membran mukus atau jaringan yang luka atau terbakar karena gel memiliki kandingan air yang tinggi yang dapat mengurangi iritasi (Klech, 1986).
Hidrogel adalah sediaan semisolid yang mengandung material polimer yang mempunyai kemampuan untuk mengembang dalam air tanpa larut dan bisa menyimpan air dalam strukturnya. Hidrogel merupakan sistem yang menyebabkan air tidak bisa bergerak karena adanya polimer tidak larut. Salah satu alasan disukainya hidrogel sebagai komponen dari sistem penghantaran dan pelepasan
obat adalah kompatibilitasnya yang relatif baik dengan jaringan biologis. Polimer yang digunakan dalam hidrogel terhidrolisis lambat dan secara bertahap melepaskan obat bebas. Kelebihan hidrogel yaitu aman digunakan secara topikal, transparan, licin, mudah digunakan, memberikan rasa dingin karena ada penguapan air serta residunya mudah dihilangkan (Zatz and Kushla, 1996). Hidrogel merupakan polimer organik seperti asam poliakrilik (carbomer), CMC-Na dan selulosa eter non ionik (hidroksipropilmetilselulosa (HPMC)) sering digunakan sebagai basis untuk tujuan pembuatan hidrogel (Barel et al, 2001). HPMC tidak larut dalam alkohol, pembentukan gel dilakukan dengan pemanasan pada suhu 50-90oC dan stabil pada pH 3-11.
H. Emulsifying Agent
Emulsifying agent adalah surfaktan yang mengurangi tegangan antar
muka antara minyak dan air, meminimalkan energi permukaan dari droplet yang terbentuk (Allen, 2002).
Emulsifying agent bekerja dengan membentuk film atau lapisan di
sekeliling butir-butir tetesan yang terdispersi dan film ini berfungsi agar mencegah terjadinya koalesen dan terpisahnya cairan dispers sebagai fase terpisah (Anief, 2003).
Penggunaan campuran dua macam emulsifying agent biasanya lebih stabil dibanding penggunaan emulsifying agent tunggal dengan menjumlahkan HLB secara langsung. Emulsifying agent dapat dicampurkan dengan perbandingan dan proporsi yang sesuai (Allen, 2002).
a) Tween 80
Tween 80 digunakan sebagai emulsifying agent pada emulsi topikal tipe minyak dalam air, dikombinasikan dengan emulsifier hidrofilik pada emulsi minyak dalam air, dan untuk menaikkan kemampuan menahan air pada salep, dengan konsentrasi 1-15%. Tween 80 digunakan secara luas pada kosmetik sebagai emulsifying agent (Smolinske, 1992). Tween 80 merupakan ester oleat dari sorbitol di mana tiap molekul anhidrida sorbitolnyanya berkopolimerisasi dengan 20 molekul etilenoksida (anhidrida sorbitol : etilenoksida = 1:20). Tween 80 berupa cairan kental berwarna kuning muda sampai kuning sawo (Anonim, 1993), berbau karamel yang dapat menyebabkan pusing (Greenberg, 1954), panas dan kadang-kadang pahit (Anonim, 1993). Tween 80 sangat larut dalam air, larut dalam etanol (95%) P dan etilasetat P, tidak larut dalam parafin cair P (Anonim, 1993), tidak larut dalam alkohol polihidrik (Greenberg, 1954). Tween 80 mempunyai titik lebur yang berada pada suhu 5°-6°C, nilai pH 6,0-8,0 dan stabil dalam larutan dengan pH 2-12 (Greenberg, 1954).
b) Span 80
Span 80 mempunyai nama lain sorbitan monooleat. Pemeriannya berupa warna kuning gading, cairan seperti minyak kental, bau khas tajam, terasa lunak. Kelarutannya tidak larut tetapi terdispersi dalam air, bercampur dengan alkohol, tidak larut dalam propilenglikol, larut dalam hampir semua minyak mineral dan nabati, sedikit larut dalam eter. Berat jenis pada 20oC adalah 1 gram. Nilai HLB 4,3. Viskositas pada 25oC adalah 1000 cps.
Span 80 dapat disiapkan dari campuran sorbitol terester sebagian dengan mono dan dianhidrida asam oleat. Digunakan dengan cara sama seperti ester sorbitan, seperti span 20 tetapi lebih lipofilik dari span 20, berguna untuk membuat krim tipe A/M, bagian kecil dari tween 60 atau tween 80 dapat ditambahkan untuk mengurangi viskositas dan membantu pembentukan emulsi, sehingga tidak perlu menggunakan homogenizer sampai konsistensinya 10%, dapat dimasukkan dalam basis tipe parafin untuk membentuk basis tipe anhidrat yang mampu menyerap sejumlah besar air (Anonim, 1988).
I. Metode Desain Faktorial
Desain faktorial adalah pendekatan eksperimental kuno yang dilakukan dengan meneliti efek dari suatu variebel eksperimental dengan menjaga variabel lain konstan. Desain faktorial digunakan dalam percobaan untuk menentukan secara simulasi efek dari beberapa faktor dan interaksinya yang signifikan. Signifikan berarti perubahan dari level rendah ke level tinggi pada faktor – faktor menyebabkan perubahan besar pada responnya (Bolton, 1990)
Perencanaan percobaan faktorial (factorial design) merupakan suatu metode rasional untuk menyimpulkan dan mengevaluasi secara obyektif efek dari besaran yang berpengaruh terhadap kualitas produk (Voigt, 1994)
Desain faktorial mengandung beberapa pengertian, yaitu faktor, level, efek, respon. Faktor merupakan setiap besaran yang mempengaruhi respon. (Voigt, 1994). Level merupakan nilai atau tetapan untuk faktor. Efek adalah
perubahan respon yang disebabkan variasi tingkat dari faktor. Efek faktor atau interaksi merupakan rata – rata respon pada level tinggi dikurangi rata – rata respon pada level rendah. Respon merupakan sifat atau hasil percobaan yang diamati. Respon yang diamati harus dikuantitatifkan (Bolton, 1990).
Desain faktorial dua level berarti ada dua faktor (misal A dan B) yang masing-masing faktor diuji pada dua level yang berbeda, yaitu level rendah dan level tinggi. Dengan desain faktorial dapat didesain suatu percobaan untuk mengetahui faktor dominan yang berpengaruh secara signifikan terhadap suatu respon. Desain faktorial dengan dua faktor dalam suatu percobaan memberikan pertanyaan sebagai berikut :
1. Apakah faktor A memiliki pengaruh yang signifikan terhadap suatu respon? 2. Apakah faktor B memiliki pengaruh yang signifikan terhadap suatu respon? 3. Apakah interaksi faktor A dan B memiliki pengaruh yang signifikan terhadap
suatu respon? (Bolton, 1990)
Desain faktorial merupakan pilihan aplikasi persamaan regresi, yaitu teknik untuk memberikan model hubungan antara variabel respon dengan satu atau lebih variabel bebas. model yang dipilih dari analisis tersebut adalah model matematika (Bolton, 1990).
Jumlah percobaan dalam desain faktorial adalah 2n, 2 menunjukkan level dan n menunjukkan jumlah faktor. Langkah untuk percobaan faktorial terdiri dari kombinasi semua level dari faktor. Desain percobaan yang paling sederhana
adalah percobaan dengan 2 faktor dan 2 level (22). Dari percobaan dengan desain faktorial 22 dapat diperoleh persamaan dengan konsep :
Y = B0 + B1(X1) + B2(X2) + B12(X1)(X2)
dimana : Y = respon hasil percobaan
X1, X2 = level, yang nilainya mulai (-1) sampai (+1)
B0, B1, B2, B12 = koefisien yang dapat dihitung dari hasil percobaan B0 = rata – rata hasil semua percobaan
B1, B2, B12 = xyn 2 ∑
(Bolton, 1990) Dalam penerapan rumus ini diperlukan empat percobaan, yaitu X1 dan X2 pada level rendah, X1 pada level tinggi dan X2 pada level rendah, X1 pada level rendah dan X2 pada level tinggi, X1 dan X2 pada level tinggi. Agar dapat mempermudah perhitungan, level tinggi dari faktor diubah menjadi +1 dan level rendah dari faktor diubah menjadi –1 (Bolton 1990).
J. Uji Iritasi Primer
Iritasi adalah suatu reaksi kulit terhadap zat kimia misalnya alkali kuat, asam kuat, pelarut, dan deterjen. Beratnya bermacam-macam, dari hiperemia, edema, dan vesikulasi sampai pemborokan. Iritasi primer terjadi di tempat kontak dan umumnya pada sentuhan pertama, karenanya berbeda dengan sensitisasi (Lu, 1995). Iritasi primer yang paling sering dimodifikasi dideskripsikan oleh John Draize dan teman-temannya pada tahun 1944 (Hayes, 2001).
Tujuan dilakukannya uji Draize yaitu untuk mengidentifikasi bahan-bahan kimia yang merupakan bahan yang sangat berbahaya, bukan untuk membandingkan produk (Hayes, 2001). Ada beberapa uji iritasi kulit yang dimodifikasi berdasarkan prosedur Draize. Modifikasi dilakukan pada spesies hewan yang digunakan, jumlah bahan uji yang dipakai, pengolesan berulang dan jenis pemeriksaan, misalnya histologi (Lu, 1995).
K. Landasan Teori
Salah satu upaya yang dapat dilakukan untuk mencegah penuaan dini yang disebabkan oleh radikal bebas yang masuk dalam tubuh adalah dengan menggunakan sediaan atau produk yang mengandung antioksidan. Teh hijau merupakan antioksidan penyegar kulit dan pengatur keseimbangan radikal bebas yang bisa memperlambat proses penuaan, aktivitas antioksidan ketekin dapat mengurangi kerusakan sel sehingga proses penuaan menjadi lebih lambat (Syah, 2006). Secara tradisional, teh hijau digunakan untuk menghambat penuaan dini dengan cara menyeduh daun teh hijau dengan air panas dan kemudian didiamkan dalam keadaan tertutup sampai dingin dan disaring kemudian digunakan untuk membasuh wajah.
Dalam penelitian ini ekstrak teh hijau akan diformulasikan dalam bentuk
emulgel. Alasan pemilihan bentuk sediaan tersebut karena gel mempunyai
kelebihan berupa kandungan air yang cukup tinggi sehingga memberikan kelembapan yang bersifat mendinginkan dan memberikan rasa nyaman pada kulit (Mitsui, 1997) dan emulsi mempunyai kelebihan berupa kemampuan penetrasi
yang tinggi pada kulit. Sistem emulsi ini menggunakan komposisi emulsifying
agent tween 80 – span 80. Komposisi emulsifying agent ini diharapkan akan
menurunkan tegangan antar muka minyak–air sehingga memberikan sistem emulsi yang memenuhi kriteria. Komposisi emulsifying agent akan menentukan sifat fisik dan stabilitas dari emulgel. Stabilitas sistem emulsi yang terbentuk dapat dicapai dengan adanya tween 80 dan span 80 yang diprediksi dapat membentuk
stable interfacial complex condensed film. Lapisan ini bersifat fleksibel, viscous,
koheren, dan tidak mudah pecah selama molekul–molekulnya tertata dengan efisien satu dengan yang lainnya.
Metode desain faktorial dapat digunakan untuk mendapatkan formula
yang optimum dilihat dari sifat fisik dan stabilitas emulgel. Dengan metode ini efek tiap – tiap faktor maupun interaksi keduanya dapat teridentifikasi dan dapat ditentukan faktor mana yang paling mempengaruhi sifat fisik, dan stabilitas
emulgel. Selain itu, dengan desain faktorial juga dapat diketahui area komposisi
optimum berdasarkan contour plot superimposed.
I. Hipotesis
Hipotesis yang hendak diuji dalam penelitian ini adalah diduga ditemukan faktor yang dominan antara tween 80, span 80 atau interaksi keduanya dalam menentukan sifat fisik dan stabilitas emulgel, serta diduga ditemukan area komposisi tween 80 dan span 80 yang optimum sehingga menghasilkan emulgel dengan sifat fisik dan stabilitas yang baik.
BAB III
METODOLOGI PENELITIAN
A. Rancangan dan Jenis Penelitian
Penelitian ini merupakan rancangan eksperimental murni menggunakan desain faktorial dan bersifat eksploratif, yaitu mencari komposisi optimum
emulsifying agent (Tween 80 dan Span 80) dalam formula emulgel ekstrak teh
hijau sebagai anti-aging dengan parameter sifat fisik dan stabilitas emulgel.
B. Variabel Penelitian 1. Variabel bebas
Variabel bebas dalam penelitian ini adalah level tween 80 dan span 80 sebagai emulsifying agent.
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah sifat fisik emulgel yang meliputi daya sebar, viskositas, dan stabiltas emulgel meliputi perubahan viskositas dan stabilitas fase emulgel setelah penyimpanan selama satu bulan. 3. Variabel pengacau terkendali
Variabel pengacau terkendali dalam penelitian ini adalah lama pengadukan, kecepatan mixer untuk membuat sediaan emulgel, lama penyimpanan.
4. Variabel pengacau tidak terkendali
Variabel pengacau tidak terkendali dalam penelitian ini adalah suhu penyimpanan, suhu dan kelembapan saat penelitian.
C. Definisi operasional
1. Teh hijau adalah teh yang dibuat melalui inaktivasi enzim polifenol oksidasenya di dalam teh segar yang berperan sebagai zat antioksidan.
2. Emulgel adalah sediaan yang dibuat dengan mencampurkan emulsi baik berupa tipe minyak dalam air maupun berupa tipe air dalam minyak dan
gelling agent sebagai pembentuk gel dengan konsentrasi tertentu.
3. Desain faktorial adalah metode optimasi yang memungkinkan untuk mengetahui efek yang dominan dalam menentukan sifat fisik emulgel dan digunakan untuk menceri area komposisi optimum emulsifying agent (tween 80 dan span 80) berdasarkan contour plot superimposed yang diprediksikan sebagai formula optimum pada penelitian ini.
4. Faktor adalah besaran yang mempengaruhi respon, dalam penelitian ini digunakan 2 faktor, yaitu tween 80 sebagai faktor A dan span 80 sebagai faktor B.
5. Level adalah nilai atau tetapan untuk faktor, dalam penelitian ini terdapat 2 level, yaitu level rendah dan level tinggi. Level rendah tween 80 dinyatakan dalam jumlah 2 g dan level tinggi sebanyak 4 g. Level rendah span 80 dinyatakan dalam jumlah sebanyak 3,5 g dan level tinggi sebanyak 5,5 g. 6. Respon adalah besaran yang diamati perubahan efeknya, besarnya dapat
dikuantitatifkan. Dalam penelitian ini adalah hasil percobaan sifat fisik
emulgel (daya sebar dan viskositas) dan stabilitas emulgel (perubahan
viskositas dan pemisahan fase).
8. Sifat fisik emulgel adalah parameter yang digunakan untuk mengetahui kualitas fisik emulgel yang meliputi daya sebar, viskositas dan perubahan viskositas selama penyimpanan (1 bulan).
9. Daya sebar adalah diameter penyebaran 1 gram emulgel pada alat uji daya sebar yang diberi beban 125 gram dan didiamkan selama 1 menit. Kriteria daya sebar optimum adalah 5 - 6 cm.
10. Viskositas adalah hambatan emulgel untuk mengalir setelah adanya pemberian gaya. Semakin besar viskositas, maka emulgel semakin tidak mudah untuk mengalir. Kriteria viskositas optimum adalah 170 – 230 d Pa.s. 11. Perubahan viskositas adalah persentasr dari selisih viskositas emulgel dalam
penyimpanan selama 1 bulan dengan viskositas emulgel setelah dibuat. Kriteria perubahan viskositas optimum adalah 25% - 30%.
12. Stabilitas fase emulgel adalah persentase volume emulgel yang stabil dibandingkan dengan volume total emulgel dalam tabung berskala pada hari ke- 0, 1, 3, 5, 7, 14, 21, 28 dan 30 setelah pembuatan emulgel.
Stabilitas fase emulgel = x100%...(1)
h h
o u
Keterangan : hu = tinggi emulgel stabil (cm) ho = tinggi emulgel mula – mula (cm)
13. Contour plot adalah grafik yang merupakan hasil dari respon sifat fisik dan stabilitas emulgel.
14. Contour plot superimposed adalah penggabungan garis-garis pada daerah optimum yang telah dipilih pada uji volume pemisahan fase, daya sebar, viskositas dan perubahan viskositas.
15. Sifat fisik dan stabilitas emulgel adalah parameter yang digunakan untuk mengetahui kualitas fisik emulgel. Dalam penelitian ini sifat fisik emulgel meliputi daya sebar, viskositas dan stabilitas emulgel meliputi perubahan viskositas emulgel setelah disimpan selama 1 bulan serta pemisahan fase yang terjadi selama penyimpanan.
16. Daerah optimum dalam penelitian ini adalah sifat fisik emulgel yang meliputi daya sebar emulgel 5-6 cm, viskositas emulgel 170 d Pa.s sampai 230 d Pa.s, perubahan viskositas emulgel kurang dari 25% - 30% dan stabilitas fase
emulgel yang lebih besar dari 91%.
D. Alat dan Bahan Penelitian 1. Bahan penelitian
Bahan yang digunakan dalam penelitian ini adalah ekstrak teh hijau (Tritunggal Artha Makmur), metanol (kualitas p.a), DPPH (Sigma, kualitas p.a), hidroksipropilmetilselulosa (HPMC) (Tritunggal Artha Makmur, farmasetis), propilen glikol (Ikapharmamindo putramas, farmasetis), Tween 80 (PT. Ikapharmamindo putramas, farmasetis), Span 80 (Ikapharmamindo putramas, farmasetis), liquid paraffin (Ikapharmamindo putramas, farmasetis), metil paraben (Ikapharmamindo putramas, farmasetis), propil paraben (Ikapharmamindo putramas, farmasetis) dan aquadest.
2. Alat penelitian
Alat yang digunakan dalam penelitian ini antara lain : gelas ukur (Iwaki TE-32 Pirex® Japan Under lic.), bekker glass (Iwaki TE-32 Pirex® Japan Under lic.), mixer (Cucina Philips® dan Power Supply IC Regulated model ad 01), timbangan analitik (Precise 2000C – 2000D1), penangas air, stopwatch (Casio®), kaca bulat berskala, alat uji daya sebar, dan Viscometer seri VT 04 (RION-JAPAN).
E. Tata Cara Penelitian 1. Pemeriksaan Ekstrak Teh Hijau
Pemeriksaan ekstrak teh hijau dilakukan secara Kromatografi lapis tipis (KLT). Ekstrak teh hijau buatan dan ekstrak teh hijau sampel serta pewarna II LP (campuran yang terdiri dari merah metal P, natrium fluoroseina P, biru metal P dan hijau malakit P sama banyak dalam isopropanol P 0,05%) ditotolkan sebanyak 10μl pada fase diam silica gel GF254. Bercak yang telah ditotolkan pada fase diam kemudian dieluasi dengan campuran etil asetat-metiletilketon P-asam format P-air (50:30:10:10) dengan jarak lambat 15 cm setelah itu lempeng diangkat dan dikeringkan, diamati dengan sinar biasa dan dengan sinar ultraviolet 366 nm (Anonim, 1980).
2. Pemeriksaan Katekin
Pemeriksaan katekin pada teh hijau dilakukan dengan menggunakan Spektrofotometer UV-VIS yaitu dengan membandingkan spektrum yang dihasilkan oleh baku pembanding katekin dengan ekstrak teh hijau yang
mengandung katekin. Pengukuran dilakukan pada panjang gelombang antara 266 - 280 nm, menggunakan konsentrasi yang sama (Anonim, 2000).
3. Uji aktivitas antioksidan
Ekstrak teh hijau dilakukan uji aktivitas antioksidan dengan menggunakan radikal bebas DPPH. Sampel pada uji aktivitas antioksidan (DPPH) adalah ekstrak teh hijau serta menggunakan vitamin C sebagai larutan pembanding.
a. Pembuatan larutan 1mM DPPH
Menimbang seksama 39,5 mg DPPH (BM 394,32) dan dilarutkan dengan 100,0 ml metanol p.a kemudian dimasukkan dalam botol yang telah dilapisi dengan alluminium foil (untuk setiap pengujian larutan harus dibuat baru).
b. Persiapan larutan DPPH tanpa penghambatan (0% penghambatan) sebagai larutan blangko. Satu mililiter larutan DPPH 1mM dipipet dan dimasukkan ke dalam labu ukur 5,0 ml kemudian ditambahkan metanol pro analisis hingga 5,0 ml dan dihomogenkan.
c. Persiapan larutan uji
Menimbang seksama 5,0 mg sampel dan dilarutkan dalam metanol pro analisis hingga 5,0 ml sehingga diperoleh larutan dengan konsentrasi 1000 μg (sebagai larutan induk). Dipipet 25, 50, 125, 250, dan 500 µl larutan induk ke dalam labu ukur 5,0 ml untuk mendapatkan konsentrasi 5, 10, 25, 50 dan 100 μg/ml.
d. Persiapan larutan pembanding
Menimbang seksama lebih kurang 5,0 mg vitamin C dan melarutkannya dalam metanol pro analisis hingga 5,0 ml sehingga memperoleh larutan dengan konsentrasi 1000μg/ml (sebagai larutan induk). Dipipet 25, 50, 125, 250 dan 500μl larutan induk ke dalam labu ukur 5,0 ml untuk mendapatkan konsentrasi 5, 10, 25, 50 dan 100μg/ml.
e. Uji aktivitas
Ke dalam setiap tabung larutan uji dan larutan pembanding ditambahkan 1ml larutan DPPH 1mM dan metanol pro analisis hingga 5,0 ml. Mulut tabung ditutup dengan alumunium foil dan dihomogenkan. Larutan DPPH tanpa penghambatan (larutan blangko), larutan uji dan larutan kontrol positif. Segera diinkubasi selama 30 menit pada 370C. Serapan diukur pada panjang gelombang 515nm.
4. Optimasi formula emulgel a. Formula
Formula yang digunakan untuk pembuatan emulgel anti aging ekstrak teh hijau mengacu pada Optimation of chlorphenesin emulgel
Chlorphenesin 0,5 g HPMC 2,5 g Liquid parafin 5 g Tween 20 0,6 g Span 20 0,9 g Propylene glycol 5 g Etanol 2,5 g Metyl paraben 0.03 g Propyl paraben 0,01 g Purified water to 100 g
Dilakukan modifikasi dengan mengganti zat aktif dan beberapa eksipiennya. Formula hasil modifikasi adalah sebagai berikut :
Ekstrak teh hijau 5 g
HPMC 4,5 g Parafin cair 5 g Tween 80 2 – 4 g Span 80 3,5 – 5,5 g Propilen glikol 5 g Metil paraben 0,15 g Propil paraben 0,05 g Aquadest ad 100 g
Formula diatas dibuat emulgel anti aging ekstrak teh hijau dengan menggunakan emulsifying agent berupa tween 80 dan span 80. Level rendah tween 80 adalah 2 gram dan level tinggi tween 80 adalah 4 gram. Level rendah span 80 adalah 3,5 gram dan level tinggi span 80 adalah 5,5 gram. Penggunaan level rendah dan level tinggi emulsifying agent berdasarkan pada literatur dan orientasi formula yang dilakukan oleh
penulis. Berikut adalah rancangan desain faktorial tween 80 dan span 80 yang digunakan dalam penelitian :
Tabel I. Level Rendah dan Level Tinggi Tween 80, Level Rendah dan Level Tinggi Span 80
Formula Tween 80 (g) Span 80 (g)
1 2 3,5 a 4 3,5 b 2 5,5 ab 4 5,5 Keterangan :
F (1) = tween 80 level rendah, span 80 level rendah F (a) = tween 80 level tinggi, span 80 level rendah F (b) = tween 80 level rendah, span 80 level tinggi F (ab) = tween 80 level tinggi, span 80 level tinggi
Berdasarkan tabel tersebut, dibuat 4 formula emulgel ekstrak teh hijau sebagai berikut :
Tabel II. Formula emulgel anti aging ekstrak teh hijau
Formula (1) a b ab
Ekstrak teh hijau 5 5 5 5
HPMC 4,5 4,5 4,5 4,5 Parafin cair 5 5 5 5 Tween 80 2 4 2 4 Span 80 3,5 3,5 5,5 5,5 Propilen glikol 5 5 5 5 Metil paraben 0,15 0,15 0,15 0,15 Propil paraben 0,05 0,05 0,05 0,05 Aquadest ad 100 100 100 100
b. Pembuatan emulgel
1. Pembuatan dispersi HMPC (hidroksipropilmetilselulosa).
HMPC didispersikan sedikit demi sedikit dalam air suling panas pada suhu 80 C, diaduk dengan pengaduk dan didiamkan 1 malam. o
2. Pembuatan emulsi : Fase minyak dibuat dengan mencampur span 80 dengan parafin cair pada suhu 70-80oC, lalu diaduk sampai homogen. Fase air dibuat dengan mencampur tween 80 sebagian air pada suhu 70-80oC, lalu diaduk sampai homogen. Setelah homogen fase minyak ditambahkan ke fase air kemudian sisa air ditambahkan sambil terus diaduk dengan menggunakan pengaduk sampai terbentuk emulsi yang homogen.
3. Pembuatan emulgel.
Emulsi dan HPMC yang sudah didispersikan dicampur sampai terbentuk emulgel kemudian ditambahkan ekstrak teh hijau, metil paraben dan popil paraben yang telah dilarutkan dalam propilen glikol. Bahan-bahan tersebut dihomogenkan dengan kecepatan pengadukan 200 rpm selama 20 menit.
5. Evaluasi sediaan emulgel : 1. Pemeriksaan Viskositas
Pengukuran viskositas menggunakan alat Viscosimeter Rion seri VT 04 dengan cara : sediaan emulgel dimasukkan dalam wadah dan dipasang
pada portable viscotester. Viskositas emulgel diketahui dengan mengamati gerakan jarum penunjuk viskositas. Uji ini dilakukan dua kali, yaitu 48 jam setelah emulgel selesai dibuat dan setelah penyimpanan selama 1 bulan.
2. Pengujian Daya Sebar
Pengukuran daya sebar dilakukan 48 jam setelah pembuatan. Sediaan emulgel ditimbang seberat 1 gram dan diletakkan ditengah kaca bulat berskala. Diatas emulgel diletakkan kaca bulat lain dan pemberat sehingga berat kaca bulat dan pemberat 125 gram, didiamkan selama 1 menit kemudian dicatat penyebarannya. Pengujian ini dilakukan sebanyak 6 kali untuk tiap-tiap formula.
3. Stabilitas Fase emulgel
Sediaan dimasukkan ke dalam tabung berskala kemudian diamati perubahan pemisahan fase yang terjadi pada hari ke-0, 1, 3, 5, 7, 14, 21, 28, dan 30. Dihitung persentase emulgel yang stabil dibandingkan dengan
total volume emulgel dalam tabung berskala. Pemisahan fase emulgel dapat dihitung dengan rumus:
Stabilitas fase emulgel = x100%...(1)
h h
o u
Keterangan : hu = tinggi emulgel stabil (cm) ho = tinggi emulgel mula – mula (cm)
4. Tipe emulsi
a. Metode Pengenceran
Emulgel diletakkan di gelas arloji kemudian ditambahkan aquadest
dengan volume dua kali lipat volume emulgel dan diaduk dengan batang pengaduk hingga merata. Pengamatan dilakukan dengan melihat apakah emulgel bercampur atau tidak.
b. Metode Pewarnaan
Tipe emulsi dibawah mikroskop dengan menggunakan zat warna :
9 Metilen Blue
Emulgel diletakkan di gelas arloji kemudian ditambahkan 5 tetes methylen blue dan diaduk dengan batang pengaduk hingga merata.
Pengamtan dilakukan dibawah mikroskop. Bila globul-globul tidak berwarna merah (jernih) dan fase luar berwarna biru maka tipe emulsi M/A.
5. Pengujian Mikromeritik
Penentuan ukuran partikel dengan metode mikroskopi, dengan alat mikroskop. Pengukuran terlebih dululu dilakukan kalibrasi lensa mikroskop kemudian dilakukan pengamatan ukuran partikel sebanyak 500 partikel dari emulgel teh hijau (Martin and Bustamante, 1993).
6. Subjective assesment
Subjective assesment emulgel dilakukan dengan cara mengoleskan emulgel
pada tangan sukarelawan. Sukarelawan diminta untuk menilai beberapa kriteria seperti yang tercantum dalam kuisioner. Sukarelawan yang dipilih
adalah yang berusia antara 20 - 50 tahun, jenis kelamin laki – laki dan perempuan. Jumlah sukarelawan adalah 29 orang (Garg et al, 2002). Hasil dari subjective assesment digunakan sebagai pertimbangan untuk menentukan batasan fisik sediaan emulgel.
7. Uji Iritasi Primer
Sejumlah 0,5 gram emulgel dioleskan pada kulit punggung kelinci dengan luasan tertentu yang telah dicukur, kemudian diberi tempelan dan ditutup dengan plester. Tempelan dibiarkan di kulit selama 4 jam, kemudian diambil dan diamati terjadinya eritema dan edema pada interval waktu 1 jam, 24 jam, 48 jam, 72 jam dan 1 minggu (Lu, 1995).
F. ANALISIS DATA
Data yang diperoleh dari uji sifat fisik emulgel meliputi daya sebar, viskositas dan perubahan viskositas dianalisis menggunakan metode desain faktorial. Dari pengolahan data, dapat dihitung efek tween 80, span 80 dan efek interaksi sehingga dapat diketahui efek yang dominan dalam menentukan setiap sifat fisik dan stabilitas emulgel. Dari persamaan desain faktorial dapat dibuat
contour plot dari setiap sifat fisik emulgel, kemudian digabungkan dalam superimposed contour plot sehingga dapat dicari area komposisi optimum emulsifying agent yang diprediksi sebagai formula emulgel yang optimum.
Analisis statistik Yate’s treatment untuk mengetahui signifikansi dari setiap faktor dan interaksi dalam mempengaruhi respon. Berdasarkan analisis
statistik ini maka dapat ditentukan ada atau tidaknya hubungan dari setiap faktor dan interaksi terhadap respon. Hal tersebut dapat dilihat dari harga F hitung dan F tabel. Sebelumnya ditentukan hipotesis terlebih dahulu, hipotesis alternatif (H
1) menyatakan adanya regresi (hubungan) antara faktor dengan respon, sedangkan H
0 merupakan negasi dari H1 yang menyatakan tidak adanya regresi (hubungan) antara faktor dengan respon. H
1 diterima dan H0 ditolak apabila harga F hitung lebih besar daripada harga F tabel, yang berarti bahwa faktor berpengaruh signifikan terhadap respon. F tabel diperoleh dari nilai Fα(numerator, denominator) dengan taraf kepercayaan 95 %. Derajat bebas faktor dan interaksi (experiment) sebagai numerator, yaitu 1, dan derajat bebas experimental error sebagai denominator, yaitu 15, sehingga diperoleh harga F tabel untuk faktor dan interaksi pada semua respon adalah F
BAB IV
HASIL DAN PEMBAHASAN A. Identifikasi Ekstrak Teh Hijau 1. Identifikasi secara Kromatografi Lapis Tipis (KLT)
Identifikasi ekstrak teh hijau secara KLT menggunakan fase diam silika gel GF 254 dan fase gerak campuran etil asetat-metiletilketon-asam format-air (50:30:10:10) dengan jarak rambat 15 cm. Hal ini bertujuan untuk melihat apakah ekstrak teh hijau yang digunakan memiliki kandungan senyawa yang sama dengan ekstrak buatan. Identifikasi dilakukan dengan melihat harga Rf yang dihasilkan sampel. Harga Rf didefinisikan sebagai perbandingan antara jarak titik pusat bercak dari awal dengan jarak garis depan pelarut dari titik awal (Stahl, 1973).
a b c a b c Sinar biasa, 254 nm Sinar UV, 366 nm Gambar 3. Lempeng KLT diamati dengan sinar biasa dan sinar UV Keterangan :
a = ekstrak buatan b = ekstrak sampel c = zat warna II LP
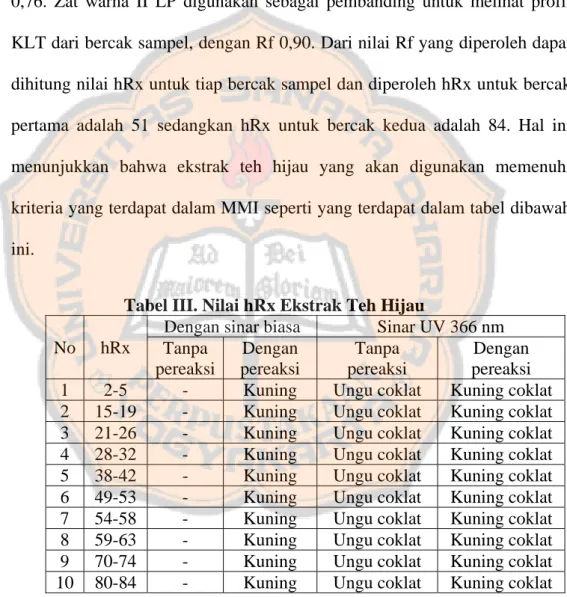
Dari gambar 3 dapat dilihat pada sinar biasa dan sinar UV 366 nm,ekstrak buatan dan ekstrak teh hijau menghasilkan tinggi bercak yang sama dan berwarna kuning kecoklatan. Hasil penelitian menunjukkan harga Rf untuk bercak pertama adalah 0,46 dan harga Rf untuk bercak kedua adalah 0,76. Zat warna II LP digunakan sebagai pembanding untuk melihat profil KLT dari bercak sampel, dengan Rf 0,90. Dari nilai Rf yang diperoleh dapat dihitung nilai hRx untuk tiap bercak sampel dan diperoleh hRx untuk bercak pertama adalah 51 sedangkan hRx untuk bercak kedua adalah 84. Hal ini menunjukkan bahwa ekstrak teh hijau yang akan digunakan memenuhi kriteria yang terdapat dalam MMI seperti yang terdapat dalam tabel dibawah ini.
Tabel III. Nilai hRx Ekstrak Teh Hijau No hRx
Dengan sinar biasa Sinar UV 366 nm Tanpa pereaksi Dengan pereaksi Tanpa pereaksi Dengan pereaksi 1 2-5 - Kuning Ungu coklat Kuning coklat 2 15-19 - Kuning Ungu coklat Kuning coklat 3 21-26 - Kuning Ungu coklat Kuning coklat 4 28-32 - Kuning Ungu coklat Kuning coklat 5 38-42 - Kuning Ungu coklat Kuning coklat 6 49-53 - Kuning Ungu coklat Kuning coklat 7 54-58 - Kuning Ungu coklat Kuning coklat 8 59-63 - Kuning Ungu coklat Kuning coklat 9 70-74 - Kuning Ungu coklat Kuning coklat 10 80-84 - Kuning Ungu coklat Kuning coklat
Dari hasil identifikasi ekstrak dengan zat warna (MMI), ditunjukkan pada tabel IV. Berdasarkan tabel tersebut dapat disimpulkan bahwa ekstrak teh
hijau yang akan digunakan dalam penelitian memenuhi syarat yang terdapat dalam MMI.
Tabel IV. Hasil Pemeriksaan Ekstrak Teh Hijau
Pemeriksaan Syarat menurut literatur Hasil pemeriksaan
Identifikasi reaksi warna
a. Sejumlah ekstrak ditambahkan 5 tetes asam sulfat pekat, terbentuk warna kuning
b. Sejumlah ekstrak ditambahkan 5 tetes asam sulfat 10 N, terbentuk warna kuning c. Sejumlah ekstrak ditambahkan 5 tetes
larutan besi (III) klorida 5 %, terbentuk warna kuning hijau
d. Sejumlah ekstrak ditambahkan 5 tetes larutan kalium hidroksida 5% terbentuk warna coklat
e. Sejumlah ekstrak ditambahkan 5 tetes asam klorida pekat, terbentuk warna kuning
f. Sejumlah ekstrak ditambahkan 5 tetes amonia (25 %), terbentuk warna coklat g. Sejumlah ekstrak ditambahkan 5 tetes
larutan asam asetat encer, terbentuk warna kuning coklat
Memenuhi syarat Memenuhi syarat Memenuhi syarat Memenuhi syarat Memenuhi syarat Memenuhi syarat Memenuhi syarat Memenuhi syarat Memenuhi syarat pH 5,0 – 7,0 5,4
2. Pemeriksaan Katekin pada Ekstrak Teh Hijau
Uji ini dilakukan untuk mengetahui secara kualitatif apakah ekstrak teh hijau yang digunakan mengandung katekin, diketahui bahwa aktivitas antioksidan teh hijau berhubungan dengan kandungan katekinnya. Katekin adalah senyawa dominan dari polifenol teh hijau yang merupakan senyawa larut dalam air, tidak berwarna dan memberikan rasa pahit. Teh hijau mengandung 16-30% senyawa katekin (Syah, 2006).