INTISARI
Para-phenylenediamine (PPD) merupakan salah satu komponen dalam pewarna rambut oksidatif. Menurut Dirjen POM RI (2008), batas konsentrasi kandungan PPD dalam sediaan pewarna rambut yang diperbolehkan yaitu 6%. Penelitian ini bertujuan untuk memvalidasi metode analisis PPD dalam formulasi pewarna rambut oksidatif.
Analisis PPD dalam pewarna rambut menggunakan metode KCKT yang disertai dengan ekstraksi padat-cair dan clean-up dengan SPE C18. Ekstraksi dilakukan dengan pelarut sodium metabisulfit 0,01 M pH 8. Pada SPE volume loading sampel yang digunakan yaitu 100 µL. Sistem KCKT yang digunakan yaitu fase terbalik dengan kolom C18, komposisi fase gerak ACM : aquades/ ammonium hidroksida 10% (10:90), laju alir 0,5 mL/ menit dan detektor UV dengan λ 254 nm.
Parameter validasi yang ditentukan yaitu spesifisitas, linearitas, akurasi, presisi, dan sensitivitas. Hasil menunjukkan bahwa metode analisis PPD: spesifik dengan nilai Rs ≥ 1,5; linear dengan koefisien korelasi (r) pada replikasi 1, 2 dan 3 berturut-turut sebesar 0,9915, 0,9942 dan 0,9932; tidak akurat dengan nilai %perolehan kembali sebesar 104,3 – 180,0% (CV= 14,5 – 85,6%); tidak presisi dinyatakan dengan f hitung 5,54 > f tabel sebesar 3,68, nilai DL yang diperoleh sebesar 686 – 942 ng/mL; nilai QL yang diperoleh sebesar 2288 – 3138 ng/mL. Kadar PPD dalam pewarna rambut oksidatif yaitu 2,92 – 4,57% b/b.
Kata kunci : para-phenylenediamine, pewarna rambut oksidatif, clean-up,
ABSTRACT
Para-phenylenediamine (PPD) is a compound found in oxidative hair dyes formulation. According to Dirjen POM RI (2008), maximum concentration of PPD in hair dyes is 6%. The purpose of this study is to validate the PPD analysis method in oxidative hairdye formulation.
Analysis PPD in hairdye is conducted using HPLC method followed by solid-liquid extraction and clean-up using SPE C18. Solvent for extraction is Sodium metabisulfit 0,01 M pH 8. For SPE method, volume for sample loading is 100 µL. Reversed-phase HPLC system in this study uses C18 column, mobile phase composition of ACM : aquadest/ ammonium hidroxide 10% (10:90), flow rate 0,5 mL/minute and UV detector at wavelength 254 nm.
Validation parameters examined are specificity, linearity, accuracy, precision, and sensitivity. The results show validity: specific with Rs ≥ 1,5; linear with r for replication 1, 2 and 3 in consecutive order are 0,9915, 0,9942 and 0,9932; not accurate with % recovery is 104,3 – 180,0%, not precise with f calculated 5,54 > f table 3,68, DL is 686 – 942 ng/mL,and QL is 2288 – 3138 ng/mL. Concentration of PPD in oxidative hair dye formulation is 2,92 – 4,57% b/b.
VALIDASI METODE ANALISIS PARA-PHENYLENEDIAMINE (PPD)
DALAM FORMULASI PEWARNA RAMBUT OKSIDATIF
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Cynthia Feliana
NIM : 118114104
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
“
The will to win, the desire to succeed, the urge to
reach your full potential... these are the keys that will
unlock
the door to personal excellence.”
- Confucius -
“
Live as if you were to die tomorrow. Learn as if you
were to live forever.
”
-
Mahatma gandhi –Karya ini kudedikasikan untuk orang tua, keluarga,
vii
Puji dan syukur saya panjatkan kepada Tuhan Yang Maha Esa atas cinta
dan berkatnya yang luar biasa, sehingga penulis dapat menyelesaikan skripsi yang
berjudul “Validasi Metode Analisis Para-Phenylenediamine (PPD) Dalam
Formulasi Pewarna Rambut Oksidatif” sebagai salah satu syarat untuk
memperoleh gelar Sarjana Farmasi (S.Farm.) di Fakultas Farmasi Universitas
Sanata Dharma.
Penulisan skripsi ini tidak lepas dari bantuan berbagai pihak dengan
adanya motivasi, kritik, saran, diskusi, dan bimbingan. Oleh karena itu penulis
ingin mengucapkan terimakasih kepada:
1. Prof. Dr. Sri Noegrohati, Apt. selaku dosen pembimbing dan penguji yang
telah meluangkan waktunya untuk memberikan bimbingan, motivasi, kritik,
dan saran selama penelitian dan penulisan skripsi ini.
2. Jeffry Julianus, M.Si. dan F. Dika Octa Riswanto, M.Sc., selaku dosen
penguji yang memberikan kritik dan saran untuk membangun skripsi ini.
3. Aris Widayati, M.Si., Ph. D., Apt. selaku dekan Fakultas Farmasi Universitas
Sanata Dharma atas teladan yang diberikan.
4. Pak Sanjaya yang telah banyak meluangkan waktunya untuk mendampingi,
memotivasi, membantu, dan menjadi teman bagi penulis selama penelitian
dan penulisan skripsi ini.
5. Seluruh dosen dan karyawan Fakultas Farmasi Universitas Sanata Dharma
atas ilmu, pengalaman, dan persahabatan yang dibagikan.
6. Papa, mama, koko dan seluruh anggota keluargaku yang tercinta yang selalu
viii
7. Kekasih sekaligus sahabat yang selalu memberikan semangat dan doa selama
penelitian dan penulisan skripsi ini.
8. Sahabat-sahabatku tercinta Centel, Nyahti, Pika, Anka, Dea, dan Gabby atas
persahabatan, doa, dan semangatnya selama ini.
9. Aphui, Bayi, dan Cancan selaku sahabat dalam perjuangan penelitian dan
penulisan skripsi ini.
10. Cingap, Elyn, Evi, Ester, Siska, Empit, Kingkong, Berle, Ahen, dan Loren
Cik Lulu, Cik Anis, Cik Steph, Cik Maria, dan Valen selaku teman-teman
baikku selama di Fakultas Farmasi Universitas Sanata Dharma atas
persahabatan dan semangat yang telah diberikan.
11. Seluruh pihak yang tidak dapat disebutkan satu persatu atas segala bantuan ,
semangat, dan doa sehingga penulis bisa sampai pada tahap ini.
Penulis menyadari bahwa masih banyak kekurangan dalam penulisan
skripsi ini atas segala keterbatasan yang dimiliki penulis. Untuk itu penulis
mengharapkan saran dan kritik yang dapat membangun dari semua pihak. Akhir
kata, penulis mempersembahkan skripsi ini demi kemajuan ilmu pengetahuan.
Yogyakarta, 5 Juni 2015
x
1. Penyiapan sampel pewarna rambut oksidatif ……… 20
2. Pembuatan larutan sodium metabisulfit 0,01 M ……….. 20
3. Pembuatan larutan sodium metabisulfit 0,01 M pH 8 ………….. 21
4. Pembuatan fase gerak untuk KCKT ………...…… 21
xi
rambut dan perbandingan ekstrak sampel pewarna rambut
sebelum dan sesudah clean-up dengan KCKT ……… 22
7. Optimasi clean-up dengan SPE C18 ………..……… 23
8. Validasi metode clean-up PPD dengan SPE C18 ……….. 23
9. Validasi metode penetapan kadar PPD dengan metode standar adisi ... 24
10. Penetapan kadar para-phenylenediamine (PPD) dalam pewarna rambut dengan metode standar adisi ………. 25
G.Analisis Hasil ………. 26
BAB IV HASIL DAN PEMBAHASAN ………. 30
A. Penyiapan sampel pewarna rambut oksidatif ……….. 30
B. Validasi metode pengukuran PPD dengan KCKT ……….. 31
C. Identifikasi para-phenylenediamine dalam pewarna rambut oksidatif ……… 34
D. Perbandingan antara ekstrak sampel pewarna rambut sebelum dan sesudah clean-updengan SPE C18 ………. 36
E. Optimasi clean-up PPD dalam sampel dengan SPE C18 ………… 37
F. Validasi metode clean-up PPD dalam sampel dengan SPE C18 ……… 42
G. Validasi metode penetapan kadar PPD dengan metode standar adisi ………...… 44
H. Pengaruh matriks pewarna rambut dalam penetapan kadar para-phenylenediamine(PPD) ……….…. 47
xii
BAB V KESIMPULAN DAN SARAN ……….. 49
A.Kesimpulan ………... 49
B.Saran ……….. 49
DAFTAR PUSTAKA ………... 50
LAMPIRAN ……… 52
xiii
DAFTAR TABEL
Halaman
Tabel I. Nilai r dan n kurva baku eksternal……..………. 33
Tabel II. Nilai r dan n kurva baku adisi metode clean-up dengan
SPE C18……….. 43
Tabel III. Rata-rata % perolehan kembali dan nilai CV perolehan
kembali metode SPE C18……….. 44
Tabel IV. Nilai r dan n kurva baku adisi metode
standar adisi ………..……….…… 45
Tabel V. Nilai % perolehan kembali dan nilai CV perolehan kembali
metode penetapan kadar dengan metode standar
adisi ……….………... 46
xiv
Gambar 6. Kurva hubungan seri massa baku PPD dan respon
instrumen (AUC) ……….. 32
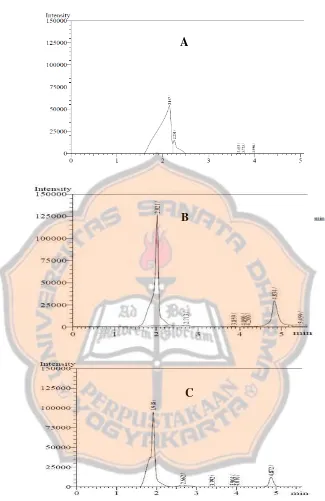
Gambar 7. (A) Kromatogram larutan sodium metabisulfit,
(B) Kromatogram baku PPD 8 µg/mL, (C) Kromatogram
sampel pewarna rambut oksidatif setelah clean-up………. 35
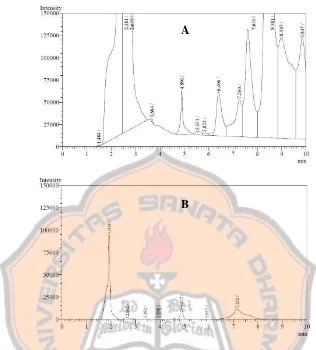
Gambar 8. (A) Kromatogram ekstrak sampel sebelum dilakukan
clean-up dengan SPE C18, (B) Kromatogram sampel
sesudah dilakukan clean-up dengan SPE C18……… 37
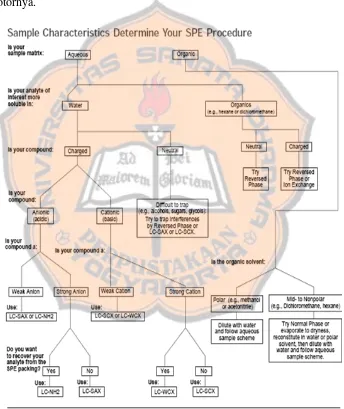
Gambar 9. Skema untuk pemilihan jenis SPE ……… 39
Gambar 10. (A) Kromatogram dengan volume loading sampel 100µL,
(B) Kromatogram dengan volume loading sampel 1 mL,
(C) Kromatogram baku PPD ………... 41
Gambar 11. Kurva hubungan antara seri massa adisi PPD dan respon
instrumen metode clean-up dengan SPE ………. 43
Gambar 12. Kurva hubungan antara massa baku adisi PPD dan respon
instrumen metode standar adisi replikasi
xv
xvi
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Sertifikat analisis baku para-phenylenediamine……….. 53
Lampiran 2. Data penimbangan untuk perhitungan keseragaman
bobot sampel pewarna rambut oksidatif ……...………… 54
Lampiran 3. Tabel hubungan n dan r
(Pearson’s correlation coefficient test) ……….. 55
Lampiran 4. Perhitungan Resolusi (Rs) ……….. 55
Lampiran 5. Persamaan regresi linear kurva baku eksternal
replikasi 1, 2, 3, dan kumulatif ……… 56
Lampiran 6. Kurva baku adisi metode clean-up dengan SPE C18 .… 56
Lampiran 7. Perolehan kembali metode clean-up dengan SPE C18…. 57
Lampiran 8. Kurva baku metode standar adisi ………... 57
Lampiran 9. Perhitungan uji signifikansi slope kurva baku adisi
3 replikasi dengan ANOVA satu arah ……… 58
Lampiran 10. Perolehan kembali dengan metode standar adisi ……….. 58
Lampiran 11. Penetapan kadar PPD dalam sampel pewarna rambut
oksidatif dengan metode standar adisi ……… 59
Lampiran 12. Uji signifikansi (uji t) antara slope kurva baku eksternal
xvii INTISARI
Para-phenylenediamine (PPD) merupakan salah satu komponen dalam pewarna rambut oksidatif. Menurut Dirjen POM RI (2008), batas konsentrasi kandungan PPD dalam sediaan pewarna rambut yang diperbolehkan yaitu 6%. Penelitian ini bertujuan untuk memvalidasi metode analisis PPD dalam formulasi pewarna rambut oksidatif.
Analisis PPD dalam pewarna rambut menggunakan metode KCKT yang disertai dengan ekstraksi padat-cair dan clean-up dengan SPE C18. Ekstraksi dilakukan dengan pelarut sodium metabisulfit 0,01 M pH 8. Pada SPE volume
loading sampel yang digunakan yaitu 100 µL. Sistem KCKT yang digunakan yaitu fase terbalik dengan kolom C18, komposisi fase gerak ACN : aquades/ ammonium hidroksida 10% (10:90), laju alir 0,5 mL/ menit dan detektor UV
dengan 254 nm.
Parameter validasi yang ditentukan yaitu spesifisitas, linearitas, akurasi, presisi, dan sensitivitas. Hasil menunjukkan bahwa metode analisis PPD: spesifik
dengan nilai Rs ≥ 1,5; linear dengan koefisien korelasi (r) pada replikasi 1, 2 dan 3 berturut-turut sebesar 0,9915, 0,9942 dan 0,9932; tidak akurat dengan nilai %perolehan kembali sebesar 104,3 – 180,0% (CV= 14,5 – 85,6%); tidak presisi dinyatakan dengan f hitung 5,54 > f tabel sebesar 3,68, nilai DL yang diperoleh sebesar 686 – 942 ng/mL; nilai QL yang diperoleh sebesar 2288 – 3138 ng/mL. Kadar PPD dalam pewarna rambut oksidatif yaitu 2,92 – 4,58% b/b.
Kata kunci : para-phenylenediamine, pewarna rambut oksidatif, clean-up, solid phase extraction, KCKT, validasi metode.
xviii ABSTRACT
Para-phenylenediamine (PPD) is a compound found in oxidative hair dyes formulation. According to Dirjen POM RI (2008), maximum concentration of PPD in hair dyes is 6%. The purpose of this study is to validate the PPD analysis method in oxidative hairdye formulation.
Analysis PPD in hairdye is conducted using HPLC method followed by solid-liquid extraction and clean-up using SPE C18. Solvent for extraction is Sodium metabisulfit 0,01 M pH 8. For SPE method, volume for sample loading is 100 µL. Reversed-phase HPLC system in this study uses C18 column, mobile phase composition of ACN : aquadest/ ammonium hidroxide 10% (10:90), flow rate 0,5 mL/minute and UV detector at wavelength 254 nm.
Validation parameters examined are specificity, linearity, accuracy, precision, and sensitivity. The results show validity: specific with Rs ≥ 1,5; linear with r for replication 1, 2 and 3 in consecutive order are 0,9915, 0,9942 and 0,9932; not accurate with % recovery is 104,3 – 180,0%, not precise with f calculated 5,54 > f table 3,68, DL is 686 – 942 ng/mL,and QL is 2288 – 3138 ng/mL. Concentration of PPD in oxidative hair dye formulation is 2,92 – 4,58% b/b.
1 BAB I
PENGANTAR
A. Latar Belakang
Pewarna rambut adalah sediaan kosmetik yang digunakan dalam tata rias
rambut untuk mewarnai rambut atau untuk mengembalikan warna rambut asalnya
(Dirjen POM, 1985). Pewarna rambut diklasifikasikan menjadi tiga jenis, yaitu
pewarna rambut temporer, pewarna rambut semi-permanen, pewarna rambut
permanen (Azis dan Muktiningsih, 1999). Dalam pewarna rambut permanen
penyusun utamanya adalah para-phenyelenediamine atau para-aminophenol.
Para- phenyelenediamine (PPD) ini mempercepat proses pewarnaan rambut dan
mungkin dapat menyebabkan efek toksik lokal maupun sistemik saat
diaplikasikan secara topikal atau tertelan (Sutrapu, Jagadeeshwar, Nagulu, dan
Vidyasagar, 2010).
Penggunaan PPD dosis tinggi dalam jangka pendek (efek akut) dapat
menimbulkan dermatitis, mata iritasi dan berair, asma, gastritis, gagal ginjal,
vertigo, tremor, kejang, dan koma pada manusia. Dermatitis kontak eczematous
mungkin terjadi dalam penggunaan jangka panjang (efek kronis) pada manusia.
Menurut Scientific Committee on Consumer Products (SCCP), PPD merupakan
agen sensitisasi kulit yang sangat kuat. Para-phenylenediamine (PPD) merupakan
suatu alergen; bahkan apabila seseorang tidak menimbulkan reaksi saat
penggunaan pertama, mereka dapat menjadi tersensitisasi oleh PPD dan dapat
terjadi reaksi buruk saat penggunaan berulang (Al-Suwaidi dan Ahmed, 2010).
Menurut Dirjen POM RI (2008), batas konsentrasi kandungan PPD
kandungan PPD pada pewarna rambut jarang dicantumkan. Pada penelitian ini,
penulis ingin melakukan validasi metode analisis PPD dalam pewarna rambut
oksidatif. Penelitian ini akan melalui serangkaian proses yang mencakup
identifikasi PPD dalam pewarna rambut dengan KCKT, perbandingan sebelum
dan sesudah clean-up dengan SPE C18, optimasi clean-up PPD dengan SPE C18,
validasi metode clean-up SPE C18, validasi metode penetapan kadar PPD dengan
metode standar adisi dan penetapan kadar PPD dalam pewarna rambut oksidatif.
Untuk menjamin bahwa metode yang digunakan dalam penelitian
berkualitas dan dapat dipercaya, maka perlu dilakukan validasi. Proses validasi
yang dilakukan dalam penelitian ini meliputi parameter spesifisitas linearitas,
sensitivitas, akurasi, dan presisi.
Isolasi PPD dari matriks sampelnya menggunakan ekstraksi solven air
karena PPD mudah larut dalam air (log Kow = -0,25). Setelah dilakukan ekstraksi,
perlu dilakukan clean-up untuk mendapatkan analit yang terpisah dari matriks
sampel. Metode clean-up yang yang digunakan adalah metode Solid Phase
Extraction (SPE) dengan fase diam C18. Metode SPE C18 dipilih karena C18
bersifat non-polar sehingga diharapkan mampu menahan ko-ekstraktan pada
sampel.
Hasil yang optimal dalam clean-up dapat dicapai dengan melakukan
optimasi terlebih dahulu. Optimasi yang dilakukan yaitu dengan memvariasi
volume loading sampel. Metode clean-up dengan SPE dikatakan berhasil jika
clean-up diinjeksikan pada Kromatografi Cair Kinerja Tinggi (KCKT) yang
metodenya telah dioptimasi dan divalidasi oleh Emelia (2015).
1. Permasalahan
a. Apakah matriks formulasi pewarna rambut oksidatif terdiri dari campuran
yang kompleks sehingga perlu dilakukan clean-up dengan metode
pemisahan yang sesuai?
b. Apakah ko-ekstraktan dapat tertahan pada sistem SPE C18-air sehingga
kurva adisi pada hasil clean-up tidak berbeda signifikan dari kurva baku
eksternal?
c. Apakah metode analisis PPD dalam pewarna rambut oksidatif dengan
ekstraksi larutan sodium metabisulfit pH 8 dan clean-up C18-air dapat
memenuhi kriteria validitas?
2. Keaslian penelitian
Sejauh penelusuran literatur, penelitian mengenai para-phenylenediamine
pernah dilakukan. Vincent, Bordin, dan Rodriguez (2002) melakukan penelitian
mengenai validasi metode analisis PPD dalam pewarna rambut dengan
menggunakan sistem KCKT dengan kolom C8, fase gerak asam asetat yang
ditambah 10% amonia hingga pH 5,9 dan clean-up sampel menggunakan
liquid-liquid extraction (LLE) dengan pelarut heksan. Al-Suwaidi dan Ahmed (2010)
melalukan penelitian mengenai identifikasi dan kuantifikasi
para-phenylenediamine dalam tato temporer. Dengan demikian, penelitian mengenai
fase gerak ACN: aquadest (10:90), dan clean-up menggunakan SPE C18 belum
pernah dilakukan dalam suatu sediaan pewarna rambut.
3. Manfaat penelitian
a. Manfaat metodologis. Penelitian ini diharapkan dapat memberikan
informasi mengenai metode analisis PPD dengan clean-up menggunakan
SPE C18 beserta parameter validasinya.
b. Manfaat praktis. Penelitian ini diharapkan dapat memberikan informasi
terkait optimasi clean-up dengan SPE C18 dan memberikan informasi
bahwa metode clean-up dengan SPE C18 dapat digunakan untuk
menetapkan kadar PPD dalam pewarna rambut dengan parameter
validitasnya.
B. Tujuan Penelitian
1. Mengetahui apakah matriks pewarna rambut oksidatif terdiri dari campuran
yang kompleks sehingga perlu dilakukan clean-up dengan metode pemisahan
yang sesuai.
2. Mengetahui apakah ko-ekstraktan tertahan pada sistem SPE C18-air sehingga
kurva adisi pada hasil clean-up tidak berbeda signifikan dari kurva baku
eksternal.
3. Mengetahui validitas metode analisis PPD dalam pewarna rambut oksidatif
dengan ekstraksi larutan sodium metabisulfit pH 8 dan clean-up dengan
5 BAB II
PENELAAHAN PUSTAKA
A. Pewarna Rambut
Sediaan pewarna rambut adalah sediaan kosmetik yang digunakan dalam
tata rias rambut untuk mewarnai rambut atau untuk mengembalikan warna rambut
asalnya (Dirjen POM, 1985). Pewarna rambut diklasifikasikan menjadi tiga jenis,
yaitu pewarna rambut temporer, pewarna rambut semi-permanen, pewarna rambut
permanen (Azis dan Muktiningsih, 1999).
Pewarna rambut permanen dikenal sebagai pewarna rambut oksidatif,
dan penyusun utamanya adalah para-phenyelenediamine atau para-aminophenol.
Pada umumnya, pewarna ini terdiri dari dua komponen yang harus dicampurkan
ketika akan digunakan. Dua komponen tersebut adalah alkaline agent (colorant)
dan hidrogen peroksida (developer). Alkaline agent memiliki efek membuka
lapisan rambut luar sehingga agen pengoksidasi dapat lebih mudah terpenetrasi
pada batang rambut. Selain alkaline agent, juga terdapat material yang disebut
prekursor warna, yang berguna untuk membentuk warna baru. Agen pengoksidasi
akan bereaksi dengan prekursor warna, dimana reaksi ini dikatalisis oleh alkaline
agent dan akan menghasilkan oksigen. Selanjutnya, agen pengoksidasi akan
menghilangkan warna alami dan terjadi pembentukan molekul berwarna oleh
prekursor warna dalam korteks rambut. Molekul ini resisten terhadap pencucian
sehingga dapat memberikan warna permanen. Oksigen yang dihasilkan akan
terlihat menggantikan warna alami rambut. Kebanyakan proses pewarnaan rambut
meliputi dua proses yang berlangsung secara berkesinambungan, dimana pada
awalnya terjadi penghilangan warna alami rambut, diikuti proses pemberian
warna baru (Helmenstine, 2003). Para-phenylendiamine (PPD) atau disebut juga
1,4-diaminobenzen atau 1,4-fenilendiamin adalah suatu amin aromatik yang
digunakan dalam hampir setiap cat rambut di pasaran (Pardede, Nababan, dan
Mahadi, 2008). Komposisi pewarna rambut oksidatif pada penelitian ini terdiri
dari:
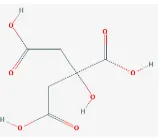
1. Para-phenylendiamine (PPD)
Gambar 1. Struktur p-Phenylenediamine (National Center for Biotechnology Information, 2015)
PPD digunakan dalam cat rambut karena memberikan hasil yang tampak
alami, menguatkan warna yang gelap dan warnanya tahan lama. PPD juga
dapat dijumpai pada pewarna pakaian dan bulu, kosmetik, tato temporer, tinta,
karet hitam, minyak dan pelumas. PPD yang terdapat dalam cat rambut
biasanya dalam konsentrasi 6% (Pardede, Nababan, dan Mahadi, 2008).
Berdasarkan Daftar Bahan yang Diizinkan Digunakan dalam Kosmetik dengan
Pembatasan dan Persyaratan Penggunaan pada Peraturan Kepala Badan
tentang Bahan Kosmetik (2008), kadar maksimum PPD yang diperbolehkan
dalam pewarna rambut adalah 6%.
PPD memiliki bobot molekul 108,14 g/mol, berwujud serbuk kristal
berwarna putih hingga sedikit merah, dan dapat menjadi lebih gelap saat
terpapar udara (United States Department of Labor, 1991).
PPD memiliki titik didih 267oC, titik leleh145-147oC, densitas >1, dan
log Kow -0,25. PPD dapat larut dalam 100 bagian air, larut dalam alkohol,
kloroform, ether, dan larut dalam benzen panas. Kelarutan dalam air pada 25oC
yaitu 4% (g/100 mL). Saat terpapar udara, PPD teroksidasi menjadi warna
ungu dan hitam. (National Center for Biotechnology Information, 2015).
Panjang gelombang maksimum: 281.9 nm (Scientific Committee on Consumer
Safety, 2012). PPD mempunyai dua nilai pKa yaitu 6,42 dan 3,04 (ChemAxon,
2014).
2. Ekstrak henna (Lawsonia inermis)
Henna atau hina (Lawsonia inermis, famili Lythraceae) merupakan
tanaman berbunga yang tumbuh di daerah sub-tropis dan tropis di Afrika dan
Asia Selatan. Henna secara komersial dikembang biakkan di Moroko, Sudan,
India, Pakistan, Yemen, dan negara lainnya.
Henna mengandung molekul pewarna, lawsone (2-hidroksi
-1,4-naftokuinon). Molekul ini memiliki kemampuan untuk mengikat protein dan
secara luas digunakan untuk mewarnai kulit (tato), rambut, kuku, dan untuk
Untuk menghasilkan warna hitam, biasanya ditambahkan PPD sebagai
pewarna oksidasi (Al-Suwaidi dan Ahmed, 2010).
3. Sodium Perborat Tetrahidrat
Gambar 2. Struktur molekul sodium perborat tetrahidrat (Chemical Books, 2010)
Sodium perborat tetrahidrat merupakan kristal putih yang tidak berbau
dengan berat molekul 153,86 g/ mol dan berat jenis 1,73 g/ mL. pH dalam
larutan 1% pada suhu 25oC adalah 10,2. Kelarutan sodium perborat tetrahidrat
dalam air 21,5 g/L (18oC). Tekanan uap 6,2 mmHg pada suhu 20oC. Titik leleh
pada suhu 65oC dan titik didih 130-150oC. pKa sodium perborat tetrahidrat
yaitu 8,5 (FMC, 2006).
Menurut Scientific Committee on Consumer Safety (2010), sodium perborat
dalam air pada suhu ruang mengalami kesetimbangan menjadi hidrogen
peroksida dan sodium metaborat mengikuti persamaan reaksi sebagai berikut:
[NaBO2(OH)2 x 3 H2O]2 ⇆ 2NaBO2 + 2H2O2 + 6 H2O (1)
4. Asam Sitrat
Asam sitrat berbentuk padat atau berupa serbuk kristal, tidak berbau,
rasanya asam. Asam sitrat mempunyai berat molekul 192,12 g/mol, berat jenis
1,665 g/mL dan titik leleh 153oC. Asam sitrat lebih larut dalam air dengan log
Kow = -1,7. Sangat larut di etanol, larut di eter, etil asetat, tidak larut dalam
benzene dan kloroform (National Center for Biotechnology Information, 2015).
5. Ekstrak Acacia concina
Acacia concina berasal dari family Acaciaceae, dikenal dengan sebutan
buah untuk rambut. Acacia concina biasa digunakan sebagai perawatan untuk
rambut di India. Bagian tanaman yang biasa digunakan untuk ekstrak yaitu
kulit pohon dan buah. Tanaman ini sudah biasa ditemukan di hutan di India.
Kulit pohonnya mempunyai kandungan saponin yang tinggi yang
merupakan foaming agent. Selain saponin terdapat juga kandungan alkaloid,
flavonoid, fitosterol, tannin, senyawa fenolic, gum, dan mucilage (Todkar,
Chavan, and Kulkarni, 2010).
6. Ekstrak Emblica officinalis
Emblica officinalis biasa disebut dengan Indian Gooseberry. Di India
tanaman ini dikenal dengan sebutan amla yang digunakan untuk pengobatan
ayurveda. Amla dapat ditemukan di atas ketinggian 5000 kaki di India. Bagian
yang biasa digunakan dalam tanaman ini yaitu buah segar, buah kering, daun,
daun, biji, akar, kulit batang dan bunga.
Tanaman ini mempunyai banyak manfaat yaitu untuk penambah daya
tahan tubuh, mengontrol diabetes, gangguan respirasi, kelainan jantung,
rambut. Pada penggunaan untuk rambut amla berfungsi untuk membantu
pertumbuhan rambut dan pigmentasi. Bagian yang digunakan untuk rambut
yaitu bagian buah. Kandungan kimia yang terdapat dalam tanaman ini yaitu
apigenin, asam galat, asam elagat, asam chebulinic, kuarsetin, asam
chebulagic, corilagin, isostrictiniin, metil galate, and luteolin (Kumar et. al.,
2012).
B. Solid Phase Extraction (SPE)
SPE merupakan metode praperlakuan sampel atau untuk clean-up sampel
seperti sampel yang mengandung garam-garam, protein, polimer, resin, dan
lain-lain. Ada dua strategi dalam SPE yaitu (1) dengan melakukan pemilihan pelarut
yang mampu menahan semua analit yang dituju pada penjerap yang digunakan,
sementara untuk senyawa - senyawa penganggu akan terelusi (2) dengan
mengusahakan supaya analit yang tertuju keluar (terelusi), sementara untuk
senyawa penganggu tertahan pada penjerap (Gandjar dan Rohman, 2007).
Ada empat tahap dalam prosedur SPE, yaitu:
a. Pengkondisian
Kolom dialiri dengan pelarut sampel untuk membasahi permukaan penjerap
dan untuk menciptakan nilai pH yang sama, sehingga perubahan kimia yang
tidak diharapkan ketika sampel dimasukkan dapat dihindari. Penjerap
nonpolar dan penjerap penukar ion dikondisikan dengan menggunakan
metanol lalu dengan aquadest. Penjerap - penjerap polar seperti diol, siano,
amino, dan silika harus dibilas dengan pelarut nonpolar seperti metilen
klorida.
b. Retensi sampel
Larutan sampel dilewatkan ke kolom baik untuk menahan analit yang
diharapkan, sementara komponen lain terelusi atau untuk menahan komponen
yang tidak diharapkan sementara analit yang diharapkan terelusi.
c. Pembilasan
Tahap ini bertujuan untuk menghilangkan seluruh komponen yang tidak
tertahan oleh penjerap selama tahap retensi.
d. Elusi
Tahap terakhir untuk mengambil analit yang dikehendaki jika analit tersebut
tertahan pada penjerap
(Gandjar dan Rohman, 2007).
C. Kromatografi
Kromatografi merupakan teknik pemisahan yang menggunakan fase
mengkuantifikasi berbagai macam komponen, baik komponen organik maupun
komponen anorganik (Gandjar dan Rohman, 2007).
Berdasarkan pada mekanisme pemisahannya, kromatografi dibedakan
menjadi kromatografi adsorbsi, kromatografi partisi, kromatografi pasangan ion,
kromatografi penukar ion, kromatografi eksklusi ukuran, dan kromatografi
afinitas. Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi atas
kromatografi kertas, kromatografi lapis tipis, yang keduanya sering disebut
dengan kromatografi planar, kromatografi gas dan kromatografi cair kinerja tinggi
(KCKT) (Gandjar dan Rohman, 2007).
D. Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi Cair Kinerja Tinggi atau KCKT merupakan teknik yang
sering digunakan dalam analisis kimia dengan kemampuannya dalam
memisahkan, menganalisis dan memurnikan suatu senyawa. Karakter KCKT
adalah dengan menggunakan pompa bertekanan tinggi untuk mempercepat
pemisahan, kolom yang dapat disesuaikan dalam memisahkan senyawa, kolom
yang dapat digunakan berulang kali, serta hasilnya lebih presisi dan reprodusibel
(Snyder, Kirkland, and Dorlan, 2010).
Sejumlah bidang yang menggunakan KCKT antara lain farmasi,
lingkungan, bioteknologi, polimer, dan industri-industri makanan. KCKT
merupakan metode yang tidak destruktif dan dapat digunakan baik untuk analisis
kualitatif maupun kuantitatif. Kelemahan metode KCKT ini adalah untuk
(MS) dan jika sampel sangat kompleks, maka resolusi yang baik sulit diperoleh
(Gandjar dan Rohman, 2007).
KCKT merupakan teknik dimana solute-solut terpisah oleh perbedaan
kecepatan elusi, karena solut-solut ini melewati suatu kolom kromatografi.
Pemisahan solut-solut ini diatur oleh distribusi solut dalam fase gerak dan fase
diam. Keberhasilan dalam menggunakan metode KCKT dipengaruhi pemilihan
jenis kolom, fase gerak, panjang dan diameter kolom, kecepatan alir fase gerak,
suhu kolom, dan ukuran sampel (Gandjar dan Rohman, 2007).
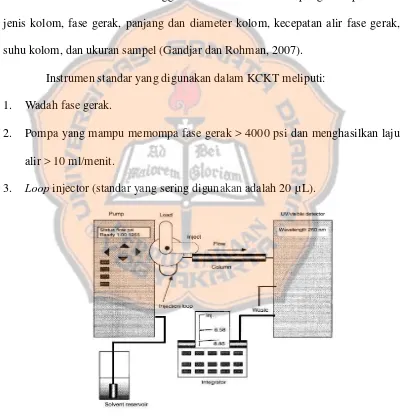
Instrumen standar yang digunakan dalam KCKT meliputi:
1. Wadah fase gerak.
2. Pompa yang mampu memompa fase gerak > 4000 psi dan menghasilkan laju
alir > 10 ml/menit.
3. Loop injector (standar yang sering digunakan adalah 20 µ L).
Gambar 4. Instrumen standar dalam KCKT (Watson, 1999)
4. Kolom yang biasanya dikemas dalam tabung stainless steel dengan berbagai
5. Detektor yang biasanya merupakan detektor UV/visibel.
6. Sistem perekam data, dapat berupa integrator atau PC software yang sesuai
untuk memproses data kromatogram.
7. Tabung penghubung di antara injektor dan detektor dengan narrow diameter
internal < 0,2 mm.
8. Instrumen yang lebih canggih mungkin memiliki sistem injeksi sampel
otomatis, memiliki oven untuk kolom, dan mampu mencampur dua atau lebih
fase gerak dengan berbagai proporsi
(Watson, 1999).
E. Validasi Metode Analisis
Validasi metode analisis adalah proses yang dibutuhkan memastikan
kualitas dan kepercayaan suatu hasil analisis (Ermer dan Miller, 2005). Suatu
metode analisis harus divalidasi untuk memastikan bahwa parameter-parameter
kinerjanya mampu untuk mengatasi masalah analisis. Suatu metode harus
divalidasi ketika:
1. Metode baru dikembangkan untuk mengatasi masalah analisis tertentu
2. Metode yang sudah baku direvisi untuk menyesuaikan perkembangan atau
ada masalah yang mengharuskan metode tersebut direvisi
3. Penjaminan mutu yang mengindikasikan bahwa metode baku telah berubah
4. Metode baku digunakan di laboratorium yang berbeda, oleh analis yang
berbeda, atau oleh instrument yang berbeda
5. Mendemonstrasikan kesetaraan antar 2 metode, seperti antara metode baku
Parameter-parameter validasi metode analisis dalam penelitian ini
meliputi:
1. Spesifisitas. Spesifisitas adalah kemampuan membedakan analit yang dituju
dengan senyawa lain yang ada dalam sampel (ICH Harmonised Tripartite,
2005).
2. Linearitas. Linearitas adalah kemampuan suatu prosedur analisis untuk
mengasilkan respon yang secara langsung proporsional dengan konsentrasi
analit dalam sampel (Ermer dan Miller, 2005).
3. Sensitifitas. Sensitifitas dapat dilihat dari nilai detection limit (DL) dan
quantitation limit (QL). DL adalah jumlah analit terendah dalam sampel yang
dapat dideteksi namun tidak harus dikuantitasi. QL adalah jumlah analit
terendah dalam sampel yang dapat ditentukan dengan presisi dan akurasi
yang dapat diterima dengan metode analisis yang (ICH Harmonised
Tripartite, 2005).
4. Akurasi. Akurasi suatu prosedur analisis merupakan kedekatan antara nilai
yang sebenarnya dengan nilai yang ditemukan dalam pengujian (Ermer dan
Miller, 2005).
5. Presisi. Presisi suatu prosedur analisis adalah kedekatan nilai yang diperoleh
antar seri pengukuran yang diperoleh dari sampel homogen yang sama pada
kondisi yang ditentukan. Presisi dapat dibagi menjadi tiga yaitu keterulangan,
presisi intermediet, dan reprodusibilitas. Keterulangan adalah presisi pada
kondisi operasional yang sama dalam jangka pendek. Presisi intermediet
peneliti, berbeda instrument, dan lain-lain. Reprodusibilitas adalah presisi
antar laboratorium (ICH Harmonised Tripartite, 2005).
F. Landasan Teori
Para-phenylenediamine (PPD) merupakan salah satu komponen utama
yang digunakan dalam pewarna rambut oksidatif. Dalam penggunaan jangka
pendek atau jangka panjang PPD dapat menimbulkan efek yang tidak diinginkan.
Penggunaannya dalam jangka pendek dapat menimbulkan sensitisasi, dermatitis,
mata iritasi dan berair, asma, gastritis, gagal ginjal, vertigo, tremor, kejang, dan
koma pada manusia. Sedangkan penggunaan jangka panjang dapat menimbulkan
dermatitis kontak eczematous dan kanker pada manusia. Menurut Dirjen POM RI
(2008), kadar PPD yang diperbolehkan dalam suatu sediaan pewarna rambut
sebesar 6%. Namun, dalam kenyataannya banyak sediaan pewarna rambut yang
tidak mencantumkan kadar PPD yang ditambahkan dalam produknya.
Pada penelitian ini akan dilakukan validasi metode analisis PPD dalam
pewarna rambut oksidatif. Metode yang valid selanjutnya dapat digunakan untuk
penetapan kadar PPD dalam pewarna rambut oksidatif sebagai salah satu sarana
penunjang penjaminan keamanan bagi pengguna. Komponen pewarna rambut
oksidatif yang diteliti terdiri atas PPD dan sodium perborat tetrahidrat serta
memiliki matriks yang kompleks yang terdiri dari ekstrak henna, ekstrak acacia
concina ,ekstrak emblica officinalis, dan asam sitrat sehingga diperlukan metode
pemisahan yang sesuai. Pemisahan PPD dari matriks sampelnya dilakukan
dengan ekstraksi solven air (kelarutan PPD dalam air pada 25oC sebesar 4% b/v)
itu, dilakukan clean-up menggunakan SPE C18 untuk memisahkan PPD dari
ko-ekstraktan yang mengganggu. PPD yang dielusi dengan air akan langsung terelusi
sementara matriks sampel akan tertahan dalam fase diam. Proses clean-up
diperlukan untuk memisahkan analit dari matriks sampel pengganggu sehingga
determinasi PPD tidak terganggu.
Hasil clean-up diinjeksikan ke KCKT fase terbalik yang sudah
dioptimasi (Emelia, 2015). Proses clean-up dikatakan berhasil apabila puncak
PPD terpisah dari puncak lainnya. Metoda analisis yang dikembangkan
merupakan metode analisis kuantitatif non-kompendial, maka parameter validasi
meliputi spesifisitas, linearitas, akurasi, presisi, dan ketahanan.
G. Hipotesis
1. Matriks formulasi pewarna rambut terdiri dari campuran yang kompleks
sehingga perlu dilakukan clean-up dengan metode pemisahan yang sesuai.
2. Ko-ekstraktan tertahan pada sistem SPE C18-air sehingga kurva adisi pada
hasil clean-up tidak berbeda signifikan dari kurva baku eksternal.
3. Metode analisis PPD dalam pewarna rambut oksidatif dengan ekstraksi
larutan sodium metabisulfit pH 8 dan clean-up C18-air dapat memenuhi
18 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Jenis penelitian ini adalah eksperimental karena terdapat perlakuan
terhadap subjek uji.
B. Variabel Penelitian
1. Variabel bebas
Variabel bebas dalam penelitian ini adalah volume loading ekstrak
sampel ke kolom SPE dan massa adisi PPD yang diadisikan ke sampel dan ke
esktrak sampel.
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah waktu retensi, resolusi, %
perolehan kembali metode SPE C18, koefisien korelasi (r) antara massa total PPD
dan AUC, slope kurva baku adisi, koefisien variansi (CV) dan % perolehan
kembali metode standar adisi.
3. Variabel pengacau terkendali
Kemurnian pelarut yang digunakan, dapat diatasi dengan menggunakan
pelarut pro analysis yang memiliki kemurnian tinggi.
C. Definisi Operasional
1. Para-phenylendiamine yang dianalisis adalah senyawa aktif yang berada
2. Sistem Kromatografi Cair Kinerja Tinggi (KCKT) yang dipergunakan adalah
seperangkat alat KCKT fase terbalik dengan jenis fase diam C18, suhu
kolom, komposisi fase gerak, serta flowrate yang optimum.
3. Solid phase extraction (SPE) adalah teknik pemisahan analit dari matriks
sampelnya menggunakan fase diam berbentuk padat. SPE yang digunakan
adalah SPE C18.
4. Parameter validasi metode clean-up PPD dengan SPE adalah linearitas yang
dilihat dari koefisien korelasi (r) dan akurasi yang dilihat dari % perolehan
kembali.
5. Parameter validasi metode penetapan kadar PPD dengan KCKT adalah
linearitas yang dilihat dari koefisien korelasi (r), sensitivitas yang dilihat dari
slope, presisi yang dilihat dari koefisien variansi (CV) dan akurasi yang
dilihat dari % perolehan kembali.
6. Pelarut adalah cairan yang digunakan untuk melarutkan PPD atau sampel
yaitu larutan sodium metabisulfit 0,1 M dan sodium metabisulfit 0,1 M pH 8.
7. Volume loading ekstrak sampel adalah volume ekstrak sampel yang
ditambahkan pada SPE pada saat retensi sampel.
D. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah baku
p-phenylenediamine (Sigma Aldrich), pewarna rambut oksidatif, metanol,
asetonitril, larutan amonia 25% dengan kualitas pro analysis (E. Merck), sodium
E. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah neraca analitik (OHAUS
Pioneer™ PA214), instrumen KCKT yang meliputi injektor (Rheodyne 7125;
Loop 20µL), pompa (Waters Model 510) dengan sistem elusi isokratik, detektor
(Waters Associates Model 441), kolom C-18 (Shinwa Chemical Industries, LTD
STR ODS – II; dimensi 150 x 4,0 mm; 5µm), seperangkat komputer dengan CBM
(Shimadzu 102) dan perangkat lunak (Shimadzu Labsolutions: GC solution versi
2.30.00SU4, alat ultrasonifikasi (Branson 3510), alat sentifugasi (MSE 0682A),
desilator aquabidest (Thermo Scientific), organic and anorganic solvent
membrane filter (Whatman) dengan ukuran pori 0,45 m, syringe, mikropipet
(Socorex), milipore filter, pH meter (Hanna), indikator pH universal (E.Merck),
tabung mikrosentrifus 1,5 mL (Eppendorf) dan seperangkat alat-alat gelas (Pyrex).
F. Tata Cara Penelitian
1. Penyiapan sampel pewarna rambut oksidatif
Dua puluh bungkus pewarna rambut oksidatif disiapkan. Serbuk pewarna
rambut ditimbang satu per satu untuk pengujian keseragaman bobot. Setelah
dilakukan uji keseragaman bobot kemudian serbuk pewarna rambut
dihomogenkan dengan menggunakan mortir dan stamper. Serbuk yang sudah
dihomogenkan disimpan dalam wadah yang kering, tertutup rapat, dan
dimasukkan ke lemari pendingin.
2. Pembuatan larutan sodium metabisulfit 0,01 M
sodium metabisulfit sebanyak 1,9 g ditimbang dan dilarutkan dalam
3. Pembuatan larutan sodium metabisulfit 0,01 M pH 8
Larutan sodium metabisulfit 0,01 M ditambah dengan larutan ammonia
10 % sedikit demi sedikit sampai larutan mencapai pH 8.
4. Pembuatan fase gerak untuk KCKT
Aquadest sebanyak 90 mL yang telah ditambah amonia 10% sebanyak
100 µL dicampurkan dengan asetonitril sebanyak 10 mL. Fase gerak disaring
menggunakan kertas saring Whatman dengan dibantu pompa vakum kemudian
gas dihilangkan dengan ultrasonifikasi selama 20 menit.
5. Validasi metode pengukuran PPD dengan KCKT
a. Pembuatan larutan stok baku PPD 2 mg/mL. Larutan stok baku PPD dibuat
dengan konsentrasi 2 mg/mL dengan menggunakan pelarut larutan natrium
metabisulfit 0,01 M.
b. Pembuatan larutan intermediet PPD 40 µg/mL. Larutan intermediet PPD
dengan konsentrasi 40 g/mL dibuat dengan pengenceran stok baku PPD
dengan konsentrasi 2 mg/mL. Pengenceran menggunakan pelarut natrium
metabisulfit 0,01 M.
c. Pembuatan larutan seri baku PPD. Seri konsentrasi larutan PPD 1, 2, 3, 4, 6,
8, dan 10 ng/µ L dibuat dengan mengencerkan larutan intermediet PPD
dengan fase gerak KCKT. Larutan seri konsentrasi PPD diinjeksikan ke
dalam KCKT fase terbalik dengan kolom C18, komposisi fase gerak ACN :
aquades/ ammonium hidroksida 10% (10:90), kecepatan alir 0,5 mL/ menit,
detektor UV dengan panjang gelombang 254 nm sesuai dengan hasil
6. Identifikasi para-phenylenediamine (PPD) dalam pewarna rambut dan perbandingan ekstrak sampel pewarna rambut sebelum dan sesudah
clean-up dengan SPE C18 dengan KCKT
Pada penelitian ini dilakukan identifikasi dalam sampel pewarna rambut
dengan menggunakan KCKT. Cara yang dilakukan yaitu dengan membandingkan
waktu retensi dan bentuk puncak antara baku PPD dan sampel pewarna rambut
untuk mengetahui apakah dalam sampel pewarna rambut terdapat PPD.
a. Ekstraksi PPD dari pewarna rambut. Sampel pewarna rambut oksidatif yang
telah dihomogenkan ditimbang seksama lebih kurang 300 mg, dimasukkan
dalam tabung sentrifus, ditambah 10 mL larutan sodium metabisulfit 0,01 M
pH 8. Suspensi dikocok dan disentifus selama 10 menit dengan kecepatan
3000 rpm. Cairan supernatan diambil, dimasukkan ke dalam labu takar 50
mL. Endapan ditambah 10 mL larutan sodium metabisulfit 0,01 M pH 8,
sentrifus selama 10 menit dengan kecepatan 3000 rpm. Cairan supernatan
diambil, dimasukkan ke dalam labu takar 50 mL. Langkah ini diulang
sebanyak dua kali. Supernatan dalam labu takar 50 mL diencerkan dengan
larutan sodium metabisulfit 0,01 M hingga batas tanda. Sejumlah 1 mL
larutan tersebut diambil dan dimasukkan ke dalam labu takar 10 mL
kemudian diencerkan dengan larutan sodium metabisulfit 0,01 M hingga
batas tanda.
b. Clean-up sampel dengan SPEC18. Sebelum digunakan SPE dialiri dengan
6 mL aquadest. Seratus mikroliter ekstrak sampel yang telah diencerkan
dilakukan dengan menggunakan 900 µL aquadest ditampung dalam tabung
mikrosentrifus yang sama.
c. Identifikasi PPD dalam eluat hasil clean-up dengan SPE. Eluat disaring
dengan menggunakan milipore dan diinjeksikan ke dalam sistem KCKT.
Kromatogram dibandingkan dengan kromatogram baku PPD konsentrasi 8
g/mL.
d. Perbandingan antara sampel pewarna rambut oksidatif sebelum dan sesudah
clean-up dengan SPE C18. Sejumlah eluat SPE dan larutan dalam labu takar
10 mL diambil dan diinjeksikan dalam KCKT. Kromatogram keduanya
dibandingkan.
7. Optimasi clean-up dengan SPE C18
Sebelum digunakan SPE dialiri dengan 6 mL aquadest. Sejumlah ekstrak
sampel yang telah diencerkan dimasukkan ke dalam SPE, ditampung dalam
tabung mikrosentrifus. Elusi dilakukan dengan menggunakan aquadest ditampung
dalam tabung mikrosentrifus yang sama. Optimasi clean-up dilakukan dengan
memvariasi volume loading sampel untuk mengetahui kapasitas SPE mengikat
pengotor dalam sampel. Volume loading sampel yang digunakan 100 µL dan 1
mL. Hasil clean-up dianalisis dengan menggunakan KCKT. Kromatogram
volume loading sampel dibandingkan jumlah dan besarnya puncak selain puncak
PPD.
8. Validasi metode clean-up PPD dengan SPE C18
a. Ekstraksi PPD dari sampel pewarna rambut oksidatif. Sampel pewarna
300 mg, dimasukkan dalam tabung sentrifus, ditambah 10 mL larutan
sodium metabisulfit 0,01 M pH 8. Suspensi dikocok dan disentifus selama
10 menit dengan kecepatan 3000 rpm. Cairan supernatan diambil,
dimasukkan ke dalam labu takar 50 mL. Endapan ditambah 10 mL larutan
sodium metabisulfit 0,01 M pH 8, sentrifus selama 10 menit dengan
kecepatan 3000 rpm. Cairan supernatan diambil, dimasukkan ke dalam labu
takar 50 mL. Langkah ini diulang sebanyak dua kali. Supernatan dalam labu
takar 50 mL diencerkan dengan larutan sodium metabisulfit 0,01 M hingga
batas tanda. Sejumlah 1 mL larutan tersebut diambil dan dimasukkan ke
dalam labu takar 10 mL kemudian diencerkan dengan larutan sodium
metabisulfit 0,01 M hingga batas tanda.
b. Validasi metode clean-up PPD dengan SPE C18. Sebelum dilakukan
clean-up, ke dalam masing-masing 300 µL ekstrak sampel yang telah diencerkan
ditambah 0, 10, 20, 30, 40 dan 50 µL baku PPD di dalam tabung
mikrosentrifus. Clean-up dilakukan dengan memasukkan 100, 103, 107,
110, 113 dan 117 µL dari masing-masing tabung mikrosentrifus . Elusi
dilakukan dengan 900, 897, 893, 890, 887 dan 883 µL aquadest. Eluat
disaring dengan menggunakan milipore dan diinjeksikan ke dalam KCKT.
9. Validasi metode penetapan kadar PPD dengan metode standar adisi
a. Pembuatan kurva baku adisi dalam matriks sampel pewarna rambut. Kurva
baku adisi dibuat dengan menambahkan 2, 4, 7, 10, 15 dan 20 mg baku PPD
b. Ekstraksi PPD dalam sampel pewarna rambut. Masing-masing sampel
dimasukkan dalam tabung sentrifus, ditambah 10 mL larutan sodium
metabisulfit 0,01 M pH 8. Suspensi dikocok dan disentrifus selama 10 menit
dengan kecepatan 3000 rpm. Cairan supernatan diambil, dimasukkan ke
dalam labu takar 50 mL. Endapan ditambah 10 mL larutan sodium
metabisulfit 0,01 M pH 8, sentrifus selama 10 menit dengan kecepatan 3000
rpm. Cairan supernatan diambil, dimasukkan ke dalam labu takar 50 mL.
Langkah ini diulang sebanyak 2 kali. Supernatan dalam labu takar 50 mL
diencerkan dengan larutan sodium metabisulfit 0,01 M hingga batas tanda.
Sejumlah 1 mL larutan tersebut diambil dan dimasukkan ke dalam labu
takar 10 mL kemudian diencerkan dengan larutan sodium metabisulfit 0,01
M hingga batas tanda.
c. Clean-up sampel dengan SPEC18. Clean-up dilakukan sesuai dengan hasil
optimasi langkah 7.
d. Determinasi PPD dengan KCKT. Eluat disaring dengan menggunakan
milipore dan diinjeksikan ke dalam KCKT.
10. Penetapan kadar para-phenylenediamine (PPD) dalam pewarna rambut dengan metode standar adisi
Sampel pewarna rambut oksidatif yang telah dihomogenkan ditimbang
seksama lebih kurang 300 mg, dimasukkan dalam tabung sentrifus, ditambah 10
mL larutan sodium metabisulfit 0,01 M pH 8. Suspensi dikocok dan disentrifus
selama 10 menit dengan kecepatan 3000 rpm. Cairan supernatan diambil,
dimasukkan ke dalam labu takar 50 mL. Endapan ditambah 10 mL larutan
3000 rpm. Cairan supernatan diambil, dimasukkan ke dalam labu takar 50 mL.
Langkah ini diulang sebanyak 2 kali. Supernatan dalam labu takar 50 mL
diencerkan dengan larutan sodium metabisulfit 0,01 M hingga batas tanda.
Sejumlah 1 mL larutan tersebut diambil dan dimasukkan ke dalam labu takar 10
mL kemudian diencerkan dengan larutan sodium metabisulfit 0,01 M hingga batas
tanda. Clean-up dilakukan sesuai dengan hasil optimasi langkah 7. Eluat disaring
dengan menggunakan milipore dan diinjeksikan ke dalam KCKT. Penetapan kadar
dilakukan dengan metode standar adisi dengan menambahkan 2, 4, 7, 10, 15 dan
20 mg baku PPD ke dalam masing-masing 300 mg sampel pewarna rambut.
G. Analisis Hasil
1. Validasi metode pengukuran PPD dengan KCKT
Parameter validasi yang ditetapkan yaitu linearitas dan sensitivitas
dengan melihat dari kurva baku PPD.
a. Linearitas. Linearitas dinyatakan dengan koefisien korelasi (r). Luas area
diplotkan terhadap massa PPD (minimum 5 konsentrasi) untuk memperoleh
persamaan regresi linear dengan persamaan y = bx + a (ICH Harmonised
Tripartite, 2005).
b. Sensitivitas. Sensitivitas dapat ditentukan dengan nilai slope, DL, dan QL.
1) Slope didapatkan dari persamaan regresi linear y= bx+a (b = slope; a =
intersep).
2) DL dapat dihitung dengan rumus:
Keterangan:
σ = standar deviasi dari respon
S = slope kurva baku eksternal
3) LOQ dapat dihitung dengan rumus:
QL= 10 � (2)
Keterangan:
σ = standar deviasi dari respon
S = slope kurva baku eksternal
(ICH Harmonised Tripartite, 2005).
2. Analisis hasil identifikasi PPD dalam sampel pewarna rambut oksidatif
Data kromatogram antara sampel dan baku PPD dibandingkan (ICH
Harmonised Tripartite, 2005).
3. Analisis hasil perbandingan sampel sebelum dan sesudah clean-up
dengan SPE C18
Data kromatogram antara sampel sebelum SPE dan sesudah SPE
dibandingkan dan nilai resolusi antara puncak analit dan puncak terdekat dihitung
(ICH Harmonised Tripartite, 2005).
Dalam KCKT, resolusi didefinisikan sebagai perbedaan antara waktu
retensi dua puncak yang saling berdekatan dibagi dengan rata-rata lebar puncak.
Resolusi (Rs) dapat dihitung dengan rumus:
Rs = 2∆
�1+�2 (3)
4. Analisis hasil optimasi clean-up PPD dalam sampel dengan SPE C18
Data kromatogram antara volume loading sampel 100 µL dan volume
loading sampel 1000 µ L dibandingkan (ICH Harmonised Tripartite, 2005).
5. Validasi metode clean-up PPD dalam sampel dengan SPE C18
Parameter validasi yang ditetapkan yaitu linearitas, akurasi, dan presisi
(keterulangan).
a. Linearitas. Linearitas dinyatakan dengan koefisien korelasi (r). Luas area
diplotkan terhadap massa total PPD yang ada dalam ekstrak pewarna
rambut yang telah diadisi (minimum 5 konsentrasi) untuk memperoleh
persamaan regresi linear dengan persamaan y = bx + a (ICH Harmonised
Tripartite, 2005).
b. Akurasi. Akurasi dinyatakan dengan % perolehan kembali.
% perolehan kembali dapat dihitung dengan menggunakan rumus:
% perolehan kembali = − ( )
( � � � ℎ ) x 100% (4)
c. Presisi (keterulangan). Presisi (keterulangan) dinyatakan dengan nilai
coefficient of variation (CV). CV dihitung pada setiap replikasi.
Rumus CV yaitu:
CV = � �
− x 100% (5)
5. Validasi penetapan kadar PPD dengan metode standar adisi
Parameter validasi yang ditetapkan yaitu linearitas, sensitivitas, akurasi
dan presisi intermediet.
a. Linearitas. Linearitas dinyatakan dengan koefisien korelasi (r). Luas area
rambut yang telah diadisi (minimum 5 konsentrasi) untuk memperoleh
persamaan regresi linear dengan persamaan y = bx + a.
b. Sensitivitas. Sensitivitas ditentukan dengan nilai slope. Slope didapatkan
dari persamaan regresi linear y= bx+a (b = slope; a = intersep).
c. Akurasi. Akurasi dinyatakan dengan % perolehan kembali.
% perolehan kembali dapat dihitung dengan menggunakan rumus (4).
d. Presisi intermediet. Presisi intermediet kurva baku adisi ditentukan dengan
uji signifikansi nilai slope 3 replikasi antarhari seri kurva baku adisi
menggunakan ANOVA satu arah.
6. Pengaruh matriks pewarna rambut dalam penetapan kadar para-phenylenediamine (PPD)
Slope kurva baku dibandingkan dengan slope kurva baku adisi untuk
mengetahui pengaruh matriks pada metode analisis PPD dalam pewarna rambut.
Perbedaan slope dihitung melalui uji signifikansi (uji t).
7. Penetapan kadar para-phenylenediamine (PPD) dalam pewarna rambut dengan metode standar adisi
Penetapan kadar dihitung dengan persamaan kurva baku adisi. Besarnya
30 BAB IV
HASIL DAN PEMBAHASAN
Para-phenylenediamine (PPD) adalah salah satu senyawa yang
digunakan dalam pewarna rambut tipe oksidasi. Penggunaan PPD dalam pewarna
rambut dapat menimbulkan alergi dan bahkan kanker. Menurut Dirjen POM RI
(2008), batas konsentrasi kandungan PPD dalam sediaan pewarna rambut sebesar
6%, namun konsentrasi kandungan PPD dalam pewarna rambut tidak
dicantumkan. Oleh karena itu, dalam penelitian ini peneliti ingin menetapkan
validasi metode analisis PPD dalam pewarna rambut oksidatif. Penetapan kadar
PPD dalam pewarna rambut oksidatif diawali dengan ekstraksi dengan solven air
kemudian dilakukan clean-up dengan SPE C18 dan diinjeksikan dalam KCKT.
Menurut Emelia (2015), metode KCKT memiliki validitas yang baik dengan
persamaan regresi linear y= 2267,62792 x – 46155,41523; koefisien korelasi (r) =
0,9922, %CV= 2-11% ; LOD= 489 ng/mL.
A. Penyiapan sampel pewarna rambut oksidatif
Sampel yang digunakan dalam penelitian ini diambil dari enam toko
yang ada di Yogyakarta. Sampel yang diambil berasal dari batch yang sama
dengan tujuan sampel mengalami proses produksi yang sama sehingga lebih
homogen. Sebelum sampel dianalisis, dilakukan uji keseragaman bobot untuk
memastikan bahwa kadar senyawa PPD yang terkandung dalam setiap sediaan
pewarna rambut seragam.
Uji keseragaman bobot dilakukan dengan cara menimbang satu per satu
kemudian dihitung bobot rata-ratanya. Syarat penyimpangan terhadap
penimbangan satu per satu terhadap bobot rata-rata tidak lebih dari 15% untuk 2
bungkus dan dan tidak lebih dari 10% untuk 18 bungkus (Syamsuni, 2005).
Bobot rata-rata hasil penimbangan 20 bungkus yaitu 9,0 g. Data hasil
penimbangan (Lampiran 2) menunjukkan ada 7 kemasan yang bobotnya
menyimpang lebih dari 10% dari bobot rata-rata dan 3 kemasan yang bobotnya
lebih dari 15% dari bobot rata-rata. Oleh karena itu, pewarna rambut oksidatif
yang digunakan dalam penelitian ini tidak memenuhi syarat keseragaman bobot.
PPD merupakan senyawa yang mudah teroksidasi (tidak stabil) saat
terpapar dengan udara. Sehingga perlu dilakukan penjaminan agar metode tetap
robust dengan cara sampel disimpan dengan mengalirkan gas nitrogen ke dalam
wadah kemudian ditutup dengan rapat dan disimpan dalam lemari pendingin. PPD
akan teroksidasi saat terpapar udara, sehingga diperlukan nitrogen untuk
menggantikan posisi udara dalam wadah dan ditutup rapat untuk mencegah
masuknya udara. Wadah disimpan dalam lemari pendingin untuk menjaga
kestabilan sampel.
B. Validasi metode pengukuran PPD dengan KCKT
Validasi metode pengukuran adalah suatu prosedur penjaminan bahwa
metode pengukuran yang digunakan dapat dipercaya dan diterima sehingga dapat
digunakan untuk pengukuran tertentu. Validasi metode pengukuran dilakukan
dengan pembuatan kurva baku PPD. Parameter validasi yang digunakan yaitu
Pembuatan kurva baku PPD bertujuan untuk mengetahui apakah
hubungan antara massa analit dan respon instrumen linear. Larutan seri
konsentrasi PPD yang digunakan yaitu 1, 2, 3, 4, 6, 8, dan 10 ng/µL. Pelarut yang
digunakan dalam pembuatan kurva baku adalah air yang diberi antioksidan
sodium metabisulfit untuk mencegah oksidasi PPD. Persamaan regresi linear yang
didapat merupakan hubungan antara massa PPD dan respon instrumen.
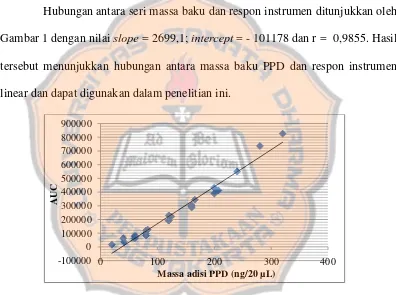
Hubungan antara seri massa baku dan respon instrumen ditunjukkan oleh
Gambar 1 dengan nilai slope = 2699,1; intercept = - 101178 dan r = 0,9855. Hasil
tersebut menunjukkan hubungan antara massa baku PPD dan respon instrumen
linear dan dapat digunakan dalam penelitian ini.
Gambar 6. Kurva hubungan seri massa baku PPD dan respon instrumen (AUC) Linearitas merupakan kemampuan metode analisis dalam memberikan
hasil uji yang secara langsung proporsional dengan konsentrasi analit pada kisaran
yang diberikan (Gandjar dan Rohman, 2007). Batasan koefisien korelasi yang
digunakan dalam penelitian ini menggunakan batasan dari Pearson’s correlation
coefficient test yang dapat dilihat pada Lampiran. Linearitas dinyatakan dalam
nilai koefisien korelasi (r), dimana koefisien korelasi memiliki hubungan dengan
banyaknya determinasi yang dilakukan (n). Bila r yang didapat dari regresi linear
nilainya lebih besar daripada yang ada pada tabel, maka secara statistik hubungan
linearitas pada kurva baku sudah terpenuhi.
Pada penelitian ini juga dilakukan uji linearitas pada hari yang berbeda
untuk memastikan bahwa instrumen yang digunakan tetap valid meskipun
dilakukan pada hari yang berbeda. Hal ini dilakukan karena berdasarkan
pengalaman selama penelitian PPD mudah teroksidasi. Hasil uji linearitas
ditunjukkan pada Tabel I.
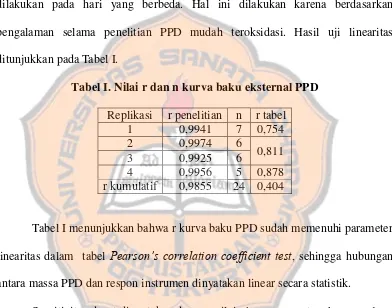
Tabel I. Nilai r dan n kurva baku eksternal PPD
Replikasi r penelitian n r tabel
1 0,9941 7 0,754
2 0,9974 6
0,811
3 0,9925 6
4 0,9956 5 0,878
r kumulatif 0,9855 24 0,404
Tabel I menunjukkan bahwa r kurva baku PPD sudah memenuhi parameter
linearitas dalam tabel Pearson’s correlation coefficient test, sehingga hubungan
antara massa PPD dan respon instrumen dinyatakan linear secara statistik.
Sensitivitas dapat dinyatakan dengan nilai slope, paramater detectionlimit
(DL) dan quantification limit (QL). Semakin besar nilai slope maka semakin baik
sensitivitas, semakin kecil nilai DL dan QL semakin baik sensitivitas. Nilai slope
kumulatif yang diperoleh yaitu 2699,1. Nilai DL dan QL yang didapat secara
C. Identifikasi para-phenylenediamine dalam pewarna rambut oksidatif
Identifikasi PPD dalam sampel pewarna rambut oksidatif perlu dilakukan
dilakukan untuk mengetahui apakah di dalam pewarna rambut oksidatif yang
digunakan terdapat PPD atau tidak. Identifikasi dilakukan dengan
membandingkan kromatogram antara baku PPD dan sampel pewarna rambut
oksidatif. Pada metode KCKT, diperlukan sampel yang analitnya sudah terpisah
dari ko-ekstraktan dalam sampel agar tidak mengganggu determinasi analit, oleh
karena itu dilakukan clean-up dengan Solid Phase Extraction (SPE). Berikut
Gambar 7. Kromatogram dengan fase diam C18, fase gerak asetonitril:air (10:90), laju
alir = 0,5 mL/menit, volume inject 20 µL (A) Larutan sodium metabisulfit,tR = 2,147
menit (B) Baku PPD 8 g/mL, tR = 4,834 menit (C) Sampel pewarna rambut oksidatif
setelah clean-up, tR PPD = 4,872 menit
Gambar 7 menunjukkan bahwa dalam sampel pewarna rambut oksidatif
terdapat PPD yang ditunjukkan oleh adanya waktu retensi (tR) yang sama pada
kromatogram baku PPD dan sampel yaitu pada tR 4,8 menit (Gambar 7B dan 7C). A
B
Puncak yang muncul di sekitar tR1,9 – 2,1 menit adalah puncak dari pelarut yang
digunakan yaitu sodium metabisulfit yang dibuktikan oleh Gambar 7A.
D. Perbandingan antara ekstrak sampel pewarna rambut sebelum dan sesudah clean-up dengan SPE C18
Formulasi pewarna rambut oksidatif dalam penelitian ini mempunyai
komposisi yang kompleks yaitu PPD, sodium perborat tetrahidrat, ekstrak henna,
ekstrak Acacia concina, ekstrakEmblica officinalis, dan asam sitrat. Oleh karena
itu, dibutuhkan proses clean-up dengan SPE yang bertujuan untuk memisahkan
PPD dari matriks sampel (ko-ekstraktan) yang mengganggu dalam deteksi analit.
Pada penelitian ini dibandingkan antara ekstrak sampel sebelum dan sesudah
dilakukan clean-up dengan SPE C18 untuk melihat apakah metode clean-up
Gambar 8. Kromatogram dengan fase diam C18, fase gerak asetonitril:air (10:90), laju alir
= 0,5 mL/menit, volume inject 20 µL (A) ekstrak sampel sebelum dilakukan clean-up dengan
SPE C18, (B) Ekstrak sampel sesudah dilakukan clean-up dengan SPE C18
Gambar 8 menunjukkan bahwa clean-up dengan SPE C18 dapat
memisahkan PPD dari matriks sampel yang mengganggu dalam determinasinya.
Pada Gambar 8B dapat dilihat puncak PPD muncul pada tR 4,8 menit dan
terpisah dari puncak lainnya dengan resolusi ≥ 1,5. Hal ini menunjukkan bahwa
metode yang digunakan sudah memenuhi parameter spesifisitas.
E. Optimasi clean-up PPD dalam sampel dengan SPE C18
Ekstraksi merupakan proses untuk mengambil analit yang dituju dari
matriks sampelnya. Ekstraksi yang dilakukan menggunakan pelarut air yang
diberi antioksidan sodium metabisulfit pada pH 8. Sodium metabisulfit dipilih A
sebagai antioksidan karena merupakan antioksidan yang kuat dan stabil sehingga
dapat mencegah oksidasi PPD. PPD merupakan senyawa yang bersifat basa lemah
dengan pKa 6,42 dan 3,04. Menurut Corbett (1972), laju auto-oksidasi PPD
minimal terjadi saat pH 8, oleh karena itu digunakan pelarut dengan pH 8 untuk
meminimalkan auto-oksidasi pada PPD dan sekaligus untuk membuat PPD dalam
bentuk molekulnya. Endapan dan cairan solven dipisahkan dengan teknik
sentrifugasi.
Metode sentrifugasi dapat memisahkan PPD yang terekstrak dengan
matriks sampel dengan proses yang memanfaatkan gaya sentrifugal untuk
sedimentasi campuran. Komponen yang mempunyai massa jenis lebih besar akan
mengendap, menyisakan cairan supernatan yang mudah diambil. PPD akan berada
dalam larutan supernatan karena PPD larut dalam air.
Clean-up merupakan praperlakukan sampel yang bertujuan untuk
memisahkan analit dari komponen-komponen matriks yang mungkin menganggu
pada saat pengukuran atau deteksi analit. Pada penelitian ini clean-up dilakukan
dengan metode solid phase extraction (SPE) karena praktis dan hemat pelarut
(Watson, 1999). Strategi yang digunakan dalam clean-up dengan SPE ada 2
macam yaitu dengan memilih pelarut yang mampu mengelusi analit sehingga
analit tertahan pada penjerap dan komponen pengganggu terelusi atau dengan
memilih pelarut yang langsung dapat mengelusi analit sementara komponen
pengganggu tertahan dalam penjerap.
Pemilihan jenis SPE yang digunakan berdasarkan skema yang terdapat
digunakan air sebagai pelarut sampel. PPD bersifat polar dengan log Kow -0,25
sehingga PPD mudah larut dalam air. PPD bersifat basa lemah sehingga pH perlu
dijaga dengan cara membuat pH pelarut menjadi pH 8 untuk menjaga PPD tetap
dalam bentuk molekulnya (netral). Oleh karena itu, PPD akan sulit tertahan dalam
penjerap sehingga diperlukan penjerap yang mampu menahan komponen
pengotornya.
Gambar 9. Skema untuk pemilihan jenis SPE (Sigma-Aldrich, 1998).
Komponen-komponen yang kemungkinan terjerap adalah