| Prosiding Pertemuan Ilmiah dan Seminar Nasional MPHPI 2011 69
OPTIMALISASI UJI AKTIVITAS ENZIM KOLAGENASE DARI ORGAN DALAM
BANDENG (Chanos chanos Forskal)
Tatty Yuniarti1, Tati Nurhayati2, Agoes Mardiono Jacoeb2
1Sekolah Tinggi Perikanan, Bogor
2Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan IPB
Abstrak
Metoda uji aktivitas enzim kolagenase tidak sepenuhnya dapat digunakan untuk uji enzim yang sama pada organisme yang berbeda. Metode uji aktivitas enzim mengacu pada Moore dan Stein (1954). Optimalisasi uji aktivitas enzim kolagenase dilakukan agar dapat diperoleh data aktivitas enzim kolagenase yang valid. Optimalisasi uji ini dilakukan dengan memodifikasi konsentrasi reagen yang digunakan dalam uji aktivitas enzim. Tujuan dari penelitian ini adalah menentukan uji aktivitas enzim kolagenase dari organ dalam bandeng (Chanos chanos, Forskal). Dari hasil penelitian, diperoleh konsentrasi dan volume reagen yang digunakan dalam uji aktivitas enzim kolagenase yaitu 5 ml substrat kolagen; 1 ml buffer tris 50 mM dengan CaCl2 5 mM; 0,2 ml enzim kolagenase; TCA 0,5% sebanyak 0,2 ml; 1 ml ninhidrin 0,2%; isopropanol 50% sebanyak 5 ml.
Kata kunci: enzim kolagenase, Chanos chanos Forskal, uji aktivitas PENDAHULUAN
Berbagai macam metode digunakan untuk memperoleh data aktivitas enzim yang akurat. Bila penelitian utama adalah purifikasi enzim atau biokimia klinis enzim, maka penelitian akan terfokus pada kondisi optimal aktivitas enzim dan data yang diperlukan adalah keseluruhan substrat dan faktor-faktor yang mempengaruhi aktivitas enzim seperti pH optimal, temperature, buffering agent, ionic strength dan substrate instability. Bila focus penelitian adalah kinetika reaksi enzim, maka data yang diperlukan adalah kecepatan katalisasi reaksi enzim. Hal yang lebih penting lagi adalah penentuan metode aktivitas enzim yang dapat diperoleh dari literature atau penelitian pendahuluan (Allison 1996).
Uji aktivitas enzim tergantung pada asal enzim, jenis substrat, tujuan dari uji enzim (Allison 1996). Hal tersebut dikarenakan enzim merupakan biokatalisator yang bekerja dengan spesifitas yang tinggi sehingga metode uji aktivitas berbeda, reagen yang digunakan, konsentrasi reagen dan volume reagen yang digunakan serta modifikasi lain (Beynon dan Bond 2001). Metode uji aktivitas enzim kolagenase (EC 3.4.24.X dan EC 3.4.21.X) juga berbeda-beda. Nathery et al. (2004) menggunakan metode spektrofotometri pada panjang gelombang 590 nm dan pewarna commasiie blue untuk menentukan uji aktivitas enzim kolagenase dari 5-10 μg kolagenase bakteri dan hewan mamalia selama 2 jam. Lim et al. (1993) menentukan aktivitas kolagenase menggunakan radioaktif [14C].
Uji aktivitas enzim kolagenase dari Moore dan Stein (1954) digunakan pada uji aktivitas enzim kolagenase dari ikan makarel (Scromber japanicus) (Park et al. 2002) dan ikan
| Prosiding Pertemuan Ilmiah dan Seminar Nasional MPHPI 2011 70
filefish (Novodon modestrus) (Kim et al. 2002) dan pilorik kaeka ikan tuna (Thunnusthynnus)
(Byunet al. 2002). Uji aktivitas ini tidak dapat digunakan pada penentuan aktivitas kolagenase dari organ dalam bandeng. Oleh karena itu dilakukan penelitian untuk menentukan uji aktivitas yang optimal agar dapat menghasilkan data yang akurat. Tujuan penelitian ini adalah untuk menentukan konsentrasi ninhidrin, TCA dan L-leusin pada uji aktivitas enzim kolagenase dari organ dalam bandeng (Chanos chanos Forskal).
METODE Bahan dan Alat
Bahan utama yang digunakan pada penelitian adalah organ dalam bandeng fase
post rigor yaitu pilorik kaeka, hepatopankreas dan usus. Kolagen untuk substrat enzim, dibuat
dari kulit ikan bandeng dengan metode Lestari (2005). Bahan-bahan kimia yang digunakan adalah Triton-X 100, CaCl2, asam trikloro asetat, L-leusin, 1-propanol, dan pereaksi Bradford. Logam-logam yang digunakan untuk karakterisasi yaitu NaCl, CaCl2, MnCl2 dan CoCl2, inhibitor yang digunakan adalah EDTA, PMSF dan pepstatin. Peralatan yang digunakan antara lain spektrofotometer sinar tampak, sentrifus dingin, shaker inkubator, oven, mikropipet, homogenizer.
Metode Penelitian
Ektraksi enzim kolagenase diperoleh dari organ dalam bandeng, mengacu pada metode Kim et al. (2002) yang dimodifikasi. Substrat kolagen terbuat dari kulit bandeng. Pada penelitian ini akan dilakukan modifikasi konsentrasi ninhidrin, konsentrasi TCA dan jumlah enzim kolagenase yang ditambahkan secara bertahap.
Optimalisasi metode uji aktivitas kolagenase mengacu pada metoda spektrofotometri (Moore dan Stein 1954, diacu dalam Kim et al. 2002) yaitu sebanyak (0,2; 5; 10) ml larutan kolagenase ditambah dengan 5 mlml kolagen dan 1 ml 0,05 mM tris-HCl pada pH 7,5 yang mengandung 5 mM CaCl2. Reaksi ini dilakukan pada suhu 37 °C selama 1 jam. Reaksi dihentikan dengan penambahan 0,2 ml; (0,2; 0,5; 1; 2; 5; 10; 50)% TCA. Setelah 10 menit pada suhu ruang, larutan disentrifus pada 1.800 rpm selama 20 menit. Supernatan, sebanyak 0,2 ml dicampur dengan 1,0 ml larutan ninhidrin (0,2; 0,5; 1; 1,5; 2%), diinkubasi pada suhu 100 °C selama 20 menit, kemudian didinginkan pada suhu ruang. Campuran kemudian ditambah dengan 5 ml 50% 1-propanol dan diukur serapannya menggunakan spektrofotometer pada panjang gelombang 570 nm. Larutan buffer Tris-HCl digunakan sebagai blanko, dan L-leusin digunakan sebagai standar (asam amino hasil hidrolisis kolagenase). Satu unit aktivitas kolagenase didefinisikan sebagai jumlah enzim yang menyebabkan perubahan 1 μmol substrat per menit.
| Prosiding Pertemuan Ilmiah dan Seminar Nasional MPHPI 2011 71 UA= Ast- Abl Ast-Abl × P × 1 T Dimana:
A = Jumlah enzim yang menyebabkan perubahan 1 μmol substrat per menit pada suhu 37 °C, pH 8,0
Asp = Absorbansi sampel Ast = Absorbansi standar Abl = Absorbansi blanko P = Faktor pengenceran T = Waktu inkubasi
HASIL DAN PEMBAHASAN
Prinsip dari ujian aktivitas enzim kolagenase adalah enzim kolagenase memecah keseluruhan dari tiga rantai α menjadi ¾ dan ¼ molekul. Temperature pemecahan kolagen adalah 34-35 °C dan 28-29 °C. Molekul kolagen yang terpecah akan mengalami konformasi pada suhu 35 °C yang dapat diekstrak dengan pelarut organik, selama 60 menit (Condrex 2008). Reaksi pemecahan kolagen disajikan di bawah ini.
Kolagen + H2O kolagenase Peptida
Optimalisasi uji aktivitas kolagenase dilakukan secara bertahap. Pada tahap pertama dilakukan modifikasi jumlah enzim yang ditambahkan, kemudian konsentrasi TCA dan terakhir adalah konsentrasi ninhidrin. Asam trikloroasetat berfungsi sebagai agen untuk presipitasi atau memisahkan endapan protein dengan asam amino bebas (Beynon dan Bond 2001). Pada konsentrasi TCA sebesar 2%, 5%, 10% dan 50%, Tidak terdeteksi adanya aktivitas kolagenase, sehingga tidak dilakukan uji aktivitas lanjut dan data tidak ditampilkan. Diduga tidak terdeteksinya aktivitas enzim kolagenase karena TCA tidak hanya menghentikan aktivitas enzim dan mengendapkan protein, tetapi pada konsentrasi yang tinggi, TCA mendegradasi asam amino hasil hidrolisis enzim kolagenase, sehingga tidak memberikan warna ungu ketika ditambahkan ninhidrin (Beynon dan Bond 2001). Pada konsentrasi 0,2% dan 0,5% TCA aktivitas kolagenase terdeteksi dengan baik.
Bicsak dan Harper (1984) menggunakan soybean trypsin inhibitor 0,02% sebanyak 50 µl dan EDTA 100 mM sebanyak 50 µl kemudian memisahkan protein dan asam amino hasil hidrolisis kolagenase dari katak bullfrog (Rana catesbiana) dengan cara didiamkan semalam pada 37 °C kemudian disentrifuge menggunakan Beckman Microfuge 152 (10.000xg) selama 5 menit. Pewarnaan menggunakan 5 ml Biofluor dan dihitung selama 10 menit dengan Beckman LS3133 T scintillation counter.
| Prosiding Pertemuan Ilmiah dan Seminar Nasional MPHPI 2011 72
Penambahan 0,1-0,5% ninhidrin semakin meningkatkan absorbansi, menunjukkan semua perlakuan dapat terdeteksi adanya asam amino bebas dari larutan substrat kolagen yang didegradasi oleh enzim kolagenase dari ekstrak organ dalam bandeng. Ninhidrin digunakan untuk mendeteksi dan menduga adanya asam amino secara kuantitatif dalam jumlah kecil. Pemanasan ninhidrin yang berlebihan akan menghasilkan warna ungu pada semua asam amino yang mempunyai gugus α amino bebas. Pada kondisi yang sesuai intensitas warna yang dihasilkan dapat dipergunakan untuk mengukur konsentrasi asam amino secara kolorimetrik. Metoda ini sangat sensitif untuk pengukuran konsentrasi asam amino (Lehninger 1993). Namun pengukuran absorbansi yang optimal adalah pada absorban 0,200-0,800 (Adijuwana 1992).
Penambahan larutan enzim sebanyak 0,2 ml menunjukkan aktivitas yang signifikan. Semakin banyak jumlah enzim yang ditambahkan dengan volume substrat kolagen yang tetap, maka akan semakin kecil nilai absorbannya. Diduga karena enzim kolagenase mempunyai kerja yang spesifik dan dalam jumlah yang sedikit dalam lingkungan yang sesuai aktivitasnya tinggi untuk memecah substrat (Suhartono 1989). Hasil modifikasi reagen TCA, ninhidrin dan enzim disajikan pada Tabel 1.
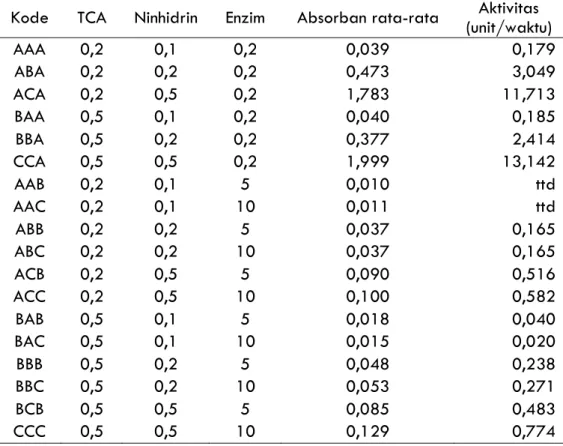
Tabel 1 Hasil uji aktivitas kolagenase organ dalam bandeng pada berbagai konsentrasi reagen
Kode TCA Ninhidrin Enzim Absorban rata-rata Aktivitas (unit/waktu) AAA 0,2 0,1 0,2 0,039 0,179 ABA 0,2 0,2 0,2 0,473 3,049 ACA 0,2 0,5 0,2 1,783 11,713 BAA 0,5 0,1 0,2 0,040 0,185 BBA 0,5 0,2 0,2 0,377 2,414 CCA 0,5 0,5 0,2 1,999 13,142 AAB 0,2 0,1 5 0,010 ttd AAC 0,2 0,1 10 0,011 ttd ABB 0,2 0,2 5 0,037 0,165 ABC 0,2 0,2 10 0,037 0,165 ACB 0,2 0,5 5 0,090 0,516 ACC 0,2 0,5 10 0,100 0,582 BAB 0,5 0,1 5 0,018 0,040 BAC 0,5 0,1 10 0,015 0,020 BBB 0,5 0,2 5 0,048 0,238 BBC 0,5 0,2 10 0,053 0,271 BCB 0,5 0,5 5 0,085 0,483 CCC 0,5 0,5 10 0,129 0,774
| Prosiding Pertemuan Ilmiah dan Seminar Nasional MPHPI 2011 73
Prosedur uji aktivitas kolagenase yang dimodifikasi adalah masukan 5 ml substrat kolagen, tambahkan 1 ml buffer tris 50 mM dengan CaCl2 5 mM, vortex hingga homogen,tambahkan 0,2 ml enzim kolagenase, inkubasikan dalam 37 oC selama 1 jam, keluarkan dari inkubator dan tambahkan TCA 0,5% sebanyak 0,2 ml, tunggu selama 19 menit, kemudian endapkan dengan sentrifus 1800 rpm selama 10 menit, ambil supernatan sebanyak 1 ml, tambahkan 1 ml ninhidrin 0,2% dan divortex, biarkan bereaksi selama 10 menit, kemudian dipanaskan pada suhu 100 oC selama 20 menit, Keluarkan dari oven dan biarkan dingin, tambahkan isopropanol 50% sebanyak 5 ml, divorteks kembali, ukur absorbannya pada panjang gelombang 570 nm.
KESIMPULAN
Uji aktivitas kolagenase metoda Moore dan Stein (1954) dapat diterapkan pada uji aktivitas enzim kolagenase dari organ dalam bandeng, tetapi memerlukan modifikasi. Modifikasi yang dilakukan adalah konsentrasi TCA sebesar 0,5%, konsentrasi ninhidrin sebesar 0,2% dan jumlah enzim 0,2 ml.
DAFTAR PUSTAKA
Allison RD. 1996. Current Protocols in Protein Science: New York, John Wiley & Sons, Inc. Beynon RJ, Bond JS. 2001. Proteolisis Enzymes: a Practical Approach. New York: Oxford
University Press.
Biscak TA, Harper E. 1984. Purification and Characterization of Tadpole Back-skin Collagenasewith Low Gelatinase Activity. The Journal Of Biological Chemist 259 (21): 13145-13150.
Bleeg HS. 1976. Collagenolytic enzymes assayed by spectrophotometry with suspensions of reconstituted collagen fibrils. Biochem. Biophys. Acta 445(3): 753-62.
Byun HG, Park JP, Sung NI, Kim SK. 2002. Purification and characterization of a serine proteinase from the tuna piloric caeca. J Food Biochem 26(6): 479-494.
Chondrex, Inc. 2008. Collagenase Assay Kit. Catalog # 3001 and 3002. USA.
Kim SK, Park PJ, Kim JB dan Sahidi F. 2002. Purification and characterization of a collagenolytic protease from filefish (Novodon modestrus). J. Biochem Mol Bio 35(2): 165-171.
Lim DV, Jackson RJ, Von Gruenigen. 1993. Purification and assay of bacterial collagenases.
Journal of microbiologi methods 18(3): 241-253.
Nathery A, Lyons JG, Grady RLO. 1984. A spectrophotometric collagenase assay. Analitical
Biochemistry 159: 390-395.
Park PJ, Lee SH, Byun HG, Kim SH, Kim SK. 2002. Purification and characterization of a collagenase from the Mackarel, Scomber japonicus. J Biochem Mol Bio. 35(6): 576-582. Suhartono MT. 1989. Enzim dan Bioteknologi. Bogor: IPB.
Yuniarti T, Nurhayati T, Jacoeb AM. 2010. Purifikasi dan karakterisasi kolagenase dari organ dalam bandeng (Chanos chanos Forskal). Biota. 15(3): 379-384