PENGARUH LAMA DAN SUHU STERILISASI PANAS BASAH TERHADAP VISKOSITAS DAN DAYA SEBAR
SEDIAAN EMULGEL ANTI-ACNE EKSTRAK KULIT BUAH MANGGIS (Garcinia mangostana L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Rosiana Cahyono
NIM: 108114179
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH LAMA DAN SUHU STERILISASI PANAS BASAH TERHADAP VISKOSITAS DAN DAYA SEBAR
SEDIAAN EMULGEL ANTI-ACNE EKSTRAK KULIT BUAH MANGGIS (Garcinia mangostana L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Rosiana Cahyono
NIM: 108114179
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
“The trouble is, you think you have time”
–
Buddha-
“If you have the motivation,
I don’t think anything in this world is impossible.
First, you have to start moving.
If you move, something will start”
–Kaito Kid, Kamen Rider Diend-
“If I wish for it, fate will always be my ally”
-Tendou Souji, Kamen Rider Kabuto-
Karya kecilku ini kupersembahkan untuk : Papa, Mama, Mak
Ricardo Kenny Chandra, S.Farm
Bapak/Ibu dosen dan staff pengajar Fakultas Farmasi USD
Sahabat-sahabatku tersayang
Serta
vii
PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas rahmat
dan karunia-Nya yang diberikan sehingga penyusunan skripsi yang berjudul
“PENGARUH LAMA DAN SUHU STERILISASI PANAS BASAH
TERHADAP VISKOSITAS DAN DAYA SEBAR SEDIAAN EMULGEL ANTI-ACNE EKSTRAK KULIT BUAH MANGGIS (Garcinia mangostana L.)” dapat dilaksanakan dengan baik. Skripsi ini disusun sebagai salah satu syarat untuk meraih gelar Sarjana Farmasi (S.Farm.) di Fakultas Farmasi, Universitas
Sanata Dharma, Yogyakarta.
Selama proses penelitian dan penyusunan skripsi ini, penulis mendapatkan
banyak bantuan dan dukungan dari berbagai pihak. Oleh karena itu, penulis
mengucapkan terima kasih kepada:
1. Papa, Mama dan Mak tercinta yang selalu memberi doa, dukungan dan
semangat kepada penulis selama proses penyusunan skripsi.
2. Ipang Djunarko, M.Sc., Apt., selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma.
3. C.M. Ratna Rini Nastiti, M.Pharm., Apt., selaku Ketua Program Studi
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
4. Dr. Sri Hartati Yuliani, M.Si., Apt., selaku dosen pembimbing yang telah
memberikan bimbingan, masukan, pengarahan serta motivasi dalam
viii
5. C.M. Ratna Rini Nastiti, M.Pharm., Apt. sebagai dosen penguji yang telah
memberikan kritik dan saran yang membangun selama proses pembuatan
skripsi.
6. Melania Perwitasari, M.Sc., Apt. sebagai dosen penguji yang telah
memberikan kritik dan saran yang membangun selama proses pembuatan
skripsi.
7. Enade Perdana Istyastono, Ph.D., Apt., yang telah memberikan masukan
dan saran kepada penulis.
8. Seluruh dosen dan karyawan Fakultas Farmasi Universitas Sanata
Dharma.
9. Mas Agung, Pak Musrifin, Pak Mukminin, Mas Bimo dan seluruh laboran
serta Mas Darto yang telah membantu peneliti pada proses pelaksanaan
penelitian di laboratorium.
10.Kristin Yunita dan Vivian, teman seperjuangan yang saling memberi
dukungan serta motivasi dalam menyelesaikan penelitan dan penyusunan
skripsi.
11.Ricardo Kenny Chandra, S.Farm., atas dukungan, semangat, doa,
kesabaran dan masukan yang selalu diberikan kepada penulis selama
proses penelitian dan penyusunan skripsi.
12.Sahabatku Anggun, Stien, Neno, Nover, Kezia atas kebersamaanya selama
ix
13.Teman-teman FST B 2010 atas kebersamaan, canda tawa, dan pengalaman
berharganya untuk penulis selama menjalani kuliah di Fakultas Farmasi
Universitas Sanata Dharma.
14.Semua pihak yang tidak dapat penulis sebutkan satu per satu yang telah
membantu dalam proses penyusunan skripsi ini.
Akhir kata, penulis menyadari bahwa masih banyak kekurangan dalam
penyusunan skripsi ini mengingat keterbatasan kemampuan dan pengetahuan
penulis.Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun
dari semua pihak.Semoga skripsi ini dapat memberikan manfaat bagi pembaca.
Penulis
x
PERNYATAAN KEASLIAN KARYA ………... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ……….. vi
xi
B. Variabel Penelitian dan Definisi Operasional ………... 17
1. Variabel penelitian ……….. 17
2. Definisi operasional ……… 17
C. Alat Penelitian ………... 18
D. Bahan ……… 19
E. Tata Cara Penelitian ……….. 19
1. Verifikasi ekstrak kulit manggis dan bakteri Staphylococcus epidermidis………. 19
2. Formula ………... 19
3. Pembuatan emulgel ………. 20
xii
5. Evaluasi sediaan emulgel ……….... 23
F. Analisis Hasil ……… 24
BAB IV. HASIL DAN PEMBAHASAN ………. 25
A. Identifikasi dan Verifikasi Kulit Manggis ………... 25
B. Pembuatan Emulgel Ekstrak Kulit Manggis ………. 26
C. Uji pH ………... 32
D. Sterilisasi Emulgel Ekstrak Kulit Manggis ….……….. 32
E. Uji Sterilitas Emulgel Ekstrak Kulit Manggis ..……… 34
F. Uji Sifat Fisis Emulgel Ekstrak Kulit Manggis ……… 37
1. Pengamatan Warna Emulgel ………... 38
2. Uji Viskositas dan Daya Sebar ………... 39
BAB V. KESIMPULAN DAN SARAN ……….. 44
A. Kesimpulan ………... 44
B. Saran ………. 44
DAFTAR PUSTAKA ………... 45
LAMPIRAN ……….. 47
xiii
DAFTAR TABEL
Tabel I. Formula emulgel acuan ………... 20 Tabel II. Formula emulgel yang telah dimodifikasi (100 g emulgel) … 20 Tabel III. Variasi suhu dan lama sterilisasi pada metode sterilisasi
panas basah ……….. 22
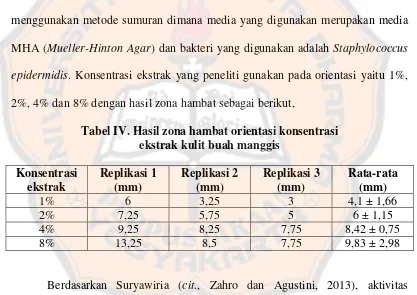
Tabel IV. Hasil zona hambat orientasi konsentrasi ekstrak kulit buah
manggis ………... 29
Tabel V. Klasifikasi aktivitasi antibakteri berdasarkan diameter zona
hambat ………. 29
xiv
DAFTAR GAMBAR
Gambar 1. Struktur alfa mangostin ………... 7
Gambar 2. Hasil identifikasi KLT ekstrak kulit manggis……….. 26
Gambar 3. Hasil uji pH emulgel ektrak kulit manggis ………. 32
xv
DAFTAR LAMPIRAN
Lampiran 1. Certificate of analysis dry extract ……… 48
Lampiran 2. Material safety data sheet mangosteen PE ……… 49
Lampiran 3. Hasil orientasi konsentrasi ekstrak kulit manggis pada
emulgel ……… 51 Lampiran 4. Penampakan emulgel anti-acne ekstrak kulit manggis
sebelum dan sesudah sterilisasi ………... 52
Lampiran 5. Penampakan emulgel anti-acne ekstrak kulit manggis
yang dioles pada kulit ………. 59
Lampiran 6. Hasil uji sterilitas emulgel anti-acne ekstrak kulit manggis 60
Lampiran 7. Hasil analisis statistik data viskositas dan daya sebar
emulgel anti-acne ekstrak kulit manggis menggunakan R .
xvi
INTISARI
Emulgel ekstrak kulit manggis merupakan suatu sediaan yang dapat digunakan sebagai obat jerawat. Sediaan yang digunakan untuk mengobati jerawat harus terjamin sterilitasnya karena jerawat dapat dikategorikan sebagai luka terbuka. Proses sterilisasi yang yang melibatkan panas seperti proses sterilisasi panas basah dapat mempengaruhi sifat fisik sediaan emulgel dimana sifat fisik sediaan dapat mempengaruhi penerimaan pasien terhadap sediaan tersebut. Penelitian ini dilakukan dengan tujuan untuk melihat pengaruh suhu dan lama sterilisasi panas basah terhadap viskositas dan daya sebar emulgel ekstrak kulit manggis.
Emulgel ekstrak kulit manggis disterlisasi dengan variasi suhu dan lama sterilisasi tertentu dan selanjutnya diuji sterilitasnya. Nilai viskositas dan daya sebar emulgel diukur 48 jam setelah proses pembuatan dan 48 jam setelah proses sterilisasi. Data yang didapatkan dianalisis secara statistik menggunakan R 3.0.1 untuk melihat adanya pengaruh suhu dan lama sterilisasi panas basah terhadap viskositas dan daya sebar emulgel ekstrak kulit manggis.
Hasil analisis menunjukkan terdapat perbedaan nilai viskositas dan daya sebar emulgel sebelum dan sesudah proses sterilisasi, namun pada saat sterilisasi tidak terdapat pengaruh suhu dan lama sterilisasi terhadap viskositas dan daya sebar emulgel ekstrak kulit manggis.
xvii
ABSTRACT
Emulgel with mangosteen pericarp extract is a preaparation which could be used as anti acne. Anti-acne preparation should be sterlized to ensure their sterility because ance could be categorized as an open wound. Sterilization process which involve heat such as steam sterilization could affect physical properties of emulgel. Physical properties could affect aceptibility to the patient. The aim of this research was to examine the effect of temperature and duration of steam sterilization on the viscosity and spreadability of emulgel.
Emulgel was sterlized with multiple sterilization temperature and duration then followed by sterility test. The value of viscosity and spreadability of emulgel measured 48 hours after preparation process and 48 hours after sterilization process. The acquired data then statically analyzed with R 3.0.1 to examine the effect of of temperature and duration of steam sterilization to viscosity and spreadabilty of emulgel.
The result showed that there was a difference between the value of viscosity and spreadability before and after sterilization process, but there is no effect of temperature and duration during steam sterilization on the viscosity and spreadability of emulgel with mangosteen pericarp extract.
1
BAB I PENGANTAR
A. LATAR BELAKANG
Wajah merupakan salah satu bagian tubuh yang penting dan membutuhkan
perlindungan agar selalu tetap bersih. Tidak hanya bagi kaum wanita, kebersihan
wajah bagi kamu pria juga penting adanya untuk menjaga penampilan. Salah satu
penyakit kulit yang kerap ditemui dan dapat mengganggu penampilan wajah
adalah jerawat. Staphylococcus epidermidis dan Propionibacterium acnes telah
dikenal sebagai bakteri penyebab utama terbentuknya jerawat. Bakteri tersebut
memiliki kemampuan untuk mensintesis lipase. Lipase ini akan mendegradasi
sebum trigliserida menjadi asam lemak bebas, yang mana hal ini akan memicu
respon inflamasi (Sukatta, Rughtaworn, Pitpiangchan, Dilokkunanant, 2008).
Oleh karena itu dibutuhkan anti-acne yang berguna untuk mengatasi jerawat
sehingga penampilan wajah dapat selalu terjaga.
Buah manggis dikenal sebagai buah dengan kandungan yang memiliki
banyak manfaat. Buah yang sering dijuluki “Queen of Fruits” mengandung lebih dari 40 jenis senyawa xanthone dan paling banyak ditemukan pada kulit manggis
(Subroto, 2008). Salah satu derivat xanthone yang paling banyak ditemukan pada
kulit manggis adalah alfa mangostin yang memiliki aktifitas antimikroba untuk
bakteri gram positif (Koh, Qiu, Zou, Lakshminarayanan, Li, Zhou, et al., 2012).
Alfa mangostin sebagai derivat xanthone yang berperan utama dalam
Pridgeon, Becnel, Clark, Lan, 2010). Oleh karena itu, ekstrak kulit manggis
diformulasikan dalam emulsi tipe m/a yang ditambahkan dengan gelling agent
sebagai peningkat stabilitas. Ketika sediaan emulsi dikombinasikan dengan gel
akan membentuk suatu sediaan baru yang disebut dengan emulgel. Sediaan
emulgel dapat meningkatkan acceptability pengguna karena memberikan sensasi
dingin dan tidak meninggalkan kesan greasy saat penggunaannya (Singla, Saini,
Joshi, Rana, 2012).
Jerawat dapat dikategorikan sebagai luka terbuka, oleh karena itu sediaan
yang digunakan untuk mengobati jerawat harus terjamin sterilitasnya (Benson and
Watkinson, 2012). Salah satu teknik sterilisasi yang sering digunakan yaitu
sterilisasi panas basah dengan menggunakan autoklaf pada suhu 121o C selama 15
menit (Ansel, Popovich, 2009). Pada teknik sterilisasi terdapat suhu sterilisasi dan
lama sterilisasi yang menjadi faktor kritis, karena suhu dan lama sterilisasi dapat
mempengaruhi efektifitas dari alfa mangostin. Salah satu karakteristik alfa
mangostin yang terkait dengan faktor kritis pada teknik sterilisasi yaitu melting
point alfa mangostin antara 180-182o C (Ghazali et al., 2010). Tidak hanya itu,
suhu dan lama sterilisasi dapat mempengaruhi sifat fisik sediaan yaitu viskositas
dan daya sebar sediaan. Sterilisasi dengan panas dapat mempengaruhi reologi dari
sediaan berpolimer seperti emulgel (Bindal, Narsimhan, Hem, Kulshreshtha,
1. Permasalahan
Bagaimana pengaruh suhu dan lama sterilisasi metode panas basah
terhadap viskositas dan daya sebar emulgel ekstrak kulit buah manggis?
2. Keaslian Penelitian
Sejauh pengetahuan peneliti, penelitian mengenai “Pengaruh Lama dan Suhu Sterilisasi Panas Basah terhadap Viskositas dan Daya Sebar Sediaan
Emulgel Antiacne Ekstrak Kulit Buah Manggis (Garcinia mangostana L.)”
belum pernah dilakukan. Terdapat penelitian terkait mengenai ekstrak kulit
manggis sebagai anti acne yaitu Somantri (2012), “Formulasi sediaan gel ekstrak etanol kulit buah manggis (Garcinia mangostana L.) dan uji aktivitas
terhadap bakteri penyebab jerawat”, pada penelitian tersebut dibuat tiga formula dengan variasi bahan pembentuk gel (carbomer dan HPMC) dan
konsentrasi basis gel (carbomer dan HPMC). Kesimpulan dari penelitian
tersebut adalah formula kedua dengan basis carbomer 1% memiliki zona
hambat luas terhadap Staphylococcus aureus yaitu 13 mm dan memiliki sifat
fisik yang paling baik.
Penelitian serupa lainnya yaitu oleh Sukatta et al., (2008),
“Development of Mangosteen Anti-Acne Gel” mengenai optimasi formula gel
anti-acne dengan ekstrak mangostin menggunakan desain faktorial. Hasil dari
penelitian tersebut adalah gel dengan konsentrasi carbopol ultrez 10 0,5 % dan
menghambat bakteri penyebab jerawat. Zona hambat yang dihasilkan pada
Staphylococcus epidermidis adalah 10 mm.
3. Manfaat Penelitian
a. Manfaat teoretis
Hasil penelitian diharapkan memberikan informasi ilmiah
mengenai pengaruh suhu dan lama sterilisasi metode panas basah terhadap
viskositas dan daya sebar emulgel ekstrak kulit buah manggis.
b. Manfaat praktis
Penelitian ini diharapkan dapat digunakan sebagai pertimbangan
dalam proses sterilasi emulgel ekstrak kulit buah manggis.
c. Manfaat metodologis
Diharapkan pada penelitian ini didapatkan hasil sediaan emulgel
ekstrak kulit manggis yang steril, dapat memenuhi persyaratan viskositas
dan daya sebar yang dapat diterima oleh konsumen.
B. Tujuan Penelitian 1. Tujuan umum
Penelitian ini bertujuan untuk mengetahui pengaruh suhu dan lama
sterilisasi metode panas basah terhadap viskositas dan daya sebar emulgel
2. Tujuan Khusus
Tujuan khusus dari penelitian ini yaitu mengetahui pengaruh suhu
dan lama sterilisasi metode panas basah terhadap viskositas dan daya sebar
6
BAB II
PENELAAHAN PUSTAKA
A. Jerawat
Jerawat adalah kondisi abnormal kulit akibat gangguan berlebihan
produksi kelenjar minyak (sebaceous gland) yang menyebabkan penyumbatan
saluran folikel rambut dan pori-pori kulit. Peradangan pada kulit terjadi jika
kelenjar minyak memproduksi minyak kulit (sebum) secara berlebihan sehingga
terjadi penyumbatan pada saluran kelenjar minyak (Harmanto, 2006)
Propionibacterium acnes dan Staphylococcus epidermidis telah dikenal
sebagai bakteri penyebab utama tumbuhnya jerawat. Tidak hanya kedua bakteri
tersebut, Staphylococcus aureus juga memiliki kemampuan untuk mensintesis
lipase yang mendegradasi sebum trigliserida menjadi asam lemak bebas dimana
kondisi tersebut akan memicu respon inflamasi (Sukatta et al., 2008).
Staphylococcus epidermidis adalah bakteri aerob dan bersifat gram
positif dan umumnya berada pada kulit. Sedangkan propionibacterium acnes
adalah bakteri anaerob yang bersifat gram positif. Bakteri ini berada pada kelenjar
sebaseus pada kulit dan memproduksi asam lemak bebas diantara kelenjar
sebaseus yang mana dapat menyebabkan terjadinya iritasi pada dinding follicular
dan menginduksi terjadinya inflamasi yang mengarah pada infeksi kutan
B. Manggis
Buah manggis mengandung senyawa aktif seperti vitamin, katekin
(antioksidan) dan polisakarida. Selain itu, buah manggis juga mengandung
xanthone yang telah terbukti secara ilmiah memiliki beragam manfaat. Khasiat
xanthone antara lain sebagai anti-aging, antioksidan, cardio-protective, mencegah
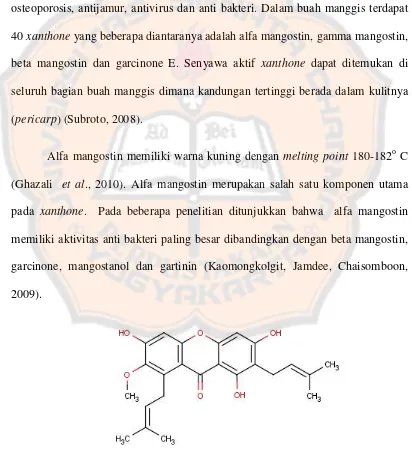
osteoporosis, antijamur, antivirus dan anti bakteri. Dalam buah manggis terdapat
40 xanthone yang beberapa diantaranya adalah alfa mangostin, gamma mangostin,
beta mangostin dan garcinone E. Senyawa aktif xanthone dapat ditemukan di
seluruh bagian buah manggis dimana kandungan tertinggi berada dalam kulitnya
(pericarp) (Subroto, 2008).
Alfa mangostin memiliki warna kuning dengan melting point 180-182o C
(Ghazali et al., 2010). Alfa mangostin merupakan salah satu komponen utama
pada xanthone. Pada beberapa penelitian ditunjukkan bahwa alfa mangostin
memiliki aktivitas anti bakteri paling besar dibandingkan dengan beta mangostin,
garcinone, mangostanol dan gartinin (Kaomongkolgit, Jamdee, Chaisomboon,
2009).
Menurut Potihirat, Chomnawang, Gritsanapan (2008), ekstrak etanol kulit
manggis dengan kadar alfa mangostin sebesar 18,03% b/b memiliki KHM dan
KBM sebesar 7,81 µg/ml dan 62,50 µg/ml untuk S. epidermidis. Sedangkan KHM
dan KBM untuk P. acnes adalah 7,81 µg/ml dan 15,63 µg/ml.
C. Emulgel
Sediaan emulsi dapat berupa campuran air dan minyak dengan sistem
minyak dalam air maupun air dalam minyak. Emulsi dengan sistem minyak dalam
air digunakan untuk menjebak obat yang bersifat lipofil, dimana obat yang
bersifat hidrofil akan terjebak dalam emulsi sistem air dalam minyak. (Singla et
al., 2012). Gel merupakan sediaan yang terbentuk dari cairan yang tidak dapat
bergerak karena adanya tegangan permukaan antara cairan tersebut dengan
jaringan yang terbentuk oleh gelling agent. Gel memiliki kelebihan dapat
melepaskan obat lebih cepat daripada salep dan krim, tidak lengket, mudah dicuci,
larut dalam air, akan tetapi gel tidak dapat bercampur dengan obat yang bersifat
hidrofob (Chirag, Tyagi, Gupta, Sharma, Prajapati, Potdar, 2013).
Keterbatasan sediaan gel dapat diatasi dengan menggabungkan sediaan gel
dengan emulsi. Dengan menggabungkan sediaan emulsi dan gel maka terbentuk
sediaan emulgel yang memiliki kelebihan-kelebihan antara lain, dapat bercampur
dengan obat yang bersifat hidrofob, memiliki stabilitas yang lebih baik
dibandingkan dengan serbuk, krim dan salep, tidak lengket, mudah dibersihkan
D. Bahan Formulasi 1. Emulsifying agent
Emulsifying agent merupakan surfaktan yang dapat mengurangi
tegangan permukaan antara minyak dan air, sehingga energi permukaan dapat
berkurang melalui pembentukan droplet. Setiap surfaktan memiliki nilai HLB
yang berbeda-beda. Surfaktan dengan nilai HLB tinggi digunakan untuk
meningkatkan kelarutan minyak pada medium air. Bagian lipofil dari
surfaktan akan menjebak minyak ke dalam bagian lipofil dari misel.
Sedangkan bagian hidrofil dari surfaktan akan mengelilingi droplet minyak
(Allen,2002).
Surfaktan yang dikombinasikan dengan surfaktan lain dapat
menghasilkan emulsi yang lebih stabil daripada emulsi dengan surfaktan
tunggal. Kombinasi surfaktan membutuhkan rasio dan proporsi yang tepat
sehingga didapatkan nilai HLB yang sesuai (Allen, 2002).
a. Polyoxyethylene Sorbitan Fatty Acid Ester (Tween 20)
Tween 20 merupakan surfaktan non ionik yang banyak digunakan
sebagai emulsifying agent pada preparasi emulsi minyak dalam air. Tween
20 yang dikombinasikan dengan emulsifying agent lain digunakan pada
konsentrasi antara 1-10%. Tween 20 memiliki bau yang khas dan pada
suhu 25o C memiliki warna kuning. Nilai HLB dari tween 20 adalah 16,7
b. Sorbitan Esters (Span 20)
Tween 20 merupakan surfaktan non ionik yang umumnya
digunakan sebagai emulsifying agent pada preparasi krim, emulsi dan
salep untuk sediaan topikal. Span biasanya dikombinasikan dengan tween
menggunakan perbandingan tertentu untuk menghasilkan emulsi air dalam
minyak atau minyak dalam air. Konsentrasi span yang digunakan sebagai
emulsifying agent pada emulsi minyak dalam air ketika dikombinasikan
dengan emulsifying agent lain yaitu 1-10%. Nilai HLB dari Span 20 adalah
4,7 (Rowe et al., 2009).
2. Gelling agent
Karbopol merupakan polimer sintetis dari asam akrilat yang mana
membentuk crosslinked dengan alil sukrosa atau alil eter dari pentaeritritol.
Karbopol mengandung antara 52% dan 68% gugus asam karboksilat (COOH).
Karbopol memiliki fungsi antara lain sebagai emulsifying agent, gelling agent
dan stabilizing agent. Konsentrasi karbopol yang digunakan sebagai gelling
agent pada sediaan yaitu antara 0,5-2%. Karbopol akan mengalami
dekomposisi ketika dipanaskan pada suhu 260o C selama 30 menit. Gel dapat
disterilisasi menggunakan autoklaf dengan sedikit perubahan pada viskositas
atau pH (Rowe et al., 2009).
Penambahan air pada karbopol menyebabkan polimer membesar pada
media air dan membentuk jaringan gel. Dengan adanya penambahan amin
organik sebagai agen netralisasi memungkinkan karbopol menjadi lebih kental
3. Triethanolamin
Triethanolamin merupakan alkalizing agent yang dapat digunakan
sebagai pembentuk karbopol. Karbopol menjadi akan lebih kental ketika
dinetralisasi pada ph 6-11. Karbopol dapat dinetralisasi menggunakan amin
organik seperti triethanolamin (Rowe et al., 2009).
4. Parafin Cair
Parafin cair atau bisa disebut dengan mineral oil digunakan sebagai
fase minyak. Pada emulsi minyak dalam air digunakan sebagai emollient
sedangkan pada formulasi kapsul dan tablet digunakan sebagai lubrikan.
Konsentrasi parafin cair yang dipakai pada sediaan emulsi topikal antara
1-32%. Parafin cair dapat disterilisasi dengan metode panas kering (Rowe et al.,
2009).
5. Propilen Glikol
Propilen glikol dapat digunakan sebagai humektan pada sediaan
topikal dengan konsentrasi yang digunakan yaitu kurang lebih 15%. Fungsi
lain dari propilen glikol yaitu disinfektan, pengawet dan solvent. Pada sediaan
topikal, propilen glikol dapat dikategorikan sebagai iritan rendah. Propilen
glikol yang berbentuk larutan dapat disterilisasi menggunakan autoklaf (Rowe
et al., 2009).
6. Pengawet
Metil paraben digunakan sebagai pengawet antimikroba pada sediaan
topikal dengan konsentrasi antara 0,02-0,3%. Aktivitas antimikroba pada metil
disterilisasi menggunakan autoklaf pada suhu 120oC selama 20 menit tanpa
mengalami dekomposisi (Rowe et al., 2009).
Propil paraben digunakan secara luas sebagai antimikroba pada
kosmetik, makanan dan formulasi farmasetika. Konsentrasi yang digunakan
paraben pada sediaan topikal yaitu antara 0,01-0,6%. Aktivitas propil paraben
dapat meningkat dengan penggunaan kombinasi dengan pengawet lain seperti
metil paraben. Penggunaan campuran paraben sering digunakan pada
formulasi topikal dan oral. Larutan propil paraben pada pH 3-6 dapat
disterilisasi menggunakan autoklaf tanpa mengalami dekomposisi (Rowe et
al., 2009).
7. Alkohol
Alkohol digunakan secara luas pada formulasi farmasetika dan
kosmetik. Alkohol umumnya digunakan sebagai pelarut, selain itu dapat juga
digunakan sebagai desinfektan dan pengawet antimikroba. Konsentrasi
alkohol yang digunakan sebagai pelarut pada sediaan topikal yaitu antara
60-90%. Larutan alkohol dapat disterilisasi menggunakan autoklaf atau
menggunkan metode filtrasi (Rowe et al., 2009).
8. Aquadest
Aquadest memiliki sifat berupa cairan jernih, tidak berwarna, tidak
berbau dan tidak mempunyai rasa. Aquadest atau air suling dibuat dengan
proses penyulingan. Penyimpannya pada wadah yang tertutup baik (Dirjen
E. Sterilisasi
Sterilisasi merupakan pendestruksian seluruh organisme hidup termasuk
spora. Pemilihan metode sterilisasi sediaan farmasetika didasarkan pada bahan
sediaan dan preparasinya. Terlepas dari metode yang digunakan, sediaan
farmasetika harus lulus uji sterilitas untuk membuktikan efektifitas dari sediaan
tersebut. Terdapat lima metode sterilisasi yang digunakan untuk produk
farmasetika yaitu sterilisasi panas basah, sterilisasi panas kering, filtrasi, sterilisasi
gas dan sterilisasi radiasi (Ansel et al., 2009).
Sterilisasi panas basah dapat dilakukan dengan menggunakan autoklaf.
Banyak produk farmasetika tidak tahan panas sehingga tidak dapat disterilisasi
menggunakan metode panas kering yang biasanya membutuhkan suhu sekitar
170o C. Ketika pemanasan dilakukan di bawah kondisi atmosfer, suhu yang
dicapai tidak dapat lebih dari 100o C, sehingga peningkatan tekanan dibutuhkan
untuk dapat mencapai suhu lebih dari 100o C. Tekanan hanya dibutuhkan untuk
meningkatkan suhu sistem namun tidak membantu mempengaruhi proses
pembunuhan mikroorganisme, yang mempengaruhi proses pembunuhan
mikroorganisme adalah suhu. Pada umumnya sterilisasi panas basah dilakukan
pada suhu 121o C (Ansel et al., 2009).
Sediaan topikal semisolid yang bertujuan untuk mengobati luka terbuka
atau luka bakar, produk sekali pakai, harus berbentuk sediaan steril. Metode
jenis wadah. Uji sterilitas perlu dilakukan pada wadah untuk menguji kerapatan
wadah dalam melindungi sediaan steril (Benson et al., 2012).
Penambahan polimer pada sediaan steril digunakan untuk meningkatkan
viskositas dan stabilitasnya. Sediaan steril baik semisolid maupun cairan dengan
viskositas tinggi tidak dapat disterilisasi secara filtrasi, melainkan menggunakan
metode sterilisasi panas. Namun, sterilisasi dengan panas dapat mempengaruhi
reologi dari sediaan berpolimer. Adanya pemanasan dapat menurunkan viskositas
dari sediaan (Bindal et al., 2003).
F. Uji sifat fisis
Viskositas adalah suatu pernyataan pertahanan dari suatu cairan untuk
mengalir, semakin tinggi viskositas akan semakin besar tahanannya.
Penggolongan bahan menurut tipe aliran dan deformasinya dibagi menjadi dua
yaitu, sistem Newton dan sistem non-Newton. Tipe alir plastis, pseudoplastis, dan
dilatan termasuk dalam sitem non-Newton (Martin, Swarbick dan Cammarata,
1983).
Daya sebar adalah kemampuan dari suatu sediaan untuk menyebar di
tempat aplikasi. Besarnya daya sebar bergantung pada viskositas sediaan. Dengan
meningkatnya viskositas sediaan maka waktu retensi sediaan pada tempat aplikasi
juga meningkat, namun kemampuan menyebar sediaan tersebut akan menurun.
Faktor-faktor yang mempengaruhi daya sebar yaitu viskositas sediaan, lama
Salah satu uji yang digunakan untuk menguji daya sebar adalah
parallel-plate method. Parallel-plate method merupakan metode yang paling banyak
digunakan untuk mengukur daya sebar suatu sediaan semisolid. Kelebihan metode
ini adalah sederhana. Namun metode ini memiliki kekurangan yaitu kurang presisi
dan pembacaan data yang subyektif (Garg et al., 2002).
G. Landasan Teori
Manggis mengandung xanthone yang telah terbukti secara ilmiah memiliki
beragam manfaat. Salah satu khasiat xanthone adalah sebagai anti bakteri dan alfa
mangostin merupakan salah satu komponen utama pada xanthone yang memiliki
aktivitas anti bakteri paling besar. Berdasarkan khasiatnya sebagai anti bakteri,
ekstrak kulit manggis dapat diformulasikan sebagai sediaan anti jerawat yang
dapat menghambat pertumbuhan bakteri Staphylococcus epidermidis. Alfa
mangostin memiliki kelarutan yang rendah di air sehingga cocok dibuat dalam
bentuk sediaan emulgel dengan tipe emulsi o/w, selain itu adanya gelling agent
dapat meningkatkan stabilitas sediaan.
Emulgel merupakan sediaan topikal gabungan dari dua sistem yaitu sistem
emulsi di dalam sistem gel. Sistem emulsi ini menggunakan emulsifying agent
tween 20 dan span 20 dimana merupakan surfaktan non ionik dan menggunakan
Karbopol 940 sebagai gelling agent. Kelebihan emulgel antara lain, dapat
bercampur dengan obat yang bersifat hidrofob, mudah dibersihkan, mudah
Sediaan topikal semisolid yang ditujukkan untuk mengobati luka terbuka
atau luka bakar harus berbentuk sediaan steril. Salah satu metode yang digunakan
untuk sterilisasi adalah metode panas basah dengan mengggunakan autoklaf.
Sterilisasi dengan panas dapat mempengaruhi reologi dari sediaan berpolimer
yang ditandai dengan penurunan viskositas sediaan tersebut.
H. Hipotesis
Suhu dan lama sterilisasi metode panas basah berpengaruh terhadap
17
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang dilakukan merupakan jenis penelitian eksperimental murni
karena adanya perlakuan khusus pada setiap subyek uji (emulgel ekstrak kulit
manggis) dengan rancangan acak lengkap pola searah.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas. Variabel bebas pada penelitian ini adalah suhu dan lama
proses sterilisasi menggunakan autoklaf.
b. Variabel tergantung. Variabel tergantung pada penelitian ini adalah
viskositas dan daya sebar emulgel ekstrak kulit manggis.
c. Variabel pengacau terkendali. Variabel pengacau terkendali pada penelitian
ini adalah keaseptisan kerja, formula sediaan, jenis dan ukuran mixer, suhu
pencampuran.
d. Variabel pengacau tak terkendali. Variabel pengacau tak terkendali pada
penelitian ini adalah suhu ruangan pada saat proses pembuatan emulgel.
2. Definisi operasional
a. Ekstrak kulit manggis adalah ekstrak yang dibuat dari kulit manggis
b. Emulgel ekstrak kulit manggis adalah sediaan topikal semisolid hasil
emulsifikasi Tween 20 dan Span 20 sebagai emulsifying agent dan
karbopol 940 sebagai gelling agent dengan penambahan ekstrak kulit
manggis 3% pada 100 gram sediaan untuk mengobati jerawat yang dibuat
sesuai dengan prosedur pada penelitian ini.
c. Sterilmerupakan kondisi bebas dari bakteri.
d. Sterilisasi adalah usaha penghilangan jasad renik dari suatu benda atau
bahan tertentu.
e. Sterilisasi panas basah merupakan salah satu metode sterilisasi yang
menggunakan uap air panas, dengan menggunakan autoklaf.
f. Lama sterilisasi merupakan durasi dilakukannya sterilisasi sediaan dalam
suhu dan tekanan yang tetap.
g. Suhu sterilisasi merupakan suhu yang digunakan selama sterilisasi sediaan
dilakukan.
h. Viskositasadalah tahanan emulgel untuk mengalir.
i. Daya sebar adalah kemampuan emulgel untuk menyebar pada permukaan
tertentu setelah pemberian tekanan.
C. Alat Penelitian
Alat-alat gelas (beaker glass, kaca pengaduk, erlenmeyer), mortir, neraca
digital, waterbath, pipet ukur, cawan petri, tabung reaksi, mixer merk Philip
modifikasi (Elecsa,USD), viscotester seri VT 04 (RION-JAPAN), stopwatch, alat
D. Bahan
Ekstrak kering kulit buah manggis yang diperoleh dari PT. Borobudur,
Karbopol 940 sebagai gelling agent, paraffin cair, Tween 20 dan Span 20 (kualitas
farmasetis) sebagai emulsifying agent, propilen glikol, metil paraben, propil
paraben, aquadest, media nutrient agar (NA) (Oxoid), R 3.0.1.
E. Tata Cara Penelitian
1. Verifikasi ekstrak kulit manggis dan bakteri Staphylococcus epidermidis
a. Identifikasi bahan
Ekstrak kulit manggis yang diperoleh dari PT. Borobudur telah
diuji identitasnya dan dibuktikan dengan Certficate of Analysis.
b. Verifikasi alfa mangostin
Pemeriksaan kandungan alfa mangostin pada ekstrak kulit
manggis dilakukan secara Kromatografi Lapis Tipis (KLT). Ekstrak kulit
manggis yang telah dilarutkan pada etil asetat dan standar alfa mangostin
sebagai pembanding ditotolkan pada fase diam silica gel 60F254. Fase
gerak yang digunakan campuran kloroform : etil asetat : methanol (28 : 3,5
: 1,75) (Yuliani, 2013). Setelah elusi selesai, hasil elusi dicek pada
panjang gelombang 254nm.
2. Formula
Formula yang digunakan untuk pembuatan emulgel antiacne ekstrak
kulit manggis mengacu pada Optimation of Chlorphensin Emulgel
Tabel I. Formula emulgel acuan
Dilakukan modifikasi dengan mengganti zat aktif dan beberapa
eksipiennya. Formula hasil modifikasi adalah sebagai berikut :
Tabel II. Formula emulgel yang telah dimodifikasi (100 g emulgel)
Bahan Emulgel Satuan (g)
Karbopol didispersikan sedikit demi sedikit dalam 60 mL
b. Pencampuran ekstrak kulit manggis dengan etanol
Ekstrak yang telah ditimbang kemudian dilarutkan dalam etanol
70% sebanyak 7,5 gram.
c. Pembuatan emulgel
Fase minyak dibuat dengan mencampur paraffin cair, span 20 dan
ekstrak kulit buah manggis yang telah dilarutkan dalam etanol. Fase air
dibuat dengan melarutkan propil paraben dan metil paraben ke dalam
propilen glikol. Setelah larut, selanjutnya ditambahkan tween 20 ke dalam
fase air. Fase air dan fase minyak dipanaskan secara terpisah pada
waterbath dengan menggunakan suhu antara 70-80o C. Selanjutnya, fase
minyak dimasukkan ke dalam fase air dan dicampur menggunakan mixer
dengan kecepatan 300 rpm selama 10 menit.
Emulsi yang sudah terbentuk selanjutnya dicampurkan dengan
karbopol 940 yang sudah dikembangkan dan ditambah dengan aquadest.
Bahan tersebut dicampur menggunakan mixer dengan kecepatan 300 rpm
selama 10 menit. Kemudian Trietanolamin (TEA) ditambahkan ke dalam
campuran dan diaduk kembali menggunakan mixer dengan kecepatan 300
rpm selama 5 menit.
d. Sterilisasi panas basah
Emulgel yang telah dibuat kemudian dimasukkan ke dalam beaker
glass, ditutup menggunakan aluminium foil dan direkatkan. Emulgel
dimasukkan ke dalam autoklaf, autoklaf ditutup dengan rapat. Suhu dan lama
Tabel III. Variasi suhu dan lama sterilisasi pada metode sterilisasi panas basah
Suhu Sterilisasi (oC) Lama sterilisasi (menit) 110 5; 10; 15; 20; 25
Media yang digunakan untuk uji sterilitas adalah nutrient agar
(NA). Untuk 1 L media, ditimbang 28 gram NA. NA yang sudah
ditimbang sesuai dengan kebutuhan kemudian dimasukkan ke dalam labu
erlenmeyer dan dicampurkan ke akuades. Media dipanaskan diatas hot
plate magnetic stirrer hingga diperoleh larutan berwarna kuning jernih.
Media NA dituangkan dalam tabung reaksi dengan volume 15 mL. Media
disterilkan dengan autoklaf selama 15 menit pada suhu 121o C. Setelah
media NA disterilkan selanjutnya dituang ke cawan petri dan dibiarkan
hingga memadat.
b. Uji sterilitas
Uji sterilitas dilakukan dengan menyiapkan emulgel ekstrak kulit
manggis. Ose dipanaskan dari pangkal ke ujung hingga membara. Emulgel
diambil sebanyak 1 ose, selanjutnya ose digoreskan pada permukan NA
dalam cawan petri secara zig-zag. Cawan petri dilapisi dengan
pada suhu kamar selama 24 jam. Hasil yang diperoleh diamati dan
dibandingkan dengan kontrol kontaminasi media dan kontrol emulgel
tanpa sterilisasi.
5. Evaluasi sediaan emulgel
a. Uji pH emulgel
Pengukuran pH ini menggunakan indikator universal, yaitu dengan
memasukan indikator pH universal (ph strips) ke dalam emulgel ekstrak
kulit manggis yang telah dibuat. Nilai pH yang diinginkan berada pada
rentang pH yang tidak mengiritasi kulit yaitu antara 4-6,5.
b. Uji sifat fisik emulgel
1. Uji viskositas
Pengukuran viskositas menggunakan alat Viscotester Rion seri VT
04 dengan cara sediaan emulgel ditimbang sebanyak 100 gram,
dimasukkan ke dalam gelas stainless steel kemudian dipasang pada
portable viscotester. Viscotester dinyalakan dan diamati angka yang
ditunjukkan oleh jarum pada layar. Nilai viskositas diperoleh jika
jarum sudah konstan pada nilai tertentu. Pengujian viskositas
dilakukan dalam dua periode yaitu 48 jam setelah emulgel selesai
dibuat dan 48 jam setelah proses sterilisasi. Dilakukan replikasi
sebanyak tiga kali untuk tiap formula.
2. Uji daya sebar
Pengukuran daya sebar dilakukan 48 jam setelah pembuatan dan 48
gram dan diletakkan di tengah kaca bulat berskala. Di atas emulgel
diletakkan kaca bulat lain dan ditambah beban hingga berat kaca dan
pemberat adalah 125 gram (Garg et al., 2002), selanjutnya didiamkan
selama 1 menit kemudian dicatat penyebarannya. Dilakukan replikasi
sebanyak 3 kali untuk tiap formula.
F. Analisis Hasil
Data yang terkumpul adalah data uji viskositas dan uji daya sebar 48 jam
setelah pembuatan, serta uji viskositas dan daya sebar 48 jam setelah proses
sterilisasi.
Untuk melihat signifikansi pengaruh suhu dan lama sterilasi terhadap
viskositas dan daya sebar, dilakukan uji ANAVA. Data dianalisis dengan uji
Saphiro-Wilk untuk melihat kenormalan distribusi data dan uji kesamaan variansi
Levene’s test untuk melihat kesamaan varians. Jika data sesuai dengan kriteria uji
statistik parametrik, maka analisis dilanjutkan dengan pengujian signifikansi
menggunakan ANAVA. Jika hasil yang didapat menunjukkan adanya perbedaan
signifikan, maka analisis dilanjutkan dengan uji posthoc menggunakan uji Tukey.
Jika data tidak memenuhi kriteria uji statistik parametrik, maka analisis data
menggunakan Kruskal-Wallis dengan post-hoc Wilcoxon. Analisis data dilakukan
25
BAB IV
HASIL DAN PEMBAHASAN
A. Identifikasi dan Verifikasi Ekstrak Kulit Manggis
Pada penelitian ini digunakan ekstrak kulit manggis yang berasal dari PT.
Borobudur, Semarang. Ekstrak kulit manggis yang digunakan berupa ekstrak
kering yang telah diidentifikasi dan dibuktikan dengan Certificate of Analysis
(CoA) (Lampiran 1).
Sebelum ekstrak kulit manggis digunakan, perlu dilakukan verifikasi
untuk memastikan kebenaran identitas dari ekstrak tersebut. Verifikasi yang
dilakukan berupa KLT (Kromatografi Lapis Tipis) dengan pembanding standar
alfa mangosteen. Pembanding yang digunakan berupa standar alfa mangostin
karena alfa mangostin merupakan salah satu senyawa khas yang hanya terdapat
pada buah manggis. Fase diam yang digunakan berupa silica gel 60F254 yang
dapat berfluoresensi pada panjang gelombang 254 nm, sedangkan fase gerak yang
digunakan berupa kloroform : etil asetat : metanol (28 : 3.5 : 1.75). Hasil yang
didapatkan adalah Rf standar 0,46 dan Rf ekstrak 0,47. Hal ini menunjukkan Rf
yang dimiliki ekstrak mirip dengan Rf pembanding alfa mangostin. Jadi,
berdasarkan hasil tersebut dapat disimpulkan bahwa ekstrak kulit manggis yang
a b c d e
Keterangan : a dan b = hasil elusi standar alfa mangostin c, d dan e = hasil elusi ekstrak
Gambar 2. Hasil identifikasi KLT ekstrak kulit manggis
B. Pembuatan Emulgel Ekstrak Kulit Manggis
Kandungan xanthone dalam buah manggis terbukti memiliki sifat sebagai
antibakteri. Alfa mangostin merupakan kandungan utama pada xanthone dan
memiliki sifat anti bakteri yang paling besar dibandingkan dengan beta mangostin,
garcinone, mangostanol dan gartinin (Kaomongkolgit et al., 2009). Pada
penelitian Pothitirat et al., dikatakan bahwa ekstrak etanol kulit manggis memiliki
KHM dan KBM sebesar 7,81 µg/ml dan 62,50 µg/ml untuk S. epidermidis
(Pothitirat et al., 2009). Penelitian tersebut dapat memperkuat bukti bahwa ekstrak
kulit manggis memiliki sifat antibakteri dan dapat diformulasikan sebagai sediaan
obat jerawat.
Pemilihan sediaan emulgel dengan emulsi tipe o/w didasarkan pada
kelarutan zat aktif yang digunakan. Zat aktif yang digunakan merupakan alfa
mangostin yang memiliki kelarutan rendah pada air, namun dapat larut pada
etanol dan eter (Nadkarni, nadkarni, 1999). Oleh karena itu, dibuat sistem emulsi
dan dikelilingi oleh fase luar yaitu fase air. Penambahan etanol pada formulasi
digunakan untuk melarutkan ekstrak kulit buah manggis kemudian alfa mangostin
akan dipartisi ke minyak, sehingga zat aktif dapat masuk ke dalam fase minyak.
Selain itu, pemilihan sediaan bergantung pada fungsi dari sediaan tersebut.
Apabila sediaan obat jerawat yang dibuat berupa emulsi tipe w/o dengan fase luar
berupa minyak maka sediaan tersebut dapat memperparah keadaan jerawat
pengguna, karena penggunaan minyak yang berlebihan dapat bersifat
komedogenik. Penambahan gelling agent pada sediaan emulsi dapat memberikan
rasa dingin yang dapat meningkatkan acceptability pengguna (Chirag et al.,
2013).
Alasan lain pemilihan sediaan emulgel yang tidak kalah penting yaitu
warna yang dihasilkan oleh sediaan emulgel dimana warna sediaan erat
hubungannya dengan tingkat penerimaan pasien. Ekstrak yang digunakan peneliti
merupakan ekstrak kulit manggis yang mempunyai warna kecoklatan, namun
dengan basis emulgel yang berwarna putih maka warna coklat dari ekstrak kulit
manggis dapat tersamarkan dan sediaan menjadi berwarna lebih menarik. Sediaan
emulgel dengan warna yang lebih menarik diharapkan dapat meningkatkan
penerimaan pasien terhadap emulgel anti-acne ekstrak kulit buah manggis.
Formula yang digunakan pada penelitian ini merupakan formula
modifikasi dari formula (Magdy, 2004). Modifikasi yang dilakukan adalah
penambahan jumlah tween 20, span 20 dan etanol. Modifikasi dilakukan dengan
diinginkan. Jumlah tween 20, span 20 dan etanol yang digunakan pada formula
acuan yaitu 0,6; 0,9; 2,5 sedangkan pada formula modifikasi digunakan 1; 1,5;
7,5 tiap 100 gram sediaan emulgel.
Fungsi dari setiap bahan yang digunakan pada penelitian ini yaitu tween
20 dan span 20 sebagai emulsifying agent, karbopol 940 sebagai gelling agent,
triethanolamin (TEA) berfungsi sebagai agen penetralisasi karbopol, paraffin cair
sebagai emollient, propilen glikol sebagai humektan, metil paraben dan propil
paraben sebagai pengawet, etanol sebagai pelarut ekstrak dan aquadest sebagai
fase air. Penggunaan etanol 70% untuk melarutkan ekstrak kulit buah manggis
berdasarkan pada pelarut yang digunakan saat ekstraksi kulit buah manggis,
pelarut yang digunakan dapat dilihat pada lampiran CoA ekstrak kulit buah
manggis (Lampiran 1.)
Emollient dan humektan memiliki fungsi sebagai pelembab yang dapat
menjaga kelembapan kulit, namun emollient dan humektan memiliki mekanisme
yang berbeda. Mekanisme humektan dalam menjaga kelembaban yaitu dengan
membentuk gugus hidrogen dengan air yang terdapat pada lingkungan. Emollient
yang merupakan jenis minyak dapat melapisi rongga-rongga di antara stratum
corneum, sehingga kandungan air yang berada di dalam kulit tidak dapat keluar.
Emollient yang digunakan peneliti pada formulasi bersifat non-komedogenik,
sehingga pengunaan emollient pada sediaan tidak akan memperparah keadaan
jerawat pengguna.
Penggunaan kombinasi dua pengawet yaitu metil paraben dan propil
paraben dan propil paraben yang digunakan pada sediaan konsentrasinya tidak
melebihi 0,01% sehingga tidak mempengaruhi efisiensi dari karbopol (Allen,
2002).
Penggunaan bobot ekstrak sebanyak 3 gram pada 100 gram sediaan
emulgel didasarkan pada orientasi yang telah peneliti lakukan sebelumnya.
Orientasi yang dilakukan berupa uji antimikroba dari tiap konsentrasi ekstrak
yang sudah diformulasikan pada emulgel. Uji antimikroba yang digunakan
menggunakan metode sumuran dimana media yang digunakan merupakan media
MHA (Mueller-Hinton Agar) dan bakteri yang digunakan adalah Staphylococcus
epidermidis. Konsentrasi ekstrak yang peneliti gunakan pada orientasi yaitu 1%,
2%, 4% dan 8% dengan hasil zona hambat sebagai berikut,
Tabel IV. Hasil zona hambat orientasi konsentrasi ekstrak kulit buah manggis
antibakteri berdasarkan zona hambatnya dapat diklasifikasikan sebagai berikut,
Tabel V. Klasifikasi aktivitas antibakteri berdasarkan diameter zona hambat Aktivitas antibakteri Diameter zona hambat (mm)
Lemah <5
Sedang 5-10
Kuat 10-20
Pada Tabel IV, dapat dilihat bahwa zona hambat semakin besar seiring
dengan meningkatnya penambahan ekstrak pada emulgel. Namun, pemilihan
konsentrasi ekstrak juga didasarkan pada penampilan sediaan karena penampilan
sediaan dapat berpengaruh pada penerimaan pasien. Penampilan sediaan tiap
konsentrasi dapat dilihat pada lampiran 3, dan dapat disimpulkan bahwa dengan
meningkatnya konsentrasi ekstrak yang ditambahkan, warna emulgel akan
semakin gelap dan emulgel menjadi semakin kental. Oleh karena itu, konsentrasi
ekstrak 4% dan 8% tidak peneliti pilih karena penampilannya yang kurang
menarik. Emulgel dengan konsentrasi ekstrak 1% juga tidak dipilih peneliti karena
zona hambat yang dihasilkan masih termasuk dalam kategori lemah. Konsentrasi
ekstrak yang dipilih peneliti adalah 3% karena diharapkan zona hambat yang
didapatkan lebih besar daripada emulgel dengan konsentrasi ekstrak 2%, selain itu
menurut peneliti penampilan emulgel dengan konsentrasi 3% masih menarik.
Pembuatan emulgel dilakukan melalui dua tahap yaitu tahap emulsifikasi
dan penambahan gelling agent. Tahap emulsifikasi diawali dengan pembuatan
fase minyak dan fase air. Masing-masing fase dipanaskan secara terpisah
menggunakan waterbath pada suhu antara 70-80o C. Selanjutnya fase minyak
dimasukkan ke dalam fase air dan dicampur menggunakan mixer dengan
kecepatan 300 rpm selama 10 menit.
Tahap selanjutnya setelah emulsi terbentuk yaitu tahap penambahan
gelling agent. Karbopol 940 yang sebelumnya sudah dikembangkan ditambahkan
ke dalam emulsi dan dicampur menggunakan mixer dengan kecepatan 300 rpm
kembali menggunakan mixer selama 5 menit dengan kecepatan 300 rpm. TEA
merupakan amin organik yang dapat berfungsi sebagai agen netralisasi. Sebelum
mengalami proses netralisasi, karbopol berada dalam bentuk tak terionkan dan
memiliki pH sekitar 3. Pada pH ini, karbopol memiliki sifat yang fleksibel
struktur random coil (Pena, 1989). Dengan penambahan amin organik seperti
TEA, gugus karboksilat pada karbopol akan ternetralisasi menjadi garam.
Kemudian gugus karboksilat yang terionisasi akan memiliki muatan negatif
sehingga akan terbentuk gaya tolak-menolak antar gugus karboksilat. Gaya tolak
menolak tersebut mengakibatkan swelling dan thickening dari struktur karbopol
(Abdullah et al., 2013).
Penggunaan dua tipe emulsifying agent pada penelitian ini memiliki
prinsip kerja sebagai berikut, bagian hidrokarbon dari molekul span berada dalam
droplet minyak dan bagian lainnya berada dalam fase air. Kepala sorbitan yang
besar pada molekul span mencegah ekor hidrokarbon bergabung rapat dalam fase
minyak. Ketika tween ditambahkan, ekor hidrokarbon dari tween akan berada
dalam droplet minyak dan rantai polioksietilennya berada dalam fase air bersama
dengan cincin sorbitan. Rantai hidrokarbon tween yang berada dalam droplet
minyak akan berada di antara rantai hidrokarbon span dan penyusunan ini
menghasilkan gaya tarik menarik Van der Waals yang efektif. Sehingga, lapisan
antarmuka menjadi lebih kuat dan stabilitas dari emulsi o/w meningkat (Martin et
C. Uji pH
pH suatu sediaan topikal merupakan salah satu hal yang penting, karena
pH yang terlalu asam dapat mengiritasi kulit penggunanya. Rentang pH yang baik
untuk kulit normal antara 4-6,5 (Baranoski and Ayello, 2008). Pengecekkan pH
emulgel dilakukan sebelum dan sesudah sterilisasi dan pH yang dihasilkan tetap
sama yaitu pH berkisar antara 5-6. Selain itu, pada rentang pH tersebut memiliki
viskositas yang optimal (Pena, 1989).
Gambar 3. Hasil uji pH sediaan emulgel ekstrak kulit manggis
D. Sterilisasi Emulgel Ekstrak Kulit Manggis
Luka terbuka melibatkan kerusakan internal maupun eksternal pada
jaringan kulit (Roddick, 2012). Adanya kerusakan jaringan yang terjadi pada
jerawat yang salah satunya diakibatkan oleh peningkatan jumlah sebum, sehingga
jerawat dapat dikategorikan sebagai luka terbuka (Fabbrocini et al., 2010).
Sediaan topikal semisolid yang bertujuan untuk mengobati luka terbuka harus
sterilisasi untuk sediaan luka terbuka maka bisa terjadi infeksi yang dapat
memperparah luka karena adanya kontaminasi dari sediaan. Sehingga perlu
dilakukan sterilisasi pada sediaan emulgel ekstrak kulit manggis untuk menjamin
sterilitasnya.
Sterilisasi merupakan pendestruksian seluruh organisme hidup dan
termasuk spora. Terdapat lima metode sterilisasi yang biasa digunakan untuk
produk farmasetika yaitu sterilisasi panas basah, sterilisasi panas kering, filtrasi,
sterilisasi gas dan sterilisasi radiasi (Ansel et al., 2009).
Pada penelitian ini metode sterilisasi yang dipilih yaitu metode sterilisasi
panas basah dengan menggunakan autoklaf. Pemilihan metode didasarkan pada
karakteristik dari ekstrak kulit manggis dan bahan-bahan yang digunakan dalam
formulasi. Salah satu kandungan dalam ekstrak kulit manggis yaitu beta
mangostin, memiliki melting point 162-163o C, sedangkan alfa mangostin
memiliki melting point 180-182o C (Ghazali et al., 2010). Metode sterilisasi panas
kering biasanya menggunakan suhu antara 160o atau 170o C selama tidak kurang
dari 2 jam, sedangkan metode panas basah menggunakan suhu dan waktu yang
lebih rendah dibandingkan dengan metode panas kering. Beta mangostin memiliki
efek sinergis dengan alfa mangostin, sehingga penggunaan metode panas kering
dengan suhu di atas melting point beta mangostin dapat memungkinkan terjadinya
perubahan bentuk kristal dan atau perubahan efektifitas yang dapat mempengaruhi
efektifitas sediaan sebagai anti jerawat.
Prinsip dari sterilisasi panas basah menggunakan autoklaf yaitu adanya
organisme. Adanya peningkatan tekanan menyebabkan suhu dapat meningkat
dengan cepat, namun adanya perubahan tekanan tidak mempengaruhi mekanisme
destruksi dari mikroorganisme. Mekanisme destruksi mikroorganisme hanya
dipengaruhi oleh suhu. Kelebihan metode ini dibandingkan dengan metode panas
kering adalah adanya lembab yang dapat membunuh bakteri lebih efektif ,
membutuhkan waktu yang lebih cepat dan suhu yang lebih rendah. Namun
kekurangan dari metode ini adalah metode ini tidak dapat digunakan untuk
sterilisasi bahan maupun sediaan yang tidak dapat ditembus oleh lembab atau
yang dapat rusak karena adanya lembab (Ansel et al., 2009).
Pemilihan suhu sterilisasi didasarkan pada ketersediaan alat yang
digunakan, sehingga dipilih suhu 110o C, 115o C, 121o C dan 127 o C. Terdapat
lima variasi waktu yang digunakan yaitu 5, 10, 15, 20 dan 25 menit. Variasi waktu
tersebut dianggap peneliti masih termasuk waktu yang efisien dimana sterilisasi
autoklaf biasanya dilakukan selama 15 menit dengan suhu 121o C, selain itu
pemanasan yang terlalu lama dikhawatirkan dapat mempengaruhi efektifitas dari
sediaan.
E. Uji Sterilitas Emulgel Ekstrak Kulit Manggis
Sediaan yang telah mengalami proses sterilasi perlu dilakukan uji sterilitas
untuk menjamin sterilitas sediaan tersebut. Berdasarkan WHO, terdapat dua
metode uji sterilitas yaitu metode filtrasi menggunakan membran dan metode
inokulasi langsung. Metode filtrasi menggunakan membran digunakan untuk
sediaan yang berbentuk cairan, sedangkan metode inokulasi langsung digunakan
digunakan adalah metode inokulasi langsung dimana sediaan emulgel langsung
diinokulasikan pada media. Digunakan metode inokulasi langsung karena bentuk
sediaan berupa emulgel sehingga metode filtrasi tidak dapat digunakan (WHO,
2012).
Cawan petri yang akan digunakan dicuci terlebih dahulu selanjutnya
dikeringkan dan dibungkus menggunakan kertas payung, kemudian dimasukkan
ke dalam oven pada suhu 60o C selama lebih dari 24 jam. Tujuan sterilisasi cawan
petri adalah meminimalkan adanya kontaminan pada peralatan uji sterilitas.
Menurut WHO, media yang digunakan sebagai media uji sterilitas yaitu
fluid thioglycollate medium dan soya-bean casein digest karena media tersebut
cukup sensitif untuk menggambarkan adanya kontaminasi bakteri. Namun, pada
penelitian ini media yang digunakan untuk uji sterilitas adalah Nutrient Agar
karena NA merupakan broad spectrum media dimana mengandung nutrient yang
cukup untuk pertumbuhan bakteri pada umumnya dan sering digunakan sebagai
media kultur, sehingga media NA sudah dapat menggambarkan sterilitas suatu
sediaan uji terhadap bakteri (Taylor, 2001).
Uji sterilitas dilakukan dengan menginokulasikan 1 ose emulgel pada
media NA secara zig-zag. Sebelum ose digunakan, ose dipanaskan dulu agar
steril. Pemanasan dilakukan dengan memijarkan ose pada api bunsen. Setiap akan
membuka dan menutup cawan petri, cawan petri dilalukan pada api bunsen untuk
menghindari adanya kontaminan. Uji sterilisasi dilakukan dalam LAF (Laminar
bunsen, hal tersebut dilakukan untuk menghindari adanya kontaminan yang dapat
membuat hasil penelitian menjadi bias.
Kontrol kontaminasi media diperlukan dalam uji sterilitas untuk menjamin
tidak ada kontaminan pada media uji, sehingga dapat dipastikan apabila terdapat
pertumbuhan bakteri hasil tersebut benar-benar berasal dari sediaan uji. Selain
kontrol kontaminasi, kontrol sediaan tanpa sterilisasi juga perlu dilakukan untuk
digunakan sebagai pembanding sterilitas.
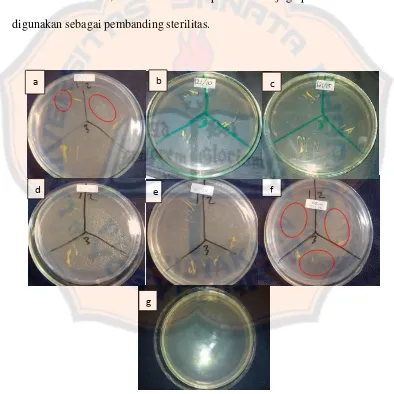
Keterangan : lingkaran merah menunjukkan adanya pertumbuhan bakteri pada media
Gambar 4. Hasil uji sterilisasi emulgel pada suhu 121o C selama a. 5 menit, b. 10 menit, c. 15 menit, d. 20 menit, e. 25 menit, f. kontrol emulgel tanpa
sterilisasi, g. kontrol kontaminasi media a
d e f
g
Tabel VI. Hasil uji sterilisasi emulgel ekstrak kulit manggis Keterangan : + : adanya pertumbuhan bakteri
- : tidak ada pertumbuhan bakteri
Hasil pada Tabel VI, menunjukkan bahwa pada keempat suhu dengan
pemanasan 20 dan 25 menit tidak ada pertumbuhan bakteri, sedangkan pada suhu
121o C dan 127 o C dengan pemanasan di atas 10 menit sudah menunjukkan tidak
ada pertumbuhan bakteri. Dengan tidak adanya pertumbuhan bakteri berarti
emulgel ekstrak kulit manggis sudah steril. Perbandingan sterilitas emulgel tanpa
sterilisasi dan emulgel dengan sterilisasi pada suhu 121o C dapat dilihat pada
Gambar 4. Pada Gambar 4, terlihat bahwa emulgel tanpa sterilisasi dapat
ditumbuhi oleh bakteri, hasil tersebut menunjukkan bahwa sediaan emulgel yang
tidak disterilisasi dapat terkontaminasi bakteri. Hasil kontrol kontaminasi media
yang dapat dilihat pada Gambar 4 menunjukkan media tidak ditumbuhi oleh
kontaminan.
F. Uji Sifat Fisis Emulgel Ekstrak Kulit Manggis
Pengamatan sifat fisik emulgel ekstrak emulgel kulit manggis yang
meliputi uji viskositas dan uji daya sebar perlu dilakukan karena hal tersebut
sediaan. Adanya proses sterilisasi panas basah dapat mengubah struktur polimer
pada sediaan emulgel. Adanya pemanasan pada proses sterilisasi dapat
menurunkan viskositas dari sediaan (Bindal et al., 2003). Besarnya daya sebar
bergantung pada besarnya viskositas suatu sediaan. Dengan menurunnya nilai
viskositas, kemampuan menyebar sediaan akan meningkat namun waktu retensi
sediaan pada tempat aplikasi akan mengalami penurunan (Garg et al., 2002).
1. Pengamatan warna emulgel
Pengamatan penampilan fisik merupakan pengamatan pertama yang
dilakukan untuk melihat apakah terdapat perbedaan warna dan bentuk pada
emulgel yang belum mengalami proses sterilisasi dan yang sudah mengalami
proses sterilisasi. Pengamatan warna dan bentuk sediaan perlu dilakukan
karena warna dan bentuk sediaan dapat mempengaruhi penerimaan pasien
terhadap sediaan tersebut.
Pada Gambar 6, terlihat bahwa tidak terdapat perubahan warna
emulgel ekstrak kulit manggis setelah proses sterilisasi suhu tertinggi yaitu
127o C pada menit ke lima sampai menit ke 25. Selain itu, warna emulgel
sebelum proses sterilisasi dibandingkan dengan warna emulgel setelah proses
sterilisasi dan tidak terdapat perbedaan warna pada emulgel tersebut (Gambar
5 dan Gambar 6).
Gambar 6. Sediaan emulgel setelah mengalami proses sterilisasi pada suhu 127o C selama a. 5 menit, b. 10 menit, c. 15 menit, d. 20 menit, e. 25
menit
2. Uji viskositas dan daya sebar
Viskositas merupakan suatu pernyataaan tahanan suatu cairan untuk
mengalir. Semakin tinggi viskositas maka sediaan tersebut semakin kental,
namun semakin rendah viskositas maka sediaan tersebut semakin encer
(Martin et al., 1983).
a b c
Pengecekkan viskositas dilakukan sebelum dan setelah proses
sterilisasi yaitu 48 jam setelah pembuatan emulgel dan 48 jam setelah proses
sterilisasi. Hal tersebut dilakukan agar nilai viskositas yang diperoleh tidak
terpengaruh gaya geser yang diberikan selama pembuatan emulgel dan tidak
terpengaruh pemanasan akibat proses sterilisasi.
Pengukuran viskositas dilakukan dengan menggunakan alat viscotester
Rion-Japan seri VT-04. Emulgel ditimbang sebanyak 100 gram dan
dimasukkan ke dalam gelas stainless steel. Setelah penimbangan, emulgel
didiamkan terlebih dahulu selama kurang lebih 5 menit agar pengukuran
viskositas tidak terpengaruh adanya gaya geser pada saat penimbangan
emulgel. Pemilihan nomor rotor yang digunakan bergantung pada kekentalan
sediaan yang akan diteliti viskositasnya. Semakin kental sediaan, nomor rotor
yang digunakan semakin tinggi. Pada penelitian ini, nomor rotor yang
digunakan adalah nomor dua. Nilai viskositas yang didapatkan dalam satuan
dPas. Viscotester jenis ini memiliki kelebihan yaitu mudah digunakan dan
praktis. Namun, kekurangan dari viscotester ini adalah pembacaan skala
viskositas yang subjektif.
Hasil pengukuran viskositas sediaan emulgel sebelum dan sesudah
sterilisasi tertera pada Tabel VII,
Tabel VII. Nilai viskositas emulgel anti-acne ekstrak kulit manggis (dPa.s)
Keterangan : a = Nilai viskositas sebelum sterilisasi
b = Nilai viskositas setelah sterilisasi
Daya sebar adalah kemampuan dari suatu sediaan untuk menyebar di
tempat aplikasi (Garg et al., 2002). Pengukuran daya sebar bertujuan untuk
melihat besarnya diameter penyebaran emulgel saat diaplikasikan.
Metode pengukuran daya sebar yang digunakan pada penelitian ini
adalah parallel plate method. Metode ini merupakan metode yang paling
banyak digunakan karena metode ini sederhana. Namun, kekurangan metode
Pengukuran daya sebar dilakukan 48 jam setelah pembuatan emulgel
dan 48 jam setelah proses sterilisasi (Garg et al., 2002). Hal ini dilakukan
dengan tujuan agar hasil yang didapatkan tidak terpengaruh gaya geser yang
diberikan saat pembuatan emulgel serta adanya pemanasan akibat proses
sterilisasi.
Tabel VIII. Nilai daya sebar emulgel anti-acne ekstrak kulit manggis (cm)
Lama
Keterangan : a = Nilai viskositas sebelum sterilisasi
b = Nilai viskositas setelah sterilisasi
Pada tabel VII dan tabel VIII dapat dilihat adanya pergeseran
dapat terjadi dikarenakan adanya pemberian panas pada sterilisasi yang
mengakibatkan ikatan antar monomer merenggang atau putus sehingga
viskositas sediaan mengalami penurunan. Pemutusan ikatan monomer gelling
agent diperkirakan hanya terjadi pada rantai samping (side chain) bukan pada
backbone, karena tidak terjadi pemisahan fase emulgel namun terjadi
pergeseran nilai viskositas dan daya sebar setelah proses sterilisasi. Walaupun
terdapat pergeseran, namun seluruh nilai viskositas dan daya sebar sediaan
setelah proses sterilisasi masih termasuk dalam range viskositas yang
dikehendaki peneliti yaitu antara 200-300 dPa.s dengan daya sebar antara 3-5
cm.
Nilai viskositas dan daya sebar emulgel sebelum sterilisasi dan
sesudah sterilisasi dihitung selisihnya sehingga didapatkan nilai selisihnya
pada tabel VII dan tabel VIII. Nilai selisih tersebut kemudian dianalisis
menggunakan ANOVA. Hasil uji statistik dapat dilihat pada Lampiran 7,
dimana hasil tersebut menunjukkan suhu dan lama sterilisasi panas basah tidak
memberikan pengaruh yang signifikan terhadap viskositas dan daya sebar
sediaan, karena pada suhu 110o C sudah terjadi perenggangan atau pemutusan
ikatan antar monomer gelling agent. Oleh karena itu, adanya penambahan
lama dan suhu sterilisasi diatas 110o C tidak memberikan perbedaan yang
44
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan hasil penelitian yang dilakukan, maka dapat disimpulkan
tidak terdapat perubahan viskositas dan daya sebar yang signifikan terhadap
variasi suhu dan lama sterilisasi yang diberikan. Sterilisasi sediaan dapat
dilakukan pada suhu 115o C selama 20 menit untuk mendapatkan sediaan emulgel
anti-acne ekstrak kulit buah manggis yang steril.
B. Saran
Berdasarkan penelitian yang telah dilakukan, saran yang dapat peneliti
berikan, antara lain
1. Perlu dilakukan penelitian mengenai pengaruh sterilisasi panas basah terhadap
efektifitas sediaan sebagai anti jerawat.
2. Perlu dilakukan penelitian pengaruh sterilisasi dengan metode lain seperti
sterilisasi gas atau radiasi.
3. Perlu dilakukan uji stabilitas sediaan dalam penyimpanan.
4. Perlu dilakukan uji sterilitas emulgel anti-acne ekstrak kulit buah manggis