PROSES OPTIMASI ADSORPSI LOGAM Pb
OLEH LIMBAH
CANGKANG SOTONG (
Sepia recurvirostra
) DALAM LARUTAN
Dedy Citra Permata , Refinela, Admin Alifb
aLaboratorium Kimia Fisika, Jurusan Kimia MIPA, Universitas Andalas bLaboratorium Elektrokimia, Jurusan Kimia MIPA, Universitas Andalas
e-mail : [email protected]
Jurusan Kimia FMIPA Unand, Kampus Limau Manis, 25163
Research about adsorption of metal ion Pb (plumbum) by cuttlefish shell has been investigated through batch experiment. Characterization of cuttlefish shell was evaluated using Fourier Transform Infrared (FTIR) and Scanning Electron Microscope-Energy Dispersive X-Ray (SEM-EDX), estimated the active functional group was –OH and C=O. Based on the experiment optimum condition adsorption metal ion Pb(II) was pH 4, adsorben dosage 0,2 gram, initial consentration of metal ion solution 175 mg/L, contact time 30 minute and temperature 25⁰C with maximum adsorption capacity 41,5767 mg/g.. Measuring of metal ion concentration evaluated
using Atomic Adsorption Spectroscopy (AAS). This research show that cuttlefish shell could be employed as an efficient adsorbent for removal heavy metal ion.
Keyword : Adsorption, Cuttlefish shell, Plumbum, adsorption capacity
I.
PENDAHULUAN
Pencemaran air oleh logam berat telah lama menjadi masalah serius yang perlu ditanggulangi. Logam berat pencemar lingkungan terdiri dari beberapa unsur yang dikategorikan atas pencemar prioritas tinggi, sedang dan rendah yang umumnya terlarut dalam air dalam berbagai senyawa. Toksisitas logam pada manusia menyebabkan beberapa akibat negatif, tetapi yang terutama adalah timbulnya kerusakan jaringan, terutama jaringan detoksikasi dan ekskresi (hati dan ginjal). [1]
Salah satu logam pencemar prioritas tinggi adalah logam berat timbal (Pb). Akumulasi Pb pada tubuh manusia akan menimbulkan berbagai dampak yang merugikan bagi kesehatan, diantaranya kerapuhan tulang, rusaknya kelenjar reproduksi, kerusakan otak, dan keracunan akut pada sistem saraf pusat. [2]
Beberapa metode kimia maupun biologi telah dicoba untuk menanggulangi logam berat yang terdapat di dalam limbah, diantaranya adsorpsi, pertukaran ion, dan
pemisahan dengan membran. Proses adsorpsi lebih banyak digunakan karena lebih ekonomis. [3]
Pemanfaatan sistem adsorpsi untuk pengambilan ion logam-logam berat dari perairan telah banyak dilakukan. Proses adsorpsi lebih banyak dipakai dalam industri karena mempunyai beberapa keuntungan, yaitu lebih ekonomis dan juga tidak menimbulkan efek samping yang beracun. Pada proses adsorpsi ini diperkirakan beberapa senyawa pada biosorben yang dapat menjadi penyerap logam berat tersebut. Selain itu juga dimungkinkan terjadinya proses ion exchange pada adsorpsi tersebut.
elemen yang terkandung didalam biosorben tersebut.
II. Metodologi Penelitian
2.1. Bahan kimia, peralatan dan instrumentasi
NaOH, NH4OH, HCl, Aquabides bebas
pirogen, Garam Pb(NO3)2 sebagai prekursor
logam Pb, dan cangkang sotong.
Neraca Analitis, SEM-EDX, water shaker, FTIR, SSA dan alat-alat gelas.
2.2. Prosedur penelitian
Persiapan Biosorben
Cangkang sotong dihaluskan, diayak hingga mendapatkan ukuran 125 µm, dicuci dengan aquabides, disaring, produk dikarakterisasi dengan FTIR. Dilanjutkan dengan pencucian menggunakan alkohol 96%, lalu dipanaskan pada suhu ± 800C
selama 24 jam. Produk kering dicuci dengan HCl 1 M, disaring, lalu dicuci dengan aquabides hingga pH netral, dikeringkan pada suhu ± 800C selama 24 jam dan
kemudian dilakukan karakterisasi dengan SEM-EDX. Pada biosorben yang telah digunakan untuk adsorpsi juga dilakukan karakterisasi dengan FTIR.
Prosedur Biosorpsi
Sebanyak 50 mL larutan Pb(II) 50 mg/L dimasukkan kedalam erlenmeyer 250 mL, diatur pH larutan dengan penambahan NaOH/NH4OH 1 M atau HCl 1 M.
Selanjutnya, ditambahkan 1 gram adsorben. Campuran dishaker dengan waktu tertentu, kemudian dihentikan. Setelah setimbang dilakukan penyaringan. Pada filtrat ditentukan konsentrasi sisa ion logam Pb(II) dengan menggunakan Spektroskopi Serapan Atom (SSA).
Persentase Pb yang hilang di hitung dengan menggunakan rumus :
% Pb(II) yang hilang = [ ( Ci – Ce) / Ci]
x100%
Dimana, Ci = Konsentrasi awal Ion logam Ce = Konsentrasi setelah setimbang
Kapasitas adsorpsi dihitung dengan perhitungan sebagai beriukut :
Penentuan pengaruh pH terhadap proses biosorpsi dilakukan dengan variasi pH 4-8 terhadap larutan adsorbat. Dimana waktu kontak yang digunakan adalah 1 jam dan konsentrasi awal larutan Pb(II) adalah 50 mg/L. Penentuan pengaruh dosis adsorben terhadap proses biosorpsi dengan variasi 0,2-1 gram dengan waktu kontak yang digunakan adalah 1 jam dan pH yang digunakan sesuai dengan pH optimum yang di dapatkan pada prosedur optimasi pH dan konsentrasi awal larutan garam yang digunakan adalah 50 mg/L. Penentuan pengaruh konsentrasi awal larutan Pb(II) terhadap proses biosorpsi dengan variasi 25-200 mg/L. Prosedur dengan waktu kontak yang digunakan adalah 1 jam dan pH yang digunakan sesuai dengan pH optimum yang di dapatkan pada prosedur optimasi pH, dan dosis adsorben yang digunakan sesuai dengan dosis optimum yang di dapatkan pada proses optimasi dosis adsorben. Penentuan pengaruh waktu kontak terhadap proses biosorpsi dengan variasi 5-90 menit dimana pH, dosis adsorben dan konsentrasi awal larutan garam, yang digunakan sesuai dengan yang didapatkan pada prosedur optimasi masing-masing parameter tersebut. Untuk Penentuan termodinamika dilakukan variasi suhu 25-40°C dengan interval 5°C dimana waktu kontak, pH, konsentrasi awal larutan garam dan dosis adsorben digunakan sesuai dengan yang didapatkan pada prosedur optimasi masing-masing parameter tersebut.
III. Hasil dan Pembahasan
3.1 Karakterisasi Cangkang Sotong
Karakterisasi cangkang sotong dilakukan denga FTIR dan EDX. Spektrum FTIR cangkang sotong dengan pencucian akuabides dan setelah proses adsorpsi logam Pb(II) digunakan untuk menentukan jenis gugus fungsi yang terdapat pada cangkang sotong tersebut, hasil analisa FTIR dapat dijelaskan oleh gambar 4.1 dan 4.2. Pada gambar tersebut terlihat bahwa munculnya puncak pada daerah 3422 cm-1
daerah 2918 cm-1 menandakan adanya
puncak –CH3, dan pada daerah 1788 cm-1
menandakan adanya puncak C=O. Karakterisasi dengan FTIR setelah dan sebelum adanya proses adsorpsi tidak menunjukkan perbedaan yang signifikan, hal ini dikarenakan pada penelitian ini proses adsorpsi yang terjadi merupakan interkasi fisika. Hasil dar FTIR ini juga diperkuat dengan analisa kandungan unsur cangkang sotong dengan menggunakan EDX.[15][16]
Gambar 4.1 Spektrum FTIR cangkang sotong dengan
pencucian akuabides
Gambar 4.2 Spektrum FTIR cangkang sotong setelah
proses adsorpsi
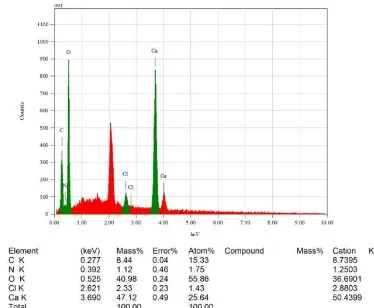
Analisa EDX bertujuan untuk mengetahui komposisi dari adsorben tersebut. Hasil analisa diperlihatkan pada gambar 4.8
Gambar 4.3 Karakterisasi EDX cangkang sotong
Pada gambar 4.3 dapat dilihat bahwa dalam cangkang sotong tersebut terdapat C, N, O, Cl dan Ca, hasil analisa ini bersesuaian dengan analisa FTIR yang telah dilakukan. Unsur yang paling besar terdapat dalam cangkang sotong adalah Ca dengan massa 47,12 %, kemudian O dengan massa 40,98 %. Hasil karakterisasi cangkang sotong dengan EDX mempunyai kesesuaian dengan karakterisasi FTIR.
3.2. Analisa Hasil Optimasi 3.2.1 Optimasi pH
Tingkat distribusi kosentrasi Hidrogen didalam larutan adalah faktor yang mempengaruhi proses adsorpsi. Kapasitas adsorpsi logam akan berbeda pada setiap tingkat keasaman. Oleh karena itu, kondisi keasamaan optimum untuk proses adsorpsi Pb(II) dari larutan perlu diteliti. Dari percobaan yang telah dilakukan diperoleh grafik seperti pada gambar 4.4
Gambar 4.4 Pengaruh pH terhadap proses adsorpsi
logam Pb(II) dari larutan dengan dosis adsorben 1 gram, konsentrasi awal larutan logam 50 mg/L, waktu kontak 1
jam, suhu ±30⁰C dan kecepatan shaker
125 rpm
Berdasarkan grafik dapat dilihat bahwa semakin tinggi pH kapasitas penyerapan logam Pb(II) oleh cangkang sotong semakin menurun, hal ini terjadi karena yang dihitung kapasitas penyerapan ion Pb (II) oleh cangkang sotong, bukan jumlah ion Pb (II) yang diserap. Namun pada pH 6 terjadi penurunan kapasitas yang dratis, disebabkan karena pada pH 6 ion logam Pb(II) lebih banyak yang mengendap dibandingkan yang terserap. Sebelum dilakukan proses adsorpsi pada variasi pH,
3 4 5 6 7 8 9
0 0.5 1 1.5 2 2.5
pH
q
(
m
g
/g
juga di lakukan kontrol pada masing-masing pH untuk mengetahui seberapa banyak logam yang mengendap pada setiap pH, sehingga dapat ditentukan jumlah ion Pb(II) teradsorpsi oleh biosorben. Optimumnya didapatkan pada pH 4 dengan kapasitas adsorpsi 2,390 mg/g. Keadaan ini kemungkinan terjadi karena pada pH makin tinggi maka larutan akan bersifat basa sehingga kelarutan Pb makin kecil akibat terbentuknya endapan Pb(OH)2. Hal ini
memungkinkan Pb yang terserap semakin sedikit.[24]
Pada penelitian ini telah dilakukan pengujian konsentrasi dari ion logam yang mengendap yang kemudian dijadikan sebagai kontrol, sehingga dapat ditentukan jumlah ion Pb(II) bersih teradsorpsi. Dari data percobaan didapatkan kesimpulan pada keadaan pH tinggi ion logam tersebut hanya sedikit yang teradsorpsi karena sebagian besarnya mengalami pengendapan.
3.1.2 Optimasi Dosis Adsorben
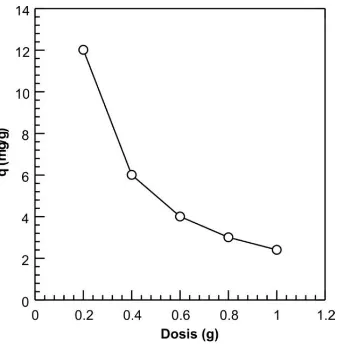
Faktor lain yang mempengaruhi kapasitas adsorpsi logam adalah dosis adsorben.. Pengaruh dosis adsorben tersebut dapat dilihat dari gambar 4.5.
Gambar 4.5 Pengaruh dosis adsorben terhadap proses
adsorpsi logam Pb(II) dari larutan dengan pH 4, konsentrasi awal larutan logam 50
mg/L, waktu kontak 1 jam, suhu ±30⁰C dan
kecepatan shaker 125 rpm
Dari Gambar 4.5 dapat dilihat bahwa kapasitas adsorpsi semakin menurun
seiring bertambahnya dosis adsorben, hal ini di sebabkan karena yang dihitung jumlah ion logam yang teradsorpsi dalam 1 gram adsroben (mg/g), bukan jumlah ion logam yang diserap. Kondisi optimum untuk dosis adsorben ialah 0,2 gram dengan kapasitas penyerapan sebesar 12,018 mg/g. Dosis 0,2 gram merupakan kondisi ideal bagi adsorben cangkang sotonguntuk dapat menyerap ion Pb(II) dengan kosentrasi awal 50 mg/L dan 50 mL di bandingankan dengan jumlah dosis yang lain.[25]
3.1.3 Optimasi Konsentrasi Awal Logam
Penentuan kapasitas penyerapan ion logam oleh adsorben pada variasi kosentrasi dilakukan pada pH dan dosis optimum, untuk menentukan kapasitas adsorpsi dari adsorben, diamati pola adsorpsi oleh adsorben dengan memvariasikan kosentrasi awal larutan Pb(II). Pada penelitian ini digunakan beberapa variasi konsentrasi awal Pb(II) yaitu 25-200 mg/L.
Gambar 4.6 Pengaruh konsentrasi awal ion logam terhadap proses adsorpsi logam Pb(II) dari larutan dengan pH 4, dosis adsorben 0,2 g, waktu
kontak 1 jam, suhu ±30⁰C dan kecepatan
shaker 125 rpm
Dari Gambar 4.6 dapat dilihat bahwa kapasitas terus meningkat dengan peningkatan kosentrasi awal ion logam. Kapasitas maksimum penyerapan ion logam Pb(II) terlihat pada konsentrasi 175 mg/L dengan kapasitas adsorpsi 39,838 mg/g. Adsorben memiliki sejumlah situs aktif dimana tiap situs aktif memiliki probabilitas yang sama untuk berikatan dengan molekul adsorbat. Selama situs aktif belum jenuh
0 25 50 75 100 125 150 175 200 225 0
5 10 15 20 25 30 35 40 45
C awal (mg/L)
q
(m
g/
oleh adsorbat, maka kenaikan konsentrasi adsorbat akan diikuti pula dengan kenaikan jumlah adsorbat yang diikat. Jika semua situs aktif telah mengikat molekul adsorbat, maka kenaikan konsentrasi adsorbat tidak lagi diikuti pertambahan jumlah molekul teradsorpsi. [26] Penurunan kapasitas terjadi
pada konsentrasi > 175 mg/L yang mana terjadi algomerasi ion Pb(II)
3.1.4 Optimasi Waktu Kontak
Pengaruh waktu kontak penyerapan logam Pb(II) dapat dilihat pada grafik berikut.
Gambar 4.7 Pengaruh waktu kontak terhadap proses adsorpsi logam Pb(II) dari larutan dengan pH 4, dosis adsorben 0,2 g, konsentrasi
awal ion logam 175 mg/L, suhu ±30⁰C dan
kecepatan shaker 125 rpm
Dari grafik dapat dilihat kondisi optimum waktu kontak proses adsorpsi ion logam Pb(II) didapatkan pada waktu 30 menit dengan kapasitas adsorpsi 41,512 mg/g. Grafik juga meperlihatkan bahwa semakin lama waktu interaksi antara biosorben dengan larutan ion logam maka semakin besar pula kapasitas penyerapan ion logam tersebut. Pada menit-menit awal adsorpsi Pb (II) oleh cangkan sotong menunjukan kenaikan jumlah Pb (II) yang teradsorpsi secara seginifikan. hal ini diduga karena jumlah situs aktif yang tersedia pada permukaan adsorben masih banyak yang belum terisi atau kondisinya belum jenuh sehingga memudahkan Pb (II) untuk berinteraksi dengan adsorben. Setelah 30 menit, jumlah ion Pb (II) yang teradsopsi terlihat relatif tetap seiring bertambahnya waktu kontak. Hal ini disebabkan situs aktif
pada adsorben sudah terisi penuh oleh ion Pb(II), kondisi ini dianggap telah mencapai kesetimbanga untuk adsorpsi. [27]
3.1.5 Optimasi Suhu
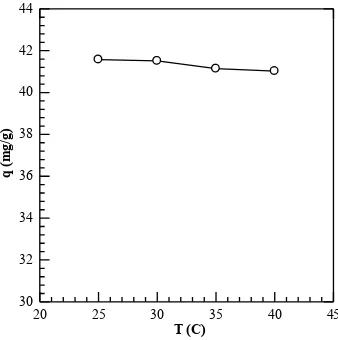
Pengaruh suhu pada proses adsorpsi ion logam Pb(II) dapat dilihat pada grafik berikut.
Gambar 4.5 Pengaruh suhu terhadap proses adsorpsi logam Pb(II) dari larutan dengan pH 4, dosis adsorben 0,2 g, konsentrasi awal ion logam 175 mg/L, waktu kontak 30 menit, kecepatan shaker 125 rpm
Pada grafik dapat dilihat bahwa semakin tinggi suhu, maka kapasitas penyerapannya juga semakin kecil. Pada percobaan ini dapat dilihat bahwa kapasitas maksimum penyerapan logam Pb(II) oleh cangkang sotong adalah pada suhu 25⁰C dengan kapasitas penyerapan maksimumnya adalah 41,577 mg/g, menandakan bahwa reaksi penyerapan ini merupakan reaksi eksotermik, karena dapat dilihat bahwa kapasitas penyerapan akan menurun seiring dengan penambahan suhu.
[28]. Hal ini dikarenakan pada suhu tinggi
pergerakan dari partikel logam menjadi lebih cepat sehingga kemungkinan kontak antara logam dan biosorben semakin sedikit
[29]
.
IV. Kesimpulan
Optimasi proses adsorpsi ion logam Pb(II) oleh cangkang sotong didapatkan kondisi pH optimum 4, dosis adsorben 0,2 gram, konsentrasi awal ion logam 175 mg/L, waktu kontak optimum untuk mencapai
kesetimbangan 30 menit, dan temperatur optimum 25°C dengan kapasitas adsorpsi maksimum adalah 41,5767 mg/g. Karakterisasi cangkang sotong dengan FTIR dan SEM-EDX, diduga gugus yang berperan aktif dalam proses adsorpsi adalah gugus – OH dan C=O. Penggunaan limbah cangkang sotong sebagai adsorben tampaknya lebih ekonomis dan merupakan alternatif yang bermanfaat. Penelitian ini berhasil menunjukkan bahwa cangkang sotong dapat digunakan menjadi adsorben yang lebih efisien untuk penghilangan Pb(II) dari limbah air.
V. Ucapan terima kasih
Saya sangat berterima kasih kepada analis laboratorium terpadu kopertis wilayah X dan kepada DIKTI yang telah mendanai penelitian ini
Referensi
1. Darmono. Logam dalam sistem mahluk hidup. Penerbit Universitas Indonesia, Jakarta, 1995, Hal. 10-12, 21-23, 26
2. Sembodo, Bregas. Model Kinetika Langmuir untuk Adsorpsi Timbal pada Abu Sekam Padi, Skripsi, Jurusan Teknik Kimia Fakultas Teknik UNS, 2006Raya, Indah., Ramlan, 2012, The Bioaccumulation Of Cd(II) Ions On
Euchema Cottoni Seaweed, Marina Chi,ica Act, Vol.13, No.2
3. Danorta dan Enny Kriswiyanti, Model Kesetimbangan Adsorpsi Cr dengan Rumput Laut, Jurusan Teknik Kimia Fakultas Teknik UNS, 2007.
4. Nurzakiah, Komposisi Asam Lemak dan Kolesterol Sotong (Sepia recurvirostra), Skripsi, Fakultas Perikanan dan Ilmu Kelutan, Bogor.2009
5. Jereb P, Roper CFE, Cephalopods of the world, FAO Species Catalogue for Fishery Purpose, 2005,No.4, Vol.1 : 114-115
6. Reilly, C. Metal contamination food, Second edition, Elsevier science
Publisher LTD. London and New York. 1991
7. Apriadi, Dandy, Kandungan Logam Berat Hg, Pb dan Cr pada Air, Sedimen dan Kerang Hijau (Perna viridis L.) di Perairan Kamal Muara Teluk Jakarta,
Skripsi , Fakultas Perikanan dan Ilmu Kelutan, Bogor,2011
8. Rohilan, I, Keadaan Sifat Fisika dan Kimia Perairan di Pantai Zona Industri Krakatau Steel Cilegon. Skripsi. Program Studi Ilmu Kelautan, Fakultas Perikanan, Institut Pertanian Bogor, 1992.
9. EPA, Water qualitiy criteria. Environmental protection agency. Ecology research series. Washington, 1973.
10. Wijaanto, Yogi Rifki, Darjito dan Yuniar Ponco Prananto, Pengaruh pH dan Waktu Kontak pada Adosrpsi Pb(II) Menggunakan Limbah Adsorben Kitin Terfosforilasi dari Limbah Cangkang Bekicot (achatina fulica).
Jurusan Kimia FMIPA Universitas Brawijawa, 2013
11. Herman, D.Z, Tinjauan Terhadap Tailing Mengandung Unsur Pencerman Arsen (As), Merkuri (Hg), Timbal (Pb), dan Kadmium (Cd) dari Sisa Pengolahan Biji Logam, Pusat Sumber Daya Geologi, Bandung), 2006.
12. Kundari, Noor Anis dan Slamet Wiyuniata, Tinjauan Kesetimbangan Adsorpsi Tembaga dalam Limbah Pencuci PCB dengan Zeolit, Sekolah Tinggi Teknologi Nuklir, Batan, 2008
13. Seseno, Hadi Prasetyo, Model Adsorpsi Mn+2, Cd+2 dan Hg+2 dalam Sistem
Air-Sedimen di Sepanjang Sungai Code Yogyakarta,Jurusan Teknik Lingkungan, Fakultas Sains Terapan, Jurnal Teknologi, 2011 Volume 4 Nomor 2, hal 174-179
15. DUYGU, Dilek(Yalcin)., Tualay, BAYKAL., Ilkay, ACIKGOZ., Kazim, YILDIZ., [review], 2009, Fourier Transform Infrared (FT-IR) Spectroscopy for Biological Stuies, , Vol. 22, No.3 : 117-121
16. Areekijseree, Mayuva., Kamolchanok, Panishkan., Natdhera, Sanmanee., Kanokporn, Swangjang., 2009, Microanalysis by SEM-EDX on Structure and Elemental Composition of SoilsfromDifferent Agriculture Areass in The Western Region of Thailand, Journal of Microscopy Society of Thailand, Vol. 23, No.1: 152-156
17. Gandjar, I, G dan Rohman, A. Kimia Farmasi Analisis. Cetakan Pertama. Yogyakarta: Pustaka Belajar. 2007, Hal. 22-23.
18. Mohsin Kazmi, Nadeem Feroze, Hassan Javed, Muhammad Zafar And Naveed Ramzan, Biosorption of Copper (II) on Dry Fruit by Product: Characterization, Kinetic and Equilibrium Studies, 2012, No.6, Vol. 34, hal 1356-1365
19. Hossain, M.A. H. H. Ngo, W. S. Guo. T. V. Nguyen. Biosorption of Cu(II) From Water by Banana Peel Based Biosorbent : Experiment and Models of Adsorption and Desorption, Journal of Water Sustainability, Vol.2: 87-104
20. Goldstein, J. I., et al. Scanning Electron Microscopy and X-ray Micronalysis, 3rd ed, Plenum Press, New York. 2003
21. Desi Anggraeni, Nuha , Analisa SEM (Scanning Electron Microscopy) dalam Pemantauan Proses Oksidasi Magnetite
Menjadi Hematite, Kampus ITENAS
Bandung. 2008,
22. Tucker, Maurice, Techniques in Sedimentology, Blackwell Scientific Publication, Oxford/London, England,
23. Bijaksana, S., Rock Magnetic Methods for Environmental Studies. ASEANIP Regional
Seminar on the Physics of Metals and Alloys, 1996.
24. Tangio, Julhim S, Adsorpsi Logam Berat Timbal (Pb) dengan Menggunakan Biomassa Enceng Gondok (Eichhornia crassipes),
Jurusan Kimia Fakultas Metematika dan Ilmu Pengetahuan Alam Universitas Gorongtalo, 2012.
25. Afrianita. Reri, Yommi Dewilda dan Rafiola Fitri, Efisiensi dan Kapasitas Penyerapan Fly Ash sebagai Adsorben dalam Penyisihan Logam Timbal (Pb) Limbah Cair Industri, Jurusan Teknik Lingkungan Universitas Andalas, Padang, 2013, Hal 6.
26. Utami. Umi Baroroh Lili, Taufiqur Rohman dan Mahmud , Adsorpsi Pb(II) oleh Kitosan Terlapiskan pada Arang Aktif Cangkang Sawit, Program Studi Kimia FMIPA Universitas Lambung Mangkurat ; Banjarbaru, 2009.
27. Nurlamba. Nessha Siti, Zackiyah, dan Wiwi Siswaningsih. Kajian Kinetika Interaksi Kitosan-Bentonit dan Adsorpsi Diazinon Terhadap Kitosan-Bentonit, Progam Sutdi Kimia, Jurusan Pendidikan Kimia, Univeristas Pendidikan Indonesia. 2010
28. Diantariani, N.P, Proses Biosorpsi dan Desorpsi Ion Cr(VI) Pada Biosorben Rumput Laut Euchema spinosum, 2008, No.1, Vol.2: 45-52
29. Rao, K.S. S.Anand. P Venkateswarlu,