(Averrhoa carambolaL.) PADA MENCIT PUTIH BETINA GALUR SWISS
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh: Dewi Susanti NIM: 068114126
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
UJI EFEK ANTIINFLAMASI DAN ANALGESIK JUS BUAH BELIMBING (Averrhoa carambolaL.) PADA MENCIT PUTIH BETINA GALUR SWISS
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh: Dewi Susanti
NIM: 068114126
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
v
HALAMAN PERSEMBAHAN Tuhanku,,
Engkau yang selalu berbicara padaku ketika aku kesepian Memberikanku dukungan ketika aku dirundung kecemasan
Mendengarkan suaraku saat aku jatuh
Engkau yang sudi menjadi penghiburan bagiku dalam perjalanan, Tempat berteduh di waktu hujan,
Tempat bernaung di kala panas, Tongkat penuntun dalam kelelahan,
Dan penolong dalam bahaya Engkau yang membuatku berhasil
Mencapai tujuanku, Sekarang, dan juga nanti
Pada akhir hidupku
Tulisan ini saya persembahkan untuk:
Tuhan Yesus,
walaupun karya ini terlalu kecil untuk sebuah ungkapan syukur,
Mama dan Papa, yang telah melahirkan, mendidik, dan mengasihi saya
selalu,
Kakak saya tercinta Yuli Suprihatini, yang tidak pernah berhenti menyayangi
dan mengajari saya arti berjuang yang sesungguhnya,
Ayis Suti Wibowo dan Anjar Murtiningsih, kakak kandung sekaligus pengganti
orangtua bagi saya
vii PRAKATA
Rasa syukur dan terima kasih penulis panjatkan kepada Tuhan Yesus, sebab
atas segala anugerah dan penyertaanNya penulis dapat menyelesaikan skripsi yang
berjudul “Uji Efek Antiinflamasi dan Analgesik Jus Buah Belimbing (Averhoa
carambolaL.) Pada Mencit Putih Betina Galur Swiss”, dengan baik.
Dari awal proses penyusunan proposal skripsi, pelaksanaan penelitian sampai
pada tahap penulisan skripsi, banyak hambatan dan kedala yang terjadi. Namun,
berkat adanya dukungan, doa, bantuan, bimbingan, dan kerjasama dari berbagai
pihak, semua bisa terselaikan dengan baik. Sehingga pada kesempatan ini, dengan
segenap hati penulis mengucapkan terima kasih kepada:
1. Rita Suhadi, MSi., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata
Dharma.
2. Bapak Yosef Wijoyo, M.Si., Apt., selaku dosen pembimbing yang telah
memberikan arahan, masukkan, dan saran selama penyusunan skripsi ini.
3. Bapak Drs. Mulyono, Apt., selaku dosen penguji yang telah memberikan
masukkan, saran, dan kritik yang membangun, serta berbagai referensi buku
dan jurnal.
4. Ibu Phebe Hendra, Ph.D., Apt., selaku dosen penguji yang telah memberikan
masukkan, saran, dan kritik yang membangun.
5. Bapak Ipang Djunarko, M.Sc., Apt., yang banyak memberikan bimbingan dan
viii
6. Mama, Papa, dan Ci Yuli di Surga, yang selalu menjadi motivasi penulis
untuk memberikan yang terbaik.
7. Kakak saya, Ayis Suti Wibowo, atas kasih sayang, pengorbanan, motivasi
yang selalu menguatkan, dan selalu ada baik dalam keadaan bahagia maupun
di saat paling buruk dalam hidup penulis.
8. Seluruh dosen dan karyawan Fakultas Farmasi yang telah berbagi
pengetahuan.
9. Fakultas Teknik Mekatronika Universitas Sanata Dharma yang telah bersedia
memberikan pinjaman alat berupa Jangka Sorong untuk penelitian ini.
10. Mas Parjiman, Mas Heru, dan Mas Kayat, selaku laboran yang banyak
membantu proses penelitian.
11. Keluarga saya terkasih di Purworejo, Bulek Sutarni, Lek Madi, Budhe
Legiem, Bayu, Bela, Erlin, Mas Ripto. Juga seluruh keluarga di Jakarta,
Bogor, Bandung,love you all!
12. Keluarga Purnomo, Om Cipto, Tante Yana, Ci Yoana, Kak Ino, Ezer, Edo.
Serta keluarga Meilina D. Pattikawa dan Patrick Gunawan Hartono, atas
segala ketulusan hati menjadikan penulis selayaknya keluarga.
13. Rekan penelitian ini, Tanti, Jeffry, dan Ricky, Gun, Felix, untuk tenaga,
waktu, dan pikiran yang secara tulus diberikan.
14. Sahabat saya, Regina Citra Dewanti, untuk setiap penghiburan dan uluran
ix
In, Dek Adrian, Mbak Indira, Dek Ardo, Mbak Nunung, Bu Yeti untuk
kehangatan sebuah keluarga.
15. Keluarga Su (baik), Cita, Krisna, Ginji, dan Fea, atas persahabatan yang unik
dan indah.
16. Para sahabat, Della, Esti, Helen, Mike, Devita, Rere, Lita, Grace, Wiwit,
Ciput, Henny, Riri, Jati, Sammy, atas dukungan dan semangat yang diberikan.
Ryan, atas pinjamanblender-nya. Dan seluruh teman-teman angkatan 2006.
17. Reynold Steve McWhiter and all his family there,thanks for the love and care
you gave to me.
18. Semua teman dan pihak-pihak yang tidak dapat disebutkan satu-persatu.
Semoga Tuhan selalu melimpahkan berkat dan karunia-Nya, atas segala
kebaikan dan jasa yang telah diberikan.
Penulis menyadari adanya kekurangan dalam skripsi ini, untuk itu penulis
selalu terbuka untuk saran, masukkan, dan kritik yang membangun. Akhir kata,
semoga karya ini bisa bermanfaat bagi perkembangan ilmu dan pengetahuan serta
xi INTISARI
Buah belimbing (Arverrhoa carambola L.) dikenal karena bentuk bintangya yang unik dan dapat digunakan sebagai obat tradisional. Penelitian ini dilakukan untuk membuktikan kebenaran khasiat jus buah belimbing sebagai obat antiinflamasi dan analgesik. Penelitian ini merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah. Subyek uji yang digunakan adalah mencit putih betina galurSwiss, berumur 2-3 bulan dengan berat badan 20-30 gram.
Obyek uji dalam penelitian ini adalah jus buah belimbing yang terbagi dalam 3 peringkat dosis, yaitu 1,67; 3,34; dan 6,67 g/kg BB. Penelitian pertama merupakan penelitian daya antiinflamasi dengan menggunakan karagenin sebagai penginduksi edema pada telapak kaki mencit dan diklofenak 4,48 mg/kg BB sebagai kontol positifnya. Penelitian kedua merupakan penelitian daya analgesik mengunakan metode geliat, dengan asam asetat sebagai pengiduksi geliat dan parasetamol 91 mg/kg BB sebagai kontrol positif.
Hasil penelitian menunjukkan bahwa jus buah belimbing dosis 3,34 dan 6,67 g/kg BB terbukti memiliki efek antiinflamasi dan analgesik. Daya antiinflamasi jus buah belimbing dosis 1,67; 3,34; dan 6,67 g/kg BB berturut-turut adalah 22,91%; 54,58%; dan 36,06%; sedangkan daya analgetikanya sebesar 3,24%; 70,27%; dan 56,76%. Dosis optimal jus buah belimbing yang berkhasiat sebagai antiinflamasi maupun analgesik yaitu dosis 3,34 g/kg BB.
xii ABSTRACT
Starfruit (Averrhoa carambola L.) is known for its uniqueness star shape and can be used as traditional medicine. This study aims to prove that starfruit juice really has anti-inflammatory and analgesic effect. This is a pure experimental research with one-way pattern, random and complete research design. The subject of this study was Swiss white female mice which ranging age are 2-3 months and its weight between 20-30 g.
The object of this study was star fruit juice which doses are divided into 3 groups, 1,67; 3,34; and 6,67 g/kg BW. The anti-inflammatory test using carrageenin-induced edema in hind paw of the mice assay and diclofenac 4,48 mg/kg BW as positive control was performed first. Then the study continued with analgesic assay using writhing test, acetic acid as the writhing inducer and acetaminophen 91 mg/kg BW as the positive control.
The result shows that the star fruit juice at the dose 3,34 and 6,67 g/kg BW has anti-inflammatory and analgesic effect. The anti-inflammatory potency of the star fruit juice at the dose 1,67; 3,34; and 6,67 g/kg BW were 22,91%; 54,58% and 36,06%; the analgesic potency were 3,24%; 70,27%; and 56,76%, respectively. The optimal dose of star fruit juice to get both anti-inflammatory and analgesic effect is 3,34 g/kg BW.
xiii DAFTAR ISI
HALAMAN JUDUL………ii
HALAMAN PERSETUJUAN PEMBIMBING... …iii
HALAMAN PENGESAHAN……….iv
HALAMAN PERSEMBAHAN………...v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI……….vi
PRAKATA………..vii
PERNYATAAN KEASLIAN KARYA………..x
INTISARI……….xi
ABSTRACT………....xii
DAFTAR ISI………..xiii
DAFTAR GAMBAR...xviii
DAFTAR LAMPIRAN………...xx
BAB I PENGANTAR………...…1
A. Latar Belakang... 1
1. Perumusan masalah ... 4
2. Keaslian penelitian ... 4
3. Manfaat penelitian ... 7
B. Tujuan Penelitian... 7
xiv
2. Tujuan khusus... 7
BAB II PENELAAHAN PUSTAKA………..9
A. Belimbing ... 9
1. Sistematika ... 9
2. Kandungan kimia ... 9
3. Kegunaan... 9
4. Morfologi tanaman ... 10
B. Flavonoid ... 10
C. Peradangan ... 11
1. Pengertian peradangan ... 11
2. Terjadinya radang... 12
3. Tanda-tanda peradangan... 16
D. Nyeri ... 18
1. Pengertian nyeri... 18
2. Terjadinya nyeri ... 19
3. Jenis nyeri... 22
E. Antiinflamasi ... 23
F. Diklofenak ... 24
G. Analgetika... 25
xv
I. Metode Pengujian Daya Antiinflamasi ... 28
J. Metode Pengujian Daya Analgetika ... 30
K. Landasan Teori ... 37
L. Hipotesis ... 38
BAB III METODE PENELITIAN……….39
A. Jenis dan Rancangan Penelitian... 39
B. Variabel Penelitian dan Definisi Operasional ... 39
1. Variabel utama ... 39
2. Variabel Pengacau ... 39
3. Definisi Operasional... 40
C. Bahan Penelitian... 41
D. Alat Penelitian ... 42
E. Tata Cara Penelitian ... 42
1. Penelitian efek antiinflamasi ... 42
2. Penelitian efek analgesik ... 48
F. Tata Cara Analisis Hasil ... 53
BAB IV HASIL DAN PEMBAHASAN………...55
A. Determinasi Tanaman... 55
B. Penelitian Efek dan Daya Antiinflamasi ... 55
xvi
2. Efek dan Daya Antiinflamasi Jus Buah Belimbing... 62
C. Penelitian Efek dan Daya Analgesik Jus Buah Belimbing... 75
1. Uji Pendahuluan ... 75
2. Efek dan Daya Analgesik Jus Buah Belimbing... 81
D. Perbandingan Hasil Uji Daya Antiinflamasi dan Analgesik ... 89
BAB V KESIMPULAN DAN SARAN………...93
A. Kesimpulan... 93
B. Saran ... 93
DAFTAR PUSTAKA……… 94
LAMPIRAN………... 97
xvii
DAFTAR TABEL
Tabel I. Hasil analisis uji Scheffe antar kelompok rentang waktu pengukuran
edema pada kaki mencit setelah injeksi karagenin 1% ... 57
Tabel II. Hasil analisis ujiScheffeantar kelompok dosis diklofenak ... 59
Tabel III. Ringkasan hasil uji Scheffe kelompok antar waktu pemberian dosis
efektif diklofenak ... 61
Tabel IV. Rata-rata diameter edema yang terjadi pada masing-masing kelompok
perlakuan…... 64
Tabel V. Ringkasan hasil ujiScheffe% daya antiinflamasi... 68
Tabel VI. Persentase potensi relatif kelompok perlakuan terhadap diklofenak
sebagai kontrol positif... 70
Tabel VII. Hasil analisis ujiScheffeantar kelompok dosis diklofenak ... 76
Tabel VIII. Hasil analisis ujiScheffeantar kelompok dosis diklofenak ... 79
Tabel IX. Hasil analisis ujiScheffeantar kelompok rentang waktu pemberian asam
asetat ... 81
Tabel X. Rata-rata jumlah geliat dan %proteksi geliat yang terjadi pada kontrol
negatif, kontrol positif, dan kelompok perlakuan ... 83
Tabel XI. Hasil analisis ujiScheffepersentase penghambatan geliat... 85
xviii
DAFTAR GAMBAR
Gambar 1. Struktur katekin... 10
Gambar 2. Diagram ringkas dari pembentukkan mediator inflamasi yang berasal
dari fosfolipid dengan garis besar aksinya dan tempat aksi obat
antiinflamasi…... 13
Gambar 3. Terjadinya nyeri; penghantaran impuls; lokalisasi dan rasa nyeri serta
inhibisi nyeri endogen dalam bagan sederhana ... 21
Gambar 4. Struktur diklofenak ... 24
Gambar 5. Bagan kemungkinan pengaruh macam-macam obat terhadap nyeri
(menurut Keldel) ... 26
Gambar 6. Struktur parasetamol ... 27
Gambar 7. Data edema yang terjadi pada kaki mencit pada rentang waktu tertentu
setelah injeksi karagenin 1% subplantar ... 56
Gambar 8. Data hasil orientasi dosis efektif diklofenak ... 58
Gambar 9. Data hasil orientasi wakt efektif diklofenak ... 60
Gambar 10. Diagram batang rata-rata % daya antiinflamasi kelompok perlakuan
terhadap kontrol karagenin ... 66
Gambar 11. Diagram batang % potensi relative kelompok perlakuan terhadap
diklofenak sebagai kontrol positif... 70
xix
Gambar 13. Pembentukan prostaglandin melalui adisi karbon 9 dan 11 oleh radikal
superoksid ... 72
Gambar 14. Reaksi penangkapan radikal hidroksil oleh katekin... 73
Gambar 15. Hasil penetapan dosis efektif asam asetat ... 76
Gambar 16. Hasil orientasi dosis efektif parasetamol ... 78
Gambar 17. Hasil orientasi selang waktu pemberian asam asetat ... 80
Gambar 18. Diagram rata-rata % perubahan penghambatan geliat terhadap kontrol positif ... 86
Gambar 19. Grafik profil geliat kelompok perlakuan jus buah belimbing dan parasetamol ... 88
xx
DAFTAR LAMPIRAN
Lampiran 1. Surat keterangan determinasi buah belimbing ... 97
Lampiran 2. Gambar alat blender yang digunakan untuk membuat jusBelimbing,
buah belimbing yang sesuai criteria pemilihan dan jus buah belimbing
konsentrasi 20% ... 98
Lampiran 3. Gambar mencit yang menggeliat sesuai dengan definisi operasional.... 98
Lampiran 4. Gambar cara pengukuran edema dengan jangka sorong ... 99
Lampiran 5. Skema kerja uji efek antiinflamasi ... 100
Lampiran 6. Skema kerja uji efek analgesik ... 101
Lampiran 7. Data penetapan rentang waktu pengukuran edema dan analisis
statistiknya ... 102
Lampiran 8. Data Penetapan Dosis Efektif Diklofenak dan Analisis Statistiknya... 105
Lampiran 9. Data Penetapan Waktu Pemberian Dosis Efektif Diklofenak dan Analisis
Statistiknya... 108
Lampiran 10. Perhitungan penetapan peringkat dosis jus buah belimbing pada
kelompok perlakuan ... 111
Lampiran 11. Data diameter edema pada uji efek antiinflamasi jus buah belimbing112
Lampiran 12. Data % daya antiinflamasi dan analisis statistiknya... 115
Lampiran 13. Rata-rata % daya antiinflamasi dan potensi relatif kelompok perlakuan
xxi
Lampiran 14. Data penetapan dosis asam asetat dan analisis statistiknya... 119
Lampiran 15. Data penetapan dosis efektif parasetamol dan analisis statistiknya ... 121
Lampiran 16. Data penetapan rentang waktu pemberian rangsang geliat ... 124
Lampiran 17. Data jumlah geliat pada uji efek analgesik beserta analisis
statistiknya………127
Lampiran 18. Data % penghambatan geliat terhadap kontrol negatif pada uji analgesik
dan analisis statistiknya... 130
Lampiran 19. Data % perubahan penghambatan geliat terhadap kontrol positif
1 BAB I PENGANTAR A. Latar Belakang
Peradangan merupakan reaksi kompleks dalam jaringan yang melibatkan
respon pembuluh darah dan leukosit. Peradangan mungkin menjadi berbahaya dalam
beberapa situasi. Mekanisme peradangan untuk menghancurkan penginvasi dan
jaringan nekrosis memiliki kemampuan intrinsik untuk merusak jaringan normal.
Ketika peradangan tidak tepat sasaran dan merusak jaringan itu sendiri atau
peradangan tidak terkontrol dengan baik, maka hal ini bisa menjadi penyebab
kerusakan dan penyakit (Kumar, Abbas, Fausto, dan Aster, 2010).
Manifestasi klinis dan patologi dari respon peradangan disebabkan oleh
beberapa reaksi. Fenomena vaskuler pada peradangan akut ditandai dengan adanya
peningkatan aliran darah menuju daerah yang terluka, akibat dari dilatasi arteriola dan
pembukaan kapiler karena induksi mediator seperti histamin. Meningkatnya
permeabilitas vaskuler mengakibatkan akumulasi cairan protein ekstraseluler yang
menimbulkan eksudat. Protein plasma keluar dari pembuluh darah, sebagian besar
melewati cell junctioninterendotelial vena yang melebar. Kemerahan (rubor), panas
(kalor), dan bengkak (tumor) pada peradangan disebabkan karena meningkatnya
aliran darah dan edema. Leukosit yang tersirkulasi, yang didominasi neutrofil,
bermigrasi ke daerah yang terluka. Leukosit yang teraktivasi akan melepaskan
Ketika terjadi kerusakan jaringan, dan adanya pelepasan prostaglandin, neuropeptida,
dan sitokin, salah satu simpton lokal peradangan adalah nyeri (dolor) (Kumar dkk.,
2010).
Nyeri merupakan pengalaman subyektif, yang sulit untuk dideskripsikan
secara pasti, meskipun kita semua tahu apa yang dimaksud dengan nyeri (Rang, Dale,
Ritter, dan Moore, 2007). Walaupun nyeri sering berfungsi untuk mengingatkan dan
melindungi dan sering memudahkan diagnosis, pasien merasakannya sebagai hal
yang tak mengenakkan, kebanyakan menyiksa dan karena itu berusaha untuk bebas
darinya. Pada beberapa penyakit, misalnya pada tumor ganas dalam fase akhir,
meringankan nyeri kadang-kadang merupakan satu-satunya tindakan yang berharga
(Mutschler, 1986).
Secara umum, pengatasan peradangan dan nyeri dapat dijelaskan sebagai
berikut: penghambatan pembentukkan prostaglandin, yaitu suatu mediator
peradangan dan nyeri. Penghambatan bisa dilakukan dengan berbagai cara: (i)
penghambatan pembentukan asam arakidonat oleh obat-obat steroid, (ii)
penghambatan enzim siklooksigenase (COX) oleh obat-obat antiinflamasi non steroid
(AINS), dan (iii) penghambatan radikal bebas oleh senyawa antioksidan (Rang dkk.,
2007). Dengan dihambatnya prostaglandin, maka perdangan dapat diatasi. Sedangkan
rasa nyeri juga berkurang karena reseptor nyeri tidak tersensibilitasi oleh
Beberapa senyawa alam yang terdapat dalam tumbuhan memiliki aktivitas
sebagai penghambat radikal bebas atau secara luas dikenal sebagai senyawa
antioksidan. Salah satu tanaman yang memiliki kandungan senyawa antioksidan
adalah belimbing(Averrhoa carambolaL.) yang merupakan suku oksalidaceae. Buah
belimbing, memiliki kandungan polifenol dan asam askorbat yang diketahui sebagai
antioksidan (Wakte, Patil, Patil, dan Phatak, 2007). Hal ini dikuatkan dengan hasil
penelitian (Sari, 2008) yang menyatakan bahwa ekstrak etanol 96% buah belimbing
(Averrhoa carambola L.) memiliki aktivitas antioksidan yang ditunjukkan oleh nilai
IC50 sebesar 28,82 ± 0,04 µg/mL, sehingga digolongkan sebagai antioksidan kuat,
karena nilai IC50 kurang dari 200 µg/mL. Selain itu, sebelumnya juga pernah
dilakukan pengujian beberapa efek farmakologi buah Averrhoa carambolaLinn pada
hewan percobaan, yang salah satunya menunjukkan adanya efek analgesik sari buah
pada dosis 2,5; 5; dan 10 ml/kg BB (Rianti, Padmawinata, dan Andreanus, 1978).
Berdasarkan pada uraian di atas, maka peneliti tertarik untuk melakukan
penelitian mengenai ada tidaknya efek antiinflamasi dan analgesik pada jus buah
belimbing manis. Dalam penelitian ini digunakan jus, bukan sari, karena di
masyarakat jus lebih terjangkau dibandingkan sari, karena dalam pembuatan sari
dibutuhkan alatjuice extractor, yang cukup mahal.
Untuk menguji efek antiinflamasi digunakan metode rangsang edema, karena
metode ini telah digunakan oleh banyak peneliti dan telah terbukti cocok untuk
digunakan metode geliat, karena metode ini dapat mendeteksi baik analgesik sentral
maupun perifer. Metode ini juga telah banyak digunakan dan direkomendasikan
sebagai suatu metode skrining yang cukup sederhana (Vogel, 2002).
1. Perumusan masalah
Berdasarkan uraian di atas, permasalahan yang muncul dalam penelitian ini
dapat dirumuskan sebagai berikut:
a. Apakah jus buah belimbing (Averrhoa carambola L.) mempunyai efek
antiinflamasi dan atau analgesik?
b. Seberapa besar daya antiinflamasi dan atau analgesik jus buah belimbing
(Averrhoa carambolaL.)?
2. Keaslian penelitian
Berdasarkan studi pustaka yang dilakukan oleh peneliti dan sejauh
pengetahuan peneliti, penelitian tentang efek antiinflamasi dan analgesik jus buah
belimbing (Averrhoa carambola L.) belum pernah dilakukan. Penelitian yang pernah
dilakukan yaitu:
a. Pengujian Beberapa Efek Farmakologi Buah Averrhoa carambola Linn pada
hewan percobaan (Rianti dkk., 1978), dan disimpulkan bahwa sari buah
Averrhoa carambola Linn memiliki efek analgesik pada dosis 5, 10, dan 20
ml/kg BB, efek diuretik dan hipoglikemik pada dosis 5 dan 10 ml/kg BB. Sari
buah 2,5; 5; dan 10 ml/kg BB tidak menunjukkan efek antipiretik pada tikus,
buah segar) hanya menunjukkan efek hipoglikemik. Perbedaan penelitian ini
dengan penelitian yang akan dilakukan oleh penulis adalah pada penelitian ini
digunakan sari buah belimbing, sedangkan penulis menggunakan jus buah.
Selain itu, dosis yang digunakan penulis juga tidak sama dengan penelitian
sebelumnya.
b. Daya Antioksidan Ekstrak Etanol 96% Buah Belimbing(Averrhoa carambola
L.) dengan metode 2,2-diphenyl-1-picrylhydrazyl (DPPH) (Sari, 2008), dan
disimpulkan bahwa ekstrak etanol 96% buah belimbing memiliki aktivitas
antioksidan yang ditunjukkan oleh nilai IC50 sebesar 28,82 ± 0,04 µg/mL,
sehingga digolongkan sebagai antioksidan kuat, karena nilai IC50kurang dari
200 µg/mL. Kandungan senyawa yang bertanggung jawab sebagai
antioksidan adalah polifenol dan vitamin C.
c. Antioxidant and Antimicrobial Activities of Averrhoa carrambola L. Fruit
(Wakte dkk., 2007), dan disimpulkan bahwa daya antioksidan ekstrak
Averrhoa carambola L. bergantung pada konsentrasi dan tingkat kematangan
buah. Nilai IC50muda, setengah masak, dan masak secara berurutan 300, 250,
dan 250 µg/mL.
d. Senyawa Antibakteri Golongan Flavonoid dari Buah Belimbing Manis
(Averrhoa carambola Linn) (Sukadana, 2009), dan disimpulkan bahwa isolat
flavonoid fraksi FB dari ekstrak kental air buah belimbing manis diduga
dan C-4’. Identifikasi dengan spektrofotometer inframerah diduga bahwa
isolat flavonoid mengandung gugus OH, C-H aromatik, C-H alifatik, C=C
aromatik, C-O alkohol dan tidak adanya gugus C=O. Dan fraksi tersebut
diduga dapat menghambat bakteri gram positif dan gram negatif mulai dari
konsentrasi 500 ppm dan 100 ppm.
e. Anti-inflammatory and Bactericidal Properties of Selected Indigenous
Medical plants Used for Dysuria (Sripanidkulchai, Tattawasart,
Laupattarakasem and Wongpanich, 2002), dan disimpulkan bahwa pemberian
secara intraperitoneal ekstrak air akar Carica papaya (10 g/kg BB, p.o.),
Ananas comosus (20 g/kg BB, i.p.), dan tangkai pohonAverrhoa carambola
(20 g/kg BB, i.p.) pada jam pertama setelah induksi karagenin, memberikan
efek antiinflamasi yang setara dengan asam asetilsalisilat (ASA) 300 mg/kg
BB sebagai kontrol positif. Namun, setelah jam kedua dan ketiga,
ekstrak-ekstrak tersebut menunjukkan aktivitas anti-inflamasi yang lebih kuat
daripada ASA. Untuk aktivitas antibakteri, Staphylococcus aureus paling
sensitif terhadap ekstrak A. caramboladengan kadar bunuh minimum (KBM)
15,62 mg/ml atau kurang, ekstrakC. rotundus dan I. cylindrica menghambat
E. coli, Ps. aeruginosa, dan S. aureus dengan KBM 62,5 mg/mL. C. papaya
3. Manfaat penelitian
Dengan adanya penelitian tentang daya antiinflamasi dan analgesik jus buah
belimbing (Averrhoa carambola L.) diharapkan akan diperoleh manfaat sebagai
berikut:
a. Secara teoritis
Penelitian ini diharapkan dapat menambah informasi terutama dalam
bidang ilmu kefarmasian mengenai khasiat buah belimbing (Averrhoa
carambolaL.) sebagai antiinflamasi dan analgesik.
b. Secara praktis
Hasil penelitian ini diharapkan dapat membantu masyarakat dalam
penyediaan obat tradisional sebagai alternatif dalam mengurangi peradangan
dan rasa nyeri.
B. Tujuan Penelitian 1. Tujuan umum
Penelitian ini bertujuan untuk menambah informasi mengenai khasiat jus
buah belimbing terutama yang digunakan sebagai antiinflamasi dan pengurang
rasa nyeri.
2. Tujuan khusus
a. Mengetahui ada tidaknya efek antiinflamasi dengan metode Langford,
Holmes, dan Emele (1972) dan atau analgesik dengan metode geliat pada jus
b. Mengetahui besarnya daya antiinflamasi dan atau analgesik pada
masing-masing dosis jus buah belimbing (Averrhoa carambola L.) yang digunakan
9 BAB II
PENELAAHAN PUSTAKA A. Belimbing
1. Sistematika
Divisi : Spermatophyta
Sub divisi : Gymnospermae
Kelas : Dicotyledonae
Ordo : Geranilases
Famili : Oxalidaceae
Genus : Averrhoa
Spesies :Averrhoa carambolaL. (Lawrence, 1951)
2. Kandungan kimia
Buah belimbing mengandung asam oksalat (0,03% dari berat buah segar),
vitamin C (0,05% dari berat buah segar), monopolisakarida, karotenoid (Heber,
2007), serta katekin (Sukadana, 2009).
3. Kegunaan
Buah belimbing digunakan untuk mengobati diare, mual, dehidrasi, hemoroid,
demam, dan nyeri hati (Heber, 2007). Efek analgesik ditunjukkan pada sari buah
belimbing pada dosis 5, 10, dan 20 ml/kg BB, efek diuretik dan hipoglikemik pada
dosis 5 dan 10 ml/kg BB (Rianti dkk., 1978). Selain itu, Sari (2008) menyatakan
4. Morfologi tanaman
Merupakan tanaman berbatang kayu yang dapat tumbuh hingga mencapai
tinggi 5 meter. Bentuk daunnya berubah-ubah dan memiliki panjang 10-12 cm.
bunganya berwarna keunguan, yang tumbuh pada cabang tanaman. Bentuk bunga
radial dan strukturnya bersusun lima. Buahnya merupakan buah berair, panjangnya
mendekati 10 cm, dan tersusun dari lima sisi dan bentuknya menyerupai bintang jika
diiris secara melintang. Jika masak akan berwarna kuning tua (Heber, 2007).
B. Flavonoid
O
OH OH
HO
OH OH
Gambar 1. Struktur katekin
(Strobel, Allard, Perez-Acle, Calderon, Aldunate, dan Leighton, 2005) Flavonoid adalah grup komponen polifenol yang terdapat di dalam buah dan
sayuran. Familinya terbagi menjadi monomerik flavanol, flavanon, antosianindin,
flavon, dan flavonol (Watson, 2001). Lebih dari 4000 flavonoid telah teridentifikasi
di dalam berbagai buah, sayuran, dan minuman. Flavonoid menjadi menarik
akhir-akhir ini karena berbagai potensi efeknya yang menguntungkan bagi kesehatan
manusia. Flavonoid telah dilaporkan memiliki aktivitas antiviral, anti alergi,
Flavonoid dikenal sebagai kelator transisi logam; sebagian besar uji inhibisi
lipid peroksidasi mengukur kombinasi aktivitas pengkelat transisi logam (biasanya
besi) dan penangkapan radikal bebas. Flavonoid memiliki elemen struktur kimia yang
mungkin bertanggung jawab atas aktivitas antioksidan. Penelitian terkini oleh Dr.
Van Acker dan koleganya di Belanda menunjukkan bahwa flavonoid dapat
menggantikan vitamin E sebagai chain-breaking anti-oxidant di dalam membran
mikrosomal liver. Peran flavonoid sebagai antioksidan dalam sistem pertahanan
tubuh bisa didapatkan dengan komsumsi flavonoid 50-800 mg perhari. Kapasitas
flavonoid sebagai antioksidan bergantung pada struktur molekulnya. Posisi dari
gugus hidroksil dan rantai lain dalam stuktur kimia flavonoid penting untuk aktivitas
antioksidan dan penangkapan radikal bebas (Watson, 2001; Buhler and Miranda,
2000).
C. Peradangan 1. Pengertian peradangan
Peradangan merupakan suatu mekanisme respon pertahanan tubuh yang
fundamental, dirancang untuk membebaskan diri dari penyebab awal kerusakan pada
sel (misalnya mikrobia, racun) dan akibatnya (seperti nekrosis sel dan jaringan).
Tanpa peradangan, infeksi akan berlangsung tanpa terdeteksi, kerusakan tidak akan
sembuh, dan kerusakan jaringan mungkin akan bertahan sehingga sangat
2. Terjadinya radang
Inflamasi akut merupakan respon cepat tubuh dengan mengirim leukosit dan
protein plasma, seperti antibodi, menuju ke daerah infeksi atau kerusakan jaringan.
Inflamasi akut memiliki 3 komponen utama: (1) perubahan dalam kemampuan
vaskuler yang menyebabkan meningkatnya kecepatan alir darah, (2) perubahan
struktural dalam mikrovaskuler yang memungkinkan protein plasma dan leukosit dari
sirkulasi mikro, terakumulasi di daerah yang rusak, dan terkaktivasinya kedua
komponen tersebut berfungsi untuk mengeliminiasi agen penyebab kerusakan
(Kumar dkk., 2010).
Beberapa sel dan mediator-mediator terlibat dalam respon alami (merupakan
variasi sistem pertahanan tubuh) yang interaksinya sangat kompleks. Lebih detailnya
berhubungan dengan kejadian vaskuler dan peran sel serta mediator-mediator dalam
tubuh. Kejadian vaskuler merupakan awal dilatasi pada arteriola kecil yang
mengakibatkan peningkatan aliran darah, yang diikuti dengan penurunan kemudian
berhentinya aliran darah dan peningkatan permeabilitas vena pos kapiler, dengan
eksudasi cairan. Vasodilatasi disebabkan oleh adanya beberapa mediator (histamin,
prostaglandin (PG) E2 dan I2, dan sebagainya) yang dilepaskan karena adanya
interaksi antara jaringan dan mikroorganisme. Beberapa pelepasan dari mediator
tersebut (seperti histamin, platelet-activating factor (PAF) dan sitokin oleh interaksi
(TRL-PAMP) juga bertanggung jawab atas fase alami peningkatan permeabilitas
produksi beberapa mediator inflamasi, pada umumnya bradikinin, yang berhubungan
dengan kejadian seluler. Sel yang terkait dengan inflamasi, beberapa (sel endotelial
vaskuler, sel mast, dan makrofag jaringan) normalnya berada di jaringan ketika
platelet dan leukosit meningkatkan akses ke area inflamasi (Rang dkk., 2007).
Gambar 2. Diagram ringkas dari pembentukkan mediator inflamasi yang berasal dari fosfolipid dengan garis besar aksinya dan tempat aksi obat
antiinflamasi (Rang dkk., 2007).
Eicosanoid merupakan senyawa de novo dari fosfolipid. Eicosanoid yang
utama adalah asam arakidonat, yang terbentuk dari proses esterifikasi fosfolipid.
Eicosanoid berperan dalam pengontrolan berbagai proses fisiologis dan sebagian
Langkah awal dan batas kecepatan sintesis eicosanoid bergantung pada pembebasan
asam arakidonat, baik dengan satu tahap (dengan bantuan fosfolipase A2) maupun
dua tahap (dengan bantuan IP, inositol, fosfat, DAG, diasilgliserol). Tetapi,
fosfolipase A2 (PLA2) memiliki pengaruh yang besar dalam pembentukan asam
arakidonat intraseluler (gambar 2). Berbagai stimulan dapat membebaskan asam
arakidonat, tergantung pada tipe sel. Kerusakan sel umumnya juga memicu proses
pembebasan asam arakidonat.
Asam arakidonat dimetabolisme melalui beberapa cara (gambar 2), yaitu:
1. oleh enzim siklooksigenase (COX) yang terdiri dari dari dua bentuk, COX-1dan
COX-2. Enzim ini mengawali biosintesis prostaglandin dan tromboksan.
2. oleh lipoksigenase yang mengawali sintesis leukotrien, lipoksin dan komponen
lain (Rang dkk., 2007).
Radikal bebas oksigen akan terlepas secara ekstraseluler dari leukosit setelah
adanya pemaparan mikrobia, kemotaksin, dan kompleks imun, atau mengikuti
tantangan fagositik. Produksi radikal bebas oksigen bergantung pada aktivasi sistem
oksidasi NADPH. Anion superoksida, hidrogen peroksida (H2O2), dan radikal
hidroksil, merupakan spesies utama yang diproduksi oleh sel, dan anion superoksida
dapat berinteraksi dengan NO untuk membentuk spesies nitrogen reaktif (Kumar
dkk., 2010).
Seperti yang telah diketahui bahwa aktivasi fagosit melepaskan berbagai
penelitian oleh Babior pada tahun 1987, menunjukkan bahwa neutrofil yang
teraktivasi juga memproduksi radikal oksigen superoksida (O. ).Superoksida dapat
menghasilkan hidrogen peroksida dengan serangkaian reaksi (1):
2O. + 2H+→H2O2+ O2 (1)
Penelitian lebih lanjut menunjukkan bahwaO. dan H2O2juga dihasilkan pada
aktivasi sel fagosit lain, meliputi monosit, makrofag, dan eusinofil. H2O2 dapat
dengan mudah terpenetrasi ke membran sel, sedangkan O. tidak bisa. Kemudian
dengan adanya keberadaan ion dari transisi logam yang sesuai (biasanya besi), H2O2
dapat berinteraksi dengan reduksi ion besi sehingga membentuk spesies oksidasi
tinggi, yang paling penting adalah radikal hidroksil (.OH) yang menuju peroksidasi
lipid.
Fe2++ H2O2→ kompleks intermediet → Fe3++.OH + OH- (2)
Reaksi (2) dapat terjadi secara ekstraseluler jika medium di sekitar fagosit
yang teraktivasi mengandung ion besi. Derivat fagosit O. dimungkinkan berperan
dalam mengatur ion besi ke dalam bentuk reduksi:
Fe3++O. → kompleks intermediet → Fe2++ O2 (3)
Ion besi dihasilkan dari pendesakan hem pada hemoglobin oleh H2O2
kemudian O. akan mereduksi ferritin menjadi besi. Karena itulah pendarahan di
daerah inflamasi akan meningkatkan produksi radikal bebas dan memperparah
terpenetrasi ke dalam sel dan bereaksi dengan ion besi untuk membentuk .OH
(Halliwell, Hoult, and Blake, 1988).
3. Tanda-tanda peradangan
Peradangan akut adalah respon langsung dari tubuh terhadap cidera atau
kematian sel. Tanda-tanda pokok peradangan menurut Price dan Wilson (1995),
mencakup rubor (kemerahan), kalor (panas), tumor (pembengkakan), dolor (nyeri),
danfungsio laesa(perubahan fungsi).
a. Rubor
Rubor atau kemerahan, biasanya merupakan hal pertama yang terlihat di
daerah yang mengalami peradangan. Pada waktu reaksi peradangan mulai timbul,
maka arteriol yang mensuplai darah pada daerah tersebut melebar, dengan
demikian lebih banyak darah mengalir ke dalam mikrosirkulasi lokal.
Kapiler-kapiler yang sebelumnya kosong atau terisi sebagian saja, meregang dengan cepat
sehingga menjadi terisi penuh dengan darah. Keadaan tersebut dinamakan
hyperimia atau kongesti, menyebabkan warna merah lokal karena peradangan
akut. Timbulnya hyperemia pada permulaan reaksi peradangan diatur oleh tubuh
baik secara neurogenik maupun secara kimia, melalui pengeluaran zat seperti
histamin.
b. Kalor
Kalor atau panas, terjadi bersamaan dengan kemerahan dari reaksi
hanya terjadi pada permukaan tubuh, yang dalam keadaan normal lebih dingin
dari 37oC, yaitu suhu di dalam tubuh. Daerah peradangan pada kulit menjadi lebih
panas dari sekelilingnya, sebab darah (pada suhu 37oC) yang disalurkan tubuh ke
permukaan daerah yang mengalami peradangan, lebih banyak daripada yang
disalurkan ke daerah normal. Fenomena panas lokal ini tidak terlihat pada
daerah-daerah perdangan yang terjadi pada organ dalam, karena jaringan-jaringan
tersebut sudah mempunyai suhu 37oC, dan hyperemia lokal tidak menimbulkan
perubahan.
c. Tumor
Segi paling mencolok dari peradangan akut mungkin adalah
pembengkakan lokal. Pembengkakan ditimbulkan oleh adanya migrasi cairan dan
sel-sel dari sirkulasi darah ke jaringan-jaringan interstial. Campuran dari cairan
dan sel yang tertimbun di daerah peradangan disebut eksudat. Pada awal
peradangan, sebagian besar isi dari eksudat adalah cairan plasma, tetapi kemudian
sel-sel darah putih akan meninggalkan aliran darah kemudian tertimbun sebagai
bagian dari eksudat.
d. Dolor
Doloratau rasa sakit dari reaksi peradangan disebabkan oleh beberapa hal.
Perubahan pH lokal atau konsentrasi lokal ion-ion tertentu dapat merangsang
ujung-ujung nosiseptor. Hal yang sama, yaitu pengeluaran zat kimia tertentu
Selain itu, pembengkakan jaringan yang meradang mengakibatkan peningkatan
tekanan lokal yang tanpa diragukan lagi dapat menimbulkan rasa sakit.
e. Fungsio laesa
Fungsio laesa adalah salah satu reaksi peradangan yang terlihat mudah
untuk dimengerti, mengapa bagian yang bengkak terasa nyeri dan berfungsi
secara abnormal. Namun, sebetulnya tidak diketahui secara mendalam bagaimana
mekanisme terganggunya fungsi jaringan oleh adanya peradangan (Price dan
Wilson, 1995).
D. Nyeri 1. Pengertian nyeri
Nyeri merupakan pengalaman subyektif, yang sulit untuk dideskripsikan
secara pasti, meskipun kita semua tahu apa yang dimaksud dengan nyeri. Secara
khusus, nyeri merujuk pada sebuah respon yang ditujukan pada kejadian yang
berhubungan dengan kerusakan jaringan, seperti luka, inflamasi atau kanker, tetapi
nyeri yang hebat dapat muncul tersendiri oleh sebab yang tidak pasti (misal: neuralgia
trigeminal), atau tetap bertahan lama setelah sembuhnya luka. Nyeri juga dapat
muncul sebagai akibat dari adanya kerusakan otak atau saraf (misal: pasca stroke atau
infeksi herpes) (Rang dkk., 2007).
Macam-macam kondisi nyeri belakangan ini, tidak secara langsung
kecacatan dan stress; secara umum hal itu memiliki respon yang kurang baik terhadap
obat analgesik konvensional dibanding dengan menghilangkan penyebab langsung.
Pada kasus ini, kita perlu memikirkan itilah nyeri dalam konteks kelainan fungsi
saraf, dibandingkan pada schizophrenia atau epilepsi, lebih dari sekedar respon
normal terhadap luka pada jaringan. Namun demikian, diperlukan pembedaan dua
komponen, salah satu atau keduanya yang terlibat dalam keadaan nyeri patologis: (i)
saraf aferen nosiseptot perifer, yang teraktivasi oleh rangsang noksius; (ii)
mekanisme sentral oleh adanya input aferen yang menghasilkan sensasi nyeri (Rang
dkk., 2007).
2. Terjadinya nyeri
Menurut Raja dkk., 1999; Cesare & McNaughton, 1997; Julius & Basbaum,
2001 (cit., Rang dkk., 2007), pada kondisi normal, nyeri dihubungkan pada aktivitas
elektrik dalam diameter kecil pada serat utama aferen saraf perifer. Saraf ini memiliki
sensor ujung di jaringan perifer dan dapat teraktivasi oleh berbagai macam rangsang
(mekanik, termal, kimia).
Nyeri timbul jika rangsang mekanik, termal, kimia atau listrik melampaui
suatu nilai ambang tertentu (nilai ambang nyeri) dan karena itu menyebabkan
kerusakan jaringan dengan pembebasan zat nyeri (mediator nyeri). Yang termasuk
‘zat nyeri’ yang potensinya kecil adalah ion hidrogen. Pada penurunan nilai pH di
bawah 6 selalu terjadi nyeri yang meningkat pada kenaikan konsentrasi ion H+ lebih
kerusakan jaringan. Histamin pada konsentrasi relatif tinggi (10-8g/L) terbukti sebagai
zat nyeri. Asetilkolin pada konsentrasi rendah mensensibilisasi reseptor nyeri
terhadap zat nyeri lain, sehingga senyawa ini bersama-sama dengan senyawa yang
dalam konsentrasi yang sesuai secara sendiri tidak berkhasiat, dapat menimbulkan
nyeri. Pada konsentrasi tinggi, asetilkolin bekerja sebagai zat nyeri yang berdiri
sendiri. Serotonin merupakan senyawa yang menimbulkan nyeri yang paling efektif
dari kelompok transmitter. Sebagai kelompok senyawa penting lain dalam hubungan
ini adalah kinin, khususnya bradikinin, yang termasuk senyawa penyebab nyeri
terkuat. Prostaglandin, yang dibentuk lebih banyak dalam peristiwa nyeri,
mensensibilisasi reseptor nyeri dan di samping itu menjadi penentu dalam nyeri yang
lama (Mutschler, 1986). Selain prostaglandin, ada juga substantsi P yang bekerja
meningkatkan sensitivitas ujung-ujung serabut saraf nyeri tetapi tidak secara langung
merangsangnya (Guyton, 1986). Pembentukan prostaglandin dapat dilihat pada
gambar 2.
Reseptor rasa nyeri yang terdapat di kulit dan jaringan lain semuanya
merupakan ujung saraf bebas. Reseptor ini tersebar luas pada permukaan superfisial
kulit dan juga di jaringan dalam tertentu, misalnya poriosteum, dinding arteri,
permukaan sendi, dan falks serta tentorium tempurung kepala. Rasa nyeri dapat
dirasakan melalui berbagai jenis rangsangan (Guyton, 1986).
Penghantaran nyeri dimulai dari adanya potensial aksi (impuls nosiseptif)
dorsal sumsum tulang belakang. Pada tempat kontak awal ini bertemu tidak hanya
serabut aferen, yang impulsnya tumpang tindih, tetapi di sini juga terjadi refleks
somatik dan vegetatif awal (misalnya menarik tangan pada waktu tangan tersentuh
benda panas, terbentuknya eritema lokal) melalui interneuron. Disamping itu pada
tempat ini juga terjadi pengaruh terhadap serabut aferen melaui sistem penghambatan
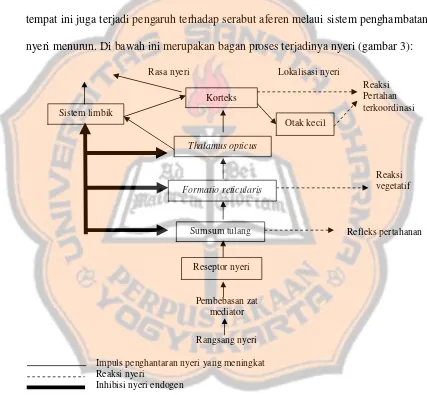
nyeri menurun. Di bawah ini merupakan bagan proses terjadinya nyeri (gambar 3):
Rasa nyeri Lokalisasi nyeri
Reaksi
Impuls penghantaran nyeri yang meningkat Reaksi nyeri
Inhibisi nyeri endogen
Gambar 3.Terjadinya nyeri; penghantaran impuls; lokalisasi dan rasa nyeri serta inhibisi nyeri endogen dalam bagan sederhana
3. Jenis nyeri a. Nyeri somatik
Nyeri somatik dibagi menjadi nyeri permukaan dan nyeri dalam:
1) Nyeri permukaan
Disebut nyeri permukaan apabila rangsang bertempat dalam kulit.
Mempunyai karakter ringan, dapat dilokalisasi dengan baik dan hilang
cepat setelah berakhirnya rangsang.
2) Nyeri dalam
Disebut nyeri dalam apabila rasa nyeri berasal dari kulit, otot,
persendian, tulang atau dari jaringan ikat. Nyeri dalam juga dirasakan
sebagai tekanan, sukar dilokalisasi dan kebanyakan menyebar ke
sekitarnya. Nyeri dalam seringkali diikuti oleh reaksi vegetatif seperti
tidak bergairah, mual, berkeringat, dan penurunan tekanan darah.
b. Nyeri viseral (dalaman)
Nyeri ini disebut juga nyeri perut karena sifat menekannya dan reaksi
vegetatif yang menyertainya. Nyeri ini terjadi antara lain pada tegangan organ
perut, kejang otot polos, aliran darah kurang dan penyakit yang disertai
E. Antiinflamasi
Obat-obat AINS merupakan obat modern yang paling luas penggunaannya.
Obat AINS meliputi berbagai kelas terapi yang berbeda. Sebagian besar obat-obat
tersebut memiliki tiga efek, yaitu:
1. efek antiinflamasi: memodifikasi reaksi inflamasi
2. efek analgesik: mengurangi nyeri berat jangka pendek
3. efek antipiretik: menurunkan kenaikan temperatur
Secara umum, berbagai efek tersebut berhubungan dengan aksi primer dari obat,
yaitu menghambat siklooksigenase arakidonat sehingga produksi prostaglandin dan
tromboksan juga terhambat. Meskipun demikian masing-masing obat memiliki
mekanisme aksi yang berbeda-beda (Rang dkk., 2007).
Aksi utama dari AINS adalah menghambat metabolisme asam arakidonat oleh
COX, seperti yang dikemukanan oleh Vine pada 1971. Baik inhibitorCOX-1maupun
COX-2 hanya menghambat reaksi utama siklooksigenase. Penghambatan COX-1
bersifat instan dan reversibel, sedangkan penghambatanCOX-2 time dependent, efek
meningkat seiring dengan bertambahnya waktu. AINS juga memiliki aksi lain selain
penghambatan COX, yaitu menghambat radikal oksigen reaktif, yang dimungkinkan
berperan dalam aktivitasnya sebagai antiinflamasi. Radikal oksigen reaktif yang
diproduksi oleh neutrofil dan makrofag, pada beberapa kondisi mengakibatkan
kerusakan jaringan, dan AINS yang mempunyai aktivitas penghambatan radikal
penghambatan COX (misalnya sulindac), dalam mengurangi kerusakan jaringan
(Rang dkk., 2007).
Obat antiinflamasi dapat mempengaruhi kerusakan oksidan dengan berbagai
cara, yaitu: (1) menghambat langsung oksidan reaktif seperti radikal hidroksil (.OH)
dan asam hipoklorid (HOCl), (2) menghambat produksi oksidan (O.) oleh neutrofil,
monosit, dan makrofag sehingga mengurangi pembentukan H2O2yang mengakibatka
.
OH ikut terhambat (Halliwell dkk., 1988).
Obat AINS juga efektif melawan nyeri yang berhubungan dengan inflamasi
atau kerusakan jaringan karena dapat mengurangi produksi prostaglandin yang
berfungsi mensensitisasi nosiseptor inflamasi seperti bradikinin (Rang dkk., 2007).
F. Diklofenak
CH2CO2H Cl
Cl
Gambar 4. Struktur diklofenak (Dollery, 1999)
Diklofenak merupakan derivat asam fenilasetat yang menyerupai flurbiprofen
dan meclofenamate. Obat ini (gambar 4) adalah penghambat siklooksigenase yang
relatif nonselektif dan kuat, juga mengurangi bioavailabitas asam arakidonat. Obat ini
memiliki sifat-sifat antiiflamasi, analgesik, dan antipiretik yang biasa. Obat-obat itu
antara 30-70% karena metabolisme lintas pertama. Obat ini memiliki waktu-paruh
1-2 jam. Seperti flurbiprofen, ia menumpuk di dalam cairan sinovial, dengan
waktu-paruh 2-6 jam dalam kompartemen ini. Metabolisme berlangsung dengan CYP3A4
dan CYP2C9 menjadi metabolit tidak aktif. Klirens empedu bisa mencapai 30% dari
klirens total (Shearn, 2002).
Diklofenak merupakan obat AINS yang poten. Diklofenak menghambat
aktivitas siklooksigenase sehingga produksi prostaglandin di jaringan berkurang.
Diklofenak digunakan secara luas untuk pengobatan rheumatoid arthritis dan
ostheoarthritis. Pada mencit, kadar diklofenak tertinggi ditemukan pada hati,
empedu, dan ginjal (Dollery, 1999).
G. Analgetika
Analgetika adalah senyawa yang dalam dosis terapeutik meringankan atau
menekan rasa nyeri, tanpa memiliki kerja anestesi umum. Berdasarkan potensi kerja,
mekanisme kerja dan efek samping, analgetika dibedakan dalam dua kelompok,
yaitu: analgetika yang berkhasiat kuat, bekerja pada pusat (hipoanalgetika,
‘Kelompok Opiat’) dan analgetika yang berkhasiat lemah (sampai sedang), bekerja
terutama pada perifer dengan sifat antipiretika dan kebanyakan juga mempunyai sifat
antiinflamasi dan antireumatik. Berikut ini merupakan kemungkinan-kemungkinan
1. mencegah sensibilasi reseptor nyeri dengan cara penghambatan sintesis
prostagladin dengan analgetika yang bekerja di perifer,
2. mencegah pembentukan rangsang dalam reseptor nyeri dengan memakai
anestetika permukaan atau anestetika infiltrasi,
3. menghambat penerusan rangsang dalam serabut sensorik dengan anestetika
konduksi,
4. meringankan nyeri atau meniadakan nyeri melalui kerja dalam sistem saraf pusat
dengan analgetika yang bekerja pada pusat atau obat narkosis,
5. mempengaruhi pengalaman nyeri dengan psikofarmaka (trankuilansia,
neuroleptika, antidepresiva) (Mutschler, 1986).
Psikofarmaka Anestetika,
Analgetika yang bekerja sentral
Saraf Anestetika konduksi
Reseptor nyeri Anestetika permukaan
Analgesik yang bekerja perifer Gambar 5. Bagan kemungkinan pengaruh macam-macam obat terhadap nyeri
(menurut Keldel) (Mutschler, 1986).
Otak
H. Parasetamol
NHCOCH3
HO
Gambar 6. Struktur parasetamol (Anonim, 1995)
Parasetamol memiliki pemerian berupa serbuk hablur berwarna putih, tidak
berbau dan berasa sedikit pahit. Parasetamol larut dalam air mendidih, dalam natrium
hidroksida 1 N, dan mudah larut dalam etanol (Anonim, 1995).
Asetaminofen atau parasetamol adalah metabolit aktif dari fenasetin yang
bertanggung jawab akan efek analgesiknya. Parasetamol diberikan secara oral dan
penyerapannya dipengaruhi oleh tingkat pengosongan perut (Shearn, 2002).
Parasetamol tidak memiliki efek antiinflamasi yang signifikan, tetapi
digunakan secara luas sebagai analgesik ringan untuk nyeri yang tidak disertai
peradangan. Parasetamol diabsorbsi dengan baik secara peroral dan tidak
menyebabkan iritasi lambung (Neal, 1997).
Mekanisme kerja parasetamol sebagai analgseik yaitu menghambat sintesis
prostaglandin. Keunggulan parasetamol yaitu memiliki selektivitas jaringan yang
lebih tinggi dibanding aspirin dan AINS, namun penyebabnya belum diketahui
I. Metode Pengujian Daya Antiinflamasi
Efek antiinflamasi dapat diukur dengan menggunakan carain vitromaupunin
vivo. Secara umum, metode pengujian obat antiinflamasi terbagi menurut lama
terjadinya edema yaitu inflamasi akut, subakut, dan kronik. Beberapa metode yang
dapat digunakan untuk mengukur daya antiinflamasi adalah sebagai berikut:
1. Metodein vitro
Metode ini digunakan untuk mengetahui peran dan pengaruh
substansi-substansi fisiologis yang terlibat dalam proses inflamasi. Substansi-substansi-substansi
tersebut antara lain: histamin, serotonin, bradikinin, substansi P, dan lain-lain.
Beberapa contoh percobaan in vitro adalah: pengikatan reseptor 3H-Bradikinin,
substansi P dan golongan takikinin, karakterisasi agonis dan antagonis
neurokinin, pengukuran kemotaksis leukosit polimorfonuklear (Vogel, 2002).
2. Metodein vivo
a. Uji permeabilitas vaskuler
Uji ini digunakan untuk mengevaluasi aktivitas penghambatan obat
melawan peningkatan permeabilitas vaskuler yang diinduksi oleh subtansi
flogistik. Mediator-mediator inflamasi dilepaskan setelah sel mast
terstimulasi. Kejadian tersebut memicu dilatasi arteriola dan vena serta
peningkatan permeabilitas vaskuler, sehingga terjadi edema. Obat yang dapat
menstabilkan membran dapat mengurangi permeabilitas kapiler. Permeabilitas
intrakutan. Kenaikan permeabilitas dapat diamati dengan menginjeksikan
pewarnaEvan’s bluepada kulit yang diinduksi (Vogel, 2002).
b. Uji granuloma
Hewan uji yang berupa tikus putih betina galur Wistar diinjeksi
dengan 10-25 mL udara secara subkutan pada bagian punggungnya, kemudian
0,50 mL minyak Croton dan karagenin sebagai iritan ditambahkan untuk
mencegah udara keluar. Obat yang akan diuji mulai diberikan setiap hari
secara peroral setelah pembentukan kantong edema. Pada hari kedua setelah
pembentukan kantung edema, udara dikeluarkan. Untuk uji aktivitas lokal,
obat yang diuji diinjeksikan pada kantong udara pada saat bersamaan dengan
iritan. Pada hari keempat, kantung dibuka dan cairan eksudat disedot,
selanjutnya diukur volume cairannya. Uji ini lebih responsif untuk uji obat
antiinflamasi steroid daripada nonsteroid (Vogel, 2002). Persen inhibisi
granuloma dihitung dengan membandingkan volume cairan eksudat kelompok
perlakuan dengan kelompok kontrol (Khanna dan Sharma, 2001).
c. Edema pada kaki
Prinsip utama dalam metode edema pada kaki ini berdasarkan pada
kemampuan senyawa uji dalam menghambat peradangan pada kaki hewan uji
yang telah diinjeksi dengan agen flogistik. Tikus jantan dengan berat badan
antara 100-150 g dipuasakan semalam, dan untuk menghindari dehidrasi,
tikus diinjeksi dengan 0,05 ml larutan karagenin 1% secara subkutan pada
telapak kaki kirinya. Besar edema diukur sesaat setelah injeksi, dan pada jam
ke 3, 6 dan 24 jam setelah injeksi.
d. Uji eritema UV
Hewan uji marmot, 16 jam sebelum perlakuan dicukur pada bagian
punggungnya, kemudian diolesi barium sulfida. Dua puluh menit kemudian
dibersihkan dengan air hangat. Pada hari berikutnya, zat uji mulai diberikan
secara peroral (10 mL/kg), 30 menit sebelum pemaparan UV. Setelah
dilakukan pemaparan UV selama 30 menit, dilakukan pengamatan terjadinya
eritema. Kelemahan metode ini adalah subyektivitas dalam menghitung
jumlah eritema, administrasi zat uji kortikosteroid secara sistemik kurang
efektif dibandingkan secara topikal, dan uji ini tidak dapat digunakan untuk
mengukur durasi efek antiinflamasi (Vogel, 2002).
J. Metode Pengujian Daya Analgetika
Metode-metode pengujian aktivitas analgetika dilakukan dengan menilai
kemampuan zat uji untuk menekan atau menghilangkan rasa nyeri yang diinduksi
pada hewan percobaan (mencit, tikus, marmot), yang meliputi induksi secara
mekanik, termik, elektrik dan secara kimia. Pada umumnya daya kerja analgetika
harus diberikan sampai ada respon nyeri atau jangka waktu ketahanan hewan
terhadap stimulus nyeri atau juga peranan frekuensi respon nyeri (Anonim, 1991).
Pengujian daya analgesik dapat menggunakan berbagi metode. Metode
pengujian daya analgesik berdasarkan pada jenis analgesik yang terbagi menjadi dua
golongan, yaitu golongan analgesik narkotika dan analgesik non narkotika. Pengujian
daya analgesik menurut Turner (1965) tersebut, yaitu:
1. Golongan analgesik narkotika
a. metode jepit ekor
Sekelompok tikus diinjeksi dengan senyawa uji pada dosis tertentu
secara subkutan atau intravena. Tiga puluh menit kemudian, jepit dipasang
pada pangkal ekor mencit yang dilapisi karet tipis selama 30 detik. Tikus yang
tidak diberi analgesik akan berusaha terus untuk melepaskan diri dari
kekangan tersebut dengan cara menggigit jepitan, tetapi tikus yang diberi
analgesik akan mengabaikan kekangan tersebut (karena rasa sakit tidak begitu
dirasakannya). Respon positif adanya daya analgesik dapat dicatat jika tidak
ada usaha dari tikus untuk melepaskan diri dari jepitan (selama 15 detik).
Metode ini lebih baik daripada uji dengan menggunakan lempeng panas,
karena rangsang yang diberikan tidak bersifat merusak (pada lempeng panas,
b. metode rangsang panas
Sebagian besar uji respon dari rangsang panas dilakukan dengan
penempatan hewan uji di atas permukaan panas atau pencelupan ekor hewan
uji ke dalam air panas. Metode lempeng panas menggunakan hewan uji
mencit yang sudah diberi larutan uji secara subkutan atau peroral, yang
dijatuhkan perlahan-lahan ke atas lempeng panas yang terdiri dari silinder
penahan. Kisaran suhu lempeng panas berkisar antara 50oC sampai 55oC,
dilengkapi dengan penangas tembaga yang berisi campuran yang sebanding
dengan campuran aseton dan etil format yang mendidih.
Waktu reaksi diambil sebagai perpanjangan jarak waktu dari saat
mencit menyentuh lempeng panas sampai ketika mencit menjilati kaki
belakangnya atau melompat-lompat keluar dari silinder. Semua tanda
kegelisahan lain seperti menendang-nendang atau berputar-putar selanjutnya
diabaikan. Metode ini hanya berguna untuk mendeteksi analgesik golongan
narkotika dan tidak sesuai untuk menguji analgesik golongan non-narkotik.
c. metode pengukuran tekanan
Alat yang digunakan dalam metode ini adalah sebuah alat untuk
mengukur tekanan yang diberikan pada tikus secara seragam. Alat tersebut
terdiri dari duasyringeyang dihubungkan antar ujung-ujungnya yang rata-rata
bersifat elastis, fleksibel, dan terdapat pipa plastik yang diisi dengan sebuah
diletakkan pada posisi vertikal dengan ujung menghadap ke atas. Ekor tikus
diletakkan di bawah penghisap syringe. Ketika tekanan diberikan pada
penghisap dari syringe yang kedua, tekanan ini akan berhubungan dengan
sistem hidrolik pada syringeyang pertama lalu dengan ekor tkus. Penurunan
tekanan yang sama pada syringe yang kedua selanjutnya akan meningkatkan
tekanan pada ekor tikus. Manometer dibaca ketika tikus memberikan respon
yaitu respon tikus yang pertama yaitu meronta-ronta kemudian akan
mengeluarkan suara (mencicit) tanda kesakitan.
d. metode potensi petidin
Metode ini tidak selalu sesuai untuk uji penapisan analgesik karena
membutuhkan jumlah hewan uji yang relatif banyak, akan tetapi metode ini
dapat digunakan untuk memperluas hasil dari uji penapisan. Semua substansi
yang diperkirakan memiliki aktivitas analgesik maupun sedatif dapat diuji
dengan metode ini. Tiap kelompok mencit yang terdiri dari 20 ekor mencit,
setengah kelompok dibagi menjadi 3 bagian dan diberikan petidin dengan
dosis 2, 4, dan 8 mg/kg BB. Setengah yang lain diberi petidin dengan senyawa
uji dengan dosis 25% dari LD50. Persen analgesik dihitung dengan bantuan
metode rangsang panas.
e. metode antagonis nalorfin
Uji analgesik dengan metode ini dibuat untuk menunjukan aksi dari
sebagian besar aksi morfin. Hewan uji yang biasa digunakan dalam metode ini
adalah mencit, tikus, dan anjing. Hewan uji diberi obat dengan dosis toksik
(pirinitramida) kemudian segera diikuti dengan pemberian morfin (5-10
mg/kg BB) secara intravena. Efek toksik dapat dilawan dalam waktu satu
menit dengan pemberian injeksi nalorfin 1,25 mg/kg BB secara intravena.
Berdasarkan teori, nalorfin dapat menggeser ikatan morfin dengan
reseptornya sehingga akan meniadakan efek dari morfin. Nalorfin pada dosis
5 mg/kg mampu membalikkan 10 mg/kg morfin. Pada kenyataannya, seluruh
obat yang berpotensi sebagai analgesik narkotik dapat dilawan dengan
nalorfin.
f. metode kejang oksitosin
Oksitosin merupakan hormon yang dihasilkan oleh kelenjar pituitari
posterior yang dapat menyebabkan kontraksi uterin, sehingga menimbulkan
kejang pada tikus. Respon kejang meliputi kontraksi abdominal, peregangan
tubuh dan tungkai serta lengan bagian belakang, dan puntiran badan pada
pinggang dengan putaran kaki belakang ke arah dalam. Respon ini dapat
dicegah dengan terlebih dahulu diberikan morfin dan senyawa uji, sehingga
ED 50 lebih kecil daripada yang dihasilkan dari prosedur yang menggunakan
panas pancaran. Selain, morfin senyawa analgesik yang bisa diuji dengan
metode ini adalah heroin, metadon, kodein, dan meperidina. Uji ini kemudian
g. metode pencelupan pada air panas
Pada metode ini tikus disuntik secara intraperitoneal dengan senyawa
uji, kemudian ekor tikus dicelupkan ke dalam air panas (suhu 58oC). Respon
tikus terlihat dari hentakan ekornya yang menghindari air panas. Munculnya
reaksi yang khas yaitu sentakan ekor yang keras, dicatat waktunya. Uji ini
diulang kembali setiap 30 menit setelah menit ke 15 penyuntikan. Jika mencit
tetap tidak beraksi dalam waktu 6 detik, mencit diangkat dari penangas.
2. Golongan analgesik non narkotika
a. metode geliat
Dalam variasi lain metode geliat menurut Witkin dkk., 1961 (cit.,
Turner, 1965), mencit jantan dengan berat badan 18-22 g, diberi rangsang
secara intraperitoneal dengan injeksi 300 mg/kg larutan asam asetat 3%.
Senyawa yang diuji diberikan secara peroral kepada 6 mencit, 15 menit
sebelum pemberian asam asetat. Setiap hewan uji kemudian ditempatkan pada
kotak kaca dan diamati jumlah geliat yang terjadi selama waktu pengamatan
20 menit. Kelompok kontrol diberi larutan salin. Untuk hasil yang akurat, 5
hewan uji dalam satu kelompok digunakan untuk tiap titik dalam kurva
peringkat dosis vs respon. Dua puluh lima menit setelah pemberian asam
Daya analgesik dihitung dengan persamaan menurut Handershot dan
Forsaith (1959) sebagai berikut:
% daya analgesik= 100-(P/K x 100%)
Keterangan:
P: jumlah geliat mencit pada kelompok perlakuan K: rata-rata jumlah geliat mencit pada kelompok kontrol
b. meotode rektodolorimetri
Pada metode ini tikus diletakkan dalam sebuah kandang yang dibuat
khusus dengan alas tembaga yang dihubungkan dengan sebuah penginduksi
yang berupa gulungan. Ujung lain dari gulungan tersebut kemudian
dihubungkan dengan silinder elektroda tembaga. Ujung yang lainnya lagi
dihubungkan pada ekor hewan uji. Sebuah amperemeter yang peka terhadap
adanya perubahan tengangan sebesar 0,1 volt selanjutnya dihubungkan
dengan konduktor yang berada di gulungan bagian atas. Tegangan yang sering
digunakan untuk menimbulkan terikan tikus adalah 1-2 volt.
c. metode podolorimeter
Metode ini menggunanakan aliran listrik untuk mengukur besarnya
daya analgesik. Alas kandang mencit yang terbuat dari kepingan metal yang
dapat mengalirkan listrik. Seekor mencit diletakkan pada kandang tersebut
yang kemudian dialiri listrik. Respon yang terjadi ditandai dengan teriakan
K. Landasan Teori
Neutrofil dan makrofag jika terlepas dari endotelium, maka akan segera
bermigrasi ke daerah kemotaksin. Di sana neutrofil dan makrofag akan memproduksi
eicosanoid, enzim proteolitik, radikal oksigen superoksida dan H2O2. H2O2 lebih
lanjut dapat berinteraksi dengan ion besi (Fe2+), menghasilkan radikal hidroksil (.OH)
yang reaktif sekali menuju peroksidasi lipid (Halliwell dkk., 1988). .OH dapat
menyerang asam arakidonat sehingga terbentuk senyawa baru yang kemudian dapat
diserang oleh O. , sehingga terbentuklah prostaglandin yang menyebabkan
peradangan (Fessenden dan Fessenden, 1982). Selain menyebabkan peradangan,
prostaglandin yang terlepas dapat mensensitisasi reseptor nyeri (nosiseptor) sehingga
akan timbul rasa nyeri.
Pendekatan dari penelitian ini adalah adanya kandungan antioksidan dalam
buah belimbing, yaitu katekin (Sukadana, 2009) pada buah belimbing mampu
menangkap radikal O. dan.OH, sehingga kedua radikal tersebut tidak menyerang
asam arakidonat. Dengan begitu maka pembentukkan prostaglandin menjadi
terhambat
Terhambatnya prostagladin membuat peradangan dapat diatasi. Rasa nyeri
yang merupakan manifestasi klinis dari peradangan juga akan berkurang. Hal itulah
yang mendasari dugaan sementara bahwa jus buah belimbing dapat berkhasiat
Untuk menguji efek antiinflamasi digunakan metode edema pada kaki, karena
metode ini telah digunakan oleh banyak peneliti dan telah terbukti cocok untuk
skrining sebaik untuk evaluasi mendalam (Vogel, 2002). Sedang untuk menguji ada
tidaknya efek analgesik, dalam penelitian ini digunakan metode geliat. Metode ini
digunakan karena sensitif, sederhana, dan repsodusibel untuk skrining analgesik
lemah (Turner, 1965). Selain itu, metode ini dapat mendeteksi baik analgesik sentral
maupun perifer. Metode ini telah digunakan oleh banyak peneliti dan bisa
dierkomendasikan sebagai metode skrining yang sederhana (Vogel, 2002).
L. Hipotesis
Jus buah belimbing (Averrrhoa carambola L.) memiliki efek antiinflamasi
39 BAB III
METODE PENELITIAN A. Jenis dan Rancangan Penelitian
Jenis penelitian uji efek analgesik dan antiinflamasi jus buah belimbing ini
termasuk jenis penelitian eksperimental murni dengan rancangan acak lengkap pola
searah.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel utama
Variabel utama dalam penelitian ini yaitu:
a. Variabel bebas
Variabel bebas dalam penelitian ini adalah dosis jus buah belimbing.
b. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah besar edema pada kaki
hewan uji dan jumlah geliat yang dihasilkan setelah perlakuan dengan jus
buah belimbing.
2. Variabel Pengacau
a. Variabel pengacau terkendali
Pada penelitian ini terdapat variabel pengacau yang harus
dikendalikan, yaitu: hewan uji mencit putih betina galur Swiss, umur 2-3
bulan, berat badan 20-30 gram, kondisi subyek uji sehat, asal buah belimbing
seperti yang terurai pada pengumpulan bahan, jalur pemberian jus dilakukan
secara peroral, jalur pemberian rangsang nyeri secara intraperitoneal, jalur
pemberian rangsang inflamasi secara subplantar.
b. Variabel pengacau tidak terkendali
Pada penelitian ini, variabel pengacau yang tidak dapat dikendalikan
adalah keadaan patologis dari mencit, kemampuan tubuh mencit untuk
mengabsorbsi jus buah belimbing, dan kemampuan mencit untuk beradaptasi
dengan peradangan maupun rasa nyeri.
3. Definisi Operasional
a. Jus buah belimbing adalah jus dengan konsentrasi 20% yang diperoleh dengan
cara mencampurkan 50 ml aquadest dan 10 gram buah belimbing segar yang
dipotong melintang dengan ketebalan ± 1 cm kemudian dijus dengan
menggunakan blender merk Philips.
b. Uji daya antiinflamasi adalah uji dengan menggunakan mencit galur Swiss
sebagai hewan uji yang dibuat radang telapak kaki kirinya, sedangkan telapak
kaki kanan hanya ditusuk dengan jarum injeksi. Pengukuran diameter kedua
kaki belakang mencit dilakukan dengan menggunakan jangka sorong (Digital
Caliper Mitutoyo), kemudian dibandingkan dengan perlakuan peroral jus buah
belimbing.
c. Uji daya analgesik adalah uji dengan menggunakan mencit galur Swiss
diamati jumlah geliat mencit dan dibandingkan dengan perlakuan peroral jus
buah belimbing.
d. Geliat didefinisikan sebagai sebuah perenggangan, tarikan ke satu sisi,
penarikan satu kaki belakang ke arah belakang, peregangan abdomen, dan
penarikan kepala dan kaki secara ekstrim ke arah belakang (opistotonus),
seingga dengan begitu bagian perut mencit menyentuh alas (Turner, 1965)
C. Bahan Penelitian Bahan yang digunakan dalam penelitian ini:
1. Untuk uji efek antiinflamasi
a. Buah belimbing (Averrhoa carambola L.) yang diperoleh dari supermarket
Superindo (Belimbing Bali) yang dibeli pada periode September 2009
-Februari 2010.
b. Larutan kalium diklofenak 3% sebagai kontrol positif
c. Larutan karagenin 1% sebagai zat penginduksi edema
d. Aquadest sebagai kontrol negatif
2. Untuk uji efek analgesik
a. Buah belimbing (Averrhoa carambola L.) yang diperoleh dari supermarket
Superindo (Belimbing Bali)
b. Suspensi parasetamol dalam CMC Na 1% sebagai kontrol positif uji
d. Larutan CMC Na 1%, sebagai kontrol negatif
D. Alat Penelitian
Alat yang digunakan dalam penelitian ini meliputi:
1. Neraca analitik (Mettler Toledo)
2. Spuit peroral dan injeksi 1 mL (Terumo)
3. Stopwatch
4. Alat-alat gelas: gelas beker, gelas ukur, pengaduk, pipet tetes
5. Jangka sorong (Digital Caliper) Mitutoyo 0-2 mm grad. 0,01 mm
6. Kotak kaca tempat pengamatan
7. Blender merk Phillips
E. Tata Cara Penelitian 1. Penelitian efek antiinflamasi a. Pengumpulan bahan penelitian
Bahan uji yang berupa buah belimbing yang diperoleh dari
supermarket Superindo (Belimbing Bali), dengan kriteria pemilihan
sebagai berikut: (1) berwarna kuning kecoklatan; (2) berdiameter tengah ±
5,5 cm; (3) memiliki panjang ± 14 cm; dan (4) memiliki berat ± 250 gram.
Bahan kimia yang digunakan, yaitu: Karagenin tipe I (Sigma
Farmakologi dan Toksikologi, Fakultas Farmasi, Universitas Sanata
Dharma Yogyakarta; NaCl 0,9% (Otsuka) dan tablet Cataflam D50
(Novartis Indonesia) yang mengandung kalium diklofenak 50 mg.
b. Pembuatan larutan kaium diklofenak 0,2%
Larutan diklofenak dibuat dengan cara menimbang dengan
seksama bahan yang setara dengan 200 mg serbuk diklofenak kemudian
dilarutkan dalam sedikit aquadest. Setelah itu, larutan dimasukkan ke
dalam labu ukur 100 mL, ditambah aquadest hingga tanda batas 100 mL,
kemudian digojog.
c. Pembuatan larutan karagenin 1%
Larutan karagenin 1% dibuat dengan cara menimbang dengan
seksama 0,10 gram serbuk karagenin kemudian dilarutkan dalam sedikit
aquadest. Setelah itu, larutan dimasukkan ke dalam labu ukur 10 mL,
ditambah aquadest hingga tanda batas 10 mL, kemudian digojog.
d. Seleksi hewan uji
Hewan uji yang digunakan adalah mencit putih betina galur Swiss,
yang berumur 2-3 bulan, dengan berat badan 20-30 gram. Semua hewan
uji sebelum diberi perlakuan, diadaptasikan terlebih dahulu selama satu
minggu dengan kondisi yang sama, yaitu dipelihara dengan kondisi dan
perlakuan yang sama meliputi kandang, pakan dan minum. Sehari
jam dengan cara tidak diberi makan, tetapi tetap diberikan minum. Hal
tersebut bertujuan untuk mengurangi variasi akibat adanya asupan
makanan.
e. Penetapan kriteria peradangan
Respon yang diamati pada uji efek antiinflamasi ini berupa besar
peradangan. Kriteria peradangan perlu ditetapkan untuk mendapatkan
keterulangan hasil. Peradangan pada kaki hewan uji diukur menggunakan
jangka sorong (Digital Caliper) Mitutoyo 0-2 mm grad. 0,01 mm; dengan
cara mengukur diameter peradangan pada telapak kaki hewan uji.
f. Penetapan rentang waktu pengukuran edema setelah injeksi subplantar karagenin 1%
Pada penetapan ini digunakan 12 ekor mencit betina, yang terbagi
dalam 4 kelompok. Masing-masing mencit diinjeksi dengan karagenin 1%
dengan dosis 25 mg/kg BB pada kaki belakang sebelah kiri secara
subplantar, sedangkan kaki belakang sebelah kanan hanya ditusuk
menggunakan jarum injeksi sebagai pembanding. Kemudian mencit
dikorbankan pada jam ke 1, 2, 3, dan 4 setelah injeksi karagenin 1%.
Berdasarkan hasil yang diperoleh akan dipilih rentang waktu yang
menghasilkan edema maksimal.
g. Penetapan dosis efektif diklofenak
Dosis kalium diklofenak dipilih berdasarkan penelitian yang