i
PENGARUH PEMBERIAN FRAKSI HEKSAN-ETANOL DARI EKSTRAK METANOL-AIR DAUN Macaranga tanarius L. JANGKA PANJANG 6 HARI TERHADAP AKTIVITAS ALKALINE PHOSPHATASE
PADA TIKUS BETINA GALUR WISTAR TERINDUKSI KARBON TETRAKLORIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh : Novita
NIM : 128114040
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
I praise You because I am fearfully and wonderfully made; Your works are wonderfull, I know that full well.
-Psalm 139:14
For Nothing will be Impossible with GOD
-Luke 1:37
Dengan penuh syukur,
Kupersembahkan karya kecil ini untuk :
Yesus Kristus dan Bunda Maria yang selalu memberikan kekuatan dan pertolongan saat aku terjatuh
Papa, Mama, Ricko dan Effen yang selalu memberikan doa dan dukungan dalam setiap langkahku
Orang tersayang dan sahabat-sahabatku yang selalu setia menemaniku Almamaterku tercinta
v
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini
tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini,
maka saya bersedia menanggung segala sanksi sesuai peraturan
perundang-undangan yang berlaku.
Yogyakarta, November 2013 Penulis
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH
UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma :
Nama : Novita
Nomor Mahasiswa : 128114040
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
PENGARUH PEMBERIAN FRAKSI HEKSAN-ETANOL DARI EKSTRAK METANOL-AIR DAUN Macaranga tanarius L. JANGKA PANJANG 6 HARI TERHADAP AKTIVITAS ALKALINE PHOSPHATASE
PADA TIKUS BETINA GALUR WISTAR TERINDUKSI KARBON TETRAKLORIDA
Beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalty kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 7 Desember 2015
Yang menyatakan,
vii
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa atas
berkat dan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi dengan judul
“Pengaruh Pemberian Fraksi Heksan-Etanol dari Ekstrak Metanol-Air Daun
Macaranga tanarius L. Jangka Panjang 6 hari Terhadap Aktivitas Alkaline Phospatase Pada Tikus Betina Galur Wistar Terinduksi Karbon Tetraklorida” ini dengan baik. Skripsi ini disusun untuk memenuhi salah satu syarat untuk
memperoleh gelar Sarjana Farmasi Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta.
Penyelesaian skripsi ini tentunya tidak lepas dari bantuan berbagai pihak,
baik secara langsung maupun secara tidak langsung. Oleh karena itu penulis hendak
mengucapkan terima kasih kepada :
1. Dekan Fakultas Farmasi Universitas Sanata Dharma yang telah mengijinkan
penulis menjalankan pembelajaran selama masa studi.
2. Ibu Phebe Hendra, M.Si., Ph.D., Apt., selaku Dosen Pembimbing Skripsi yang
telah membimbing, mendampingi, dan memotivasi selama penelitian dan
penyusunan skripsi.
3. Bapak Ipang Djunarko, M.Sc., Apt., selaku Dosen Penguji yang telah
memberikan kritik dan saran demi kemajuan skripsi ini.
4. Bapak Yohanes Dwiatmaka, M.Si., selaku Dosen Penguji yang telah
viii
5. Ibu Agustina Setiawati, M.Sc., Apt., selaku Kepala Penanggung jawab
Laboratorium Fakultas Farmasi Universitas Sanata Dharma yang memberikan
ijin dalam penggunaan fasilitas laboratorium untuk kepentingan penelitian ini.
6. Bapak Enade Perdana Istyastono, Ph.D., Apt., selaku Dosen Pembimbing
Akademik (DPA) yang telah memberikan bimbingan dan motivasi kepada
penulis selama masa perkuliahan di Fakultas Farmasi Universitas Sanata
Dharma.
7. Pak Heru, Pak Wagiran, Pak Parlan, Pak Kunto, dan Pak Bimo selaku laboran
laboratorium Fakultas Farmasi dan Pak Otok selaku pengelola gudang Farmasi
yang telah membantu penulis dalam proses pelaksanaan penelitian di
laboratorium.
8. Papa, Mama dan saudara-saudaraku Ricko dan Effen yang telah memberikan
doa, kasih sayang, motivasi, dan dukungan dari awal sampai akhir penelitian ini
sehingga penulis tetap bersemangat.
9. Sona Karisnata Inriano yang selalu memberikan dukungan, motivasi, perhatian
dan masukan dalam penelitian dan penyusunan skripsi.
10.Tim Macaranga atas segala kerjasama, bantuan, dan semangat dari awal
penelitian hingga penyusunan skripsi.
11.“Keluarga Gembira” Sona, Venny, Adis, Rei, Ella, Edward, dan Siti, sebagai
teman, sahabat sekaligus keluarga kecilku atas kebersamaan dan semangat yang
telah dibangun.
12.Teman-teman seperjuangan Cyndi, Maria, dan Rahayu yang telah berjuang
ix
13.Teman-teman main dan belajar Sina, Dhea, Lita, Edo, Dara yang telah menjadi
temen main dari awal semester dan awal penjurusan.
14.Teman-teman FSM-A dan FKK-A 2012, terima kasih atas kebersamaan,
keakraban, suka duka, semangat, dan kekeluargaan yang telah mengisi hari-hari
penulis.
15.Teman-teman angkatan 2012, terima kasih atas kebersamaan dan pengalaman
yang telah diberikan kepada penulis.
16.Semua pihak yang tidak dapat penulis sebutkan satu per satu sehingga penulis
dapat menyelesaikan skripsi ini dengan baik.
Penulis menyadari bahwa tugas akhir ini belum sempurna dan masih banyak
kekurangan sehingga penulis berharap kritik dan saran dari semua pihak demi
kemajuan di masa yang akan datang.
Akhir kata, penulis berharap semoga tugas akhir ini dapat bermanfaat bagi
semua pihak khususnya di bidang ilmu Farmasi.
Yogyakarta,
x
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ... vi
PRAKATA ... vii
DAFTAR ISI ... x
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvii
INTISARI ... xviii ABSTRACT ... xix BAB I. PENGANTAR ... 1 A. Latar Belakang ... 1 1. Rumusan masalah ... 5 2. Keaslian penelitian ... 5 3. Manfaat penelitian ... 6 B. Tujuan Penelitian ... 7 1. Tujuan umum ... 7 2. Tujuan khusus ... 7
xi
BAB II. PENELAAHAN PUSTAKA ... 8
A. Anatomi dan Fisiologi Hati ... 8
B. Hepatotoksisitas ... 11 C. Hepatotoksin ... 16 D. Karbon Tetraklorida ... 17 E. Alkaline Phospatase ... 20 F. Macaranga tanarius L. ... 22 1. Taksonomi ... 22 2. Nama lain ... 23 3. Morfologi ... 23 4. Kandungan ... 24
5. Khasiat dan kegunaan ... 26
6. Penyebaran ... 26
G. Metode Penyarian ... 27
H. Landasan Teori ... 28
I. Hipotesis ... 30
BAB III. METODE PENELITIAN ... 31
A. Jenis dan Rancangan Penelitian ... 31
B. Variabel Penelitian dan Definisi Operasional ... 31
1. Variabel utama ... 31
2. Variabel pengacau ... 31
3. Definisi operasional ... 32
xii
1. Bahan utama ... 33
2. Bahan kimia ... 33
D. Alat Penelitian ... 34
1. Alat pembuatan FHEMM ... 34
2. Alat perlakuan hewan uji ... 35
E. Tata Cara Penelitian ... 35
1. Determinasi tanaman Macaranga tanarius L. ... 35
2. Pengumpulan bahan uji ... 35
3. Pembuatan serbuk daun Macaranga tanarius L. ... 35
4. Penetepan kadar air serbuk daun Macaranga tanarius L. ... 36
5. Pembuatan ekstrak metanol-air daun Macaranga tanarius L. . ... 37
6. Pembuatan FHEMM ... 37
7. Pembuatan karbon tetraklorida dalam olive oil konsentrasi 50% .... 38
8. Pembuatan larutan CMC-Na 1% ... 38
9. Pembuatan suspensi FHEMM dalam CMC-Na 1% ... 38
10.Uji pendahuluan ... 38
11.Pengelompokan dan perlakuan hewan uji ... 39
12.Pengukuran aktivitas ALT dan AST serum pada orientasi ... 41
13.Pengukuran aktivitas ALP serum pada penelitian ... 41
F. Tata Cara Analisis Hasil ... 41
1. Uji pendahuluan ... 41
2. Perlakuan FHEMM ... 42
xiii
A. Penyiapan Bahan ... 43
1. Hasil determinasi tanaman Macaranga tanarius L. ... 43
2. Hasil penetapan kadar air serbuk daun Macaranga tanarius L. . ... 44
3. Hasil pembuatan FHEMM ... 44
B. Uji Pendahuluan ... 46
1. Penetapan dosis hepatotoksin karbon tetraklorida ... 46
2. Penetapan waktu pencuplikan darah ... 47
C. Efek Penghambatan Aktivitas Serum ALP FHEMM pada Tikus Betina Galur Wistar Terinduksi Karbon Tetraklorida ... 52
1. Kontrol negatif CMC-Na 1% ... 56
2. Kontrol hepatotoksin karbon tetraklorida ... 57
3. Kontrol FHEMM ... 58
4. Kelompok perlakuan FHEMM dosis 34,28; 68,57; dan 137,14 mg/kgBB ... 59
D. Rangkuman Pembahasan ... 65
BAB V. KESIMPULAN DAN SARAN ... 67
A. Kesimpulan ... 67
B. Saran ... 67
DAFTAR PUSTAKA ... 68
LAMPIRAN ... 73
xiv
DAFTAR TABEL
Tabel I. Purata aktivitas serum ALT pada selang waktu 0, 24, dan 48
jam setelah pemberian karbon tetraklorida dosis 2 mL/kg
BB ... 48
Tabel II. Hasil uji Tuckey HSD aktivitas serum ALT pada selang waktu
0, 24, dan 48 jam setelah pemberian karbon tetraklorida dosis
2 mL/kgBB ... 49
Tabel III. Purata aktivitas serum AST pada selang waktu 0, 24, dan 48
jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB ... 51
Tabel IV. Hasil uji Tuckey HSD aktivitas serum AST pada selang waktu
0, 24, dan 48 jam setelah pemberian karbon tetraklorida dosis
2 mL/kgBB ... 51
Tabel V. Purata aktivitas serum ALP dan % efek penghambatan akibat
praperlakuan FHEMM jangka panjang 6 hari dan pada
hari ke-7 diberikan karbon tetraklorida dosis 2 mL/kgBB ... 54
Tabel VI. Hasil uji Tuckey HSD aktivitas serum ALP akibat praperlakuan
FHEMM jangka panjang 6 hari dan pada hari ke-7
xv
DAFTAR GAMBAR
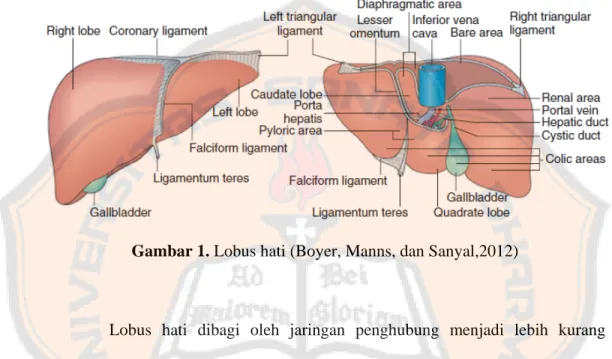
Gambar 1. Lobus hati ... 9
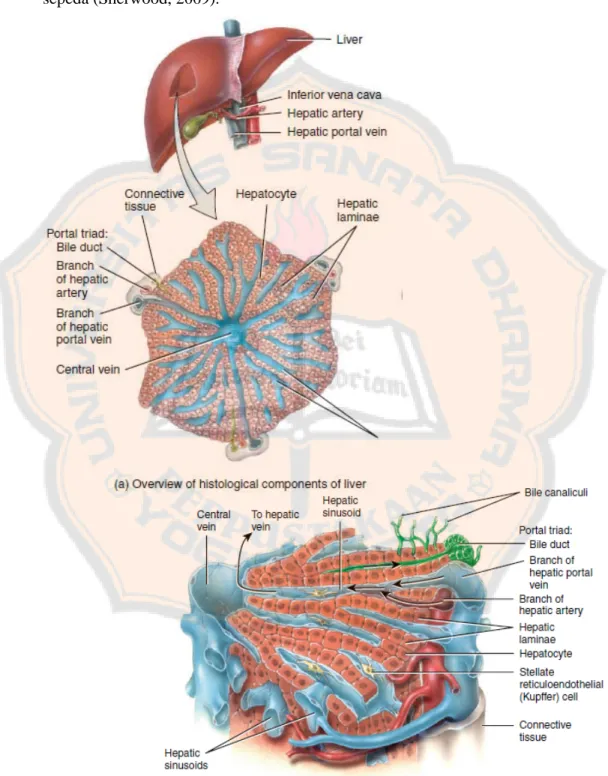
Gambar 2. Struktur mikroskopik hati ... 10
Gambar 3. Nekrosis hepatoselular, proses regenerasi ... 14
Gambar 4. Struktur molekul karbon tetraklorida ... 17
Gambar 5. Mekanisme biotransformasi dan oksidasi karbon tetraklorida ... 20
Gambar 6. Daun Macaranga tanarius L. ... 23
Gambar 7. Struktur kandungan senyawa daun Macaranga tanarius L.. ... 24
Gambar 8. Isolasi senyawa ellagitannins dari fraksi EtOAc daun Macaranga tanarius L.: mallotinic acid, corilagin, macatannin A, chebulagic acid, dan macatannin B ... 25
Gambar 9. Diagram batang purata aktivitas serum ALT pada selang waktu 0, 24, dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL /kgBB ... 48
Gambar 10. Diagram batang purata aktivitas serum AST pada selang waktu 0, 24, dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL /kgBB ... 51
xvi
FHEMM jangka panjang 6 hari dan pada hari ke-7
diberikan karbon tetraklorida dosis 2 mL/kgBB ... 54
Gambar 12. Daun Macaranga tanarius L. . ... 74
Gambar 13. Ekstrak metanol-air daun Macaranga tanarius L. . ... 74
Gambar 14. Fraksi heksan-etanol dari ekstrak metanol-air daun
Macaranga tanarius L. . ... 75
Gambar 15. Suspensi fraksi heksan-etanol dari ekstrak metanol-air daun
xvii
DAFTAR LAMPIRAN
Lampiran 1. Foto daun Macaranga tanarius L. ... 74
Lampiran 2. Foto ekstrak metanol-air daun Macaranga tanarius L... 74
Lampiran 3. Foto fraksi heksan-etanol dari ekstrak metanol-air daun Macaranga tanarius L. ... 75
Lampiran 4. Foto suspensi fraksi heksan-etanol dari ekstrak metanol-air daun Macaranga tanarius L. ... 75
Lampiran 5. Surat determinasi tanaman Macaranga tanarius L. ... 76
Lampiran 6. Surat ethical clearance penelitian ... 77
Lampiran 7. Surat lisensi program IBM SPSS Statistics 22 ... 78
Lampiran 8. Hasil Uji Statistik Orientasi Pencuplikan Darah ... 79
Lampiran 9. Hasil uji statistik aktivitas serum ALP setelah praperlakuan FHEMM pada dosis 34,28; 68,57; dan 137,14 mg/kgBB ... 87
Lampiran 10. Perhitungan persen efek penghambatan aktivitas ALP ... 93
Lampiran 11. Perhitungan konversi dosis ke manusia ... 94
Lampiran 12. Perhitungan konversi waktu tikus ke manusia ... 95
Lampiran 13. Perhitungan kadar air serbuk daun Macaranga tanarius L. .. 95
xviii
INTISARI
Penelitian ini bertujuan untuk menguji fraksi heksan-etanol dari ekstrak metanol-air daun Macaranga tanarius L. (FHEMM) sebagai agen hepatoprotektor dan membuktikan adanya pengaruh pemberian FHEMM jangka panjang 6 hari terhadap aktivitas alkaline phosphatase pada tikus betina galur Wistar terinduksi karbon tetraklorida serta mengetahui ada tidaknya kekerabatan antara dosis pemberian FHEMM dengan penurunan aktivitas alkaline phosphatase.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah. Sejumlah 30 ekor tikus dibagi secara acak dalam 6 kelompok perlakuan. Kelompok I sebagai kontrol hepatotoksin karbon tetraklorida. Kelompok II sebagai kontrol negatif diberikan CMC-Na 1%. Kelompok III sebagai kontrol perlakuan diberikan FHEMM dosis137,14mg/kgBB. Kelompok IV, V dan VI sebagai kelompok perlakuan diberikan FHEMM dosis 34,28; 68,57 dan 137,14 mg/kgBB selama 6 hari, pada hari ke-7 dilakukan pemejanan karbon tetraklorida dosis 2mL/kgBB lalu diambil darahnya 24 jam setelah pemejanan. Data aktivitas
alkaline phosphatase dianalisis secara statistik dengan taraf kepercayaan 95%, normalitas data dianalisis dengan uji Saphiro-Wilk, data yang terdistribusi normal dianalisis lebih lanjut menggunakan One-Way ANOVA dan uji Tuckey HSD. Pemberian FHEMM dosis 137,14 mg/kgBB dapat menurunkan aktivitas alkaline phosphatase secara signifikan. Tidak ada kekerabatan antara dosis pemberian FHEMM dengan penurunan aktivitas alkaline phosphatase.
Kata kunci : Macaranga tanarius L., Fraksi heksan-etanol ,Ekstrak metanol-air,
xix
ABSTRACT
The purpose of the research was to examine hexane-ethanol fraction from methanol-water extract of Macaranga tanarius L. leaves (FHEMM) as hepatoprotector agent, and to prove the effect of administration of FHEMM long-term 6 days on alkaline phosphatase activity in female Wistar rats induced by carbon tetrachloride, and to determine whether there was a relation between FHEMM doses with decreased activity of alkaline phosphatase.
This study was pure experimental research with randomized complete direct sampling design. A number of 30 rats were randomly divided into 6 groups. Group I as carbon tetrachloride hepatotoxins control. Group II as a negative control was given CMC-Na 1%. Group III as treatment control was given FHEMM dose 137.14mg/kgBW. Group IV, V and VI as the treatment group were given FHEMM at a dose 34.28; 68.57 and 137.14 mg/kgBW for 6 days, on the 7th day after the treatment, groups were given carbon tetrachloride dose 2mL/kgBW. After 24 hours, blood was taken. Alkaline phosphatase activity data were statistically analyzed with confidence limit 95%, the normality of data was analyzed using Saphiro-Wilk test. Normally distributed data was analyzed further using One-Way ANOVA and Tuckey HSD test. FHEMM administration dose 137.14 mg/kgBW influence alkaline phosphatase activity significantly. There was no relation between FHEMM doses and a decrease of alkaline phosphatase activity.
Keywords : Macaranga tanarius L., Hexane-ethanol fraction, Methanol-water extract, Alkaline phosphatase, Carbon tetrachloride
1
BAB I
PENGANTAR
A. Latar Belakang
Hati atau hepar merupakan organ terbesar di dalam tubuh yang memiliki peranan penting dalam kelangsungan hidup manusia. Hati memiliki peranan utama dalam proses metabolisme senyawa-senyawa penting yang masuk ke dalam tubuh seperti glukosa, asam amino, protein, dan lemak. Hati juga memiliki kemampuan untuk mendetoksifikasi senyawa-senyawa racun yang masuk ke dalam tubuh. Hati tersusun dari unit-unit kecil yaitu sel-sel hati (hepatosit) yang merupakan komponen penting dalam proses metabolisme (Corwin, 2007). Hepatosit mendapatkan suplai darah dari dua sumber yaitu sebagian kecil dari arteri hepatika yang kaya akan oksigen dan sebagian besar dari vena porta hepatika yang merupakan darah yang kaya akan nutrien, obat, dan toksin yang berasal dari saluran pencernaan (Tortora dan Derrickson, 2014). Hal ini menggambarkan bahwa sel-sel hati menerima suplai darah yang relatif kurang oksigen. Keadaan ini menyebabkan hepatosit rentan akan kerusakan dan penyakit. Salah satu kerusakan yang sering terjadi adalah perlemakan hati (steatosis).
Perlemakan hati merupakan suatu kondisi terjadinya penumpukan lemak berupa trigliserida di hati. Perlemakan hati dibagi menjadi dua, yaitu perlemakan hati yang disebabkan oleh alkohol dan perlemakan hati yang tidak disebabkan oleh alkohol atau biasa dikenal dengan Non-alcoholic Fatty Liver Disease (NAFLD).
NAFLD merupakan penyakit hati yang paling sering terjadi di masyarakat dan biasanya berdampingan dengan obesitas, disiplidemia, dan resistensi insulin.
Data epidemiologi menyatakan bahwa prevalensi NAFLD di Eropa dan Timur Tengah berkisar antara 20-30%, Amerika Latin 17-32%, Australia 20-30%, dan Afrika 9%. Untuk wilayah Asia, prevalensi NAFLD di Indonesia sebesar 30%, angka tersebut lebih tinggi dibandingkan sebagian besar negara lainnya yaitu Jepang (9-30%), China (5-24%), Korea Selatan (18%), India (5-28%), Malaysia (17%), dan Singapore (5%) (Loomba dan Sanyal, 2013). Prevalensi NAFLD di Indonesia berkaitan erat dengan prevalensi obesitas. Tren gaya hidup menjadi salah satu faktor utama dalam peningkatan prevalensi NAFLD (Amarapurkar dkk., 2007).
Karbon tetraklorida merupakan model hepatotoksin yang sering digunakan untuk menginduksi kerusakan sel hati tikus berupa steatosis di dalam suatu penelitian. Toksisitas karbon tetraklorida muncul ketika terjadi proses biotransformasi oleh sitokrom P4502E1 (CYP2E1) di hati. Karbon tetraklorida akan dimetabolisme oleh CYP2E1 menjadi radikal bebas triklorometil (CCl3•) dan jika bereaksi dengan oksigen akan membentuk radikal bebas triklorometil peroksi (CCl3O2•) (Panjaitan dkk., 2007). Radikal bebas triklorometil (CCl3•) dan triklorometil peroksi (CCl3O2•) dapat berikatan secara kovalen dengan lipid dan protein sehingga dapat menyebabkan terjadinya steatosis (Zimmerman, 1999). Kerusakan tersebut dapat dievaluasi melalui peningkatan aktivitas serum Alkaline phosphatase (ALP) yang merupakan enzim yang dapat ditemukan di hati, tulang, saluran empedu, usus, dan plasenta (Dudgale, 2013). Aktivitas ALP dapat
meningkat sebesar 1,5 kali dari keadaan normal pada tikus terinduski karbon tetraklorida (Obi, Omogbai, Oriafo, dan Ovat, 2001). Berdasarkan hal tersebut maka parameter hepatotoksik yang digunakan pada penelitian ini adalah ALP.
Di tengah kemajuan pengobatan modern, masih banyak masyarakat yang menggunakan bahan alam sebagai obat untuk mencegah maupun mengobati penyakit, termasuk penyakit hati seperti steatosis. Masyarakat mengangap bahan alam lebih aman untuk digunakan dan tidak menimbulkan efek samping yang berbahaya. Data World Health Organization (WHO) pada tahun 2001 menyatakan bahwa penggunaan obat herbal di Indonesia meningkat setiap tahunnya, sekitar 40% penduduk Indonesia menggunakan obat herbal dan 70% diantaranya merupakan masyarakat pedesaan.
Salah satu tanaman yang memiliki potensi sebagai obat untuk mencegah maupun mengobati penyakit hati adalah Macaranga tanarius L., tanaman Macaranga tanarius L.merupakan tanaman berupa pohon berukuran kecil hingga sedang dan memiliki daun yang hijau dan lebar. Tanaman ini banyak tumbuh di hutan-hutan sekunder, kebun bahkan dapat ditemukan di pinggir-pinggir jalan di Indonesia. Daun Macaranga tanarius L. memiliki potensi sebagai agen hepatoprotektif. Infusa daun Macaranga tanarius L. mampu menghasilkan efek hepatoprotektif pada tikus terinduksi karbon tetraklorida (Mahendra, 2011). Pemberian ekstrak metanol-air daun Macaranga tanarius L. jangka panjang 6 hari memiliki efek hepatoprotektif pada tikus terinduksi karbon tetraklorida (Windrawati, 2013). Sehingga dari penelitian ini dilakukan penelitian lanjutan yang
meneliti FHEMM jangka waktu 6 hari pada tikus galur Wistar terinduksi karbon tetraklorida.
Gunawan-Puteri dan Kawabata (2010) melakukan penelitian menggunakan fraksi etil asetat ekstrak metanol-air daun Macaranga tanarius L. dan berhasil mengisolasi lima senyawa ellagitannins yaitu mallotinic acid, corilagin, macatannin A, chebulagic acid, dan macatannin B. Tanin merupakan salah satu antioksidan alami yang mampu menangkal radikal bebas seperti triklorometil (CCl3•) dan triklorometil peroksi (CCl3O2•) yang dapat menyebabkan steatosis. Berdasarkan pemaparan diatas peneliti tertarik untuk melakukan penelitian mengenai efek penghambatan peningkatan aktivitas serum ALP dengan menggunakan fraksi heksan-etanol ekstrak metanol-air daun Macaranga tanarius L. (FHEMM).
Pemilihan pelarut fraksi heksan-etanol didasarkan pada perhitungan nilai log P dari lima senyawa yang berhasil diisolasi oleh Gunawan-Puteri dan Kawabata (2010) menggunakan program MarvinSketch©. Nilai log P dari pelarut heksan-etanol adalah 2,97. Terdapat tiga senyawa ellagitannins yang memiliki nilai log P yang mendekati nilai log P heksan-etanol, yaitu macatannin B (2,94), macatannin A (2,76), dan chebulagic acid (2,64). Ketika nilai log P dari ketiga senyawa tanin tersebut mendekati dengan nilai log P dari etanol, maka diharapkan heksan-etanol mampu menyari ketiga senyawa tanin tersebut dengan maksimal, sehingga diharapkan senyawa tanin yang terkandung di dalam FHEMM mampu untuk menangkal radikal bebas triklorometil (CCl3•) dan triklorometil peroksi (CCl3O2•)
sehingga dapat mencegah terjadinya steatosis, yang ditandai dengan penurunan aktivitas ALP.
Berdasarkan uraian diatas maka dilakukan penelitian secara paralel tentang pengaruh pemberian FHEMM terhadap kadar serum ALT, AST, ALP, LDH, biliburin, dan albumin dengan kajian jangka panjang 6 hari dan pendek 6 jam. Pada penelitian ini fokus peneliti adalah tentang pengaruh pemberian FHEMM jangka panjang 6 hari terhadap kadar ALP pada tikus betina galur Wistar terinduksi karbon tetraklorida.
1. Rumusan masalah
a. Apakah pemberian FHEMM jangka panjang 6 hari dapat menurunkan kadar ALP pada tikus betina galur Wistar terinduksi karbon tetraklorida ?
b. Apakah dosis pemberian FHEMM jangka panjang 6 hari memiliki kekerabatan dengan penurunan aktivitas kadar ALP pada tikus betina galur Wistar terinduksi karbon tetraklorida ?
2. Keaslian penelitian
Penelitian menggunakan ekstrak metanol-air daun Macaranga tanarius L. pernah dilakukan oleh Windrawati (2013) dan Adrianto (2011). Hasil penelitian melaporkan bahwa ekstrak metanol-air daun Macaranga tanarius L. memberikan efek hepatoprotektif pada tikus galur Wistar terinduksi karbon tetraklorida dan parasetamol. Rahmamurti (2012) melaporkan bahwa ekstrak etanol-air daun Macaranga tanarius L. memberikan efek hepatoprotektif pada tikus galur Wistar terinduksi karbon tetraklorida. Matsunami dkk. (2006) melakukan penelitian untuk mengetahui aktivitas
penangkalan radikal bebas dari ekstrak metanol-air daun Macaranga tanarius L., hasilnya ekstrak metanol-air daun Macaranga tanarius L. terbukti memiliki aktivitas penangkapan radikal bebas terhadap 2,2-diphenyl-picrylhydrazyl (DPPH). Ditemukan kandungan flavonoid dari fraksi etil asetat ekstrak metanol daun Macaranga tanarius L. pada penelitian yang dilakukan oleh Kawakami dkk. (2008). Gunawan-Puteri dan Kawabata (2010) berhasil mengisolasi 5 senyawa ellagitannins yang memiliki kemampuan menghambat α-glucosidase dan berpotensi sebagai obat alternatif untuk diabetes. Berdasarkan penelusuran pustaka, penelitian mengenai pengaruh pemberian jangka panjang 6 hari FHEMM terhadap kadar ALP pada tikus betina galur Wistar terinduksi karbon tetraklorida belum pernah dilakukan.
3. Manfaat penelitian
a. Manfaat teoritis
Penelitian mengenai pengaruh pemberian FHEMM jangka panjang 6 hari terhadap kadar ALP diharapkan dapat bermanfaat bagi perkembangan ilmu pengetahuan khususnya farmasi dalam hal penggunaan tanaman yang dapat menurunkan kadar ALP.
b. Manfaat praktis
Penelitian mengenai pengaruh pemberian FHEMM jangka panjang 6 hari terhadap kadar ALP diharapkan dapat memberikan informasi kepada masyarakat mengenai manfaat FHEMM yang dapat mencegah terjadinya steatosis.
B. Tujuan Penelitian
1. Tujuan umum
Menguji FHEMM sebagai agen hepatoprotektor pada tikus betina galur Wistar terinduksi karbon tetraklorida.
2. Tujuan khusus
a. Mengetahui pengaruh pemberian FHEMM jangka panjang 6 hari terhadap kadar ALP pada tikus betina galur Wistar terinduksi karbon tetraklorida. b. Mengetahui kekerabatan antara dosis pemberian FHEMM jangka panjang 6
hari dengan aktivitas penurunan kadar ALP pada tikus betina galur Wistar terinduksi karbon tetraklorida.
8
BAB II
PENELAAHAN PUSTAKA
A. Anatomi dan Fisiologi Hati
Hati merupakan organ metabolik terbesar dan terpenting di tubuh yang
memiliki berat 1-1,5 kg dan mencerminkan 1,5-2,5% dari massa tubuh tanpa lemak.
Ukuran dan bentuk hati bervariasi pada setiap individu dan umumnya variasi ini
sesuai dengan bentuk tubuh secara umum. Hati terletak di kuadran atas abdomen
dan di bawah diafragma. Hati dipertahankan di tempatnya oleh ligamen-ligamen
yang melekat pada diafragma, peritoneum, pembuluh darah besar dan organ-organ
saluran pencernaan bagian atas (Longo dan Fauci, 2010). Hati memiliki peranan
utama dalam proses metabolisme, hati dapat mendetoksifikasi atau menguraikan
zat sisa tubuh dan hormon serta obat dan senyawa asing lain, memproses secara
metabolis tiga jenis nutrien utama dalam tubuh yaitu karbohidrat, protein, dan
lemak setelah zat-zat ini diserap dari saluran cerna, mensekresikan garam empedu
yang membantu proses pencernaan dan penyerapan lemak, membentuk protein
plasma termasuk protein yang dibutuhkan untuk pembekuan darah dan yang untuk
mengangkut hormon steroid dan tiroid serta kolesterol dalam darah, menyimpan
glikogen, lemak, zat besi, dan vitamin, serta mengaktifkan vitamin D yang
dilakukan hati bersama dengan ginjal (Sherwood, 2009).
Hati terbagi menjadi empat lobus, dua lobus utamanya adalah lobus
kanan dan lobus kiri. Lobus kanan merupakan lobus paling besar dan berkontribusi
pada semua permukaan hati. Lobus kiri memiliki ukuran yang lebih kecil
kanan dan kiri dipisahkan oleh ligament falciform pada bagian superior (Gambar 1). Dua lobus lainnya adalah lobus kaudata dan lobus kuadrata yang memiliki
ukuran yang lebih kecil dibandingkan lobus kanan dan kiri (Standring,2008).
Lobus hati dibagi oleh jaringan penghubung menjadi lebih kurang
100.000 unit lobulus hati, yang merupakan unit fungsional dasar hati berupa
jaringan berbentuk heksagonal yang mengelilingi satu vena sentral (Gambar 2a)
dan terdiri dari sel-sel hati (hepatosit) berbentuk kubus. Ukuran diameter tiap
lobulus lebih kurang 1 mm dan antara lobulus satu dengan yang lainnya dipisahkan
oleh interlobular septum. Di setiap enam sudut lobulus terdapat tiga jenis pembuluh, yaitu cabang arteri hepatika, cabang vena porta hati dan vena porta
biliaris. Adanya ketiga pembuluh ini pada setiap sudut menyebabkan sudut lobulus
disebut dengan triad portal. Darah dari cabang arteri hepatika dan vena porta
mengalir dari perifer lobulus ke ruang kapiler luas yang disebut sinusoid (Gambar
2b) yang berjalan di antara jejeran hepatosit ke vena sentral seperti jari-jari roda
sepeda (Sherwood, 2009).
Setiap hepatosit melakukan beragam tugas metabolik dan sekretorik yang
sama. Satu-satunya fungsi hati yang tidak dilakukan oleh hepatosit adalah aktivitas
fagosit yang dilakukan oleh makrofag residen yang disebut sel Kupffer (Gambar
2b). Sel Kupffer terletak di dalam lapisan sinusoid, sel ini mengeluarkan bakteri
atau partikel asing lainnya yang masuk melalui darah yang melewati sinusoid.
Hepatosit juga melakukan fungsi sekresi empedu yang dikeluarkan menuju duktus
biliaris (Shier, Butler, dan Lewis, 2006).
Untuk melaksanakan beragam tugasnya, susunan anatomik hati
memungkinkan setiap hepatosit untuk berkontak langsung dengan darah dari dua
sumber yaitu 20% dari arteri hepatika yang membawa darah kaya akan oksigen dan
sisanya dari vena porta yang membawa darah kaya akan nutrien yang berasal dari
lambung, usus, pankreas, dan limpa. Darah dari vena porta juga mungkin
mengandung bakteri usus, racun, dan obat yang dicerna. Dari hal ini maka
tergambarkan bahwa sel-sel hepar mendapatkan suplai darah yang relatif kurang
oksigen sehingga sel-sel hepar rentan terhadap kerusakan dan penyakit (Corwin,
2007).
B. Hepatotoksisitas
Kerusakan hati dapat terjadi karena beberapa hal, seperti kekurangan
oksigen, infeksi, cedera imunologi, ketidakseimbangan metabolisme, kelainan
genetik, dan pemejanan bahan kimia serta obat baik sengaja maupun tidak sengaja
yang disebut dengan hepatotoksisitas. Hepatotoksisitas dapat terjadi karena
Berbagai zat tersebut mencakup toksin industri, pestisida dan yang lebih sering
adalah zat farmakologis yang digunakan dalam terapi medis (Longo dan Fauci,
2010).
Jenis-jenis kerusakan hati :
1. Perlemakan hati (Steatosis)
Steatosis pada dasarnya merupakan manifestasi dari sindrom metabolik lipid di hati. Steatosis adalah suatu keadaan terjadinya akumulasi lemak yang sebagian besar berupa droplet trigliserida di dalam hepatosit melebihi 5-10%
dari berat hati. Pada keadaan normal hati tidak menyimpan lemak, melainkan
akan dikeluarkan ke sirkulasi darah. Perlemakan hati dibagi menjadi dua, yaitu
perlemakan hati yang disebabkan oleh alkohol dan perlemakan hati yang tidak
disebabkan oleh alkohol atau biasa dikenal dengan Non-alcoholic Fatty Liver
Disease (NAFLD). Tingkat steatosis didasarkan pada proporsi jumlah hepatosit yang mengandung droplet lemak, yaitu <10% ringan, 10-30% sedang, dan
>30% berat (Tirosh, 2015). Steatosis yang terjadi karena terdapat beberapa droplet lemak kecil yang tidak menggantikan nukleus di dalam hepatosit
dikenal dengan Microvesicular steatosis, hal ini muncul seperti pada keadaan perlemakan hati akut masa kehamilan dan toksisitas asam valproic, sedangkan yang terjadi karena terdapat satu droplet besar yang menggantikan nukleus di
dalam hepatosit dikenal dengan Macrovesicular steatosis, hal ini dapat terjadi karena toksisitas etanol (Burt, Portmann, dan Ferrel, 2012).
Terdapat beragam faktor penyebab terjadinya steatosis, secara garis besar dibedakan atas faktor primer, yakni obesitas, hiperlipidemia, dan
resistensi insulin, serta faktor sekunder yang meliputi diet yang tidak seimbang,
malabsorbsi, kehamilan, alkohol, serta obat-obatan (Panjaitan dkk., 2007).
Karbon tetraklorida menyebabkan steatosis melalui penghambatan sintesis satuan protein dari lipoprotein dan penekanan konjugasi trigliserida dengan
lipoprotein (Lu dan Kacew, 2002).
2. Kolestasis
Kolestasis merupakan jenis kerusakan hati yang bersifat akut dan jarang
ditemukan dibandingkan steatosis dan nekrosis, serta lebih sulit diinduksi pada hewan percobaan, kecuali mungkin dengan steroid (Lu dan Kacew, 2002).
Empedu merupakan jalur utama untuk eliminasi bilirubin, kelebihan kolesterol,
dan xenobiotik yang kurang larut dalam air untuk dibuang melalui urin. Empedu
diproduksi oleh hepatosit. Secara fisiologis, pada keadaan kolestasis hati
menunjukkan adanya penurunan aliran empedu dan kegagalan untuk
mengeluarkan konstituen anorganik dan organik empedu. Secara khusus,
keadaan kolestasis timbul dari perubahan molekuler dan ultrastruktural yang
mengganggu masuknya molekul organik kecil, garam inorganik, protein, dan
air ke dalam ruang empedu. Hal ini menyebabkan terjadinya jaundice disertai dengan peningkatan kadar bilirubin, garam empedu, dan ALP (Burt dkk., 2012).
Secara morfologis kolestasis didefinisikan sebagai akumulasi pigmen empedu
dalam kanlikuli dan hepatosit, pelebaran ruang kanalikular dengan pengurangan
mikrovili, dan akumulasi tembaga. Kolestasis dapat disebabkan baik kegagalan
untuk mengeluarkan empedu (intrahepatik) atau obstruksi mekanik (kolestasis
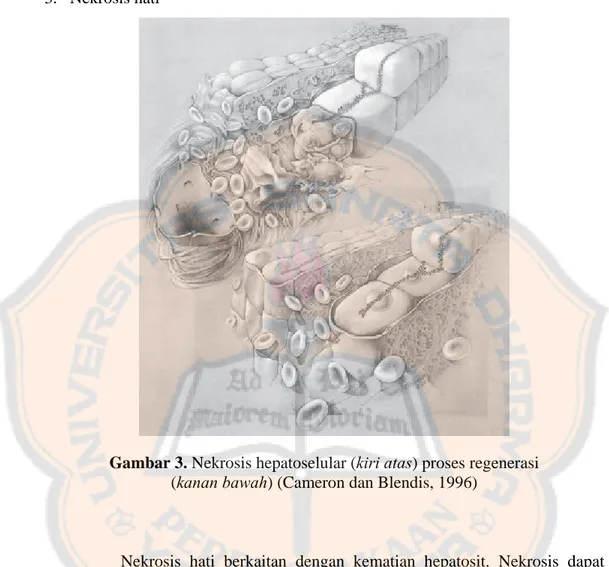
3. Nekrosis hati
Nekrosis hati berkaitan dengan kematian hepatosit. Nekrosis dapat
bersifat fokal (berpusat, mid-zonal, periferal) maupun massif, dan biasanya bersifat akut. Sejumlah bahan kimia dapat menyebabkan nekrosis hati. Hal ini
merupakan manifestasi toksisitas yang serius namun tidak sangat penting
karena hati memiliki kemampuan regenerasi yang sangat baik. Kematian sel
terjadi bersamaan dengan pecahnya membran plasma (Gambar 3) dan tidak
terjadi perubahan ultrastruktural pada membran sel sebelum pecah. Terdapat
sejumlah perubahan yang mendahului kematian sel seperti perubahan morfologi
awal yakni berupa edema sitoplasma, dilatasi retikulum endoplasma, dan
Gambar 3. Nekrosis hepatoselular (kiri atas) proses regenerasi (kanan bawah) (Cameron dan Blendis, 1996)
disagregasi polisom. Perubahan akhirnya adalah pembengkakan yang progesif
pada mitokondria, pembengkakan sitoplasma, disolusi organel dan nukleus, dan
pecahnya membran plasma (Lu dan Kacew, 2002).
4. Fibrosis
Fibrosis merupakan kerusakan pada sel hepatosit, yang ditandai oleh
deposisi kolagen, proteoglikan, dan glikoprotein. Regenerasi merupakan proses
yang bermanfaat untuk penyembuhan, namun pada proses tersebut juga
mungkin sedang terjadi proses merugikan yaitu munculnya penyakit hati kronis
progesif yang dikenal dengan fibrosis. Fibrosis dapat dianggap sebagai respon
penyembuhan luka yang berulang pada hati. Setelah terjadi cedera hati akut,
elemen seluler yang selamat dapat beregenerasi, dengan disertai respon
inflamasi untuk membersihkan sisa-sisa sel yang rusak, dan remodeling matriks
ekstraselular. Apabila kerusakan hati berlanjut maka regenerasi hati mungkin
gagal untuk mengembalikan jaringan yang rusak dan deposisi matriks menjadi
lebih luas.. Fibrosis yang meluas dapat menyebabkan perubahan bentuk hati dan
mengganggu aliran darah (Burt dkk., 2012).
5. Sirosis
Sirosis merupakan kondisi fibrosis dan pembentukan jaringan parut.
Jaringan hati normal digantikan oleh nodus-nodus fibrosa keras serta pita-pita
fibrosa yang mengerut dan mengelilingi hepatosit. Struktur permanen hati
berubah karena kerusakan sel yang berkepanjangan yaitu penyakit hati kronis >
6 bulan. Sirosis terjadi di hati sebagai respon terhadap cedera sel berulang dan
infeksi misalnya hepatitis, obstruksi saluran empedu, yang menyebabkan
penimbunan empedu di kanalikulus dan pecahnya kanalikulus, dan cedera
hepatosit akibat toksin (Corwin, 2007). Dalam sebagian besar kasus, tampaknya
sirosis berasal dari nekrosis sel tunggal terkait dengan defiensi mekanisme
perbaikan. Kondisi ini menyebabkan aktivitas fibroblastik dan pembentukan
jaringan parut. Tidak kuatnya aliran darah di dalam hati juga mugkin menjadi
faktor pendukung. Penyebab sirosis yang paling umum adalah paparan
hepatotoksin seperti alkohol. Alkohol dapat menyebabkan kerusakan
mitokondria (Lu dan Kacew, 2002).
C. Hepatotoksin
Senyawa kimia yang dapat menyebabkan kerusakan hati dikenal dengan
hepatotoksin atau hepatotoksikan. Hepatotoksin merupakan senyawa eksogen yang
dapat berupa obat-obatan, bahan kimia industri, bahan kimia alami seperti
microcystins, obat herbal, maupun suplemen makanan. Kerusakan hati dapat timbul dari senyawa utama, metabolit reaktif, atau respon imunologi yang mempengaruhi
hepatosit, sel epitel empedu dan/atau pembuluh darah di hati (Singh, Bhat, dan
Sharma, 2011).
Senyawa dan obat-obatan yang dapat menyebabkan kerusakan hati dapat
dibedakan menjadi dua, yaitu :
1. Hepatotoksin teramalkan
Hepatotoksin teramalkan merupakan senyawa atau obat-obatan yang
obat atau senyawa tersebut dalam jumlah yang cukup untuk menimbulkan efek.
Hepatotoksin teramalkan bergantung pada dosis pemberian. Contoh
hepatotoksin teramalkan adalah acetaminophen, karbon tetraklorida, fosfor, dan
kloroform (Navarro dan Senior, 2006).
2. Hepatotoksin tak teramalkan
Hepatotoksin tak teramalkan merupakan obat-obatan atau senyawa yang
dapat menimbulkan efek hepatotoksik tanpa adanya peringatan dan hanya
terjadi pada orang tertentu, serta memiliki periode latensi yang sangat
bervariasi, mulai dari beberapa hari hingga 12 bulan. Hepatotoksin tak
teramalkan tidak bergantung pada dosis (Navarro dan Senior, 2006).
D. Karbon Tetraklorida
Karbon tetraklorida merupakan cairan jernih tidak berwarna, memiliki bau
yang khas dan mudah menguap. Karbon tetrakloridamemiliki berat molekul 153,8
dengan titik didih 76,72oC dan titik leleh 22,92oC. Senyawa ini sukar larut di dalam
air (Gambar 4). Karbon tetrakloridamerupakan senyawa model hepatotoksin yang
sering digunakan sebagai penginduksi kerusakan sel hati tikus di dalam suatu
Gambar 4. Struktur molekul karbon tetraklorida (World Health Organization, 1999)
penelitian. Karbon tetraklorida diabsorbsi dengan baik di saluran pencernaan dan
pernafasan pada hewan dan manusia (WHO, 1999).
Karbon tetraklorida memiliki struktur molekul yang sangat sederhana,
ketika dipejankan pada berbagai hewan uji dapat menyebabkan nekrosis hepatik
sentrilobular dan perlemakan hati. Senyawa ini terdistribusi ke seluruh tubuh
namun efek toksik utamanya di hati. Hati menjadi target utama karena toksisitas
karbon tetraklorida bergantung pada aktivasi metabolit oleh sitokrom P4502E1
(CYP2E1). Hati memiliki sitokrom P450 dengan konsentrasi tertinggi di dalam
tubuh, terutama pada bagian sentrilobular (Trimbell, 2008). Metabolisme karbon
tetraklorida dimulai dari sitokrom P4502E1 (CYP2E1) yang memediasi transfer
elektron ke ikatan C-Cl, membentuk radikal anion yang mengeliminasi Cl sehingga
membentuk radikal triklorometil (CCl3•) yang reaktif. Radikal triklorometil dengan
oksigen membentuk radikal triklorometil peroksi (CCl3O2•) (WHO, 1999).
Radikal triklorometil (CCl3•) dan radikal triklorometil peroksi (CCl3O2•) ini
dapat menyebabkan terjadinya steatosis. Luasnya steatosis yang terjadi bergantung pada jumlah metabolit rekaktif yang dihasilkan oleh karbon tetraklorida. Steatosis terjadi akibat adanya ketidakseimbangan antara sintesis dan degradasi lipid, dan
kegagalan trigliserida untuk berpindah sebagai Very Low Density Lipoprotein (VLDL) dari hati ke sirkulasi darah. Laju sintesis dari trigliserida bergantung pada
ketersediaan substrat dan pada aktivitas enzim yang terlibat. Suplai dari asam lemak
memiliki peranan penting dalam akumulasi trigliserida. Asam lemak bebas
dikeluarkan dari plasma melalui difusi pasif atau melalui sistem transport spesifik
dalam hati, yaitu esterifikasi untuk membentuk trigliserida, fosfolipid dan ester
asam lemak lainnya, dan beta-oksidasi untuk membentuk CO2 dan badan keton.
Karbon tetraklorida dapat meningkatkan sintesis asam lemak dan trigliserida dari
asetat, dan juga meningkatkan kecepatan esterifikasi lipid dan sintesis kolesterol.
Selain itu, karbon tetraklorida juga dapat menghambat beta-oksidasi dan
menurunkan sekresi lipid seluler. Hal ini mengakibatkan ketersediaan substrat
meningkat sehingga sintesis trigliserida juga meningkat, karena produksi
trigliserida semakin meningkat dan hati tidak dapat untuk mengeluarkan trigliserida
ke sirkulasi darah menyebabkan trigliserida terakumulasi di dalam hepatosit
(Weber, Boll, dan Stampfl, 2003).
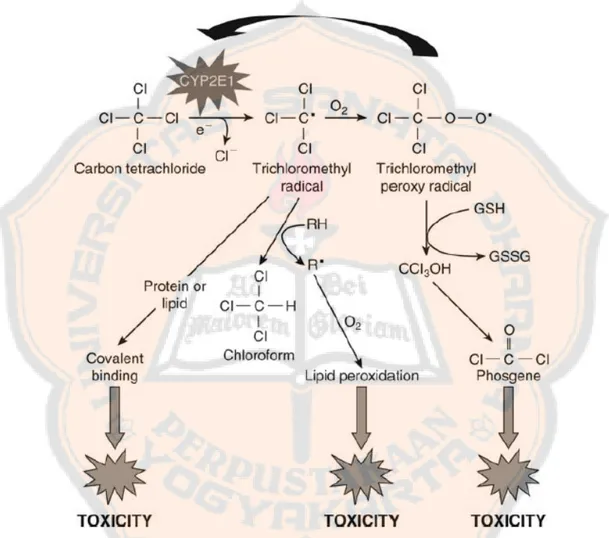
Radikal triklorometil peroksi (CCl3O2•) juga dapat berikatan dengan lipid
mikrosomal dan protein secara kovalen dan bereaksi secara langsung dengan
membran fosfolipid dan kolesterol menghasilkan fosgen dan klorin elektrofilik
yang akan memberikan efek toksik (Gambar 5). Adapun mekanisme lainnya adalah
lipid peroksidasi yang menghasilkan senyawa-senyawa yang akan menghambat
sintesis protein. Beberapa efek dari peroksidasi lipid antara lain terpengaruhinya
integritas struktur lipid pada membran yang menyebabkan kerusakan beberapa
struktur, kerusakan membran lisosom hingga pecah dan hilangnya isi organela
Setalah satu sampai tiga jam setelah pemejanan, trigliserida akan
terakumulasi di hepatosit, terdeteksi sebagai droplet lemak (Trimbell, 2008).
Kerusakan pada hepatosit akan mempengaruhi kadar enzim AST, ALT, ALP,
kadar enzim AST, ALT, ALP, dan bilirubin total, sebaliknya kadar albumin dalam
serum akan menurun (Panjaitan dkk., 2007).
E. Alkaline Phospatase
Metode yang dapat digunakan untuk mendeteksi kerusakan hepatoseluler
salah satunya adalah dengan tes enzim serum. Tes-tes ini dapat digunakan untuk
mendeteksi adanya penyakit hati, membedakan berbagai jenis gangguan hati, dan
Gambar 5. Mekanisme biotransformasi dan oksidasi karbon tetraklorida (Timbrell, 2008)
memperkirakan luas kerusakan hati yang diketahui. Hati mengandung ribuan
enzim, sebagian diantaranya terdapat di dalam serum darah. Enzim yang sering
digunakan sebagai indikator kerusakan hati selain aspartate aminotransferase (AST) dan alanine aminotransferase (ALT) adalah Alkaline phosphatase (ALP).
ALP merupakan kelompok enzim yang menghidrolisis fosfat ester pada pH
basa, dapat ditemukan selain di dalam hati juga di dalam tulang, ginjal, usus, dan
plasenta pada masa kehamilan. ALP yang terdapat di dalam hati, tulang, dan usus
dianggap berasal dari gen yang sama, berbeda dengan ALP yang terdapat di dalam
usus dan plasenta. Di dalam hati ALP secara histokimia ditemukan dalam mikrovili
kanalikuli empedu dan pada permukaan sinusoidal hepatosit (Thapa dan Walia,
2007).
Nilai normal serum ALP adalah 55-105 U/l pada wanita dewasa, 40-130 U/l
pada pria dewasa, dan 100-400U/l pada remaja (Kuntz, 2008). Nilai rata-rata ALP
bervariasi bergantung usia, dan relatif tinggi pada anak-anak dan remaja, kemudian
relatif rendah di usia dewasa, dan kembali tinggi di usia tua. Pada pria biasanya
nilai ALP lebih tinggi dibandingkan dengan wanita. Nilai ALP juga bergantung
pada berat badan dan berbanding terbalik dengan tinggi badan (Thapa dan Walia,
2007). Peningkatan aktivitas ALP dapat digunakan sebagai indikator kerusakan
hati. Peningkatan aktivitas ALP pada kerusakan atau penyakit hati merupakan
akibat dari peningkatan sintesis enzim oleh sel-sel yang melapisi kanalikuli
empedu, biasanya sebagai respon adanya kolestasis intrahepatik maupun
ekstrahepatik (Gaw, Murphy, Srivastava, Cowan, dan O’Reilly, 2013). Aktivitas
sedangkan peningkatan 10 kali dari nilai normal menunjukkan adanya obstruksi
biliaris (Lawrence dan Amadeon, 1996). Aktivitas ALP yang meningkat 2 kali dari
nilai normal menunjukkan bahwa telah terjadi NAFLD (Bayard, Holt, dan
Boroughs, 2006). F. Macaranga tanarius L. 1. Taksonomi Kingdom : Plantae Subkingdom : Viridiplantae Infrakingdom : Streptophyta Divisi : Tracheophyta Subdivisi : Spermatophytina Kelas : Magnoliopsida Superordo : Rosanae Ordo : Malpighiales Famili : Euphorbiaceae
Genus : Macaranga Thouars
Spesies : Macaranga tanarius L.
(Integrated Taxonomic Information System, 2015).
2. Nama lain
a. Indonesia : Tutup ancur, Hanuwa, Mara, Mapu
b. Malaysia : Kalo, Kundoh, Mahang puteh, Tampu
c. Filipina : Kuyunon, Himindang, Binunga
d. Inggris : Hairy mahang
e. Thailand : Hu chang lek, Mek, Pang, Lo khao
(Orwa, Mutua, Kindt, dan Jamnadass, 2009).
3. Morfologi
Macaranga tanarius L. merupakan tanaman dengan ukuran pohon kecil sampai sedang, tinggi pohon dapat mencapai 20-25 meter, memiliki dahan agak
besar. Daun berwarna hijau, berseling, agak membundar, dengan spatula besar
yang luruh (Gambar 6). Kulit tangkai daun jika dikupas atau dipotong dapat
mengeluarkan cairan berwarna coklat bening dan lekat. Perbungaan bermalai di Gambar 6. Daun Macaranga tanarius L.
ketiak, bunga ditutupi oleh daun gagang. Buah kapsul berkokus dua dan
terdapat kelenjar kekuningan di luarnya. Biji membulat dan menggelembur.
Jenis ini juga mengandung tanin yang cukup untuk menyamak jala dan kulit
(Wardiyono, 2015).
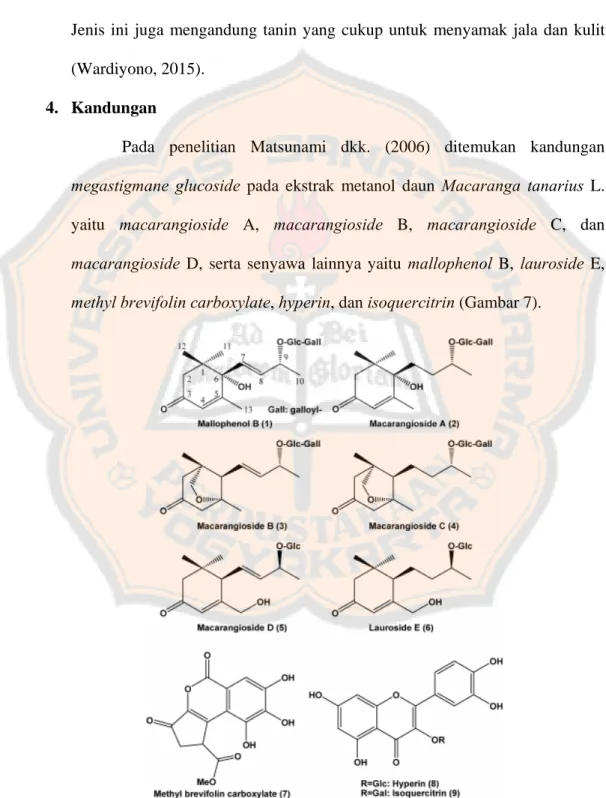
4. Kandungan
Pada penelitian Matsunami dkk. (2006) ditemukan kandungan
megastigmane glucoside pada ekstrak metanol daun Macaranga tanarius L. yaitu macarangioside A, macarangioside B, macarangioside C, dan
macarangioside D, serta senyawa lainnya yaitu mallophenol B, lauroside E,
methyl brevifolin carboxylate, hyperin, dan isoquercitrin (Gambar 7).
Gambar 7. Struktur kandungan senyawa daun
Pada tahun 2009, Matsunami dkk. menemukan tiga kandungan
glukosida baru yaitu (+)-Pionoresinol 4-0-[6”-0-gallolyl]-β
-D-glocopyranoside, Macarangioside E, dan Macaragioside F. Senyawa-senyawa hasil kedua penelitian ini menunjukkan aktivitas penangkapan radikal bebas
terhadap 2,2-diphenyl-picrylhydrazyl (DPPH).
Kawakami dkk. (2008), menemukan tujuh senyawa prenylflavonone pada fraksi etil asetat ekstrak metanol daun Macaranga tanarius L. yaitu
macaflavonone A-G, tanariflavone B, dan bersama dengan senyawa lainnya yaitu nymphaeol C, serta senyawa diterpen yaitu kolavenol. Kumazawa,
Murase, Momose, dan Fukomoto (2014) melaporkan bahwa terdapat
kandungan prenyflavonoids pada daun Macaranga tanarius L. dan terbukti memiliki aktivitas penangkapan radikal bebas terhadap
2,2-diphenyl-picrylhydrazyl (DPPH).
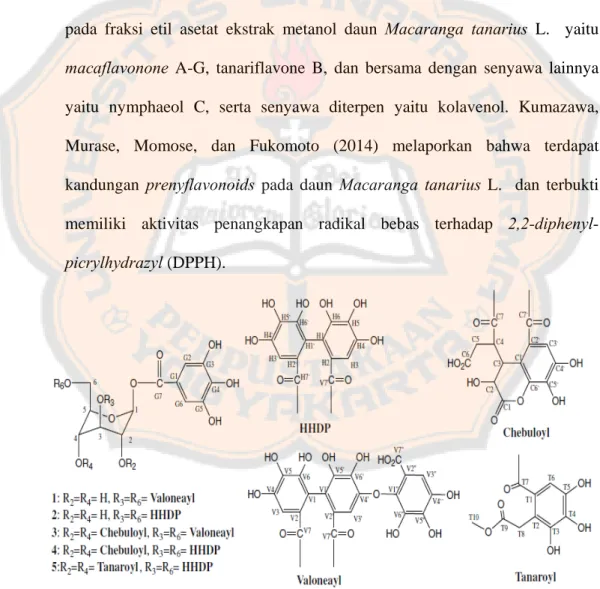
Gambar 8. Isolasi senyawa ellagitannins dari fraksi EtOAc daun Macaranga
tanarius L. : mallotinic acid (1) corilagin (2) macatannin A (3) chebulagic acid (4) dan macatannin B (5) (Gunawan-Puteri dan Kawabata, 2010)
Pada penelitian Gunawan-Puteri dan Kawabata (2010) ditemukan lima
senyawa ellagitannins (Gambar 8) pada fraksi etil asetat (EtOAc) ekstrak metanol-air daun Macaranga tanarius L., yaitu mallotinic acid, corilagin,
macatannin A, chebulagic acid, dan macatannin B.
5. Khasiat dan kegunaan
Pengobatan tradisional Malaysia dan Thailand menggunakan dekok
akar tanaman Macaranga tanarius L. sebagai obat antipiretik dan antitusif. Akar kering Macaranga tanarius L. sebagai agen emetik, sedangkan daun segar Macaranga tanarius L. digunakan untuk menutupi luka untuk mencegah peradangan. Di China tanaman Macaranga tanarius L. secara komersial ditanam dan dipanen untuk memproduksi minuman kesehatan, dan ekstraknya
ditambahkan ke dalam pasta gigi, serta daun kering dari Macaranga tanarius L. dimanfaatkan sebagai teh herbal. Tunas muda Macaranga tanarius L. dijadikan sebagai sumber sayuran di Thailand, Filipina, Indonesia dan juga
Afrika tengah (Lim, Lim dan Yule, 2009).
6. Penyebaran
Macaranga tanarius L. merupakan tanaman pionir yang dapat tumbuh dengan sangat cepat. Tanaman ini secara umum sering tumbuh di hutan
sekunder, terutama untuk hutan-hutan logging serta semak-semak belukar dan kebun-kebun (World Agroforestry Centre, 2002). Macaranga tanarius L. berasal dari daerah tropis yaitu Afrika, Madagaskar, Australia, Pasifik, dan Asia
G. Metode Penyarian
Terdapat beberapa metode penyarian, yaitu maserasi, perkolasi, infudasi,
ekstraksi berkesinambungan yang meliputi ekstraksi dengan soklet, large-scale
extraction, dan supercritical fluid extraction (SFE) (Shah dan Seth, 2010). Maserasi merupakan metode penyarian yang sangat sederhana, prinsip metode maserasi
adalah perendaman sampel. Serbuk simplisia direndam dalam cairan penyari
selama beberapa hari pada suhu kamar dan terlindung dari cahaya. Cairan penyari
(pelarut) akan menembus dinding sel dan masuk ke dalam rongga sel yang
mengandung zat aktif. Zat aktif yang terkandung di dalam sel akan terekstrak keluar
karena adanya perbedaan konsentrasi zat aktif di dalam dan luar sel. Peristiwa
tersebut akan terus berlangsung hingga terjadi kesetimbangan konsentrasi antara
larutan di dalam dan luar sel. Metode maserasi memiliki keuntungan dibanding
dengan metode lain, keuntungan metode maserasi yaitu tidak memerlukan alat
khusus dan tidak memerlukan pemanasan (Chasani, Fitriaji, dan Purwati,2013).
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif
dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai,
kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang
tersisa diperlakukan sedemikian hingga memenuhi baku yang telah ditetapkan
(Direktorat Jendral Pengawasan Obat dan Makanan RI, 1995). Ketika diinginkan
untuk memisahkan senyawa-senyawa yang terdapat di dalam ekstrak, maka dapat
dilakukan fraksinasi. Fraksinasi adalah proses pemisahan suatu zat atau kuantitas
beberapa jumlah kecil fraksi. Pemisahan yang dilakukan didasarkan pada kelarutan
tiap fraksi (Adijuwana dan Nur, 1989).
H. Landasan Teori
Hati merupakan organ viseral terbesar di dalam tubuh. Hati bertanggung
jawab pada tiga kategori utama fungsi hati, yaitu regulasi metabolisme, regulasi
hematologi, dan produksi empedu (Martini dan Nath, 2009). Hati dapat
mendetoksifikasi atau menguraikan zat sisa tubuh dan hormon serta obat dan
senyawa asing lain (Sherwood, 2009). Kerusakan hati dapat terjadi karena beberapa
hal, seperti kekurangan oksigen, infeksi, cedera imunologi, ketidakseimbangan
metabolisme, kelainan genetik, dan pemejanan bahan kimia serta obat baik sengaja
maupun tidak sengaja yang disebut dengan hepatotoksisitas (Longo dan fauci,
2010). Jenis kerusakan hati yang dapat terjadi yaitu perlemakan hati (steatosis), kolestasis, nekrosis hati, fibrosis dan sirosis (Burt dkk., 2012; Lu dan Kacew, 2002).
Karbon tetraklorida merupakan senyawa model yang sering digunakan
sebagai penginduksi kerusakan sel hati tikus seperti steatosis di dalam suatu penelitian. Ketika masuk ke dalam tubuh karbon tetraklorida akan dimetabolisme
oleh sitokrom P4502E1 (CYP2E1) menjadi radikal bebas triklorometil (CCl3•) dan
triklorometil peroksi (CCl3O2•) yang dapat berikatan secara kovalen dengan lipid
dan protein sehingga dapat menyebabkan terjadinya steatosis. Steatosis dapat dievaluasi dengan menggunakan tes enzim hati, salah satunya adalah ALP.
Terjadinya peningkatan aktivitas ALP menunjukkan bahwa telah terjadi gangguan
empedu dan pada permukaan sinusoidal hepatosit. Aktivitas ALP yang meningkat
sebesar 2 kali dari nilai normal menunjukkan bahwa telah terjadi NAFLD (WHO,
1999; Gaw dkk., 2013; Zimmerman, 1999; Thapa dan Walia, 2007; Bayard dkk.,
2006).
Macaranga tanarius L. merupakan tanaman dengan ukuran pohon kecil sampai sedang dan memiliki daun berwarna hijau, berseling, agak membundar,
dengan spatula besar yang luruh (Wardiyono, 2015). Pemberian ekstrak
metanol-air daun Macaranga tanarius L. jangka panjang 6 hari memiliki efek hepatoprotektif pada tikus terinduksi karbon tetraklorida (Windrawati, 2013).
Sehingga dari penelitian ini dilakukan penelitian lanjutan yang meneliti FHEMM
jangka waktu 6 hari pada tikus galur Wistar terinduksi karbon tetraklorida.
Di dalam fraksi etil asetat ekstrak metanol-air daun Macaranga tanarius L. terdapat senyawa tanin (Gunawan-Puteri dan Kawabata, 2010) dan flavonoid
(Kawakami dkk., 2008). Penelitian ini menggunakan fraksi heksan-etanol
didasarkan pada perhitungan nilai log P lima senyawa tanin yang berhasil diisolasi
oleh Gunawan-Puteri dan Kawabata (2010). Dari kelima senyawa tersebut terdapat
tiga senyawa tanin yang memiliki nilai log P mendekati nilai log P heksan-etanol.
Tanin merupakan salah satu senyawa antioksidan yang dapat menangkal radikal
bebas seperti radikal bebas triklorometil (CCl3•) dan triklorometil peroksi
(CCl3O2•) yang dapat berikatan secara kovalen dengan lipid dan protein sehingga
menyebabkan tejadinya steatosis. Apabila radikal bebas triklorometil (CCl3•) dan
triklorometil peroksi (CCl3O2•) tidak dapat berikatan dengan lipid dan protein maka
I. Hipotesis
Pemberian FHEMM jangka panjang 6 hari dapat menurunkan kadar ALP
31
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian mengenai pengaruh pemberian FHEMM jangka panjang 6 hari
terhadap kadar ALP pada tikus betina galur Wistar terinduksi karbon tetraklorida
merupakan jenis penelitian eksperimental murni dengan rancangan acak lengkap
pola searah.
B. Variabel Penelitian dan Definisi Operasional
1. Variabel utama
a. Variabel bebas
Variabel bebas dalam penelitian ini adalah variasi dosis pemberian
FHEMM jangka panjang 6 hari pada tikus betina galur Wistar terinduksi
karbon tetraklorida.
b. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah nilai aktivitas ALP
setelah pemberian FHEMM jangka panjang 6 hari pada tikus betina galur
Wistar terinduksi karbon tetraklorida.
2. Variabel pengacau
a. Variabel pengacau terkendali
Variabel pengacau terkendali dalam penelitian ini adalah kondisi
hewan uji yaitu tikus betina galur Wistar dengan berat badan 130-180 gram
melalui rute intraperitoneal (IP), dan pemberian FHEMM melalui rute per
oral (PO) dengan frekuensi pemberian satu kali sehari, selama enam hari
berturut-turut dan waktu pemberian yang sama; bahan uji yang digunakan
adalah daun Macaranga tanarius L. segar yang dipetik pada pagi hari di bulan Juni dari pohon Macaranga tanarius L. yang tumbuh di daerah Paingan, Maguwoharjo, Sleman.
b. Variabel pengacau tak terkendali
Variabel pengacau tak terkendali dalam penelitian ini adalah kondisi
patologis tikus betina galur Wistar yang digunakan.
3. Definisi operasional
a. Fraksi heksan-etanol dari ekstrak metanol-air daun Macaranga tanarius L. Fraksi heksan-etanol dari ekstrak metanol-air daun Macaranga tanarius L. adalah fraksi kental yang diperoleh dengan mengekstraksi serbuk kering daun Macaranga tanarius L. dengan pelarut metanol-air secara maserasi sehingga diperoleh ekstrak kental. Ekstrak kental kemudian
difraksinasi secara maserasi dengan pelarut heksan-etanol sehingga
diperoleh fraksi kental.
b. Penurunan aktivitas ALP
Penurunan aktivitas ALP adalah penurunan bermakna kadar ALP
pada kelompok perlakuan dibandingkan dengan kelompok kontrol
c. Jangka panjang 6 hari
Jangka panjang 6 hari adalah pemberian FHEMM dengan frekuensi
satu kali sehari selama enam hari berturut-turut.
C. Bahan Penelitian
1. Bahan utama
a. Hewan uji
Hewan uji yang digunakan adalah tikus betina galur Wistar dengan
berat badan 130-180 gram dan umur 2-3 bulan yang diperoleh dari
Laboratorium Imono Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta.
b. Bahan uji
Bahan uji yang digunakan adalah daun Macaranga tanarius L. segar yang dipetik pada pagi hari di bulan Juni dari pohon Macaranga tanarius
L. yang tumbuh di daerah Paingan, Maguwoharjo, Sleman. Pengumpulan
bahan uji dikerjakan oleh kelompok yang diketuai oleh Penina Kurnia Uly,
dan proses determinasi tanaman dilakukan di bagian Biologi Farmasi
Universitas Gadjah Mada Yogyakarta.
2. Bahan kimia
a. Bahan hepatotoksin yang digunakan adalah karbon tetraklorida yang
diperoleh dari Laboratorium Kimia Analisis Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
c. Pelarut FHEMM dan kontrol negatif yang digunakan adalah Natrium-Carboxymethyl Cellulosa 1% (CMC-Na 1%) yang diperoleh dari Laboratorium Biofarmasetika Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta.
d. Pelarut untuk ekstraksi serbuk daun Macaranga tanarius L. yang digunakan adalah metanol dan aquadest yang diperoleh dari CV. General Labora Yogyakarta.
e. Pelarut untuk fraksinasi ekstrak kental daun Macaranga tanarius L. yang digunakan adalah heksan dan etanol yang diperoleh dari CV. General
Labora Yogyakarta.
f. Reagen AST/GOT Thermo Scientific® milik Rumah Sakit Bethesda
Yogyakarta
g. Reagen ASL/GPT Thermo Scientific® milik Rumah Sakit Bethesda
Yogyakarta
h. Reagen ALP Thermo Scientific® milik Rumah Sakit Bethesda Yogyakarta
D. Alat Penelitian
1. Alat pembuatan FHEMM
Alat-alat yang digunakan adalah orbital shaker Optima®, timbangan analitik Mettler Toledo®, oven Memmert®, blender Miyako®, rotary vacuum evaporator IKAVAC®, penangas air, Electric Sieve Shaker Indotest Multi Lab®, ayakan nomor mesh 50, moisture balance, serta alat-alat gelas Pyrex®
berupa gelas beker, labu erlenmeyer, gelas ukur, labu ukur, batang pengaduk,
pipet tetes, corong, labu alas bulat dan cawan porselen.
2. Alat perlakuan hewan uji
Alat-alat yang digunakan adalah timbangan analitik Mettler Toledo®,
spuit injeksi PO dan syringe 3 cc Terumo®, spuit injeksi intraperitoneal dan
syringe 1 cc Terumo®, pipa kapiler, serta alat-alat gelas Pyrex® berupa gelas beker, gelas ukur, labu ukur, batang pengaduk, pipet tetes, corong, dan pipet
ukur.
E. Tata Cara Penelitian
1. Determinasi tanaman Macaranga tanarius L.
Determinasi dilakukan dengan mencocokkan secara makroskopis
tanaman Macaranga tanarius L. yang diperoleh dari Paingan, Maguwoharjo, Sleman dengan literatur. Determinasi dilakukan di bagian Biologi Farmasi
Fakultas Farmasi Universitas Gadjah Mada Yogyakarta.
2. Pengumpulan bahan uji
Bahan uji yang digunakan adalah daun Macaranga tanarius L. segar yang dipetik pada pagi hari di bulan Juni dari pohon Macaranga tanarius L. yang tumbuh di daerah Paingan, Maguwoharjo, Sleman. Pengumpulan bahan
uji dikerjakan oleh kelompok yang diketuai oleh Penina Kurnia Uly.
3. Pembuatan serbuk daun Macaranga tanarius L.
Daun Macaranga tanarius L. disortasi basah untuk memisahkan daun yang tidak segar dan bagian dari daun yang tidak diinginkan, kemudian dicuci
debu. Daun Macaranga tanarius L. yang lebar dirajang hingga menjadi ukuran yang lebih kecil untuk mempercepat proses pengeringan. Daun Macaranga tanarius L. diangin-anginkan, kemudian dikeringkan menggunakan oven dengan suhu 29oC selama lebih kurang 3 hari. Daun Macaranga tanarius L.
yang kering disortasi kering untuk memisahkan bagian dan bahan lain yang
tidak diinginkan, kemudian dilakukan penyerbukan dengan menggunakan
blender Miyako®. Serbuk diayak menggunakan Electric Sieve Shaker Indotest Multi Lab® dengan ayakan nomor mesh 50 sehingga didapatkan serbuk daun
Macaranga tanarius L. yang halus dengan ukuran partikel lebih kecil dari 300 µm. Ukuran partikel serbuk yang terlalu kecil dikhawatirkan dapat
mengkontaminasi filtrat karena serbuk tersebut dapat menembus filter,
sehingga menyebabkan filtrat menjadi tidak murni.
4. Penetapan kadar air serbuk daun Macaranga tanarius L.
Sebanyak 5,0 gram serbuk kering daun Macaranga tanarius L. yang sudah diayak, dimasukkan ke dalam alat moisture balance. Bobot serbuk kering daun tersebut ditetapkan sebagai bobot sebelum pemanasan (bobot A), setelah
itu dipanaskan pada suhu 105oC. Serbuk kering daun Macaranga tanarius L.
yang sudah dipanaskan ditimbang kembali dan dihitung sebagai bobot setelah
pemanasan (bobot B). Kemudian dilakukan perhitungan terhadap selisih bobot
A terhadap bobot B yang merupakan kadar air serbuk daun Macaranga tanarius
5. Pembuatan ekstrak metanol-air daun Macaranga tanarius L.
Ekstrak metanol-air daun Macaranga tanarius L. dibuat dengan cara mengekstraksi serbuk kering daun Macaranga tanarius L. seberat 40,0 gram yang dilarutkan dalam 200 ml pelarut metanol 50% dimaserasi pada suhu kamar
selama 24 jam menggunakan orbital shaker Optima® dengan putaran 140 rpm. Dilakukan remaserasi sebanyak 2 kali dengan menggunakan volume pelarut
metanol 50% yang sama. Rendaman serbuk disaring menggunakan corong
buchner untuk memisahkan filtrat dari residunya. Filtrat yang diperoleh diuapkan menggunakan rotary vacuum evaporator IKAVAC® dengan suhu 80oC. Ekstrak pekat yang diperoleh diuapkan di oven Memmert® dengan suhu
50oC selama 2-3 hari hingga menjadi ekstrak kental atau hingga memiliki bobot
yang tetap yaitu perbedaan antara dua penimbangan dengan selang waktu 1 jam
berturut-turut tidak lebih dari 0,25%.
6. Pembuatan FHEMM
Ekstrak kental dilarutkan kembali dengan pelarut heksan-etanol 1:1
dengan perbandingan 1:5 yaitu 1 gram ekstrak kental dilarutkan dalam 5 mL
pelarut heksan-etanol, dimaserasi pada suhu kamar selama 24 jam
menggunakan orbital shaker Optima® dengan putaran 140 rpm. Dilakukan remaserasi sebanyak 2 kali dengan menggunaka volume pelarut heksan-etanol
yang sama. Rendaman ekstrak disaring menggunakan corong buchner untuk memisahkan filtrat dengan residunya. Filtrat yang diperoleh diuapkan di oven
hingga memiliki bobot yang tetap yaitu perbedaan antara dua penimbangan
dengan selang waktu 1 jam berturut-turut tidak lebih dari 0,25%.
7. Pembuatan karbon tetraklorida dalam olive oil konsentrasi 50%
Berdasarkan penelitian Janakat dan Al-Merie (2002), larutan karbon
tetraklorida dibuat dengan konsentrasi 50% sehingga perbandingan volume
karbon tetrakloridadengan olive oil adalah 1:1. Hepatotoksin berupa karbon tetraklorida dilarutkan didalam olive oil Bertoli® dengan volume yang sama.
8. Pembuatan larutan CMC-Na 1%
Suspending agent CMC-Na 1% dibuat dengan cara menimbang
sebanyak 5,0 gram serbuk CMC-Na, kemudian dilarutkan menggunakan
aquadest 400,0 mL dan didiamkan selama 24 jam hingga CMC-Na mengembang. Larutan tersebut kemudian diadd dengan aquadest hingga 500,0 mL pada labu ukur 500,0 mL.
9. Pembuatan suspensi FHEMM dalam CMC-Na 1 %
Suspensi FHEMM dibuat dengan konsentrasi 2,4 %. Sebanyak 0,6
gram FHEMM ditimbang secara seksama kemudian dilarutkan dengan larutan
CMC-Na 1% hingga terlarut seluruhnya. Suspensi FHEMM dimasukkan ke
dalam labu takar 25 mL, dan diadd dengan larutan CMC-Na 1% hingga batas tanda, kemudian suspensi FHEMM digojog hingga homogen.
10. Uji pendahuluan
a. Penetapan dosis hepatotoksin karbon tetraklorida
Penetapan dosis hepatotoksin karbon tetraklorida didasarkan pada
penelitian tersebut dijelaskan bahwa karbon tetraklorida yang dilarutkan
dalam olive oil 1:1 dengan dosis 2 mL/kgBB dapat menginduksi kerusakan hati pada tikus galur Wistar. Dosis tersebut dapat menyebabkan kerusakan
pada sel-sel hati yang ditunjukkan melalui peningkatan aktivitas AST dan
ALT, tetapi tidak menyebabkan kematian pada tikus galur Wistar.
b. Penetapan waktu pencuplikan darah
Penetapan waktu pencuplikan darah dilakukan melalui orientasi.
Orientasi dilakukan pada tiga kelompok perlakuan waktu, yaitu jam ke-0
sebelum pemberian hepatotoksin karbon tetraklorida 50%, jam ke-24 dan
ke-48 setelah pemberian hepatotoksin karbon tetraklorida 50% secara
intraperitoneal. Setiap kelompok perlakuan waktu terdiri dari
masing-masing tiga ekor tikus. Pencuplikan darah dilakukan melalui sinus orbitalis
mata tikus dan kemudian diukur aktivias AST dan ALT. Berdasarkan
penelitian Janakat dan Al-Merie (2002), peningkatan aktivitas AST dan
ALT pada tikus terinduksi karbon tetraklorida yang dilarutkan dalam olive oil 1:1 dengan dosis 2 mL/kgBB mencapai peningkatan maksimal pada jam ke-24 setelah induksi, dan pada jam ke-48 perlahan menurun.
11. Pengelompokan dan perlakuan hewan uji
Hewan uji tikus betina galur Wistar dibagi acak menjadi 6 kelompok,
masing-masing 5 ekor. Pengelompokan tersebut sebagai berikut :
a. Kelompok I (Kelompok kontrol hepatotoksin karbon tetraklorida). Hewan
jam ke-24 setelah pemberian larutan karbon tetraklorida, dilakukan
pencuplikan darah untuk diukur aktivitas ALP.
b. Kelompok II (Kelompok kontrol negatif CMC-Na 1%). Hewan uji
diberikan larutan CMC-Na 1% secara peroral selama enam hari
berturut-turut. Pada jam ke-24 setelah pemberian larutan CMC-Na 1%, dilakukan
pencuplikan darah untuk diukur aktivitas ALP.
c. Kelompok III (Kelompok kontrol dosis 137,14 mg/kgBB FHEMM). Hewan
uji diberikan suspensi FHEMM secara peroral selama enam hari
berturut-turut. Pada jam ke-24 setelah pemberian suspensi FHEMM, dilakukan
pencuplikan darah untuk diukur aktivitas ALP.
d. Kelompok IV ( Kelompok dosis 34,28 mg/kgBB FHEMM). Hewan uji
diberikan suspensi FHEMM secara peroral selama enam hari berturut-turut.
Pada jam ke-24 setalah pemberian suspensi FHEMM, hewan uji diberikan
larutan karbon tetraklorida 50% secara intraperitoneal. Setelah 24 jam,
dilakukan pencuplikan darah untuk diukur aktivitas ALP.
e. Kelompok V (Kelompok dosis 68,57 mg/kgBB FHEMM). Hewan uji
diberikan suspensi FHEMM secara peroral selama enam hari berturut-turut.
Pada jam ke-24 setalah pemberian suspensi FHEMM, hewan uji diberikan
larutan karbon tetraklorida 50% secara intraperitoneal. Setelah 24 jam,
dilakukan pencuplikan darah untuk diukur aktivitas ALP.
f. Kelompok VI (Kelompok dosis 137,14 mg/kgBB FHEMM). Hewan uji
diberikan suspensi FHEMM secara peroral selama enam hari berturut-turut.