AKTIVITAS REAKSI HIDRORENGKAH KATALIS Ni/ZAA (ZEOLIT ALAM AKTIF), Mo/ZAA, NiMo/ZAA
TERHADAP PARAFIN
Siswodiharjo.(1), Khoirina Dwi N.(2), Dian Maruto W.(3)
(1)
Mahasiswa Jurusan Kimia, FMIPA, UNS, Surakarta
(2)
Pembimbing 1 dan Dosen Jurusan Kimia, FMIPA, UNS, Surakarta
(3)
Pembimbing 2 dan Dosen Jurusan Kimia, FMIPA, UNS, Surakarta
ABSTRAK
Telah dilakukan uji aktivitas hidrorengkah katalis logam Ni dan Mo yang teremban pada zeolit terhadap parafin. Penelitian ini bertujuan untuk menentukkan keefektifan katalis dan pengaruh jenis katalis logam Ni dan Mo yang teremban pada zeolit dalam reaksi hidrorengkah parafin. Katalis logam Ni yang teremban pada zeolit memiliki aktivitas katalis, selektivitas fraksi ringan dan konversi total yang lebih baik dibandingkan Katalis logam Ni yang teremban pada zeolit.
Uji aktivitas katalis dilakukan pada reaktor sistem alir dengan rasio katalis dan umpan 1:5, temperatur reaksi 400oC dan kecepatan alir gas H2 30 ml/menit Keefektifan katalis ditentukkan berdasarkan data kromatografi gas (Gas
chromatography = GC ) hasil hidrorengkah dibandingkan dengan data GC parafin
awal dengan waktu retensi paling pendek.
Hasil penelitian menunjukkan bahwa aktivitas aktivitas katalis dan konversi total terbaik diperoleh pada katalis ZAA yaitu sebesar 61.25 % dan 62.59 % sedangkan selektivitas fraksi ringan terbaik diperoleh pada katalis Ni/ZAA yaitu sebesar 11.15 % pada hidrorengkah parafin.
Kata kunci : Aktivitas, hidrorengkah parafin , katalis ZAA, katalis Ni/ZAA
A. Pendahuluan
Bahan bakar minyak merupakan bahan bakar utama saat ini, namun minyak bumi yang digunakan secara terus menerus akan
habis karena jumlahnya yang terbatas. Salah satu solusi untuk mengatasi masalah ini dengan memanfaatkan kembali fraksi berat
tertentu sehingga menjadi fraksi ringan.
Salah satu solusi untuk mengatasi masalah ini dengan memanfaatkan kembali fraksi berat tertentu sehingga menjadi fraksi ringan.
Beberapa penelitian yang menggunakan senyawa karbon dalam bentuk fraksi berat antara lain: Nasution (1999), telah melakukan reaksi hidrorengkah minyak berat diesel (diesel oil) dengan katalis Ni-Mo/Al2O3-SiO2. Salah satu fraksi hasil hidrorengkahnya adalah rangkaian senyawa hidrokarbon dengan 1 cincin lingkar. Ginanjar (2002), melakukan hidrorengkah tir batubara menjadi fraksi bensin menggunakan katalis Cr/ZAAH. Trisunaryanti (1995), telah melakukan hidrorengkah parafin dengan menggunakan katalis krom yang teremban pada zeolit alam. Reaksi hidrorengkah adalah proses pemecahan ikatan karbon-karbon pada hidrokarbon yang mempunyai berat molekul besar (rantai molekul panjang) menjadi hidrokarbon dengan berat molekul
rendah (rantai molekul pendek) dengan dibantu adanya gas H2
Parafin merupakan senyawa hidrokarbon yang sangat potensial untuk dikonversi menjadi fraksi yang ringan karena parafin mengandung senyawa-senyawa hidrokarbon dengan jumlah atom karbon per molekul dalam parafin sekitar 20-36 atom sehingga sangat mungkin untuk digunakan sebagai umpan dalam reaksi hidrorengkah.
Katalis dengan aktivitas hidrorengkah katalitik yang tinggi mempunyai kriteria sifat-sifat umum dalam penggunaannya seperti aktif, stabil, sensitif terhadap perubahan panas, mudah diregenerasi dan mempunyai kekuatan mekanik (Herukodri, 1990). Sifat tersebut dapat dipenuhi oleh katalis sistem logam pengemban. Logam-logam yang sering digunakan adalah logam-logam transisi.
Salah satu katalis logam transisi yang telah banyak digunakan pada industri kimia adalah Nikel (Ni). Katalis nikel yang diembankan pada pengemban digunakan sebagai katalis hidrogenasi yang dapat
mengubah etana menjadi etilen (Heracleous dan Lemonidou, 2003). Logam transisi lainnya yang juga banyak digunakan sebagai katalis adalah Molibdenum (Mo). Molibdenum yang diemban pada pengemban berfungsi sebagai katalis hidrorengkah dan desulfurisasi pada berbagai model reaksi (Egorova, 2003).
Kriteria pemilihan bahan pengemban perlu memperhatikan sifat-sifat antara lain adalah memiliki sifat inert, stabilitas termal tinggi,
memiliki rongga yang
memungkinkan terjadinya adsorpsi, mempunyai kemampuan untuk mengikat logam sebagai katalis dan memiliki luas permukaan yang besar karena reaksi yang terjadi selama proses katalitik berlangsung pada permukaan. Salah satu bahan pengemban yang sering digunakan adalah zeolit (Augustine, 1996). Syarifah et al (2001), menggunakan katalis pengembanan dengan terlebih dulu melakukan aktivasi dengan kalsinasi yang dialiri gas N2 pada suhu 500oC, oksidasi dengan gas O2 pada suhu 400oC dan direduksi dengan aliran
gas H2 pada suhu 400oC dan dimodifikasi terlebih dahulu.
Pengembanan logam transisi pada suatu pengemban dapat juga meningkatkan selektivitas katalis (Satterfield, 1980).
Fitrianto (2005), telah melakukan pengembanan logam Ni-Mo pada zeolit alam aktif dalam katalis monometal dan bimetal dengan metode impregnasi. Hasil penelitian menunjukkan bahwa pengembanan dengan satu jenis logam (monometal) lebih efektif dibandingkan pengembanan dua jenis logam (bimetal) yang ditunjukkan dengan kandungan logam dan keasaman total yang paling tinggi pada katalis monometal yaitu 1,190 (b/b) dan 1,176 % mmol/gram.
Mengacu pada pemaparan di atas bahwa senyawa dengan berat molekul lebih besar dapat diubah menjadi lebih kecil serta untuk mengetahui aktivitas katalis logam Ni dan Mo yang teremban pada zeolit yang telah dilakukan Fitrianto (2005) maka dilakukan penelitian dengan senyawa model parafin. Pemilihan parafin sebagai senyawa
model reaksi hidrorengkah didasarkan pada adanya proses pemutusan untuk menghasilkan molekul parafin yang lebih kecil.
B. Metodologi Penelitian A. Karakterisasi Parafin
Karakterisasi parafin dilakukan dengan mengambil sampel parafin secukupnya untuk analisis Kromatografi Gas, Spektroskopi massa dan Spektroskopi Inframerah di Laboratorium Kimia Organik Universitas Gadjah Mada Yogyakarta.
B. Uji Aktivitas
1). Hidrorengkah Umpan Tanpa Katalis (Hidrorengkah Termal)
Proses hidrorengkah umpan dilakukan dengan reaktor sistem alir, tanpa menggunakan katalis. Umpan sebanyak 5 g dimasukkan ke dalam reaktor umpan. Reaktor katalis dipanaskan pada suhu 400 °C, dan setelah panasnya konstan, reaktor umpan dipanaskan sampai umpan menguap sambil dialiri gas H2 dengan laju alir 30 mL/menit. Proses hidrorengkah dilakukan sampai CHH (Cairan Hasil Hidrorengkah) tidak
menetes lagi. Hasil hidrorengkah kemudian dilewatkan pada sistem pendingin berupa campuran es dan garam, dan ditampung dalam penampung. Hasil hidrorengkah yang diperoleh disebut Cairan Hasil Hidrorengkah (CHH).
2). Hidrorengkah Umpan dengan Beberapa Katalis (Hidrorengkah Katalitik)
a. Hidrorengkah umpan dengan katalis Zeolit Alam Aktif (ZAA)
Proses hidrorengkah umpan dilakukan dengan reaktor sistem alir, dengan katalis dan umpan (feed) diletakkan pada reaktor yang berbeda. Katalis ZAA sebanyak 1 g diletakkan dalam reaktor katalis dan 5 g umpan dimasukkan ke dalam reaktor umpan. Reaktor katalis dipanaskan pada suhu 400 °C, dan setelah panasnya konstan, reaktor umpan dipanaskan sampai umpan menguap sambil dialiri gas H2 dengan laju alir 30 mL/menit. Proses hidrorengkah dilakukan samapai CHH tidak menetes lagi. Hasil hidrorengkah kemudian dilewatkan pada sistem pendingin berupa
campuran es dan garam, dan ditampung dalam penampung.
b. Hidrorengkah umpan dengan katalis Ni/Zeolit Alam Aktif (ZAA)
Analog dengan langkah pada hidrorengkah umpan pada 2a, hanya saja katalis ZAA diganti dengan katalis Ni/ZAA.
c. Hidrorengkah umpan dengan katalis Mo/Zeolit Alam Aktif (ZAA)
Analog dengan langkah pada hidrorengkah umpan pada 2a, hanya saja katalis ZAA diganti dengan katalis Mo/ZAA.
c. Hidrorengkah umpan dengan katalis NiMo/Zeolit Alam Aktif (ZAA)
Analog dengan langkah pada hidrorengkah umpan pada 2a, hanya saja katalis ZAA diganti dengan katalis NiMo/ZAA.
C. Hasil Penelitian Karakterisasi Parafin a. Fisik
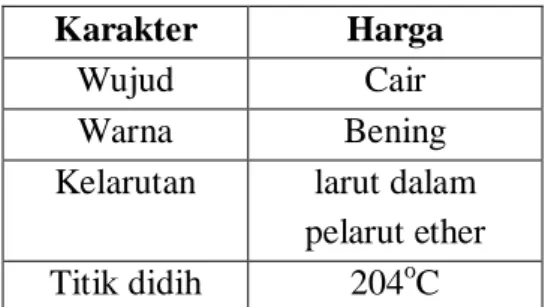
Karakter fisik parafin meliputi bentuk, warna, kelarutan, dan titik didih . Data mengenai sifat fisik parafin ditunjukan oleh Tabel 1.
Tabel 1. Karakter fisik parafin
Karakter Harga
Wujud Cair
Warna Bening
Kelarutan larut dalam pelarut ether Titik didih 204oC
Dari tabel 1 menunjukkan bahwa senyawa parafin memiliki rantai karbon yang panjang. Hal ini dapat dilihat dari titik didihnya yang tinggi yaitu ± 204 oC.
b. Kimia
Karakter kimia parafin meliputi komposisi senyawa, gugus fungsi dan jenis senyawa. Data mengenai sifat kimia parafin ditunjukan oleh Tabel 2 dan dapat dilihat pada Lampiran 1.
Tabel 2. Jenis gugus fungsional yang terdapat pada parafin
Gambar 1. Hasil analisis IR Parafin Serapan yang tajam terdapat pada kisaran bilangan gelombang 2853-2962 cm-1, ialah gugus C-H pada alkana. Puncak serapan pada kisaran 2500-2750 cm-1 menunjukkan adanya gugus S-H. Puncak serapan pada ~ 2400 cm-1 menunjukkan adanya serapan nitrogen (NH2). Puncak serapan pada kisaran 1450-1600 cm-1 menunjukkan adanya gugus C-C. Puncak serapan pada 800-1000 cm-1 menunjukkan adanya serapan C=C (alkena). Puncak serapan pada ~ 722 cm-1 menunjukkan adanya gugus -(CH2)n. Hal ini dimungkinkan karena parafin yang digunakan adalah parafin campuran.
Gambar 2. Kromatogram Parafin
Berdasarkan kromatogram diatas terdapat 9 senyawa pada range 3.348 menit sampai 25.683 menit dimana pada waktu retensi 3.348 menit merupakan pelarut sedangkan pada range 22.070 menit sampai 25.683 menit dengan 8 senyawa yang terdapat dalam parafin.
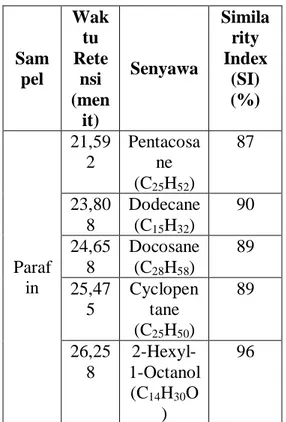
Hasil analisis Spektroskopi Massa pada parafin disajikan pada Tabel 3
Tabel 3. Komposisi Senyawa dalam Parafin Sam pel Wak tu Rete nsi (men it) Senyawa Simila rity Index (SI) (%) Paraf in 21,59 2 Pentacosa ne (C25H52) 87 23,80 8 Dodecane (C15H32) 90 24,65 8 Docosane (C28H58) 89 25,47 5 Cyclopen tane (C25H50) 89 26,25 8 2-Hexyl-1-Octanol (C14H30O ) 96
Selain mengandung senyawa diatas juga mengandung senyawa asam oktadekanoat, 1-clorooctadekana,
2-hexyl-1-decanol, 2-hexyl-1-octanol, dan acetamida
Analisis untuk mengetahui jenis senyawa yang ada dalam parafin, dilakukan analisis Spektroskopi Massa pada 5 puncak senyawa yaitu pada waktu retensi 21,592; 23,808; 24,658; 25,475; dan 26,258 menit. Analisis Spektroskopi Massa pada waktu retensi diatas adalah untuk mengetahui jenis senyawa dengan berat molekul lebih besar dalam parafin, semua waktu retensi diatas menunjukkan puncak yang lebih tinggi dibandingkan puncak lainnya. Hasilnya dapat dilihat pada tabel 3. Dari data spektra diatas masih belum dipastikan bahwa data yang diperoleh maksimal. Hal ini disebabkan pada puncak – puncak yang dianalisis belum terpisah dengan baik, juga dimungkinkan karena sampel yang digunakan masih dalam bentuk campuran parafin. Berdasarkan analisis fisik dan kimia menggunakan alat Spektroskopi Inframerah, Kromatografi gas dan spektroskopi massa menunjukkan bahwa senyawa umpan yang digunakan adalah Parafin.
2. Karakterisasi Parafin Hasil Uji Katalitik
Uji katalitik pada proses hidrorengkah parafin dilakukan secara termal dan katalitik. Pada reaksi hidrorengkah katalitik menggunakan katalis ZAA, Ni/ZAA, Mo/ZAA dan Ni-Mo/ZAA.
a. Fisik
Uji katalitik menghasilkan Cairan Hasil Hidrorengkah (CHH), gas dan kokas. Data karakter fisika parafin hasil uji katalitik dapat dilihat pada tabel 4.
Tabel 4. Karakter fisika parafin hasil uji katalitik
Karakter Harga
Bentuk Cair
Warna Putih kekuningan Kelarutan larut dalam
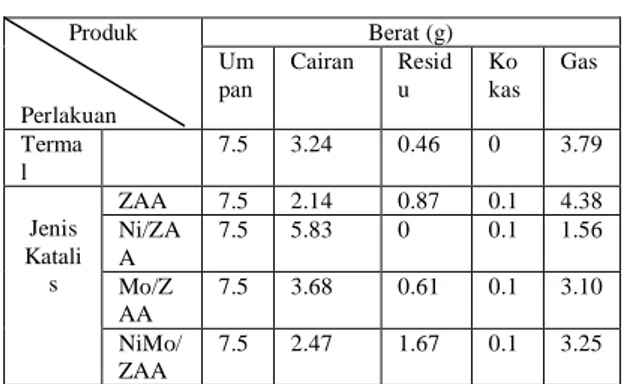
pelarut ether Dari tabel diatas menunjukkan bahwa produk cair yang dihasilkan berbeda dengan umpan, hal ini dapat dilihat dari warna yang berbeda dan diperoleh produk lain yaitu kokas. Data hasil uji katalitik diperlihatkan pada Tabel 5
Tabel 5. Hasil uji katalitik Produk Perlakuan Berat (g) Um pan Cairan Resid u Ko kas Gas Terma l 7.5 3.24 0.46 0 3.79 Jenis Katali s ZAA 7.5 2.14 0.87 0.1 4.38 Ni/ZA A 7.5 5.83 0 0.1 1.56 Mo/Z AA 7.5 3.68 0.61 0.1 3.10 NiMo/ ZAA 7.5 2.47 1.67 0.1 3.25 Hasil penelitian juga menunjukkan bahwa proses hidrorengkah termal dan katalitik, selain dihasilkan kokas dan gas, dihasilkan pula CHH dalam jumlah yang bervariasi pada variasi jenis katalis. Pengaruh jenis katalis terhadap terbentuknya CHH, kokas dan gas dari hidrorengkah parafin ditunjukkan oleh grafik pada Gambar 3 .
Gambar 3. Pengaruh Jenis Katalis terhadap Konversi CHH
Dari grafik dalam Gambar 10. Terlihat bahwa pada proses hidrorengkah menggunakan katalis Ni/ZAA menghasilkan CHH yang relatif lebih banyak dibandingkan katalis lain. Pada proses hidrorengkah dengan katalis ini
dihasilkan gas dan kokas yang lebih rendah. Karakter katalis Ni/ZAA memiliki keasaman total yang tinggi yang berarti bahwa situs asam aktif semakin banyak, sehingga proses hidrorengkah parafin akan semakin mudah berlangsung.
Gambar 4. Pengaruh Jenis Katalis terhadap Konversi Gas
Katalis ZAA menghasilkan produk gas yang lebih banyak dan produk CHH dan kokas lebih rendah. Hal ini didukung oleh karakter katalis ZAA memiliki luas permukaan paling besar yang diharapkan pusat aktif katalis akan semakin banyak sehingga aktivitas katalis akan meningkat dan gas mudah teradsorpsi pada permukaan katalis.
Gambar 5. Pengaruh Jenis Katalis terhadap Konversi Kokas
Pengaruh Jenis Katalis terhadap Konversi CHH 0 5 10 15 Tanpa katalis ZAA Ni / ZAA Mo / ZAA Ni-Mo / ZAA Jenis Katalis K o n v e rs i (% )
Pengaruh Jenis Katalis terhadap Konversi Kokas 0 0,5 1 1,5 T a n p a k a ta lis Z A A N i / Z A A M o / Z A A N i-M o / Z A A Jenis Katalis K o n v e rs i (% )
Pengaruh Jenis Katalis terhadap Koversi Gas
0 10 20 30 40 50 60 70 Tanpa katalis ZAA Ni / ZAA Mo / ZAA Ni-Mo / ZAA Jenis Katalis K o n v e rs i (% )
Data hasil penelitian menunjukkan juga adanya konversi kokas yang relatif konstan untuk semua jenis katalis.
b. Kimia
Analisis kimia dapat dilihat dari pengaruh kandungan logam Ni dan Mo terhadap efektivitas katalis menggunakan katalis ZAA sebagai pembanding. Analisis dilakukan dengan cara membandingkan kromatogram sampel parafin dengan kromatogram cairan hasil hidrorengkah katalitik, Hasil hidrorengkah parafin dengan berbagai katalis dapat dilihat pada tabel 4 berdasarkan hasil perhitungan dari lampiran 1.
1). Hidrorengkah Parafin Tanpa Katalis (Hidrorengkah termal)
Adanya senyawa produk hidrorengkah diketahui dengan munculnya puncak kromatogram baru yang memiliki masa relatif yang lebih rendah daripada umpan yang diberikan yaitu Parafin. Profil perbandingan kromatogram parafin dan kromatogram cairan hasil hidrorengkah tanpa katalis seperti terlihat pada Gambar 5. Berdasarkan
gambar 5 cairan hasil hidrorengkah tanpa katalis menunjukkan adanya perubahan waktu retensi kromatogram hasil hidrorengkah dengan kromatogram awal. Hal ini ditandai dengan bertambahnya senyawa yang mempunyai waktu retensi pada range 3.077 menit sampai 19.087 menit.
Gambar 6. Kromatogram a) Parafin b)
CHHtermal pada temperatur 400 oC
Grafik pada gambar 6, juga menunjukkan bahwa pada waktu retensi 22.07 menit sampai 25.683 menit mengalami penambahan luas distribusi senyawa dari distribusi normal senyawa mula-mula menjadi ada penambahan senyawa di waktu retensi rendah. Berdasarkan kromatogram pada gambar 6, pada range 3.077 menit sampai 4.492 menit yang diasumsikan sebagai range fraksi bensin, memiliki selektivitas pembentukan hasil yang rendah yaitu sebesar 5.42 %. Hal ini ditandai adanya distribusi senyawa
mV
a b
yang melebar di sebelah kanan kromatogram yang kurang baik dengan sedikit senyawa yang masuk kedalam range fraksi bensin.
2). Hidrorengkah Parafin dengan Katalis (Hidrorengkah Katalitik) a. Hasil hidrorengkah dengan katalis ZAA
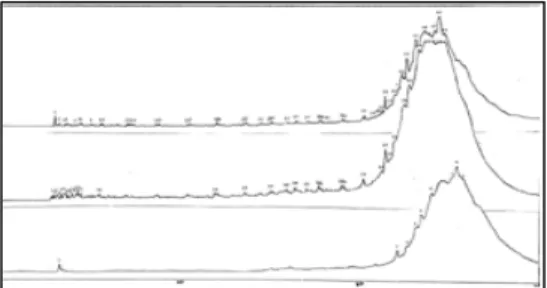
Profil perbandingan kromatogram parafin dan akromatogram cairan hasil hidrorengkah dengan menggunakan katalis ZAA terlihat pada Gambar 7.
Gambar 7. Kromatogram a) Parafinb) CHHZAA dan c) CHHTanpa katalis
pada temperatur 400 oC
Berdasarkan gambar 6 bahwa hasil hidrorengkah dengan katalis ZAA menunjukan terjadinya perubahan waktu retensi yang ditandai dengan bertambahnya senyawa pada range 2.834 menit sampai 18.755 menit serta ada perubahan distribusi senyawa range 19.844 menit sampai 24.085 menit yang semula distribusi normal,
menjadi ada penambahan senyawa yang cukup melimpah pada waktu retensi 21.558 menit sampai 24.085 menit.
Hasil hidrorengkah dengan katalis ZAA mengalami penambahan jumlah senyawa pada waktu retensi rendah relatif lebih banyak dibandingkan dengan perengkahan hidrogen termal yaitu pada range waktu retensi 2.833 menit sampai 4.352 menit. Katalis ZAA juga memiliki selektivitas pembentukan hasil yang lebih baik pada range 2.834 menit sampai 4.352 menit yaitu sebesar 7.52 % dimana pada range waktu retensi ini dianggap sebagai range fraksi bensin.
Perbandingan aktivitas katalis ZAA dengan katalis termal dapat dilihat dari waktu retensi terjauh pada masing-masing kromatogram CHHnya, yaitu 24.085 menit untuk katalis ZAA dan 24.075 menit untuk katalis termal. Hasil ini menunjukkan bahwa aktivitas katalis ZAA lebih baik daripada katalis termal karena mampu merengkahkan parafin dengan hasil yang lebih baik (waktu retensi lebih pendek).
Jika dibandingkan masing-masing senyawa kromatogram
CHHZAA dengan senyawa kromatogram CHHtanpa katalis, terdapat dua senyawa dengan waktu retensi yang sama yaitu pada waktu retensi 21.043 menit dan 22.278 menit. Hal ini berarti bahwa senyawa tersebut terbentuk karena pengaruh temperatur dan adanya gas H2.
b. Hasil hidrorengkah
menggunakan katalis Ni/ZAA Hasil hidrorengkah menggunakan katalis Ni/ZAA menunjukkan penambahan senyawa pada range 2.916 menit sampai 19.194 menit. Selain itu terdapat perubahan distribusi senyawa pada range 20.278 menit sampai 24.867 menit. Hasil hidrorengkah dengan katalis Ni/ZAA dibandingkan katalis ZAA dan hidrorengkah termal mengalami penambahan sejumlah senyawa pada range 2.916 menit sampai 7.433 menit sedangkan distribusi senyawa katalis Ni/ZAA mirip dengan distribusi senyawa pada hidrorengkah termal tetapi memiliki luas distribusi senyawa pada range 20.278 menit sampai 24.867 menit yang lebih kecil dari distrubusi senyawa hidrorengkah
menggunakan katalis ZAA. Disamping itu katalis Ni/ZAA juga memiliki selektivitas pembentukan hasil pada range yang dianggap sama dengan range fraksi bensin yaitu 2.916 menit sampai 4.816 menit yang paling baik yaitu sebesar 11.15 %.
Pada penelitian ini ditambahkan data penunjang berupa Spektroskopi Inframerah pada CHHNi/ZAA untuk mengetahui lebih jauh tentang perubahan yang terjadi setelah dilakukannya hidrorengkah.
Gambar 8. Spektra inframerah
CHHNi/ZAA dan Parafin
Dari spektra diatas menunjukkan terjadi perubahan intensitas yang mengindikasikan pula adanya proses hidrorengkah dengan katalis CHHNi/ZAA hal ini juga dapat dilihat dengan adanya sebagian puncak spektra lain yang mengalami pergeseran serapan tanpa terjadi perubahan pada gugus fungsional
yang terdapat dalam sampel CHHNi/ZAA
Profil perbandingan kromatogram parafin dan kromatogram cairan hasil hidrorengkah dengan menggunakan katalis Ni/ZAA terlihat pada gambar 7 dan dapat dilihat pada Gambar 14 dan dapat dilihat pada Lampiran 4 dan 7.
Gambar 9. Kromatograma)Parafin b) CHHZAA c) CHHTanpa katalis d)
CHHNi/ZAA pada temperatur
400 oC
Perbandingan aktivitas katalis Ni/ZAA dengan katalis ZAA dapat dilihat dari waktu retensi terjauh pada masing-masing kromatogram CHHnya, yaitu 24.867 menit untuk katalis Ni/ZAA dan 24.085 menit untuk katalis termal. Hasil ini menunjukkan bahwa aktivitas katalis ZAA lebih baik daripada katalis Ni/ZAA karena mampu merengkahkan parafin dengan hasil yang lebih baik (waktu retensi lebih kecil). Hal ini didukung oleh data karakter katalis ZAA
dimana harga luas permukaan spesifik lebih tinggi daripada katalis Ni/ZAA sehingga kontak reaktan dengan katalis lebih maksimal.
Jika dibandingkan masing-masing senyawa kromatogram CHHZAA dengan senyawa kromatogram CHHtanpa katalis, tidak terdapat senyawa dengan waktu retensi yang sama. Hal ini berarti bahwa senyawa tersebut terbentuk tanpa pengaruh temperatur dan adanya gas H2.
c. Hasil hidrorengkah menggunakan katalis Mo/ZAA
Hasil hidrorengkah parafin dengan menggunakan katalis Mo/ZAA menunjukkan adanya penurunan aktivitas katalis pada proses hidrorengkah bila dibandingkan dengan hasil hidrorengkah dengan katalis Ni/ZAA meskipun mengalami penambahan senyawa pada range 2.951 menit sampai 19.192 menit. dibanding dengan parafin awal. Disamping itu juga terdapat penambahan distribusi senyawa pada range 20.192 menit sampai 24.767 menit yang semula distribusi normal, menjadi ada penambahan senyawa pada waktu retensi yang rendah.
Gambar 10. Kromatogram a) CHHparafin b)
CHHMo/ZAA c) CHHZAA d) CHHTanpa katalis
pada temperatur 400 oC
Hidrorengkah dengan katalis ini juga menghasilkan selektivitas pembentukan hasil yang paling rendah pada range yang diasumsikan sama dengan range fraksi bensin yaitu 2.951 menit sampai 4.861 menit dibandingkan katalis yang lain yaitu sebesar 4.05 %.
Perbandingan aktivitas katalis Mo/ZAA dengan katalis ZAA dapat dilihat dari waktu retensi terjauh pada masing-masing kromatogram CHHnya, yaitu 24.767 menit untuk katalis Mo/ZAA dan 24.085 menit untuk katalis termal. Hasil ini menunjukkan bahwa aktivitas katalis ZAA lebih baik daripada katalis
Mo/ZAA karena mampu
merengkahkan parafin dengan hasil yang lebih baik (waktu retensi lebih kecil). Hal ini didukung oleh data karakter katalis ZAA dimana harga luas permukaan spesifik lebih tinggi daripada katalis Mo/ZAA.
Jika dibandingkan masing-masing senyawa kromatogram CHHMo/ZAA dengan senyawa kromatogram CHHtanpa katalis, terdapat 3 senyawa dengan waktu retensi yang sama yaitu 4.176, 4.494 menit dan 12.095 menit. Hal ini berarti bahwa senyawa tersebut terbentuk karena pengaruh temperatur dan adanya gas H2 sedangkan ZAA kurang berpengaruh pada katalis ini.
c. Hasil hidrongkah menggunakan katalis Ni-Mo/ZAA
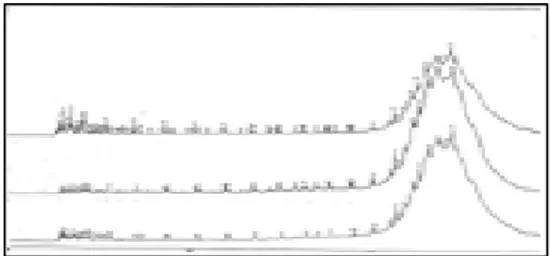
Gambar 11. Perbandingan Spiking dengan senyawa C5 dan C6 : a. Polipropilene b.
Parafin
Berdasarkan Gambar 8 yang terdapat pada Lampiran yang menunjukkan bahwa waktu retensi untuk senyawa C5 dan C6 pada parafin diasumsikan terdapat pada waktu retensi 2.283 menit dan 2.528 menit sedangkan pada propilene terdapat pada waktu retensi 3.263 menit dan 3.983 menit. Perbedaan
a
waktu retensi antara waktu retensi senyawa C5 dan C6 pada parafin dan propilene disebabkan oleh penggunaan pelarut yang berbeda dimana adanya pelarut ini akan menurunkan waktu retrensi dari senyawa C5 dan C6 pada parafin.
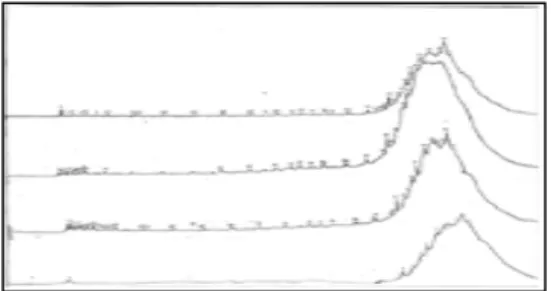
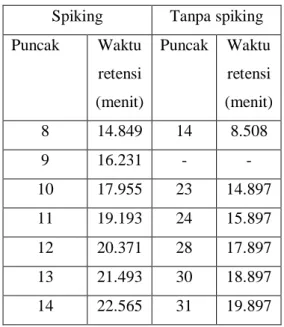
Gambar 12. Perbandingan Kromatogram hidrorengkah parafin: a. Spiking b. Tanpa spiking
Senyawa yang diasumsikan sama tetapi berbeda waktu retensi pada data GC dengan spiking dan tanpa spiking disebabkan perbedaan kondisi operasi pada suhu awal dan akhir kolom pada alat GC. Data senyawa tersebut dapat dilihat pada Tabel 5.
Tabel 5. Perbandingan senyawa yang ada pada data GC dengan spiking dan tanpa spiking
Spiking Tanpa spiking
Puncak Waktu retensi (menit) Puncak Waktu retensi (menit) 8 14.849 14 8.508 9 16.231 - - 10 17.955 23 14.897 11 19.193 24 15.897 12 20.371 28 17.897 13 21.493 30 18.897 14 22.565 31 19.897
Hasil hidrorengkah dengan katalis Ni-Mo/ZAA juga menunjukkan adanya peningkatan aktivitas katalis dibandingkan katalis Ni/ZAA dan Mo/ZAA dimana jumlah senyawa pada range 2.897 menit sampai 18.883 menit lebih banyak dibandingkan hasil hidrorengkah dengan menggunakan katalis Ni/ZAA dan Mo/ZAA. Selektivitas pembentukan hasil pada range yang diasumsikan sama dengan range fraksi bensin yaitu 2.897 menit sampai 4.433 menit menunjukkan selektivitas yang lebih besar dibandingkan dengan hidrorengkah menggunakan katalis Mo/ZAA dan hidrorengkah namun selektivitasnya lebih rendah bila dibandingkan dengan perengkahan hidrogen dengan katalis Ni/ZAA dan katalis ZAA. Hal ini mungkin a
disebabkan karena katalis Ni-Mo/ZAA memiliki keasaman total yang paling rendah sehingga aktivitas katalisnya menurun
Gambar 13. Kromatogram a) CHHMo/ZAA b)
CHHNiMo/ZAA c) CHHNi/ZAA
pada temperatur 400 oC. Jika dibandingkan masing-masing senyawa kromatogram CHHNiMo/ZAA dengan senyawa kromatogram CHHMo/ZAA, terdapat satu senyawa dengan waktu retensi yang sama yaitu 4.177 menit. Hal ini berarti bahwa senyawa tersebut terbentuk karena pengaruh logam Mo sedangkan logam Ni kurang berpengaruh pada katalis ini.
Pengaruh jenis katalis terhadap konversi total dan aktivitas katalis dalam hidrorengkah parafin disajikan dengan grafik pada gambar 14.
Gambar 14.Pengaruh Jenis Katalis terhadap Konversi Total
Gambar 15.Pengaruh Jenis Katalis terhadap Aktivitas Katalis
Berdasarkan grafik dalam gambar 14 dan 15 menunjukkan bahwa konversi total perengkahan hidrogen parafin menggunakan katalis ZAA lebih besar dibandingkan proses perengkahan hidrogen parafin menggunakan katalis lain, dalam hal ini terlihat bahwa pengembanan logam kurang berperan dalam meningkatkan Konversi total katalis. Katalis ZAA juga memiliki aktivitas katalis yang paling besar dibandingkan katalis lain, hal ini disebabkan katalis ZAA memiliki luas permukaan spesifik dan volume pori yang paling tinggi sehingga reaksi hidrorengkah berjalan maksimal.
Pengaruh Jenis Katalis terhadap Konversi Total
0 20 40 60 80 T a n p a Ka ta lis Z AA N i/ Z AA M o /Z AA N i-M o /Z AA Jenis Katalis K o n v e rs i (% )
Pengaruh Jenis Katalis terhadap Aktivitas Katalis 0 20 40 60 80 T a n p a K a ta lis Z A A N i/ Z A A M o /Z A A N i-M o /Z A A Jenis Katalis A k ti v it a s ( % )
Gambar 16.Pengaruh Jenis Katalis terhadap Selektivitas Fraksi ringan
Berdasarkan gambar 16 terlihat bahwa pada proses hidrorengkah menggunakan katalis Ni/ZAA diperoleh distribusi luas puncak paling baik dengan banyak puncak yang masuk ke dalam range fraksi bensin. Munculnya puncak-puncak tersebut menandakan bahwa katalis ini mempunyai selektivitas yang lebih baik dibanding katalis lain.
Efektivitas katalis Ni/ZAA menunjukkan hasil yang terbaik dengan persen range fraksi bensin sebesar 11.15 %. Dengan demikian berdasarkan selektivitas fraksi bensin diketahui bahwa katalis dengan kandungan logam Ni dan Mo paling tinggi (1.198 %) memberikan hasil hidrorengkah yang paling baik pada proses hidrorengkah parafin pada temperatur 400oC..
KESIMPULAN
Proses hidrorengkah parafin dan toluen menggunakan katalis ZAA, Ni/ZAA, Mo/ZAA dan Ni-Mo/ZAA dapat disimpulkan sebagai berikut :
1. Pengembanan logam Ni dan Mo pada zeolit alam aktif dapat digunakan sebagai katalis pada hidrorengkah parafin dan toluen memiliki aktivitas katalis dan konversi total yang berbeda-beda. 2. Katalis ZAA mempunyai
konversi total serta aktivitas katalis terbaik sebesar 62.59 % dan 61,25 % serta katalis Ni/ZAA memiliki selektivitas fraksi ringan terbaik yaitu sebesar 11.15 % pada proses hidrorengkah parafin.
DAFTAR PUSTAKA
Aderson , J.R and Boudart , M. 1981.
Catalysis: Science and
Technology. Vol. 1,
Springer. Verlag. New York
Pengaruh Jenis Katalis terhadap Selektivitas Fraksi Bensin 0 2 4 6 8 10 12 Tanpa Katalis
ZAA Ni/ZAA Mo/ZAA
Ni-Mo/ZAA Jenis Katalis S e le k ti v it a s
Augustine, R.L. 1996.
Heterogeneous Catalysis for
the Synthetic Chemist.
Marcel Dekker Inc. New York
Bartholomew, C.H., Farrauto,R.J. 1976. Chemistry of Nikel –
Alumina Catalyst. Journal of chemistry.45
Fitrianto, J.K, 2006. Karakterisasi dan Uji aktivitas katalis Zeolit Alam Aktif (ZAA), Ni/ZAA,Mo/ZAA,NiMo/ZA A pada reaksi hidrorengkah tir batubara. Skripsi. F-MIPA.
UNS
Gates,B.C, Katzer, J.R.Schut,G.C.A. 1979. Chemistry of catalytic
process; C racking; Process, Reaction and Catalyst.Mc
Graw – Hill Book Company. Newyork
Gates,B.C, 1992, Catalitic Chemistry
Wiley Series In Chemichal Engineering, John Wiley
and Son,Inc
Handoko, S.P. 2002. Pengaruh
perlakuan asam ,Hidrotemal
dan Impregnasi Logam
Kromium pada Zeolit dalam
Preparasi Katalis. Jurnal
ilmu dasar.Vol 3.No 2 Kirk – Otmer. 1997. Encyclopedia of
Chemical Technology.
Fourth Edition. John Willey and Sons, inc. Vol 24. No 350 – 352
Ma, Q. And Klier.K.2001.
Interaction between catalyst and support.2.Low coverage of Co and Ni at the alumina
surface and 3. Metal
Agglomeration on silica
Surface.J.Phisic.Chem.B.10
5
Nasutions, dkk. 1999. Hydrocracking
of Heavy distillate into clean diesel oil using Ni-Mo /Al2O3-SiO2.Prosiding
Seminar Nasional Kimia. F-MIPA.UGM
Olah. G.A. Molnar. 1995.
Hydrocarbon Chemistry.
John Willey and Sons, inc. Riyadi, A. 2001. Optimalisasi waktu
dan rasio katalis umpan pada proses perengkahan fraksi
samapah plastik menjadi
fraksi bensin menggunakan katalis Cr / Zeolit
alam. Skripsi . F- MIPA.
UGM
Satterfield,C.N. 1980. Heterogenous
Catalyst In Practice. Mc
Graw Hill Book Company. New york
Syarifah et al. 2000. Ni – Zeolit alam untuk perengkahan fraksi minyak bumi. Prosiding Seminar Nasional Kimia. Jurusan kimia. F-MIPA. UGM
Triyono. 1994. Kimia Fisika.
Dasar-dasar Kinetika dan Katalis.
Depdikbud Dirjen
Pendidikan Tinggi
Walters, dkk.1995. Hydrocracking of
n – Decane over zeolite –
supported metal sulfide
catalyst.1. CaY- supported metal sulfide. Journal of
American Chemistry Windarti, T. 2001. Pengaruh
kandungan logam kromium dan temperatur terhadap efektifitas katalis Cr-Zeolit alam dalam proses perengkahan Biofuel. Tesis. UGM. Yogyakarta