BAB 2
TINJAUAN PUSTAKA
2.1. Gunung Berapi
Di dataran tinggi Kabupaten Karo, Sumatera Utara, Indonesia, terdapat salah
satu gunung berapi yang dikenal dengan Gunung Sinabung. Koordinat puncak
Gunung Sinabung adalah 03 derajat 10 menit LU dan 98 derajat 23 menit BT dengan
puncak tertinggi dari gunung ini adalah 2.460 meter dari permukaan laut yang menjadi
puncak tertinggi di Sumatera Utara. Gunung ini belum pernah meletus sejak 1600
(Global Volcanism Program, 2008).
Pada tanggal 27 Agustus 2010, aktivitas Gunung Sinabung mulai terjadi dan
mengeluarkan asap dan abu vulkanis. Pada dini hari sekitar pukul 00.15 WIB tanggal
29 Agustus 2010, Gunung Sinabung mengeluarkan lava. Abu gunung ini cenderung
mengalir dari arah barat daya menuju timur laut (Ebo, 2010). Kemudian, pada
September 2013, Gunung Sibanung meletus. Letusannya melepaskan awan panas dan
abu vulkanik yang menjangkau kawasan Sibolangit dan Berastagi. Guguran lava pijar
dan semburan awan panas masih terus dihasilkan sampai Januari 2014 dan hingga kini
rentetan gempa, letusan, dan luncuran awan panas masih terjadi secara terus-menerus
(Suryani, 2014). Sampai saat ini, letusan Gunung Sinabung masih terjadi sehingga
statusnya masih dinyatakan awas.
Komponen utama erupsi gunung berapi adalah magma yang berbentuk padat,
lithic material atau memadat menjadi partikel besar yang dikenal sebagai ash (abu)
atau tephra. Erupsi gunung juga mengandung gas, dengan air (H2O), nitrogen (N2) dan
karbon dioksida (CO2). Gas ini telah menjadi sumber utama atmosfer planet dan
komponen utama atmosfer adalah N2 (78%) dan O2 (21%) yang merupakan sumber
emisi vulkanik (Robock, A., 2002).
Beberapa metode untuk mensurvei dan memprediksi aktivitas gunung api telah
digunakan saat ini, dan beberapa metode tersebut berhasil untuk beberapa gunung api.
Tetapi, mereka tidak dapat diprediksi secara sempurna kecuali metode tersebut dapat
menentukan posisi magma, waktu, sifat dasar, jarak dan durasi erupsi, dan lain-lain.
Untuk tujuan dalm hal mensurvei dan memprediksi aktivitas gunung api, fenomena
sifat dasar harus dipelajari secara keseluruhan dan detail. Hal ini penting untuk
mengetahui apakah parameter aktivitas vulkanik harus diobservasi secara kontinius.
Akan tetapi, banyak penomena yang belum dipelajari secara sempurna, khusunya dari
segi aspek kimia.
Mayoritas gunung berapi terjadi disepanjang garis tepi piring destruktif di
“daerah tumbukan” dimana satu piring fase berada di bawah yang lainnya. Pergeseran
dan tekanan menyebabkan batuan meleleh dan membentuk magma yang dipaksa naik
ke atas permukaan bumi dimana gunung api bererupsi sebagai lelehan batu (lava) atau
sebagai partikel abu atau cinder (abu api) (Collins, 2010).
Sejumlah skema dapat digunakan untuk mengklasifikasi erupsi gunung berapi.
Mereka pada umumnya diklasifikasikan pada dasar periode aktivitas mereka, jenis
aktifitas dan jenis tanah pembentuknya.
1. Periode aktifitas.
Aktif jika erupsi telah terjadi dalam waktu bersejarah, sebaliknya tidak aktif,
tidur, atau padam.
2. Jenis aktifitas.
Sebagian besar didasarkan pada kekerasan erupsi dan derajat eksploitasi. Nama
yang digunakan diturunkan dari lokasi gunung berapi yang menunjukkan jenis
3. Sifat topografis gunung
Sistem yang paling sederhana untuk klasifikasi berdasarkan periode aktivitas –
seperti aktif, diam, atau tidur. Gunung berapi dapat tetap tidak aktif untuk ratusan
atau ribuan tahun sebelum fase erupsi lainnya diselesaikan (Coates, 1981).
2.2. Air
Air adalah senyawa penting bagi semua bentuk kehidupan di bumi ini, sebagian besar
permukaan bumi tertutup oleh air sehingga sangat berpengaruh terhadap iklim. Air
yang tersebar di alam tidak ada yang berbentuk murni, akan tetapi tidak semua air di
alam sudah terpolusi. Sebagai Contoh, perairan di daerah pegunungan dan hutan yang
bebas dari polusi, masih mengandung bahan-bahan terlarut seperti CO2, O2, dan N2,
serta bahan tersuspensi seperti debu dan partikel-partikel lainnya yang terbawa dari
atmosfer.
Ciri-ciri air yang mengalami polusi sangat bervariasi tergantung dari jenis air
dan polutannya atau komponen yang mengakibatkan polusi. Polutan air dapat
dikelompokkan atas sembilan golongan berdasarkan sifat-sifatnya sebagai berikut:
- padatan
- bahan buangan yang membutuhkan oksigen (Oxigen Demanding Wastes)
- mikroorganisme
- komponen organik sintetik
- nutrient tanaman
- minyak
- senyawa anorganik dan mineral
- bahan radioaktif
- panas
Pengelompokan di atas bukan merupakan pengelompokan baku, karena suatu jenis
polutan mungkin dapat dimasukkan ke dalam lebih dari satu kelompok (Agusnar, H.
Komposisi dasar air alam tergantung pada pengikatan dan pelepasan solut
melalui pereaksi kimia dan proses fisika. Untuk kebanyakan bagian, solut mengalami
lingkaran geologikal dimana material memasuki larutan sebagai produk reaksi udara
dengan batu, vulkanisasi, dan lain-lain, dialirkan ke perairan dimana mereka
mengalami reaksi lebih lanjut, disimpan di dalam sendimen, dan akhirnya dibentuk
menjadi batuan baru, yang mengulangi siklus di atas. Lebih singkatnya, proses ini
memiliki jangka waktu yang sangat panjang. Material volatil yang masuk ke dalam
atmosfer untuk bagian dari siklus tersebut, dan beberapa elemen merupakan bagian
dari biokimia, seperti geomaterial, pemprosesan. Perpindahan secara fisika pada
material yang sangat kecil mengendap di dalam air dan sebagai debu dan hemburan air
laut di dalam air juga mempunyai bagian di dalam proses ini ((Bailey, R.A. 1978).
Air merupakan sumber kehidupan untuk makhluk hidup karena penting untuk
proses kehidupan. Air dikenal sebagai sumber alam yang paling berlimpah, dan
berikut merupakan pembagian kualitas air:
− Air merupakan satu-satunya material yang memiliki tiga sifat fisika di permukaan bumi; yaitu gas, cair, dan padat.
− Air bersifat renewable karena siklus hidrologinya.
− Dalam bentuk asli air berwarna bening, tidak berasa, dan transparan. Semua sifat memiliki keuntungan yang besar, seperti pertumbuhan tanaman. Contoh,
ketransparanan air membiarkan cahaya berpenetrasi di dalam sungai dan laut
sehingga penting dalam sumber makanan hewan dan tumbuhan.
− Air mempunyai viskositas yang sangat rendah. Mobilitasnya membiarkannya untuk mudah berpindah.
− Air merupakan salah satu dari sedikit senyawa yang mengembang ketika membeku.
− Air mempunyai kapasitas panas yang sangat tinggi dari semua zat alam kecuali ammonia.
− Air mempunyai tegangan permukaan yang tidak umum sehingga tidak hanya membiarkan zat untuk mendorong dirinya sendiri, tetapi juga mendukung objek
dengan densitas yang lebih tinggi dan membasahi material lainnya.
Sifat unik yang dimiliki air menjadikan zat ini merupakan pelarut yang sangat
sempurna untuk berbagai material, sehingga air adalah dasar medium transportasi
untuk nutrient dan hasil limbah dalam proses kehidupan. (Manahan, E.S, 1984).
Ion di dalam air, baik ion ringan maupun ion berat, jarang sekali berbentuk
atom tersendiri, tetapi biasanya terikat oleh senyawa lain sehingga berbentuk molekul.
Ikatan itu dapat berupa garam organik, seperti senyawa metal, etil, fenil maupun
garam anorganik berupa oksida, klorida, sulfide, karbonat, dihidroksida, dan
sebagainya. Bentuk ion dari garam tersebut biasanya banyak ditemukan dalam air
kemudian bersenyawa atau diserap dan tertimbum dalam tanaman dan hewan air. Ion
kemudian bersenyawa dalam bahan kimia jaringan dan membentuk senyawa organik.
Ion ringan atau elemen makro tertentu, yang biasanya esensial dan bersenyawa dengan
protein jaringan makhluk hidup, berguna untuk proses pertumbuhan. Sedangkan ion
berat yang nonesensial juga dapat bersenyawa dengan protein jaringan dan tertimbun
serta berikat dengan protein, sehingga senyawa disebut metalotionein yang dapat
menyebabkan toksik (Darmono, 1995).
2.3. Ion
Ion berasal dari kerak bumi yang berupa bahan-bahan murni, organik, dan anorganik.
Ion merupakan bahan pertama yang dikenal oleh manusia dan digunakan sebagai
alat-alat yang berperanan penting dalam sejarah perdaban manusia. Ion mula-mula diambil
dari pertambangan di bawah tanah (kerak bumi). Secara alami siklus perputaran ion
adalah, dari kerak bumi kemudian ke lapisan tanah, kemudian ke makhluk hidup
(tanaman, hewan, dan manusia), ke dalam air, mengendap dan akhirnya kembali ke
makro dan ion mikro, dimana ion makro ditemukan lebih dari 1.000 mg/kg dan ion
Tabel 2.1. Ion-ion Makro dan Mikro yang Ditemukan dalam Kerak Bumi
(Darmono, 1995)
Kelompok Ion Simbol Jumlah (mg/kg)
Makro Aluminium Al 81.300
Besi Fe 3+ 50.000
Kalsium Ca 36.300
Kalium K 25.900
Magnesium Mg 20.900
Mangan Mn 1.000
Mikro Barium Ba 425
Nikel Ni 75
Seng Zn 70
Tembaga Cu 55
Plumbum Pb 12,5
Uranium, U 2,7
Timah putih Sn 2
Kadmium Cd 2+ 0,2
Merkuri Hg 0,08
Perak Ag 0,07
Emas Au 0,004
*Ion ringan
2.4. Besi (Fe 3+)
Besi adalah salah satu elemen kimiawi yang dapat ditemui pada hampir setiap tempat
di bumi, pada semua lapisan geologis dan semua badan air. Pada umumnya, besi yang
ada di dalam air dapat bersifat:
− Terlarut sebagai Fe 2+ (Fero) atau Fe 3+ (Feri)
− Tersuspensi sebagai butir koloidal (diameter <1 μm) atau lebih besar, seperti
Fe2O3, FeO, Fe(OH)3 dan sebagainya
− Tergabung dengan alat zat organis atau zat padat yang inorganis (seperti tanah liat)
Pada air permukaan jarang ditemukan kadar Fe lebih besar dari 1 mg/l, tetapi
di dalam air tanah kadar Fe dapat jauh lebih tinggi. Konsentrasi Fe yang tinggi ini
dapat dirasakan dan dapat menodai kain dan perkakas dapur (Alerts, G. 1984).
2.5. Kadmium (Cd 2+)
Kadmium banyak digunakan di dalam industri metalurgi, pelapisan ion, pigmen,
baterai, peralatan elektronik, pelumas, peralatan fotografi, gelas, keramik, tekstil, dan
plastic (EckenFender, 1989). Di dalam air, Cd 2+ terdapat dalam jumlah yang sangat
sedikit (renik) dan bersifat tidak larut dalam air. Kadar Cd 2+ dalam kerak bumi sekitar
0,2 mg/kg (Moore, 1991).
Kadar Cd2+ pada perairan tawar alami sekitar 0,0001 – 0.01 mg/liter,
sedangkan pada perairan laut sekitar 0,0001 mg/liter (McNeely et al., 1979). Menurut
WHO, kadar Cd2+ maksimum pada air diperuntukkan bagi air minum adalah 0,005
mg/liter (Moore, 1991). Pada perairan yang diperuntukkan bagi kepentingan pertanian
dan perternakan, kadar Cd2+ sebaiknya tidak melebihi 0,005 mg/liter. Untuk
melindungi kehidupan pada ekosistem akuatik, perairan sebaiknya memiliki kadar
Cd2+ sekitar 0,0002 mg/liter (Moore, 1991).
Kadmium bersifat kumulatif dan sangat toksik bagi manusia karena dapat
dan mengakibatkan kemandulan pada pria dewasa. Toksisitas kadmium dipengaruhi
oleh pH dan kesadahan. Selain itu, keberadaan zinc dan timbal dan meningkatkan
toksisitas kadmium. (Effendi, 2003).
2.6. Kobal (Co2+)
Kobal termasuk unsur renik yang dibutuhkan dalam pertumbuhan dan reproduksi
tumbuhan dan hewan. Bersama-sama dengan ion yang lain, misalnya tembaga, zinc,
besi, dan magnesium, kobal dibutuhkan oleh enzim sebagai koenzim yang berfungsi
untuk mengikat molekul substrat (Effendi, H. 2003). Perairan tawar alami biasanya
memiliki kadar kobal < 0,001 mg/liter, perairan di daerah pertambangan dan industri
memiliki kadar kobal antara 0,001 – 0,01 mg/liter (Moore, 1991); sedangkan perairan
laut memiliki kadar kobal sangat rendah, yakni sekitar 0,0005 mg/liter . Pada perairan
yang diperuntukkan bagi kepentingan pertanian, kadar kobal sebaiknya tidak melebihi
0,05 mg/liter (Effendi, H. 2003).
Kobal merupakan salah satu elemen penting untuk tubuh manusia. Kekurangan
elemen esensial ini dapat menstimulasi beberapa penyakit sedangkan kobal berbahaya
dan menganggu kesehatan jika kelebihan. Co2+ dari golongan ion esensial
membutuhkan beberapa aktivitas metabolisme di dalam organisme. Efek toksologi
jumlah besar Co2+ menstimulasi vasodilasi, kemarahan dan cardiomyophaty di dalam
manusia dan hewan.
2.7. Spektrofotometri Serapan Atom (SSA)
Peristiwa serapan atom pertama kali diamati oleh Fraunhofer, ketika menelaah
garis-garis hitam pada spektrum matahari. Sedangkan yang memanfaatkan prinsip serapan
atom pada bidang analisis adalah seorang Australia bernama Alan Walsh di tahun
Metode Spektrofotometri Serapan Atom (SSA) berprinsip pada absorpsi
cahaya oleh atom. Atom-atom menyerap cahaya tersebut pada panjang gelombang
tertentu, tergantung pada sifat unsurnya. Spektrum atomik untuk masing-masing unsur
terdiri atas garis-garis resonansi. Garis-garis lain yang bukan garis resonansi dapat
berupa spektrum yang berasosiasi dengan tingkat energi molekul, biasanya berupa
pita-pita lebar atau garis tidak berasal dari eksitasi tingkat dasar yang disebabkan
proses atomisasinya (Khopkar, 2007)
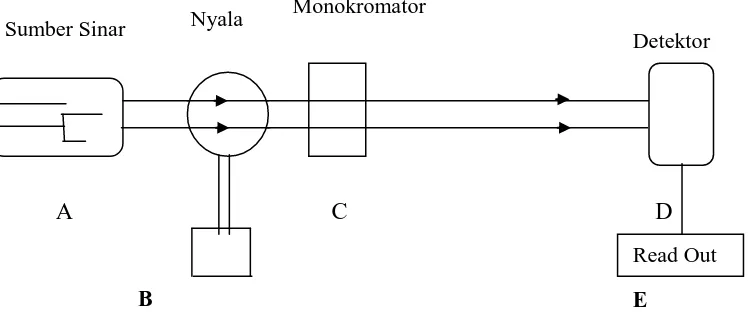
Sistem peralatan spektrofotometer serapan atom dapat dilihat pada gambar
berikut ini ;
A C D
Gambar 2.1 Sistem peralatan Spektrofotometer Serapan Atom (SSA)
(Rohman, 2007).
Berikut penjelasan dari sistem peralatan Sepktrofotometri Serapan Atom :
A. Sumber sinar
Sumber sinar yang biasa dipakai adalah lampu katoda berongga. Lampu ini
terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda.
Katoda sendiri berbentuk silinder berongga yang terbuat dari ion atau dilapisi
dengan ion tertentu. Tabung ion ini diisi dengan gas mulia (neon atau argon)
dengan tekanan rendah. Neon biasanya lebih disukai karena memberikan
intensitas pancaran lampu yang lebih rendah. (Rohman, 2007)
B. Tempat Sampel
Dalam analisis spektrofotometri serapan atom, sampel yang akan dianalisis
Read Out Sumber Sinar Nyala
Monokromator
Detektor
Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel
menjadi uap atom – atom yaitu dengan nyala (flame) dan dengan tanpa nyala
(flameless) (Rohman, 2007).
C. Monokromator
Monokromator berfungsi untuk memisahkan dan memilih panjang gelombang
yang di gunakan dalam analisis. Dalam monokromator juga terdapat suatu alat
yang digunakan untuk memisahkan radiasi resonansi dan kontinyu yang
disebut dengan chopper ( Rohman, 2007)
D. Detektor
Dalam spektrofotometer serapan atom detektor berfungsi mengubah intensitas
radiasi yang datang menjadi arus listrik. Ada dua cara yang dapat digunakan
dalam sistem deteksi yaitu: (a) yang memberikan respon terhadap radiasi
resonansi dan radiasi kontinyu; dan (b) yang hanya memberikan respon
terhadap radiasi resonansi. Cara terbaik adalah dengan menggunakan detektor
yang hanya peka terhadap radiasi resonan yang termodulasi (Rohman, 2007).
E. Sistem Pencatat ( Read-Out)
Sistem pencatat yang digunakan pada spektrofotometer serapan atom berfungsi
untuk mengubah sinyal yang diterima menjadi sinyal digital, yaitu dalam
satuan absorbansi. Hasil pembacaan dapat berupa angka atau berupa kurva dari
suatu recorder yang menggambarkan absorbansi atau intensitas emisi
(Rohman, 2007).
Pada spektroskopi pembangkit sinyal adalah hasil antaraksi energi radiasi
elektromagnet dengan elektron dalam atom/molekul analit yang menyebabkan transisi
elektron valensi atom /molekul dari tingkat energi elektron dasarnya ke tingkat energi
elektron tertentu yang lebih tinggi atau meningkatkan energi vibrasi-rotasi ikatan antar
atom dalam molekul (Satiadarma, K. 2004).
Teknik spektrofotometri serapan atom memiliki bentuk umum dengan
spektroskopi lainnya di dalam instrument yang terdiri dari sumber, sel, monokromator
dan detektor. Ada dua jenis instrument di dalam SSA yaitu; single-beam dan
- Instrumen SSA Single-Beam
Jenis instrument SSA yang sedikit rumit adalah single-beam. Bagian optik dari
jenis instrument single-beam terdiri atas: lampu katoda cekung, lampu dan nyala
api, monokromator, dan detektor.
Instrumen SSA single-beam dikalibrasi dengan mengisi blank dan mengatur
elektronik untuk membaca absorbansi 0. Kalibrasi lebih lanjut dilakukan dengan
mengisi larutan standart. Data hasil absorbansi diplot dengan konsentasi untuk
memperoleh kurva standar .
- Instrumen SSA Double-Beam
Instrumen SSA double-beam dikenalkan karena ketidakstabilan yang disebabkan
oleh pengapungan sumber intensitas dan elektronik. Instrumen double-beam lebih
stabil. Hal ini disebabkan karena adanya komponen baru yaitu sektor mirror yang
memberi kemungkinan garis edar refensi optic.
Instrumen double-beam harus dikalibrasi sebelum digunakan untuk mengukur
konsentrasi analit. Metode kalibrasi adalah sama dengan intrumen single-beam.
Sampel dianalisis dengan prosedur yang sama. Instrumen double-beam cenderung
lebih stabil, sehingga mereka cenderung membutuhkan kalibrasi yang lebih
sedikit. Instrumen double-beam secara frekuensi lebih sensitive dan lebih tepat
penggunaanya. Tetapi instrumen ini mudah menyimpang dari hukum Beer, karena
deviasi ini terjadi pada nilai absorbansi yang tinggi dan nilai di dalam kurva